-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Novinky v terapii folikulárního lymfomu
Therapy of follicular lymphoma - latest developments
Follicular lymphoma (FL) belongs to the most common forms of non-Hodgkin’s lymphomas. This overview summarizes the important news regarding the therapy of FL from the past 5 years. In principle, in the therapy we can use: watch and wait strategy, radiotherapy, chemotherapy, rituximab, interferon alfa, ibritumomab, tositumomab, autologous hematopoietic stem cell transplantation, allogeneic transplantation, vaccines, and some other new drugs. The order of these therapeutic procedures does not mean this is the sequence in which they should be used. Since FL is a chronic, relapsing disease, a proper procedure(s) should be used in proper patients in a proper sequence. The clinical course of the disease as well as the therapy of FL are variable. Today, we also have to consider the cost of treatment. Therefore, it is necessary, FL patients are treated in experienced centers.
Key words:
follicular lymphoma, rituximab, interferon alfa, ibritumomab, allogeneic transplantation, autologous hematopoietic stem cell transplantation
Autoři: J. Mayer 1; A. Obořilová 1; I. Vášová 1; Z. Král 1; M. Matuška 2; D. Feltl 2
Působiště autorů: Interní hematoonkologická klinika FN Brno 1; Radioterapeutická klinika FN s poliklinikou Ostrava 2
Vyšlo v časopise: Transfuze Hematol. dnes,13, 2007, No. 1, p. 4-11.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Folikulární lymfom (FL) je jeden z nejčastěji se vyskytujících nehodgkinských lymfomů. Tento přehled má za cíl shrnout podstatné novinky o terapii této choroby z posledních cca 5 let. Jako principiální možnosti se u nemocných s folikulárním lymfomem nabízejí: pouhé bedlivé sledování nemocného (watch and wait strategy), radioterapie, chemoterapie, rituximab, interferon-α, ibritumomab, tositumomab, autologní transplantace, alogenní transplantace, vakcíny a další nové terapeutické postupy a další monoklonální protilátky. Pořadí těchto možností v žádném případě neznamená, že mají být takto uplatňovány. Vzhledem ke zpravidla chronicky relabujícímu průběhu choroby je potřeba různé postupy různě skládat, dohromady i po sobě a spíše o nich uvažovat jako o jednotlivých stavebních kamenech terapie. Pro folikulární lymfom více než pro řadu jiných chorob platí známá odpověď na to, zda je medicína věda nebo umění: je to umění aplikovat vědu do praxe. Terapie folikulárního lymfomu je nesmírně mnohostranná, podobně jako nakonec i manifestace samotné choroby. Dnes k tomu navíc přistupuje i hledisko finanční, terapie se stává mimořádně drahou. Je-li však dobře vedena, může se také stát i terapií mimořádně účinnou. Za každé situace je potřeba zvažovat všechna pro a proti toho či onoho postupu a pokusit se rozhodnout správně. A to vyžaduje hluboké znalosti a zkušenosti. Proto by terapie této zdánlivě indolentní choroby měla být vedena pouze na pracovištích, kde je toto zaručeno.
Klíčová slova:
folikulární lymfom, rituximab, interferon alfa, ibritumomab, alogenní transplantace, autologní transplantaceÚvod
Folikulární lymfom (FL) je jeden z nejčastěji se vyskytujících nehodgkinských lymfomů. O této chorobě byla z našeho pracoviště vydána monografie (1). Od té doby se ale objevila celá řada zcela nových a zásadních informací týkajících se jak molekulární patogeneze, tak terapie této choroby. Rozhodli jsme se proto na tuto monografii navázat a nejnovější praktické poznatky týkající se léčby stručně shrnout. Tento přehled tedy nelze chápat jako zcela kompletní, ale doplňující uvedenou monografii o poslední poznatky.
Stratifikace rizikovosti a přirozený průběh nemoci
V současné době je asi nejrozšířenější tzv. FLIPI index (FLIPI = Follicular Lymphoma International Prognostic Index) (2). Tento index stratifikuje nemocné do 3 základních skupin, jak je patrné z tabulky 1.
Tab. 1. FLIPI - Follicular Lymphoma International Prognostic Index. 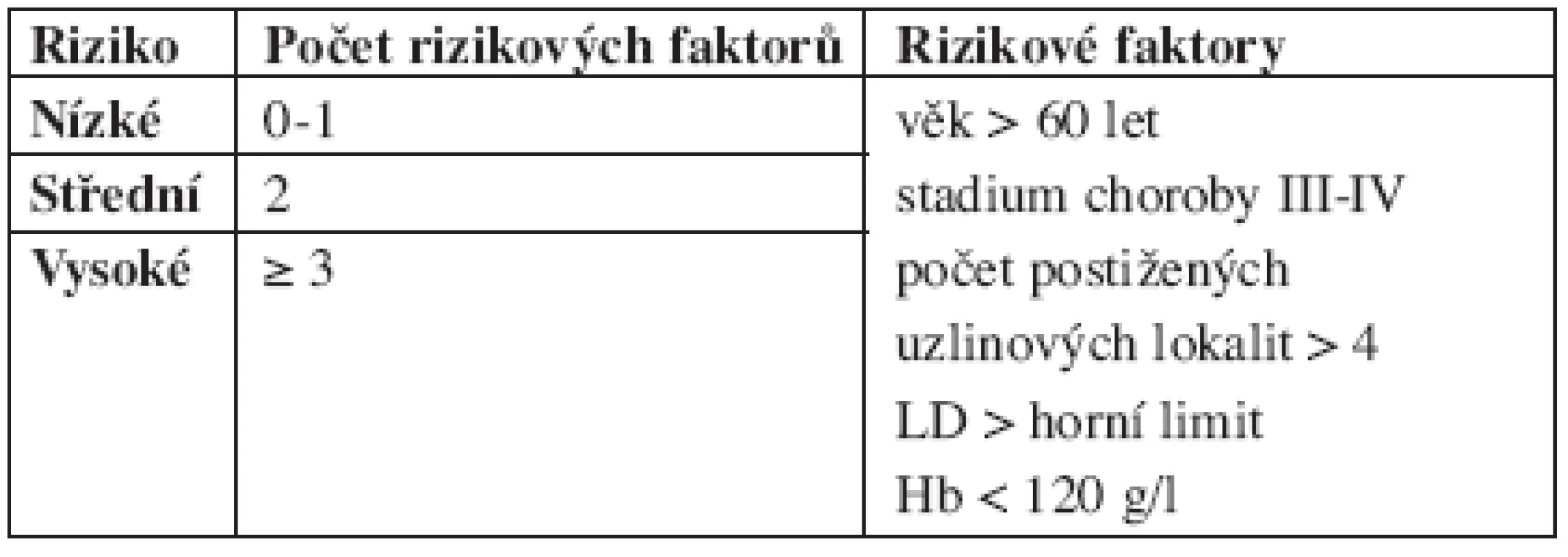
Počet uzlinových lokalit je hodnocen klinicky, nebo podle CT vyšetření a je hodnocen jako 2, jde-li o bilaterální postižení. K bližšímu vysvětlení uzlinových lokalit může sloužit originální schéma, viz obrázek 1.
Obr. 1. Schéma uzlinových lokalit k výpočtu rizika pro FLIPI index. Podle: Solal-Céligny et al., Blood 2004. 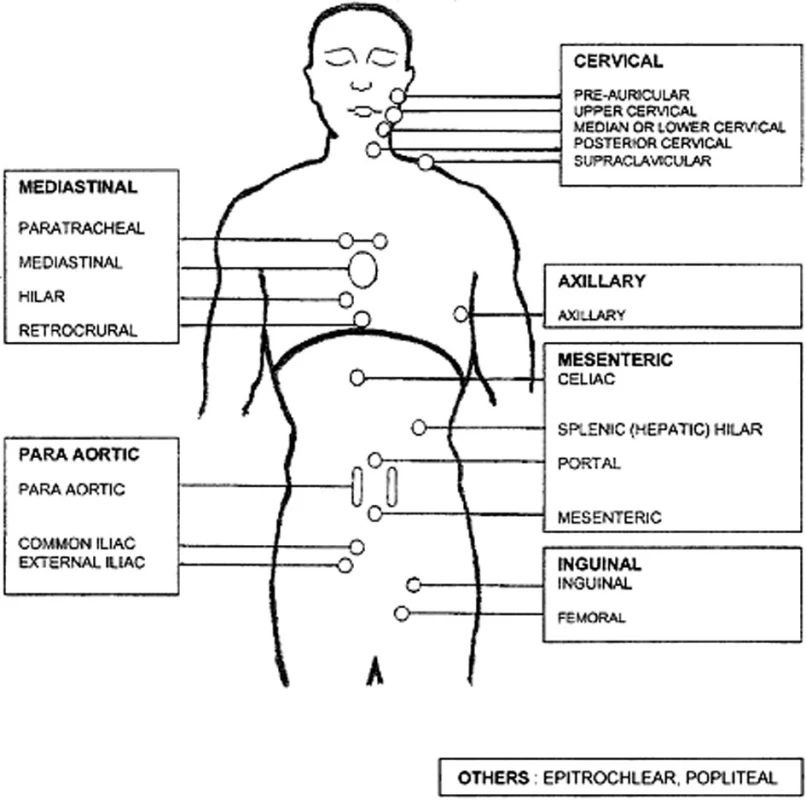
Tento index má jasný vztah k přežívání pacientů, jak je patrno z obrázku 2.
Obr. 2. Přežívání nemocných podle FLIPI indexu. Dle: Solal-Céligny et al., Blood 2004. 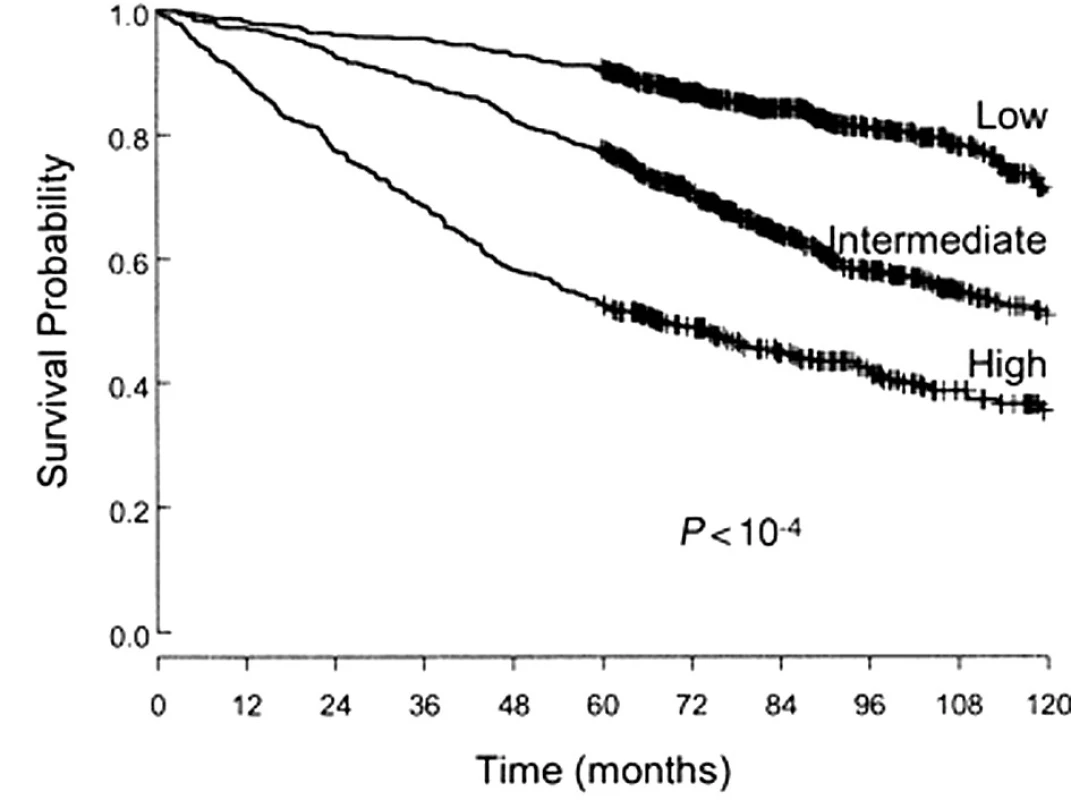
Choroba má mnohdy nevyzpytatelný průběh a je charakterizována spontánními remisemi, ale na druhé straně i transformací do vysokého stupně malignity. Stále ale platí, že terapie není vždy nezbytně nutná a zpravidla se k ní sahá v případě klinicky agresivnějšího chování lymfomu. Existují různé definice tohoto stavu, ale jako vodítko lze vzít následující situace:
- B-symptomy
- Rychlá progrese choroby (< 3 měsíce)
- Život ohrožující infiltrace orgánů, komprese
- Klinicky signifikantní infiltrace kostní dřeně s poruchou její funkce
- Infiltrace kostí, makroskopická infiltrace jater nebo ledvin
- Nodální nebo extranodální masy > 7 cm
- > 3 lokality s průměrem > 3 cm
- Signifikantní splenomegalie, výpotky
- Cirkulující lymfomové buňky v signifikantním množství.
Základní pilíře terapie
Principiálně je vhodné se držet následujících pravidel:
- Je vhodné mít dopředu koncepci zahrnující dlouhodobější průběh a počítající i s možným relapsem
- Je vhodné vybírat postupy, které jsou navzájem dobře kompatibilní
- Je vhodné nemocné zařazovat do léčebných protokolů a studií
Jako příklad můžeme uvést použití režimů s fludarabinem jako první linie. V tomto případě je ale problematické uvažovat o následné autologní transplantaci periferních kmenových buněk, neboť je vysoká pravděpodobnost, že bude velmi obtížné získání takového transplantátu pro problémy s vyplavováním CD34+ buněk.
Jako principiální možnosti se u nemocných s folikulárním lymfomem nabízejí:
- Pouhé bedlivé sledování nemocného (watch and wait strategy)
- Radioterapie
- Chemoterapie
- Rituximab
- Interferon-α
- Ibritumomab
- Tositumomab
- Autologní transplantace
- Alogenní transplantace
- Vakcíny a další nové terapeutické postupy
- Další monoklonální protilátky
Pořadí těchto možností v žádném případě neznamená, že mají být takto uplatňovány. Vzhledem ke zpravidla chronicky relabujícímu průběhu choroby je potřeba různé postupy různě skládat, dohromady i po sobě a spíše o nich uvažovat jako o jednotlivých stavebních kamenech terapie. Pro folikulární lymfom více než pro řadu jiných chorob platí známá odpověď na to, zda je medicína věda nebo umění: je to umění aplikovat vědu do praxe.
Strategie „watch and wait”
Je stále aktuální pro některé nemocné bez agresivněji se chovající choroby. Řada prací ukázala, že u takových pacientů současně dostupné možnosti terapie nejsou jednoznačně přínosné. V tabulce 2 je přehled zásadních studií, které to ukázaly. Důležité je, že testovány byly velmi rozmanité přístupy, ale žádný nepřinesl jasné pozitivní výsledky. Obrázek 3 ukazuje výsledky poslední studie, kterou publikovali Ardeshna et al. (3).
Tab. 2. Přehled velkých studií ukazujících minimální nebo žádný přínos včasné terapie u asymptomatických pacientů s folikulárním lymfomem. 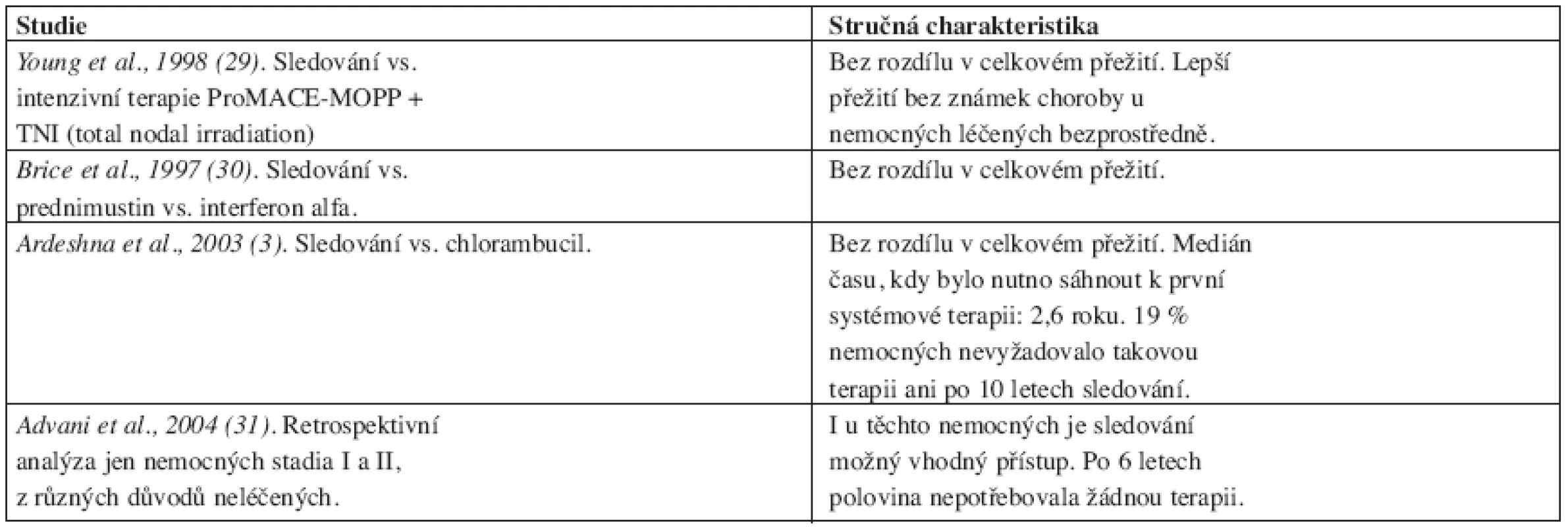
Obr. 3. Celkové přežití při včasné terapii chlorambucilen nebo při počáteční „watch and wait“ strategii. Podle: Ardeshna et al., Lancet 2003. 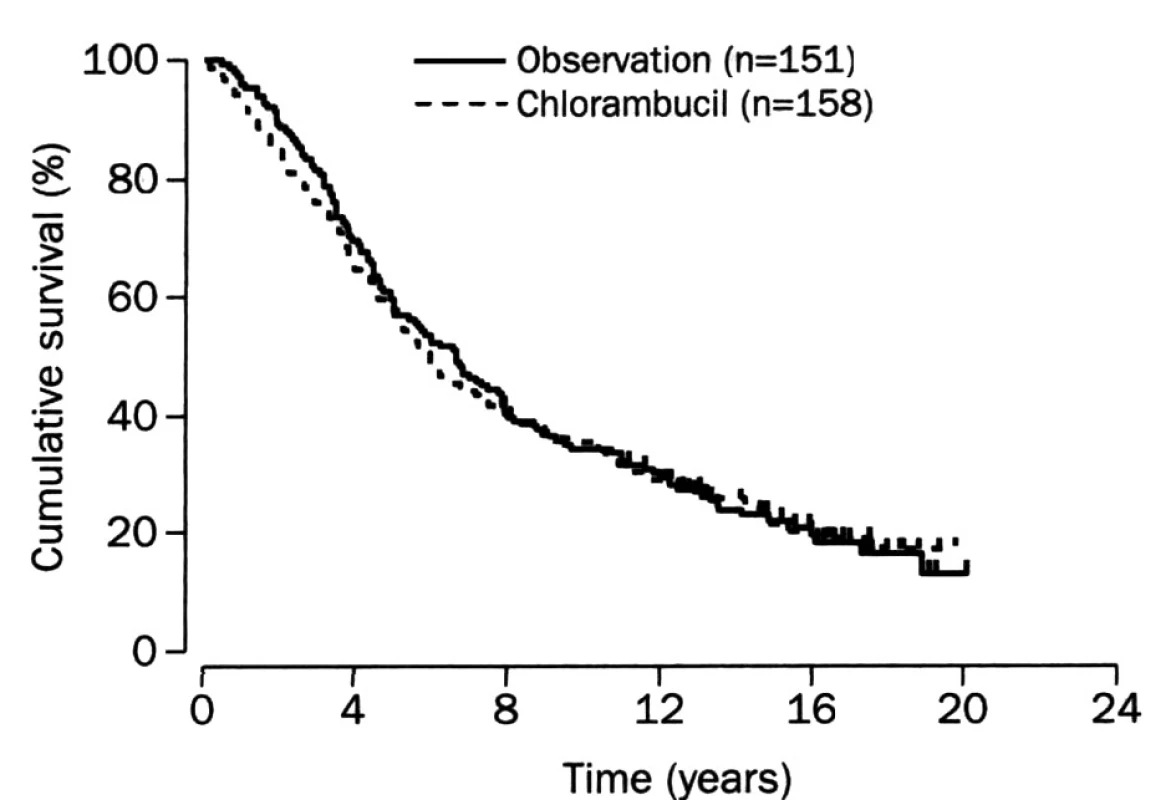
Radioterapie
Radioterapie může být principiálně použita jako samostatná - s kurativním nebo paliativním záměrem, či jako kombinovaná léčba s chemoterapií. Kurativní záměr bývá zpravidla u nemocných s lokalizovaným postižením, stadia I a II. Radioterapie zahrnuje zpravidla „involved-field“ a dávka bývá okolo 35 Gy během 3–4 týdnů. Při tomto způsobu terapie se dosahuje vynikajících výsledků z hlediska lokální kontroly choroby, ale jsou relativně časté pozdní relapsy v neozářených místech. Rozsáhlé zhodnocení výsledků u 669 nemocných ukázalo, že frekvence relapsů po 5, 10 a 20 letech byla 38 %, 48 % a 56 % a celkové přežití po 5 a 10 letech bylo 79 % a 62 % (4). Seymour et al. (5) proto kombinovali radioterapii s chemoterapií a zdá se, že tento přístup frekvenci pozdních relapsů snižuje – 80 % a 72 % nemocných bylo beze známek choroby po 5 a 10 letech sledování a přežití po 10 letech 80 %. Léčebný protokol zahrnoval 10 kúr chemoterapie COP-Bleo (CHOP-Bleo u rizikových nemocných) a s tím, že po 3. chemoterapii byla vložena radioterapie.
Zajímavý přístup k lokální kontrole choroby publikovali Haas et al. (6). Tito autoři zjistili velmi dobrou odpověď i na dávku pouze 4 Gy (1x4 Gy či 2x2 Gy) a bylo možné ji v případě potřeby opakovat.
Samotná chemoterapie
Orina et al. (7) provedli rozsáhlou metaanalýzu studií srovnávajících různé režimy pro léčbu 1. linie. Ukázalo se, že největší pravděpodobnost dosažení kompletní remise (CR) je u režimů CHOP či kombinovaných režimů obsahujících fludarabin. K podobným závěrům co se týče výhodnosti použití antracyklinů dospěli i Rigacci et al. (8). Bylo také ale upozorněno na určitá rizika režimů s fludarabinem. McLaughlin et al. (9) referují o sekundárních myelodyspláziích a může se také vyskytnout problém s následnou mobilizací periferních kmenových buněk (peripheral blood stem cells, PBSC) (10). Také u našeho souboru nemocných léčených primární terapií FND (fludarabin, Novantrone (mitoxantron) a dexametazon) se nepodařilo mobilizovat dostatečné množství PBSC u 8 ze 13 pacientů.
Objevují se také informace o výhodnosti nového cytostatika bendamustinu (11, 12). Mechanismus účinku je komplexní a zahrnuje alkylační aktivitu. U nás zatím není registrován.
Interferon-α
V roce 2005 byla publikována metaanalýza studií s interferonem-α u folikulárního lymfomu (13). Výsledky se dají stručně shrnout následovně:
- přidání interferonu k iniciální chemoterapii nezvyšuje léčebné odpovědi
- studie byly velmi heterogenní
- určitý přínos interferonu pro prodloužení přežití byl vidět tam, kde se interferon přidal k relativně intenzivní iniciální chemoterapii, v dávce alespoň 5 mil. jednotek nebo v dávce alespoň 36 mil. jednotek/měsíc a spíše dohromady s chemoterapií než jako udržovací terapie
- interferon prodlužoval trvání remisí bez ohledu na intenzitu chemoterapie, dávku, nebo jestli byl podáván jako udržovací terapie nebo jako součást kombinace s chemoterapií.
Rituximab
Tomuto mimořádně úspěšnému a účinnému léku jsme nedávnou věnovali celou monografii (14). Zde se proto zaměříme na poslední nejnovější data týkající se folikulárního lymfomu. Rituximab působí na zcela jiném principu než např. cytostatika nebo radioterapie. Jde o monoklonální chimerickou protilátku, zaměřenou proti struktuře CD20, vyskytující se na buňkách B linie a tudíž i na lymfomových buňkách. Hlavní složky působení rituximabu jsou aktivace komplementu, aktivace ADCC (antibody – dependent cellular cytotoxicity) a indukce apoptózy. Rituximab navíc působí synergisticky s řadou klasických antilymfomových látek, i když ne se všemi (15). Na našem pracovišti se tímto problémem dlouhodobě zabýváme a potvrdili jsme např. synergistický efekt u dexametazonu a fludarabinu, ale zjistili jsme neočekávaný antagonistický efekt spolu s prokarbazinem, viz obrázek 4. Přes nyní již bohaté klinické zkušenosti s rituximabem a významné postavení tohoto léku v terapii lymfomů je nutné ve výzkumech jeho mechanismu účinku stále pokračovat.
Obr. 4. Působení rituximabu spolu s dexametazonem, fludarabinem a prokarbazinem na růst buněk linie SU-DHL-4 (odpovídá folikulárnímu lymfomu). Různé koncentrace antilymfomových látek, vždy konstantní koncentrace rituximabu. Vlastní data. 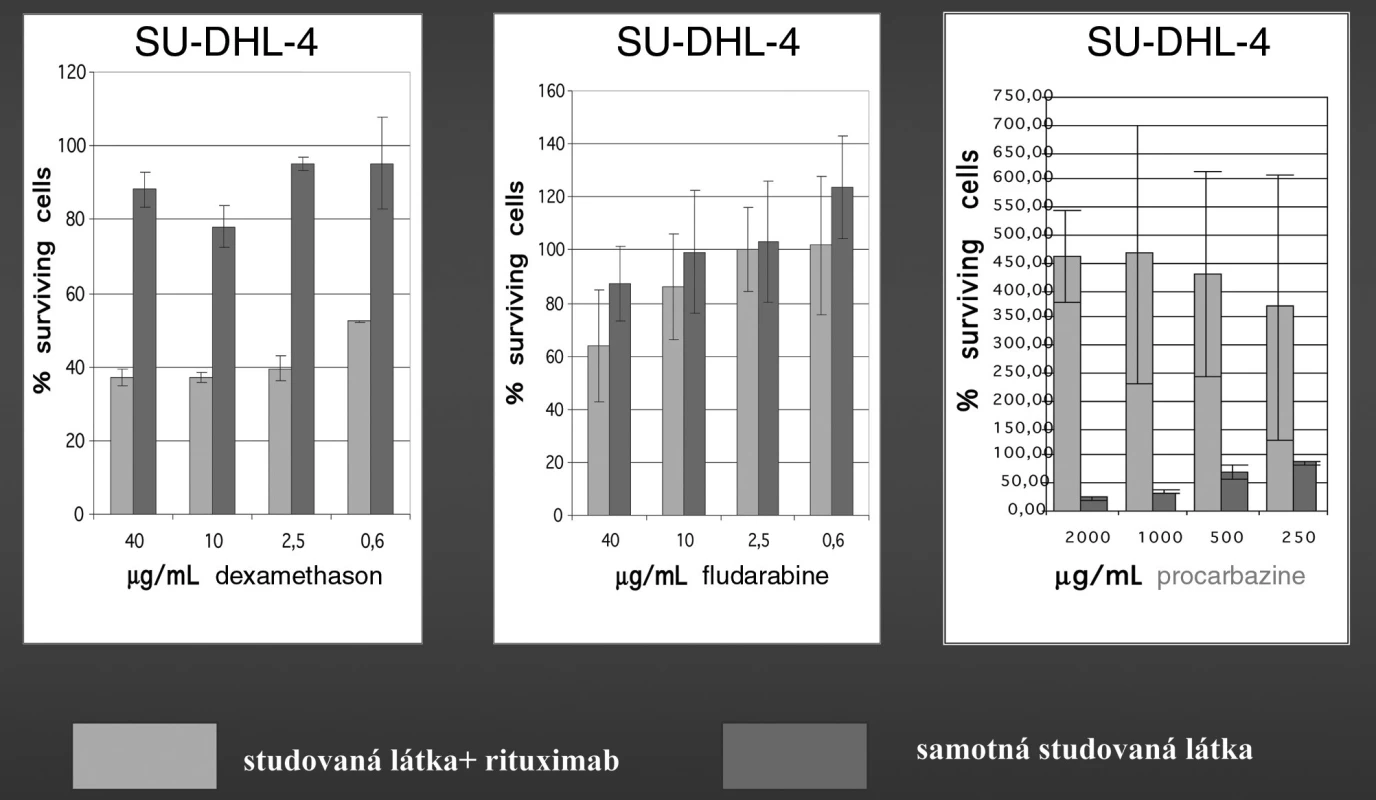
Rituximab byl jako první monoklonální protilátka schválen americkou FDA pro použití v onkologii. Principiálně je možné jej použít jako:
- Monoterapie
- Kombinovaná terapie
- Léčba první i další linie
- Udržovací terapie
- Po předchozím použití rituximabu (retreatment)
- Spolu s transplantací krvetvorných buněk
- Kombinace výše uvedeného. Nyní je již k dispozici řada dat z velkých klinických studií, ať již publikovaných in extenso, nebo ve formě abstrakt, abychom si mohli udělat kvalitní představu o významu tohoto léku v terapii folikulárních lymfomů. Následně budou základní data přehledně uvedena.
Rituximab u nově diagnostikovaných nemocných
Výsledky zásadních studií jsou shrnuty v tabulce 3 a na obrázku 5a a 5b.
Tab. 3. Velké studie zkoumající využití rituximabu v terapii nově diagnostikovaných nemocných. 
Zkratky: ORR (overall response rate), CR (complete remission), EFS (event free survival), TTF (time to treatment failure), OS (overall survival). Obr. 5. a) a b) Základní data ze 2 velkých randomizovaných studií již publikovaných in extenso zkoumajících význam rituximabu v úvodní terapii nově diagnostikovaných nemocných s folikulárním lymfomem. Podle: Marcus et al., Blood 2005, (4a) a Hiddemann et al., Blood 2005 - zde zobrazeno trvání léčební odpovědi (4b). 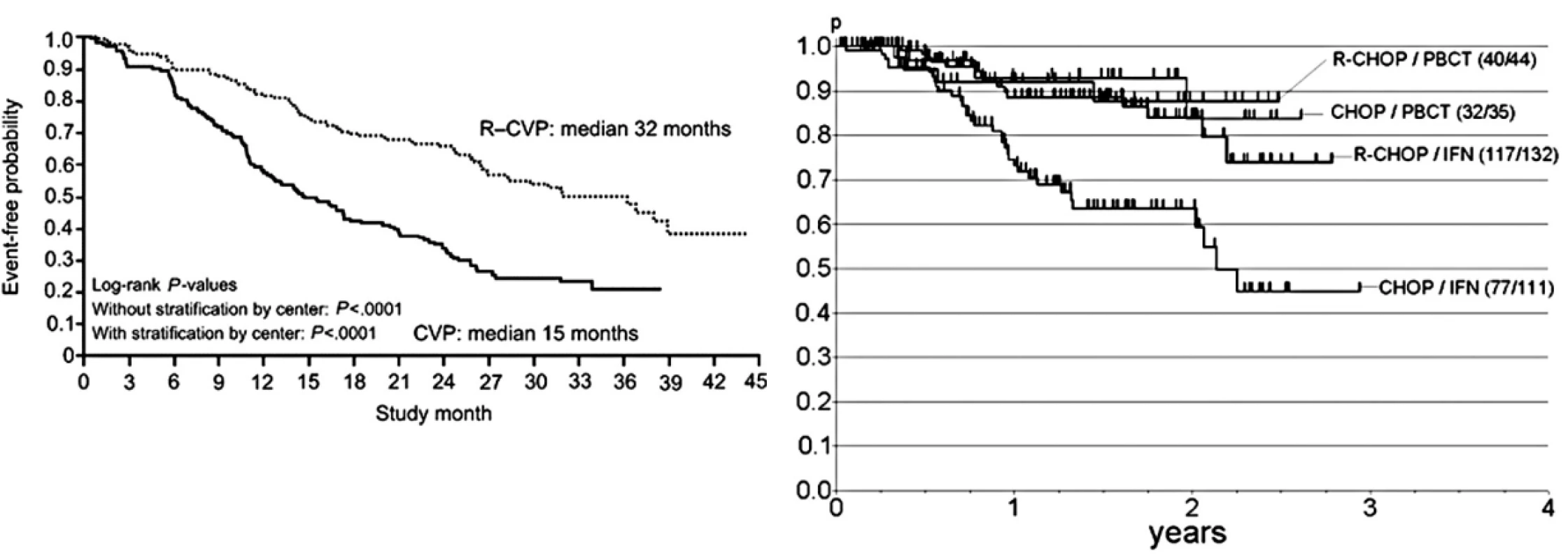
Rituximab u nemocných s relapsem či rezistentní chorobou
Také v této indikaci má přidání rituximabu velký význam, jak ukázaly 2 randomizované studie. Forstpointner et al. (16) ukázali, že přidání rituximabu k režimu FCM (fludarabin, cyclofosfamid a mitoxantron) zlepšuje procento dosažených léčebných odpovědí a přežívání bez známek progrese. Van Oers et al. (17) ukázali u této skupiny nemocných také benefit režimu R-CHOP oproti CHOP.
Rituximab v udržovací terapii
Zde se jedná o novější indikaci tohoto léku a ukazuje se, že je to indikace velmi významná. V současné době jsou k dispozici data z více rozsáhlých studií a výsledky jsou pro přehlednost shrnuty v tabulce 4.
Tab. 4. Velké studie zkoumající využití rituximabu (R) v udržovací terapii u nemocných s folikulárním lymfomem. 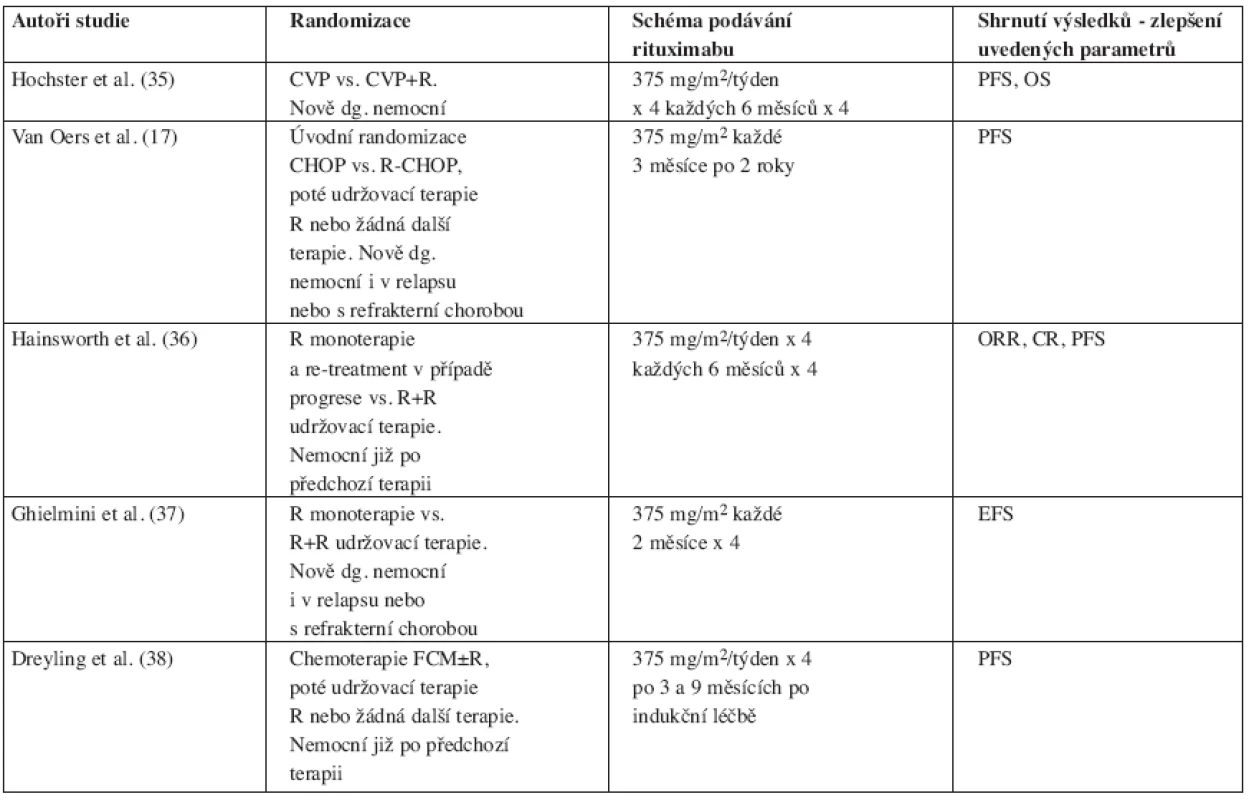
Zkratky: PFS (progression free survival), OS (overall survival), ORR (overall response rate), CR (complete remission), EFS (event free survival). Ibritumomab a tositumomab
Jde o monoklonální protilátky také zaměřené proti osvědčené struktuře CD20, ale spojené zároveň se zdrojem záření. Základní charakteristiky jsou uvedeny v tabulce 5. Tositumomab není u nás registrován, ibritumomab (Zevalin) je pro terapii dostupný. Vzhledem k pouze beta typu záření u preparátu Zevalin se jedná de facto o velmi pohodlnou ambulantní terapii. Před vlastní jednorázovou aplikací se dvakrát podá malá dávka rituximabu, aby se eliminovaly cirkulující B-lymfocyty, které by mohly vyvázat většinu podaného radioaktivního léku. Nejvyšší dávku záření potom absorbuje tumor, kolem 15 Gy, vyšší dávku také absorbují slezina a játra (18). Pochopitelně dojde k určitému ozáření všech orgánů. Výhoda radioimunokonjugátů je v tom, že jsou ozářeny i nádorově buňky v těch místech, kde se vlastní protilátka účinně neváže (tzv. crossfire effect). Vlastní aplikace se provádí na odděleních nukleární medicíny. Hlavním vedlejším účinkem je myelosuprese a proto je nutné, aby pacienti indikovaní pro tento typ terapie měli určitou dřeňovou rezervu (18).
Tab. 5. Základní charakteristiky 2 komerčně dostupných preparátů anti-CD20 konjugovaných se zdrojem radioaktivního záření. 
Ibritumomab byl první radioimunokonjugát, schválený americkou FDA v roce 2002. Ibritumomab (Zevalin) vykazuje signifikantní terapeutickou aktivitu u předléčených nemocných a u nemocných s relapsem či rezistentní chorobou vykazoval lepší léčebné výsledky, než rituximab (19). Použití Zevalinu nevylučuje další následnou terapii nemocného. Zkoumá se využití Zevalinu v souvislosti s autologní transplantací krvetvorných buněk a jako konzolidační terapie na závěr léčby nově diagnostikovaných nemocných (20).
Autologní transplantace krvetvorných buněk
Postavení této léčebné metody kupodivu stále není zcela vyjasněno a další nové léčebné metody, které se objevují, budou jistě tuto indikaci stále ovlivňovat. Principiálně lze uvažovat o použití u nemocných v 1. CR jako konsolidace této remise, nebo u relabujících nemocných. Další otázka je, zdali transplantát tzv. čistit (purging), tedy pokusit se ho zbavit možné příměsi nádorových buněk, ze kterých by mohlo dojít k relapsu, nebo nikoliv a použít transplantát nečištěný. Dvě studie založené na datech z registrů čištění určitým způsobem podporují (21, 22). Existuje ovšem jedna (a jediná) randomizovaná studie, která význam čištění neprokázala, zato ale prokázala význam vysokodávkované terapie u nemocných s relabovanou chorobou jak z hlediska přežití bez příznaku choroby, tak z hlediska celkového přežití (23). Tato studie se nazývala CUP trial (Chemotherapy, Unpurged, Purged transplantation) – viz také obrázek 6.
Obr. 6. Význam tzv. čištění transplantátů a vysokodávkované chemoterapie s podporou transplantace krvetvorných buněk u nemocných s relabovaným folikulárním lymfomem. Podle Schouten et al., J Clin Oncol 2003. 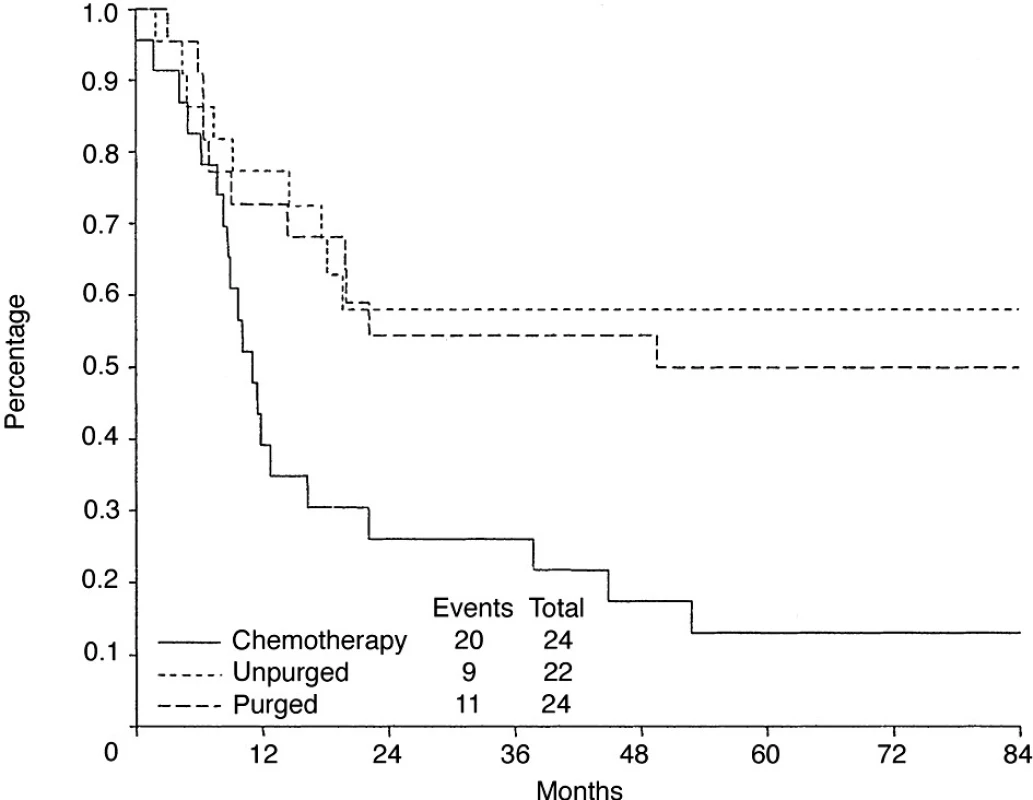
V poslední době byly publikovány tři studie, které zkoumaly význam autologní transplantace pro léčbu nově diagnostikovaných nemocných. Všechno to byly ale studie z doby před érou rituximabu (24–26). Shodovaly se v tom, že je možné dosáhnout intenzivnější terapií delšího bezpříznakového období a jedna dokonce prokázala delší celkové přežití (24). V těchto studiích byla vysokodávkovaná terapie založena na celotělovém ozáření a je zde obava z vyššího rizika sekundárních malignit (26). Jedna již dříve zmíněná studie (27) (tab. 3 a obr. 5b) zahrnovala i nemocné léčené rituximabem. Zatím nepozorovala rozdíly mezi nově diagnostikovanými nemocnými, kteří byli léčeni buďto režimem CHOP nebo R-CHOP s následnou konzolidací vysokodávkovanou radiochemoterapií.
Alogenní transplantace
Alogenní transplantace rozhodně není metodou terapie pro nově diagnostikované nemocné. Je zatížena relativně vysokým procentem různých komplikací. Může se ale stát jedinečnou metodou záchranné terapie pro mladší nemocné s relabující chorobu a má jistě potenciál tyto nemocné choroby definitivně zbavit. Zkušenosti z našeho pracoviště to potvrzují (zatím nepublikovaná data). Výrazné redukce řady závažných toxických projevů mohou dosáhnout moderní tzv. nemyeloablativní režimy nebo režimy s redukovanou intenzitou (28). Proto je potřeba na tuto metodu myslet a vhodné nemocné zavčas odeslat ke konzultaci na specializované pracoviště. Orientační vodítko, kdy o konzultaci požádat, je věk do 60 let, dobrý celkový stav a první relaps choroby. Lze samozřejmě uvažovat o transplantaci i u relapsů pokročilejších.
Další nové terapeutické postupy
Ve fázi intenzivního zkoumání je řada dalších postupů. Zde některé uvedeme jen pro informaci, v žádném případě se nejedná o rutinní postupy. Je však velmi pravděpodobné, že se některé z nich dostanou i do ČR na specializovaná pracoviště ke klinickým zkouškám. Jde např. o:
- Bortezomib ± rituximab
- HGS-ETR1 – mapatumumab, agonista TRAIL-R1 (DR4)
- Epratuzumab (anti-CD22)
- Galiximab (anti-CD80)
- Protinádorové vakcíny
Závěr
Terapie folikulárního lymfomu je nesmírně mnohostranná, podobně jako nakonec i manifestace samotné choroby. Dnes k tomu navíc přistupuje i hledisko finanční, terapie se stává mimořádně drahou. Je-li však dobře vedena, může se také stát i terapií mimořádně účinnou. Za každé situace je potřeba zvažovat všechna pro a proti toho či onoho postupu a pokusit se rozhodnout správně. A to vyžaduje hluboké znalosti a zkušenosti. Proto by terapie této zdánlivě indolentní choroby měla být vedena pouze na pracovištích, kde je toto zaručeno.
Prof. MUDr. Jiří Mayer, CSc.
Interní hematoonkologická klinika FN Brno
Jihlavská 20
625 00 Brno
e-mail: jmayer@fnbrno.cz
Došlo do redakce: 10. 8. 2006
Přijato: 31. 1. 2007
Zdroje
1. Mayer J. Folikulární lymfomy. Lékařská fakulta Masarykovy univerzity Brno, Edice kontinuálního vzdělávání v medicíně, Brno, 2001; 86.
2. Solal-Céligny P, Roy P, Colombat P, et al. Follicular lymphoma international prognostic index. Blood 2004; 101 : 1258–1265.
3. Ardeshna KM, Smith P, Norton A, et al. Long-term effect of a watch and wait policy versus immediate systemic treatment for asymptomatic advanced-stage non-Hodgkin lymphoma: a randomised controlled trial. Lancet 2003; 362 : 519–522.
4. Petersen PM, Gospodarowicz M, Tsang R, et al. Long-term outcome in stage I and II follicular lymphoma following treatment with involved field radiotherapy alone. Proceedings of ASCO 2004; abstract No 6521.
5. Seymour JF, Pro B, Fuller FM, et al. Long-term follow-up of a prospective study of combined modality therapy for stage I-II indolent non-Hodgkin’s lymphoma. J Clin Oncol 2003; 21(11): 2115–2122.
6. Haas RLM, Poortmens P, de Jong BMP, et al. High response rates and lasting remissions after low-dose involved field radiotherapy in indolent lymphomas. J Clin Oncol 2003; 21 : 2474-2480.
7. Orina JN, Moore SG, Lechowicz MJ, Flowers CR. Determining the benefits of chemotherapy for achieving complete response in patients with untreated advanced stage follicular lymphoma: a systematic review and meta-analysis. Blood 2005; 106(11): abctract No 290.
8. Rigacci L, Federico M, Martelli M, et al. The role of anthracyclines in combination chemotherapy for treatment of follicular lymphoma: retrospective study of the Intergruppo Italiano Linfoni on 761 cases. Leukemia and Lymphoma 2003; 44 : 1911–1917.
9. McLaughlin P, Estey E, Glassman A, et al. Myelodysplasia and acute myeloid leukemia following therapy for indolent lymphoma with fludarabine, mitoxantrone, and dexamethasone (FND) plus rituximab and interferon alpha. Blood 2005; 105 : 4573–4575.
10. Nickening C, Dreyling M, Hoster E, et al. MCP (mitoxantrone/chlorambucil/prednisolone) chemotherapy impairs the subsequent collection of stem cells in comparing to CHOP induction in patients with indolent lymphomas – results of a prospective randomized trial of the German Low Grade Lymphoma Study Group. Blood 2005; 106(11): abstract No 3331.
11. Herold M, Schulze A, Niederwieser D, et al. BOP versus COP in advanced indolent lymphomas, results of a randomized multicenter phase III study of the East German Study Group Hematology/Oncology (OSHO). Blood 2002; 100(11): abstract No 3082.
12. Friedberg JW, Cohen P, Cheson BD, et al. Bendamustine HCL (Treanda) treatment results in high rates of objective response in patients with rituximab-refractory and alkylator-refractory indolent B-cell non-Hodgkin’s lymphoma: results from a phase II multicenter single-agent study (SDX-105-01). Blood 2005; 106(11): abstract No 229.
13. Rohatiner AZS, Gregory WM, Peterson B, et al. Meta-analysis to evaluate the role of interferon in follicular lymphoma. J Clin Oncol 2005; 23 : 2215–2223.
14. Mayer J. Klinické využití chimerické monoklonální protilátky Rituximab. Lékařská fakulta Masarykovy univerzity Brno, Edice kontinuálního vzdělávání v medicíně, Brno 2004; 71.
15. Chumchalová J, Trbušek M, Bukovská S, et al. Unexpected antagonistic effect of rituximab with procarbazine disclosed during an in vitro testing of rituximab–mediated sensitization of B-cell lines to commonly used anticancer drugs. Haematologica 2006; 91(Suppl. 1): abstract No 1119.
16. Forstpointner R, Dreyling M, Repp R, et al. The addition of rituximab to a combination of fludarabine, cyclophosphamide, mitoxantrone (FCM) significantly increases the response rate and prolongs survival as compared with FCN alone in patients with relapsed and refractory follicular and mantle cell lymphomas: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 2004; 104 : 3064–3071.
17. Van Oers MHJ, Van Glabbeke M, Teodorovic I, et al. Chimeric anti-CD20 monoclonal antibody (rituximab, Mabthera) in remission induction and maintenance treatment of relapsed/resistant follicular non-Hodgkin’s lymphoma: final analysis of a phase III randomized intergoup clinical trial. Blood 2005; 106:(11): abstract No 353.
18. Marcus R. Use of 90Y-Ibritumomab tiutexan in non-Hodgkin’s lymphoma. Semin Oncol 2005; 32(Suppl. 1): S36–S42.
19. Witzig TE, Gordon LI. Cabanillas F, et al. Randomized controlled trial of Yttrium -90-labelled ibritumomab tiutexan radioimmunotherapy versus rituximab immunotherapy for patients with relapsed or refractory low-grade, follicular, or transformed B-cell non-Hodgkin’s lymphoma. J Clin Oncol 2002; 20 : 2453–2463.
20. Marcus R, Imrie K, Belch A, et al. CVP chemotherapy plus rituximab compared with CVP as first-line treatment for advanced follicular lymphoma. Blood 2005; 105 : 1417–1423.
21. Bierman PJ, Sweetenham JW, Loberiza FR, et al. Syngeneic hematopoietic stem cell transplantation for non-Hodgkin’s lymphoma: a comparison with allogeneic and autologous transplantation - the Lymphoma Working Committee of the International Bone Marrow Transplant Registry and the European Group for Blood and Marrow Transplantation. J Clin Oncol 2003; 21 : 3744–3753.
22. Van Besien K, Loberiza FR, Bajorunaite R, et al. Comparison of autologous and allogeneic hematopoietic stem cell transplantation for follicular lymphoma. Blood 2003; 102 : 3521–3529.
23. Schouten HC, Qian W, Kvaloy S, et al. High-dose therapy improves progression-free survival and survival in relapsed follicular non-Hodgkin’s lymphoma: Results from the randomized European CUP trial. J Clin Oncol 2003; 21 : 3918–3927.
24. Sebban C, Belanger C, Brousse N, et al. Comparison of CHVP + interferon with CHOP followed by autologous stem cell transplantation with a TBI conditioning regimen in untreated patients with high tumor burden follicular lymphoma: results of the randomized GELF94 trial. Blood 2003; 102(11): abstract No 354.
25. Lenz G, Dreyling M, Schiegnitz E, et al. Myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission prolongs progression-free survival in follicular lymphoma: results of a prospective, randomized trial of the German Low-Grade Lymphoma Study Group. Blood 2004; 104 : 2667–2674.
26. Deconinc E, Foussard C, Milpied N, et al. High-dose therapy followed by autologous purged stem-cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma: a randomized multicenter study by GOELAMS. Blood 2005; 105 : 3817–3823.
27. Hiddemann W, Kneba M, Dreyling M, et al. Frontline therapy with rituximab added to the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone (CHOP) significantly improves the outcome for patients with advanced-stage follicular lymphoma compared with therapy with CHOP alone: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 2005; 106 : 3725–3732.
28. Doubek M, Ráčil Z, Mayer J. Klinické využití humanizované monoklonální protilátky ameltuzumab. Lékařská fakulta Masarykovy univerzity Brno, Edice kontinuálního vzdělávání v medicíně, Brno 2006; 103.
29. Young RC, Longo DL, Glatstein E, et al. The treatment of indolent lymphomas: watchful waiting v aggressive combined modality treatment. Semin Hematol 1988; 25(2, Suppl. 2): 11–16.
30. Brice P, Bastion Y, Lepage E, et al. Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa: a randomized study from the Groupe D’Etude des Lymphomes Folliculaires. J Clin Oncol 1997; 15 : 1110–1117.
31. Advani R, Rosenberg SA, Horning SJ. Stage I and II follicular non-Hodgkin’s lymphoma: long-term follow-up of no initial therapy. J Clin Oncol 2004; 22 : 1454–1459.
32. Herold M, Pasold R, Srock S, et al. Rituximab plus mitoxantrone, chlorambucil, prednisolon (R-MCP) is superior to MCP alone in advanced indolent and follicular lymphoma – results of a phase III study (OSHO 39). Ann Oncol 2005; 16(Suppl. 5): abstract No 060.
33. Ladetto M, Ricca I, Benedetti F, et al. Rituximab-supplemented high-dose sequential chemotherapy has superior response rate and event-free survival compared to R-CHOP in poor risk follicular lymphoma at diagnosis: Results from a multicenter randomized GITMO trial. Blood 2005; 106(11): abstract No 675.
34. Foussard C, Mounier N, Van Hoof A, et al. Update of the FL2000 randomized trial combining rituximab to CHVP-Interferon in follicular lymphoma patients. J Clin Oncol 2006; 24(Suppl.): abstract No 7508.
35. Hochster HS, Weller E, Gascoyne RD, et al. Maintenance rituximab after CVP results in superior clinical outcome in advanced follicular lymphoma: results of the E1496 phase III trial from Eastern Cooperative Oncology Group in the Cancer and Leukemia Group B. Blood 2005; 106(11): abstract No 349.
36. Hainsworth JD, Litchy S, Schaffer DW, et al. Maximizing therapeutic benefit of rituximab: maintenance therapy versus re-treatment at progression in patients with indolent non-Hodgkin’s lymphoma – a randomized phase II trial of the Minnie Pearl Cancer Research Network. J Clin Oncol 2005; 23 : 1088–1095.
37. Ghielmini M, Schmitz SFH, Cogliatti SB, et al. Prolonged treatment with rituximab in patients with follicular lymphoma significantly increases event-free survival and response duration compared with the standards weekly x 4 schedule. Blood 2004; 103 : 4416–4423.
38. Dreyling M, Forstpointner R, Gramatzki M, et al. Rituximab maintenance improves progression-free and overall survival rates after combined immuno-chemotherapy (R-FCM) in patients with relapsed follicular and mantle cell lymphoma: final results of a prospective randomized trial of the German Low-Grade Lymphoma Study Group. J Clin Oncol 2006; 24(Suppl.): abstract No 7502.
Štítky
Hematológia Interné lekárstvo Onkológia
Článok vyšiel v časopiseTransfuze a hematologie dnes
Najčítanejšie tento týždeň
2007 Číslo 1- Nejasný stín na plicích – kazuistika
- Těžké menstruační krvácení může značit poruchu krevní srážlivosti. Jaký management vyšetření a léčby je v takovém případě vhodný?
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
-
Všetky články tohto čísla
- Vztah sérových hladin volných lehkých řetězců imunoglobulinu ke stupni pokročilosti mnohočetného myelomu
- Zprávy o knihách
- Porucha v regulácii chromatínu ako molekulárny mechanizmus MLL-ENL leukemogenézy
- Výsledky a komplikace splenektomie u pacientů s těžkou trombocytopenií při ITP rezistentní na úvodní konzervativní léčbu – zkušenosti centra
- Zprávy o knihách
- Od monitorovania hladiny fúzneho génu Bcr/Abl u pacienta s chronickou myeloidnou leukémiou k odhaľovaniu rezistencie k imatinibu – kazuistika
- ÚVODNÍK
- Kaposiho sarkom po alogenní transplantaci periferních krvetvorných buněk s nemyeloablativní přípravou – kazuistika
- 4. ČESKO – SLOVENSKÁ MEZIOBOROVÁ KONFERENCE LÉKAŘSKÉ MYKOLOGIE
- Doporučení Sesterské sekce České Hematologické Společnosti ČSL JEP na obsazení hematologických jednotek intenzivní péče, respektive center pro transplantace krvetvorných buněk, nelékařským personálem.
- Zprávy o knihách
- K osmdesátinám prof. MUDr. Ladislava Chrobáka, CSc.
- Novinky v terapii folikulárního lymfomu
- Dr. Adolf Georg Gadhof, Frankfurt am Main
- Transfuze a hematologie dnes
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Výsledky a komplikace splenektomie u pacientů s těžkou trombocytopenií při ITP rezistentní na úvodní konzervativní léčbu – zkušenosti centra
- Vztah sérových hladin volných lehkých řetězců imunoglobulinu ke stupni pokročilosti mnohočetného myelomu
- Od monitorovania hladiny fúzneho génu Bcr/Abl u pacienta s chronickou myeloidnou leukémiou k odhaľovaniu rezistencie k imatinibu – kazuistika
- Novinky v terapii folikulárního lymfomu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



