-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Kontinentní a inkontinentní derivace moči, měchýř šetřící postupy
Continent and incontinent urinary diversion, bladder sparing approaches
Bladder cancer represents the second most common malignant disease in Europe. The invasive and locally advanced bladder cancers are both urological malignant diseases associated with high mortality rate. The standard surgical treatment for most patients with infiltrating bladder cancer without any marks of generalization includes radical cystectomy. Since radical cystectomy is an extensive surgery (mortality in European studies around 3.7%, early post-operative morbidity 30%) there is a tendency to replace it by less effective but also less demanding therapeutic modalities in elderly patients and patients in whom surgery represents a significant risk. The collective urinary tract has three functions: the one of transportation, storage and evacuation. The individual segments of urinary collective tract are morphologically and functionally inter-related. In case one of the segments is absent (urinary bladder in case of cystectomy, which ensures both storage and evacuation), its function has to be replaced artificially. This substitutive method is called urinary diversion. Ideally the substitution of bladder enables to secure both of its functions – storage and evacuation – in less ideal cases at least replacing the emptying function. Specific segments of gastrointestinal tract are used for urinary diversion. There are several techniques for urinary diversion available. The choice of technique in individual patients is based on objective parameters and surgeon’s preferences. The major objective of any approach is the preservation of physiologic renal function and smooth urinary evacuation if possible. Each choice should be considered individually, based on the objective parameters, including size, localization and biological potential of the tumour, anatomic factors, the overall patient status and comorbidities. The subjective factors include the individual centre and surgeon experience. Of great importance is also detailed and comprehensible discussion with the patient, who must be informed about the individual options, their risks and benefits.
Key words:
bladder cancer, radical cystectomy, urinary diversion, ureteroileostomy, sigma-rectum pouch, heterotopic bladder substitute, orthotopic bladder substitute
Autoři: A. Čermák; D. Pacík; V. Vít
Vyšlo v časopise: Urol List 2012; 10(3): 34-43
Souhrn
Karcinom močového měchýře je druhým nejčastějším onkologickým onemocněním v Evropě. Invazivní a lokálně pokročilý karcinom močového měchýře jsou urologické malignity s vysokou mortalitou. Základem chirurgické léčby většiny pacientů s infiltrujícím nádorem močového měchýře bez známek generalizace je radikální cystektomie. Radikální cystektomie je rozsáhlý operační výkon (mortalita v evropských studiích kolem 3,7 %, časná pooperační morbidita kolem 30 %), a proto je u pacientů v pokročilejším věku či s vysokým operačním rizikem nahrazována sice méně efektivními, ale i méně zatěžujícími terapeutickými modalitami. Vývodné cesty močové mají funkci jednak transportní, funkci rezervoáru a funkci evakuační. Jednotlivé úseky vývodných cest močových na sebe morfologicky i funkčně navazují. Pokud některá část chybí (v případě cystektomie to je močový měchýř, který má funkci jímací a evakuační), je třeba jeho funkci nahradit jiným způsobem. Tento náhradní způsob se označuje jako derivace moči. Náhrada funkce močového měchýře spočívá v ideálním případě v zajištění obou jeho funkcí, tedy jímací i evakuační, v méně příznivých případech v náhradě alespoň jeho funkce evakuační. Pro močovou derivaci se používají některé části gastrointestinálního traktu. V rekonstrukční části operace je k dispozici řada typů operací zajišťujících derivaci moči. Jejich volba u konkrétního nemocného je dána mimo parametry objektivní také zvyklostmi pracoviště a jednotlivých operatérů. Rozdělení operací zajišťujících derivaci moči můžeme provádět podle různých kritérií. Základním cílem všech je zachování fyziologické funkce ledvin při pokud možno bezproblémová eliminace moči. Každá volba by měla být posuzována individuálně a vždy závisí na několika objektivních parametrech, jako jsou velikost, lokalizace a biologický charakter tumoru, anatomické poměry, celkový zdravotní stav nemocného a jeho přidružené choroby. Mezi subjektivní faktory můžeme zařadit zkušenosti pracoviště a operatéra. Důležitá je také srozumitelná a podrobná předoperační informovanost a diskuze s pacientem, který musí být seznámen s možnostmi volby typu derivace moči, jejich výhodami a riziky.
Klíčová slova:
karcinom močového měchýře, radikální cystektomie, derivace moči, uretroileostomie, sigma-rektum pouch, heterotopická neovezika, ortotopická neovezikaRadikální cystektomie (RACE), ať již klasická otevřená nebo laparoskopická, roboticky asistovaná (RoRACE), jsou metody propracované a mají své dané indikace. Derivace moči po cystektomii je způsob, jak co nejvíce fyziologicky nahradit původní jímací a evakuační funkci dolních cest močových. V několika posledních dekádách byla vyvinuta řada způsobů derivace. Jejich výběr závisí na urologovi a jeho pacientovi. Při rozhodování o výběru metody je třeba volit způsob s největším benefitem pro pacienta, je třeba dodržovat zásady fyziologie organizmu, indikace a kontraindikace a v neposlední řadě je nutné respektovat přání pacienta.
V současné době je možné používané derivace rozdělit do tří hlavních skupin: 1. derivace střevním konduitem (obvykle ileálním segmentem), 2. ortotopická neovezika a 3. pouch s katetrizovatelným stomatem. Tyto tři skupiny mají řadu variací, jsou různě technicky složité a mají různý vliv na fyziologické pochody v organizmu. Podle toho, jak se přibližují fyziologické funkci dolních cest močových, mají také dopad na kvalitu života pacienta.
HISTORIE
Urologie vznikla a soustavně se rozvíjela jako operační disciplína v rámci všeobecné chirurgie. Není bez zajímavosti, že nejdéle známou operací na světě je operace urologická – cirkumcize. Ve starém Egyptě byla cirkumcize prováděná ještě pazourkovým nožem. Její indikace však nebyly jen zdravotní, nýbrž zpočátku nábožensko--kultovní a společenské. Cirkumcize byly původně vyhrazeny jen šlechticům. Přístup na královský faraonův dvůr byl povolen jen obřezaným. Lékařská péče se ve starověku soustředila z praktických důvodů na neduhy močových orgánů. Z nich se nejčastěji vyskytovaly močové kameny. O tom, že jimi lidstvo trpělo od pradávna, svědčí nálezy močových kamenů v mumiích až 9 000 let starých. Není tedy divu, že operační vynětí močových kamenů bylo už v nejstarších dobách vedle operace katarakty, cirkumcize a amputace končetin jedinou známou operační léčbou civilizace označované jako civilizace nilská [10]. S operací močových cest, i když v jednodušší podobě, se tedy setkáváme od počátku civilizace.
Historické informace o použití trávicího ústrojí k derivaci moči jsou zaznamenány již před 160 lety. V roce 1852 v Londýně Sir John Simon operoval 13letého chlapce, kterému vytvořil cíleně píštěl mezi terminálními úseky močovodů a rektem. Ureteroproktostomii zajistil protažením terminálních částí močovodů extrofického měchýře do rekta. Hedvábné stehy protáhl do rekta pomocí stříbrné trubičky zavedené do terminálního úseku uretru pomocí jehly vyrobené z hodinového péra. Vznikla tak píštěl, která měla zajistit drenáž moči do střevního segmentu. Pacient však za rok zemřel na kalkulózní pyelonefritidu [1,2]. Komplikace, především refluxní pyelonefritidy, vedly k dalším pokusům a nutně k rozvoji nových technik.
Od konce 19. stol. se začíná datovat éra příspěvků také českých chirurgů do světové chirurgie a urologie. Rozvoj medicíny v 18. a 19. stol. byl tehdy spojen s rozvojem vysokého učení, tj. tehdejších univerzit, které v Českých zemích byly dvě – od 14. stol. v Praze a od 16. stol. v Olomouci. V celém Habsburském mocnářství byla však skutečným centrem vzdělání Vídeň a Praha.
Na vídeňské univerzitě působila na lékařské fakultě řada vynikajících českých profesorů, kteří proslavili českou vědu po celé Evropě. Vzpomeňme alespoň na některé z nich: z chirurgů to byl především prof. Eduard Albert, nar. v Žamberku r. 1841, dále prof. Rokytanský, prof. Škoda a další. Z mladší generace chirurgů vynikal především prof. Karel Maydl (1853–1901), který po obnovení české lékařské fakulty Karlovy univerzity přestoupil z Vídně do Prahy a stal se prvním přednostou české chirurgické kliniky lékařské fakulty, a dále jeho žák a nástupce prof. Otakar Kukula (1867–1925). Oba se v rámci všeobecné chirurgie věnovali i chorobám urologickým a zanechali po sobě nesmazatelnou stopu v evropské urologické vědě. Prof. Maydl vypracoval a publikoval originální operační metodu k nápravě exstrofie močového měchýře a prof. Kukula publikoval monografii O lithiase močového měchýře v Čechách, která byla ve své době jednou ze stěžejních publikací pro rodící se urologii evropské úrovně [10]. Zmíněný Karel Maydl provedl v roce 1892 v Praze antirefluxní operaci s použitím terčíku trigona implantovaného do sigmatu [3,4]. Podle Maydlem vytvořené intususcepce na jejunostomii byl zkonstruován a je používán antirefluxní mechanizmus močových derivací. Karel Pawlik vytořil v roce 1889 první ortotopickou neoveziku u ženy. Jako rezervoár použil pochvu [5]. V roce 1962 referoval Eduard Hradec práci o použití netubulizovaného střeva ke tvorbě neovezik u žen [6]. V moderní době naší urologie má nezastupitelné místo Ladislav Jarolím, který jako první v roce 1993 zahájil v tehdy nově vzniklé České republice (ale i Slovenské republice) používání ženské neoveziky z detubulizovaného střeva [7–9]. Ladislav Jarolím byl i nadále průkopníkem a realizátorem nových metod a technik, které uváděl do praxe, a tak se s nimi bylo možno seznámit ve světovém písemnictví. K derivaci moči bylo zpočátku nejčastěji používáno sigma, ale již zmínění refluxní komplikace způsobené vysokým intraluminálním tlakem vedly ke vzniku nových metod. V 50. letech minulého století byla nejrozšířenější ureteroileostomie, která chránila horní cesty močové a nezatěžovala organizmus metabolickou acidózou ze zpětného vstřebávání moči stěnou trávicího ústrojí [11]. V 80. letech se prakticky přestalo používat k tvorbě rezervoárů střevo v tubulární podobě a byla zahájena éra nízkotlakých rezervoárů [12,13]. Sférický nebo oválný tvar vytvořený z tubulární struktury umožňuje touto rekonfigurací vytvoření většího objemu a vykazuje podle fyzikálních zákonů nižší intrakavitální tlak. Větší objem, ale hlavně nízký tlak jsou základní požadavky při tvorbě močových rezervoárů, aby byla chráněna ledvinná funkce. Při detubulizaci, kdy je protínána celá stěna střevního segmentu na antimezenteriální (eventuálně antimezokolické) straně, provádíme především protnutí cirkulárních a spirálovitých svalových snopců, čímž dosahujeme porušení typických peristaltických stahů. Rekonfigurací střeva a sešitím jiných částí stěny vytvoříme rezervoár s peristaltickými a antiperistaltickými vlnami, které vytváří proti sobě interakci, a nevzniká tak náhlé lokalizované zvýšení intrakavitálního tlaku. Detubulizací vznikne plochý obdélníkový štěp. Ten je možné meandrovitě nebo spirálně složit a konfigurovat do požadovaného tvaru. Meandrovitě lze uspořádat pouch do tvaru U, S, Z, W, spirálovitě lze vytvořit až dvě otočky. Vždy ovšem musíme dbát na to, aby nedošlo k přetočení zaškrcení cévní stopky mezenteria a k ischemii a následné infarsaci použitého segmentu.
TYPY DERIVACE MOČI
- inkontinentní ureteroileostomie
- rezervoáry s kontinentním kutánním stomatem – heterotopické rezervoáry
- kontinentní náhrady močového měchýře, tzv. ortotopické substituce
- kontinentní derivace moči kontrolované análním sfinkterem
- paliativní derivace
Inkontinentní ureteroileostomie
Ileální klička nebo konduit. V roce 1950 představil Bricker metodu, při které použil krátký (15–20cm) segment distální části ilea pro derivaci moči po cystektomii [11]. Močovody oddělné od močového měchýře byly anastomozovány k poximálnímu konci exkludové kličky terminálního ilea. Transport moči byl zajištěn střevním segmentem, který byl vyveden jako kožní stomie. Moč je poté jímána do zevního zařízení (sáčku), který je připevněn k samolepicí podložce na kůži. K rozšíření této techniky přispěly následující faktory: dostatečná délka tenkého střeva, která je obvykle k dispozici i po ozařování pánve, pohyblivost segmentu, dostatečné cévní zásobení spolehlivými cévními arkádami mezenteria tenkého střeva, snadná proveditelnost techniky a menší výskyt komplikací (ve srovnání s ureterosigmoideostomií). Při nutnosti následné radioterapie na oblast malé pánve nedochází k poškození především močovodů.
Graf 1. Použití jednotlivých typů derivací (R. Hautman et al. pro WHO – 7 000 pacientů). 
Výhody: technická jednoduchost, méně metabolických komplikací.
Nevýhody: vyžaduje speciální jímače (urinály), místo stomie nesmí být v kožní rýze (vstoje, v předklonu, vsedě), okolí stomie musí být hladké, bez jizev.
Rezervoáry s kontinentním kutánním stomatem – heterotopické rezervoáry
Kontinentní rezervoáry s cévkovatelným stomatem umožňují jímání moči do pouche z detubulizované části střeva. Moč je z rezervoáru odváděna pomocí intermitentní katetrizace malým kožním stomatem. Tento druh derivace je vhodný u pacientů, u nichž byla odstraněna uretra z důvodu nádoru infiltrujícího nebo přesahujícího hrdlo močového měchýře nebo postihujícího močovou trubici. Kontinentní rezervoár se vytváří z delšího segmentů (50–75 cm) tenkého stř̌eva. Detubulizací a kombinací segmentů tenkého i tlustého střeva (Indiana pouch) a v některých případech pomocí části žaludku je vytvořen nízkotlaký rezervoár sférického tvaru. Močovody jsou pro zabránění refluxu anastomozovány ve směru izoperistaltického ileálního segmentu intususcepcí s vytvořením papily nebo tunelizovanou reimplantací v místě tenie tlustého střeva.
Obr. 1A. Inkontinentní ureteroileostomie; 
Obr. 1B. RTG obraz ureteroileostomie, vylučovací urografie. 
Stoma lze vytvořit z apendixu nebo tubularizované části tenkého střeva. Kontinence je zajištěna vytvoř̌ením podslizničního kanálu a vytvořením tunelizované implantace do rezervoáru. Ihned po operaci je nutná trvalá derivace s pravidelným vyplachováním pouche malým množstvím sterilního fyziologického roztoku (50 ml) s vyplachováním hlenu vytvořeného střevní sliznicí. Rezervoár postupně, až po několika měsících, zvětší svůj objem do velikosti umožňující katetrizaci každých 6 hod. Pokud nedojde k přeplnění rezervoáru, je systém dostatečně kontinentní i v noci.
Pro tento způsob derivace (kontinentní rezervoár s cévkovatelným stomatem) jsou indikovaní pacienti nevhodní pro implantaci ortotopické neoveziky (např. po radioterapii). Nejvhodnějšími kandidáty pro tuto techniku jsou mladší pacienti, kteří se chtějí vyhnout používání zevního zařízení. Vybraní pacienti musejí být dostatečně motivovaní a informovaní o nutnosti přísné rehabilitace (ve srovnání s Brickerovou derivací).
Obr. 1. Izolovaný střevní segment pro vytvoření rezervoáru Indiana pouch. 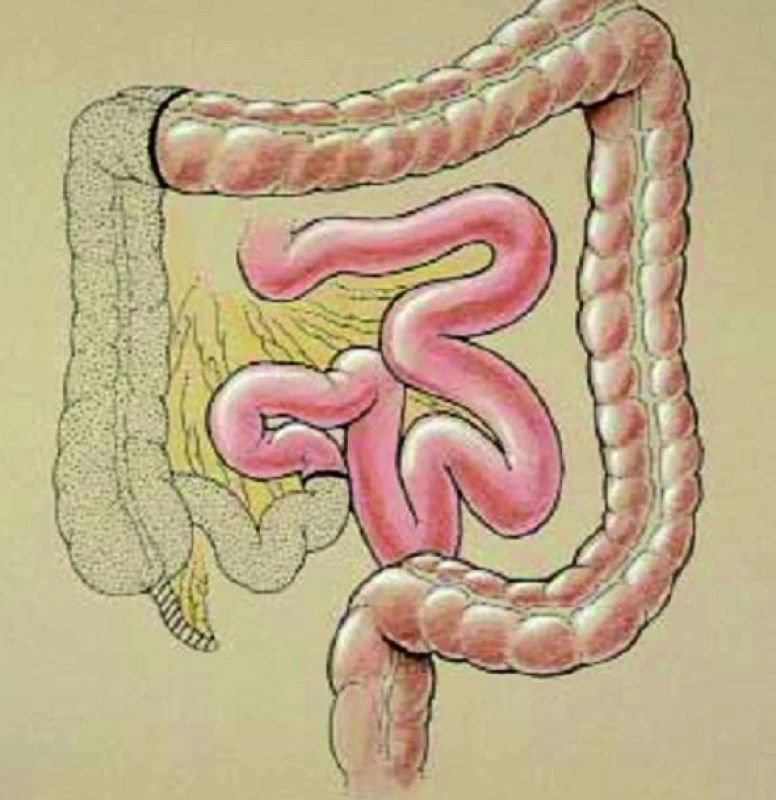
Obr. 2. Detubulizace segmentu kolon na antimezenteriální straně. 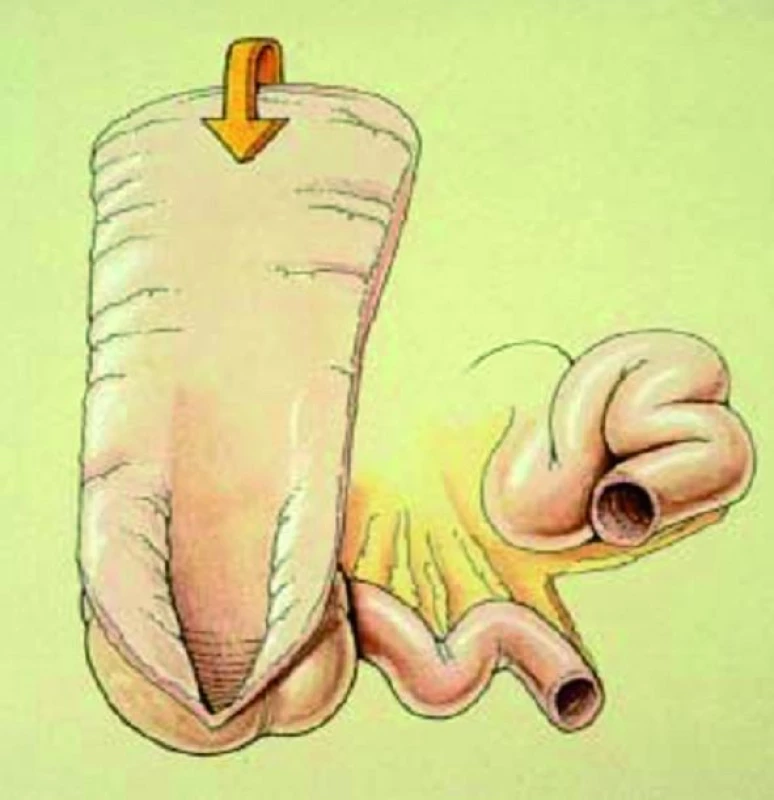
Obr. 3. Rekonfigurace kolon a vytvoření rezervoáru Indiana pouch. 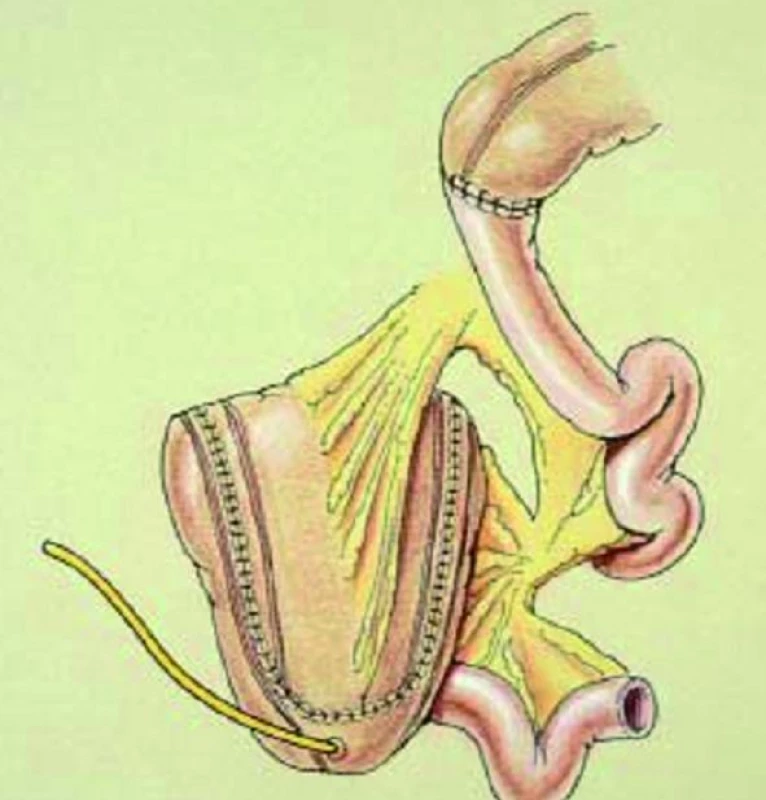
Kontinentní náhrady močového měchýře, tzv. ortotopické substituce
Nízkotlaký rezevoár
Tuto metodu je možné provádět u správně vybrané skupiny pacientů (obě pohlaví), u nichž byla zachována močová trubice. Močový měchýř je kompletně odstraněn včetně prostaty semenných váčků. Při této technice je rezervoár vytvořený z detubularizované části střeva umístěné v pánvi.
Nejčastěji se používají rezervoáry z ilea podle Hautmanna, Kocka a Studera. Neovezika podle Richarda Hautmanna [14] je konstruována z detubulizovaného ilea konfigurovaného do tvaru písmene W a s antirefluxní Le Ducovou implantací ureterů [15]. Nils Kock použil pro antirefluxní implantaci ureterů intususcepci přívodné kličky [16]. Technika Urse Studera je založena na modelaci neoveziky z 40–44 cm detubulizovaného ilea a ponechání tubulizované, 20 cm dlouhé přívodné kličky, do které jsou implantovány uretery bez antirefluxního mechanizmu [17].
Neovezika je napojena na ponechanou močovou trubici jako při radikální prostatektomii. Kontinence je zajištěna ponechaným funkčním svěračem. Tato technika se původně prováděla pouze u mužů. V současné době je tato indikace rozšířena také u žen, u nichž umožňuje zachování distálních 2/3 močové trubice dosažení výborného stupně kontinence (musí být splněna kritéria onkologické bezpečnosti). Pacienti se vyprazdňují pomocí břišního lisu, mají slabší proud moči a v některých případech musejí pro dosažení úplného vyprázdnění provádět autokatetrizaci. Doba rehabilitace, během níž dochází k postupnému zvětšování objemu rezervoáru, je delší než v případě ileálního konduitu – až po několika měsících se rezervoár zvětší do velikosti umožňující pacientovi močit jednou za 6 hod. Tento způsob derivace umožňuje dosáhnout výborné kontinence během dne. V průběhu noci trpí řada pacientů noční inkontinencí. V případě retence močové je nutno močový měchýř vyprázdnit autokatetrizací.
Obr. 4. Zúžení eferentní větve rezervoáru. 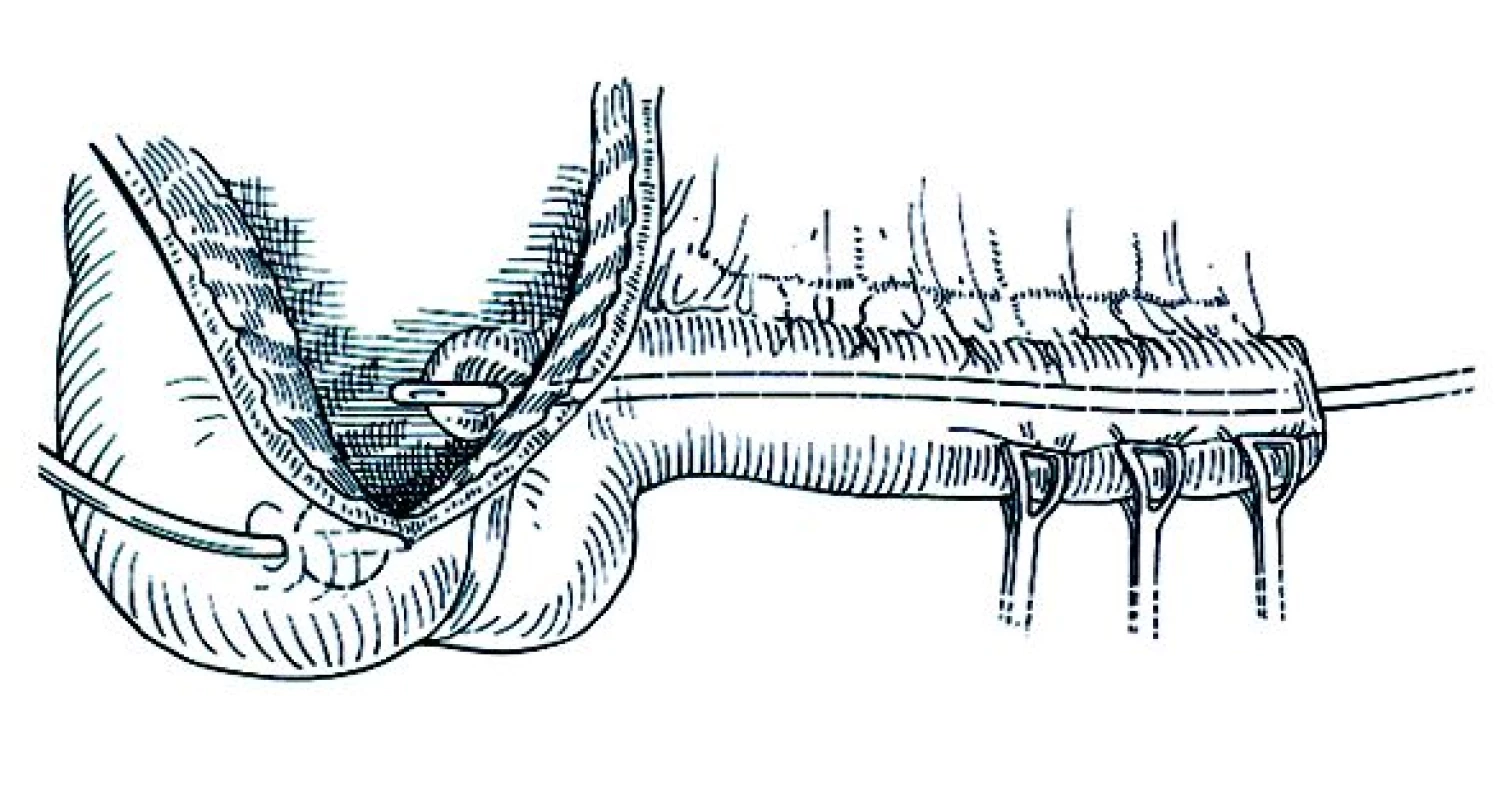
Obr. 5. Dokončení zúžení eferentní větve, odstranění tkáně GIA staplerem. 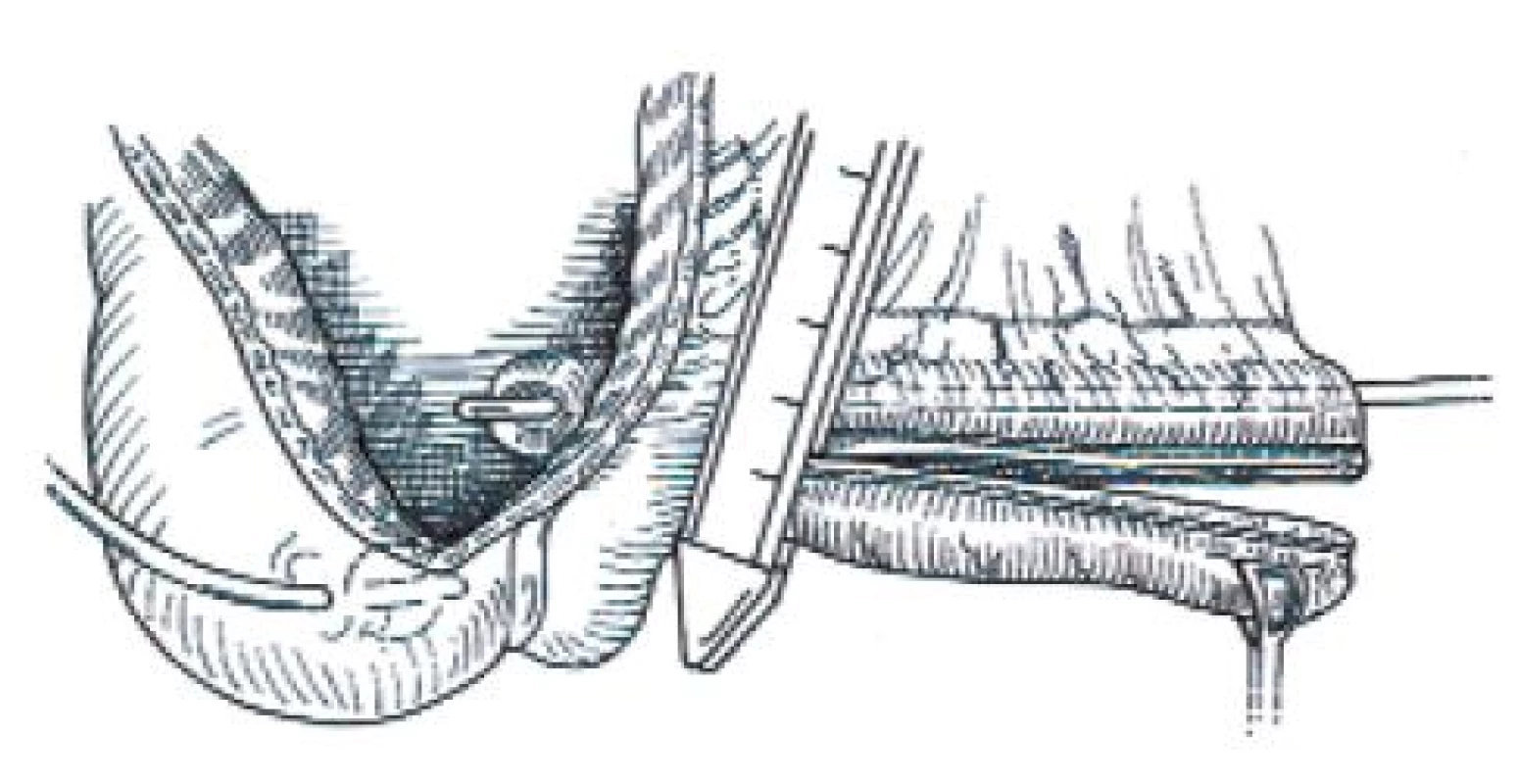
Obr. 6. Plikace ileocékální chlopně 5–7 Lembertovými stehy. Stehy blíže céka jsou širší než stehy směrem k eferentní větvi. Po dotažení stehů svírá eferentní větev se stěnou céka úhel 90°. Při zavádění katétru F18 je mírný odpor. Těsnost chlopně a správnou kontinenci dosáhneme uvolněním nebo přidáním stehů. 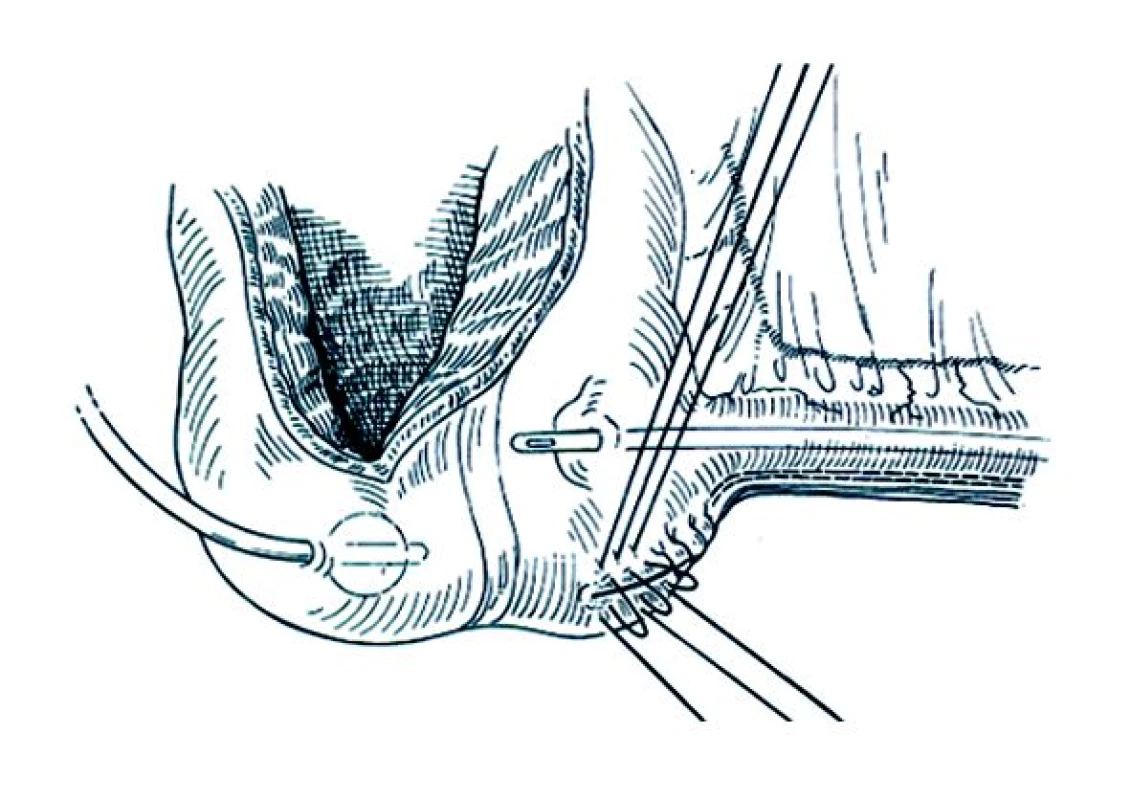
Kontinence
Kontinence je obsažena v názvu metody. Z důvodu, že je při radikální cystoprostatektomii odstraněn detruzor močového měchýře a svalová vlákna v oblasti prostatické močové trubice, nelze očekávat dosažení 100% kontinence a současného kompletního vyprázdňování neoveziky. Rozdíly jsou v denní a noční kontinenci. Zhruba 85–90 % pacientů dosahuje denní kontinence bez vložky nebo s jednou vložkou [1]. Noční inkontinence se pohybuje mezi 20 a 30 % operovaných [18].
Vyprazdňování neoveziky (vzhledem k absenci svalových vláken detruzoru) se děje pomocí břišního lisu. Pacient musí být důkladně poučen o nácviku mikce, která se děje zvýšením intraabdominálního tlaku použitím tzv. Valsalvova manévru, eventuálně v kombinaci s Crédeho hmatem. Ideální je nácvik s opakovaným kontrolováním postmikčního rezidua ultrazvukovým (UZ) vyšetřením. Toto vyšetření může provádět lékař nebo sestra pomocí jednoduchého přístroje BladderScan®. Nácvik správného vyprazdňování a Crédeho hmatu je možné provádět až po úplném zhojení operační rány.
Indikace
Ortotopická neovezika je vhodná pro pacienty s minimální rizikem recidivy bez potřeby adjuvantní radioterapie. Nevhodná je u pacientů polymorbidních, s renální insuficiencí, stavů před radioterapií nebo po RT.
Sexuální funkce
Podstatná část mužské populace s invazivním nádorem močového měchýře indikovaným k radikální cystektomii se věkově nachází v období šestého decenia a méně. To znamená, že v řadě případů se jedná o sexuálně aktivní muže, pro které je informace o zhoubném onemocnění, ale i o pravděpodobnosti ukončení sexuální aktivity, velkým zásahem do psychiky a kvality života (QL). Z tohoto důvodu se především v posledním desetiletí řada chirurgických škol a pracovišť začala zabývat otázkou operačních technik šetřících sexuální funkce a zachovávajících lepším způsobem kontinenci. Tyto techniky jsou však většinou založeny na nižší onkologické radikalitě operačního výkonu. K dispozici máme v současnosti zhruba tři typy výkonů, které se liší svým rozsahem, radikalitou, vlivem na zachování sexuálních funkcí, ale také možným snížením úrovně onkologické bezpečnosti. Jedná se o:
- výkony šetřící nervy
- výkony šetřící chámovod, semenné váčky a prostatické pouzdro nebo část prostaty
- výkony šetřící chámovod, semenné váčky a prostatu
V případě nervy šetřících výkonů dochází k zachování potence u 17–100 % pacientů, její prezervace klesá ve věkové skupině nad 60–65 let, při současném provedení uretrektomie a u unilaterálních výkonů. Denní kontinence je zachována u 80–100 % a noční u 47–75 % pacientů. V případě výkonů šetřících chámovody, semenné váčky a část prostaty dochází k zachování potence u 80–100 % pacientů. Denní kontinence je zachována u 79–100 % a noční u 31–100 % pacientů. V případě výkonů šetřících chámovody, semenné váčky a celou prostatu dochází k prezervaci potence u 70–100 % a antegrádní ejakulace u 50 % pacientů. Kontinence bývá zachována u 95–100 % pacientů přes den a 74–88 % pacientů v noci.
Z rozboru publikovaných prací vyplývá, že v posledních dvou desetiletích došlo a stále dochází k rozvoji operačních technik, pomocí nichž je možné u mužů po radikální cystektomii zachovat sexuální funkce. Zdá se, že existuje určitá nevelká skupina mužů, která může z těchto postupů profitovat. Bude se jednat o muže mladšího věku s příznivými onkologickými charakteristikami nádoru. Přesnější indikační kritéria však bude nutné teprve stanovit a vývoj v této oblasti půjde nepochybně ruku v ruce se zdokonalováním diagnostiky, předoperačního stagingu a ostatních druhů léčby nádorů močového měchýře a prostaty [19,20].
Obr. 8A. Příprava střevního segmentu W, ortotopická neovezika dle Hautmana. 
Obr. 8B. Konfigurace neoveziky dle Hautmanna. 
Obr. 8C. Umístění neoveziky do pánve a anastomóza střeva s uretrou. 
Kontinentní derivace moči kontrolované análním sfinkterem
Ureterosigmoideostomie byla velmi populární v polovině minulého století, avšak komplikace vzniklé v důsledku této techniky vedly k postupnému opouštění metody. Nezávažnějšími komplikacemi byla pyelonefritida, poruchy acidobazické rovnováhy, poškození renálních funkcí a závažné změny v elektrolytovém hospodářství. Rudolf Hohenfellner z Mainzu vytvořil nízkotlaký rektosigmoidální rezervoár, který snížil počet komplikací [21,22]. Novými typy, které opět snížily počet komplikací, jsou Mainz pouch II a Motol pouch. Princip úpravy ureterosigmoideostomie je v detubulizaci střeva (Mainz pouch II) a v dalším oddělení močových cest od střevního segmentu střeva s pasáží stolice (Motol pouch) [23–25]. Metoda je relativně jednoduchá a nabízí alternativu u starších pacientů. Nevýhodou je skutečnost, že při dlouhodobém působení moči na střevní sliznici (mladší pacienti s dlouhou dobou přežití) je popsán vyšší výskyt nádorového onemocnění zažívacího traktu.
Indikace
Nízkotlaký rezervoár kontrolovaný análním sfinkterem je vhodný u pacientů starších s kratší dobou přežití. Pacient musí mít předoperačně vyloučenou neurogenní poruchu měchýře a musí být schopen udržet v rektu náplň tekutiny alespoň 400 ml. Musí být poučen, že nelze očekávat obvyklý průběh flatulence. Metoda není vhodná u stavů po ozáření pánve ani u pacientů s předpokládanou radioterapií.
Paliativní derivace
Paliativní derivace se používá, jak již název napovídá, u stavů, kdy nelze provést jiný typ derivace. Paliativní derivace slouží k zajištění drenáže moči u stavů pokročilého onemocnění či při celkově špatném stavu a krátké předpokládané době přežití. Jedná se o případy, kdy nelze provést cystektomii nebo již cystektomie byla provedena, ale došlo k progresi onemocnění lokálně nebo metastázováním do lymfatických uzlin a vznikla obstrukce vývodných cest močových s následnou uremií. V některých případech nelze provést derivaci z důvodu onemocnění střeva nebo při stavech po ozáření či při četných plastických srůstech v dutině břišní. Nejjednodušší metodou je založení punkční nefrostomie v lokální anestezii. Rizika nefrostomie jsou inkrustace, ucpávání, infekce a nutné pravidelné výměny. Alternativou je kožní ureterostomie. Kožní ureterostomie může být vyvedena oboustranně, samostatně pro každý močovod. V případě, že je možné provést břišní operaci, lze vytvořit anastomózu močovodů a ty vyvést jako jednostrannou kožní stomii. Rizikem kožní ureterostomie je její postupná stenotizace (8,3 %).
Výhody perkutánní nefrostomie:
- jedná se o přímou derivaci ledviny
- umožňuje sledovat separovaně diurézu z drénované ledviny
- výkon lze provést i za přítomnosti pokročilých patologických změn v močovém měchýři a prostatě i v dutině břišní
- nefrostomický přístup lze využít k antegrádnímu zavedení ureterálního stentu
Nevýhody:
- pacient má mimotělní drenáž, která způsobuje dyskomfort a zhoršuje kvalitu života
- nefrostomie se může dislokovatmoč často kolem nefrostomie v určitém malém množství obtéká a irituje okolní kůži
- při výkonu může dojít k poranění okolních orgánů
- punkce nedilatovaného dutého systému ledviny je obtížná
- dechové exkurze znesnadňují punkci pohybující se ledviny
- často dochází k zalomení mimotělní části nefrostomického drénu nebo odvodné části sběrného sáčku, což vede k obstrukci drenáže
- jedná se o cizorodý materiál, který zvláště při malém příjmu tekutin inkrustuje
- zvláště při špatné průchodnosti může docházet k uroinfekci
- jsou nutné pravidelné výměny [26]
To je způsobeno tím, že sliznice tenkého střeva umožňuje volný průnik vody vyrovnávající koncentraci s koncentrovanější močí vyloučenou ledvinami během noci, což vede navzdory dehydrataci ke zvýšení objemu moči. Konstrukce kontinentních rezervoárů (ať již ortotopických či katetrizovatelných) je kontraindikována u pacientů s narušenou renální funkcí (Cr > 2,0). Tito pacienti mají vyšší riziko vzniku závažných metabolických komplikací vyvolaných rozsáhlým absorpčním povrchem stř̌eva.
Obr. 9A. Konfigurace střeva pro neoveziku Kock pouch. 
Obr. 9B–D. Intususcepce přívodné kličky. 
Obr. 9E. Konfigurace rezevoáru Kock pouch. 
Komplikace
Každý způsob derivace moči je alternativa funkce močových cest. Každou funkci (transportní, jímací a evakuační) lze nahradit s menším nebo větším úspěchem. Nikde se však, vzhledem ke specifickým vlastnostem urotelu, nejedná o rovnocennou náhradu. Tkáňové inženýrství zatím neumožňuje vytvoření plnohodnotné náhrady.
Časné pooperační komplikace
Míra časných pooperačních komplikací je zhruba 16 % a jen malá část souvisí s derivací moči. Obvykle se jedná o komplikaci rozsáhlého operačního výkonu – cystektomie a derivace moči.
Ileus
Ileus je reakce na déletrvající rozsáhlý operační výkon a manipulaci se střevem. Peroperačně je zaváděna nazogastrická sonda (NGS), která je ponechána v časném pooperačním období a v krátkém časovém úseku slouží k enterální výživě. V našem pooperačním schématu zahajujeme enterální výživu první pooperační den, aby byla podpořena peristaltická aktivita střeva. Je potřeba dodávat přípravky, které se vstřebávají v dvanácterníku a proximální části ilea. Autoři velkých center doporučují ponechání nazogastrické sondy jen po nezbytně krátkou dobu, protože pacient polyká vzduch kolem sondy do žaludku a NGS tento vzduch neodvádí. Dochází tak k distenzi žaludku a zvýšené náplni střev plynem.
Ischemie stomatu
Při poruše cévního zásobení může dojít k ischemii. Ta vzniká při nesprávném ošetření cévních arkád. Vzniká buď ischemie při podvazu cév nebo tlaková ischemie při vytahování vaskulárního pediklu zvláště u obézních pacientů.
Urinózní sekrece
Při dehiscenci některé části novotvořeného systému může docházet k urinózní sekreci. Vždy, když je sekrece většího objemu tekutiny z drénů, je třeba pomýšlet na únik moči. Zvýšená sekrece může být z důvodu peritoneální sekrece, lymfatické nebo urinózní sekrece. Je nezbytné provést biochemický rozbor sekretu, a pokud jsou hodnoty kreatininu vyšší, než je normální sérová hodnota, je třeba hledat místo úniku. V první řadě je třeba propláchnout ureterální stenty a katétry do rezervoáru. Radiologickými zobrazovacími metodami se snažíme nalézt místo úniku. Naprostou většinu případů lze zhojit konzervativně.
Krvácení
Ihned po operaci obvykle dochází k hemorhagické sekreci, která záhy ustává. Pokud krvácení přetrvává a má odezvu na poklesu krevního obrazu, je nutné vyšetřit a eventuálně korigovat patologické koagulační parametry. Při větším krvácení z drénů i přes konzervativní terapii je nutné přistoupit k operační revizi.
Oligurie, anurie
Nižší výdej moči jde obvykle na vrub nedostatečné nebo nesprávné pooperační péče. V našich podmínkách vždy peroperačně nebo předoperačně zavádíme centrální venózní katétr pro monitorování centrálního žilního tlaku (CŽT). CŽT nám dává přesnou informaci o potřebě substituce tekutin. Vždy při nesprávné bilanci tekutin je třeba vyšetřit celou močovou soustavu k vyloučení obstrukce horních cest močových nebo retenci moči v přeplněném rezervoáru.
Obr. 10A. příprava segmentu ilea dle Studera (44 cm detubulizovaného střeva, 22 cm izoperistaltické přívodné kličky). 
Obr. 10B. Konfigurace neoveziky, sešití zadních částí detubulizovného střeva. 
Obr. 10C. Sešití předních částí střeva a vytvoření rezervoáru. 
Obr. 10D. Konfigurace Studer pouch. 
Obr. 10E. Anastomóza neoveziky s uretrou. 
Plicní embolie, žilní trombóza
Jakékoli operace v malé pánvi, a tou cystektomie s lymfadenektomií bezesporu jsou, mohou být komplikovány žilní trombózou a embolií. Funkční vyšetření (dopplerovké vyšetření žil) a biochemická vyšetření (D-dimery apod.) a zobrazovací vyšetření (CT plic, scintigrafie plic) musí vyloučit podezření na embolizační příhodu. Podle rozsahu onemocnění by měla být zvážena plná antikoagulační terapie nebo zavedení filtru do dolní duté žíly.
Urosepse
Předoperační příprava obvykle zajistí průběh bez infekčních komplikací. V našem protokolu musí mít pacient před operací negativní nález v moči. Předoperačně standardně připravujeme střevo jednorázovým vyrázdněním ortográdním roztokem. Těsně předoperačně nebo perioperačně aplikujeme širokospektré antibiotikum a metronidazol. K infekci může dojít i v pooperačním období. V případě obstrukce horních cest močových nebo při přeplnění rezervoáru je nutné zajistit průchodnost drenů. V případě ucpávání drénu hlenem jsou nuntné pravidelné šetrné proplachy tak, aby byla zajištěna průchodnost drenů, ale nebyl poškozen rezervoár přeplněním. Další situace mohou vzniknout při infikování nahromaděné tekutiny v dutině břišní (infikovaná lymfokéla, hematom, urinom). Zde je potřeba zajistit vyprázdnění abscesové dutiny, obvykle postačí perkutánní drenáž a aplikace antibiotik podle kutivačního nálezu.
Pozdní pooperační komplikace
Nejčastěji používanou tkání pro močovou derivaci je střevní segment. Ten má však jiné vlastnosti, především resorbční a sekreční. Čím větší je plocha střeva a čím proximálnější segment je použit, tím jsou významnější metabolické změny. S metabolickými změnami by měl být důkladně seznámen každý operatér, protože dobře provedená operace je jen část úspěchu. Důsledná péče po celý zbytek pacientova života je předpokladem pro dobrou kvalitu života bez komplikací.
Metabolické poruchy
Trvalý kontakt střevní sliznice s močí ovlivňuje elektrolytové hospodářství a jaterní metabolizmus. Vzniká meta-bolická acidóza, poruchy tvorby a vstřebávání vitaminů, vstřebávání žlučových kyselin. Z poruchy metabolizmu minerálů vzniká osteomalacie. Míra negativních vlivů je úměrná rozsahu expozice, době působení moči ve střevě a stavu renálních funkcí [1].
Hypechloremická acidóza
Při expozici moči secernuje střevní sliznice natriové a bikarbonátové ionty. Reabsorbuje ionty amoniové, vodíkové a chloridové. Hlavní roli ve vlivu na pH vnitřního prostředí hraje transport natriových a vodíkových iontů výměnou za ionty amoniové (NH³ a NH4), které jsou reabsorbovány. Amoniový iont tak působí jako kompetitivní inhibitor absorpce natria. Amoniové ionty se váží na chlor, a tím vzniká hyperchloremická acidóza. V ileu je absorpce K+ větší než ve tlustém střevě.
Použití tračníku může vést k hyperosmolaritě séra s následným poklesem hladiny aldosteronu, vyvolávajícím zvýšenou sekreci adiuretinu. Tyto metabolické poruchy působí vysokou koncentraci moči, ze které sliznice tračníku absorbuje více natria a chloridových iontů.
Vstřebávání chloru klesá s prodlužující se dobou od vytvoření intestinální derivace. Pacienti s renální insuficiencí a děti mají nižší schopnost kompenzovat metabolickou acidózu. Je u nich proto výhodné užít pro derivaci žaludeční segment. Žaludek je primárně sekreční orgán s významnou sekrecí vodíkových a chloridových jontů, a acidóza proto při jeho užití pro močovou derivaci nehrozí.
Obr. 11A. Mainz pouch II – vytvoření rezervoáru. B. Mainz pouch II – implantace močovodů. 
Obr. 11B. Mainz pouch II – implantace močovodů. 
Obr. 12A. RTG snímek perkutátnní nefrostomie s dilatovaným močovodem. 
Obr. 12B. Zavedená perkutánní nefrostomie. 
Korekce metabolické hyperchloremické acidózy spočívá v podávání alkalizujících prostředků, jako je natrium bikarbonát (NAHCO3). Užívají se tablety obvykle 500 mg několikrát denně. Jejich množství se určuje podle aktuálního pH podle vyšetření acidobazické rovnováhy. Antacida mohou na druhou stranu ovlivňovat resorpci dalších léčiv. Proto je doporučováno dodržovat mezi podáním dalšího léku alespoň tříhodinový interval. Dlouhodobá aplikace může způsobit poruchu vstřebávání fosfátů skrze mechanizmus reakce hliníku s fosfáty za vzniku nerozpustných solí. Důsledkem může být osteomalacie. U kardiaků je dobré volit lék s nízkým obsahem sodíku. U nemocných s poruchou funkce ledvin je třeba dávat pozor na rozvoj hypermagnezemie.
Porucha vstřebávání vitaminu B12
Vitamin B12 je důležitý především pro správnou funkci krvetvorby, podílí se na syntéze DNA a ATP a je nezbytný pro správnou funkci nervového systému. Hlavním zdrojem tohoto vitaminu v potravě jsou živočišné produkty: vejce, mléko, sýry, maso a vnitřnosti.
Vitamin B12 se primárně absorbuje v terminálním ileu. Po resekci terminálního ilea roste riziko nedostatku tohoto vitaminu, což se projeví až po vyčerpání zásob, to je po 3–5 letech. Užití < 50 cm terminálního ilea může způsobovat nedostatečné vstřebávání vitaminu B12. Nedostatek vitaminu B12 může vést k ireverzibilním neurologickým a hematologickým poruchám. V důsledku více vlivů se u postižených projevují známky deprese, dezorientace a drobné poruchy paměti. Vyšším projevem nedostatku vitaminu je megaloblastická anémie a poškození nervového systému, které mohou vést až k projevům Alzheimerovy choroby. Od doby 1–5 let po operaci vyžadující užití více než 50 cm části ilea se doporučuje monitorovat hladinu tohoto vitaminu. Substituce spočívá v nitrosvalové aplikaci vitaminu B12 v dávce 100 μg/měsíc.
Obr. 13B. Vyvedení kožní ureterostomie. 
Porucha kostního metabolizmu
Chronická acidóza ovlivňuje kostní metabolizmus aktivací osteoklastů s následkem kostní resorpce a zhoršuje a-hydroxylaci 25-hydroxycholelalciferolu v ledvinách vedoucí k deficitu vitaminu D. Jeho absorpce je zhoršena i kvůli resekci ilea. Nedostatek vitaminu D působí poruchu kostní mineralizace. Kostní minerály – kalcium, karbonát a natrium se při acidóze spotřebovávají směnou za vodíkové.
Průjem
Při tvorbě kontinentního rezervoáru z delších částí ilea (až 75 cm) se ve vzácných případech (< 1 %) vyskytuje neustupující průjem nebo malabsorpce. Je vhodná úprava dietního režimu a medikamentózní terapie po konzultaci s gastroenterologem.
Infekce močových cest
Pozitivní nález leukocytů a bakterií v moči ze stomie (ureteroileostomie nebo z rezervoáru) vede často praktické lékaře k nasazování razatní antibiotické terapie, přestože většina pacientů je asymptomatických. Nezřídka se jedná o moč odebranou z jímacího sáčku. Terapii je nutno zahájit v případě, že infekce je symptomatická. Vždy je nutno vyloučit obstrukci horních cest močových a litiázu.
Tvorba hlenu
Pro tvorbu kontinentního rezervoáru je potřeba velká část střevního segmentu. Ten, i když je použit pro derivaci moči, má stále vlastnosti střeva a reaguje na humorální podněty gastrointestinálního systému. Výsledkem je tvorba hlenu. Hlen se může hromadit v rezervoáru a pacient není schopen jej vymočit. V tom případě jsou nutné proplachy 50 ml sterilního fyziologického roztoku. Důležité je provést instilaci, ale také aktivní odsátí, protože zavedeným drénem hlen obvykle neodteče. K mukolýze lze použít N-acetylcystein – např. ACC® Long 1–2 šumivé tab. denně.
Tvorba močových konkrementů
Většina konkrementů je asymptomatická. Konkrementy jsou objeveny náhodně nebo při pátrání po příčině recidivující uroinfekce nereagující na antibiotika. V rezervoáru je někdy objeveno až neuvěřitelné množství velkých konkrementů. Příčinou je uroinfekce, tvorba hlenu a nedostatečné vyprazdňování pouche. Solitární konkrementy se obvykle vyskytují jako inkrustace na svorce nebo stehu. Většina konkrementů je tvořena struvitem. U pacientů s litiatickou anamnézou musíme vyloučit litiázu v průběhu horních cest močových. Zde jsou konkrementy nejčastěji detekovány v místě ureterointestinální anastomózy. Litiázu lze odstranit pomocí klasického endoskopického instrumentária. Vždy je nutno pečlivě dbát na kompletní odstranění všech reziduálních fragmentů. To může být v případě objemného rezervoáru někdy obtížné. Při nálezu objemných konkrementů je výhodnější provést operační revizi a z malé incize provést extrakci veškeré litiázy.
Obtížné cévkování stomatu
Obtížné zavedení cévky do stomatu paradoxně nebývá způsobeno jeho stenózou, ale naopak při jeho rozšíření. Široké lumen stomie nejčastěji v prefasciální oblasti může způsobovat obtíže při zavádění cévky. Někdy dochází k jivení a stenotizaci kožní stomie. V obou případech je potřebná operační revize.
Obr. 7. RTG obraz asymptomatické litiázy v Indiana pouch. 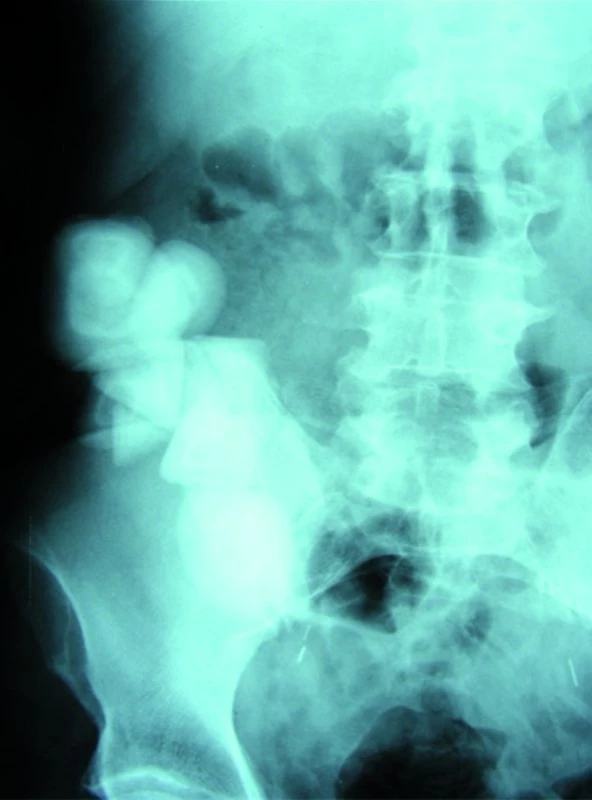
Obr. 8. Extrakce mnohočetné litiázy z pouche. 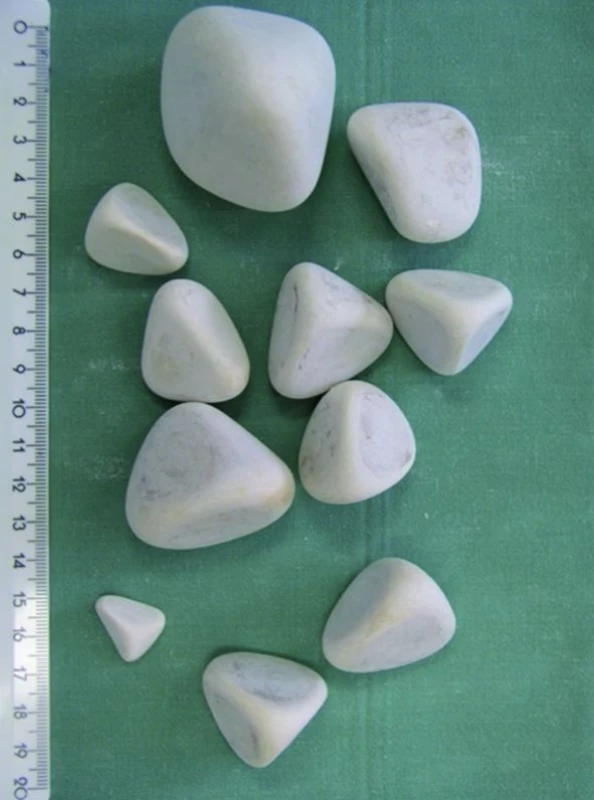
Hydronefróza
Hydronefróza jako pozdní komplikace vzniká nejčastěji v důsledku striktury ureterointestinální anastomózy. Zavedení stentu nebo dilatace má jen dočasný efekt a velmi rychle recidvuje. Pro nápravu je obvykle nutná operační revize. Další příčiny hydronefrózy mohou být stenóza stomie (méně často) nebo zúžení aferentní chlopně. Obstrukce z důvodu recidivujícího karcinomu vyžaduje obvykle pouze paliativní řešení zavedením punkční nefrostomie.
Parastomální hernie
Parastomální hernie vzniká obvykle až za určité období po operaci. Nejčastěji se vyskytuje u ureteroileostomie dle Brickera. Obvykle vzniká v místě, kde prochází mezenterium. U katetrizovatelného stomatu, zvláště do oblasti umbiliku, vzniká zřídka. Vyklenutí parastomální hernie činí funkční potíže s aplikací a netěsností nalepovací podložky jímače. Vždy je nutná chirurgická korekce. Důležité je, aby v místě korekce byly miminální jizvy, protože ty způsobují další komplikace s netěsnostmi podložky. Vhodné je provést střední laparotomii a provést úpravu defektu fascie z vnitřní strany stěny břišní.
Tab. 1. Metabolické komplikace: selektivní vstřebávání v jednotlivých částech střeva. 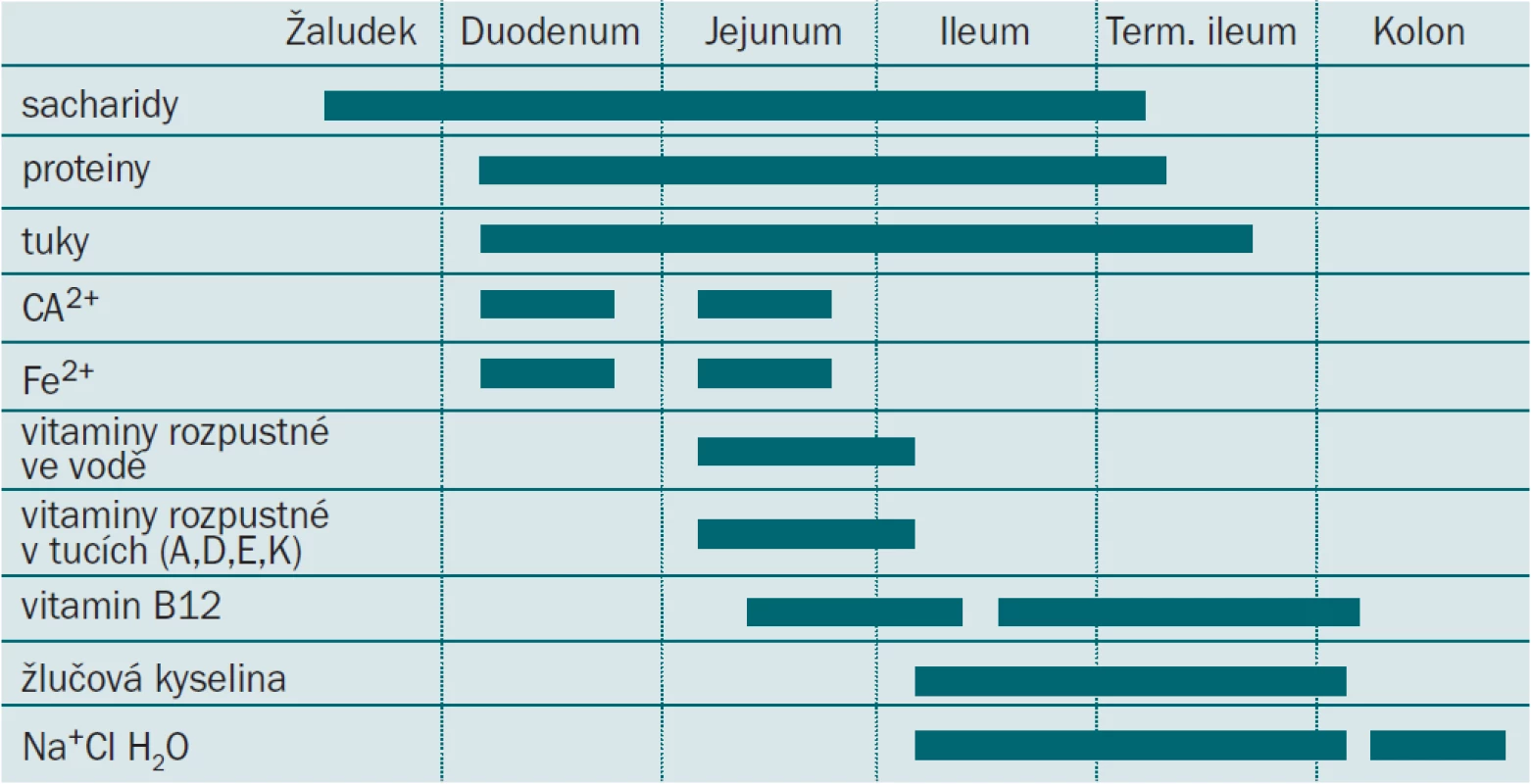
Karcinom ureterointestinální anastomózy
Při dlouhodobé expozici (15–20 let) byl popsán výskyt karcinomu střeva. Častější výskyt byl při chronickém působení moči na sliznici trávicího traktu s obsahem stolice. To se týkalo především náhrad kontrolovaných análním sfinkterem. Zejména u pacientů s makroskopickou hematurií se doporučuje provádět pravidelné endoskopické vyšetření rezervoáru, včetně cytologického a bioptického odběru.
ZÁVĚR
Cystektomie a derivace moči představují rozsáhlý operační výkon a významný zásah do kvality pacientova života. Vždy musí být dodržena zásada onkologické bezpečnosti. Výběr vhodného typu derivace závisí na celkovém stavu pacienta, na jeho přání a očekávání. Pacient musí být před operací důkladně poučen, aby neměl nerealistická očekávání. Pacient musí být schopen dodržovat doporučení a musí být schopen spolupracovat, aby nedošlo k poruše funkce zvoleného typu derivace moči.
prim. MUDr. Aleš Čermák
Urologická klinika FN Brno
Jihlavská 20, 625 00 Brno
acermak@fnbrno.cz
Zdroje
1. Jarolím L. Derivace moči po cystektomii. Urol List 2008; 6(2): 53–59
2. Simon J. Ectopia vesicae (absence of the anterior walls of the bladder and pubis abdominal parieties); operation for directing the orifices of the ureters into the rectum; temporary success; subsequent death; autopsy. Lancet 1852; 2 : 568–570.
3. Maydl K. Prvé případy radikálního léčení rozštěpeného měchýře. Čas Lék Čes 1894; 33 : 337–343.
4. Maydl K. Neue beobechtungen von ureterenimplantaionen in die flexura romana bei ectopia vesicae. Wien med Wschr 1896; 46 : 1241, 1333, 1373.
5. Pawlík K. Exstirpace močového měchýře. Čas Lék Čes 1890; 29 : 705–706.
6. Hradec E. Chirurgische behandlung der strahlenschäden an der weiblichen harnblase. Urol Int 1962; 14 : 89–110.
7. Jarolím L, Babjuk M, Hanuš T et al. Ortotopická náhrada močového měchýře u ženy po cystektomii se zachováním funkční uretry. Rozhl Chir 1996; 75(4): 222–226.
8. Jarolím L, Babjuk M, Hanuš T et al. 20 orthotopic neobladders in females. Eur Urol 1996; 30 : 264.
9. Jarolím L, Babjuk M, Hanuš T et al. Female urethra sparing cystectomy and orthotopic bladder replacement. Eur Urol 1997; 31(2): 173–177.
10. Kučera F, Záťura F. Urologie jako samostatný vědní obor. Čes Urol 1998; 1 : 34–35.
11. Bricker EM. Bladder substitution after pelvic evisceration. Surg Clin N Am 1950; 30(5): 1511–1521.
12. Thüroff JW, Alken P, Riedmiller H et al. 100 cases of Mainz-pouch (mixed augmentation ileum "n zecum for bladder augmentation and continent urinary diversion. World J Urol 1985; 11(3): 179–184.
13. Jarolím L. Kontinentní ileocékální měchýř (Mainz pouch). Rozhl Chir 1988; 67(10): 625–632.
14. Hautmann RE. The ileal neobladder to the female urethra. Urol Clin North Am 1997; 24(4): 827–835.
15. Jarolím L. Le Ducova implantace ureterů do neoveziky. Rozhl Chir 1989; 68(11): 714–717.
16. Skinner DG, Boyd SD, Lieskovsky G et al. Lower urinary tract reconstruction following cystectomy: experience and results in 126 patients using the Kock ileal reservoir with bilateral ureteroileal urethrostomy. J Urol 1991; 146(3): 756–760.
17. Studer UE, Danuser H, Merz VW et al. Experience in 100 patients with an ileal low pressure bladder substitute combined with an afferent tubular isoperistaltic segment. J Urol 1995; 154(1): 49–56.
18. Smith E, Yoon J, Theodorescu D. Evaluation of urinary continence and voiding function: early results in men with neo-urethral modification of the Hautmann orthotopic neobladder. J Urol 2001; 166(4): 1346–1349.
19. Zachoval R, Záleský M, Vik V et al. Sexuální funkce šetřící radikální cystektomie. Urol List 2008; 6(2): 36–47.
20. Colombo R, Bertini R, Salonia A et al. Overall clini - cal outcomes after nerve and seminal sparing radical cystectomy for the treatment of organ confined blad - der cancer. J Urol 2004; 171(5): 1819–1822.
21. Hohenfellner R. Ureterosigmoidostomy. Revisite Akt Urol 1990; 21 : 63–66.
22. Fisch M, Hohenfellner R. Der sigma-rektum pouch: eine modifikation der harnleiterdarmimplantation. Akutelle Urol 1991; 22 : 1–9.
23. Fisch M, Wammack R, Mueller SC et al. The MAINZ pouch II (Sigma rectum pouch). J Urol 1993; 149(2): 258–263.
24. Jarolím L, Babjuk M, Hanuš T et al. Kontinentní močová derivace s použitím detubulizovaného rektosigmatu (sigma-rectum pouch) Čas Lék Čes 1996; 135 : 664-667.
25. Jarolím L, Babjuk M, Hanuš T et al. One layer suture in Mainz pouch II – 50 cases. Eur Urol 1996; 30 : 755.
26. Zachoval R, Urban M, Záleský M et al. Double J stent versus nefrostomie při drenáži horních močových cest. Urol List 2004; 2 : 43–46.
Štítky
Detská urológia Urológia
Článek Slovo úvodemČlánek Ze zahraničních periodik
Článok vyšiel v časopiseUrologické listy
Najčítanejšie tento týždeň
2012 Číslo 3- Vyšetření T2:EGR a PCA3 v moči při záchytu agresivního karcinomu prostaty
- Lék v boji proti benigní hyperplazii prostaty nyní pod novým názvem Adafin
-
Všetky články tohto čísla
- Minimálně invazivní, ablační techniky při léčbě malých renálních tumorů
- Lokalizované nádory ledvin, epidemiologie, etiologie, chirurgická léčba, operační postupy a jejich indikace, role lymfadenektomie
- Roboticky asistovaná radikální cystektomie: technika podle Mayo Clinic
- Slovo úvodem
- Kontinentní a inkontinentní derivace moči, měchýř šetřící postupy
- Opakovaná hospitalizace a míra výskytu komplikací u pacientů po PCNL v závislosti na komorbidních faktorech
- Hodnota léčby, riziko a zodpovědnost v urologické praxi
- Kompletní duplikace měchýře a uretry jako organická příčina dysfunkce dolních močových cest
- Raritní komplikace zavedení double J stentu – migrace do pravé síně srdeční
- Současný pohled na léčbu malých nádorů ledvin
- Ze zahraničních periodik
- EAU Guidelines pro laserové technologie
- Urologické listy
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Raritní komplikace zavedení double J stentu – migrace do pravé síně srdeční
- Kontinentní a inkontinentní derivace moči, měchýř šetřící postupy
- Současný pohled na léčbu malých nádorů ledvin
- Roboticky asistovaná radikální cystektomie: technika podle Mayo Clinic
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




