-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vyšetření aktivity destičkových funkcí se vztahem k rezistenci na kyselinu acetylsalicylovou
Autoři: J. Malý
Působiště autorů: II. interní klinika Lékařské fakulty UK a FN, Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc.
Vyšlo v časopise: Vnitř Lék 2005; 51(2): 157-162
Kategorie: Editorialy
Editorial: Stejskal D et al. Vnitř Lék 2004; 50(8): 591–599 a dvěma „Dopisům redakci“, uveřejněným v tomto čísle časopisu Vnitřní lékařství.
Byl jsem požádán, abych se vyjádřil k polemice mezi doc. MUDr. M. Peckou, CSc. a prim. MUDr. D. Stejskalem, která probíhá na stránkách časopisu Vnitřní lékařství a týká se článku Stejskal D et al. Využití stanovení agregability trombocytů po indukci kationickým propylgalátem v odhadu recidiv kardiovaskulárních komplikací [15].
Nebudu se zabývat tím, zda se mají používat SI jednotky v rukopise – jde o samozřejmou náležitost, ani tím, zda se má použít standardní průměr odběrové jehly. Laboratorním pracovníkům je jasné, že vzhledem k nestabilitě destiček má být odběr ke stanovení funkcí destiček proveden za standardních a neměnných kautel a za přítomnosti laborantky.
Polemika i článek jsou však zajímavé ze dvou pohledů a těm bych se chtěl věnovat:
- a) hledisko metodiky vyšetřování destičkových funkcí a významu pro klinické závěry;
- b) hledisko laboratorního průkazu a klinického významu aspirinové rezistence.
K metodické části bych chtěl poukázat na nutnost enormní opatrnosti s odběry materiálu na vyšetření funkcí krevních destiček a na opatrnost při zacházení se vzorky. Krevní destičky se snadno aktivují a udržet je v neaktivním stavu až do okamžiku vyšetření žádá značnou zkušenost a obratnost. Aktivity destiček v primární hemostáze jsou vzájemně provázány a agregace je pouze jednou nedílnou součástí primární hemostázy.
Krevní destičky v primární hemostáze se aktivují ve čtyřech krocích. Změny jsou schematicky ukázány na obr. 1:
- a) adherují na poškozený endotel a umělé povrchy;
- b) uvolňují ze zásobních granulí aktivační působky, především ADP;
- c) agregují spolu a vytvářejí hemostatickou zátku;
- d) vytvářejí prokoagulační povrch pro aktivní koagulační proteiny.
Obr. 1. Aktivace krevních destiček v hemostáze. 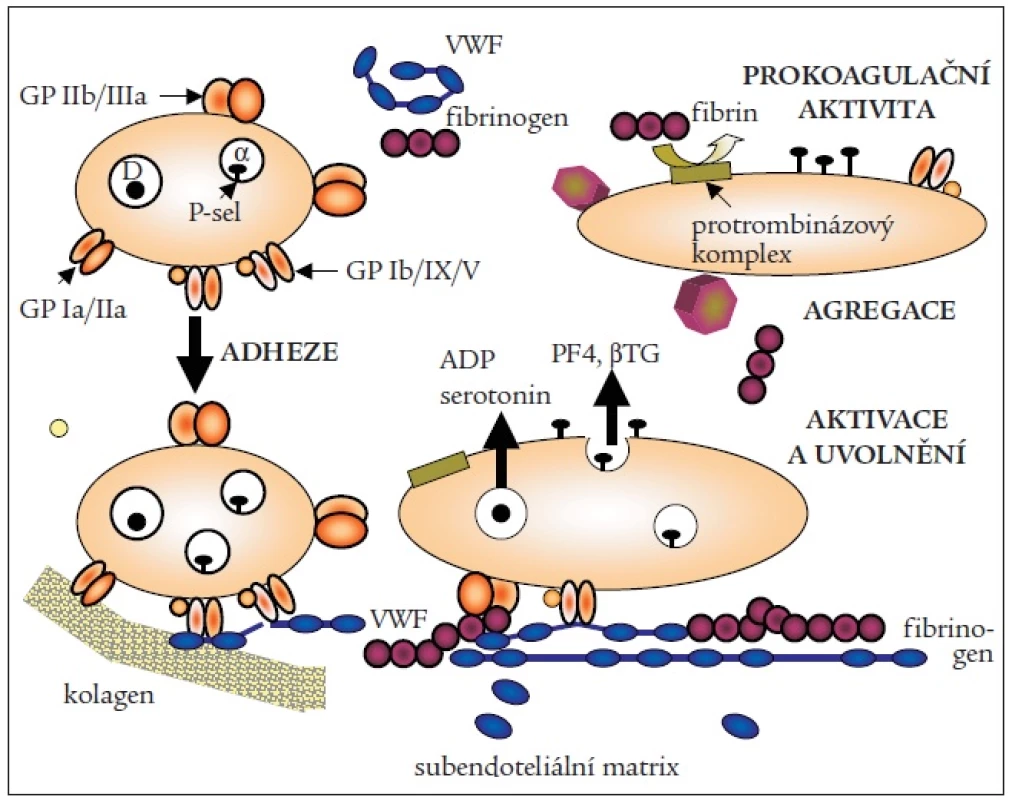
vWF – von Willebrandův faktor, GP IIb/IIa – glykoprotein IIb/IIIa, GP Ia/IIa – glykoprotein Ia/IIa, GP Ib/IX/V – lykoprotein Ib/IX/V, PF4 – destičkový faktor 4, β TG – β tromboglobulin, ADP – adenozindifosfát Destičky jsou stimulovány poraněním endotelu a adherují k subendoteliální matrix a absorbují plazmatické proteiny včetně von Willebrandova faktoru a fibrinogenu. Destičky adherují na von Willebrandův faktor pomocí receptoru destičkových glykoproteinů (GP) Ib/IX/V a prostřednictvím fibrinogenu pomocí glykoproteinu (GP) IIb/IIIa. Adherující destičky mění po kontaktu s kolagenem svůj tvar. Vytvářejí pseudopodie a rozprostírají se po exponovaném povrchu. Současně s tím dochází ke změnám povrchových vlastností membrány destiček a k uvolňovací reakci. Destičková adheze stimuluje intracelulární signál, který vede k uvolnění destičkového faktoru 4 (PF4) a β tromboglobulinu (β TG) růstového destičkového faktoru, faktoru V a dále trombospondinu z α granulí, zároveň se uvolňují fosfolipidy, které dovolují zahájení koagulační reakce na povrchu destiček a vedou k tvorbě fibrinu. Adenozindifosfát (ADP) se uvolňuje z denzních granulí a aktivuje GP IIB/IIIa receptor a podmiňuje agregaci krevních destiček. Spolu s ním se uvolňuje z denzních granulí ATP, serotonin a Ca2+ ionty.
Hlavními fyziologickými induktory agregace je ADP a tromboxan A2 (TXA2), který vzniká metabolickým pochodem zahájeným aktivací destičkové fosfolipázy. Na agregaci se též podílí trombin vzniklý v malém množství na povrchu destiček. Agregace trombocytů je závislá na přítomnosti dvou dalších glykoproteinů (GP IIb a Gp IIIa) v membráně destiček, fibrinogenu a Ca2+. Fibrinogen spojuje destičky a podmiňuje tím tvorbu agregátů. Zatímco TXA2 podporuje uvolňování ADP, druhý prostaglandin – prostacyklin PGI2, který vzniká v cévních endoteliích uvolňováním ADP, brzdí, inhibuje agregaci destiček a zabraňuje tvorbě destičkových trombů mimo místo poranění. Vede navíc k lokální vazodilataci.
Při vyšetřování destičkových funkcí je vždy ošidné se soustředit na vyšetření jedné z destičkových aktivit, zejména proto, že reakce v primární hemostáze jsou provázané a krevní destička je schopna vyvolat například agregační odpověď nejméně 5 nezávislými podněty.
Vyšetřovací metody destiček se v minulých desetiletích soustředily především na zjišťování krvácivých stavů destičkového původu. Metod, jak prokázat destičkovou hyperaktivitu a z ní usuzovat na větší schopnost trombogeneze, je poměrně málo a jejich interpretace je pro komplexnost změn a interakce s endotelem a krevními elementy stále problematická. Vyšetření destičkových funkcí se často omezuje pouze na vyšetření agregace krevních destiček a z tohoto vyšetření se dělají zásadní klinické závěry. Vyšetření agregace destiček je jedna laboratorní metoda se svými metodickými zásadami a specifickou interpretací. Při pátrání po chorobách destiček zůstává základním přístupem k vyšetření destičkových funkcí vyšetření anamnézy a fyzikální vyšetření. Další vyšetřovací metody jsou uvedeny v tab. 1.
Tab. 1. Základní vyšetřovací metody při zjišťování poruch destičkových funkcí. 
Nejužívanější laboratorní metodou k vyšetření funkce destiček je vyšetření agregace destiček. Vyšetření destičkové agregace se provádí jednak z plné krve pomocí impedanční techniky nebo v destičkami bohaté plazmě (PRP) turbidimetrickou technikou. Agregace destiček z plné krve se vyšetřuje často v souvislosti s uvolňováním ADP z denzních granulí na lumiagregometru. Turbidimetrické měření agregace destiček vyžaduje přípravu PRP z plné krve. Na kvalitu vyšetření destičkové agregace mají vliv četné faktory, především počet destiček, teplota, stupeň a rychlost míchání a čas provedení výkonu. Jestliže není stanovení aktivity destiček provedeno do 3 hodin od odběru krve ze žíly, není výsledek možno považovat za validní. S výsledky testu často interferuje léčba, protože destičkové funkce ovlivňuje přímo řada léků a i složení potravy. Turbidimetrické stanovení agregace krevních destiček využívá spektrofotometrie, kdy dochází ke změnám průchodu světla suspenzí destiček po přidání agonistů. K vyvolání agregace se běžně užívá ADP a adrenalin, po kterých dochází k dvouvlnové agregační křivce, přičemž první vlna je odpovědí na aktivaci membránového glykoproteinu IIb/IIIa a druhá vlna vychází z vyprázdnění zásobních granulí. Ostatní agonisté – kyselina arachidonová, trombin a kolagen – vyvolávají pouze jednovlnovou agregační křivku. Další reagencií, která se používá při vyvolání agregační odpovědi v PRP, je ristocetin, který zvyšuje vazbu von Willebrandova faktoru na komplex glykoproteinu Ib/X/V, a pomoci této agregační odpovědi lze usuzovat na destičkové dysfunkce nebo von Willebrandovu chorobu [2].
Hyperaktivita destiček je jistě jednou z příčin aterotrombózy a na její stanovení se pohlíží z mnoha vyšetření. Možná vyšetření hyperaktivity destiček jsou uvedena v tab. 2.
Tab. 2. Destičkové parametry, které mají vztah k hyperaktivitě destiček. 
Při interpretaci vyšetření destičkových funkcí je třeba si uvědomit, že řada léků má jako hlavní či vedlejší efekt změnu některé z destičkových funkcí. V tab. 3 jsou uvedeny některé léky a situace, které jistě mají na interpretaci vyšetření destičkových funkcí vliv.
Tab. 3. Léky, které působí změnu destičkových funkcí. 
V tab. 4 jsou uvedeny léky užívané v léčbě a prevenci arteriálních tromboembolizmů, při které hlavní farmakologické působení spočívá v ovlivnění destičkových funkcí [3].
Tab. 4. Léky s protidestičkovým účinkem využívané léčebně. 
Druhým problémem, který je předmětem polemiky, je jev nazývaný rezistence na kyselinu acetylsalicylovou (ASA). V současné literatuře se diskutuje řada otázek, na které se hledá odpověď:
- Jsou všichni nemocní citliví k ASA?
- Existuje rezistence na ASA nebo jde jen o důsledek poddávkování ASA lékařem či nonkomplianci nemocného, který lék neužívá dostatečně?
- Jakými metodami se dá rezistence zjišťovat? Jsme schopni označit nemocného s ASA rezistencí?
- Jaká je prevalence rezistence na ASA?
- Má rezistence na ASA klinický význam nebo jde o laboratorní jev?
- Je to rezistence trvalá, přechodná, či závislá na dávce ASA?
Kyselina acetylsalicylová je bezpochyby nejstarším a nejužívanějším lékem, který má nepochybný protidestičkový efekt. V roce 1838 Rafaele Piria objevil salicylovou kyselinu a v roce 1859 ji Herman Kolb syntetizoval. V roce 1899 pak Felix Hoffmann syntetizoval acetylsalicylovou kyselinu. Teprve v roce 1950 bylo prokázáno prodloužení krvácivosti po podání ASA a v roce 1970 byl prokázán její antitrombotický efekt.
Snahou objektivizovat vliv protidestičkové léčby u nemocných s vysokým rizikem arteriálních uzávěrů se zabývá řada prací. Výsledky prací na toto téma jsou shrnuty v analýze 287 studií, které referovaly o výsledcích 135 000 pacientů s protidestičkovou léčbou proti kontrolám. Bylo porovnáno 77 000 pacientů v různých režimech protidestičkové léčby. Hlavním sledovaným výsledkem byly: výskyt závažných cévních uzávěrů, dále nefatální srdeční infarkty, nefatální ikty nebo úmrtí na cévní onemocnění. Výsledky jsou shrnuty v publikaci Antithrombotic Trialist’s Collaboration (BMJ 2002; 324 : 71–86). Výsledky svědčí pro tyto závěry:
- Protidestičková léčka je vhodná u všech rizikových nemocných.
- Protidestičková léčba snižuje závažné cévní příhody u rizikových nemocných, srdeční infarkt, nefatální ikty, tranzientní ischemické ataky, nestabilní anginu pectoris, obliterující aterosklerózu tepen dolních končetin. Dále snižují rizika embolie při fibrilaci síní a rizika cévních uzávěrů u jiných nemocných s vysokým rizikem.
- Protidestičková léčba se má podávat dlouhodobě.
- Nízkodávkovaná kyselina acetylsalicylová (ASA) (75–150 mg/den) je stejně účinná jako vysoké dávky ASA.
- Antagonisté ADP-receptorů jsou jediné, které se ukazují jako efektivnější než ASA (% odds reduction).
- Kombinace ASA s jiným protidestičkovým lékem (klopidogrel, antagonisté GPIIb/IIa) je pro nemocné výhodná [6].
Inhibice funkce krevních destiček působením acetylsalicylové kyseliny (ASA) je zprostředkována cestou nevratné inhibice cyklooxygenázy. Tato inhibice je účinná již při nízkých dávkách ASA v denní dávce 80 až 160 mg. Monitorování antiagregační léčby pomocí acetylsalicylové kyseliny nebylo do současné doby dobře proveditelné. Sledování léčby pomocí kolagenové křivky, případně křivky získané za použití adenozindifosfátu (ADP) neposkytuje srovnatelné a interpretovatelné výsledky. Navíc zjištěné hodnoty mohou být ovlivněny přítomností heparinu. V průběhu let se ukázalo, že někteří nemocní neprofitují z podání ASA a byl diskutován pojem ASA rezistence. Jde dosud o nepřesně definovaný stav, kdy je nutno minimálně hovořit o tzv. klinicky vyjádřené rezistenci a rezistenci laboratorní.
Jako klinická rezistence se označují situace, kdy prevence acetylsalicylovou kyselinou nezabránila další trombotické příhodě. Výhodnější by bylo nazvat tento jev „selháním léčby acetylsalicylovou kyselinou“. Je třeba si uvědomit, že však nemusí jít vždy o „nedostatečnou odpověď“, protože inhibice agregace vyvolaná například trombinem není ovlivnitelná kyselinou acetylsalicylovou, a tedy k trombotické příhodě může dojít při rozsáhlém aterosklerotickém postižení i při adekvátní inhibici destičkové funkce. Jde tedy o komplexní problém, kde není „viníkem“ acetylsalicylová kyselina, ale jde o důsledek progresivního průběhu nemoci či jiným způsobem vyvolanou aktivaci krevní destičky.
Acetylsalicylová kyselina ireverzibilně inhibuje acetylací cyklooxygenázu-1 (COX-1). Ireverzibilní blokáda syntézy vyplývá z toho, že krevní destička, jako bezjaderná částice, nemá genetickou výbavu k novotvorbě enzymů potřebných k syntéze prostanoidů. Cyklooxygenáza katalyzuje transformaci kyseliny arachidonové uvolněné z fosfolipidové vrstvy buněčné membrány v endoteliích cévní stěny na intermediární produkt – prostaglandin H2. Tento meziprodukt se přetváří působením tromboxansyntázy na tromboxan A2 (TXA2), který je hlavním induktorem shlukování trombocytů a současně významným vazokonstriktorem. Inhibicí cyklooxygenázy-1 je potlačena tvorba prostaglandinů a zejména tromboxanu A2. K zastavení aktivity COX-1 stačí dávka kyseliny acetylsalicylové nižší než 100 mg. Nová tvorba COX-1 restituuje až s novotvorbou trombocytů. Doba života trombocytu je přitom asi 7–14 dní. Běžně užívané chronicky podávané dávky ASA účinné k potlačení tvorby TXA2 se pohybují mezi 75 a 325 mg, přičemž je prokázáno, že nízké i vysoké dávky při chronické medikaci potlačují téměř stoprocentně tvorbu TXA2. Podávání nízkých i vysokých dávek ASA inhibuje též tvorbu prostacyklinu, důležitého vazodilatačního a antitrombotického působku, nicméně endotelie jsou schopny rychlé syntézy COX-1 de novo a obnoví tím tvorbu prostanoidů. Aspirin ve vysokých dávkách působí protizánětlivě díky inhibici další izoformy cyklooxygenázy, a sice typu 2 (COX-2). Tento izoenzym se stává aktivním zejména po zánětlivé aktivaci endotelu, za fyziologické situace je přítomen pouze v malé frakci destiček. Exprese tohoto izoenzymu narůstá také ve chvíli nutné rychlé trombocytární regenerace. V inhibici COX-2 je ASA až 170krát méně účinná než v inhibici COX-1. Nutno také zdůraznit, že vysoké dávky ASA mohou mít antitrombotický účinek nezávisle na inhibici COX-1 posílením fibrinolytické aktivity, potlačením tvorby protrombinu, zlepšením endoteliální funkce a obecně protizánětlivým působením. ASA kromě přímého protidestičkového působení působí na LDL a ovlivňuje endoteliální dysfunkci u aterosklerotických nemocných a oslabuje zánětlivou odpověď jako antioxidant. Působí tedy i nezávisle na prostaglandinech.
Nová metoda ke sledování antiagregační léčby pomocí ASA využívá k vyvolání agregační odpovědi kationtové substance propylgalátu (Cationic Propyl Gallate – CPG). Stanovení probíhá v optickém agregometru za použití destičkami bohaté (PRP) a chudé (PPP) plazmy. Měří se výška maximální amplitudy (Ma), rychlost náběhu agregační křivky (Ms – slope) a doba potřebná k dosažení 50 % ma (T50). Je-li to možné, změří se agregační odpověď před podáním protidestičkové terapie (ASA), a pak se provádějí pravidelná měření v průběhu terapie, dokud se nedosáhne optimálního snížení hodnoty slope. Kontroly po dosažení této hodnoty je potom možné provádět v delších časových intervalech. Heparin do hodnoty 4,0 IU/ml nemá vliv na výsledek vyšetření. Počty destiček pod 100 × 109/l mohou významně ovlivnit výsledek testu. Nelze stanovit vzorky s chylózní, ikterickou a hemolytickou plazmou [1,14]. Příčiny aspirinové resistence nejsou zcela jasné a její stanovení je diskutabilní. Tab. 5 ukazuje možné příčiny aspirinové rezistence.
Tab. 5. Faktory ovlivňující aspirinovou rezistenci [4,10,11]. ![Faktory ovlivňující aspirinovou rezistenci [4,10,11].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/e46a4f5a15fd339e288e5aa34f86c83a.png)
Tak jako se obtížně definuje aspirinová rezistence, je obtížné její laboratorní stanovení. Podle použitých metodik ve studiích se liší i její prevalence (tab. 6).
Tab. 6. Vybrané studie a laboratorní testy sledující zjišťující rezistenci na ASA [8,12]. ![Vybrané studie a laboratorní testy sledující zjišťující rezistenci na ASA [8,12].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/6202965d0a7e6ddb27e01fd79d629ec3.png)
Na více souborech bylo prokázáno, že nemocní s rezistencí na ASA mají větší četnost fatálních i nefatálních koronárních příhod než respondeři. Rezistence na ASA je považována za nový rizikový faktor arteriální trombózy [5,7,8]. Jednou z možností, jak obejít ASA rezistenci, by mohlo být použití protidestičkových léků, které neblokují syntézu prostaglandinů. Thienopyridiny blokují ADP a inhibují vazbu na fibrinogen pomocí receptoru GPIIb/IIIa, ale na GPIIb/IIIa přímo nepůsobí. Inhibice ADP indukované agregace je 50–60% po 4–6 dnech. Dochází i k blokádě uvolňování ADP z denzních granulí, a tím se blokuje sekundární agregace vyvolanou Ca2+ a serotoninem a release z velmi denzních granulí (α) (trombospodin a fibrinogen).
Tab. 7. Laboratorní testy používané k měření protidestičkového působení ASA [12]. ![Laboratorní testy používané k měření protidestičkového působení ASA [12].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/50da9eb882e48e35fb48239299f6f70d.png)
Na našem pracovišti jsme se také zabývali ASA rezistencí. Vyšetřili jsme 342 nemocných s ischemickou chorobou srdeční, kteří brali 100 mg ASA denně pomocí agregace po kationickém propylgallátu (CPG) a pomocí vyšetření primární hemostázy na přístroji PFA 100. Při dávce 100 mg ASA byla prevalence rezistence po CPG u nemocných s ICHS 12,1 % a prevalence pomocí PFA 100 15,3 %. Při titraci dávky u nonrespondentů (zvýšení na 200 mg) vede ke snížení počtu rezistentních nemocných na 7,6 %. Naopak, 20 % nemocných citlivě reaguje na nižší dávky než 100 mg ASA. Domníváme se, že vyšetření ASA rezistence zřejmě odhaluje destičkovou hyperaktivitu [13,14].
prof. MUDr. Jaroslav Malý, CSc.
www.fnhk.cz
e-mail: maly@lfhk.cuni.cz
Doručeno do redakce: 1. 1. 2005
Zdroje
1. Schwartz KA, Schwartz DE, Davis JA. Detection and monitoring of aspirin inhibition of platelet function using the cationtic propyl gallate platelet aggregation assay. In: Abstract Book American Society of Hematology Meeting, 1998 : 17–19.
2. Kottke–Marchant K, Corcoran G. The Laboratory Diagnosis of Platelet Disorders. An Algorithmic Approach. Arch Pathol Labor Med 2001; 126 : 133–146.
3. Maree AO, Fitzgerald DJ. Aspirin and coronary artery disease. Thromb Haemost 2004; 92 : 1175–1181.
4. Bhatt DL. Aspirin resistance: more than just a laborotary curiosity. JACC 2004; 43 : 1127–1129.
5. Gum PA, Kottke–Marchant K, Welsh PA et al. A prospective, blinded determination of the natural history of aspirin resistance among stable patients with cardiovascular disease. J Am Coll Cardiol 2003; 19 : 961–965.
6. Antithrombotics Trialist’s Collaboration. Collaborative metaanalysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction and stroke in high risk patiens. BMJ 1999; 318 : 759–764.
7. Chen WH, Lee PY, Ng W et al. Aspirin resistance in associated with a high incidence of myonecrosis after non-urgent percutaneous coronary intervention despote clopidrogel pretreatment. J Am Coll Cardiol 2004; 43 : 1122–1126.
8. Eikelboom JW, Hirsh J, Weitz JI et al. Aspirin resistant thromboxane biosynthesis and the risk of myocardial infarction, stroke, or cardiovascular death in patients at high risk for cardiovascular events. Circulation 2002; 105 : 1650–1655.
9. Hankey GJ, Eikelboom JW. Aspirin resistance. BMJ 2004; 328 : 477–479.
10. Kurth T, Glynn RJ, Walker AM et al. Inhibition of clinical benefits of aspirin on first myocardial infarction by nonsteroidal intiinflamatory drugs. Circulation 2003; 108 : 1191–1195.
11. MacDonald TM, Wei L. Effect of ibuprofen on cardioprotective effect of aspirin. Lancet 2003; 361 : 572–574.
12. Mason PJ, Freedman JE, Jacobs AK Aspirin resistance: current concepts. Rev Cardiovasc Med 2004; 53 : 156–163.
13. Malý J, Pecka M, Dulíček P et al. Vyšetření aktivity destiček se vztahem k resistenci na kyselinu acetylsalicylovou. Sborník XI. Slovensko-České konference o hemostáze a trombóze. Bratislava: Universita Komenského 2004 : 26–29.
14. Pecka M, Gregor J, Urbánková J et al. Use of propyl gallate in monitoring of antiaggregation therapy with ASA in patients with cardiovascular syndrome. In: Cocheri S, Gensini G, Palareti G, Prisce D, Monduzzi D (eds). Reports from the 17th International Congress on Thrombosis 2002 : 15–18.
15. Stejskal D et al. Vyšetření aktivity (viz titul). Vnitř Lék 2004; 50 (8): 591–599.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2005 Číslo 2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Geriatrie jako interdisciplinární vědní obor na prahu 21. století
- Adiponektin – nový adipocytární hormon ve vztahu k obezitě a inzulinové rezistenci
- Heparinem indukovaná trombocytopenie (HIT)
- Heparinem indukovaná trombocytopenie
- Smíšená kryoglobulinemie jako extrahepatální manifestace infekce virem hepatitidy C
- Vyšetření aktivity destičkových funkcí se vztahem k rezistenci na kyselinu acetylsalicylovou
- Pedální bypass v léčbě ischemie diabetické nohy – střednědobé výsledky
- Pulzní tlak v mladé populaci stanovený 24hodinovým ambulantním monitorováním krevního tlaku a jeho vztah k metabolickým a antropometrickým parametrům
- Hodnocení apoptózy buněk akutní myeloidní leukemie a B−lymfocytární chronické lymfatické leukemie po kultivaci s cytostatiky a její vztah k mnohočetné rezistenci
- Vlastní zkušenosti se vznikem a trváním spontánní remise u dospělých diabetiků typu 1
- Vliv kombinovaného aerobního a silového tréninku na funkci levé komory srdeční u nemocných po akutním infarktu myokardu
- Geriatrics as an inter-disciplinary science on the threshold of the 21st century
- Kmenové buňky: nový příslib v medicíně
- Syndróm z rozpadu nádoru – tumor lysis syndrome
- Adiponektin – nový adipocytární hormon se vztahem k obezitě a inzulinové rezistenci
- Kongenitální adrenální hyperplazie, defekt 17α−hydroxylázy jako vzácná příčina hypertenze a hypokalemie
- Heparinem indukovaná trombocytopenie u pacientky se stenózou kmene levé věnčité tepny
- Léčba chronické infekce virem hepatitidy C pegylovaným interferonem a ribavirinem u pacienta se smíšenou kryoglobulinemií
- Redakční pošta
- Redakční pošta
- Redakční pošta
- Studium na lékařské fakultě – potřeba tradice i změn
- Radovan Slezák et al. Malé ilustrované repetitorium
- Pavel Ševčík, Jana Skřičková, Vladimír Šrámek et al. Záněty plic v intenzivní medicíně
- Stanislav Havelka, Jozef Hoza et al. Revmatologie období růstu. Diagnostika, terapie, rehabilitace
- Pavel Maruna. Proteiny akutní fáze. Fyziologie, diagnostika, klinika
- Jiří Widimský jr et al. Arteriální hypertenze – současné klinické trendy
- Pavel Kohout et al. Výživa u pacientů s idiopatickými střevními záněty
- Jan Příborský: Peniciliny
- XI. sjezd České internistické společnosti Brno 20.–23. října 2004
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Pulzní tlak v mladé populaci stanovený 24hodinovým ambulantním monitorováním krevního tlaku a jeho vztah k metabolickým a antropometrickým parametrům
- Kongenitální adrenální hyperplazie, defekt 17α−hydroxylázy jako vzácná příčina hypertenze a hypokalemie
- Syndróm z rozpadu nádoru – tumor lysis syndrome
- Vlastní zkušenosti se vznikem a trváním spontánní remise u dospělých diabetiků typu 1
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



