-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Pozitivita sérových protilátok proti endomýziu, jejunu a histopatologická diagnostika celiakie u detí
Positive tests for serum anti-endomisium antibodies (AEA) and anti-jejunal antibodies (JAB) and histopathological diagnosis of celiac disease in children
Non-invasive examination methods are increasingly important in diagnosing celiac disease. New options for diagnosing celiac disease have been discovered in addition to the established biochemical, hematological and other methods as a result expansive progress of clinical genetics and immunology. At the same time, detection of circulating auto-antibodies is becoming ever more frequent in clinical practice. As a result, many new, clinically highly heterogeneous cases of the disease have been diagnosed and consequently the prevalence of the disease in both child and adult population has grown. Detection of anti-endomysial antibodies (AEA), characteristic for their high sensitivity and specificity, plays an important role in diagnosing and monitoring celiac disease in pediatric practice. Nevertheless, histopathological diagnosis remains the critical tool for definitive diagnosis of the disease. The article refers to relations between the degree of positivity of AEA and JAB antibodies in the IgA class and the respective grade in the Marsh grading system. The objective of the study was to examine AEA and JAB antibodies and the histological picture of the duodenal mucosa in 20 children and adolescents with celiac disease aged from 2 to 18 years. The authors developed a semiquantitative scale of positivity of both the antibodies, which they compared trying to find a correlation between these and the histopathological picture of the duodenal mucosa. The authors point out the need of timely determination of AEA and t-TG (tissue transglutaminase) in patients whose anamnesis, clinical picture or laboratory results may be indicative of celiac disease.
Key words:
anti-endomisium antibodies – anti-jejunal antibodies – celiac disease – fibrin – Marsh grading system
Autori: Pe Makovický 1; Pa Makovický 1; M. Klimik 2; M. Greguš 3; M. Zimmermann 4
Pôsobisko autorov: Ústav patológie FN Nitra, Slovenská republika, prednosta doc. MUDr. Dušan Ďurčanský, CSc. 1; Oddelenie klinickej imunológie FN Nitra, Slovenská republika, prednosta prim. MUDr. Michal Klimik 2; Gastroenterologické oddelenie Nitra, Slovenská republika, prednosta prim. MUDr. Miloš Greguš 3; Ústav klinickej mikrobiológie FN Nitra, Slovenská republika, prednostka mim. prof. MUDr. Anna Líšková, Ph. D. 4
Vyšlo v časopise: Vnitř Lék 2008; 54(1): 25-30
Kategória: Původní práce
Súhrn
V diagnostike celiakie získavajú v súčasnosti stále väčší význam neinvazívne vyšetrovacie metódy. Popri tradičných biochemických, hematologických, ale aj iných vyšetreniach boli v dôsledku expanzívneho rozvoja klinickej genetiky a imunológie odhalené nové možnosti diagnostiky celiakie. Súčasne sa v klinickej praxi začína stále častejšie využívať vyšetrenie cirkulujúcich autoprotilátok. Ich zavedenie viedlo k odhaleniu mnohých nových klinicky značne heterogénnych prípadov a tým aj k zvýšeniu prevalencie ochorenia v populácii detí i dospelých. Významné postavenie v diagnostike a monitoringu celiakie v pediatrickej praxi má stanovenie antiendomyziálnych protilátok (AEA), ktoré sa vyznačujú vysokou senzitivitou a špecificitou. Kardinálnym nástrojom na definitívne diagnostikovanie celiakie však naďalej ostáva histopatologická diagnóza. V texte sa uvádzajú vzťahy medzi úrovňou intenzity pozitivity autoprotilátok AEA a JAB (antijejunálnych) v triede IgA a so stupňom Marshovho histologického gradingu. Cieľom práce bolo vyšetriť AEA a JAB autoprotilátky a histologický obraz duodenálnej sliznice u 20 detí a adolescentov s celiakiou vo veku 2-18 rokov. Autori vytvorili semikvantitatívnu stupnicu pozitivity oboch protilátok, ktorú vzájomne porovnávajú a hľadajú vzťah medzi nimi a histopatologickým obrazom duodenálnej sliznice. Poukazuje sa na potrebu včasného stanovenia AEA a t-TG (tkanivová transglutamináza) u pacientov, ktorých anamnéza, klinický obraz, alebo výsledky laboratórnych vyšetrení môžu poukazovať na prítomnosť celiakie.
Kľúčové slová:
antiendomyziálne protilátky - antijejunálne protilátky - celiakia - lepok - Marshov histologický grading - tenké črevoÚvod
Celiakia je autoimunitné ochorenie, u ktorého poznáme spúšťač, tesnú genetickú väzbu a špecifickú humorálnu autoimunitnú odpoveď. Gliadínové peptidy reagujú s HLA-DQ2 a HLA-DQ8 pozitívnymi imunokompetentnými bunkami a tým sa zahajuje kaskáda reakcií, ktorých najnápadnejším prejavom sú zápalové zmeny a atrofia klkov sliznice tenkého čreva. Tieto zmeny ustupujú po bezlepkovej diéte. Celiakiu je možné definovať tiež ako neprimeranú, T-lymfocytmi sprostredkovanú autoimunitnú reakciu na glutén [11]. U geneticky predisponovaných osôb sú antigénne fragmenty gliadínu účinne prezentované T-lymfocytárnemu systému za rozvoja imunopatologickej reaktivity. Špecifická T-lymfocytárna reaktivita sa rozvíja aj voči natívnym formám gliadínov a komplexov medzi gliadínom a tkanivovou transglutaminázou. Tento proces možno prinajmenšom teoreticky vysvetliť ako proces intermolekulového rozširovania terčov imunopatologickej reaktivity. Aktivované T-lymfocyty regulujú imunopatologický zápal v črevnej sliznici. Charakteristickým rysom je aktivita TH2, ktorá stimuluje B-lymfocyty k tvorbe protilátok proti gliadínu a autoprotilátok.
V klinickej praxi sa rozlišuje viacero foriem ochorenia [10,12,20,27,29,30]. Na jedného pacienta s klasickým obrazom pritom pripadá niekoľko nediagnostikovaných prípadov s atypickou symptomatológiou [10,17,30]. Podľa literárnych údajov sú však všetky formy vo vzťahu s antigénom v potrave, pričom sa táto reakcia v značnej miere líši od bežných potravinových alergií sprostredkovaných IgE a histamínom [2,25]. V priebehu posledných desaťročí bol v snahe zlepšenia diagnostiky celiakie opísaný výskyt jednotlivých cirkulujúcich autoprotilátok. Ako prvé boli v roku 1958 Bergerom [1] opísané antigliadínové protilátky (AGA). Následne boli zistené vzťahy medzi antiretikulínovými protilátkami (ARA) a ochorením [31]. Neskôr boli aj v spojitosti s kožnou chorobou Herpetiformis dermatitis Dühring Chorzelskim et al [14] opísané antiendomyziálne protilátky (AEA). Podobne v priebehu uvedenej kožnej choroby v kombinácii s celiakiou boli Kárpátiovou et al [18] opísané antijejunálne protilátky (JAB). Za posledný zistený autoantigén celiakie sa považuje tkanivová transglutamináza (t-TG), ktorá bola objavená v roku 1997 Dietrichom et al [5].
Typickým nálezom u pacientov s celiakou sú zvýšené hodnoty AEA (IgA), ktorých prítomnosť je v priamej súvislosti so slizničným poškodením tenkého čreva. V literárnych zdrojoch sa uvádza, že AEA pravdepodobne reagujú so štruktúrami intercelulárnej matrix, s retikulínovými vláknami a s endomýziom hladkého svalstva [24]. Špecificita AEA je uvádzaná v rozmedzí 90-100 % a senzitivita 97-100 % [22]. Farrell et al [8] uvádzajú špecificitu AEA 97-100 % a senzitivitu 85-98 %. Kotalová et al [21] uvádza 100% špecificitu i senzitivitu AEA k celiakii stanovovaných na ľudskom pupočníku. Práve prakticky 100% potvrdenie diagnózy na základe pozitivity AEA je dnes predmetom celosvetových štúdií rôznych vedeckých pracovísk. Diagnostickým dôkazom aj naďalej ostáva biopsia z tenkého čreva s charakteristickým histopatologickým nálezom so zmenou k normálnemu nálezu po nasadení bezlepkovej diéty.
Keďže sa v rutinnej klinickej praxi využívajú v screeningu celiakie najmä sérologické vyšetrenia, porovnávame v predloženej práci úroveň intenzity pozitivity AEA a JAB. Stupeň pozitivity autoprotilátok je porovnávaný aj so stupňom poškodenia sliznice tenkého čreva, ktorý je vyjadrený histologickým gradingom podľa Marsha.
Súbor pacientov a metodika
Náš súbor tvorila skupina 20 pacientov. Z toho 13 dievčat vo vekovom rozmedzí 2-18 rokov (Ø 11,46 rokov) a skupina 7 chlapcov vo vekovom rozmedzí 2-17 rokov (Ø 6,57 rokov). Vzťahy medzi základnými a histopatologickými údajmi sú uvedené v tab. 1. Ambulantne, resp. v priebehu hospitalizácie boli mimo základných laboratórnych vyšetrení vykonané aj vyšetrenia autoprotilátok AEA a JAB formou nepriamej imunofluorescenčnej metódy. Odobratá vzorka krvi bola spracovaná centrifugáciou najneskôr do 2 hodín po dodaní do laboratória Ústavu patológie FN Nitra (ÚP FN). Sérum bolo odpipetované do vopred označených skúmaviek a takto prakticky okamžite fixované v mraziacom boxe vychladenom na -30 °C.
AEA boli stanovované na ľudskom pupočníku a JAB na tenkom čreve. Tkanivo pupočníka sme získali odberom po fyziologickom pôrode. Takto získané tkanivo bolo spracované v tvare mozaiky a zmrazené pri teplote -80 °C v podchladenom acetóne/petroléteri. Z mozaikových foriem boli na zmrazovacom mikrotóme (cryocut Leica) narezané sériové rezy o hrúbke 5 µm, ktoré boli nanesené na čisté, odmastené a označené podložné sklíčka. Sklíčka z rezmi boli pri pokojovej izbovej teplote sušené po dobu 30 min a následne fixované v kyvetách s bezvodým acetónom v chladiacom boxe po dobu 5 min. Po fixácii boli sklíčka krátko ešte sušené a potom uložené do kyviet s obsahom fosfátového pufra o pH 7,6 (PBS) po dobu 5 min. Medzitým rozmrazené sérum bolo odpipetované do vopred označených skúmaviek a riedené 1 : 10 s PBS. Sérum bolo podľa označení na podložných sklíčkach aplikované na cryocutové rezy pôvodom z ľudského pupočníka (AEA). Následne boli sklíčka uložené vo vlhkej komôrke k 30minútovej inkubácii pri pokojovej izbovej teplote. Po inkubácii bolo prebytočné sérum opláchnuté s PBS a sklíčka boli uložené v kyvetách s PBS po dobu 10 min. Po premytí bolo tkanivo prevrstvené konjugátom fluoresceínu (SwAHU IgA/FITZ) a sklíčka boli opäť uložené k inkubácii vo vlhkej komôrke po dobu 30 min. Po inkubácii bol prebytočný konjugát zliaty a sklíčka boli opätovne uložené v kyvetách s PBS po dobu 10 min. Po uplynutí tejto doby boli preparáty opatrne ošetrené suchou gázou a uložené do krabice na preparáty, kde oschli. Takto vyhotovené boli do jedného dňa odčítané v spektre fluorescenčného mikroskopu Nicon s halogénovou lampou 103 W.
Po potvrdení pozitivity bola časť zostatkového materiálu v rovnakej koncentrácii s PBS aplikovaná aj na originálne komerčné podložné sklíčka s rezmi tenkého čreva (JAB). Preparáty boli v laboratórnom procese spracované podobne podľa vyššie uvedeného postupu, bez potreby fixácie. Po ich vyhotovení boli zamontované do glycerínu, prekryté krycím sklíčkom a obdobne do jedného dňa odčítané v spektre fluorescenčného mikroskopu. Pri semikvantitatívnom vyhodnocovaní bola použitá zaužívaná stupnica ÚP FN. Boli definované 4 stupne (negatívne, +, ++, +++), ktoré boli na výsledkovom liste doplnené popisom patológa. Jednotlivé stupne pozitivity boli posudzované subjektívne na základe doterajších skúseností patológa. Všetky preparáty boli vyhotovené i hodnotené na ÚP FN jedným pracovníkom, ktorý vykonával túto činnosť už po dlhé obdobie. Definované stupne boli kvantifikované a boli vypočítané základné variačno-štatistické charakteristiky. Rozdiely medzi skupinami boli testované v programe SAS ver. 9.1 (SAS/STAT - two sample t test).
Po potvrdení pozitivity AEA a JAB boli pacienti odosielaní na gastroenterologické vyšetrenie spojené s bioptickým odberom vzoriek z jednotlivých častí duodena (D1, D2 a D3). Vzorky boli po odbere pred vložením do fixačného roztoku orientované klkmi hore, aby bolo možné zrealizovať kolmé rezy. Vzorky boli fixované v 8% roztoku formalínu, vyexidované kompletne a zaliate do parafínu. Na sánkovom mikrotóme boli narezané sériové rezy o hrúbke 3-6 μm. Následne boli rezy farbené prehľadným farbením: hematoxylínom-eozínom a preparáty boli vyhodnocované subjektívne v svetelnomikroskopickom obraze mikroskopu Olympus BX40.
Výsledky
Vzťahy medzi základnými údajmi a histopatologickými nálezmi
Tieto nálezy ukazuje tab. 1.
Tab. 1. Vzťahy medzi základnými údajmi a histopatologickými nálezmi. 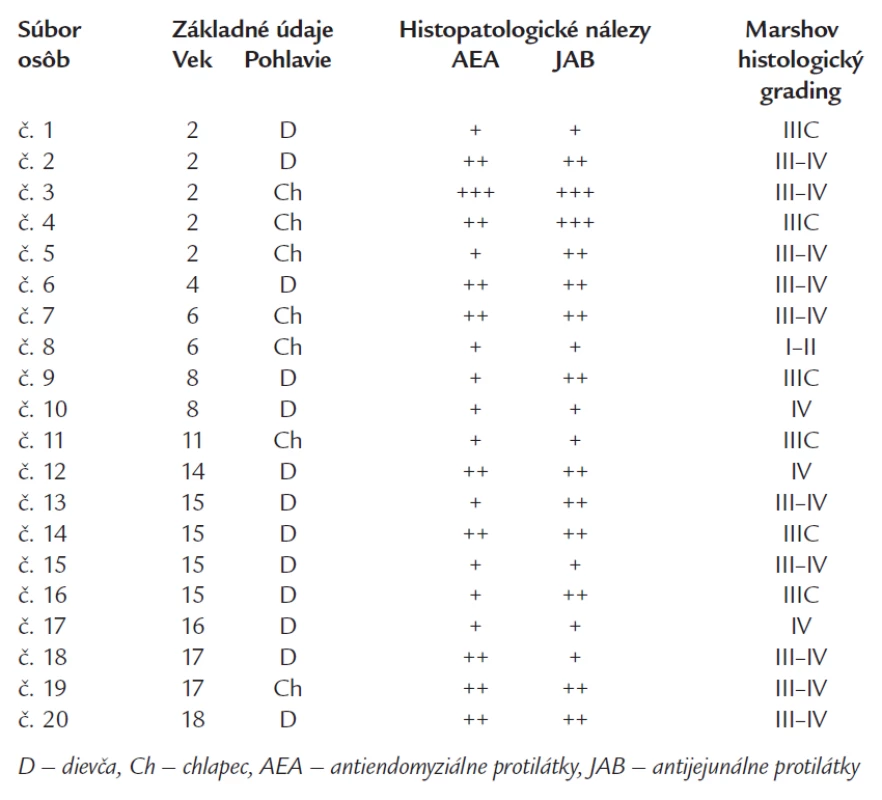
Základné variačno-štatistické charakteristiky
Výsledky ukazuje tab. 2.
Tab. 2. Základné variačno-štatistické charakteristiky. 
Rozdiely medzi skupinami boli testované pomocou párového t-testu na hranici významnosti α = 0,05. Hodnota t-testu bola 1,485; P = 0,1457 pri α = 0,05. Tieto výsledky znamenajú, že nulová hypotéza platí. Rozdiely medzi porovnávanými skupinami neboli štatisticky významné pri hladine významnosti α = 0,05.
Fluorescenčno mikroskopický nález
Nález dokumentuje typickú celoplošnú pozitivitu, čo sa odráža jasnou fluorescenciou patričných funkčných miest AEA. Ide o rôzny stupeň pozitivity na periférii hladkosvalových buniek, ktorá pozostáva z endomýzia s mikroskopickým obrazom umelej sieťoviny. Pozitivita sa manifestuje aj v rôsolovitom väzive, resp. Whartonovom rôsole, obdobne v reakcii s retikulárnymi vláknami. Pozitivita JAB je viditeľná ako žlto-zelená žiarivá luminiscencia funkčných miest v časti lamina propria mucosae a lamina muscularis mucosae s lokalizáciou na periférii hladkosvalových buniek, ktorá je tvorená bazálnou laminou a retikulárnymi vláknami.
Histopatologický nález
Svetelnomikroskopický obraz signifikantných fragmentov duodenálnej sliznice i podslizničia s nálezom subtotálnej, totálnej až vilóznej atrofie klkov a chronickým zápalom rôzneho stupňa (index klku ku krypte 1 : 1 až 0 : 1). V signifikantne väčšej skupine ide o chronickú enterititídu s ťažko narušenou mikroštruktúrou, vyhladeným edematózne prestúpeným slizničným reliéfom i plytkými eróziami. V prípadoch ťažko zmeneného terénu s morfologickým obrazom, ktorý znemožňuje jednoznačné posúdenie charakteru sliznice, nachádzame len reziduálne štruktúry krýpt s kompenzačnou kryptálnou hyperpláziou a hyperpláziou Brunerových žliaz. Pre materiál je charakteristická ťažká architektonálna porucha v zmysle totálne vyhladeného slizničného povrchu, ktorý je prestúpený denzným zmiešaným zápalovým infiltrátom s predominanciou intraepitelových lymfocytov a plazmatických buniek. Súčasťou zápalového procesu je aj prítomnosť eozinofilov. Histologicky spadá obraz do morfologickej entity celiakie.
Diskusia
V posledných rokoch sme svedkami stúpajúceho počtu novodiagnostikovaných prípadov celiakie. Uvedené je však dôsledkom intenzívnejšieho screeningu, ako aj dôsledkom sústavného skvalitňovania metodík využívaných v diagnostike ochorenia. V tomto trende sa zároveň analogicky aj v literárnych údajoch uvádza nárast prevalencie ochorenia [10-13,26,30]. Zavedenie sérologických vyšetrení umožňuje rozpoznanie atypických foriem celiakie aj v detskej populácii, pričom sa v klinickej praxi využívajú v súčasnosti predovšetkým AEA a t-TG. Z doterajších výsledkov pritom vyplýva, že všetky formy celiakie sú charakteristické pozitivitou AEA [10,30]. Preto sa stanovenie AEA javí ako dobrý test v diagnostickom procese a indikácii bioptického odberu vzoriek z tenkého čreva určených na histopatologické vyšetrenie. Niektoré literárne údaje dokumentujú prítomnosť ochorenia aj s negatívnymi AEA. Jedná sa o pediatrických pacientov do 2 rokov života. Uvádza sa, že títo pacienti nemajú schopnosť produkcie AEA, ktorá sa posúva do vyššieho veku [3]. Ani u pacientov so selektívnym deficitom IgA nemusia byť AEA pozitívne [26]. Napriek tomu, že AEA sa vyznačujú vysokou senzitivitou a špecificitou, nie je možné stanoviť diagnózu iba na základe tejto pozitivity [15,21,28]. Výsledky doterajších štúdií dokumentujú, že vyšetrenia autoprotilátok sa môžu uplatniť len v rovine pomocných vyšetrení [9,21,23,28]. Pre definitívne potvrdenie diagnózy je potrebné histopatologické vyšetrenie vzoriek z jednotlivých častí tenkého čreva.
Fluorescenčné vyšetrenie na substitučných rezoch s ľudským pupočníkom a následne na komerčných podložných sklíčkach s tenkým črevom sme volili s cieľom zistiť, či sa pozitivita odrazí rovnakou intenzitou na oboch typoch tkanív. Naše výsledky dokumentujú vysokú citlivosť AEA a JAB s malými odchýlkami vyjadrenými stupňom v úrovni pozitivity. Uvedené je dokumentované aj rozdielmi medzi porovnávanými skupinami, ktoré pri hladine významnosti α = 0,05 neboli štatisticky významné. Ide však o floridnú celiakiu s výrazným histopatologickým nálezom. V práci Kotalovej et al [21] sa uvádza, že JAB a AEA nie sú celkom identické. Autori štúdie pozorovali situácie, keď JAB boli výrazne pozitívne a AEA negatívne a naopak. Pozler et al [28] porovnávajú vo svojej práci substráty k AEA v podobe opičieho pažeráka a ľudského pupočníka. V závere odporúčajú použiť dostupnejšie rezy z ľudského pupočníka, alebo rezy z neonatálnej pečene odobratej nekropticky. V štúdiách zameraných na porovnávanie citlivosti jednotlivých autoprotilátok k chorobe sa ich doporučuje členiť podľa živočíšneho druhu tkaniva, na ktorom je väzba dokazovaná [18,21,28].
Protilátky AEA sú v klinickej praxi postupne nahradzované jednoduchším a menej nákladným testom t-TG. AEA sa tak začínajú používať ako kontrola dodržiavania zásad bezlepkovej diéty [4,16]. Stanovenie JAB sa používa prakticky už len v štúdiách. Na okraj klinického záujmu sa dostali aj ARA, podobne ako aj AGA. Uvedené protilátky sú však v klinickej praxi zmysle screeningu rôznych autoimunitných a systémových ochorení stále vyšetrované. Možnou výhodou je snáď ich dostupnosť pre pracoviská s nižším finančným rozpočtom vzhľadom k možnostiam vlastnej výroby. Celoštátna snaha o akreditáciu laboratórií s privilégiom vyššej úhrady výkonu poisťovňou však preferuje realizáciu objektívnejších vyšetrení s minimálnym stupňom subjektivity. Aj preto sa do popredia dostalo vyšetrenie t-TG. V menších zariadeniach je však nevýhodou relatívne dlhá doba čakania na výsledok t-TG a to predovšetkým vzhľadom k potrebe nahromadenia väčšieho množstva materiálu. Tento nedostatok je substituovaný existenciou niekoľkých väčších pracovísk aj s ponukou vyšetrenia t-TG. V praxi sa však ukazuje, že zlou manipuláciou, nevhodným odberom, včítane nesprávneho balenia materiálu určeného na vyšetrenie dochádza k predlžovaniu a opakovaniu vyšetrení aj s množstvom falošných výsledkov. Preto treba podľa nás klinických pracovníkov z privátnych ambulancií i menších štátnych zariadení poučiť o správnej manipulácii s materiálom pri jeho odbere, fixácii, označení a obzvlášť o zásadách pri jeho odosielaní na vzdialenejšie pracoviská s ponukou vzácnejších vyšetrení, včítane uvedeného t-TG.
Čo sa týka rozdielov miery semikvantitatívneho vyjadrenia pozitivity AEA a JAB, doporučujeme klinikom, aby si na začiatku, resp. pri podozrení na celiakiu vždy dali urobiť čo najväčšiu škálu vyšetrení, včítane vyšetrenia t-TG. V súčasnosti prevláda v klinickej praxi trend, že pri pozitivite t-TG nie je nutné vyšetrovať iné autoprotilátky. V porovnaní s pozitivitou proti t-TG je ich výpovedná hodnota totižto nízka. V tomto zmysle uvádzame, že stupeň pozitivity jednotlivých autoprotilátok je odrazom aktivity ochorenia. Následné opakovanie vyšetrení po istom časovom intervale potom umožní klinickému kolegovi lepší pohľad na účinnosť nasadenej terapie, včítane dodržiavania zásad bezlepkovej diéty pacientom. Opakovanie vyšetrení na cirkulujúce autoprotilátky má podľa nás zvlášť význam v pediatrickej praxi. Podľa nás je potrebné hneď ako je to možné aktívne viesť deti k uvedomeniu, aby sa vystríhali vedomej, či nevedomej konzumácie akéhokoľvek množstva lepku. Tým sa už v tomto období vytvárajú u nich správne stravovacie návyky. S dospelými novodiagnostikovanými pacientmi je v tomto zmysle spolupráca ťažšia a prehrešky v diéte sú často zľahčované. Keďže deti sú adaptabilnejšie a učenlivejšie treba ich od začiatku viesť k uvedomeniu, aby sa vyhýbali lepku. Lepok je totižto často obsiahnutý aj v surovinách, polotovaroch, potravinách či farmaceutikách, ktoré navonok nemajú nič spoločné s obilninami. Mimo toho možno takýmto spôsobom usmerňovať aj rodičov detí s celiakiou. Je totižto zrejmé, že rodičia v tomto období aktívne vplývajú na návyky detí, čo sa v plnej miere týka aj stravovacích návykov. Navyše sa vytvára dôvera medzi rodičom a pediatrom a dieťaťom. Keďže v bezlepkovej diéte niet kompromisov je podľa nás potrebné kontrolovať hodnoty autoprotilátok u detí s celiakiou v kratších časových intervaloch ako u dospelých. V domácej i zahraničnej literatúre nachádzame v tomto zmysle množstvo informácií, ale v klinickej praxi niet univerzálneho postupu. Každopádne však možno predpokladať, že protilátky JAB nebudú pri ekvivalencii AEA a t-TG zachované ani v diagnostickom algoritme a ani v kontrole dodržiavania zásad bezlepkovej diéty.
Už celé desaťročia sa rôzne práce venujú možnostiam diagnostiky celiakie už v jej iniciálnom štádiu. V rutinnej klinickej praxi je problematická najmä diagnostika atypických foriem celiakie, prípadne celiakie s pridruženým priebehom iného patologického procesu. V našej práci popisujeme pri pozitivite AEA a JAB výrazný histopatologický nález, ktorý zdôvodňujeme prejavom pokročilej fázy ochorenia. Prokopová [30] uvádza, že čím závažnejšie sú histopatologické zmeny na sliznici tenkého čreva, tým je vyššia aj senzitivita AEA. Aj Buc [2] konštatuje, že titre AEA sú vo vzťahu so závažnosťou choroby. Výsledky prác mnohých autorov pritom poukazujú, že po nasadení bezlepkovej diéty vymizne ako prvá práve pozitivita AEA. Vyšetrenie AEA je v diagnostike celiakie preto možné realizovať len u pacientov s lepkom v strave. Aj tieto závery determinujú potrebu porovnávať klinický obraz s čo najširším spektrom výsledkov laboratórnej diagnostiky. Frič a Zavoral [11] upozorňujú na zdĺhavý proces rôznych vyšetrení pri atypickej, ale i typickej forme celiakie. To sa však vzťahuje aj na pediatrických pacientov a preto je pre včasnú diagnostiku celiakie prínosom skoré stanovenie AEA a t-TG na základe anamnézy, klinického obrazu a výsledkov laboratórnych vyšetrení aj v ambulancii lekára prvého kontaktu.
Záver
Zavedenie nových sérologických vyšetrení prinieslo kvalitatívnu zmenu v diagnostike celiakie aj v klinickej praxi pediatra. V našej práci sme chceli poukázať na potrebu včasného stanovenia AEA a t-TG u pacientov, ktorých anamnéza, klinický obraz, alebo výsledky laboratórnych vyšetrení poukazujú na možnú celiakiu a tým predísť rozvoju vážnejších foriem ochorenia a jeho komplikácii. Pritom sa zmieňujeme o komplementárnom chovaní AEA a JAB. O ich zachovaní v diagnostickom algoritme, včítane ich využitia v procese kontroly dodržiavania zásad bezlepkovej diéty detským pacientom. Z pohľadu rutinnej praxe klinického kolegu sú uvedené výhody a nevýhody AEA, resp. t-TG. Uvádza sa, aby sa pri zasielaní materiálu na vzdialenejšie pracoviská s ponukou vzácnych vyšetrení, včítane vyšetrenia t-TG dodržiavali prísne zásady manipulácie vzhľadom k možnosti výskytu falošných výsledkov. Doporučuje sa, aby boli AEA a t-TG bežne vyšetrované už v ambulancii lekára prvého kontaktu.
Ing. Peter Makovický, Ph.D.
www.fnnitra.sk
e-mail: pmakovicky@email.cz
Doručeno do redakce: 18. 7. 2007
Přijato po recenzi: 27. 9. 2007
Zdroje
1. Berger E. Zur allergischen pathogenese der cöliakie. Bibliotheca Paediatrica 1958; 67(Suppl 1): 55-56.
2. Buc M. Celiakia - súčasný pohľad na imunopatogenézu choroby. Int Med 2004; 4 : 352-357.
3. Burgin-Wolf A, Gaze H, Hadziselimovic F et al. Antigliadin and antiendomysium antibody determination for coeliac disease. Arch Dis Child 1991; 66 : 941-947.
4. Dewar D, Pereira SP, Ciclitira PJ. The pathogenesis of coeliac disease. Int J Biochem Cell Biol 2004; 36 : 17-24.
5. Dietrich W, Ehnis T, Bauer M et al. Identification of tissue transglutaminase as the autoantigen of celiac disease. Nat Med 1997; 50 : 797-801.
6. Dvořák M. Biochemická vyšetření u malabsorpčního syndromu. Prakt Lék 1992; 72 : 24-26.
7. Dvořák M. Glutenová enteropathie v pohledu praktického lékaře. Prakt Lék 1998; 78 : 326-327.
8. Farrell RF, Kelly CP. Diagnosis of celiac sprue. Am J Gastro 2001; 96 : 3237-3246.
9. Ferreira M, Davies SL, Butler M et al. Endomysial antibody: is the best screening test for coeliac disease? Gut 1992; 33 : 1633-1637.
10. Frič P. Celiakální sprue (aktuální přehled). Vnitř Lék 2003; 49 : 465-473.
11. Frič P, Zavoral M. Céliakální sprue dospělých - opomíjená choroba. Prakt Lék 2003; 83 : 62-65.
12. Goldemund K. Celiakie. Pediatrie pro praxi 2001; 2 : 106-111.
13. Gregar I, Kolek A, Kojecký Z et al. Celiakie dospělých - klinické projevy a přidružená onemocnění. Prakt Lék 2000; 80 : 617-620.
14. Chorselski TP, Sulej J, Tchorsewska H et al. IgA class endomysium antibodies in dermatitis herpetiformis and celiac disease, 325-334. In: Beutner EH, Nisengard RJ, Albibi B (eds.): Defined-immunofluorescence and related cytochemical methods. Ann NY Acad Sci 1983.
15. Ilavská A, Paulovičová E, Mikulecký M. Význam vyšetrenia sérologických markerov u pacientov s celiakiou. Čas Lék Čes 2002; 141 : 487-490.
16. Ilavská A, Beňo I, Gomolčák P et al. Môžu byť sérologické markery ukazovateľom diétnych chýb u pacientov s celiakiou? Vnitř Lék 2004; 50 : 208-212.
17. Janatková I, Malíčková K, Fučíková T et al. Diagnostický přínos stanovení autoprotilátek u gluten-senzitivní enteropatie. Epidemiol Mikrobiol Imunol 2002; 51 : 125-130.
18. Kárpáti S, Török E, Kósnai I. IgA class antibody against human jejunum in sera of children with dermatitis herpetirormis. J Invest Derm 1986; 87 : 703-706.
19. Kočna P Glutenová enteropathie - nové diagnostické přístupy a screening, 20-23. In: 3. Sjezd Společnosti klinické biochemie. Hradec Králové, 1997.
20. Kohout P. Diagnostika a léčba celiakie. Int Med 2006; 7-8 : 324-326.
21. Kotalová R, Nevoral J, Šmídová J. Tkáňové protilátky v diagnostice celiakální sprue. Čes Slov Pediat 1996; 51 : 680-687.
22. Kumar V, Lerner A, Valeski JE et al. Endomysial antibodies in the diagnosis of celiac disease and the effect of gluten on antibody titers. Immunol Invest 1989; 18 : 533-544.
23. Lukáš Z, Blatný J, Litzman J et al. Diagnostika celiakální sprue. Čes Slov Pediat 1999; 54 : 566-571.
24. Meško D, Pullmann R, Nosáľová G. Vademékum klinickej biochémie. Martin: Osveta 1998. 1647 s.
25. Michalík I, Bauerová M. Celiakálne ochorenie známe i neznáme. Výživa a zdravie 2001; 46 : 10-12.
26. Nevoral J, Kotalová R. Celiakie I. část - Historie, etiopatogeneze, morfologie, protilátky. Čes Slov Pediat 1993; 48 : 426-429.
27. Páv I. Celiakia v ambulantnej praxi. Via Pract 2006; 3 : 22-24.
28. Pozler O, Nožička Z, Slížová D et al. Sérové protilátky proti endomysiu a proti retikulinu. Prakt Lék 1997; 77 : 332-335.
29. Pozler O, Neumann D. Diabetes a celiakie. Vnitř Lék 2004; 50 : 412-414.
30. Prokopová L. Celiakie - závažné onemocnění. Vnitř Lék 2003; 49 : 474-481.
31. Seah PP, Fry L, Hoffbrand AV et al. Tissue antibodies in dermatitis herpetiformis and adult coeliac disease. Lancet 1971; 1 : 834 - 836.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Z odborné literaturyČlánek Celiakální sprue - editorialČlánek Hodnocení proliferačního a apoptotického indexu plazmatických buněk v průběhu mnohočetného myelomuČlánek Využití detekce galaktomananu pro diagnostiku invazivní aspergilózy u hematoonkologických nemocnýchČlánek Diferencovaný přístup k preskripci fyzické aktivity u nemocných s dysfunkcí levé komory srdeční
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2008 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Statinová intolerance
- Genetický podklad a screening familiární hypercholesterolémie
- Metabolit živočišné stravy produkovaný střevní mikroflórou zvyšuje riziko závažných kardiovaskulárních příhod
- DESATORO PRE PRAX: Aktuálne odporúčanie ESPEN pre nutričný manažment u pacientov s COVID-19
-
Všetky články tohto čísla
-
Doporučení diagnostických a léčebných postupů u arteriální hypertenze - verze 2007
Doporučení České společnosti pro hypertenzi - Z odborné literatury
- Fibrilace síní - kardiovaskulární epidemie - editorial
- Konvenční léčba fibrilace síní - editorial
- V diagnostice i terapii houbových infekcí nastal v posledních letech velký pokrok, stále však nedostačující - editorial
- Farmakogenetika léčby statiny - editorial
- Sledování účinnosti antikoagulační léčby u nemocných s fibrilací síní v závislosti na věku
- Pozitivita sérových protilátok proti endomýziu, jejunu a histopatologická diagnostika celiakie u detí
- Hodnocení proliferačního a apoptotického indexu plazmatických buněk v průběhu mnohočetného myelomu
- Konvenční léčba fibrilace síní řízená ambulantními kardiology v ČR: přehled diagnostických a léčebných výkonů, medikamentózní léčby a hospitalizací
- Využití detekce galaktomananu pro diagnostiku invazivní aspergilózy u hematoonkologických nemocných
- Medicína v roce 2008: Je vidět světlo na konci tunelu?
- Diferencovaný přístup k preskripci fyzické aktivity u nemocných s dysfunkcí levé komory srdeční
- Farmakogenetika léčby statiny
- Léčba Waldenströmovy makroglobulinemie a léčba nemocí způsobených monoklonálním IgM gamaglobulinem
- Celiakální sprue - editorial
- Celiakální sprue – Memorandum EKCS
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
-
Doporučení diagnostických a léčebných postupů u arteriální hypertenze - verze 2007
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Využití detekce galaktomananu pro diagnostiku invazivní aspergilózy u hematoonkologických nemocných
- Hodnocení proliferačního a apoptotického indexu plazmatických buněk v průběhu mnohočetného myelomu
- Farmakogenetika léčby statiny
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



