-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Granulomatóza z Langerhansových buněk
Langerhans cell granulomatosis
Langerhans cell granulomatosis is a rare disease of unknown aetiology and characterized by an infiltration of alveolar septa with activated Langerhans cells and eosinophylic granulocytes. Accumulation of these cells leads to a development of multiple cystic formations. The involvement of the lungs is usually present on its own, more rarely it is seen as part of a systemic disease involving skeleton or posterior pituitary. The disease prognosis in adult patients is usually good, 80% of patients achieve remission or stabilization of the disease either spontaneously or following a corticosteroid therapy, 10 – 20% of cases progress to respiratory failure.
Key words:
Langerhans cell granulomatosis – diagnostics – BAL – treatment
Autoři: J. Homolka 1, 2; I. Haškovcová 3
Působiště autorů: I. klinika tuberkulózy a respiračních nemocí 1. lékařské fakulty UK a VFN Praha, přednosta prof. MU Dr. Jiří Homolka, DrSc. 1; Pneumologická klinika 1. lékařské fakulty UK a FTN Praha, přednosta prof. MU Dr. Jiří Homolka, DrSc. 2; Ústav patologie 1. lékařské fakulty UK a VFN Praha, přednosta prof. MU Dr. Ctibor Povýšil, DrSc. 3
Vyšlo v časopise: Vnitř Lék 2010; 56(Supplementum 2): 74-75
Kategorie: Histiocytóza z Langerhansových buněk a některá další vzácná hematologická onemocnění
Souhrn
Granulomatóza z Langerhansových buněk je vzácné onemocnění neznámé etiologie, charakterizované infiltrací alveolárních sept aktivovanými Langerhansovými buňkami a eozinofilními granulocyty. Akumulace těchto buněk vede k tvorbě mnohočetných cystických útvarů. Postižení plic u dospělých se vyskytuje převážně samostatně, vzácněji v rámci systémového onemocnění s postižením skeletu nebo neurohypofýzy. Prognóza onemocnění u dospělých jedinců je většinou dobrá, u 80 % nemocných dochází k remisi nebo stabilizaci onemocnění spontánně nebo po kortikoterapii, pouze u 10 – 20 % pacientů dochází k progresi onemocnění s respiračním selháním.
Klíčová slova:
granulomatóza z Langerhansových buněk – diagnostika – BAL – léčbaPlicní forma granulomatózy z Langerhansových buněk (PGLB) je vzácné onemocnění neznámé etiologie, charakterizované v plicích infiltrací alveolárních sept aktivovanými Langerhansovými buňkami a eozinofilními leukocyty [1,2,4 – 6]. Proliferace Langerhansových buněk nemá nádorový charakter. Aktivované Langerhansovy buňky poškozují plicní matrix produkcí oxidových radikálů a proteáz. Tato poškození vede k tvorbě mnohočetných cystických útvarů. Onemocnění se vyskytuje častěji u dětí (více u dívek, poměr chlapci : dívky 1 : 8) [6]. V dospělosti postihuje převážně mladé muže, kuřáky cigaret s maximem výskytu od 20 do 40 let věku [5]. I zdraví kuřáci mají vyšší počet Langerhansových buněk v peribronchiálním intersticiu a v alveolech.
Soubor nemocných
Z 5 222 nemocných přijatých na I. kliniku TRN 1. LF UK a VFN mělo 12 nemocných PGLB (0,22 % souboru). Jednalo se o 6 mužů a 6 žen průměrného věku 41 ±17 let, 11 kuřáků a jednu nekuřačku. Nejčastějšími symptomy onemocnění byla námahová dušnost a kašel. Nemocní měli mírnou obstrukční ventilační poruchu (FEV1 74,1 ± 17,6 % n.h.) se středně těžce sníženou difuzní kapacitou plic pro CO (DLCO – 53,8 ± 17,3 % n.h.). HRCT skeny hrudníku prokazovaly změny kompatibilní s diagnózou PGLB. Diagnóza byla podpořena vyšetřením bronchoalveolární lavážní tekutiny immunocytologicky (CD1+ buňky 32,9 ± 13,6 %, průkaz S - 100 proteinu). U všech kuřáků jsem doporučili zákaz kouření, u 7 nemocných jsme podali ještě glukokortikoidy. U 3 nemocných jsme pozorovali progresi onemocnění, jeden nemocný v průběhu sledování zemřel na respirační insuficienci.
Podrobné nálezy u jednotlivých nemocných jsou uvedeny v tab. 1.
Tab. 1. Nálezy u jednotlivých pacientů. 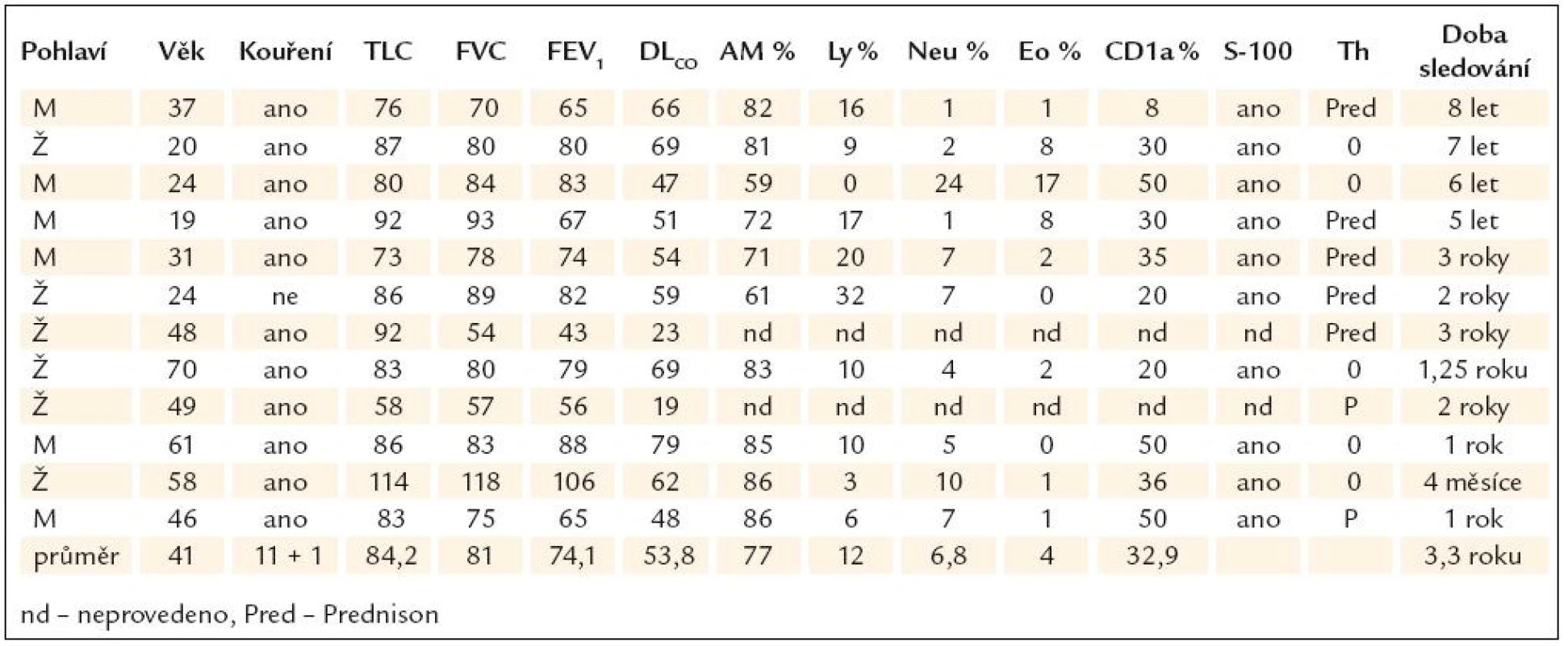
Diskuze
Plíce jsou u PGLB postiženy častěji u dospělých než u dětí. U dospělých se vyskytuje postižení plicní nejčastěji izolovaně, kdežto u dětí je často součástí multisystémového onemocnění. 90 % dospělých pacientů s plicní formou jsou kuřáci cigaret [5].
Klinicky může být onemocnění asymptomatické (ve 30 – 50 %) nebo se může manifestovat širokou škálou příznaků, nejčastěji suchým kašlem, námahovou dušností, febriliemi, schváceností, ztrátou hmotnosti, hemoptýzou. Někdy vyhledá nemocný lékaře pro náhle vzniklou dušnost a bolest na hrudi pleurálního charakteru při pneumotoraxu (15 %). V průběhu onemocnění může dojít k rozvoji diabetes insipidus (5 – 10 %).
Na skiagramu hrudníku tvoří histiocytární ložiska obraz uzlíků hvězdicovitého tvaru. U pokročilejšího onemocnění je RTG nález charakteru voštinovité plíce s cystami a bulami. Intersticiální změny jsou většinou symetrické s maximem ve středních třetinách plicních polí. I u pokročilého onemocnění nález šetří oblast kostofrenických úhlů. Někdy může být přítomen i pleurální výpotek nebo pneumotorax [3].
Na výpočetní tomografii hrudníku se infiltrace plic projeví tvorbou malých cyst do velikosti 10 mm a mikronodulárními denzitami. Prasknutím těchto cyst a jejich komunikaci s pleurální dutinou dochází ke spontánnímu pneumotoraxu. Noduly odpovídají histologickému nálezu granulomů. Nález denzit typu mléčného skla není pro toto onemocnění typický [3].
Při vyšetření funkce plic nacházíme jak restriktivní ventilační poruchu, tak i obstrukci, nebo kombinovanou ventilační poruchu. Ventilační parametry mohou být i v normě. Záleží na pokročilosti onemocnění. S progresí choroby spojené s tvorbou bul a cyst dochází ke zvyšování reziduálního objemu a poměru RV/ TLC. Nejcitlivějším funkčním parametrem při tomto onemocnění je snížení difuzní kapacity plic (DLCO).
U plicního postižení při granulomatóze z Langerhansových buněk je diagnózu možno stanovit pomocí bronchoalveolární laváže. Langerhansovy buňky lze v získaném materiálu identifikovat průkazem CD1a pozitivních buněk nebo elektronmikroskopickým vyšetřením lavážní tekutiny s nálezem Birbeckových granul. Langerhansovy buňky se pozitivně barví na S - 100 protein, CD1a glykoprotein a v elektronové mikroskopii jsou v jejich cytoplazmě přítomna Birbeckova granula. V případě plicní formy granulomatózy z Langerhansových buněk je v lavážní tekutině více než 5 % CD1a buněk, zatímco u zdravých osob je počet CD1a buněk menší než 1 % [7]
Přínosem v diagnóze může být i plicní biopsie, kde nacházíme charakteristický obraz granulomů a cystických změn. Časné stadium onemocnění se vyznačuje přítomností granulomů a vyplněním alveolů Langerhansovými buňkami a pneumocyty 2. typu. V pokročilém stadiu je přítomna fibróza s tvorbou cyst a voštinovité plíce. Fibroblastická proliferace v granulomech nahrazuje buněčné infiltráty centripetálně [1,2,5].
Diferenciálně diagnosticky je nutno odlišit granulomatózu z Langerhansových buněk od kryptogenní fibrotizující alveolitidy, exogenní alergické alveolitidy, lymfangioleiomatózy, Wegenerovy granulomatózy nebo sarkoidózy [1,4].
Při léčbě onemocnění záleží na rozsahu onemocnění, zda se jedná o postižení jednoho systému, nebo zda jde o postižení. U obou je však nejdůležitější zákaz kouření. U izolovaného postižení plic je po zanechání kouření možná spontánní remise. Jinak základní léčbou je kortikoterapie (prednison v dávce 0,5 – 1 mg/ kg s postupným snižováním po dobu 6 – 9 měsíců). Další volbou v léčbě jsou cytostatika etopozid nebo vinblastin. U pacientů s progresí onemocnění přes léčbu vedoucí k těžké hypoxemii s event. plicní hypertenzí je indikována transplantace plic.
Prognóza u plicního postižení je v 80 – 90 % dobrá, v 10 – 20 % špatná. K prognosticky nepříznivým faktorům patří věk, celkové symptomy, opakované pneumotoraxy, výrazná porucha funkce plic, pokročilé změny na skiagramu hrudníku charakteru voštinovité plíce a HRCT hrudníku, mimoplicní postižení s výjimkou kostní léze.
prof. MUDr. Jiří Homolka, DrSc.
www.ftn.cz
e-mail: jhomolka@cesnet.cz
Doručeno do redakce: 21. 7. 2010
Zdroje
1. Homolka J, Křepelka J, Velenská Z. Záměna histiocytózy X za kryptogenní fibrotizující alveolitidu. Prakt Lék 1991; 71 : 20 – 22.
2. Kodet R, Zítková M. Morfologické a rentgenové plicní nálezy při disseminované histiocytóze X. Čs Pediat 1985; 40 : 634 – 638.
3. Moore AD, Godwin JD, Müller NL et al. Pulmonary histiocytosis X: comparison of radiographic and CT findings. Radiology 1989; 172 : 249 – 254.
4. Skácel Z, Marel M, Vraštilová P et al. Histiocytóza z Langerhansových buněk. Stud Pneumol Phthiseol 2000; 60 : 150 – 156.
5. Tazi A. Adult pulmonary Langerhans’ cell histiocytosis. Eur Respir J 2006; 27 : 1272 – 1285.
6. Yağci B, Varan A, Cağlar M et al. Langerhans cell histiocytosis: retrospective analysis of 217 cases in a single center. Pediatr Hematol Oncol 2008; 25 : 399 – 408.
7. Zeppa P, Cozzolino I, Russo M et al. Pulmonary Langerhans cell histiocytosis (histiocytosis X) on bronchoalveolar lavage: a report of 2 cases. Acta Cytol 2007; 51 : 480 – 482.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2010 Číslo Supplementum 2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Intermitentní hladovění v prevenci a léčbě chorob
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Postižení plic u pacientů s multiorgánovou formou histiocytózy z Langerhansových buněk. Popis 8 pacientů a přehled literatury
- Přínos PET-CT pro diagnostiku a sledování plicní formy histiocytózy z Langerhansových buněk
- Přehled léčby histiocytózy z Langerhansových buněk u osob dospělého věku
- Použití kladribinu v první linii léčby multifokální anebo multiorgánové formy histiocytózy z Langerhansových buněk u dospělých osob
- Radioterapie histiocytózy z Langerhansových buněk
- Hemofagocytující lymfohistiocytóza
- Erdheimova-Chesterova nemoc v obrazech
- Nekrobiotický xantogranulom – vzácná kožní komplikace u nemocného s mnohočetným myelomem
- Leukemie z dendritických buněk CD4+56+, typ DC2
- Systémová mastocytóza
- Histiocytóza z Langerhansových buněk u dospělých
- Histiocytóza z Langerhansových buněkz pohledu patologa
- Diagnostická patológia non-Langerhansových histiocytóz
- Histiocytóza z Langerhansových buněk u dětí a dospívajících
- Slovo úvodem
- Granulomatóza z Langerhansových buněk
- Projevy histocytózy z Langerhansových buněk v ORL oblasti
- Projevy histiocytózy z Langerhansových buněk v orofaciální oblasti
- Představení histiocytárních chorob, o nichž pojednává toto supplementum časopisu Vnitřní lékařství
- Histiocytóza z Langerhansových buněk – kožní aspekty onemocnění
- Postižení CNS histiocytózou z Langerhansových buněk a Erdheimovou-Chesterovou nemocí. Přínos PET-CT vyšetření pro diagnostiku a vyhodnocení léčebné odpovědi
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Hemofagocytující lymfohistiocytóza
- Erdheimova-Chesterova nemoc v obrazech
- Systémová mastocytóza
- Histiocytóza z Langerhansových buněk u dětí a dospívajících
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



