-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Familiární hypercholesterolemie včera a dnes.
Vlastní zkušenosti a nálezy u našeho souboru nemocných s familiární hypercholesterolemií
Familial hypercholesterolemia – past and present.
My experiences and findings in our group of patients with familial hypercholesterolemiaCurrently, the familial hypercholesterolemia (FH) rises the interest. The reason is that this genetic disorder is targeted by newly emerged and highly effective hypolipidemic agents, PCSK-9 inhibitors, lomitapid and mipomersen. Present paper discusses 2 patient study groups, before 50 years and nowadays. Although direct statistical analysis is impossible some changes in clinical features of FH might be found over the course of the time. In fact, the basic FH characteristic has not changed dramatically. Severe isolated hypercholesterolemia with total cholesterol 9–10 mmol/l, LDL-cholesterol 7–8 mmol/l and normal values of triglycerides dominates in laboratory analysis. Interestingly, the values of triglycerides increase and almost reach the pathological range in comparison to the values from the period 50 years ago. The values of HDL-cholesterol are normal. Manifestation of CHD in male patients over 40 years of age and in female patients over 50 years of age is not exceptional (rarely occur cases of myocardial infarction in third decade of age). Typical clinical manifestation of FH is xanthomatosis. The early detection and aggressive treatment in FH patients cause that xanthoma tendinosum, xanthelesma and arcus lipoides are less frequent as decades ago. Obesity, diabetes mellitus (DM) and hypertension do not belong to typical clinical sign of FH.
Keywords:
CAD – familial hypercholesterolaemia – HDL-cholesterol – LDL-cholesterol – triglycerides – xanthoma
Autoři: Richard Češka; Michal Vrablík; Tereza Altschmiedová; Martina Prusíková; Zuzana Urbanová; Josef Šobra
Působiště autorů: Centrum preventivní kardiologie III. interní kliniky 1. LF UK a VFN Praha, přednosta prof. MUDr. Štěpán Svačina, DrSc., MBA
Vyšlo v časopise: Vnitř Lék 2014; 60(11): 963-969
Kategorie: Přehledné referáty
Souhrn
V současné době je věnována familiární hypercholesterolemii (FH) po letech opět zvýšená pozornost. Je tomu tak především proto, že se toto geneticky podmíněné onemocnění stává cílem velmi účinných nových hypolipidemik, PCSK-9 inhibitorů, lomitapidu a mipomersenu. Předložené sdělení se zabývá popisem 2 souborů nemocných (vždy ve své době z největších na světě), před 50 lety a nyní. I když přímé statistické srovnání není možné, lze přeci jen najít v klinickém obrazu FH jisté vývojové změny. Faktem však je, že základní charakteristika FH se zásadně nezměnila. V biochemickém obrazu dominuje těžká izolovaná hypercholesterolemie s hodnotami celkového cholesterolu 9–10 mmol/l, s hodnotami LDL-cholesterolu 7–8 mmol/l a s normálními hodnotami triglyceridů. Je zajímavé, že právě triglyceridy se při srovnání s dobou před 50 lety významně zvyšují a dosahují hraničních hodnot. Hladiny HDL-cholesterolu jsou normální. Manifestace ICHS ve věku od 40 let u mužů a od 50 let u žen není výjimkou (ojediněle se vyskytují i případy infarktu myokardu již ve 3. dekádě života). Klasickou klinickou manifestací FH je xantomatóza. Pravděpodobně v důsledku časné detekce nemocných s FH a účinné agresivní léčby se se šlachovými xantomy, s xanthelasma palpebrarum a arcus lipoides setkáváme méně často než před desítkami let. Obezita, diabetes mellitus (DM) ani hypertenze nepatří mezi typické klinické příznaky FH.
Klíčová slova:
familiární hypercholesterolemie – HDL-cholesterol – ICHS – LDL-cholesterol – triglyceridy – xantomÚvod
Na počátku nelze opomenout několik historických údajů, ale především pilotní práci věnovanou familiární hypercholesterolemii (FH), kterou vydal jako první monografii na světě o tomto onemocnění prof. J. Šobra v roce 1970.
Když jsem se odhodlával k určitému srovnání alespoň základních klinických i biochemických nálezů z doby před půl stoletím a dnes, trochu jsem se obával, že ve srovnání nevyjde současnost (zejména pokud jde o naši preciznost ve shromažďování údajů) příliš dobře. Naštěstí zapůsobil nejen lidský faktor, ale také schopnost některých kolegů maximálně využít počítačových technologií a elektronických medií, a tak můžeme konstatovat, že se podařilo problematiku FH v centru založeném prof. Šobrou trochu posunout kupředu. A to navzdory faktu, že Šobra byl ve své době nejdříve jediným expertním centrem pro celé Československo a pacienti dojížděli až z Košic, zatímco s námi o pacienty kompetuje nejen široká síť MedPed, ale i mnozí jednotliví lékaři, kteří se o pacienty s těžkou hypercholesterolemií starají sami. Šobrův, na svou dobu obrovský soubor, jehož výsledky budu prezentovat, tvořilo 196 osob. V té době největší soubor na světě byl soubor Adlesbergův, který čítal 390 osob.
Naše centrum má v současné době v péči celkem 835 nemocných s FH (763 dospělých a 72 dětí do 18 let). Takže nárůst pacientů opravdu je, a významný.
FH v 60. letech minulého století
Na tomto místě bych si dovolil demonstrovat to, jak byla FH studována a jak popsal svůj soubor Šobra.
Ve studovaném souboru bylo zahrnuto celkem 196 osob, 94 mužů a 102 žen, průměrného věku 38,9 let, muži i ženy měli stejný věkový průměr. Kompletní data pak autor shromáždil u souboru 142 nemocných, 69 mužů a 73 žen, průměrného věku 44,3 let. Je pozoruhodné, že soubor tvořilo 103 členů 20 postižených rodin s FH a dále pak „pouze“ 39 jednotlivých pacientů.
Latentní forma onemocnění (bez jediného příznaku včetně koronární insuficience) byla prokázána u 53 nemocných, tedy 38 % sledovaného souboru. Průměrný věk těchto osob byl 33,5 roku. Průměrná hladina cholesterolu byla 317 mg/dl (= 8,2103 mmol/l).
Klinicky manifestní forma FH, tj. nález alespoň jednoho z typických klinických příznaků FH (arcus senilis, xanthelasma palpebrarum, xanthoma, koronární insuficience) byla nalezena u 66 žijících pacientů (62 %) průměrného věku 50 let. Průměrná koncentrace cholesterolu byla 385 mg/dl (= 9,971 mmol/l). Na infarkt myokardu (IM) zemřelo 23 pacientů s typickými nálezy pro FH.
Rozdíl mezi hladinami cholesterolu u latentní a manifestní formy FH byl statisticky významný na hladině p = 0,001. Pokud jde o zastoupení obou forem podle věku, manifestní forma začala převažovat (nikdy však zcela zásadně, dosahovala hodnot ≥ 60 %) od věku nad 30 let.
Není překvapivé, že hladiny cholesterolu stoupají s věkem, a to jak u normální populace (kontrolních osob), tak u nemocných s FH. Statisticky významné rozdíly lze prokázat v každé věkové skupině (graf 1), maximální koncentrace dosahují zejména nemocní s FH ve věku 40 a více let.
Graf 1. Věk a cholesterol. Upraveno podle Šobry J [19] ![Věk a cholesterol. Upraveno podle Šobry J [19]](https://pl-master.mdcdn.cz/media/image/a0f21bbe61a88223899c676fc18bac1c.jpg?version=1537795638)
Arcus senilis corneae se vyskytoval ve skupině nemocných s FH ve 30,3 %. Průměrný cholesterol byl 399 mg/dl (= 10,334 mmol/l).
Xanthelasma palpebrarum se vyskytovalo u 22,7 % pacientů souboru FH. Cholesterol byl u nositelů xanthelasma palpebrarum 381 mg/dl (= 9,868 mmol/l).
Jakákoliv forma xantomatózy byla u nemocných s FH přítomna u 10 %. Průměrná cholesterolemie těchto nemocných byla 469 mg/dl (= 12,147 mmol/l). Je zjevné, že pacienti s xantomatózou jsou ze skupiny nemocných s nejvyššími hodnotami cholesterolu.
Projevy koronární insuficience patří mezi klinicky nejzávažnější, ale i nejčastější komplikace FH. Za mimořádně závažné považoval již Šobra to, že ischemická choroba srdeční může být jediným klinickým projevem FH, který ale může vést k jejich náhlému úmrtí. Velmi významným faktem je i velmi časná manifestace ICHS, často to může být už ve 3. decéniu (v případě homozygotů již od 1. decénia).
V sestavě 142 nemocných s FH byla diagnostikována ICHS u 49 pacientů, tj. u 34,5 %. Z tohoto počtu zemřelo na IM 23 nemocných, 13 žijících nemocných prodělalo IM a dalších 13 pacientů mělo syndrom anginy pectoris (graf 2). Pacienti, kteří zemřeli na IM, zemřeli ve věku 53,5 let, u nemocných, kteří „pouze“ IM prodělali, byl průměrný věk 48,4 roku a konečně u nemocných se stenokardiemi byl průměrný věk 52 let. Hladiny cholesterolu u nemocných po IM, resp. se stenokardiemi byly 404 mg/l (= 10,464 mmol/l), resp. 393 mg/dl (= 10,179 mmol/l).
Graf 2. ICHS podle věku. Upraveno podle Šobry J [19] ![ICHS podle věku. Upraveno podle Šobry J [19]](https://pl-master.mdcdn.cz/media/image/bb474b1e05d727dea5750093eed4230e.jpg?version=1537796254)
U 4 nemocných diagnostikoval Šobra ischemickou chorobu dolních končetin (ICHDK) jako další možnou manifestaci aterosklerózy.
Obezita byla prokázána pouze u 12,5 % studovaného souboru. Tato data jsou plně konzistentní s opakovaně prezentovaným faktem, že nemocní s FH jsou spíše štíhlí a obezita rozhodně nepatří mezi typické průvodní jevy FH, ani do jejího klinického obrazu. Naopak, mnozí autoři se domnívají, že do obrazu FH patří spíše „štíhlost“.
Arteriální hypertenzi ve svém souboru Šobra prokázal u 17,5 %. Tedy situace ne nepodobná výše zmíněné obezitě. Rozhodně nelze tvrdit, že by nemocní s FH častěji trpěli hypertenzí.
V popisovaném souboru byly zachyceny 2 cévní mozkové příhody (CMP), jedna hemoragická a jedna ischemická.
Diabetes mellitus (DM) neměl žádný z členů rodin s prokázanou FH (kteří tvořili většinu popisovaného souboru s FH). Jednotlivci s prokázanou FH (mimo rodiny) měli ojediněle DM2T – ti však byli ze sledovaného souboru vyřazeni. Opět konzistentní nález se současnými názory.
Naše výsledky v současnosti
Jak je uvedeno výše, v současné době má naše Centrum preventivní kardiologie (pokračovatel a nástupce Šobrovy lipidové kliniky) v péči celkem 835 nemocných s FH, z toho 763 dospělých a 72 dětí do 18 let.
V dalším textu budeme vycházet ze zúženého souboru 558 dospělých, u kterých jsou k dispozici pokud možno kompletní data. Mužů je 163 a žen 395, průměrného věku 59,5 ± 18,4 roku. Průměrný věk žen je vyšší, 62,2 ± 17,9 let, mužů 53 ± 18,0 let. V souboru je 467 probandů a 91 rodinných příslušníků. (Hned na tomto místě musíme uvést, že velmi nízké procento záchytu FH v rodinách považujeme za největší vlastní chybu a chceme zdůraznit, že zlepšením diagnostiky na základě rodinné anamnézy a genetické epidemiologie je možné zachytit a preventivně včas zasáhnout u velké skupiny zatím asymptomatických nemocných).
Hladiny lipidů jsou uvedeny v tab. 1. Prezentované hodnoty jsou uvedeny jak v Šobrově souboru, tak u pacientů současného centra nativně, bez farmakologické léčby (i proto je náš uvedený soubor jen menším výběrem ze souboru celého.
Tab. 1. Naše a Šobrovy výsledky (mmol/l). Upraveno podle Šobry J [19] ![Naše a Šobrovy výsledky (mmol/l). Upraveno podle Šobry J [19]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/d0047f0a592d0366a116f50b8f7c66dd.jpg)
TC – celkový cholesterol TG – triglyceridy FH – familiární hypercholesterolemie Koncentrace celkového cholesterolu v našem souboru byla 9,732 ± 1,713 mmol/l. Koncentrace triglyceridů je v našem souboru 1,762 ± 0,654 mmol/l, koncentrace HDL-cholesterolu je 1,722 ± 0,409 mmol/l a koncentrace LDL-cholesterolu je 7,227 ± 1,689 mmol/l.
Dále je velmi zajímavé srovnání hodnot lipidogramů u různých podskupin našich nemocných, jako je soubor dospělých jedinců, dětí, soubor dospělých pacientů s prokázanou mutací LDL receptoru a soubor dospělých pacientů s prokázaným familiárním defektem apolipoproteinu B-100 (FDB pozitivní), tab. 2.
Tab. 2. Srovnání lipidogramů různých podskupin našeho souboru 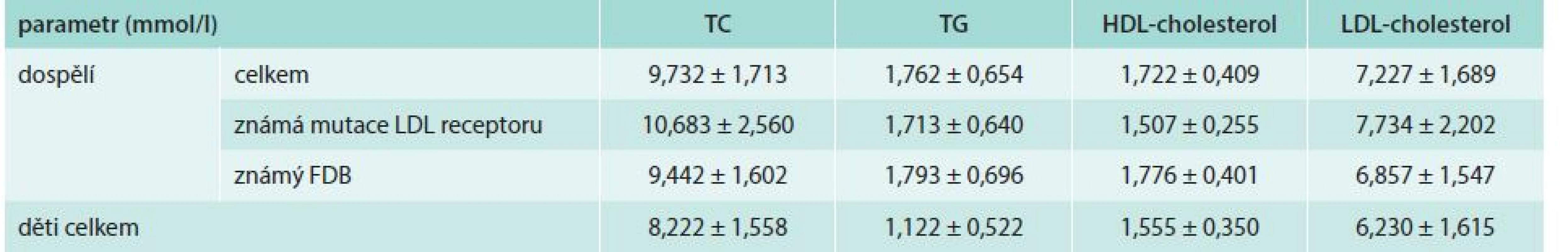
TC – celkový cholesterol TG – triglyceridy FDB – familiární defekt apolipoproteinu B-100 Uvedené výsledky asi nejsou překvapivé. Celkový cholesterol 9,7 mmol/l, LDL-cholesterol lehce přes 7 mmol/l, HDL-cholesterol přitom zcela v normě (FH opravdu není problémem HDL-cholesterolu a už vůbec ne triglyceridů). To, že pacienti s prokázanou mutací v LDL receptoru mají výraznější poruchu lipidogramu, je asi pochopitelné ve srovnání s nemocnými, kteří „jen“ splňují kritéria klinické diagnózy FH (a tudíž databáze MedPed). Možná bychom očekávali nižší hodnoty u nemocných s FDB, který bývá považován za „méně vyjádřenou“ formu geneticky podmíněné hypercholesterolemie. Ostatně i naše dříve publikované výsledky, především u homozygota FDB (v té době druhá kazuistika na světě) spíše ukazovaly na nižší hodnoty cholesterolu a LDL-cholesterolu. Teprve ve větší skupině se rozdíl mezi FH a FDB setřel.
Další zajímavý údaj přinášejí níže uvedená data. Jedná se o pacienty s velmi významnou odchylkou (významným zvýšením) celkového cholesterolu (TC) a LDL-cholesterolu. Z praktického hlediska má význam především fakt, že jako kritérium „těžce postiženého“ nebo „severe“ FH se považuje LDL-cholesterol > 8 mmol/l, tedy z našeho souboru tvoří „severe“ FH zhruba 1/4 (přesněji 24 %). Tito nemocní by v budoucnu měli být kandidáty současné moderní léčby novými hypolipidemiky.
Budu to zdůrazňovat opakovaně, ale zvýšení triglyceridů (TG) nepatří do obrazu FH. A jestli jsou TG zvýšeny, pak pouze lehce. Průměrná hodnota jen minimálně, v desetinách mmol/l, překračovala normální hodnotu a zcela normální hladiny TG byly u více než u poloviny nemocných (tab. 3). I tak se však domnívám, že zvýšení TG v našem souboru je novějším fenoménem, který je důsledkem životního stylu, typického pro českou populaci počátkem třetího tisíciletí.
Tab. 3. Zastoupení pacientů v našem souboru dle hladin jednotlivých lipidových parametrů 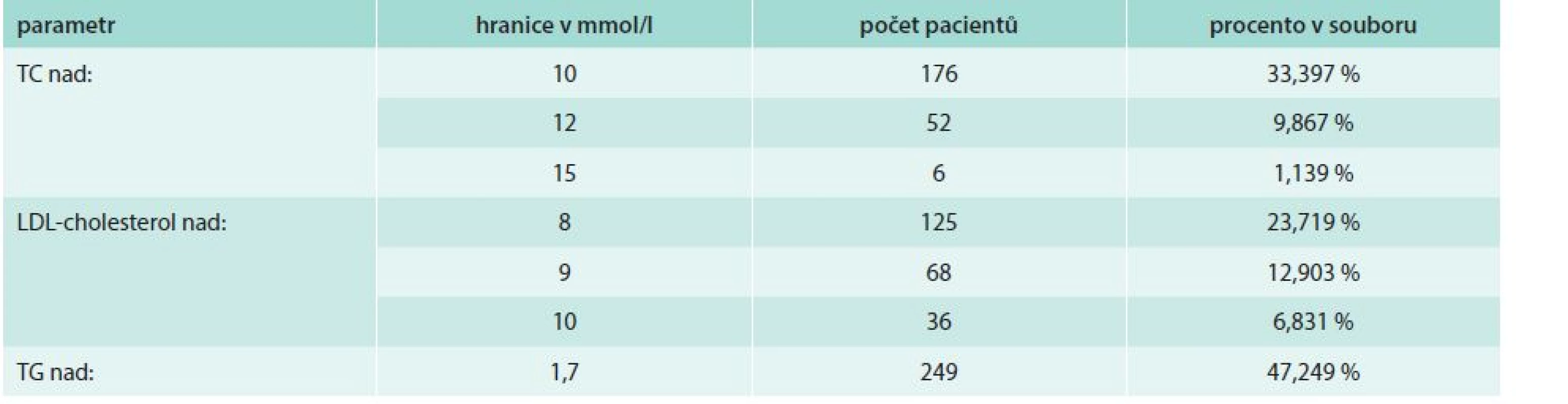
TC – celkový cholesterol TG – triglyceridy Pokud jde o klinické projevy FH, nalezli jsme šlachové xantomy u necelých 5 %, arcus lipoides corneae u necelých 3 % a xanthelasma palpebrarum u téměř 6 % osob z námi sledovaného souboru.
K diagnostice, a tím pádem i výskytu manifestní aterosklerózy (nebo kardiovaskulárních onemocnění vcelku) nebylo přistoupeno zcela systematicky a jednotně, a proto se diagnóza opírá někdy o klinická data, někdy o data anamnestická, někdy jde o výsledky standardních i vysoce sofistikovaných vyšetření invazivní kardiologie. Navíc nezahrnujeme pod pojem sekundární prevence pozitivní výsledky „pátrání po subklinické ateroskleróze“. S těmito výhradami uvedeme, že v sekundární prevenci byla přesně 1/3 našeho souboru a 2/3 byly v prevenci primární. Velmi časnou manifestaci aterosklerotické komplikace (u muže do 45 let a do 55 let u ženy) jsme nalezli u 87 nemocných, tedy 15,6 % ze všech kompletně dokumentovaných pacientů. Časnou manifestaci (do 55 let u muže a do 65 let u ženy) dokumentujeme u 76 pacientů, tedy 13,6 %. Nemocných s manifestací KVO ve věku vyšším než 55 let u mužů a 65 let u žen jsme pak u našich FH pacientů prokázali jen u 4 %.
Když si poté analyzujeme samotný soubor v sekundární prevenci, tedy 186 nemocných, vidíme velmi netypické rozložení výskytu KVO. Nejvíce je zastoupena skupina nejmladších (muž do 45 a žena do 55 let) ve 47 %, dalších 41 % pak tvoří pacienti ve věku muž do 55 a žena do 65 let. Nejmenší počet nemocných, u kterých se vyskytla manifestní ateroskleróza, pak byl ve skupině nejstarší, tedy muži nad 55 a ženy nad 65 let. Bylo jich jen 12 % ze všech „manifestních ateroskleróz“.
Jak se změnila FH za 50 let?
Srovnání obou souborů je samozřejmě více než obtížné. Přeci jen ale vypovídá o několika aspektech péče o nemocné s FH. Začnu rozdíly, u kterých opravdu asi nelze vyvozovat závěry, které by odpovídaly „tvrdým“ důkazům evidence based medicíny. Už vznik obou souborů byl rozdílný. Šobra byl ve své době jediným, kdo se zabýval problematikou familiární hypercholesterolemické xantomatózy. A právě na xantomatózu byl kladen velký důraz. Doporučováni byli nemocní z oddělení ortopedických (šlachová xantomatóza a ruptury Achillovy šlachy při infiltraci cholesterolem), očních (xantelazmata) či kožních (různé lokalizace xantomů). Při klinickém vyšetření bylo pátrání po xantomatóze prioritní. V současné době se nejvíce nemocných dostává do našeho centra buď pro těžkou hypercholesterolemii, kterou nelze zvládnout v terénu běžnou léčbou, při intoleranci statinů, a také z oddělení intenzivní kardiologie pro časné manifestace ICHS. Šobrův soubor je tvořen (správně) příslušníky rodin s FH. Naši nemocní s FH jsou prakticky výhradně jednotlivci (proč nejsou zahrnuti příslušníci rodin má celou řadu subjektivních i objektivních důvodů z reálného života i medicíny v roce 2014).
Šobrův soubor je skoro o 20 let mladší. Samozřejmě, že obrovský rozdíl představuje historická terapie, kterou představoval (z dnešního hlediska u FH absolutně neúčinný) klofibrát, ve srovnání s vysokou dávkou statinu, navíc často v kombinaci s ezetimibem.
To, že Šobra nalézal xantomata, arcus senilis či xantelazmata významně častěji než my, má dva hlavní důvody. První je popsán výše v popisu vzniku jeho souboru. Co je však i z klinického hlediska podstatnější je to, že xantomatózy objektivně ubývá. Důvodem je nezpochybnitelná regrese (a také nerozvinutí) xantomů při a po intenzivní hypolipidemické léčbě.
Pokud jde o ICHS, jsou velké rozdíly už v diagnostice a klasifikaci. Přesto lze nalézt nějaké společné aspekty. Především je to manifestace v mladším věku, kterou prokázal Šobra, a ke stejnému závěru docházíme i u našeho souboru. Nízký výskyt KVO ve vyšším věku je vysvětlitelný dvěma faktory. Bohužel se řada nemocných vyššího věku a manifestace KVO nedožije. Druhá možnost je pro nás stále velkou motivací k výzkumu. Je to fakt, že někteří nemocní s FH se dožívají vysokého věku, aniž by se u nich rozvíjela byť jen subklinická ateroskleróza. Identifikovat protektivní faktory, ev. najít určité genetické vlohy, které zabrání (třeba ve vzájemné interakci) manifestaci KVO u FH, představuje velký cíl. ICHS byla a je dominující klinickou manifestací aterosklerózy. CMP i ICHDK se vyskytovala i vyskytuje jen u minimálního počtu nemocných.
Z metabolických onemocnění je především zajímavé, že obezita nepatřila ani nepatří v současnosti mezi typické klinické nálezy u pacientů s FH. Její výskyt u FH odpovídá výskytu v populaci, nebo je dokonce významně nižší. Druhou významnou metabolickou chorobou, která rovněž nebývá často přítomná u FH, byl a je DM 2. typu. Šobra dokonce ve svém souboru neprokázal DM2T u žádného z nemocných s FH, ani my jsme neprokázali výskyt DM2T vyšší než v běžné populaci.
Zajímavé je to, že nativní hodnoty cholesterolu se u nemocných s FH před půl stoletím prakticky nelišily od hodnot, které nacházíme u pacientů s tímto onemocněním my. Další parametry, které sledoval Šobra, jsme již neměřili, mnohé modernější parametry nebyly v polovině minulého století dostupné (ani známé). To ale nic nemění na faktu, že dieta a životní styl nehrají u FH významnou roli, hladiny TC a LDL-cholesterolu jsou determinovány především geneticky, a jediným parametrem, který zřejmě ovlivňují, jsou (u menší části nemocných) triglyceridy (dříve a nyní v dětství u FH hluboce v normě, nyní v dospělosti hraniční).
Jak tedy vypadá pacient s FH? Trochu subjektivně
Samozřejmě, že následující řádky je třeba brát s velkou rezervou. Ale i tak. Pacient/pacientka s FH přichází k vyšetření buď v rámci prevence (ideálně genetické prevence – z rodiny s FH nebo s časnou manifestací KVO), pro nález vysoké hodnoty TC a vysokého LDL-cholesterolu nebo pro (před)časnou manifestaci aterosklerózy a jejích komplikací. Obvykle přichází ve věku 30–50 let.
Jedná se o muže či ženu s celkovým cholesterolem mezi 8–10 mmol/l a LDL-cholesterolem > 7 mmol/l se zcela normální koncentrací HDL-cholesterolu a normálními (nebo maximálně hraničně zvýšenými) koncentracemi TG. Jedná se o osobu s normálním BMI, spíše štíhlou. Nález xantomů či arcus senilis corneae bude spíš výjimečný. Xanthelasmata palpebrarum se sice vyskytovat mohou (nejsou však diagnostická), některá xantelazmata mohou být normocholesterolemická.
V rodinné anamnéze (která je opravdu zásadní a je třeba jí věnovat dostatečnou pozornost) najdeme velmi pravděpodobně údaj o předčasné manifestaci ICHS u přímých příbuzných. Někdo v rodině se pravděpodobně léčí „pro cholesterol“.
Sám nemocný může udávat anamnestický údaj o ICHS v předchorobí. Pokud ne, musíme se pokusit podrobným rozborem anamnézy vyloučit/potvrdit příznaky kardiovaskulárního onemocnění.
V předložené publikaci se nevěnujeme současné ani experimentální léčbě, která je podrobně rozebrána v dalším článku v tomto čísle Vnitřního lékařství.
Obrazová příloha. Xantomy, xanthelasma palpebrarum, arcus lipoides corneae
Obrazová příloha: Xantomy, xanthelasma palpebrarum, arcus lipoides corneae
Publikace byla podpořena granty IGA MZd ČR č. NT 14186 (3/2013) a č. NT 12217 (5/2011).
prof. MUDr. Richard Češka, CSc., FACP, FEFIM
rcesk@lf1.cuni.cz
III. interní klinika 1. LF UK a VFN, Praha
www.vfn.cz
Doručeno do redakce 30. 9. 2014
Přijato po recenzi 22. 10. 2014
Zdroje
1. Nordestgaard BG, Chapman MJ, Humphries SE et al. European Atherosclerosis Society Consensus Panel: Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society. Eur Heart J 2013; 34(45): 3478–3490a.
2. Kastelein JJ, Wedel MK, Baker BF et al. Potent reduction of apolipoprotein B and low-density lipoprotein cholesterol by short-term administration of an antisense inhibitor of apolipoprotein B. Circulation 2006; 114(16): 1729–1735.
3. Horton JD, Cohen JC, Hobbs HH. PCSK9: a convertase that coordinates LDL catabolism. J Lipid Res 2009; 50(Suppl): S172-S177.
4. Qian YW, Schmidt RJ, Zhang Y et al. Secreted PCSK9 downregulates low density lipoprotein receptor through receptor-mediated endocytosis. J Lipid Res 2007; 48(7):1488–1498.
5. Cohen CJ, Boerwinkle E, Mosley TH et al. Sequence variations in PCSK9, low LDL and protection against coronary heart disease. N Engl J Med 2006; 354(12): 1264–1272.
6. Češka R et al. Cholesterol a ateroskleróza, léčba dyslipidémií. 4th ed. Triton: Praha 2012. ISBN 978–80–7387–599–2.
7. Hobbs HH, Brown MS, Goldstein JL. Molecular genetics of the LDL receptor gene in familial hypercholesterolemia. Hum Mutat 1992; 1(6): 445–466.
8. Rader DJ, Cohen J, Hobbs HH. Monogenic hypercholesterolemia: new insights in pathogenesis and treatment. J Clin Invest 2003; 111(12): 1795–1803.
9. Innerarity TL, Weisgraber KH, Arnold KS et al. Familial defective apolipoprotein B-100: low density lipoproteins with abnormal receptor binding. Proc Natl Acad Sci USA 1987; 84(19): 6919–6923.
10. Qian YW, Schmidt RJ, Zhang Y et al. Secreted PCSK9 downregulates low density lipoprotein receptor through receptor-mediated endocytosis. J Lipid Res 2007; 48(7): 1488–1498.
11. Garcia CK, Wilund K, Arca M et al. Autosomal recessive hypercholesterolemia caused by mutations in a putative LDL receptor adaptor protein. Science 2001; 292(5520): 1394–1398.
12. Brown MS, Goldstein JL. A receptor-mediated pathway for cholesterol homeostasis. Science 1986; 232(4746): 34–47.
13. Gudnason V, Sigurdsson G, Nissen H et al. Common founder mutation in the LDL receptor gene causing familial hypercholesterolaemia in the Icelandic population. Hum Mutat 1997; 10(1): 36–44.
14. Tichý L, Freiberger T, Zapletalová P et al. The molecular basis of familial hypercholesterolemia in the Czech Republic: Spectrum of LDLR mutations and genotype-phenotype correlations. Atherosclerosis 2012; 223(2): 401–408.
15. Chmara M, Wasag B, Zuk M et al. Molecular characterization of Polish patients with familial hypercholesterolemia: novel and recurrent LDLR mutations. J Appl Genet 2010; 51(1): 95–106.
16. Nauck MS, Koster W, Dorfer K et al. Identification of recurrent and novel mutations in the LDL receptor gene in German patients with familial hypercholesterolemia. Hum Mutat 2001; 18(2): 165–166.
17. Widhalm K, Dirisamer A, Lindemayr A et al. Diagnosis of families with familial hypercholesterolaemia and/or Apo B-100 defect by means of DNA analysis of LDL-receptor gene mutations. J Inherit Metab Dis 2007; 30(2): 239–247.
18. Fahed AC, Nemer GM. Familial hypercholesterolemia: the lipids or the genes? Nutr Metab (Lond) 2011; 88(1): 23.
19. Šobra J. Familiární hypercholesterolemická xanthomatosa. Avicenum: Praha 1970.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2014 Číslo 11- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Účinnost a bezpečnost inzulinu lispro u obézních pacientů s diabetes mellitus 2. typu: retrospektivní metaanalýza sedmi randomizovaných kontrolovaných studií
- Pražské evropské dny interní medicíny 2014
-
Vrbíková J, Fanta M, Koryntová D. Syndrom polycystických ovarií.
Průvodce ošetřujícího lékaře. - Za profesorem Zdeňkem Plachetou
-
Úvodní slovo předsedy České internistické společnosti J. E. Purkyně profesora MUDr. Richarda Češky, CSc., FACP, FEFIM
Interna a ateroskleróza: Více rozdílů nebo pojítek? -
K preventivní medicíně musí lékař dozrát
Rozhovor s prof. MUDr. Hanou Rosolovou, DrSc. - Empagliflozin: další z tichých revolucionářů – editorial
- Nový SGLT2 inhibitor empagliflozin: moderní a bezpečná léčba diabetu
- Prevence kardiovaskulárních onemocnění v běžné klinické praxi: lze dosáhnout zlepšení?
- Markery reziduálního kardiovaskulárního rizika
- Nové pohledy na hormonální substituční terapii
- Novinky v oblasti hypolipidemické léčby
- Nefarmakologická léčba – výsledky z Poděbrad
-
Familiární hypercholesterolemie včera a dnes.
Vlastní zkušenosti a nálezy u našeho souboru nemocných s familiární hypercholesterolemií - LDL-aferéza v léčbě familiárních hyperlipoproteinemií
- Rozšiřující se možnosti antikoagulační léčby tromboembolické nemoci
- Co mají společného žilní a tepenná onemocnění?
- Kardiovaskulární rizikový profil u 40letých mužů a 50letých žen v České republice: výsledky průřezové studie
-
Adherence pacientů s diabetem 2. typu k aplikaci inzulinových analog: vynechávání, časový posun a snižování dávek
Výsledky průzkumu GAPP2TM (Global Attitudes of Patient and Physicians) v České republice
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Nové pohledy na hormonální substituční terapii
- LDL-aferéza v léčbě familiárních hyperlipoproteinemií
- Nový SGLT2 inhibitor empagliflozin: moderní a bezpečná léčba diabetu
- Rozšiřující se možnosti antikoagulační léčby tromboembolické nemoci
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy















