-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Současný přístup k diagnostice, léčbě a prevenci tuberkulózy
Current approach to diagnostics, treatment and prevention of tuberculosis
Tuberculosis is world-wide spread infectious disease with persistant high incidence, mainly in the densely populated countries with low income. Czech Republic belongs to the countries with highly efficient control of tuberculosis and continuously decreasing incidence of the disease. High-risk population for tuberculosis in the Czech Republic are the homeless people, who together with migrants from the countries with high incidence of tuberculosis represent reservoir of infection for our population. Treatment of tuberculosis is long-term, combined and controlled. Minimal efficious duration of the treatment is 6 moths. The most severe form of tuberculosis is multidrug-resistant tuberculosis (MDR-TB) caused by the strains resistant to basic antituberculous drugs, i.e. rifampicin and isoniasid, the treatment of which lasts 2–3 years. Preventive measures against tuberculosis comprise BCG vaccination in new-born and treatment of latent tuberculous infection in the individuals with risk of development of tuberculosis. Discovery of new drugs and new vaccine against tuberculosis together with financial and material resources designated for systematic search for the patients with tuberculosis and their treatment in the developing countries may enable continuous decrease of incidence of tuberculosis, whilst we can only dream about its fully erradication.
Key words:
diagnosis – epidemiology – prevention – treatment – tuberculosis
Autori: Martina Vašáková
Pôsobisko autorov: Pneumologická klinika 1. LF UK a Thomayerovy nemocnice, Praha
Vyšlo v časopise: Vnitř Lék 2017; 63(11): 815-820
Kategória: Přehledné referáty
Súhrn
Tuberkulóza je celosvětově rozšířeným infekčním onemocněním, s přetrvávající vysokou incidencí, a to hlavně v nejlidnatějších a nejchudších státech světa. Česká republika (ČR) patří k zemím s velmi účinnou kontrolou tuberkulózy a se stále klesající incidencí této nemoci. Rizikovou skupinou v České republice jsou převážně lidé bez domova, kteří představují v ČR spolu s přistěhovalci ze zemí s vysokou incidencí tuberkulózy rezervoár infekce pro naši populaci. Léčba tuberkulózy je dlouhodobá, kombinovaná a kontrolovaná. Minimální účinná doba podávání antituberkulotik je 6 měsíců. Nejzávažnější formou tuberkulózy je multirezistentní tuberkulóza způsobená kmeny rezistentními na základní antituberkulotika, tedy rifampicin a izoniazid. Její léčba trvá 2–3 roky. Mezi preventivní opatření do jisté míry zabraňující rozvoji tuberkulózy patří BCG vakcinace novorozenců a léčba latentní tuberkulózní infekce u jedinců s rizikem rozvoje tuberkulózy. Objev nových léků a případně nové vakcíny proti tuberkulóze spolu s finančními a hmotnými prostředky určenými pro systematické vyhledávání nemocných a jejich léčbu v zemích rozvojového světa snad umožní postupné snížení incidence tuberkulózy celosvětově, i když o její úplné eradikaci zatím můžeme stěží snít.
Klíčová slova:
diagnóza – epidemiologie – léčba – prevence – tuberkulózaÚvod
Tuberkulóza (TB) je celosvětově rozšířeným infekčním onemocněním, jehož incidence bohužel neklesá, neboť nejhorší epidemiologická situace je v nejlidnatějších a ekonomicky nejslabších zemích. Historie TB sahá až do neolitu a původce lidské TB, Mycobacterium tuberculosis, je pravděpodobně starší než druh bovinní. Přítomnost genomu Mycobacterium tuberculosis byla prokázána v kostních ostatcích levantinské populace z doby před více než 8 000 lety [1]. Mykobakterie jako původce TB objevil Robert Koch již před více než 100 lety a základní antituberkulotika máme již více než 50 let, přesto doposud nebyla vynalezena účinná vakcína proti TB a navíc se objevují rezistentní kmeny mykobakterií, na které nacházíme léčbu jen obtížně. Biologické chování mykobakterií s jejich schopností efektivně unikat mechanizmům imunitní odpovědi a nutnost dlouhodobé (několikaměsíční až několikaleté) jsou jednou z hlavních překážek v úspěšném boji proti TB. Tuberkulóza je způsobena skupinou obligátních patogenů pojmenovanou Mycobacterium tuberculosis complex. Toto bakteriální společenství zahrnuje několik blízce příbuzných druhů – Mycobacterium tuberculosis, Mycobacterium bovis, Mycobacterium africanum, Mycobacterium microti, Mycobacterium canettii a Mycobacterium pinnipedii. Vyvolavatelem většiny onemocnění je Mycobacterium tuberculosis, Mycobacterium bovis se uplatňuje jen výjimečně a onemocnění způsobená ostatními druhy jsou zcela raritní. Mycobacterium tuberculosis je schopno života v extracelulárním prostoru, ale přežívá i intracelulárně, rezervoárem pro nové vzplanutí nemoci jsou tzv. dormantní mykobakteria, která jsou obtížně zasažitelná léčbou [2].
Epidemiologie
Epidemiologické ukazatele TB vykazují zcela odlišné ukazatele v rozvinutých zemích, v nichž incidence onemocnění obecně klesá, v kontrastu s lidnatými zeměmi se špatnými socioekonomickými podmínkami, v nichž přetrvává zcela neúnosná situace s obrovským výskytem nemoci i s mortalitou. Navzdory pokrokům, které byly celosvětově učiněny v kontrole TB, tuberkulóza je v současnosti 2. nejčastěji smrtící infekční chorobou světa (po AIDS). Mortalita v důsledku onemocnění TB klesla o 47 % oproti roku 1990, což ve skutečnosti znamená, že v období let 2000–2014 politika prosazování efektivní diagnostiky a léčby TB zachránila 43 milionů životů. Incidence TB klesla celosvětově v průměru o 1,5 % od roku 2000. Počet hlášených případů z roku 2015 sice vzrostl oproti předchozím letům, je to ale dáno spíše zlepšením systému hlášení případů než vzestupem počtu nemocných. Tuberkulóza v roce 2015 zabila 1,4 milionu lidí, z toho 0,4 milionu HIV pozitivních. V témže roce onemocnělo TB 10,4 milionu lidí, z toho 5,9 milionu mužů, 3,5 milionu žen a 1,0 milionu dětí. Z těchto nemocných bylo 1,2 milionu zároveň HIV pozitivních. Počet infikovaných, tedy jedinců s tzv. latentní tuberkulózní infekcí (LTBI – latent tuberculosis infection), na celém světě je odhadován téměř na 2 miliardy [3]. Česká republika patří k zemím s velmi účinnou kontrolou TB se stále klesající incidencí této nemoci, což je dáno jednak naší geografickou polohou, životní úrovní a historicky rozsáhlými zkušenostmi. Z ČR pochází i autor tzv. krátkodobého režimu kontrolované léčby TB (DOTS – directly observed treatment, short course) Karel Stýblo, který tento léčebný režim vyzkoušel poprvé v praxi v Tanzánii v 70. letech minulého století, kde při jeho aplikaci došlo poprvé k poklesu předtím extrémně vysoké incidence této závažné nemoci. V současné době je incidence TB v České republice velmi nízká, a to i v porovnání s většinou ostatních vyspělých evropských zemí. Ne vždy však byla situace tak růžová. Ještě před 100 lety byl výskyt TB v ČR velmi vysoký, v letech 1900–1918 na tuto nemoc v ČR zemřelo 641 000 osob a v roce 1957 mortalita dosáhla neuvěřitelných 376,1/100 000 osob. V témž roce bylo evidováno 137 990 aktivních případů TB (prevalence 1 029/100 000), z toho 9 762 dětí do 14 let. Průlomem bylo Usnesení vlády Republiky československé ze dne 21. 12. 1955 č. 3 593 o opatřeních v boji proti TB, v němž byla stanovena řada kroků v oblasti zdravotnictví a sociální politiky, jež následně vedly konečně ke snižování výskytu TB. Zásadní roli sehrál i objev a rozšíření základních antituberkulotik, zvýšení počtu lůžek pro nemocné s TB na 0,8/100 000 a postupná eradikace TB skotu. Až do roku 1968 však nebyla nařízena izolace nemocných s TB, byla pouze činěna opatření, aby nemocní nemohli TB šířit v zaměstnání. Opatření byla úspěšná, a tak výskyt TB setrvale klesal až na 486 nových případů TB v roce 2015. Průměrný věk nemocných s TB v roce 2015 byl 53 let s převahou mužů, dětských případů TB bylo pouze 5 a 11 pacientů mělo MDR TB (multidrug-resistant TB) a 2 pacienti byli zároveň HIV pozitivní. 29 nemocných na TB zemřelo. I v ČR je mezi pacienty s TB patrný trend zvyšujícího se zastoupení migrantů ze zemí s vyšším výskytem TB, aktuálně u nás tito pacienti představují 20 % z nově zjištěných případů TB [3]. Politika kontroly TB v České republice je tedy nepopiratelně efektivní a nepotvrdily se obavy, že zrušení plošné vakcinace bude mít dopad – hlavně v populaci dětí – na zvýšení incidence TB. Rizikovou skupinou pro TB jsou převážně lidé bez domova, kteří spolu s přistěhovalci ze zemí s vysokou incidencí TB představují v ČR rezervoár infekce pro naši populaci.
Nejzávažnějším zdrojem tuberkulózní nákazy je nemocný člověk, hlavně ten, který vylučuje mykobakterie prokazatelné přímo mikroskopicky. Inkubační doba je 4 týdny až 2 roky od skončení expozice. Nejčastějším způsobem přenosu nákazy je inhalační cesta. Možný je i přenos přímým kontaktem s infekčními sekrety nemocných, při kontaktu s infikovanými předměty nebo přenos zažívacím traktem. Tuberkulózní infekce může postihnout jakýkoli orgán v těle, nejčastěji jsou ale postiženy plíce, které představují i nejčastější bránu vstupu infekce do těla. Z infikovaných osob onemocní během života méně než 10 %, zbylých 90 % má tzv. latentní tuberkulózní infekci (LTBI), která může znamenat riziko vzplanutí nemoci v případě oslabení imunitního systému těchto jedinců.
Klinický nález a vyšetřovací metody
Primární TB vzniká v dětském věku a často probíhá bez příznaků, většinou je jedinou známkou proběhlé primární TB zhojený tzv. Ghonův komplex na skiagramu hrudníku.
Postprimární TB u dospělých se může manifestovat v řadě orgánů a může probíhat chronicky nebo akutně. U většiny nemocných se manifestuje únavou, nechutenstvím, hubnutím, poklesem fyzické výkonnosti, subfebriliemi, nočním pocením a kašlem suchým nebo produktivním, případně s vykašláváním krve, dušností a pohrudniční bolestí [4].
Latentní tuberkulózní infekce (LTBI) znamená přítomnost mykobakterií v organizmu vyvolávající imunitní reakci, která se projeví pozitivitou testů – tuberkulinového kožního testu nebo testu z odebraného vzorku krve, z níž je stanovována reaktivita T-lymfocytů na mykobakteriální antigeny, tzv. IGRA testu. Při LTBI nejsou tedy zobrazovacími metodami prokazatelné známky poškození orgánů a jedinec nemá žádné subjektivní potíže ani klinické příznaky a není infekční pro své okolí.
Objektivní nález je u TB často velmi chudý nebo nespecifický. Pouze v pokročilých fázích TB je patrný výrazný úbytek tělesné hmotnosti až kachexie. Nemocný suše pokašlává, případně může být objektivně klidově dušný při rozsáhlém plicním postižení.
Fyzikální nález na plicích je však obvykle normální, pouze při přítomnosti pleurálního výpotku můžeme pozorovat poklepově ztemnění a poslechově oslabení na postižené straně. Při postižení kloubů a kostí se nad postiženou lokalitou objevuje bílé zduření (tumor albus), v případě tvorby tzv. studených abscesů se mohou tyto provalit navenek a vzniknout chronické, obtížně se hojící píštěle. Při cervikální tuberkulózní lymfadenitidě pozorujeme prominence na krku palpačně odpovídající spečeným paketům uzlin, které nejsou posunlivé vůči okolí a často též kolikvují a tvoří lymfadenokutánní píštěle. Postižení ledvin a močových cest má minimum symptomů, obvykle je zachyceno jako tzv. sterilní pyurie. Postižení orgánů může být i vícečetné.
Z instrumentálních vyšetřovacích metod je nejpřínosnější radiologické vyšetření. Radiologický nález je v případě plicní tuberkulózy poměrně charakteristický, a tak lze s velkou pravděpodobností podezření na TB vyjádřit. Nicméně je třeba mít na paměti, že radiologický obraz TB mohou imitovat i jiné plicní patologie. Zadopřední a boční skiagram hrudníku je základním vyšetřením, a to u plicní i mimoplicní formy TB. Typickou lézí u postprimární TB jsou stíny s projasněními a diseminace nodulárních stínů, případně rozsáhlejší plošná zastínění. Maximum nálezu obvykle bývá v horních plicních polích (obr. 1). V případě mimoplicní TB pak používáme zobrazovací metody pro identifikaci lézí v postižených oblastech dle klinického nálezu (počítačová tomografie – CT mozku, případně magnetická rezonance – MR mozku; CT, případně MR kostí, měkkých tkání nitrobřišních orgánů, ultrasonografické vyšetření ledvin a uzlin, cystoskopie, vylučovací urografie, kolonoskopie) [4].
Obr. 1. Zadopřední skiagram hrudníku u pacienta s rozsáhlou tuberkulózou plic 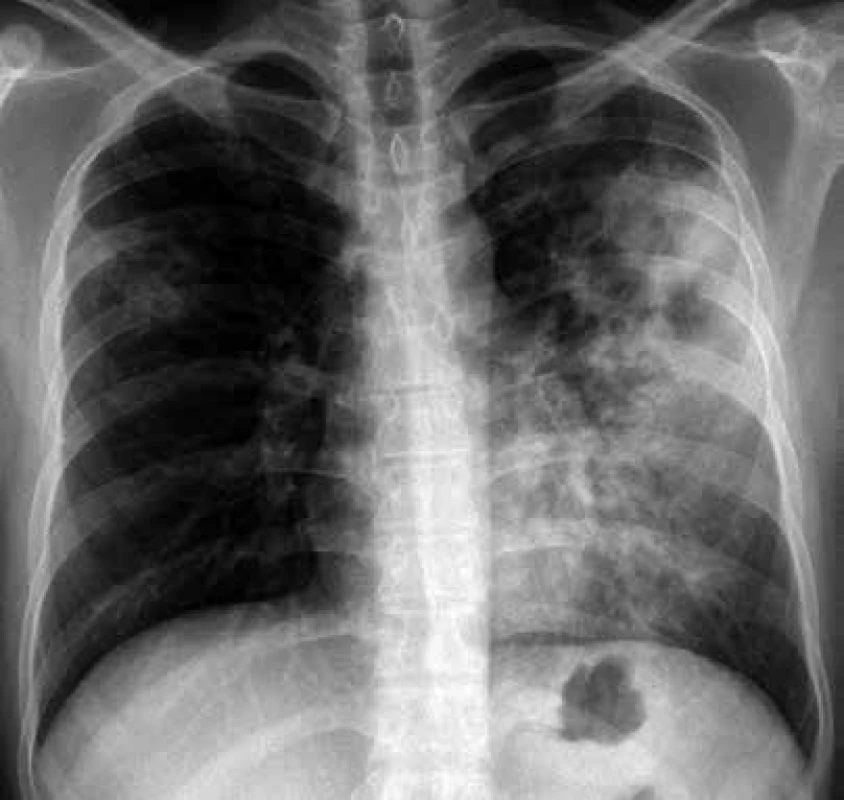
Průkaz TB se opírá o mikrobiologické vyšetření, a to hlavně o pozitivní výsledky kultivace mykobakterií TB z různých materiálů – ze sputa, aspirátu či z výplachu získaného při bronchoskopickém vyšetření, z výpotku, z mozkomíšního moku nebo z jiné tělní tekutiny. Nemocní, kteří vykašlávají velká množství mykobakterií, jsou i mikroskopicky pozitivní; znamená to tedy, že mykobakterie jsou identifikovatelné mikroskopickým vyšetřením jako tzv. acidorezistentní tyče po nátěru biologického materiálu na sklíčko a po speciálním obarvení (Ziehlovo-Neelsenovo barvení). Kultivace biologického materiálu na Mycobacterium tuberculosis je dlouhodobá, kultury se odečítají obvykle po 3, 6 a 9 týdnech, kdy je klasická kultivace ukončena. Nedílnou součástí mikrobiologického kultivačního vyšetření je i stanovení citlivosti mykobakterií na základní antituberkulotika, v případě rezistence pak stanovení rozšířené citlivosti kmene. Kromě klasické mikroskopie a kultivace jsou k detekci mykobakterií využívány i modernější rychlé kultivační metody založené na detekci CO2 uvolňujícího se v přítomnosti metabolicky aktivních mykobakterií (Bactec) a molekulární metody (PCR – polymerase chain reaction/polymerázová řetězová reakce, LCR – ligase chain reaction/ligázová řetězová reakce). Součástí molekulárních metod může být i vyšetření na geny rezistence pro rychlou identifikaci multirezistentní Mycobacterium tuberculosis (GeneXpert MTB/RIF) [3,4].
Další laboratorní vyšetření nejsou pro TB zásadně přínosná, výjimkou je stanovení adenozindeaminázy ve výpotku, které může podpořit podezření na TB pohrudnice. Při průkazu TB je doporučeno zjistit HIV status pacienta, neboť TB se u těchto nemocných objevuje častěji a měli bychom při souběžné HIV infekci ve spolupráci se specializovaným infekčním oddělením u těchto nemocných co nejdříve zahájit antiretrovirovou léčbu.
Imunologické testy založené na uvolňování interferonu γ lymfocyty, ale i jinými buňkami při kontaktu s antigeny mykobakterií (Quantiferon TB, T-spot) identifikují imunitní odpověď proti Mycobacterium tuberculosis. Jejich pozitivita je tedy známkou, že se dotyčný s Mycobacterium tuberculosis setkal a nakazil se. Nicméně těmito testy nelze odlišit, zda má dotyčný pouze LTBI nebo tuberkulózu jako nemoc se všemi klinickými, radiologickými a mikrobiologickými znaky. Dalším imunologickým testem, a to testem in vivo, je tuberkulinový kožní test (TST – tuberculin skin test), tzv. Mantoux II, který však nedokáže odlišit přecitlivělost na Mycobacterium tuberculosis od reakce na jiná mykobakteria včetně vakcinačního kmene.
Nápomocné je i histopatologické vyšetření vzorku plic, pohrudnice, uzlin nebo jiné tkáně získané chirurgickou, bronchoskopickou nebo punkční biopsií, které prokazuje v typických případech epiteloidní granulom, někdy s nekrózou. Důležité je vyšetřit vzorek tkáně také na přítomnost Mycobacterium tuberculosis, a to imunohistochemicky či molekulárně geneticky.
Jako definitivní případ TB je označen pacient, u něhož byla stanovena pozitivita mykobakterií kultivačně či molekulárně genetickými metodami při kompatibilním klinickém a radiologickém nálezu, a pak pacient, u kterého specialista pneumolog usoudí, že se jedná o tuberkulózu a zahájí léčbu [2]. Pro účely další léčby a sledování TB dělíme na plicní a mimoplicní. Plicní TB je onemocnění postihující plicní parenchym. Onemocnění pacienta trpícího současně plicní i mimoplicní formou TB je klasifikováno jako plicní TB. Mimoplicní TB označuje postižení jiných orgánů než plic, např. pleury, lymfatických uzlin (včetně hilových nebo mediastinálních), břicha, urogenitálního traktu, kůže, kloubů a kostí, mening [4].
Léčba
Léčba TB probíhá na specializovaných plicních odděleních, při mimoplicní TB ve spolupráci s příslušnými experty (urology, ortopedy, lékaři ORL, infektology). Léčba TB je dlouhodobá, kombinovaná a kontrolovaná. Minimální účinná doba podávání antituberkulotik je 6 měsíců. Kombinace léků se podává v jednorázové ranní dávce, a to pod kontrolou ošetřujícího personálu (DOTS directly observed treatment, short-course). Základními antituberkulotiky jsou izoniazid, rifampicin, etambutol a pyrazinamid a streptomycin (tab. 1). Ústavní léčba (iniciální fáze terapie) v našich podmínkách trvá minimálně 2 měsíce a podává se 4kombinace (u dříve léčených až 5kombinace) antituberkulotik za účelem debacilizace. Další léčba (pokračovací fáze) trvá minimálně 4 měsíce a podává se 2kombinace (u dříve léčených 3kombinace) antituberkulotik, většinou ambulantně. U malé části nemocných, obvykle s infekcí kmenem Mycobacteria rezistentním na léky (MDR TB), může být léčba doživotní [5–8].
Tab. 1. Dávkování základních antituberkulotik. 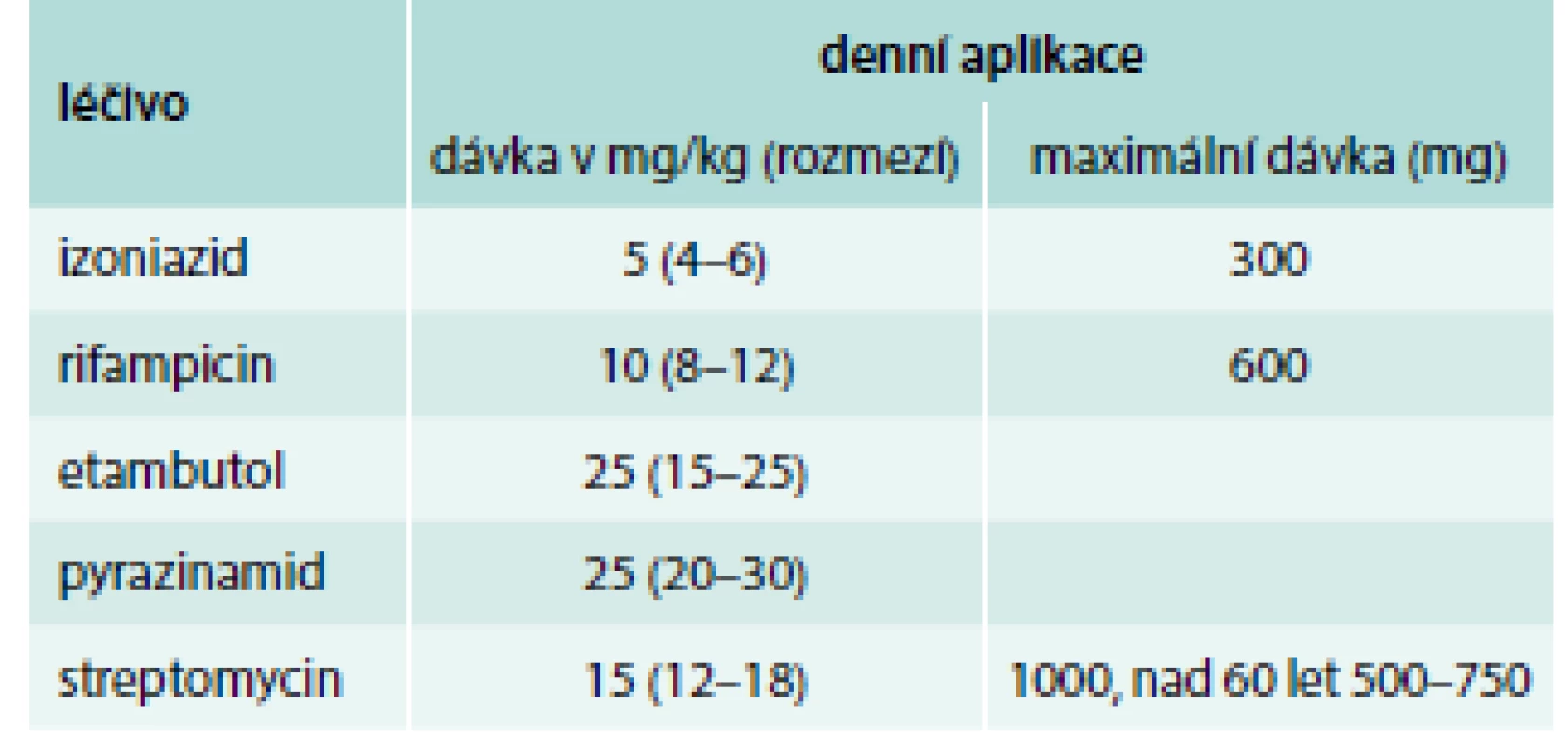
Upraveno podle [9] Režimy léčby závisejí na tom, zda se jedná o nové onemocnění, o recidivu TB, nebo o onemocnění rezistentními kmeny mykobakterií. Novým pacientem je nemocný, který nebyl v minulosti léčen antituberkulotiky nebo který užíval antituberkulózní léčbu po dobu kratší než 1 měsíc bez ohledu na to, zda nález byl či nebyl bakteriologicky ověřen (tab. 2) [9].
Tab. 2. Standardizované režimy pro nové pacienty s tuberkulózou. 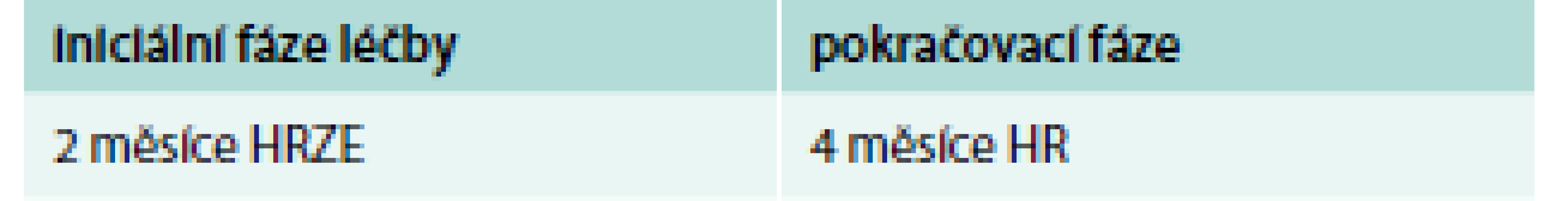
E – etambutol H – izoniazid R – rifampicin Z – pyrazinamid Upraveno podle [9] U nemocných s rezistencí na izoniazid je léčebný výsledek horší než u nemocných se zachovanou citlivostí na izoniazid i v případě, že jim je po 6 měsíců podáván rifampicin. Doporučené režimy pro nemocné, u nichž je podezření na možnou rezistenci na izoniazid, jsou uvedeny v tab. 3.
Tab. 3. Standardizované režimy pro nové pacienty s tuberkulózou z oblastí s vysokým výskytem rezistence na izoniazid*. 
E – etambutol H – izoniazid R – rifampicin Z – pyrazinamid *testy citlivosti nebyly provedeny nebo jejich výsledek není před začátkem pokračovací fáze k dispozici Upraveno podle [9] Komplikovanější je situace v případě pacientů, kteří byli antituberkulotiky léčeni již dříve. Předchozí antituberkulózní léčba je silnou determinantou lékové rezistence a nemocní s předchozí léčbou tvoří významný podíl (13 %) všech globálně hlášených případů rezistence na antituberkulotika (údaj z roku 2007). Ze všech forem lékové rezistence je nejdůležitější identifikovat MDR-TB, protože léčba těchto nemocných základními antituberkulotiky není prakticky vůbec účinná, a navíc se dále násobí rezistence. Rychlá identifikace MDR-TB (molekulární testy na bázi PCR-GeneXpert MTB/RIF) a zahájení léčby dle doporučení Světové zdravotnické organizace léky převážně druhé linie poskytuje lepší šanci na vyléčení a zabraňuje dalšímu šíření rezistence. Celosvětově je u dříve léčených prokázána MDR-TB až v 15 %, což je 5krát více než u nových případů. V případě již léčeného pacienta proto rozšiřujeme léčebný režim na iniciální 5kombinaci a 3kombinaci v pokračovacím režimu (tab. 4).
Tab. 4. Standardizované režimy pro dříve léčené pacienty s tuberkulózou. 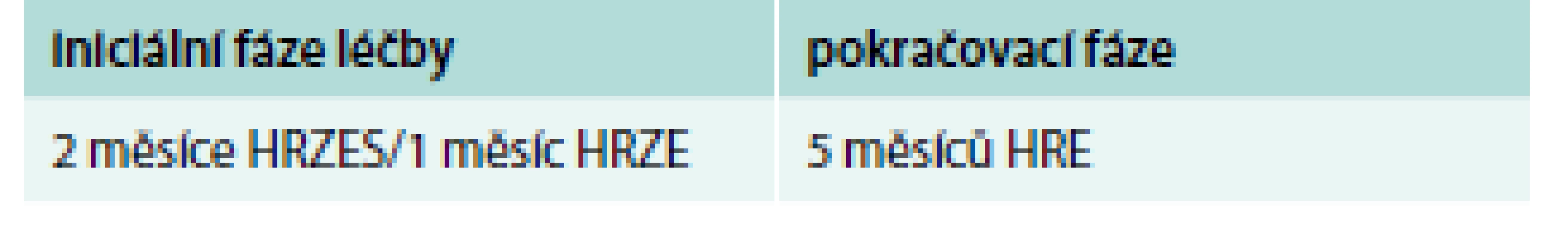
E – etambutol H – izoniazid R – rifampicin S – streptomycin Z – pyrazinamid Upraveno podle [9] Při již prokázané MDR-TB pak volíme speciální režimy léčby bez isoniazidu a rifampicinu s přidáním chinolonu, makrolidu a aminoglykosidu a následně pak upravujeme léčbu dle rozšířené citlivosti (tab. 5).
Tab. 5. Léky používané v terapii MDR-TB dle Světové zdravotnické organizace (antituberkulotika 2. linie). 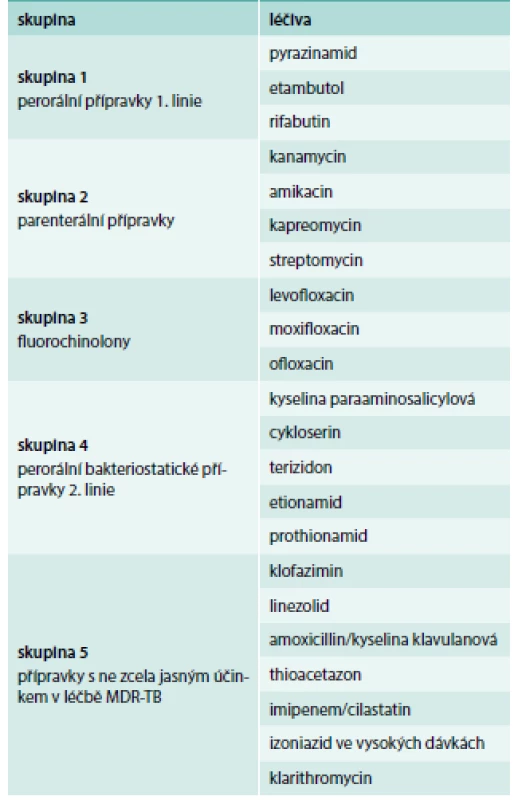
MDR-TB – multidrug-resistant tuberculosis/multirezistentní tuberkulóza Upraveno podle [9] Léčba MDR-TB trvá obvykle nejméně 2 roky, iniciální fáze je doporučována nejméně v 6měsíčním trvání a délka pokračovací fáze by měla probíhat nejméně 20 měsíců, každopádně pacient by měl být léčen ještě 20 měsíců od posledního pozitivního kultivačního nálezu. V některých případech je nutná kromě medikamentózní léčby i léčba chirurgická, která vede k odstranění perzistující kaverny, a to zvláště v případě, jde-li o extenzivně nebo totálně rezistentní mykobakterie [5–8].
Pro léčbu mimoplicní TB se používají stejné režimy jako pro plicní TB. Někteří odborníci však doporučují u tuberkulózní meningitidy kvůli riziku vážných následků léčbu režimy trvajícími 9–12 měsíců, u pacientů s TB kloubů a kostí je doporučován 9měsíční režim, a to kvůli obtížím při hodnocení léčebného efektu. Pokud není podezření na rezistenci, doporučuje se u tuberkulózní meningitidy a perikarditidy adjuvantní podávání kortikoidů. U tuberkulózní meningitidy má být použit streptomycin místo etambutolu.
Chirurgická léčba hraje v terapii mimoplicní TB jen malou roli a je používána při řešení pozdních komplikací nemoci, jako je hydrocefalus, obstrukce močových cest, konstriktivní perikarditida a neurologické postižení u Pottovy choroby (spinální TB).
Po dlouhých 40 letech byla pro TB schválena a registrována nová antituberkulotika – bedaquilin (přípravek schválen FDA v roce 2012) a delamanid (přípravek schválen EMA v roce 2013). Bedaquilin i delamanid by měly být účinné jak u citlivých, tak i u multirezistentních a u extenzivně rezistentních kmenů mykobakterií [9], v současné době však jsou rezervována jen pro MDR-TB. Jejich nevýhodou je časný vznik rezistence a extrémně vysoká cena.
Hlášení a prevence
Všechny nově zjištěné aktivní tuberkulózní nálezy plicní a mimoplicní lokalizace podléhají povinnému hlášení. Hlášení podává lékař (pracoviště), který zahajuje antituberkulózní léčbu, v případech zjištěných post mortem hlásí nález patolog ve spolupráci s územně příslušným ambulantním zařízením oboru pneumologie a ftizeologie. Za sběr dat a hlášení o nově zjištěných případech TB odpovídá pneumolog s úvazkem u krajské hygienické stanice, který je pro daný region určen krajským hygienikem. Jeden rok po podání povinného hlášení TB se podává kontrolní hlášení, podle kterého lze hodnotit průběh a výsledek léčby.
Mezi preventivní opatření do jisté míry zabraňující rozvoji TB patří BCG (Bacillus Calmette-Guérin) vakcinace novorozenců a léčba latentní tuberkulózní infekce u jedinců s rizikem rozvoje TB. V ČR je od 1. listopadu 2010 prováděna vakcinace pouze u rizikových novorozenců s cílem snížit riziko časného rozvoje TB u dětí v komunitách s vyšší prevalencí TB (vyhláška č. 299/2010 Sb. ze dne 25. 10. 2010). Dle Přílohy 3 této vyhlášky je novorozenec ohrožen zvýšeným rizikem nákazy TB v níže uvedených situacích:
- jeden nebo oba z rodičů dítěte nebo sourozenec dítěte nebo člen domácnosti, v níž dítě žije, má aktivní TB
- dítě nebo člen domácnosti se narodilo nebo souvisle pobývalo/pobývá v zemi s výskytem TB > 40/100 000 obyvatel
- dítě bylo v kontaktu s nemocným s TB
Indikace k očkování vyplývá z anamnestických údajů poskytnutých lékaři novorozeneckého oddělení nebo praktickému lékaři pro děti a dorost zákonnými zástupci dítěte. Pokud novorozenec splní kritéria rizikovosti pro vznik TB, je u něj BCG vakcinace řazena mezi povinná očkování [10]. Musíme si nicméně uvědomit, že stávající BCG vakcína není dostatečně účinná a bohužel ani bezpečná a v případě kontaktu vakcinovaného dítěte s TB dokonce chrání pouze v 65 %, což prokázala již studie prováděná v některých krajích ČR v 80. a 90. letech minulého století [11]. Navíc tato studie prokázala, že výskyt fatálních a závažných komplikací BCG vakcinace je vyšší než incidence TB v očkované populaci. Z tohoto důvodu je stále netrpělivě očekáván vývoj účinnější a bezpečnější vakcíny, na který jsou celosvětově vynakládány nemalé finanční prostředky [9].
U pacientů, kteří jsou vystaveni vyššímu riziku rozvoje TB, je indikován screening a případně léčba latentní tuberkulózní infekce. Jedná se o nemocné, kteří by měli podstoupit léčbu, při níž dochází k významnému oslabení imunity proti mykobakteriím, Jedná se především o léčbu zaměřenou proti tumor nekrotizujícímu faktoru α. Podstupují ji pacienti s některými revmatickými onemocněními a s idiopatickými střevními záněty. Nově se však ukazuje, že rovněž kandidáti na transplantaci kostní dřeně i solidních orgánů jsou po transplantaci ve významném riziku rozvoje TB. V ČR existují doporučení České pneumologické a ftiseologické společnosti pro diagnostiku a léčbu latentní tuberkulózní infekce u pacientů před biologickou léčbou i před transplantací solidních orgánů a krvetvorných buněk (www.pneumologie.cz).
V rámci globálních snah o zlepšení kontroly TB ve světě je nyní aktuální projekt Světové zdravotnické organizace End TB Strategie, přijatá Organizací spojených národů v září roku 2015 a časově pokrývající období let 2016–2035. Vyhlášení si klade za cíl redukovat úmrtí na TB ve světě o 90 % a o 80 % snížit incidenci TB dokonce roku 2030. Cílem je celosvětově snížit incidenci TB ≤ 10/100 000 obyvatel, čili na úroveň států s nízkou náloží TB.
Závěr
Příznivá situace v oblasti výskytu TB v České republice je důkazem dobré funkce a koordinace jednotlivých složek účastnících se kontroly tohoto celosvětově epidemiologicky závažného onemocnění. Objev nových léků a případně nové vakcíny proti TB spolu s finančními a hmotnými prostředky určenými pro systematické vyhledávání nemocných TB a jejich léčbu v zemích rozvojového světa snad umožní postupné snížení incidence TB celosvětově, i když o její úplné eradikaci zatím můžeme stěží snít.
prof. MUDr. Martina Vašáková, Ph.D.
martina.vasakova@ftn.cz
Pneumologická klinika 1. LF UK a Thomayerovy nemocnice,
Praha
www.ftn.cz
Doručeno do redakce 21. 8. 2017
Přijato po recenzi 26. 9. 2017
Zdroje
1. Hershkovitz I, Donoghue HD, Minnikin DE et al. Tuberculosis origin: The Neolitic scenario. Tuberculosis (Edinb) 2015; 95(Suppl 1): S122-S126. Dostupné z DOI: <http://dx.doi.org/10.1016/j.tube.2015.02.021.>.
2. Zatloukal P, Kos S. Tuberkulóza. In: Kolek V et al. Doporučené postupy v pneumologii. Maxdorf: Praha 2013 : 141–163. ISBN 978–80–7345–359–6.
3. Global tuberculosis report 2016. ISBN 9789241565394. Dostupné z WWW: <http://apps.who.int/iris/bitstream/10665/250441/1/9789241565394-eng.pdf?ua=1>. [17.8.2017].
4. Kolek V, Kašák V, Vašáková M et al. Pneumologie. 2.ed. Maxdorf: Praha 2014. ISBN 978–80–7345–387–9.
5. Kolek V et al. Doporučené postupy v pneumologii. Maxdorf: Praha 2013. ISBN 978–80–7345–359–6.
6. Horsburgh CR, Barry CE, Lange C. Treatment of tuberculosis. N Engl J Med 2015; 373(22): 2149–2160. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMra1413919>.
7. Treatment of tuberculosis guidelines. 4th ed. Geneva: World Health Organization (WHO) 2010. ISBN 978 92 4 154783 3. Dostupné z WWW: <http://apps.who.int/iris/bitstream/10665/44165/1/9789241547833_eng.pdf>.
8. Yew WW, Lange C, Leung CC. Treatment of tuberculosis: update 2010. Eur Resp J 2011; 37(2): 441–462. Dostupné z DOI: <http://dx.doi.org/10.1183/09031936.00033010>.
9. Vašáková M et al. Moderní farmakoterapie v pneumologii. Maxdorf: Praha 2013. ISBN 978–80–7345–351–0.
10. Vašáková M. BCG vakcinace v České republice v podmínkách nové vyhlášky 299/2010 Sb., ze dne 25. 10. 2010. Stud Pneumol Phtiseol 2011; 71(1): 28–30.
11. Daňková D, Trnka L, Švandová E. Projekt přerušení BCG vakcinace novorozenců na vybraném území České republiky. Souhrnná zpráva za roky 1986–1993. Stud Pneumol Phtiseol 1995(4); 55 : 281–292.
12. Homolka J. Biologická léčba preparáty blokujícími účinek TNF alfa. In: Kolek V et al. Doporučené postupy v pneumologii. Maxdorf: Praha 2013 : 167–170. ISBN 978–80–7345–359–6.
13. Polcová V, Vašáková M, Valentová Bartáková L. Tuberkulóza a latentní tuberkulózní infekce u transplantací. In: Kolek V et al. Doporučené postupy v pneumologii. Maxdorf: Praha 2013 : 170–176. ISBN 978–80–7345–359–6.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Současná náplň pneumologieČlánek Nozokomiální pneumonieČlánek Cystická fibróza dospělýchČlánek Nemalobuněčný karcinom plicČlánek Neinvazivní ventilace
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2017 Číslo 11- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Současná náplň pneumologie
- Cílené vyhledávání nemocných s chronickou obstrukční plicní nemocí: stručný přehled
- Diagnostika a léčba komunitní pneumonie – v jednoduchosti je klíč k úspěchu
- Nozokomiální pneumonie
- Pneumonie u imunokompromitovaných
- Idiopatická plicní fibróza. Umíme ji vždy správně diagnostikovat a léčit?
- Exogenní alergické alveolitidy: minimum pro praxi
- Sarkoidóza – nadále záhadné onemocnění
- Současný přístup k diagnostice, léčbě a prevenci tuberkulózy
-
Non-CF bronchiektázie dospělých: stručný přehled pro praxi
Dokument Sekce chorob s bronchiální obstrukcí České pneumologické a ftizeologické společnosti České lékařské společnosti J. E. Purkyně - Cystická fibróza dospělých
- Kardiovaskulární riziko spánkové apnoe a kazuistika
- Komplikace po transplantaci plic
- Nemalobuněčný karcinom plic
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
- Maligní mezoteliom pleury – dosud nepokořený nádor
- Spirometrie – základní vyšetření funkce plic
- Postavení bronchologie v pneumologické diagnostice
- Ultrasonografické vyšetření hrudníku v rukou lékaře klinika
- Neinvazivní ventilace
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Spirometrie – základní vyšetření funkce plic
- Neinvazivní ventilace
- Pneumonie u imunokompromitovaných
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



