-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Pancytopenie, panhypopituitarizmus a jaterní cirhóza: rozbor složité kazuistiky
Pancytopenia, panhypopituitarism and liver cirrhosis: analysis of a difficult clinical case
Panhypopituitarism following craniopharyngioma resection has systemic impact with potential influence on physiological hematopoiesis. There is a growing body of evidence of liver fibrosis/cirrhosis risk development due to altered metabolism and lipid accumulation. The authors present a case report of a woman with a history of craniopharyngioma resection followed by aggravating pancytopenia with suspected indolent lymphoproliferative disorder and possible acquired bone marrow aplasia syndrome due to paroxysmal nocturnal hemoglobinuria. A complex hemostasis disorder with deficiency of multiple coagulation factors (FXII, FXI, FX, FIX, FVII, FX, FV, FXIII, antitrombin, protein C, protein S) was accidentally detected. Despite normal sonographic liver imaging, all possible causes of chronic liver disease were systematically excluded (viral hepatitis, hemochromatosis, Wilson´s disease, α-1-antitrypsin deficiency); anti-LKM-1 and anti-ENA antibodies were detected. Finally, the magnetic resonance imaging confirmed image of liver cirrhosis – with signs of portal hypertension.
Keywords:
coagulopathy – liver cirrhosis – pancytopenia – panhypopituitarism
Autori: Pavel Polák 1,2; Jan Kamelander 1; Jana Michalcová 1,2; Jiřina Zavřelová 1,3; Libor Červinek 4; Tomáš Rohan 5; Zuzana Pazdičová 5; Václav Odstrčilík 6; Miroslav Penka 1,2,3
Pôsobisko autorov: Oddělení klinické hematologie FN Brno, pracoviště Bohunice 1; LF MU, Brno 2; Katedra laboratorních metod LF MU, Brno 3; Interní hematologická a onkologická klinika LF MU a FN Brno, pracoviště Bohunice 4; Klinika radiologie a nukleární medicíny LF MU a FN Brno, pracoviště Bohunice 5; Klinika ústní, čelistní a obličejové chirurgie LF MU a FN Brno, pracoviště Bohunice 6
Vyšlo v časopise: Vnitř Lék 2019; 65(11): 715-720
Kategória: Kazuistiky
Súhrn
Panhypopituitarizmus po resekci kraniofaryngeomu má systémové důsledky s potenciálním dopadem na fyziologickou hematopoézu. Současně přibývá důkazů o riziku rozvoje jaterní fibrózy až cirhózy v důsledku akumulace lipidů při alterovaném metabolizmu. Autoři předkládají kazuistiku ženy po resekci kraniofaryngeomu dispenzarizované pro progredující pancytopenii, u níž bylo podezření na indolentní lymfoproliferativní onemocnění s možným podílem syndromu získaného selhání kostní dřeně při paroxyzmální noční hemoglobinurii. U pacientky byla náhodně zjištěna komplexní porucha hemostázy s deficitem četných koagulačních faktorů (FXII, FXI, FX, FIX, FVII, FX, FV, FXIII, antitrombin, protein C, protein S). Navzdory normálnímu sonografickému obrazu jater byla cíleně vylučována veškerá možná chronická jaterní onemocnění (virové hepatitidy, hemochromatóza, Wilsonova choroba, deficit α-1-antitrypsinu); byly prokázány protilátky anti-LKM1 a antiENA. Teprve magnetická rezonance definitivně potvrdila obraz jaterní cirhózy – již se známkami portální hypertenze.
Klíčová slova:
jaterní cirhóza – koagulopatie – pancytopenie – panhypopituitarizmus
Úvod
Komplexní porucha hemostázy tvoří integrální součást projevů pokročilého onemocnění jater a její řešení patří ke každodenní náplni práce hematologa s hemostazeologickým zaměřením. Autoři předkládají kazuistiku pacientky s náhodně zjištěnou komplexní koagulopatií, jejíž složitý diferenciálně-diagnostický rozbor vedl ke stanovení diagnózy jaterní cirhózy.
Popis případu
V lednu roku 2019 přišla na Kliniku ústní, čelistní a obličejové chirurgie LF MU a FN Brno, pracoviště Bohunice, 24letá žena k elektivní extrakci retinovaných zubních radixů působících opakované lokální záněty. Vzhledem k těžké trombocytopenii (28 × 109/l) a prodloužení protrombinového času (PT 1,39 R), aktivovaného parciálního tromboplastinového času (aPTT 1,62 R) a trombinového času (26,2 s) byl konzultován hematolog k doporučení předintervenční přípravy. Současně byl zjištěn středně těžký deficit antitrombinu (42 %) při normální koncentraci fibrinogenu (2,54 g/l). V krevním obraze byla zjištěna i leukocytopenie 2. stupně a anémie 1. stupně. Pacientka měla vietnamské předky, narodila se však v České republice, kterou nikdy ve svém životě neopustila. U rodičů se nevyskytlo onemocnění krve, porucha krevního srážení, podle nepřímé anamnézy získané od probandky neprodělali ani infekční hepatitidu. V 7 letech věku (roku 2002) byl pacientce diagnostikován kraniofaryngeom, který byl několikrát resekován a ozářen – důsledkem byl rozvoj kompletního panhypopituitarizmu a bilaterální hemianopsie. Byla zavedena dlouhodobá hormonální substituce adiuretinem, hydrokortizonem a tyreotropinem, v minulosti přechodně užívala i somatotropin, jehož substituce však byla při minimální odezvě vzestupu inzulinu podobného růstového faktoru 1 (Inzulin-like Growth Factor 1 – IGF1) hodnocena jako neefektivní, a proto byla přerušena. Stravu udávala bez omezení, alkohol nepila vůbec, pravidelně exponována toxickým látkám nebyla. S výjimkou bledšího koloritu pokožky byl fyzikální nález bez pozoruhodností, aktuální hmotnost byla 72,8 kg a tělesná výška 168 cm. V roce 2009 byla opakovaně konzultována hematology pro recidivující těžkou epistaxi a silnější krvácení po poranění, v krevním obraze byla poprvé zaznamenána mírná pancytopenie, v koagulogramu byl mírně prodloužený aPTT (1,34 R), tab. 1. Při podrobnějším došetření byl přechodně dokumentován lehký až středně těžký kvantitativní deficit von Willebrandova faktoru (10–37 %), který se však v dalším průběhu spontánně upravil; v té době nebyl prokázán kvantitativní deficit jiných koagulačních faktorů (FVIII, FXI, FIX, FXII). Od roku 2014 probíhala další dispenzární péče na Interní hematologické a onkologické klinice LF MU a FN Brno, pracoviště Bohunice. V říjnu roku 2014 byl prokázán velmi malý klon paroxyzmální noční hemoglobinurie (PNH) na monocytech – 0,3 %, který při kontrolách nejevil známky expanze. V rámci šetření pancytopenie bylo v březnu roku 2017 provedeno vyšetření hrudníku a dutiny břišní výpočetní tomografií (Computed Tomography – CT), která zobrazila vícečetné lymfatické uzliny v mediastinu i v retroperitoneu mírně nadhraniční velikosti, několik nespecifických nodularit v plicním parenchymu, splenomegalii (16,3 × 9,3 × 15,0 cm), s normálním obrazem jater a portálního řečiště. I proto bylo v dubnu roku 2017 doplněno histologické vyšetření kostní dřeně, které však nepotvrdilo podezření na lymfoproliferativní onemocnění, byl přítomen 10–20% infiltrát polyklonálních T-lymfocytů. V té době již byla přítomna těžká trombocytopenie a bylo dokumentováno postupné prodlužování PT-R i aPTT-R. V průběhu let byla opakovaně zaznamenána kolísavá a jen mírně zvýšená aktivita aminotransferáz při zachovalé konjugační schopnosti bilirubinu, postupně se však zvyšovala aktivita laktátdehydrogenázy v séru, což potencovalo podezření na indolentní lymfoproliferativní onemocnění – další došetření pacientka v té době odmítla. Vývoj základních laboratorních parametrů v čase uvádí tab. 1. Pro doporučení přípravy na aktuálně zamýšlené extrakce zubních kořenů bylo doplněno vyšetření rotačním tromboelastometrem (ROTEM), které prokázalo pomalejší aktivaci hemostázy (redukce α úhlu) a sníženou pevnost koagula. Stomatologický výkon byl proveden s maximální možnou šetrností po předchozí nitrožilní aplikaci 10 mg vitaminu K, dvou transfúzních jednotek čerstvě zmražené plazmy, etamsylátu (Dicynone®) a kyseliny tranexamové (Exacyl®) při současné důsledné lokální hemostáze a sutuře resorbovatelným materiálem. Období během a po výkonu nebylo zatíženo aktivními krvácivými projevy s výjimkou větších plošných bukálních hematomů. Současně bylo zahájeno extenzivní pátrání po příčině prodloužení PT-R, aPTT-R i trombinového času s nálezem různě závažného deficitu četných bílkovin koagulační kaskády (tab. 2). Naopak nebyl prokázán kvantitativní deficit von Willebrandova faktoru, FVIII ani fibrinogenu. V rámci diferenciální diagnostiky aPTT bylo doplněno i vyšetření antifosfolipidových protilátek (lupus anticoagulans, protilátky proti β2-glykoproteinu 1 a protilátky proti kardiolipinu), u kterých byl zjištěn pouze hraniční titr protilátek proti kardiolipinu ve třídě IgG. Pomýšleno bylo i na případnou přítomnost protilátek s inhibičním působením jednotlivých koagulačních faktorů (tzv. inhibitorů), nicméně vyšetření cirkulujícího antikoagulans na bázi aPTT bylo negativní. Naopak byla prokázána polyklonální hypergamaglobulinemie se zvýšenou koncentrací volných lehkých řetězců κ (49,72 mg/l, norma do 19,4 mg/l) i λ (120,28 mg/l, norma do 26,3 mg/l), avšak s fyziologickým poměrem 0,41 (norma 0,26–1,65). Ve spektru bílkovin byla zachycena mírná hypoalbuminemie (32,7 g/l) a těžká hypoprealbuminemie (0,07 g/l). Nápadná byla i mírná hypoglykemie 3,7 mmol/l. Testy k odhalení případné hemolýzy byly nejednoznačné (volný hemoglobin v normě 38,7 mg/l, snížený haptoglobin na 0,03 g/l, mírně zvýšená aktivita laktátdehydrogenázy v séru na 4,93 µkat/l), počet schistocytů opakovaně 3–4/1 000 buněk (norma do 3/1 000 buněk), v moči nebyl prokázán hemosiderin. Komplex deficitu naprosté většiny hemostaticky účinných faktorů, hypoalbuminemie, hypoprealbuminemie i hypohaptoglobinemie a hypoglykemie nutily pomýšlet především na porušenou funkci jater, pro což nepřímo svědčila i mírně snížená aktivita cholinesterázy (69 µkat/l). Cíleně byly vyloučeny virové hepatitidy A, B, C i E, nákaza virem lidské imunitní nedostatečnosti (Human Immunodeficiency Virus – HIV), deficit ceruloplazminu i α1-antitrypsinu. Nebyla prokázána hyperferitinemie, která by svědčila pro možnou hemochromatózu. Koncentrace α fetoproteinu byla rovněž v normě (2,55 kU/l). Proběhla i sonografická kontrola dutiny břišní – játra byla přiměřené echogenity i velikosti, přítomna byla splenomegalie (16,0 × 6,5 cm), avšak rychlost průtoku krve portálním řečištěm byla fyziologická, v retroperitoneu byla zachycena solitární lymfatická uzlina hraniční velikosti 13 mm. Byly však prokázány protilátky antiLKM1 ve třídě IgG (28,96 RU/ml, norma do 19,9 RU/ml; antiLKM v titru 1 : 10 byly negativní) a protilátky proti extrahovatelnému nukleárnímu antigenu (antiENA, index 2,0, norma do 0,99). Naopak revmatoidní faktor, protilátky proti cirkulujícím citrulinovým peptidům (antiCCP), antimitochondriální protilátky (antiAMA), protilátky proti hladké svalovině (antiASMA), antinukleární protilátky (ANA) a protilátky proti cytoplazmě neutrofilů (ANCA) byly negativní. Dále byla zjištěna klinicky asymptomatická kryoglobulinemie (blíže dosud neurčeno) a deficit faktorů komplementu C3 (0,48 g/l, norma 0,-91,8 g/l) a C4 (0,08 g/l, norma 0,1–0,4 g/l). Nebyl prokázán deficit vitaminů nezbytných pro adekvátní hematopoézu (vitamin B12, folát); zjištěna byla zvýšená aktivita erytropoetinu v séru 37,8 U/l. Lipidogram byl kompletně v normě (celkový cholesterol 3,2 mmol/l, triglyceridy 0,93 mmol/l, LDL-cholesterol 1,2 mmol/l, HDL-cholesterol 1,5 mmol/l); glykosylovaný hemoglobin vyšetřen nebyl. Cíleně bylo provedeno kontrolní flowcytometrické vyšetření k vyloučení klonu paroxyzmální noční hemoglobinurie s negativním výsledkem. Flowcytometrie periferní krve rovněž neprokázala případnou klonální populaci lymfocytů. Navzdory absenci známek chronického postižení jater recentním sonografickým vyšetřením bylo na základě zjištěných abnormalit doplněno vyšetření jater magnetickou rezonancí s nálezem nepravidelně konturovaných jater s poklesem signálu vlivem podílu tuku se známkami portální hypertenze s varikozitami ve stěně kardie žaludku a se splenomegalií (17,5 × 7,5 cm); navíc byly popsány četné lymfatické uzliny v povodí v. portae velikosti až 12 mm, v retroperitoneu lymfadenopatie zjištěna nebyla, zobrazení žlučovodů bylo fyziologické. Doplněné fibroelastografické vyšetření prokázalo obraz hepatopatie charakteru fibrózy/cirhózy s neostrými konturami jater a s hrubozrnným parenchymem, bez možnosti přesného elastografického vyhodnocení. Invazivní vyšetření (kontrolní vyšetření kostní dřeně, biopsie jater) nebyla v této fázi provedena pro výrazná rizika krvácivých komplikací. Pacientka byla předána do další specializované a komplexní hepatologické péče.
Tab. 1. Vývoj hlavních laboratorních parametrů v čase 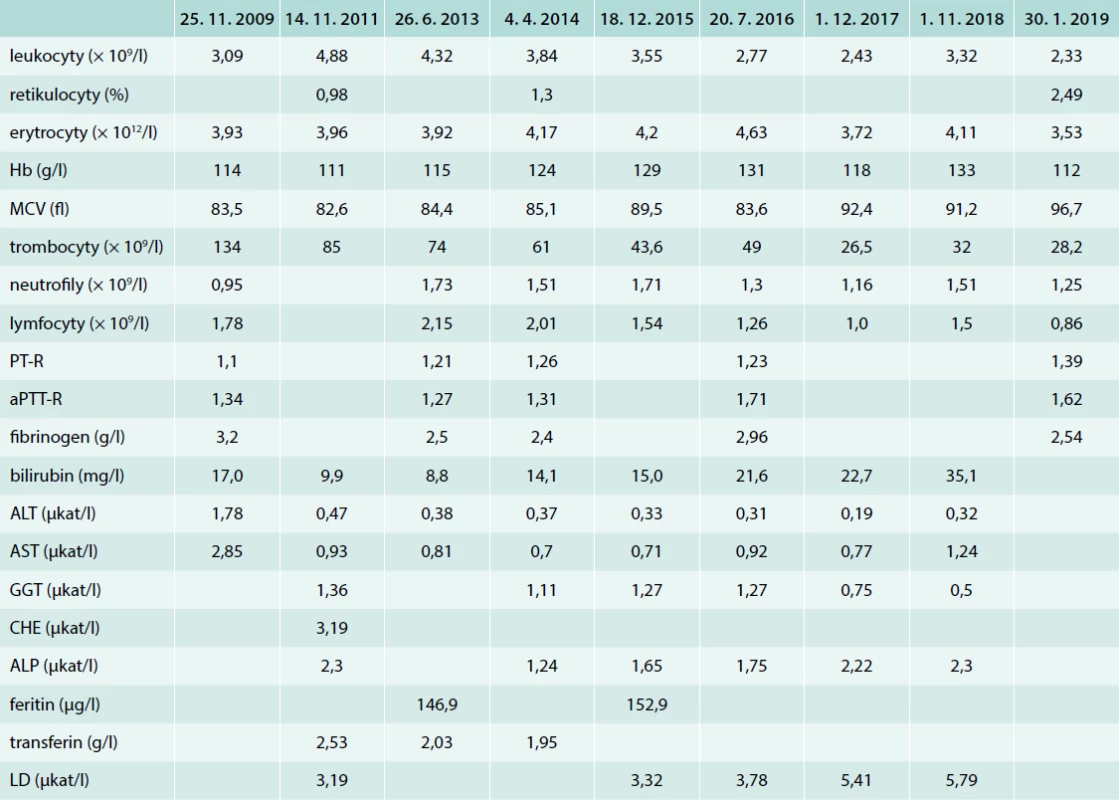
ALP – alkalická fosfatáza ALT – alaninaminotransferáza aPTT-R – aktivovaný parciální tromboplastinový čas-ratio AST – aspartátaminotransferáza CHE – cholinesteráza GGT – gamaglutamyltransferáza LD – laktátdehydrogenáza MCV – střední objem erytrocytu/Mean Cell Volume PT-R – protrombinový čas-ratio Tab. 2. Aktivita/koncentrace jednotlivých bílkovin účastnících se hemostázy (koagulačních faktorů) 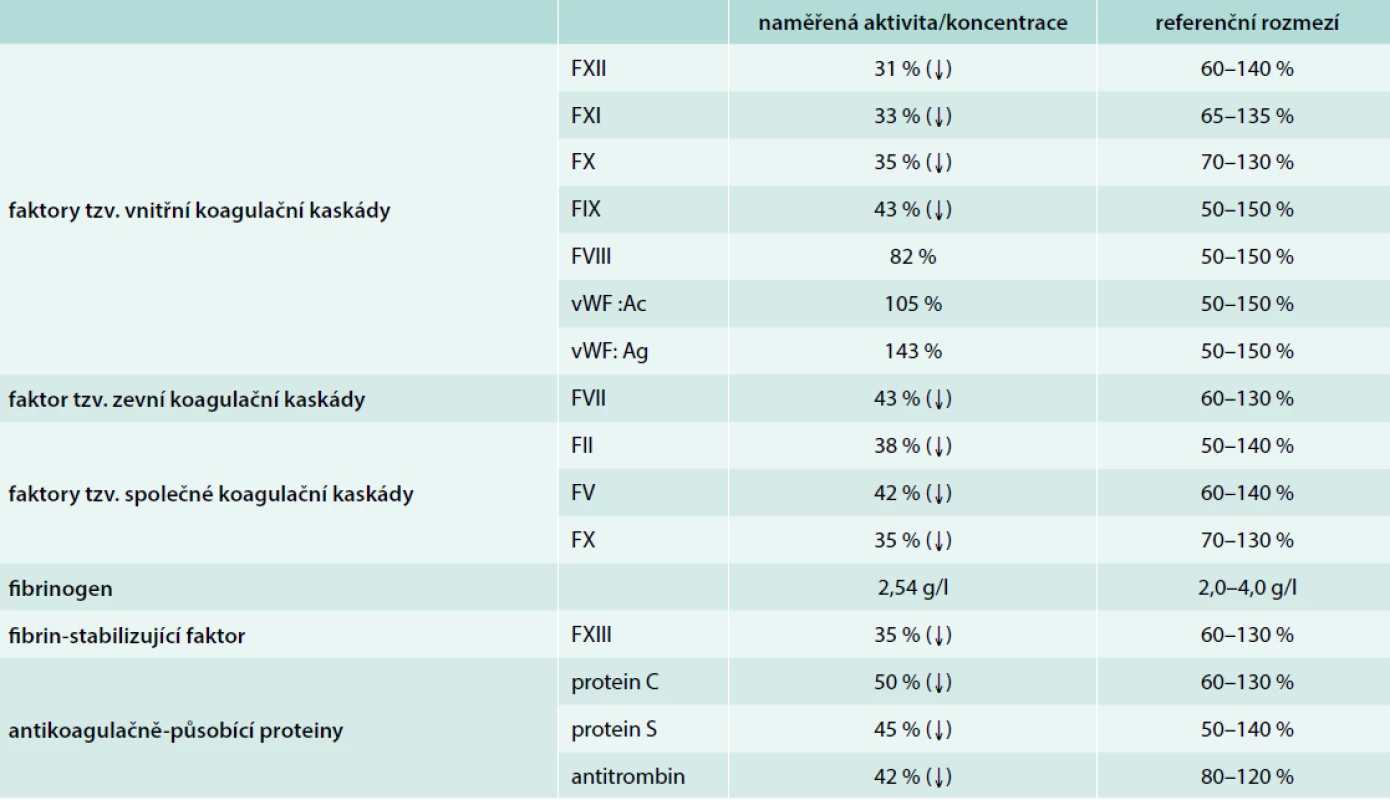
vWF: Ac – aktivita von Willebrandova faktoru vWF: Ag – antigen von Willebrandova faktoru Diskuse
Předkládaná kazuistika v sobě zahrnuje více prolínajících se složitých souvislostí. Prakticky prvním hematologickým příznakem byla klinicky nevýznamná pancytopenie poprvé zjištěná v listopadu roku 2009. Podobné odchylky však nejsou u pacientů s panhypopituitarizmem – a to i navzdory adekvátní substituční terapii – žádnou výjimkou a v některých případech mohou být dokonce prvním projevem závažné endokrinní dysbalance [1–3]. Vzácně byly též popsány případy postupného selhání kostní dřeně v důsledku fibrotizace v souvislosti s kraniofaryngeomem – tzv. fibrodysplasia ossificans progressiva [4]. Ani tuto raritní nozologickou jednotku nebylo možno zpočátku spolehlivě vyloučit: pokročilá fibrotizace kostní dřeně se zpravidla projevuje rozvojem extramedulární hematopoézy vedoucí typicky k hepato/splenomegalii, někdy však i k lymfadenopatii či k postižení jakékoli jiné orgánové soustavy. U pacientů trpících tímto syndromem bývají popisovány anomálie skeletu zápěstních a zánártních kůstek, což se u probandky radiologicky neprokázalo a během rozšiřování spektra jednotlivých patologických nálezů u prezentované pacientky se tato možnost stávala stále méně pravděpodobnou.
Postupně progredující trombocytopenie vedla od roku 2009 k hlubšímu pátrání po možných příčinách, přitom byla poprvé zjištěna splenomegalie, retroperitoneální lymfadenopatie a zvýšená aktivita laktátdehydrogenázy. Z těchto důvodů bylo cíleně vylučováno lymfoproliferativní onemocnění – histologické a flowcytometrické vyšetření kostní dřeně provedené v roce 2014 nevedlo ke stanovení jasné hematoonkologické diagnózy, avšak nezvyklý nález zmnožení polyklonálních T-lymfocytů stále znamenal reálné riziko klonální selekce a rozvoj indolentního lymfomu. Nicméně ani v této chvíli nebyly klinické projevy charakteristické, neboť lymfomy vycházející z T-lymfocytů mívají zpravidla agresivní průběh se systémovými projevy a s mediánem přežití několika málo měsíců [5]. Pacientka se navíc k možnosti opakovaného vyšetření kostní dřeně stavěla negativně. Retrospektivně se jako pravděpodobná jeví i snížená syntéza trombopoetinu v hepatocytech jako jeden z etiologických faktorů trombocytopenie.
Pomýšleno bylo i na vzácné a ve svých projevech pleiomorfní onemocnění – paroxyzmální noční hemoglobinurii (PNH). Mezi hlavní projevy PNH patří různě závažná hemolytická anémie, případně i trombocytopenie a leukocytopenie a různě závažná konzumpční koagulopatie, pravidlem bývá deficit složek komplementu vlivem jejich setrvalé degradace; někdy PNH doprovází i T-lymfoproliferativní onemocnění. Je dobře dokumentována skutečnost, že PNH se nezřídka vyvíjí z aplastické anémie (AA) anebo naopak do AA v průběhu času přechází, onemocnění však může i spontánně vymizet [6–8]. V popsaném případě byl jednou zjištěn zcela minoritní klon PNH na monocytech (0,3 %), což však samo o sobě nebylo dostatečným důvodem k zahájení ev. terapie, a proto nezbylo než i v tomto ohledu zvolit strategii důsledného sledování dalšího vývoje nemoci. Kontrolní flowcytometrické vyšetření periferní krve počátkem roku 2019 – tedy v době již těžké trombocytopenie – neprokázalo ani takto reziduální klon PNH, nebyly přítomny přesvědčivé známky probíhající hemolýzy a nebyla naplněna ani kritéria pro aplastickou anémii.
Během hemolytických epizod bývá typicky signifikantně zvýšen počet schistocytů v periferní krvi, současně bývá výrazně zvýšená aktivita laktátdehydrogenázy, zvýšená koncentrace volného hemoglobinu a snížená koncentrace haptoglobinu v séru. Mírná forma intravaskulární hemolýzy byla popsána i u pokročilé malnutrice, při níž bývá důsledkem nestability erytrocytární membrány při změněném kvantitativním i kvalitativním zastoupení jednotlivých bílkovinných i lipidových složek. Těžká malnutrice může současně vést k tzv. gelatinózní přestavbě kostní dřeně projevující se pancytopenií a extramedulární hematopoézou (při dobře vedené realimentaci mohou být tyto změny i plně reverzibilní) [9]. Zvýšená aktivita laktátdehydrogenázy vede hematologa vždy v první řadě k pomýšlení na nádorové onemocnění, není však zdaleka specifická a doprovází i chronická onemocnění jater či hemolytická onemocnění. Haptoglobin je bílkovina syntetizovaná hepatocyty – zjištěný deficit tedy může znamenat i primární poruchu na úrovni jaterní buňky. Při hodnocení markerů hemolýzy je třeba vždy vyloučit i případnou preanalytickou chybu ve smyslu dlouhého intervalu mezi odběrem krve a doručením do laboratoře, či nešetrné zacházení se vzorky během transportu. V daném případě není bez zajímavosti, že při chronické hemolýze bývá i deficit proteinu C a proteinu S [10]. Těžkou malnutrici mohou mimo výše uvedených možných poruch hematopoézy doprovázet i výrazné poruchy hemostázy – zpravidla bývá různě těžký deficit koagulačních faktorů, jejichž syntéza je dependentní na vitaminu K (FII, FV, FVII, FIX, FX, protein C, protein S) s následným prodloužením PT-R i aPTT-R, při další progresi malnutrice se odchylky od normy akcentují prakticky na všech úrovních [10]. U popisované pacientky byl nález těžké hypoprealbuminemie (laboratorní korelát proteino-energetické malnutrice) spíše překvapivý, protože habitem byla pacientka normostenička nevykazující známky jednoznačné sarkopenie. Navíc nebyla zaznamenána prakticky žádná změna PT-R a aPTT-R v odstupu po intravenózní aplikaci 10 mg vitaminu K. V některých případech těžkého deficitu vitaminu K je však k docílení korekce základních koagulačních časů nutná dlouhodobá pravidelná substituční terapie vitaminem K [10]. Pomýšleno bylo i na chronickou formu diseminované intravaskulární koagulopatie (DIC), tato možnost se při komplexním hodnocení veškerých nálezů jevila jako nepravděpodobná. Normální aktivitu von Willebrandova faktoru lze v daném případě vysvětlit jeho syntézou v endotelu cév, naopak fyziologická koncentrace fibrinogenu je v daném terénu spíše překvapivá. Vyšetření C3 a C4 složek komplementu prokázalo jejich deficit – pravděpodobně při chronické konzumpci. Deficit těchto proteinů bývá u PNH, systémového lupus erythematodes, u membranoproliferativní glomerulonefritidy, u osteomyelitidy a u kryoglobulinemie [10]. Pacientka neměla klinické ani další laboratorní projevy systémového lupusu, chronické glomerulonefritidy či osteomyelitidy, proto bylo ještě doplněno screeningové vyšetření kryoglobulinů – s pozitivním výsledkem. Význam tohoto nálezu v tomto případě bude ještě třeba stanovit.
Vzhledem k vietnamským kořenům pacientky bylo nutno pomýšlet i na případnou vrozenou hemoglobinopatii (talasemii), klinicky relevantní forma tohoto onemocnění je však při normálním MCV a MCH prakticky vyloučena [10].
Zvýšená koncentrace erytropoetinu korelovala s chronickou anémií, přesto byla nápadná diskrepance tohoto laboratorního nálezu a normálního (oproti očekávání nikoli zvýšeného) počtu retikulocytů v periferní krvi. Tento fakt nepřímo svědčil pro primární poruchu erytropoézy v kostní dřeni. Laboratorní stanovení erytropoetinu, adrenokortikotropního hormonu, tyreotropinu, některých dalších hormonů hypofýzy, ale i četných koagulačních faktorů může být navíc ovlivněno hypergamaglobulinemií (ať již monoklonální či polyklonální) – v případě erytropoetinu mohou být naměřené koncentrace falešně vyšší. Jiné možné příčiny zvýšené koncentrace erytropoetinu v séru typu nádoru mozečku či von Hippel-Lindauovy choroby byly prakticky vyloučeny [10]. Téměř s jistotou lze v souvislosti s hypergamaglobulinemií vyloučit ovlivnění výsledku měření koncentrace antitrombinu a fibrinogenu. K vyloučení interference se stanovením aktivity protrombinu (FII) byla porovnána hodnota původní a hodnota ve vysoce naředěném vzorku, mezi nimiž nebyl významný rozdíl. Test cirkulujícího antikoagulans na bazi aPTT pro tuto interferenci rovněž nesvědčil.
Polyklonální hypergamaglobulinemie se zpravidla vyskytuje u onemocnění s chronicky stimulovaným imunitním systémem: může se jednat o chronické parazitární či protozoární infekce typu malárie, leishmaniózy či schistosomiázy, o autoimunitní onemocnění, jako je systémový lupus erythematodes (SLE), revmatoidní artritida (RA) či Sjögrenův syndrom (SS) anebo o Castlemanovu chorobu, bývá však i u chronických onemocnění jater [10,11]. Výše uvedené nákazy nepřicházely u probandky prakticky v úvahu, protože v životě neopustila středoevropský region. Pro SLE, RA ani SS neměla pacientka klinické projevy, nebyl prokázán ani revmatoidní faktor (bývá typicky přítomen u SS) či protilátky proti cyklickému citrulinovanému peptidu. Teoreticky byla zvažována možnost multicentrické Castlemanovy choroby, k definitivnímu potvrzení této diagnózy by bylo třeba histologické vyšetření lymfatické uzliny, což by představovalo neúměrné zatížení a riziko pro pacientku. Proti této možnosti svědčila absence klinických známek systémové imunitní hyperreaktivity [10].
V literatuře se vyskytují údaje o různě pokročilé hepatocelulární insuficienci v důsledku nealkoholického ztukovatění jater (Non-Alcoholic Fatty Liver Disease – NAFLD) u pacientů léčených pro kraniofaryngeom. Jako hlavní etiologický faktor jsou udávány systémová endokrinní dysregulace, deficit somatotropinu a tzv. hypotalamická obezita [12]. Jung provedl retrospektivní studii 75 pacientů operovaných pro kraniofaryngeom v dětství, u 47 % z nich byla vysoká pravděpodobnost přítomnosti NAFLD, jednoznačně diagnostikováno bylo toto onemocnění u 22 jedinců (u 6 z nich během 1. roku od operace). Autoři doporučují pomýšlet na NAFLD v případě zvýšené aktivity aminotransferáz > 40 U/l, což odpovídá 0,68 µkat/l – tuto hranici překračovala aktivita aspartátaminotransferázy v popsaném případě prakticky setrvale od roku 2009. I po úspěšné transplantaci jater však může NAFLD během několika málo let recidivovat, což je stav zatížený vysokou mortalitou [13]. Současně byly u pacientky zjištěny protilátky antiLKM1 a antiENA, a proto bude ještě nutno cíleně vyloučit i případný podíl autoimunitní hepatitidy na hepatocelulární insuficienci (dle aktuálně platného skóre pro diagnostiku autoimunitní hepatitidy spadá pacientka do kategorie „pravděpodobné autoimunitní hepatitidy“) [14].
Závěr
Etiologie jaterní cirhózy v popsané kazuistice není ještě plně dořešena, může se jednat o kombinaci NAFLD a autoimunitní hepatitidy. Kazuistika však demonstruje, že na chronické jaterní onemocnění je za jistých okolností třeba pomýšlet i v případě pouze hraničně zvýšené aktivity jaterních enzymů a normálního konvenčního sonografického zobrazení jater – v tomto případě byla hlavním vodítkem komplexní porucha hemostázy.
Doručeno do redakce 22. 5. 2019
Přijato po recenzi 9. 9. 2019
MUDr. Pavel Polák, Ph.D.
Oddělení klinické hematologie FN Brno, pracoviště Bohunice
Zdroje
- Kim DY, Kim JH, Park YJ et al. Case of complete recovery of pancytopenia after treatment of hypopituitarism. Ann Hematol 2004; 83(5): 309–312. Dostupné z DOI: <http://dx.doi.org/10.1007/s00277–003–0800–4>.
- Holmes GI, Shepherd P, Walker JD. Panhypopituitarism secondary to a macroprolactinoma manifesting with pancytopenia: case report and literature review. Endocr Pract 2011; 17(2): e32-e36. Dostupné z DOI: <http://dx.doi.org/10.4158/EP10298.CR>.
- Lang D, Mead JS, Sykes DB. Hormones and the bone marrow: panhypopituitarism and pancytopenia in a man with a pituitary adenoma. J Gen Intern Med 2015; 30(5): 692–696. Dostupné z DOI: <http://dx.doi.org/10.1007/s11606–014–3161-x>.
- Hüning I, Gillessen-Kaesbach G. Fibrodysplasia ossificans progressiva: clinical course, genetic mutations and genotype-phenotype correlation. Mol Syndromol 2014; 5(5): 201–211. Dostupné z DOI: <http://dx.doi.org/10.1159/000365770>.
- Licata MJ, Janakiram M, Tan S et al. Diagnostic challenges of adult T-cell leukemia/lymphoma in North America – a clinical, histological, and immunophenotypic correlation with a workflow proposal. Leuk Lymphoma 2018; 59(5): 1188–1194. Dostupné z DOI: <http://dx.doi.org/10.1080/10428194.2017.1365862>.
- Sahin F, Ozkan MC, Mete NG et al. Multidisciplinary clinical management of paroxysmal nocturnal hemoglobinuria. Am J Blood Res 2015; 5(1): 1–9.
- Boyer T, Grardel N, Copin MC et al. Paroxysmal nocturnal hemoglobinuria (PNH) and T cell large granular lymphocyte (LGL) leukemia – an unusual association: another cause of cytopenia in PNH. Ann Hematol 2015; 94(10): 1759–1760. Dostupné z DOI: <http://dx.doi.org/10.1007/s00277–015–2439–3>.
- Čermák J. Aplastická anémie. Vnitř Lék 2018; 64(5): 501–507.
- Orlandi E, Boselli P, Covezzi R et al. Reversal of bone marrow hypoplasia in anorexia nervosa: case report. Int J Eat Disord 2000; 27(4): 480–482.
- Greer JP, Arber DA, Blader B et al. Wintrobe´s clinical hematology. 13th ed. Lippincott Williams and Wilkins: Philadelphia, USA 2014. ISBN 978–1451172683.
- Maier KP. Hepatitis – Hepatitisfolgen. 6th ed. Hans Huber: Bern 2010. ISBN 978–3456846743
- Alfani R, Vassallo E, De Anseris AG et al. Pediatric fatty liver and obesity: not always just a matter of non-alcoholic fatty liver disease. Children (Basel) 2018; 5(12). pii: E169. Dostupné z DOI: <http://dx.doi.org/10.3390/children5120169>.
- Jung SY, Lee YJ, Lee HJ et al. Nonalcoholic fatty liver disease in long-term survivors of childhood-onset craniopharyngioma. Ann Pediatr Endocrinol Metab 2017; 22(3): 189–196. Dostupné z DOI: <http://dx.doi.org/10.6065/apem.2017.22.3.189>.
- Liberal R, Grant CR, Longhi MS et al. Diagnostic criteria of autoimmune hepatitis. Autoimmun Rev 2014; 13(4–5): 435–440. Dostupné z DOI: <http://dx.doi.org/10.1016/j.autrev.2013.11.009>.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2019 Číslo 11- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Funkční onemocnění trávicího traktu a bolest
- Môže warfarín zabrániť vzniku nádorov?
- Imunodeficience v rámci diferenciální diagnostiky intersticiálních plicních procesů
- Proč je v léčbě arteriální hypertenze důležité rychle dosáhnout cílových hodnot krevního tlaku
- Interferon-alfa v léčbě myeloproliferativních onemocnění
-
Sekundární prevence ischemické choroby srdeční a chorob periferních tepen kombinací antiagregační a antikoagulační léčby
Odborné stanovisko České kardiologické společnosti, České internistické společnosti ČLS J.E. Purkyně a České angiologické společnosti ČLS J.E. Purkyně k výsledkům studie COMPASS - Epidurální absces páteře – raritní komplikace Crohnovy choroby: kazuistika
- Pancytopenie, panhypopituitarizmus a jaterní cirhóza: rozbor složité kazuistiky
- Odešel profesor Ivo Dvořák
- Primář Jiří Spáčil oslavil 80. narozeniny
- Profesor Jan Petrášek slaví devadesáté narozeniny
- Nedostatek vitaminu D a jeho zdravotní dopady
- Mýty a fakty o liečbe artériovej hypertenzie: naozaj vieme o artériovej hypertenzii všetko?
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Funkční onemocnění trávicího traktu a bolest
- Interferon-alfa v léčbě myeloproliferativních onemocnění
- Nedostatek vitaminu D a jeho zdravotní dopady
- Imunodeficience v rámci diferenciální diagnostiky intersticiálních plicních procesů
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



