-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Presepsin: co je nutné vědět pro korektní interpretaci
Presepsin: what is important for correct interpretation
Introduction: Presepsin (soluble CD14 subtype) is a new biomarker of infection and sepsis. Correct interpretation is based on the knowledge of analytical reliability, biological variation, decision limits, and diagnostic effectivity. Aim: The aim of the study was to verify analytical precision of presepsin measurements, to assess biological variation in healthy subjects, to verify reference and decision limits, to assess diagnostic effectivity, and to compare data with commonly used septic biomarkers – procalcitonin (PCT), CRP and interleukin 6 (IL6).
Material and methods: Analytical precision (repeatability and intermediate precision) was estimated by repeated measurements of commercial control materials. Biological variation was evaluated in a group of 20 healthy volunteers in a 7-week experiment. Reference ranges were extracted from the literature and compared with data from healthy subjects.
Results: Precisions of presepsin measurements were 2.0–4.0 % (“within-run”) and 6.1–9.5 % (“between-run”). Intraindividual biological variation of presepsin was 22.3 %, interindividual variation 20.8 %. Index of individuality was 1.07, reference change value (RCV – critical difference) was 72 %. Upper reference limit was around 180 ng/l.
Conclusion: Analytical quality of presepsin measurement is suitable for clinical use. Biological variation parameters enable the use of reference limits, upper reference limit of presepsin is around 180 ng/l. None of the tested biomarkers has universal cut-off value, multiple biomarkers are needed and repeated measurements are advisable.
Keywords:
analytical reliability – CRP – decision limits – interindividual biological variation – interleukin 6 – intraindividual biological variation – presepsin – procalcitonin – reference limits
Autoři: Antonín Jabor 1,2; Zdenek Kubíček 1; Magda Labanczová 1; Janka Franeková 1,2
Působiště autorů: Oddělení klinické biochemie, pracoviště laboratorních metod IKEM, Praha 1; 3. LF UK, Praha 2
Vyšlo v časopise: Vnitř Lék 2019; 65(7-8): 490-496
Kategorie: Původní práce
Souhrn
Úvod: Presepsin (solubilní CD14 subtyp) je novějším biomarkerem infekce a sepse. Pro korektní interpretaci je potřebná znalost analytické spolehlivosti, biologické variability, rozhodovacích limitů a diagnostické efektivity.
Cíl: Cílem naší studie bylo ověřit preciznost stanovení presepsinu, zjistit jeho biologickou variabilitu u zdravých dobrovolníků, ověřit referenční a rozhodovací meze, posoudit diagnostickou efektivitu a porovnat tyto údaje s běžně používanými septickými biomarkery, jako jsou prokalcitonin (PCT), C reaktivní protein (CRP) a interleukin 6 (IL6).
Materiál a metody: Preciznost byla stanovena opakovaným měřením komerčních kontrolních materiálů za podmínek opakovatelnosti a mezilehlé preciznosti. Pro studii biologické variability byl použit soubor 20 zdravých dobrovolníků, kteří byli sledováni po dobu 7 týdnů. Hodnocení referenčních hodnot bylo provedeno rozborem literárních údajů a porovnáním s výsledky experimentu u zdravých dobrovolníků.
Výsledky: Preciznost stanovení byla na úrovni variačních koeficientů 2,0–4,0 % („v sérii“) a 6,1–9,5 % („mezi sériemi“). Intraindividuální biologická variabilita presepsinu byla 22,3 %, interindividuální variabilita 20,8 %. Index individuality byl 1,07, hodnota kritické diference (RCV – Reference Change Value) byla 72 %. Horní referenční mez je podle použité metodiky stanovení a použité referenční populace kolem 180 ng/l.
Závěry: Analytická kvalita stanovení presepsinu je dostatečná, parametry biologické variability umožňují použití referenčních mezí, horní referenční mez presepsinu je asi 180 ng/l. U žádného ze sledovaných biomarkerů nelze používat univerzální cut-off hodnoty, je nutné použití více biomarkerů a sledování vývoje jejich koncentrací v čase.
Klíčová slova:
analytická spolehlivost – CRP – interindividuální biologická variabilita – interleukin 6 – intraindividuální biologická variabilita – presepsin – prokalcitonin – referenční meze – rozhodovací limity
Úvod
Diagnostika a terapie sepse zůstává problémem, nová definice podle panelu Sepsis-3 je jak obhajována [1], tak kritizována [2]. Použití biomarkerů infekce a sepse je nicméně stále nutným doplňkem metod detekce infekčních agens klasickými (hemokultura) i novějšími (molekulární diagnostika) postupy. Správná interpretace všech neinvazivních laboratorních metod je založena na podrobných informacích o analytické spolehlivosti, referenčních rozmezích, biologické variabilitě a diagnostické efektivitě z hlediska přidané hodnoty v porovnání s ostatními biomarkery infekce a sepse. V případě presepsinu (solubilní CD14 subtyp) se těmito aspekty zabývá méně prací, většinou převládají data z jednotlivých klinických studií i metaanalýz. Cílem naší práce bylo zhodnotit analytickou spolehlivost, biologickou variabilitu, referenční rozmezí a diagnostickou efektivitu presepsinu a provést porovnání s dalšími biomarkery zánětu, infekce a sepse, především s CRP, prokalcitoninem (PCT) a interleukinem 6 (IL6).
Pacienti a metody
Hodnocení analytické spolehlivosti metody stanovení presepsinu
Koncentrace presepsinu byly měřeny na analyzátoru Pathfast (Mitsubishi Chemical, Japonsko) pomocí jednorázových kazet. Metoda pracuje na principu chemiluminiscenční enzymové imunoanalýzy, během 15 min lze vyšetřit až 6 vzorků plné krve nebo EDTA plazmy, kompaktní stolní přístroj je možné používat v režimu point-of-care testing. Rozsah měření je 20–20 000 ng/l, výrobce udává celkovou preciznost do 5 %. Koncentrace prokalcitoninu a IL6 byly stanoveny originálními reagenciemi na analyzátoru Cobas 8000 a Cobas 6000, Roche. Koncentrace CRP byly stanoveny originálními reagenciemi na analyzátoru Architect ci16200, Abbott Laboratories. Vlastními experimenty jsme ověřili preciznost za podmínek opakovatelnosti (označované též jako preciznost intra-assay, v sérii) a mezilehlou preciznost (též preciznost inter-assay, mezi sériemi).
Studie biologické variability a referenčního rozmezí presepsinu a porovnání s dalšími biomarkery zánětu a sepse
Do studie hodnotící referenční rozmezí a biologickou variabilitu (CVI, intraindividuální biologická variabilita, označovaná jako within-subject variation, a CVG, interindividuální biologická variabilita, between-subject variation) presepsinu bylo zařazeno celkem 20 subjektů (10 mužů, 10 žen, kavkazoidní rasa). Podrobně byl tento soubor pacientů popsán v publikacích o biologické variabilitě ELF skóre [3] a párech těžkých a lehkých řetězců imunoglobulinů κ a λ [4], kde jsou uvedeny také podmínky zpracování vzorků a použité statistické metody (Flignerův-Killeenův test, Shapirův-Wilkův test, Kolmogorovův-Smirnovův test, výpočty pomocí smíšeného lineárního regresního modelu) s ohledem na publikaci Bragy [5]. Hodnoty zjištěné v tomto experimentu porovnáváme s vlastními a literárními údaji o biologické variabilitě PCT, CRP a IL6. Literární údaje o referenčních mezích presepsinu porovnáváme s výsledky experimentu biologické variability presepsinu.
Výsledky
Analytická spolehlivost
Opakovatelnost stanovení presepsinu byla vyšetřena v rámci pravidelných verifikací metod s cílem zjistit nejistotu měření. Mezilehlá preciznost presepsinu byla určena testováním komerčního kontrolního materiálu pro kontrolu kvality v průběhu 26 dnů pro zjištění mezilehlé preciznosti. Pro porovnání udáváme údaje opakovatelnosti a mezilehlé preciznosti vyjádřené jako variační koeficient (CV – coefficient of variation, v %) pro IL6, PCT a CRP (tab. 1). Údaje získané v rámci kontroly kvality byly vyhodnoceny pomocí programu Unity Real Time, Bio-Rad Laboratories, verze 2.4.3.002.
Tab. 1. Odvození hodnot opakovatelnosti („v sérii“) a mezilehlé preciznosti („mezi sériemi“) na dvou koncentračních hladinách firemního kontrolního materiálu pro presepsin. Porovnání s analytickými charakteristikami pro IL6 (Cobas 6000, Roche), CRP (Architect ci16200, Abbott Laboratories) a PCT (Cobas 8000, Roche) 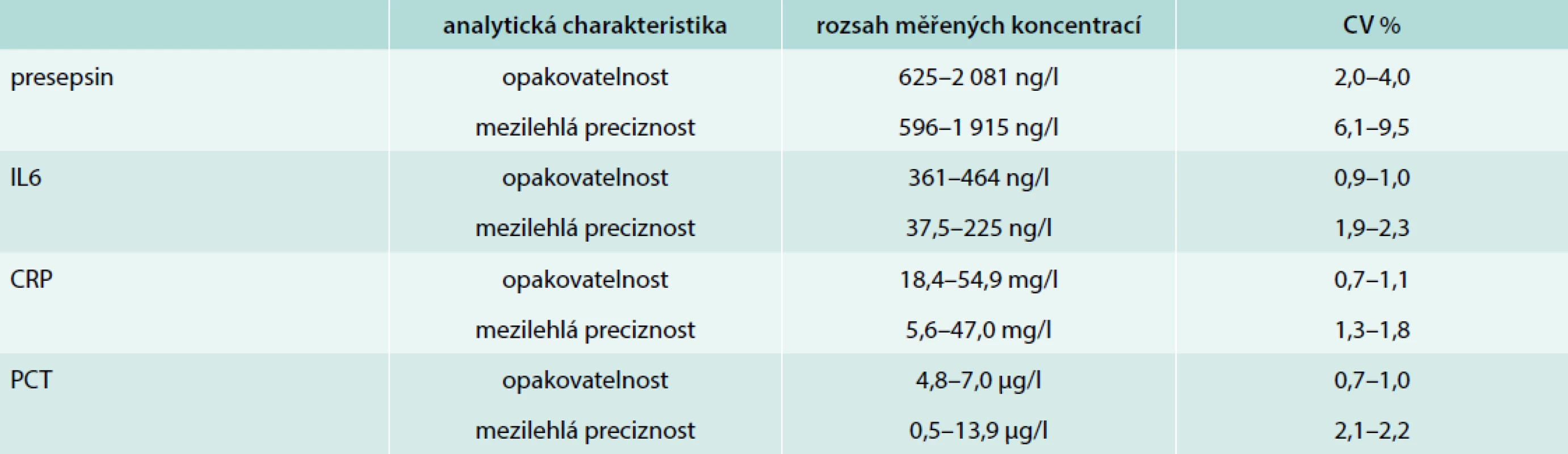
Biologická variabilita
Graf 1 a graf 2 ukazují výsledky vlastního experimentu pro odhad biologické variability presepsinu a IL6.
Graf 1. Výsledky experimentu pro odhad biologické variability presepsinu. Graf ukazuje výsledky u všech experimentálních osob, pouze jeden jedinec (žena S11) byl vzhledem ke zdravotnímu stavu vyloučen 
Graf 2. Výsledky experimentu pro odhad biologické variability IL6. Graf ukazuje výsledky u experimentálních osob s vyloučením jedinců S2 (muž, všechny hodnoty IL6 pod mezí detekce analytické metody) a S11 (žena, zdravotní důvody). Pro výpočet odhadu biologické variability byl vyloučen jedinec S18 (nesplnil podmínky testování homogenity rozptylů pomocí Flignerova-Killeenova testu) 
Výsledky výpočtu odhadů biologické variability jsou uvedeny v tab. 2. Vlastní data jsou uvedena pro presepsin a IL6 (pro ty jedince a jejich hodnoty, u nichž byla statistickými nástroji potvrzena možnost jejich použití), literární údaje jsou pro CRP a prokalcitonin.
Tab. 2. Analytická (CVA), intraindividuální (CVI) a interindividuální (CVG) variabilita, index individuality (II) a kritická diference (RCV – Reference Change Value) zjištěné na souboru 20 zdravých dobrovolníků 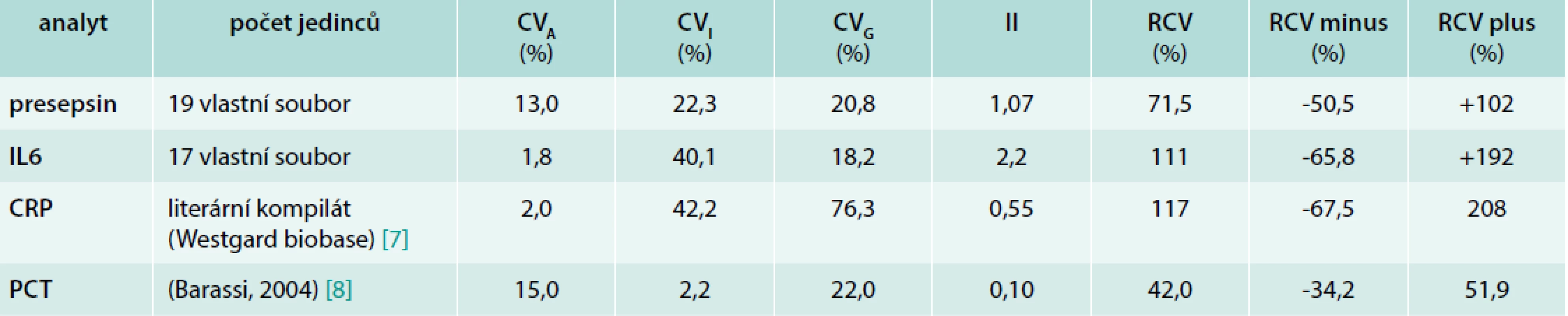
Pozn: pro výpočet biologické variability IL6 byla použita statistická metoda SD ANOVA Referenční meze
Referenční meze presepsinu v plazmě podle různých literárních údajů ukazuje tab. 3.
Tab. 3. Referenční rozmezí presepsinu v plazmě podle různých pramenů 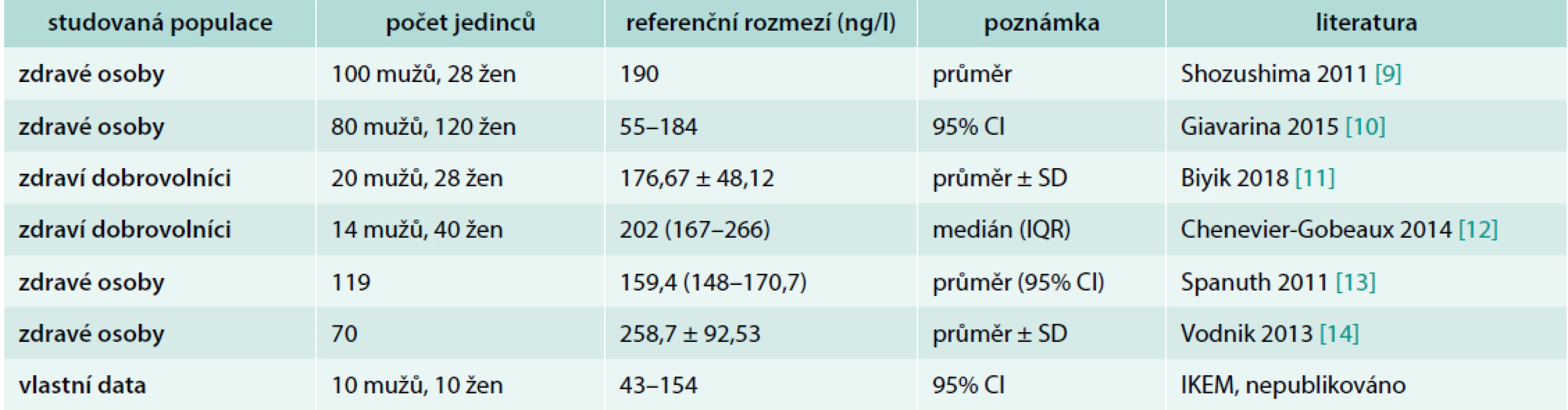
Diskuse
Předpokladem použití jakéhokoli laboratorního testu je přinejmenším znalost analytických charakteristik, referenčního rozmezí, klinických cut-off a rozhodovacích mezí, biologické variability (jak intraindividuální, tak interindividuální) a kritických diferencí (RCV). Dalším kritériem je znalost výpovědní hodnoty testu v diferenciálně diagnostických situacích. Určení jak referenčních mezí, tak rozhodovacích limitů závisí na zvolené populaci, tj. výběr klinických cut-points závisí na správném výběru kohorty pacientů. V naší práci jsme se pokusili odpovědět na základní otázky, které musí být položeny před použitím jakéhokoli laboratorního testu. Provedli jsme jak vlastní experimentální měření pro vybrané biomarkery infekce a sepse, tak konfrontaci s literárními údaji.
Je analytická metoda stanovení presepsinu spolehlivá?
Metoda stanovení presepsinu nemá mezinárodní kalibraci, je ale v podstatě standardizována „průmyslově“ – existuje jen jeden výrobce a jeden analytický systém. Pro metodu rovněž není dostupný komerční systém mezilaboratorního porovnávání a pro verifikaci metody není dostupný referenční materiál třetí strany (jak doporučuje norma ČSN EN ISO 15189) určený pro tyto účely. Verifikaci je tedy možné provést například pomocí firemního kontrolního materiálu (Pathfast Presepsin Ctrl 1 a 2). Tab. 1 ukazuje, že analytická spolehlivost stanovení presepsinu je na úrovni běžných imunochemických stanovení a metoda je vhodná pro klinické použití. Vyšší preciznost metod stanovení IL6, CRP a prokalcitoninu je patrná (tab. 1), ale jak pro presepin, tak pro ostatní vyjmenované metody je analytická kvalita s ohledem na vysoká zvýšení koncentrací biomarkerů v patologii zcela akceptovatelná.
Jsou údaje o biologické variabilitě presepsinu potřebné?
Experimenty zaměřené na biologickou variabilitu by měly být prováděny ve skupině alespoň 10 osob a hodnocení by mělo být opakováno alespoň 6krát [5]. Během naší studie byla sledována skupina 20 osob po dobu 7 týdnů. Jak je patrné z tab. 2, presepsin patří do skupiny testů, u nichž je podobná intraindividuální a interindividuální biologická variabilita. Výsledný index individuality (1,07) připouští použití referenčních mezí (to platí pro testy s II v rozmezí 0,6–1,1). Jsou-li hodnoty II < 0,6 (jak je tomu především v případě prokalcitoninu), je použití referenčních hodnot téměř bezpředmětné a je nutné monitorování nebo určení individuálního „referenčního rozmezí“. V našem experimentu byla problémem řada jedinců s neměřitelně nízkými hodnotami IL6 (pod mezí detekce analytické metody). Výsledky těchto individuálních měření bylo nutné vyloučit, ale nemělo to vliv na konečné výsledky, které byly v případě IL6 odvozeny na dostatečném počtu 96 měření. IL6 je testem s poměrně nízkou interindividuální variabilitou a II 2,2 (tab. 2), což umožňuje použití referenčních mezí. Hodnoty RCV presepsinu, IL6, CRP a prokalcitoninu naznačují, že významná změna proti předchozí hodnotě se pohybuje mezi 42 % (PCT) až 117 % (CRP). Tyto zdánlivě vysoké hodnoty RCV jsou balancovány vysokým nárůstem koncentrací septických ukazatelů v patologii (např. u PCT o stovky až tisíce procent). Je ale nutné počítat s tím, že biologická variabilita – zjištěná na souboru zdravých jedinců – nemusí nutně odpovídat biologické variabilitě v nemocné populaci. Přenositelnost údajů z experimentu do kliniky tedy není absolutní.
Jsou u biomarkerů sepse potřebné referenční hodnoty?
Bylo by možné akceptovat tezi, že referenční hodnoty nemají u infekčních a septických biomarkerů význam, protože je nutné monitorování. Na druhé straně je ale znalost referenčních mezí pro referenční (zcela bezpříznakovou) populaci základní charakteristikou testu a ukazuje určitou „míru bezpečnosti“ při použití daného biomarkeru, především v situacích prvního vyšetření u daného jedince. Znalost intraindividuální variability může interpretaci zjemňovat s využitím „intraindividuálních“ referenčních mezí u analytů s nízkým indexem individuality. Podle indexů individuality (tab. 2) lze použít horní referenční mez pro IL6 a presepsin, ale monitorování je u těchto parametrů jistě lepší volbou a v případě CRP a PCT je monitorování nutností.
V praxi je obtížné referenční meze stanovit v laboratoři pro danou populaci (problémem je jak získání dostatečného počtu referenčních jedinců, tak finanční a organizační náročnost experimentu). Proto je doporučeno buď převzít referenční meze od výrobce diagnostické soupravy, nebo vybrat relevantní referenční meze z literárních pramenů [15]. V obou případech je nutné referenční meze verifikovat postupem podle standardu CLSI [16]. Verifikace spočívá ve výběru 20 referenčních jedinců a laboratoř ověří, zda minimálně 18 z nich je uvnitř referenčního intervalu, který se verifikuje. Pokud ano, považuje se interval za ověřený. Pokud jsou 3 nebo 4 jedinci mimo interval, opakuje se test s dalšími (jinými) 20 referenčními jedinci. Pokud jich je opět alespoň 18 uvnitř intervalu, jsou referenční meze verifikovány. Jinak referenční interval nelze převzít. Pokud jsme tento postup aplikovali na vlastní soubor referenčních jedinců, ani jeden z publikovaných referenčních intervalů neodpovídal námi použité skupině 20 referenčních jedinců, i když prakticky nejblíže byl referenční interval Giavariniho [10].
Práce uvádějící referenční rozmezí presepsinu jsou spíše ojedinělé (tab. 3), populace nejsou dobře definované, počty jedinců jsou často malé a způsob statistického vyhodnocení je velmi často nesprávný. Např. Shozushima [9] nebere ohled na negaussovskou distribuci dat a udává koncentrace u zdravých jedinců pomocí průměru a směrodatné odchylky (294,2 + 121,4 ng/l), podobně také udává hodnoty pro SIRS (333,5 + 130,6 ng/l), lokální infekci (721 + 611,3 ng/l), sepsi (817,9 + 572,7 ng/l) a těžkou sepsi (1 992,9 + 1 509,2 ng/l). Diskutabilní je také práce Biyika [11], mezi jehož 48 zdravými dobrovolníky bylo 67 % kuřáků a 20 % diabetiků! Chenevier-Gobeauxová [12] použila neparametrický přístup, ale udává pouze interkvartilové rozpětí (167–266 ng/l). Výjimkou mezi pracemi popisujícími referenční meze je práce Giavariniho [10], který použil adekvátní mezinárodně doporučovaný protokol pro odhad referenčních mezí CLSI C28-A3c, nezjistil větší rozdíl mezi muži a ženami a v diskusi uvádí, že „The upper reference limit for the presepsin is much lower than every cut-off limit so far proposed, both for sepsis and also for systemic inflammatory response syndrome.“ Pokud jsme použili stejný protokol v IKEM, došli jsme k podobným hodnotám 43–154 ng/l v souboru dobrovolníků, kteří podstoupili experiment biologické variability. Horní referenční mez, minimálně pro evropskou populaci, se tedy pohybuje kolem 180 ng/l podle použitého souboru referenčních jedinců.
Jak používat klinické rozhodovací limity presepsinu?
Cut-off hodnoty presepsinu se podle literárních údajů liší v různých rozhodovacích situacích. V jedné ze základních prací použil Shozushima cut-off 415 ng/l pro odlišení SIRS a sepse a dospěl k senzitivitě 80 % a specifičnosti 81 % [9]. Podobný cut-off 413 ng/l použil Godnic na malém souboru pacientů v intenzivní péči a zjistil 85% senzitivitu detekce infekce při specifičnosti 63 % [17]. Obvykle jsou ale uvedeny vyšší cut-off hodnoty [6,18–21]. PPV a NPV publikují jen někteří autoři. Romualdo uvádí pro cut-off 729 ng/l PPV 30 % a NPV 94 % [21], Kweon pro nižší cut-off 430 ng/l uvádí PPV 89 % a NPV 80 % [22]. Metaanalytické zpracování 8 studií pro odlišení sepse a SIRS na 1 757 pacientech uvádějí Zheng et al [23]. Cut-off hodnoty byly mezi 317 až 729 ng/l, poolovaná senzitivita dosáhla hodnoty 77 % a poolovaná specifičnost hodnoty 73 %, při sumární hodnotě AUC 0,86 (AUC – Area Under Curve/oblast pod křivkou). V podstatě je ale použití publikovaných cut-off hodnot možné pouze v klinických situacích, které jsou identické nebo alespoň analogické s aktuální klinickou situací nebo klinickým prostředím. Jednoznačně je potřebné hodnoty septických biomarkerů monitorovat a v případě presepsinu jsou hodnoty > 500 ng/l vždy podezřelé, hodnoty > 1 000 ng/l vyžadují velkou pozornost. To potvrzuje práce brněnských autorů, kteří sledovali dynamiku změn CRP, PCT a presepsinu u zemřelých a přežívajících pacientů. Koncentrace PCT a presepsinu byly u přežívajících septických pacientů významně nižší v prvním dnu, v maximální hodnotě a na konci hospitalizace v porovnání se zemřelými pacienty. Hodnoty CRP se naproti tomu mezi přežívajícími a zemřelými nelišily [24]. Další údaje o interpretaci presepsinu přináší rovněž práce v tomto čísle časopisu [25].
Jaký je význam presepsinu ve speciálních situacích?
Všechny 4 uvedené septické markery jsou zvýšeny v rámci syndromu systémové zánětlivé odpovědi (SIRS – Systemic Inflammatory Response Syndrome). Např. u odpovědi organizmu na operační zákrok je toto ovlivnění nejnižší u presepsinu a nejvyšší u IL6, v případě nekomplikovaného průběhu bez infekce nebo sepse se koncentrace presepsinu, IL6 a PCT normalizují do 3. dne, v případě CRP může zvýšení přetrvávat i více než týden. Velké zvýšení hodnot PCT přináší aplikace antitymocytárního globulinu nebo kortikosteroidů v rámci indukční imunosupresivní léčby u transplantací solidních orgánů. Naopak snížení hodnot po indukční léčbě lze pozorovat u IL6 a CRP, které jsou ovlivněny nejen ATG a kortikosteroidy, ale také baziliximabem nebo rituximabem. Presepsin nebývá indukční imunosupresivní léčbou ovlivněn.
Vliv renálních funkcí nebyl spolehlivě doložen. Rozhodovací limity jsou pravděpodobně vyšší, ale schopnost identifikovat pacienty s infekcí nebo sepsí je u presepsinu zachována.
Vlivy hemodialýzy, použití mimotělního oběhu, extrakorporální oxygenace nebo implantace VAD (Ventricular Assist Device) na koncentrace infekčních biomarkerů nebyly rovněž spolehlivě doloženy. Zdá se ale, že spolehlivost všech biomarkerů včetně presepsinu v těchto situacích klesá [26].
Závěr
Presepsin je nový biomarker infekce a sepse, jehož koncentraci v krvi/plazmě lze stanovit u lůžka nebo v laboratoři spolehlivou analytickou metodou s variačním koeficientem < 10 % v dlouhodobém sledování. Experimentálně zjištěná intraindividuální biologická variabilita presepsinu (22,3 %) spolu s interindividuální variabilitou (20,8 %) poskytují index individuality 1,07 s možností využít referenční meze. Podle hodnoty RCV se při opakovaných vyšetřeních za zvýšenou hodnotu považuje koncentrace o 72 % vyšší než předchozí. Tato změna je větší než u PCT (RCV kolem 40 %) a nižší než u IL6 a CRP (RCV kolem 110 %). Většina literárně udávaných referenčních mezí presepsinu nebyla stanovena adekvátními postupy a za referenční rozmezí lze považovat pro evropskou populaci hodnoty do 180 ng/l. Použití univerzálních cut-off hodnot všech infekčních biomarkerů není oprávněné, protože v průběhu onemocnění se optimální diskriminační hodnoty mění, mění se riziko nebo pravděpodobnost infekce anebo sepse, vliv má antibiotická terapie a další interferující vlivy. Nutné je použití více biomarkerů a sledování vývoje jejich koncentrací v čase.
Poděkování
Za technickou asistenci děkujeme Jitce Komrskové, Martině Matouškové, Vladimíře Smržové, Štěpánce Strnadové, Michaele Tetourové, Tereze Vackové a Jiřímu Vymětalíkovi.
Práce byla podpořena z grantu MZ ČR číslo AZV MZ 15–27579A.
Doručeno do redakce 4. 1. 2019
Přijato po recenzi 6. 2. 2019
MUDr. Janka Franeková, Ph.D.
Oddělení klinické biochemie, pracoviště laboratorních metod IKEM, Praha
Zdroje
- Singer M, Deutschman CS, Seymour CW et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA 2016; 315(8): 801–810. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2016.0287>.
- Simpson SQ. New sepsis criteria: a change we should not make. Chest 2016; 149(5): 1117–1118. Dostupné z DOI: <http://dx.doi.org/10.1016/j.chest.2016.02.653>.
- Jabor A, Kubíček Z, Fraňková S et al. Enhanced liver fibrosis (ELF) score: Reference ranges, biological variation in healthy subjects, and analytical considerations. Clin Chim Acta 2018; 483 : 291–295. Dostupné z DOI: <http://dx.doi.org/10.1016/j.cca.2018.05.027>.
- Jabor A, Kubíček Z, Komrsková J et al. Within-subject biological variation of pairs of heavy/light immunoglobulin IgM chains (HLC IgM κ and λ) is low and requires monitoring: A comparison with HLC IgA, HLC IgG, and free light immunoglobulin chains (FLC) in healthy subjects. Clin Chim Acta 2018; 486 : 311–312. Dostupné z DOI: <http://dx.doi.org/10.1016/j.cca.2018.08.023>.
- Braga F, Panteghini M. Generation of data on within-subject biological variation in laboratory medicine: An update. Crit Rev Clin Lab Sci 2016; 53(5): 313–325. Dostupné z DOI: <http://dx.doi.org/10.3109/10408363.2016.1150252>.
- Franeková J, Sečník P, jr., Lavríková P et al. Serial measurement of presepsin, procalcitonin, and C-reactive protein in the early postoperative period and the response to antithymocyte globulin administration after heart transplantation. Clin Transplant 2017; 31(1): e12870. Dostupné z DOI: https://doi.org/10.1111/ctr.12870
- Westgard biobase. Desirable Specifications for Total Error, Imprecision, and Bias, derived from intra - and inter-individual biologic variation. Dostupné z WWW: <https://www.westgard.com/biodatabase1.htm>. (Přečteno 28.12.2018).
- Barassi A, Pallotti F, Melzi d’Eril G. Biological variation of procalcitonin in healthy individuals. Clin Chem 2004; 50(10): 1878. Dostupné z DOI: <http://dx.doi.org/10.1373/clinchem.2004.037275>.
- Shozushima T, Takahashi G, Matsumoto N et al. Usefulness of presepsin (sCD14-ST) measurements as a marker for the diagnosis and severity of sepsis that satisfied diagnostic criteria for systemic inflammatory response syndrome. J Infect Chemother 2011; 17(6): 764–769. Dostupné z DOI: <http://dx.doi.org/10.1007/s10156–011–0254-x>.
- Giavarina D, Carta M. Determination of reference interval for presepsin, an early marker for sepsis. Biochem Med (Zagreb) 2015; 25(1): 64–68. Dostupné z DOI: <http://dx.doi.org/10.11613/BM.2015.007>.
- Biyik I, Caglar FNT, Isiksacan N et al. Serum presepsin levels are not elevated in patients with controlled hypertension. Int J Hypertens 2018 : 8954718. Dostupné z DOI: <http://dx.doi.org/10.1155/2018/8954718>.
- Chenevier-Gobeaux C, Trabattoni E, Roelens M et al. Presepsin (sCD14-ST) in emergency department: the need for adapted threshold values? Clin Chim Acta 2014; 427 : 34–36. Dostupné z DOI: <http://dx.doi.org/10.1016/j.cca.2013.09.019>.
- Spanuth E, Ebelt H, Ivandic B et al. Diagnostic and prognostic value of presepsin (soluble CD14 subtype) in emergency. 21st International Congress of Clinical Chemistry and Laboratory Medicine, IFCC-WorldLab – EuroMedLab, Berlin, 2011. Poster 0333. Dostupné z WWW: <http://medi-lab.hu/doc/Poster_sCD14-ST.pdf>.
- Vodnik T, Kaljevic G, Tadic T et al. Presepsin (sCD14-ST) in preoperative diagnosis of abdominal sepsis. Clin Chem Lab Med 2013; 51(10): 2053–2062. Dostupné z DOI: <http://dx.doi.org/10.1515/cclm-2013–0061>.
- Tate JR, Yen T, Jones GR. Transference and validation of reference intervals. Clin Chem 2015; 61(8): 1012–1015. Dostupné z DOI: <http://dx.doi.org/10.1373/clinchem.2015.243055>.
- Clinical and Laboratory Standard Institute (CLSI). Defining, establishing, and verifying reference intervals in the clinical laboratory: Approved guidelines. 3rd ed. CLSI: Wayne (USA) 2008. Dostupné z WWW: <https://clsi.org/media/1421/ep28a3c_sample.pdf>.
- Godnic M, Stubljar D, Skvarc M et al. Diagnostic and prognostic value of sCD14-ST–presepsin for patients admitted to hospital intensive care unit (ICU). Wien Klin Wochenschr 2015; 127(13–14): 521–527. Dostupné z DOI: <http://dx.doi.org/10.1007/s00508–015–0719–5>.
- Ulla M, Pizzolato E, Lucchiari M et al. Diagnostic and prognostic value of presepsin in the management of sepsis in the emergency department: a multicenter prospective study. Crit Care 2013; 17(4): R168. Dostupné z DOI: <http://dx.doi.org/10.1186/cc12847>.
- Ishikura H, Nishida T, Murai A et al. New diagnostic strategy for sepsis-induced disseminated intravascular coagulation: a prospective single-center observational study. Crit Care 2014; 18(1): R19. Dostupné z DOI: <http://dx.doi.org/10.1186/cc13700>.
- Behnes M, Bertsch T, Lepiorz D et al. Diagnostic and prognostic utility of soluble CD 14 subtype (presepsin) for severe sepsis and septic shock during the first week of intensive care treatment. Crit Care 2014; 18(5): 507. Dostupné z DOI: <http://dx.doi.org/10.1186/s13054–014–0507-z>.
- Romualdo LG, Torrella PE, González MV et al. Diagnostic accuracy of presepsin (soluble CD14 subtype) for prediction of bacteremia in patients with systemic inflammatory response syndrome in the Emergency Department. Clin Biochem 2014; 47(7–8): 505–508. Dostupné z DOI: <http://dx.doi.org/10.1016/j.clinbiochem.2014.02.011>.
- Kweon OJ, Choi JH, Park SK et al. Usefulness of presepsin (sCD14 subtype) measurements as a new marker for the diagnosis and prediction of disease severity of sepsis in the Korean population. J Crit Care 2014; 29(6): 965–970. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jcrc.2014.06.014>.
- Zheng Z, Jiang L, Ye L et al. The accuracy of presepsin for the diagnosis of sepsis from SIRS: a systematic review and meta-analysis. Ann Intensive Care 2015; 5(1): 48. Dostupné z DOI: <http://dx.doi.org/10.1186/s13613–015–0089–1>.
- Beňovská M, Bučková D, Petříková D et al. Presepsin jako diagnostický a prognostický nástroj při posuzování sepse. Klin Biochem Metab 2015; 23(3): 89–94. Dostupné z WWW: <http://www.cskb.cz/res/file/KBM-pdf/2015/2015–3/KBM-3–2015–89-Benovska.pdf>.
- Káňová M, Dobiáš R, Liszková K et al. Presepsin v diagnostice sepse. Vnitř Lék 2019; 65(7–8): 497–505.
- Kettner J, Holek M, Franekova J et al. Procalcitonin Dynamics after Long-Term Ventricular Assist Device Implantation. Heart Lung Circ 2017; 26(6): 599–603. Dostupné z DOI: <http://dx.doi.org/10.1016/j.hlc.2016.09.014>.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2019 Číslo 7-8- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Nech brouka žít… Ať žije astma!
- Intermitentní hladovění v prevenci a léčbě chorob
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Je to sepse, nebo není? A je presepsin tou správnou odpovědí? – editorial
- U nemocných s idiopatickými střevními záněty je potřeba vitaminu D vyšší: intervenční studie
- Pľúcna embólia: retrospektívny pohľad na známe ochorenie
- Stres v preventivní kardiologii
- Presepsin: co je nutné vědět pro korektní interpretaci
- Presepsin v diagnostice sepse
- Aortální disekce a jiné akutní aortální syndromy na urgentním příjmu
- Nehematogenní působení erytropoetinu
- Idiopatický střevní zánět a 1. typ autoimunitní formy pankreatitidy: kazuistika
- Diosmin – stále důležitá modalita v léčbě žilní nedostatečnosti
- Jiří Beneš. Antibiotika – systematika, vlastnosti, použití
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Presepsin v diagnostice sepse
- Aortální disekce a jiné akutní aortální syndromy na urgentním příjmu
- Pľúcna embólia: retrospektívny pohľad na známe ochorenie
- Diosmin – stále důležitá modalita v léčbě žilní nedostatečnosti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



