Primární hyperaldosteronizmus – nejčastější forma sekundární hypertenze
Primary hyperaldosteronism – the most common form of secondary hypertension
Primary aldosteronism is the most common form not only of endocrine, but also secondary hypertension, associated with increased cardiovascular risk. It is caused by autonomous overproduction of aldosterone by the adrenal cortex. Clinically, it manifests with hypertension often resistant to treatment and hypokalaemia. The screening tool is the increased ratio of aldosterone/ renin due to increased concentrations of aldosterone and low levels of renin, and the diag-nosis is confirmed by the lack of suppression of aldosterone during confirmatory tests. Before indication for surgical treatment, adrenal venous sampling is used in the majority of patients to assess lateralization. In other cases is indicated treatment with aldosterone receptor blockers is indicated. Given the complexity of the diagnostic process, patients with suspected PH should be treated only in specialized centres.
Keywords:
primary aldosteronism – hypertension – aldosterone – renin
Authors:
B. Štrauch; J. Widimský jr.
Authors‘ workplace:
III. interní klinika – klinika endokrinologie a metabolismu 1. LF UK a VFN v Praze, Centrum pro výzkum, diagnostiku a léčbu hypertenze
Published in:
Kardiol Rev Int Med 2015, 17(2): 155-160
Category:
Internal Medicine
Overview
Primární hyperaldosteronizmus je nejčastější formou nejen endokrinní, ale i sekundární hypertenze spojenou se zvýšeným kardiovaskulárním rizikem. Je způsoben autonomní nadprodukcí aldosteronu kůrou nadledvin. Klinicky se projevuje hypertenzí, často rezistentní, spojenou s hypokalemií. Screeningovým nástrojem je zvýšení poměru aldosteron/ renin způsobené zvýšením koncentrace aldosteronu a nízkými hladinami reninu. Diagnóza je potvrzena chyběním suprese aldosteronu v průběhu konfirmačních testů. K posouzení lateralizace používáme před zvažovaným operačním řešením u většiny pacientů separované odběry z nadledvinných žil na hormonální stanovení. V ostatních případech je indikována léčba blokátory aldosteronových receptorů. Vzhledem ke složitosti diagnostického procesu by pacienti s podezřením na PH měli být vyšetřováni pouze ve specializovaných centrech.
Klíčová slova:
primární hyperaldosteronizmus – hypertenze – aldosteron – renin
Úvod – definice, historie a prevalence primárního hyperaldosteronizmu
Primární hyperaldosteronizmus (PH) je syndrom způsobený autonomní nadprodukcí aldosteronu kůrou nadledvin. Přestože byl PH zřejmě poprvé popsán v roce 1953 v polském odborném časopise Litynským, je prvenství připisováno a nyní je syndrom nazýván podle J. W. Conna, který jej podrobně popsal v roce 1955 – Connův syndrom [1]. V 80. letech 20. století po zavedení nového, relativně jednoduchého screeningového testu – poměru aldosteron/ renin – došlo k nárůstu záchytu PH. Dle posledních výzkumů je jednou z nejčastějších forem sekundární hypertenze s frekvencí až 10 % u neselektované populace [2] a až 20 % u hypertoniků odeslaných k vyšetření na specializované hypertenziologické pracoviště [3].
PH je charakterizován retencí sodíku, volumovou arteriální hypertenzí, zvýšenou exkrecí draslíku ledvinami vedoucí k rozvoji hypokalemie. Nejčastějšími formami (tab. 1) jsou bilaterální hyperplazie nadledvin a unilaterální adenom kůry nadledviny. Ostatní formy jsou méně časté – unilaterální hyperplazie nadledviny bývá diagnostikována až na základě histologického vyšetření po operaci. Byly popsány tři familiární formy – familiární hyperaldosteronizmus typ I (FH ‑ I) neboli také dexametazon ‑ supresibilní hyperaldosteronizmus je autozomálně dominantně dědičnou formou PH podmíněnou přítomností chimérického genu aldosteron ‑ syntázy s regulační oblastí genu pro 11 - beta hydroxylázu. V oblasti zona fasciculata, kde normálně k syntéze aldosteronu nedochází, je exprimován produkt tohoto genu. Následkem toho je syntéza aldosteronu řízena ACTH, a tedy po podání nízké dávky dexametazonu dochází k ústupu hyperaldosteronizmu a normalizaci krevního tlaku. Familiární hyperaldosteronizmus typ II (FH ‑ II) je charakterizován výskytem aldosteron-produkujícího adenomu nebo bilaterální hyperplazie nadledvin v rodinách po vyloučení FH ‑ I, geneticky je podezření na lokalizaci abnormality v oblasti chromozomu 7p22 [4]. Nově byl popsán familiární hyperaldosteronizmus III. typu (zárodečná mutace genu KCNJ5 pro draslíkový kanál). Velmi vzácně může být příčinou PH karcinom kůry nadledviny.
![Frekvence různých podtypů PH. Doplněno a upraveno podle [27].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/e28a851d9bf8b41d55becdcd251ef794.png)
Patofyziologie a klinické projevy PH
PH je charakterizován autonomní nadprodukcí aldosteronu. Aldosteron zvyšuje krevní tlak prostřednictvím retence sodíku zprostředkované intracelulárně lokalizovanými mineralokortikoidními receptory buněk distálního tubulu ledvin. Jejich aktivace vede ke zvýšení reabsorpce Na+ a ztrátám K+, a tím k expanzi extracelulárního objemu.
Typickým klinickým projevem PH je arteriální hypertenze. U většiny případů plně vyjádřeného syndromu jde o středně těžkou až těžkou hypertenzi často rezistentní na kombinovanou farmakoterapii (tři druhy antihypertenziv včetně diuretika). Navíc bývá u PH často narušen diurnální rytmus krevního tlaku ve smyslu oslabení nočního poklesu tlaku [5].
Současně s těžkou hypertenzí je typickým klasickým projevem PH hypokalemie, která je způsobena zvýšeným vylučováním kalia v renálních tubulech (zvýšením aktivity Na – K + + H antiportů), což způsobí u těžších forem PH až metabolickou alkalózu.
Klinicky se hypokalemie dle tíže může projevit (spíše vzácněji) neuromuskulárními poruchami, svalovou slabostí, mírnou polyurií (při kaliopenické nefropatii). Těžká hypokalemie může být manifestována prvním projevem PH ve formě maligní arytmie [6]. V posledních letech je při častějším záchytu PH popisován častější výskyt normokalemických případů – překvapivě až u 50 % pacientů s adenomem [7], a u dokonce 83 % s idiopatickým hyperaldosteronizmem.
Mírná hypernatremie je běžná u PH na rozdíl od sekundárního hyperaldosteronizmu. Dále lze zachytit i hypomagnezemii způsobenou zvýšenou exkrecí hořčíku ledvinami.
Komplikace PH
Významným důvodem, proč v klinické praxi pátrat po PH, jsou výsledky experimentálních i klinických studií, které svědčí pro to, že nadbytek aldosteronu může způsobovat nežádoucí poškození kardiovaskulárního systému (remodelace a fibrózy) nezávisle na jeho efektu na zvýšení krevního tlaku, a to častěji než u pacientů s esenciální hypertenzí (EH). Bylo prokázáno, že pacienti s PH, ve srovnání s pacienty s EH, mají zvýšenou plazmatickou koncentraci aminoterminálního propeptidu prokolagenu typu I, markeru syntézy a metabolizmu kolagenu, což svědčí pro zvýšenou fibroprodukci [8]. To bylo potvrzeno studií, která prokázala vyšší množství celkového kolagenu a kolagenu III. typu a ztluštění medie v malých podkožních tepénkách získaných biopsií u pacientů s PH než u pacientů s EH srovnatelného věku, body mass indexu a hodnot krevního tlaku [9].
V několika studiích byly posuzovány markery poškození kardiovaskulárního systému u pacientů s PH, byla zjištěna vyšší intimomediální tloušťka společné karotidy než u pacientů s EH [10], s regresí po specifické léčbě, časnější po adrenalektomi, než po konzervativní léčbě [11]. Pro poškození velkých elastických cév nadbytkem aldosteronu se zvýšením jejich tuhosti může svědčit studie prokazující zvýšení karotido ‑ femorální rychlosti šíření pulzní vlny u pacientů s PH [12] a zejména její pokles jeden rok po provedené adrenalektomii na rozdíl od konzervativní terapie spironolaktonem [13].
Co se týká poškození myokardu, jsou k dispozici data z několika studií, v první byl pozorován vyšší index hmotnosti levé komory srdeční spolu s markery diastolické dysfunkce levé komory srdeční u pacientů s PH ve srovnání s EH [14]. V dalších studiích byl prokázán větší efekt chirurgické terapie PH ve srovnání se spironolaktonem v redukci hmotnosti levé komory srdeční [15,16]. Tato data podporují výsledky retrospektivních studií u pacientů s PH, které ukazují na vyšší výskyt kardiovaskulárních onemocnění než u srovnatelných pacientů s EH stejného pohlaví, věku a hodnot tlaku [17].
PH je považován za jednu z endokrinně podmíněných forem diabetes mellitus. Pomocí clampových studií byla prokázána snížená inzulinová senzitivita u PH ve srovnání s esenciální hypertenzí [18] a její zlepšení po operaci [19]. Výsledky řady dosud provedených studií se však rozcházejí v tom, jestli je u PH skutečně zvýšený výskyt manifestní hyperglykemie a diabetes mellitus [20].
Diagnostika a diferenciální diagnostika PH
První otázku, kterou bychom si měli na úvod položit, je základní – proč pátrat po PH?Hlavním důvodem je včasná detekce, která umožní při cílené terapii zabránit rozvoji kardiovaskulárních komplikací (častějších/ významnějších u PH ve srovnání s esenciální hypertenzí). Včasná chirurgická léčba umožní téměř u všech pacientů normalizaci tlaku bez nutnosti další antihypertenzní terapie nebo snížení počtu antihypertenziv a u většiny i regresi poškození kardiovaskulárního systému (podrobně viz odstavec o komplikacích PH).
Screening PH by měl být proveden v těchto případech, kdy je největší pravděpodobnost diagnózy PH [21]:
- Jinak nevysvětlitelná hypokalemie spontánní nebo diuretiky navozená.
- Hypertenze 2. a 3. stupně.
- Farmakorezistentní hypertenze (TK > 140/ 90 mm Hg při trojkombinaci antihypertenziv včetně diuretika).
- Juvenilní hypertenze a/ nebo CMP v mladém věku pod 50 let (potenciální FH ‑ I).
- Incidentalom nadledviny a hypertenze.
- Zjištění orgánového poškození závažnějšího stupně, než by odpovídalo tíži hypertenze.
Indikaci screeningu je však nutno zvážit např. u pacientů vyššího věku, polymorbidních, kde stanovení diagnózy nepovede k chirurgickému řešení a je možné při hypokalemii a rezistentní hypertenzi empiricky do terapie přidat spironolakton. Schéma diagnostického postupu u PH je uvedeno na obr. 1.
![Schéma diagnostického a terapeutického postupu u primárního hyperaldosteronizmu.
Upraveno podle [21].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/6688d3e390b3e9dfca7c039a0ff02623.jpg)
Velmi senzitivním, ale zároveň relativně jednoduchým nástrojem využívaným ve screeningu je poměr aldosteron ‑ renin (ARR). Výpočet ARR je jednoduchý – jde o podíl plazmatického aldosteronu a plazmatické reninové aktivity nebo přímého imunoreaktivního reninu, nicméně při interpretaci je nutno věnovat pozornost použitým jednotkám (ARR v různých jednotkách viz tab. 2).
![Diagnostická kritéria zvýšení poměru aldosteron/renin v závislosti na typu stanovení a použitých jednotkách. Použitý převodní faktor z plazmatické reninové aktivity (PRA) (ng/ml/h) na přímý renin (mU/l) je 8,2 (může být jiný v závislosti na typu stanovení).
Upraveno podle [21].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/87650cb0fba52bbaff6ab95c86981cf0.jpg)
Mezi důležité faktory ovlivňující senzitivitu testu patří doba odběru (doporučován je odběr v ranních hodinách minimálně 1 – 2 hod po probuzení ve vertikální poloze, žádná restrikce příjmu soli před odběrem, vhodná je korekce hypokalemie). Vzhledem k tomu, že většina antihypertenziv může ovlivnit koncentraci aldosteronu a/ nebo plazmatickou reninovou aktivitu či koncentraci přímého reninu (tab. 3), je vhodné před odběry upravit antihypertenzní medikaci, je‑li to vzhledem ke klinickému stavu možné. Betablokátory snižují plazmatickou reninovou aktivitu (PRA), a tím mohou způsobit falešně pozitivní ARR, je tedy nutné je vysadit dva týdny před odběrem (mimo případy, kdy by tento postup byl rizikový, např. u pacientů s ICHS po IM apod.). Naopak thiazidová, kalium šetřící diuretika a antagonisté mineralokortikoidních receptorů (spironolakton, eplerenon) PRA zvyšují, mohou způsobit falešnou negativitu screeningového testu a měly by být vysazeny nejméně dva týdny (spironolakton nejméně 4 – 6 týdnů, vzhledem k protrahovanému účinku). Rovněž inhibitory angiotenzin konvertujícího enzymu, blokátory angiotenzinových receptorů (sartany), přímé inhibitory reninu je vhodné vysadit dva týdny před odběrem. Dihydropyridinové blokátory kalciového kanálu mohou způsobit v některých případech falešně negativní výsledek. Dále bychom se měli vyhnout i centrálně působícím antihypertenzivům. Jako náhradní antihypertenzní terapii bez ovlivnění stanovení lze použít buď alfablokátory (doxazosin), a/ nebo retardovaný verapamil. Nověji jsou uváděny další interferující léky jako steroidní hormonální antikoncepce, kde jsou k dispozici i preparáty obsahující drospirenon příbuzný spironolaktonu, které mohou vést k falešně pozitivním výsledkům [22], a dále i SSRI antidepresiva, která mohou způsobit naopak falešnou negativitu screeningového testu [23].
![Faktory, které ovlivňují poměr (ARR) aldosteron/plazmatická reninová aktivita (PRA) nebo renin a mohou vést k falešně pozitivním a falešně negativním výsledkům.
Upraveno dle [21].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/1b2c1793ce7369a711407fc84724f2b2.png)
Je nutno také brát v úvahu další faktory, např. ve vyšším věku dochází k poklesu PRA, v černošské populaci je sklon k nižší PRA, což může způsobit falešně pozitivní výsledek ARR.
Dle guidelines je za abnormální považován ARR ≥ 30 [ng/ dl]/ [ng/ ml/ h] [21] (hodnotu v jiných jednotkách viz tab. 2). Zároveň by však měla být hladina aldosteronu vyšší nebo alespoň na horní hranici normy (≥ 15ng/ dl) a renin alespoň na dolní mezi normy.
Diagnózu PH je nutné definitivně potvrdit některým ze supresních testů (tab. 4). Měly by být prováděny ve specializovaných centrech. Principem těchto testů je expanze plazmatického objemu, která by za fyziologického stavu měla potlačit produkci reninu, a tím vést ke snížení koncentrace aldosteronu, což chybí u PH. Existují čtyři druhy konfirmačních testů a užití konkrétního testu se liší dle zvyku daného pracoviště. Vždy před provedením testu je nutné normalizovat kalemii, aby nedošlo k supresi sekrece aldosteronu, a tím k falešně negativnímu výsledku. Nejčastěji se v našich podmínkách provádí test s podáním infuze 2 l fyziologického roztoku během 4 hod, který by měl začít v ranních hodinách, po minimálně 1 hod v horizontální poloze s provedením odběru na koncentraci aldosteronu, PRA (reninu) před podáním infuze a po podání infuze. Dle některých studií je test provedený vleže považován za málo senzitivní a recentně bylo zjištěno, že jeho provedení vsedě zvyšuje jeho senzitivitu [24]. Při koncentraci aldosteronu pod 5 ng/ dl po infuzi je PH málo pravděpodobný, při koncentraci nad 10 ng/ dl je test pozitivní, hodnoty mezi 5 a 10 ng/ dl představují tzv. šedou zónu. Test by neměl být prováděn u pacientů s renální insuficiencí, srdečním selháním, těžkou hypokalemií. Nejvíce senzitivním se zdá být fludrokortizonový supresní test, ale jeho nevýhodou je, že vyžaduje několikadenní hospitalizaci, má komplikovaný protokol, nezanedbatelné riziko hyperkalemie a výrazné elevace krevního tlaku.
![Konfirmační testy pro PH. Přehled dle [21].
V naší praxi nejčastěji využíváme test s fyziologickým roztokem.](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/4b2a2a817ca2887653ca1dc645165164.png)
Diferenciální diagnostika podtypů PH
Po laboratorním potvrzení diagnózy PH dále přistupujeme k určení jeho podtypu. U všech pacientů bychom měli provést CT nadledvin, kde lze diagnostikovat unilaterální nebo bilaterální zvětšení nadledvin. Solitární benigní adenomy jsou většinou unilaterální a menší než 3 cm v průměru (obr. 2). U útvarů menších než 1 cm (až 20 % adenomů) je detekce na CT obtížnější. U idiopatického hyperaldosteronizmu nalézáme často nodulární hyperplazii, kde může dojít k záměně uzlu za aldosteron produkující adenom. Dále je nutno vzít v úvahu i častý výskyt afunkčních lézí nadledvin, jejichž výskyt roste s věkem. Ve studii s 203 pacienty s PH, kteří byli vyšetřeni pomocí CT i separovaných odběrů z nadledvinových žil, bylo CT přesné pouze u 53 %. Na základě CT nálezu by u 42 pacientů (22 %) zůstal neodhalený potenciálně chirurgicky léčitelný aldosteron produkující adenom a 48 pacientů (25 %) by bylo operováno zbytečně [25]. Nejpřesnějším vyšetřením s vysokou senzitivitou a specificitou k posouzení lateralizace nadprodukce aldosteronu v případě zvažované chirurgické léčby jsou separované odběry z nadledvinových žil prováděné ve specializovaných centrech. Úspěšnost provedení vyšetření je značně závislá na zkušenosti radiologa, hlavně vzhledem k obtížné kanylaci pravé nadledvinové žíly. Provádíme stanovení plazmatického aldosteronu a kortizolu z pravé a levé nadledvinové žíly a z periferní žíly. V používaných kritériích, při neexistenci jasných guidelines, jsou mezi pracovišti v různých zemích jisté odlišnosti, recentně bylo publikováno konsenzuální stanovisko expertů k této problematice [26], podrobnosti stran analýzy výsledků přesahují rámec tohoto sdělení.
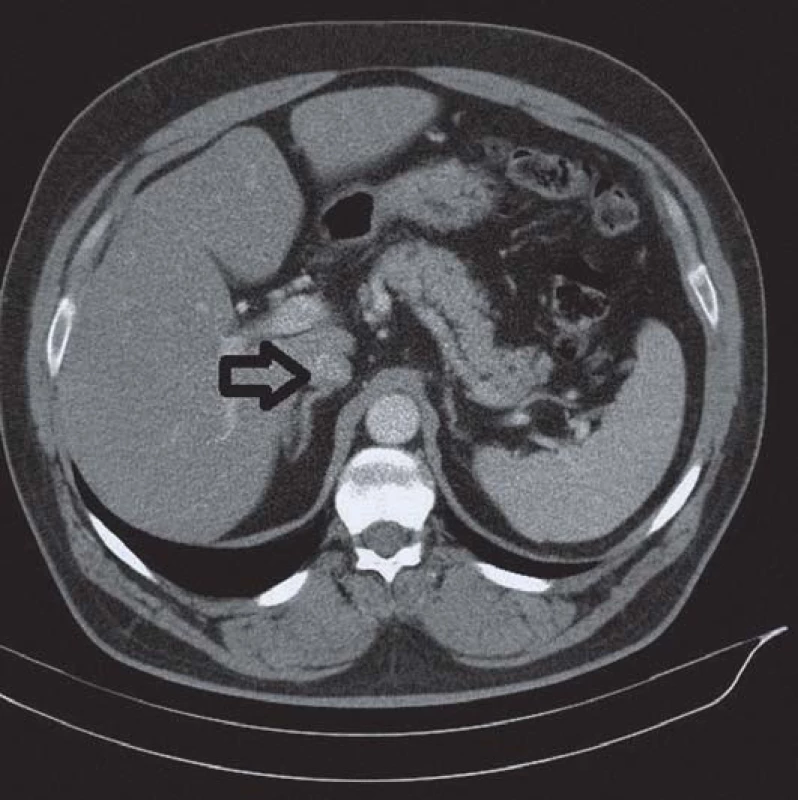
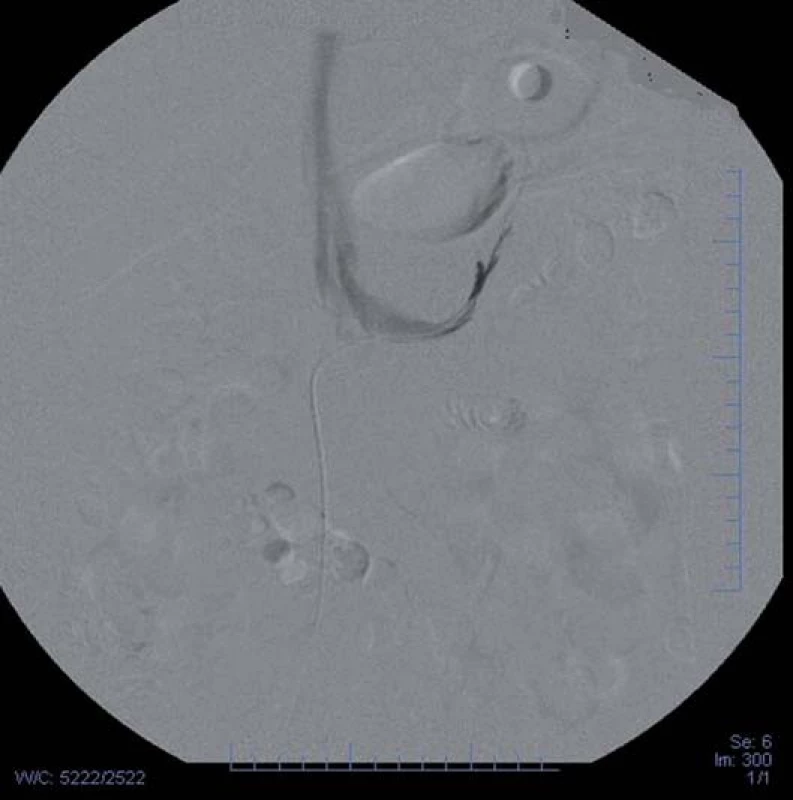
Genetický screening FH ‑ I by měl být proveden u mladších pacientů s rodinnou anamnézou hypertenze nebo krvácivé cévní mozkové příhody ve věku do 50 let.
Terapie PH
V případě průkazu unilaterální nadprodukce pomocí separovaných odběrů lze indikovat unilaterální laparoskopickou adrenalektomii. Bez provedení separovaných odběrů lze indikovat adrenalektomii pouze výjimečně – u mladých pacientů (věk ≤ 40 let), s jednoznačným nálezem unilaterálního adenomu na CT či MR (> 1 cm), morfologicky normální druhostrannou nadledvinou, významnou hypokalemií ≤ 3,0 mmol/ l a výrazně zvýšeným plazmatickým aldosteronem (≥ 30 ng/ dl) [27], kde je pravděpodobnost bilaterální nadprodukce minimální.
Podle poslední studie z centra provádějícího přesnou diagnostiku podtypů PH pomocí separovaných odběrů bylo dosaženo unilaterální adrenalektomií „biochemického vyléčení“ PH u 95 % pacientů. Hypertenze byla vyléčena u 55 % a zlepšení kontroly bylo pozorováno u 36 % pacientů [28].
Dnes je v převážné většině případů ve světě i u nás tato operace prováděna laparoskopickou cestou buď transabdominálním, nebo retroperitoneoskopickým přístupem. Ve srovnání s klasickou adrenalektomií je u laparoskopické adrenalektomie nižší výskyt komplikací a kratší doba hospitalizace.
Pokud byla diagnostikována bilaterální hyperplazie či hyperaldosteronizmus nebyl klasifikován (odmítnutí případné operace pacientem, neselektivní výsledek separovaných odběrů z nadledvinových žil) a v případě kontraindikace chirurgického výkonu, je namístě farmakoterapie blokátorem aldosteronových receptorů, v praxi nejčastěji spironolaktonem. Při zahájení terapie spironolaktonem používáme dávky až 100 mg denně, udržovací dávky se však obvykle pohybují mezi 25 a 75 mg denně. I přesto zůstává častým vedlejším účinkem (vzhledem k neselektivnímu působení i na receptory pro androgeny a gestageny) u mužů gynekomastie, ztráta libida, u žen nepravidelnosti menstruačního cyklu, bolesti hlavy a dyspepsie. V případě intolerance spironolaktonu lze použít eplerenon. Dle randomizované studie srovnávající účinnost, bezpečnost a snášenlivost eplerenonu a spironolaktonu (podávaných v relativně vysokých dávkách 100 – 300 mg/ den, resp. 75 – 225 mg/ den) byl spironolakton sice účinnější ve smyslu snížení krevního tlaku, ale dle očekávání způsobil větší výskyt gynekomastie a bolestí prsů u žen [29]. Afinita k androgenním a gestagenním receptorům je u eplerenonu až 500× nižší než u spironolaktonu, proto nemá z tohoto hlediska žádné nežádoucí účinky. Určitou nevýhodou eplerenonu je vzhledem k jeho nižší intenzitě účinku (50 – 75 % ve srovnání se stejnou dávkou spironolaktonu) nutnost podávat vyšší dávky – 25 – 50 mg 2× denně. Širšímu využití eplerenonu v léčbě brání i fakt, že není v Evropě bohužel v této indikaci (léčba PH nebo alespoň hypertenze) registrován a jeho předepisování a hrazení veřejným zdravotním pojištěním je možné pouze ve specializovaných centrech, a to pouze u pacientů prokazatelně netolerujících spironolakton. Dlouho byla komplikací i jeho vysoká cena, s vypršením patentové ochrany se však na našem trhu objevily generické preparáty, a tak došlo k jejímu poklesu.
Při léčbě antagonisty aldosteronových receptorů jsou nutné pravidelné kontroly mineralogramu a renálnich funkcí. V případě nedostatečné kontroly krevního tlaku monoterapií, což je celkem časté, je nejvhodnější kombinace s thiazidovými diuretiky a s kalciovými blokátory [21]. K léčbě PH lze použít i amilorid, je však mnohem méně účinný než blokátory aldosteronových receptorů [21].
FH ‑ I léčíme buď nízkými dávkami dexametazonu (0,5 mg denně), ale stejně úspěšně i nízkými dávkami spironolaktonu [21].
Závěr
PH je nejčastější potenciálně vyléčitelnou formou sekundární hypertenze spojenou se zvýšeným kardiovaskulárním rizikem. Vzhledem k tomu je nezbytné PH včas diagnostikovat, přesně stanovit podtyp a rozhodnout o specifické terapii. Vzhledem ke složitosti diagnostického procesu by pacienti s podezřením na PH měli být vyšetřováni pouze ve specializovaných centrech.
Práce byla podpořena Programem rozvoje vědních oblastí na Univerzitě Karlově – PRVOUK P35/ LF1/ 5.
Práce byla podpořena výzkumným grantem NT14155 - 3/ 2013 IGA Ministerstva zdravotnictví České republiky.
Doručeno do redakce: 18. 3. 2015
Přijato po recenzi: 10. 4. 2015
MU Dr. Branislav Štrauch, Ph.D.
www.vfn.cz
branislav.strauch@vfn.cz
Sources
1. Conn JW. Part I. Painting background. Part II. Primary aldosteronism, a new clinical syndrome, 1954. J Lab Clin Med 1990; 116 : 253 – 267.
2. Rossi GP, Bernini G, Caliumi C et al. A prospective study of the prevalence of primary aldosteronism in 1,125 hypertensive patients. J Am Coll Cardiol 2006; 48 : 2293 – 2300. doi: 10.1016/ j.jacc.2006.07.059.
3. Strauch B, Zelinka T, Hampf M et al. Prevalence of primary hyperaldosteronism in moderate to severe hypertension in the Central Europe region. J Hum Hypertens 2003; 17 : 349 – 352. doi: 10.1038/ sj.jhh.1001554.
4. Carss KJ, Stowasser M, Gordon RD et al. Further study of chromosome 7p22 to identify the molecular basis of familial hyperaldosteronism type II. J Hum Hypertens 2011; 25 : 560 – 564. doi: 10.1038/ jhh.2010.93.
5. Zelinka T, Strauch B, Pecen L et al. Diurnal blood pressure variation in pheochromocytoma, primary aldosteronism and Cushing's syndrome. J Hum Hypertens 2004; 18 : 107 – 111. doi: 10.1038/ sj.jhh.1001644
6. Zelinka T, Holaj R, Petrak O et al. Life ‑ threatening arrhythmia caused by primary aldosteronism. Med Sci Monit 2009; 15: CS174 – CS177.
7. Mulatero P, Stowasser M, Loh KC et al. Increased diagnosis of primary aldosteronism, including surgically correctable forms, in centers from five continents. J Clin Endocrinol Metab 2004; 89 : 1045 – 1050. doi: 10.1210/ jc.2003 ‑ 031337.
8. Stehr CB, Mellado R, Ocaranza MP et al. Increased levels of oxidative stress, subclinical inflammation, and myocardial fibrosis markers in primary aldosteronism patients. J Hypertens 2010; 28 : 2120 – 2126. doi: 10.1097/ HJH.0b013e32833d0177.
9. Rizzoni D, Paiardi S, Rodella L et al. Changes in extracellular matrix in subcutaneous small resistance arteries of patients with primary aldosteronism. J Clin Endocrinol Metab 2006; 91 : 2638 – 2642. doi: 10.1210/ jc.2006 ‑ 0101.
10. Holaj R, Zelinka T, Wichterle D et al. Increased intima ‑ media thickness of the common carotid artery in primary aldosteronism in comparison with essential hypertension. J Hypertens 2007; 25 : 1451 – 1457. doi: 10.1097/ HJH.0b013e3281268532.
11. Holaj R, Rosa J, Zelinka T et al. Long‑term effect of specific treatment of primary aldosteronism on carotid intima ‑ media thickness. J Hypertens 2014; 33 : 874 – 882. doi: 10.1097/ HJH.0000000000000464.
12. Strauch B, Petrak O, Wichterle D et al. Increased arterial wall stiffness in primary aldosteronism in comparison with essential hypertension. Am J Hypertens 2006; 19 : 909 – 914. doi: 10.1016/ j.amjhyper.2006.02.002.
13. Strauch B, Petrak O, Zelinka T et al. Adrenalectomy improves arterial stiffness in primary aldosteronism. Am J Hypertens 2008; 21 : 1086 – 1092. doi: 10.1038/ ajh.2008.243.
14. Tsioufis C, Tsiachris D, Dimitriadis K et al. Myocardial and aortic stiffening in the early course of primary aldosteronism. Clin Cardiol 2008; 31 : 431 – 436. doi: 10.1002/ clc.20270.
15. Catena C, Colussi G, Lapenna R et al. Long‑term cardiac effects of adrenalectomy or mineralocorticoid antagonists in patients with primary aldosteronism. Hypertension 2007; 50 : 911 – 918. doi: 10.1161/ HYPERTENSIONAHA.107.095448.
16. Indra T, Holaj R, Strauch B et al. Long‑term effects of adrenalectomy or spironolactone on blood pressure control and regression of left ventricle hypertrophy in patients with primary aldosteronism. J Renin Angiotensin Aldosterone Syst 2014. In press. doi: 10.1177/ 1470320314549220.
17. Savard S, Amar L, Plouin PF et al. Cardiovascular complications associated with primary aldosteronism: a controlled cross ‑ sectional study. Hypertension 2013; 62 : 331 – 336. doi: 10.1161/ HYPERTENSIONAHA.113.01060.
18. Sindelka G, Widimsky J, Haas T et al. Insulin action in primary hyperaldosteronism before and after surgical or pharmacological treatment. Exp Clin Endocrinol Diabetes 2000; 108 : 21 – 25.
19. Catena C, Lapenna R, Baroselli S et al. Insulin sensitivity in patients with primary aldosteronism: a follow‑up study. J Clin Endocrinol Metab 2006; 91 : 3457 – 3463. doi: 10.1210/ jc.2006 ‑ 0736.
20. Strauch B, Widimsky J, Sindelka G et al. Does the treatment of primary hyperaldosteronism influence glucose tolerance? Physiol Res 2003; 52 : 503 – 506.
21. Funder JW, Carey RM, Fardella C et al. Case detection, diagnosis, and treatment of patients with primary aldosteronism: an endocrine society clinical practice guideline. J Clin Endocrinol Metab 2008; 93 : 3266 – 3281. doi: 10.1210/ jc.2008 ‑ 0104.
22. Ahmed AH, Gordon RD, Taylor PJ et al. Effect of contraceptives on aldosterone/ renin ratio may vary according to the components of contraceptive, renin assay method, and possibly route of administration. J Clin Endocrinol Metab 2011; 96 : 1797 – 1804. doi: 10.1210/ jc.2010 ‑ 2918.
23. Ahmed AH, Calvird M, Gordon RD et al. Effects of two selective serotonin reuptake inhibitor antidepressants, sertraline and escitalopram, on aldosterone/ renin ratio in normotensive depressed male patients. J Clin Endocrinol Metab 2011; 96 : 1039 – 1045. doi: 10.1210/ jc.2010 ‑ 2603.
24. Ahmed AH, Cowley D, Wolley M et al. Seated saline suppression testing for the diagnosis of primary aldosteronism: a preliminary study. J Clin Endocrinol Metab 2014; 99 : 2745 – 2753. doi: 10.1210/ jc.2014 ‑ 1153.
25. Young WF, Stanson AW, Thompson GB et al. Role for adrenal venous sampling in primary aldosteronism. Surgery 2004; 136 : 1227 – 1235. doi: 10.1016/ j.surg.2004.06.051.
26. Rossi GP, Auchus RJ, Brown M et al. An expert consensus statement on use of adrenal vein sampling for the subtyping of primary aldosteronism. Hypertension 2014; 63 : 151 – 160. doi: 10.1161/ HYPERTENSIONAHA.113.02097.
27. Mattsson C, Young WF Jr. Primary aldosteronism: diagnostic and treatment strategies. Nat Clin Pract Nephrol 2006; 2 : 198 – 208. doi: 10.1038/ ncpneph0151.
28. Citton M, Viel G, Rossi GP et al. Outcome of surgical treatment of primary aldosteronism. Langenbeck's Arch Surg 2015; 400 : 325 – 331. doi: 10.1007/ s00423 ‑ 014 ‑ 1269 ‑ 4.
29. Parthasarathy HK, Menard J, White WB et al. A double‑blind, randomized study comparing the antihypertensive effect of eplerenone and spironolactone in patients with hypertension and evidence of primary aldosteronism. J Hypertens 2011; 29 : 980 – 990. doi: 10.1097/ HJH.0b013e3283455ca5.
Labels
Paediatric cardiology Internal medicine Cardiac surgery CardiologyArticle was published in
Cardiology Review

2015 Issue 2
-
All articles in this issue
- Náhlá srdeční smrt
- Skórovací systémy preventivní kardiologie
- Skórovací systémy u pacientů s akutním koronárním syndromem
- Skórovací systémy u fibrilace síní
- Skórovací systémy u tromboembolické nemoci
- Klinické klasifikace a skórovací systémy u srdečního selhání
- Role echokardiografie v hodnocení aortální stenózy a mitrální regurgitace
- Přímé versus nepřímé metody stanovení intenzity zatížení v kardiovaskulární rehabilitaci
- Skórovací systémy před kardiochirurgickou operací
- Primární hyperaldosteronizmus – nejčastější forma sekundární hypertenze
- Cushingův syndrom a kardiovaskulární riziko
- Saturace jodem v České republice a ve světě – nedostatky a perspektivy
- Akutní stavy v tyreologii
- Diferenciální diagnostika hyponatremie
- Endokrinologie stárnutí – krátký přehled
- Cardiology Review
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Klinické klasifikace a skórovací systémy u srdečního selhání
- Skórovací systémy u tromboembolické nemoci
- Diferenciální diagnostika hyponatremie
- Akutní stavy v tyreologii
