Fingolimod v reálné klinické praxi
Fingolimod in Real Clinical Practice
Aim:
To assess retrospectively the clinical efficacy of fingolimod in one or two years of treatment in patients with active multiple sclerosis.
Patients and methods:
223 patients were treated with fingolimod for at least one year, 109 of whom were treated for two years. 126 patients were switched to fingolimod from interferon beta or glatiramer acetate, 3 patients were treatment-naive and 94 patients were switched from natalizumab.
Results:
In patients switched from IFN beta or GA, the relapse rate decreased by 72% in the first year and by 64% in the first 2 years, in patients switched from natalizumab the decrease was 25% in the first year and 31% during 2 years of treatment. 66% of patients in the overall group and in both subgroups remained relapse-free during the first year of treatment and 50.5% over the 2 years of fingolimod treatment. 80% of patients had stable or improved EDSS in the first year and also after 2 years of treatment. 94.6% of patients did not have a 6-months confirmed disability progression within one or 2-year observational period. No evidence of clinical activity of the disease was observed in 64.6% of patients in the first year and in 50% of patients after the first 2 years of treatment. 16.7% of patients with the washout period of 63 days or less after the last infusion of natalizumab relapsed, while the washout period longer than 63 days led to a relapse in 25% of patients.
Conclusion:
Fingolimod is an effective escalation treatment in patients failing on DMDs or as the first line treatment in patients with high activity of MS. After termination of natalizumab treatment, fingolimod is an effective alternative for the majority of patients.
Key words:
multiple sclerosis – fingolimod – natalizumab – escalation
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Chinese summary - 摘要
芬戈莫德在临床中的实际应用目标:
回顾性评估芬戈莫德在一年或两年治疗活动性多发性硬化症(MS)患者中的临床疗效。
患者和方法:
223名患者用芬戈莫德治疗至少一年,其中109例接受治疗两年。 126名患者从干扰素β(IFN)或醋酸格拉默(GA)转为芬戈莫德,3名患者为无创性治疗,94名患者从那他珠单抗切换。
结果:
在从IFNβ或GA转换的患者中,第一年的复发率下降了72%,前2年的复发率下降了64%,从那他珠单抗转移的患者第一年下降了25%,2年内治疗下降了31%。整个组和两亚组66%的患者在治疗的第一年仍无复发,而在芬戈莫德治疗的2年中仍为50.5%。 80%的患者在第一年和治疗2年后均有稳定或改善的EDSS。 94.6%的患者在一年或两年观察期内没有6个月确诊的残疾进展。在第一年64.6%的患者和治疗前2年的50%患者中没有观察到该疾病的临床活动证据。最后一次输注natalizumab后,16.7%的清除期为63天或更少的患者复发,而超过63天的清除期导致25%的患者复发。
结论:
芬戈莫德是一种有效的升级治疗,在DMD患者失败或作为MS高活动度患者的第一线治疗。在那他珠单抗治疗终止后,芬戈莫德是大多数患者的有效选择。
关键词:
多发性硬化 - 芬戈莫德 - 那他珠单抗 - 升级
Authors:
V. Tichá 1; L. Sobíšek 2; E. Havrdová 1
Authors‘ workplace:
Neurologická klinika a Centrum klinických neurověd, 1. LF UK a VFN v Praze
1; Fakulta informatiky a statistiky, VŠE v Praze
2
Published in:
Cesk Slov Neurol N 2017; 80/113(2): 213-219
Category:
Short Communication
doi:
https://doi.org/10.14735/amcsnn2017213
Overview
Cíl:
Retrospektivní zhodnocení klinické účinnosti fingolimodu v prvním a druhém roce léčby u pacientů s aktivní roztroušenou sklerózou.
Soubor a metodika:
Jeden rok bylo léčeno 223 pacientů a 109 z nich dva roky fingolimodem. Na fingolimod bylo převedeno 126 pacientů z interferonu beta nebo glatiramer acetátu, 3 pacienti nebyli dosud léčeni a 94 pacientů bylo převedeno z natalizumabu.
Výsledky:
Četnost relapsů poklesla ve skupině pacientů převedených z interferonu beta nebo glatiramer acetátu o 72 % během prvního roku a o 64 % během prvních 2 let a ve skupině převedené z natalizumabu o 25 % v prvním roce a o 31 % během prvních 2 let. První rok léčby nemělo žádný relaps 66 % pacientů, během 2 let léčby bylo bez relapsu 50,5 % pacientů. Stabilní nebo zlepšené EDSS mělo v obou podskupinách během 1 i 2 let léčby 80 % pacientů. Potvrzenou šestiměsíční progresi EDSS nemělo 94,6 % pacientů z celé skupiny a bez známek klinické aktivity nemoci bylo v prvním roce 64,6 % a prvních 2 letech 50 % pacientů. Při wash-out periodě kratší než 63 dnů po ukončení natalizumabu se vyskytl relaps v prvních 6 měsících u 16,7 % pacientů a při wash-out periodě delší než 63 dnů u 25 % pacientů.
Závěr:
Fingolimod je účinný pro eskalaci léčby u pacientů selhávajících na Disease Modifying Drug nebo jako lék první volby u pacientů s vysokou aktivitou nemoci. Ve většině případů je účinnou alternativou léčby pro ty pacienty, kteří ukončí léčbu natalizumabem.
Klíčová slova:
roztroušená skleróza – fingolimod – natalizumab – eskalace
Úvod
Fingolimod je perorální lék schválený v Evropské unii k eskalaci léčby relaps remitentní formy roztroušené sklerózy (RS) u pacientů s přetrvávající aktivitou nemoci při léčbě interferonem beta nebo glatiramer acetátem či jako lék první volby u pacientů s rychle progredující závažnou relaps remitentní formou RS [1]. V České republice byl fingolimod uveden na trh v říjnu 2012. Úhradová kritéria platná v České republice v době, kdy zahajovali pacienti z našeho souboru léčbu fingolimodem, vyžadovala nejméně dvě ataky během roku léčby léky první volby nebo nejméně dvě ataky během 1 roku a známky aktivity anebo progrese na magnetické rezonanci (MR) u dosud neléčených pacientů. Fingolimod je také hrazen zdravotními pojišťovnami v případě intolerance injekční léčby [2].
Mechanizmus účinku fingolimodu je zcela nový. Aktivní metabolit fingolimodu, fingolimod-1-fosfát, působí jako funkční antagonista receptorů pro sfingosin-1-fosfát (S1P) [3], které se vyskytují v pěti podtypech na různých tkáních lidského organizmu, zejména v imunitním a kardiovaskulárním systému a v centrálním nervovém systému (CNS). Navázání fingolimodu na receptory pro S1P vede k jejich rychlé internalizaci a degradaci [4]. Léčebný účinek je zprostředkován především lymfopenií navozenou fingolimodem při selektivním zablokování signálu pro výstup CCR7+ naivních a centrálních paměťových T lymfocytů a B lymfocytů z lymfatických uzlin [5]. Dosud ne zcela jasnou úlohu v klinickém účinku fingolimodu může hrát jeho přímé působení na nervových buňkách CNS a glií, které také exprimují receptor pro S1P [6].
Fingolimod byl registrován na základě výsledků dvou klinických studií, placebem kontrolované studie FREEDOMS [7] a studie TRANSFORMS [8] porovnávající účinky fingolimodu s intramuskulárním interferonem beta. Obě studie prokázaly signifikantní vliv fingolimodu na snížení roční četnosti relapsů a na riziko progrese neurologického postižení. Fingolimod je určen k monoterapii v dávce 0,5 mg denně.
Skríningová vyšetření před zahájením léčby fingolimodem zahrnují krevní obraz s diferenciálním rozpočtem, jaterní testy, vyšetření IgG protilátek proti varicella-zoster viru a sérologické vyšetření k vyloučení aktivní hepatitidy, dále krevní tlak a pulz, EKG a optickou koherenční tomografii (Optical Coherence Tomography; OCT) nebo vyšetření očního pozadí k vyloučení přítomnosti makulárního edému. Vzhledem k vyššímu výskytu bazaliomů během léčby fingolimodem je doporučeno před zahájením léčby a dále jedenkrát ročně kožní vyšetření. První dávka fingolimodu by měla být podána za šestihodinové monitorace EKG ke sledování nově vzniklé arytmie (nejčastěji A-V blok 1. stupně) a pravidelného měření krevního tlaku a pulzu. Během léčby fingolimodem je nutné pravidelně sledovat počet lymfocytů v periferní krvi a jaterní testy. Po 3 měsících léčby je doporučeno provést kontrolní EKG a OCT k vyloučení makulárního edému.
Cílem této práce je retrospektivní zhodnocení klinické účinnosti a bezpečnosti po jednom a dvou letech léčby fingolimodem u pacientů, kteří byli zařazení do této léčby v Centru pro diagnostiku a léčbu demyelinizačních onemocnění 1. LF UK a VFN v Praze.
Soubor a metodika
Do konce června 2014 zahájilo léčbu fingolimodem v našem centru 254 pacientů s klinicky definitivní relaps remitentní RS. Do 30. 6. 2015, kdy byla uzavřena data pro tuto analýzu, jich 29 (11,4 %) léčbu ukončilo. Nejčastějším důvodem byla přetrvávající aktivita RS (16 pacientů), dále přechod do sekundárně progresivní RS (3 pacienti) a plánování gravidity (3 pacientky). Dvě pacientky ukončily léčbu již po první dávce fingolimodu pro přetrvávající bradykardii do druhého dne a jedna pacientka ukončila léčbu pro exacerbaci tachykardií po vysazení betablokátorů před zahájením léčby fingolimodem. Čtyři pacienti léčbu ukončili pro nežádoucí účinky – těžkou komplikovanou migrénu, zhoršení psoriázy, otoky a exantém na dolních končetinách a recidivující herpes simplex. U žádného pacienta nebyla léčba během sledovaného období ukončena z důvodů gastrointestinální intolerance, hepatopatie nebo těžké lymfopenie.
Do retrospektivní analýzy bylo zařazeno 223 pacientů, u kterých byla dostupná jednoletá data sledování po zahájení léčby fingolimodem. U 109 z nich byla dostupná dvouletá data. Nezařadili jsme pacienty, kteří ukončili léčbu dříve než po 3 měsících, a pacienty, kteří byli dříve léčeni fingolimodem v placebem kontrolované klinické studii. Zdrojem klinických dat byla databáze iMED (www.imed.org), do které jsou pravidelně zadávána strukturovaná data získaná z běžné klinické dokumentace.
Byly hodnoceny tyto klinické parametry: aktivita RS pomocí roční četnosti relapsů a míra neurologického postižení podle Kurtzkeho škály EDSS (Expanded Disability Status Scale) ve tříměsíčních intervalech. Oba parametry byly hodnoceny v posledních 2 letech před zahájením léčby fingolimodem a v prvním, resp. prvním a druhém roce léčby fingolimodem. Dále jsme hodnotili počet pacientů s šestiměsíční potvrzenou progresí v EDSS a počet pacientů bez známek klinické aktivity RS (bez relapsu a bez progrese v EDSS) během léčby fingolimodem.
U skupiny pacientů převedených z natalizumabu na fingolimod jsme hodnotili počet pacientů bez relapsu a celkový počet relapsů během 6 a 12 měsíců po poslední infuzi natalizumabu. Tyto dva parametry jsme také porovnávali u skupiny pacientů s wash-out periodou mezi poslední infuzí natalizumabu a zahájením léčby fingolimodem kratší než 63 dnů (42 pacientů) a wash-out periodou 63 a více dnů (52 pacientů).
Statistická analýza
Změna četnosti relapsů v celé skupině pacientů, ve skupině pacientů léčených léky měnící průběh nemoci (Disease Modifying Drug; DMD) a ve skupině léčených původně natalizumabem byla sledována 2 roky před nasazením léčby fingolimodem a 2 roky během něho. Byla porovnána průměrná četnost relapsů v období 1 rok před nasazením léčby s obdobím 1 rok po něm. Dále byla porovnána četnost relapsů v období 2 let před nasazením léčby s obdobím 2 let po něm. Statistická signifikance absolutní změny průměrné četnosti výskytu byla testována pomocí jednovýběrového t-testu o střední hodnotě, kde testovaná hypotéza (H0) byla stanovena jako průměrná absolutní diference = 0 a jednostranná alternativní hypotéza (H1) jako průměrná absolutní diference < 0. Riziko relapsu po ukončení léčby natalizumabem v závislosti na délce wash-out periody bylo testováno chí kvadrát testem nezávislosti v kontingenční tabulce. Všechny statistické testy hypotéz byly vyhodnoceny na 5% hladině významnosti. Příprava dat a statistické výpočty byly provedeny ve statistickém systému R (www.r-project.org). Tabulky a grafy byly připraveny v tabulkovém procesoru MS Excel 2010.
Výsledky
Soubor pacientů
Náš soubor tvoří 149 (67 %) žen a 74 (33 %) mužů průměrného věku 38,5 let a trvání RS v průměru 12,4 roku (tab. 1). Průměrné EDSS ve chvíli zahájení léčby fingolimodem bylo 3,3 a průměrná četnost relapsů v posledním roce před zahájením léčby fingolimodem byla 1,2 relapsu za rok. Soubor našich pacientů byl fakticky tvořen dvěma populacemi pacientů, které se lišily jednak v typu léčby, kterou měli pacienti před přestupem na fingolimod, jednak v některých vstupních parametrech. Proto jsme klinické parametry účinnosti léčby fingolimodem hodnotili pro každou skupinu zvlášť. První skupinu tvoří 94 pacientů léčených původně natalizumabem, kteří změnili léčbu především pro vysoké riziko progresivní multifokální leukoencefalopatie. Do druhé skupiny bylo zahrnuto 126 pacientů léčených interferonem beta nebo glatiramer acetátem, kteří naplnili kritéria eskalace na léčbu fingolimodem, a tři pacienti dosud neléčení, kteří splnili kritéria úhrady fingolimodu jako léku první volby. Pacienti převedení na fingolimod z natalizumabu byli až na výjimky dobře stabilizováni na natalizumabu, jejich četnost relapsů v posledním roce před změnou léčby byla nízká (0,54). Tito pacienti měli také vyšší vstupní hodnotu EDSS (3,5), delší trvání choroby a vyšší věk. Naopak pacienti léčení DMD nebo dosud neléčení měli vysokou aktivitou nemoci – jejich četnost relapsů v posledním roce před zahájením léčby fingolimodem byla 1,64. Tato skupina pacientů měla v průměru nižší vstupní EDSS (3,1), nižší věk a kratší trvání RS.
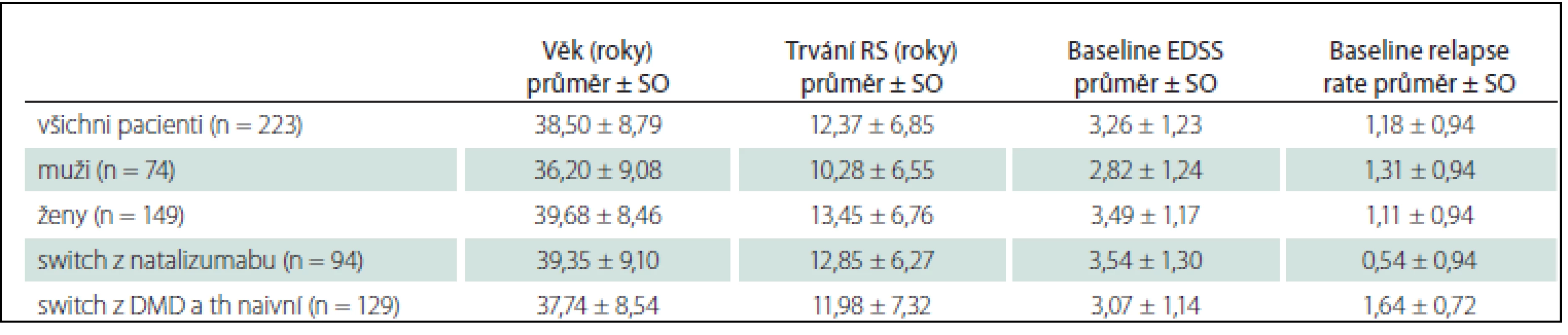
Průměrná doba léčby natalizumabem před zahájením léčby fingolimodem byla 822 dnů a průměrná délka wash-out periody po poslední infuzi natalizumabu do zahájení léčby fingolimodem byla 64,7 dnů.
Změna četnosti relapsů
V prvním roce léčby fingolimodem poklesla v celé skupině pacientů četnost relapsů o 63 % z 1,18 na 0,43 relapsu za rok oproti poslednímu roku na předchozí terapii (tab. 2). Ve skupině pacientů léčených DMD nebo dosud neléčených se snížila četnost relapsů o 72 % z 1,64 na 0,46 relapsu za rok. Obě tyto změny jsou vysoce statisticky významné. Ve skupině pacientů léčených původně natalizumabem poklesla roční četnost relapsů o 25 %. Při hodnocení skupiny pacientů s dvouletými daty jsme zjistili, že za první 2 roky léčby fingolimodem poklesla četnost relapsů z 1,79 relapsu za 2 roky na 0,96, tedy o 54 % ve srovnání s posledními 2 roky na původní léčbě. Pacientům léčeným DMD nebo neléčeným se snížila četnost relapsů o 64 % z 2,44 na 0,87 relapsů za 2 roky. Obě tyto změny jsou opět statisticky významné. I ve skupině léčené natalizumabem se snížila četnost relapsů z 1,15 za poslední 2 roky na 0,78, tedy o 31 %. Graf 1 ukazuje četnost relapsů v předposledním a posledním roce před změnou léčby na fingolimod a v prvním, resp. druhém roce na léčbě fingolimodem u celé sledované skupiny i zvlášť pro pacienty původně léčené DMD nebo neléčené a léčené natalizumabem.
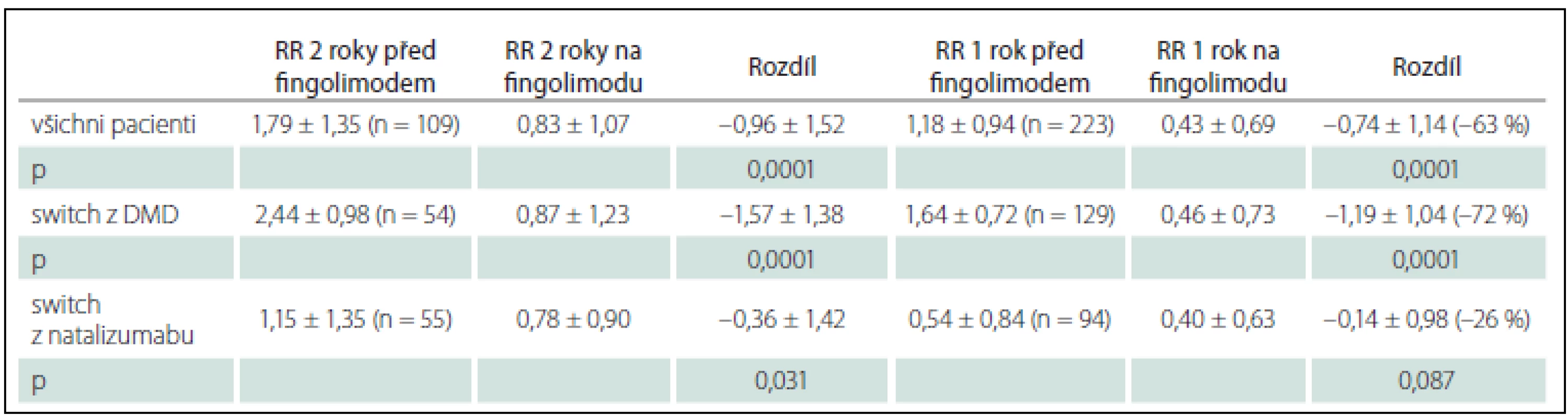

Počet relapsů v prvním roce a 2 letech léčby fingolimodem
Během prvního roku léčby neprodělalo 148 pacientů (66,4 %) žádný relaps (graf 2, tab. 3). Ve skupině léčené původně natalizumabem to bylo 62 pacientů (66 %) a ve skupině léčené původně DMD nebo neléčené 86 pacientů (66,7 %). Dva a více relapsů mělo 19 pacientů (8,5 %) z celého souboru.

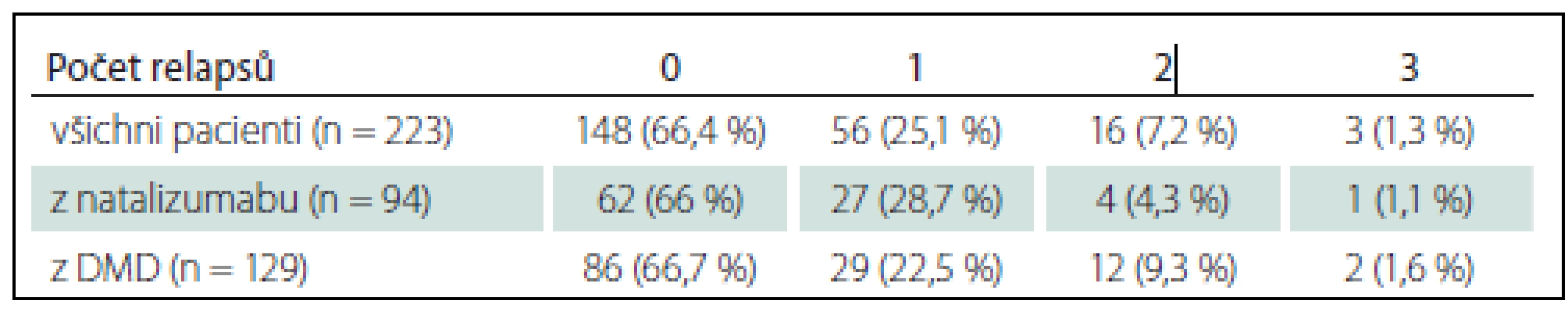
Během 2 let léčby fingolimodem neprodělalo žádný relaps 55 pacientů (50,5 %) ze 109 hodnocených, z 55 pacientů převedených z natalizumabu bylo po 2 roky bez relapsu 24 (43,6 %) a z 54 pacientů převedených z DMD nebo neléčených nemělo relaps 31 (57,4 %). Dva a více relapsů prodělalo 21 pacientů (19,5 %) z celého souboru (graf 3, tab. 4).

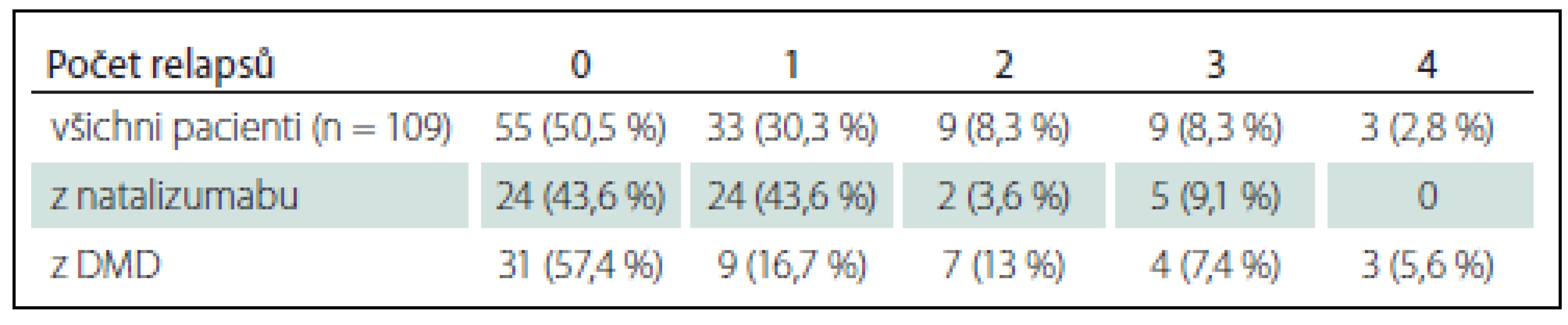
Progrese neurologického postižení
U celé skupiny 223 pacientů došlo během posledních 2 let před zahájením léčby fingolimodem ke zhoršení EDSS v průměru o 0,29 bodu, přičemž výraznější nárůst byl ve skupině pacientů léčených DMD nebo neléčených – o 0,39 bodu, ve skupině léčených natalizumabem byl nárůst 0,21 bodu EDSS škály (graf 4). V celé skupině i v obou podskupinách byl nárůst EDSS rychlejší v posledním roce před převedením na fingolimod ve srovnání s předposledním rokem. V prvním roce léčby fingolimodem se zhoršilo EDSS u celé skupiny o 0,09 bodu, v obou podskupinách srovnatelně. Během prvního roku léčby fingolimodem mělo zlepšené nebo stabilní EDSS 79,1 % pacientů ve skupině převedených z DMD nebo neléčených a 83 % pacientů původně léčených natalizumabem (tab. 5). Hodnocení skupiny pacientů s dostupnými dvouletými daty ukázalo, že zlepšené nebo stabilní EDSS mělo v prvních 2 letech léčby fingolimodem 82,4 % pacientů původně léčených DMD a neléčených a 80,4 % převedených z natalizumabu (tab. 6).



Konfirmovaná šestiměsíční progrese EDSS a pacienti bez klinické aktivity nemoci
Z celé hodnocené skupiny nemělo 211 pacientů (94,6 %) během sledovaného období 1 nebo 2 let léčby fingolimodem potvrzenou šestiměsíční progresi EDSS. Nebyl zjištěn statisticky významný rozdíl mezi oběma podskupinami pacientů podle původní léčby (p = 0,978). Bez známek klinické aktivity RS, tedy bez relapsu a bez progrese v EDSS, bylo v prvním roce 144 (64,6 %) z 223 pacientů a během 2 let léčby fingolimodem 55 (50 %) ze 109 pacientů.
Riziko relapsu po ukončení léčby natalizumabem v závislosti na délce wash-out periody
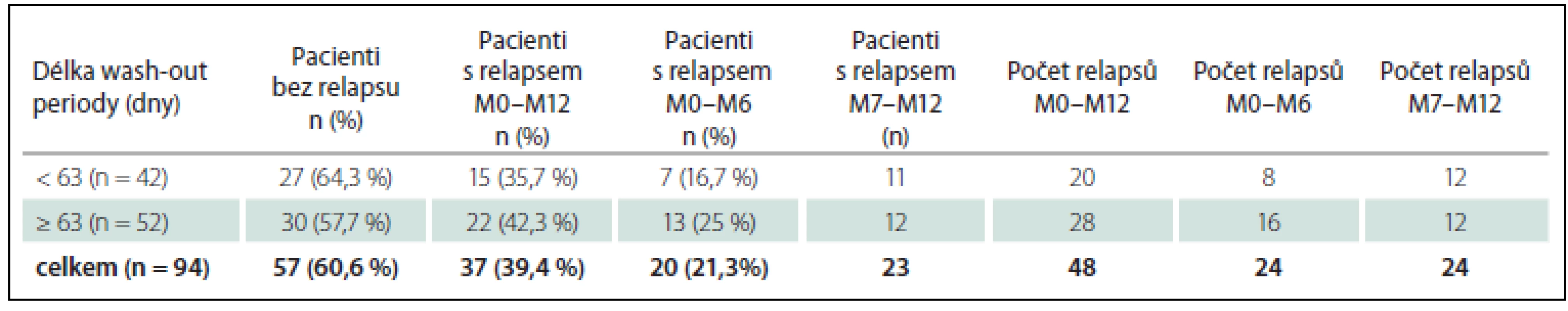
Z 94 pacientů převedených z natalizumabu neprodělalo relaps během prvních 12 měsíců od ukončení léčby natalizumabem 57 pacientů (60,6 %) (tab. 7). Ve skupině pacientů s wash-out periodou kratší než 63 dnů to bylo 27 (64,3%) a ve skupině s wash-out periodou 63 dnů a delší nemělo relaps 30 pacientů (57,7%). Během prvních 6 měsíců po ukončení léčby natalizumabem se vyskytlo v celé skupině celkem 24 relapsů u 20 pacientů (21,3 %), z toho osm relapsů u 7 (16,7 %) pacientů s wash-out periodou kratší než 63 dnů a 16 relapsů u 13 pacientů (25 %) s wash-out periodou 63 dnů a delší.
Diskuze
Klinická účinnost fingolimodu u pacientů s aktivní RS byla ověřena ve dvou dvojitě slepých studiích [7,8]. Obě klinické studie prokázaly schopnost fingolimodu významně snížit četnost relapsů a riziko progrese neurologického postižení oproti placebu a intramuskulárnímu interferonu beta 1a. Účinnost fingolimodu v reálné klinické praxi ukázaly také post marketingové studie [9,10].
Četnost relapsů v prvním roce léčby fingolimodem klesla v celé naší skupině o 63 %, z toho ve skupině pacientů převedených z DMD nebo dosud neléčených o 72 %. Tyto hodnoty jsou ve shodě s výsledky publikovaných sledování z reálné klinické praxe [9,11,12]. Stejně tak i počet pacientů bez relapsu za první rok léčby fingolimodem (66,7 %) se v naší skupině pacientů převedených z DMD nebo neléčených shodoval se zkušenostmi v publikovaných pracích [9,11]. Podíl pacientů s potvrzenou šestiměsíční progresí v EDSS po 12 měsících byl v naší skupině velmi podobný výsledkům německé studie (5,4 vs. 7,2 %) [9].
Ve srovnání s dalšími pracemi, které hodnotí účinnost fingolimodu v reální klinické praxi [11,12], bylo v naší skupině po prvním roce léčby nižší procento pacientů bez progrese neurologického postižení (téměř 90 vs. 79 %) a v průměru došlo v naší skupině ke zhoršení v EDSS o 0,08 bodu, zatímco citované práce uvádějí zlepšení EDSS o 0,07 – 0,5 bodu. Důvodem dosažení lepšího klinického efektu na progresi neurologického postižení může být zahájení léčby fingolimodem v časnějším stadiu nemoci – pacienti zařazení do těchto studií měli oproti naší skupině nižší vstupní EDSS (2,4 a 2,5 oproti 3,26 v naší skupině) a kratší trvání nemoci (10,3 vs. 12,4 let u našich pacientů). Navíc byli tito pacienti zařazováni na základě indikačních kritérií EMA, která umožňují eskalaci na fingolimod již po jedné atace na léčbě léky první volby, zatímco naši pacienti mohli podle indikačních kritérií platných tehdy v České republice zahájit léčbu fingolimodem až po dvou atakách.
Účinnosti fingolimodu po převedení z léčby natalizumabem a riziku relapsu během wash-out periody se věnovalo několik studií z reálné klinické praxe, jejichž výsledky jsou rozporuplné. Některé práce uvádějí relaps po ukončení léčby natalizumabem u 40 – 60 % pacientů [13 – 15]. Jiné práce zaznamenaly podstatně nižší procento relabujících pacientů – během wash-out periody mělo relaps 27 % a v průběhu 6, resp. 9 měsíců po zahájení léčby fingolimodem prodělalo relaps 20 % [16,17]. V naší skupině 94 pacientů převedených z natalizumabu na fingolimod prodělalo v prvních 12 měsících léčby relaps 34 % pacientů, průměrná roční četnost relapsů poklesla během prvního roku léčby fingolimodem z 0,54 na 0,40.
Riziko relapsu po vysazení natalizumabu je závislé podle některých prací na délce wash-out periody, přičemž za rizikovou je považována wash-out perioda delší než 2, resp. 3 měsíce [17 – 20]. Skupina našich pacientů převedených z natalizumabu na fingolimod měla průměrnou délku wash-out periody 64,7 dnů. Výsledky v našem souboru ukazují, že zkrácení wash-out periody na maximálně 2 měsíce vedlo k nižšímu riziku relapsu v prvních 6 a 12 měsících po ukončení léčby natalizumabem (relaps prodělalo 16,7 % a 37,5 % pacientů s wash-out periodou kratší než 63 dnů vs. 25 % a 42,3 % pacientů s wash-out periodou delší než 63 dnů).
Nová indikační kritéria pro léčbu fingolimodem platná v České republice od 1. 6. 2016 již umožňují převést pacienta po jedné středně těžké nebo těžké atace na lécích první volby na fingolimod a zahájit tak účinnější léčbu v časnějším stadiu nemoci s předpokladem lepšího klinického účinku. Ačkoliv byly v našem souboru pacientů a ve shodě s jinými pracemi dvě třetiny pacientů po roce a více než polovina pacientů po 2 letech léčby fingolimodem bez relapsu, stále jsme pozorovali u 10,9 % pacientů během prvního roku a u 26 % pacientů během dvou letech léčby fingolimodem 2 a více relapsů. Tito pacienti mohou být převedeni na léky s vyšší účinností, ale i s vyššími bezpečnostními riziky léčby, jako je natalizumab nebo alemtuzumab (a v budoucnu ocrelizumab).
Všichni pacienti zařazení do našeho souboru měli v rámci doporučeného sledování nežádoucích účinků léčby pravidelně kontrolované hladiny lymfocytů, jaterní testy, krevní tlak a OCT a v úvodu léčby také EKG. Dále byli všichni pacienti vyšetřeni před zahájením léčby, po 6 měsících a dále jedenkrát ročně MR mozku. Výsledky sledování bezpečnosti léčby a vývoj MR parametrů účinnosti léčby fingolimodem budou předmětem samostatných publikací.
Závěr
Léčba fingolimodem u pacientů nedostatečně stabilizovaných na léčbě DMD nebo dosud neléčených vedla k významnému snížení aktivity nemoci během prvního roku, resp. dvou let léčby. Po převedení z léčby natalizumabem na fingolimod zůstala aktivita nemoci nízká. U dvou třetin pacientů vedla léčba fingolimodem během prvního roku k úplné klinické stabilizaci, tedy nepřítomnosti relapsů a progrese v EDSS.
Fingolimod je účinný pro eskalaci léčby u pacientů selhávajících na DMD nebo jako lék první volby u pacientů s vysokou aktivitou nemoci a ve většině případů je účinnou alternativou léčby pro pacienty, kteří ukončí léčbu natalizumabem. Včasná eskalace léčby na fingolimod podle současných indikačních kritérií, tedy již po jedné středně těžké nebo těžké atace na lécích první volby, může vést k lepší stabilizaci nebo dokonce zlepšení neurologického postižení u léčených pacientů a zkrácení wash-out periody na maximálně 2 měsíce snižuje riziko relapsu v prvních 6 i 12 měsících po ukončení léčby natalizumabem.
Během dvouletého sledování pacientů léčených fingolimodem se neobjevily žádné nové dosud nepopsané nežádoucí účinky a léčba byla obecně tolerována velmi dobře.
Seznam použitých zkratek
DMD – léky měnící průběh nemoci (Disease Modifying Drug)
EDSS – Expanded Disability Status Scale
EMA – European Medicines Agency
OCT – optická koherenční tomografie
RS – roztroušená skleróza
S1P – sfingosin-1-fosfát
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Veronika Tichá
Neurologická klinika a Centrum klinických neurověd
1. LF UK a VFN v Praze
Kateřinská 30
120 00 Praha 2
e-mail: Veronika.Ticha@vfn.cz
Přijato k recenzi: 10. 10. 2016
Přijato do tisku: 12. 1. 2017
Sources
1. Community register of medicinal products for human use: 18 Product information Gilenya. [accessed 2017 Feb 28]. Dostupné z URL: http://ec.europa.eu/health/documents/community-register/html/h677.htm.
2. SÚKL: Gilenya 0,5mg. [accessed 2017 Feb 28]. Dostupné z URL: http://www.sukl.cz/modules/medication/detail.php?code=0168462&tab=prices.
3. Cohen JA, Chun J. Mechanisms of fingolimod‘s efficacy and adverse effects in multiple sclerosis. Ann Neurol 2011;69(5):759 – 77. doi: 10.1002/ ana.22426.
4. Hla T, Brinkmann V. Sphingosine 1-phosphate (S1P): Physiology and the effects of S1P receptor modulation. Neurology 2011;76(Suppl 3):S3 – 8. doi: 10.1212/ WNL.0b013e31820d5ec1.
5. Singer BA. Fingolimod for the treatment of relapsing multiple sclerosis. Expert Rev Neurother 2013;13(6): 589 – 602. doi: 10.1586/ ern.13.52.
6. Tichá V. Fingolimod v léčbě roztroušené sklerózy. Farmakoterapie 2015;2(Suppl):3 – 41.
7. Kappos L, Radue EW, O‘Connor P, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. N Engl J Med 2010;362(5):387 – 401. doi: 10.1056/ NEJMoa0909494.
8. Cohen JA, Barkhof F, Comi G, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N Engl J Med 2010;362(5):402 – 15. doi: 10.1056/ NEJMoa0907839.
9. Ziemssen T, DiazLorente M, Fuchs A, et al. 24-month interim results of PANGAEA: a 5-year registry study evaluating long-term safety, efficacy and pharmacoeconomic data of German multiple sclerosis patients on fingolimod therapy. Neurology 2014;82(10):152.
10. Baldi E, Guareschi A, Vitetta F, et al. Previous treatment influences fingolimod efficacy in relapsing-remitting multiple sclerosis: results from an observational study. Curr Med Res Opin 2014;30(9):1849 – 55. doi: 10.1185/ 03007995.2014.921144.
11. Correia I, Batista S, Marques IB, et al. The effectiveness of fingolimod in a Portuguese real-world population. Mult Scler Relat Disord 2016;6 : 41 – 8. doi: 10.1016/ j.msard.2016.01.003.
12. Fonseca J. Fingolimod real world experience: efficacy and safety in clinical practice. Neurosci J 2015; 2015 : 389360. doi: 10.1155/ 2015/ 389360.
13. Sempere AP, Martín-Medina P, Berenguer-Ruiz L, et al. Switching from natalizumab to fingolimod: an observational study. Acta Neurol Scand 2013;128(2):e6 – 10. doi: 10.1111/ ane.12082.
14. Hoepner R, Havla J, Eienbröker C, et al. Predictors for multiple sclerosis relapses after switching from natalizumab to fingolimod. Mult Scler 2014;20(13):1714 – 20. doi: 10.1177/ 1352458514533398.
15. Havla J, Tackenberg B, Hellwig K, et al. Fingolimod reduces recurrence of disease activity after natalizumab withdrawal in multiple sclerosis. J Neurol 2013;260(5):1382 – 7. doi: 10.1007/ s00415-012-6808-8.
16. Cohen M, Maillart E, Tourbah A, et al. Switching from natalizumab to fingolimod in multiple sclerosis: a French prospective study. JAMA Neurol 2014;71(4):436 – 41. doi: 10.1001/ jamaneurol.2013.6240.
17. Jokubaitis VG, Li V, Kalincik T, et al. Fingolimod after natalizumab and the risk of short-term relapse. Neurology 2014;82(14):1204 – 11. doi: 10.1212/ WNL.0000000000000283.
18. de Seze J, Ongagna JC, Collongues N, et al. Reduction of the washout time between natalizumab and fingolimod. Mult Scler 2013;19(9):1248. doi: 10.1177/ 1352458513490551.
19. Fragoso YD, Adoni T, Alves-Leon SV, et al. Alternatives for reducing relapse rate when switching from natalizumab to fingolimod in multiple sclerosis. Expert Rev Clin Pharmacol 2016 : 1 – 6. doi: 10.1586/ 17512433.2016.1145053.
20. Kappos L, Radue EW, Comi G, et al. Switching from natalizumab to fingolimod: a randomized, placebo--controlled study in RRMS. Neurology 2015;85(1):29 – 39. doi: 10.1212/ WNL.0000000000001706.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2017 Issue 2
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Hope Awakens with Early Diagnosis of Parkinson's Disease Based on Skin Odor
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Current Insights into the Antispasmodic and Analgesic Effects of Metamizole on the Gastrointestinal Tract
- Metamizole vs. Tramadol in Postoperative Analgesia
-
All articles in this issue
- Loketní nerv
- Nastupující tonus u předčasně narozených dětí jako projev vývoje nervové soustavy a možnosti jeho hodnocení
- Možnosti aktivování plastických a adaptačních procesů v centrálním nervovém systému pomocí fyzioterapie u nemocných s roztroušenou sklerózou mozkomíšní
- Transkraniální magnetická stimulace ve výzkumu kortikální inhibice u depresivní poruchy a schizofrenie, efekt antipsychotik
- Toxické účinky pesticidů
- Role specifické buněčné imunity v patogenezi roztroušené sklerózy se zaměřením na Th17 a Treg lymfocyty
- Incidence cévní mozkové příhody v Evropě – systematická review
- Okulárna myasténia gravis v Slovenskej republike
- Emoční uvědomění u adolescentů – pilotní studie ověřující základní psychometrické vlastnosti české verze Škály úrovně emočního uvědomění pro děti LEAS-C
- Fingolimod v reálné klinické praxi
- „Awake“ resekce gliomu v poloze pacienta v polosedě – kazuistika
- Anti-NMDAR encefalitida v dětském věku – kazuistika
- Febrilní křeče – doporučený postup pro vyšetření dítěte s nekomplikovanými febrilními křečemi, adaptovaný doporučený postup American Academy of Pediatrics
- Doporučení pro diagnostiku a léčbu symptomů dolních močových cest u pacientů s roztroušenou sklerózou v České republice – mezioborový konsenzus expertů dle metodiky DELPHI
- Přesnost uložení elektrod pro hlubokou mozkovou stimulaci pomocí bezrámového systému NexFrame©
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Loketní nerv
- Incidence cévní mozkové příhody v Evropě – systematická review
- Anti-NMDAR encefalitida v dětském věku – kazuistika
- Febrilní křeče – doporučený postup pro vyšetření dítěte s nekomplikovanými febrilními křečemi, adaptovaný doporučený postup American Academy of Pediatrics
