Využití optické koherenční tomografie u neuromyelitis optica a onemocnění jejího širšího spektra
The use of optical coherence tomography in neuromyelitis optica spectrum disorders
Optical coherence tomography (OCT) is an imaging technique that allows repeated non-invasive assessment of retinal layers. The report summarizes the use of OCT in the diagnostics of optic neuritis (ON) as one of the main characteristics of neuromyelitis optica spectrum disorder (NMOSD). ON in NMOSD leads to widespread destruction of ganglion cells and their fibers across the retina, resulting in a thinning of retinal nerve fiber layer (RNFL) in all peripapillary segments, as well as in a thinning of ganglion cell layer in macula. Unlike in NMOSD, ON in MS results in a predominant thinning of peripapillary RNFL in temporal segment. OCT helps differentiation between ON in the context of MS and NMOSD and thus contributes to early diagnosis of MS and NMOSD.
Keywords:
optical coherence tomography – neuromyelitis optica spectrum disorders
Authors:
J. Lízrová Preiningerová
Authors‘ workplace:
Neurologická klinika a Centrum klinických neurověd, 1. LF UK a VFN v Praze
Published in:
Cesk Slov Neurol N 2020; 83/116(supplementum 1): 37-43
doi:
https://doi.org/10.14735/amcsnn2020S37
Overview
Optická koherenční tomografie (optical coherence tomography; OCT) je zobrazovací metoda, která umožňuje opakované neinvazivní detailní zobrazení vrstev sítnice. Článek popisuje použití OCT v diagnostice zánětu očního nervu (ON) jako jednoho z hlavních znaků neuromyelitis optica a poruch jejího širšího spektra (NMOSD). U NMOSD dochází při ON k destrukci gangliových buněk a jejich vláken v celé ploše sítnice, a proto na OCT pozorujeme snížení vrstvy retinálních nervových vláken (RNFL) ve všech peripapilárních segmentech i v makule a snížení vrstvy gangliových buněk v makule. Tento vzorec postižení je odlišný od nálezu po ON u RS, kde dochází ke snížení peripapilární vrstvy RNFL zvláště v temporálním kvadrantu. Vyšetření OCT nám pomáhá odlišit ON u RS a NMOSD a přispívá tak ke správné časné diagnóze těchto nemocí.
Klíčová slova:
optická koherenční tomografie – neuromyelitis optica a onemocnění jejího širšího spektra
Úvod
Optická koherenční tomografie (optical coherence tomography; OCT) je neinvazivní zobrazovací metoda, která na základě analýzy infračerveného paprsku odraženého od vrstev tkáně umožňuje detailní zobrazení vrstev sítnice. Tento článek popisuje použití optické koherenční tomografie v diagnostice zánětu očního nervu (optická neuritida; ON) u neuromyelitis optica a poruch jejího širšího spektra (neuromyelitis optica spectrum disorder; NMOSD) a shrnuje současné poznatky o nálezech na sítnici u NMOSD.
Neuromyelitis optica (NMO) byla po dlouhou dobu považována za agresivní formu RS. Objev patogenních protilátek proti akvaporinu-4 (AQP4-IgG) byl prvním krokem k definici NMO jako samostatného onemocnění, u něhož je autoimunitní reakce namířena proti membránám bohatým na akvaporin-4 (AQP4). Autoprotilátky proti AQP4 jsou detekovatelné u 50–80 % pacientů (v závislosti na kohortě a použité metodě stanovení protilátek) splňujících klinická kritéria NMO, resp. NMOSD [1,2]. U části AQP4-IgG séronegativních pacientů splňujících kritéria NMOSD byly kolem roku 2014 detekovány autoprotilátky proti myelinovému oligodendrocytárnímu glykoproteinu (MOG-IgG), které se naopak u pacientů s přítomností AQP4-IgG prakticky nevyskytují [3,4]. U nemocí charakterizovaných přítomností MOG-IgG je autoimunitní reakce namířena proti antigenu na povrchu myelinu (nikoliv proti astrocytům a Müllerovým buňkám). Ačkoliv se mohou klinické příznaky nemocí s přítomností MOG-IgG velmi podobat příznakům AQP4-IgGpozNMOSD, jde patofyziologicky o jiný proces a diagnóza nemocí asociovaných s MOG-IgG se proto od NMOSD začíná v literatuře oddělovat [5].
Při hodnocení dostupné literatury popisující nálezy na OCT u NMOSD je nutno pamatovat na to, že diagnostika některých autoprotilátek nebyla v době jejich vzniku známa, popř. se užívaly jiné laboratorní metody jejich stanovení, a proto mohou být zkoumané kohorty značně heterogenní.
Klinický obraz ON u NMOSD
Akutní ON je jedním z kardinálních příznaků NMOSD a v 70 % případů postihne postupně obě oči. ON se projevuje snížením centrální zrakové ostrosti, často i bolestí za okem akcentovanou pohybem bulbu a poruchou barvocitu. V akutní fázi ON při NMOSD není klinický obraz ani nález na fundu odlišitelný od tzv. typické ON objevující se v rámci RS. Na možnou přítomnost NMOSD může u ON upozornit postižení obou zrakových nervů (u 20 % případů NMOSD je oboustranný zánět očního nervu prvním příznakem nemoci), těžký nezlepšující se zrakový deficit a neodpovídavost příznaků ON na léčbu vysokou dávkou kortikoidů [6]. Postižení zraku po jedné epizodě ON je u NMOSD mnohem závažnější než u RS [6–9]. Ke slepotě v jednom oku dochází u 22 % pacientů s NMOSD po první atace a u 60 % pacientů po rekurentních ON [10]. Přítomnost AQP4-IgG je jednoznačně velmi špatným prognostickým faktorem při probíhající ON [11–14] a také rizikem opakování ON s destruktivními účinky [11].
Nález na OCT
U ON pozorujeme pomocí OCT změny zvláště ve vrstvě nemyelinizovaných vláken gangliových buněk (retinal nerve fiber layer; RNFL) běžících po vnitřním povrchu sítnice směrem k papile, vrstvě těl gangliových buněk (ganglion cell layer; GCL) a vnitřní plexiformní vrstvě (inner plexiform layer; IPL), v níž se nachází výběžky gangliových a bipolárních buněk. Ve vnějších vrstvách sítnice ke změnám nedochází.
Optická neuritida u NMOSD způsobuje závažné postižení sítnice [7,15,16]. Průměrný pokles tloušťky peripapilární vrstvy retinálních nervových vláken (pRNFL) po jedné ON byl 31 μm ve studii Ratchforda et al z roku 2009 (n = 26, 60 % AQP4-IgG séropozitivních), což je o 24 μm více než u pacientů v kohortě ON u RS. Následná epizoda ve stejném oku vedla k poklesu pRNFL o dalších 10 μm [7]. Další studie tyto nálezy potvrzují [11–13,15,16]. Hlavním rozlišovacím znakem mezi ON u NMOSD a ON u RS na OCT je kromě míry postižení i rozdílná topografie ztráty vláken v peripapilární oblasti (obr. 1) i v oblasti makuly. Následkem ON u NMOSD dochází k úbytku vláken v pRNFL nejen v temporálním kvadrantu (jako je tomu u RS), ale i v kvadrantu horním, dolním a nazálním [1]. Na rozdíl od ON u RS, kdy zánět očního nervu i bez léčby spontánně ustoupí a RNFL poklesne v prvních 3–6 měsících v průměru o 6 µm, při ON u NMOSD dochází ke kontinuálnímu úbytku RNFL, dokud zánět probíhá. Zánětlivé změny sítnice u NMOSD přestáváme být schopni hodnotit, když dojde ke ztenčení pRNFL na 30 µm a její tloušťka je tvořena hlavně cévními strukturami (obr. 2). V naší kohortě pacientů s NMOSD jsme prokázali korelaci mezi poklesem RNFL a délkou trvání choroby, ale neprokázali jsme korelaci mezi titry AQP4-IgG a poklesem RNFL [17].
Fig. 1. Peripapillary thickness of RNFL as measured
by optical coherence tomography. Results
of RNFL thickness are color coded with
values between 5th and 95th percentile of normal
coded in green, values between 1st and
5th percentile yellow and values below 1st percentile
red.
(a) depicts normal fi nding.
(b, c) show a loss of RNFL post optic neuritis
in multiple sclerosis with a decrease in
RNFL in temporal quadrant (yellow and red).
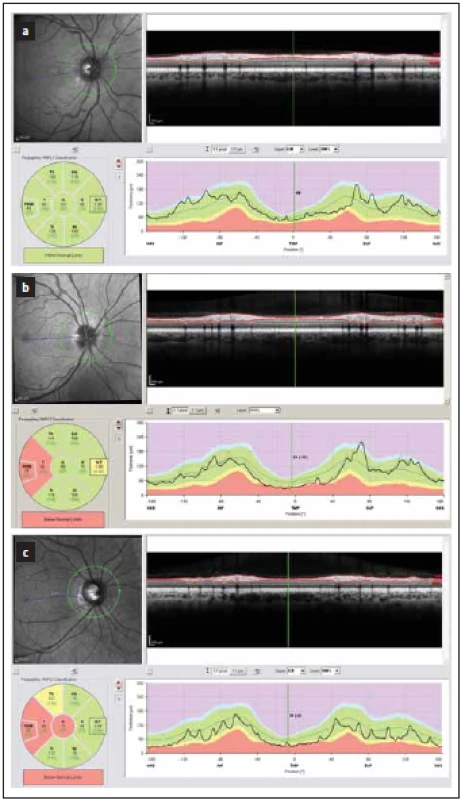
RNFL – retinal nerve fiber layer
(d–f) zobrazují nálezy po proběhlém zánětu
zrakového nervu u neuromyelitis optica a onemocnění
jejího širšího spektra. V těchto očích je
zjevný výrazný pokles tloušťky RNFL ve všech
peripapilárních segmentech (červeně a žlutě).
Fig. 1. Peripapillary thickness of RNFL as measured
by optical coherence tomography. Results
of RNFL thickness are color coded with
values between 5th and 95th percentile of normal
coded in green, values between 1st and
5th percentile yellow and values below 1st percentile
red.
(d–f) show a loss of RNFL in all peripapillary
segments (yellow and red) in patients post
optic neuritis in neuromyelitis optica spectrum
disorders.
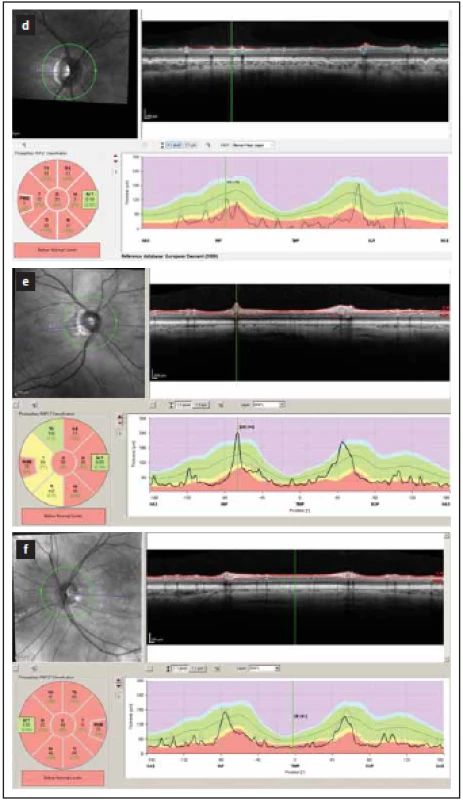
RNFL – retinal nerve fi ber layer
Celkový objem makuly (total macular volume; TMV) (obr. 3) je po ON u NMOSD významně snížený [7]. Na OCT můžeme pozorovat následky rozsáhlé destrukce gangliových buněk sítnice, při níž se významně sníží tloušťka GCL, IPL i RNFL v makule a to v mnohem větší míře, než po ON u RS [18]. Ve studii autorů z Charité (2017) byl objem GCL + IPL v oblasti makuly po ON u AQP4-IgGpozNMOSD (n = 19) významně snížený (1,54 vs. 1,87 mm3 u zdravých kontrol). Vrstva GCL je přirozeně nejsilnější v parafoveolární oblasti. Právě tam dochází i k největšímu úbytku gangliových buněk a foveolární jamka se tím mírně rozšiřuje [19]. Zatímco tloušťka vrstev GCL + IPL po ON u RS byla ve studii australských autorů (2019) snížena o cca 22 % v celém rozsahu makuly, vrstva GCL + IPL byla po ON u NMOSD snížena o 25–35 % s maximem těsně parafoveolárně [20].
Fig. 2. Longitudinal follow up of peripapillary RNFL thickness (right eye) in a patient with AQP4-IgGposNMOSD. Two episodes of optic
neuritis occurred during the follow-up – in October 2010 and in February 2011.
(a) shows fi nding in the acute phase of optic neuritis.
(b) shows fi ndings 4 months later. The thickness of RNFL still falls within normal values in most peripapillary segments (coded in
green) however, the curve of RNFL thickness has been fl attened and shows a loss of RNFL in all segments. A slight increase in RNFL
thickness on this day in comparison with the prior exam is caused by edema caused by the second optic neuritis in the right eye. The
blood vessels artifi cially increase the RNFL thickness (marked by a yellow arrow).
(c) shows retinal fi ndings a full year after the onset of fi rst optic neuritis in the eye. RNFL has been thinned and cannot be reliably
quantifi ed.
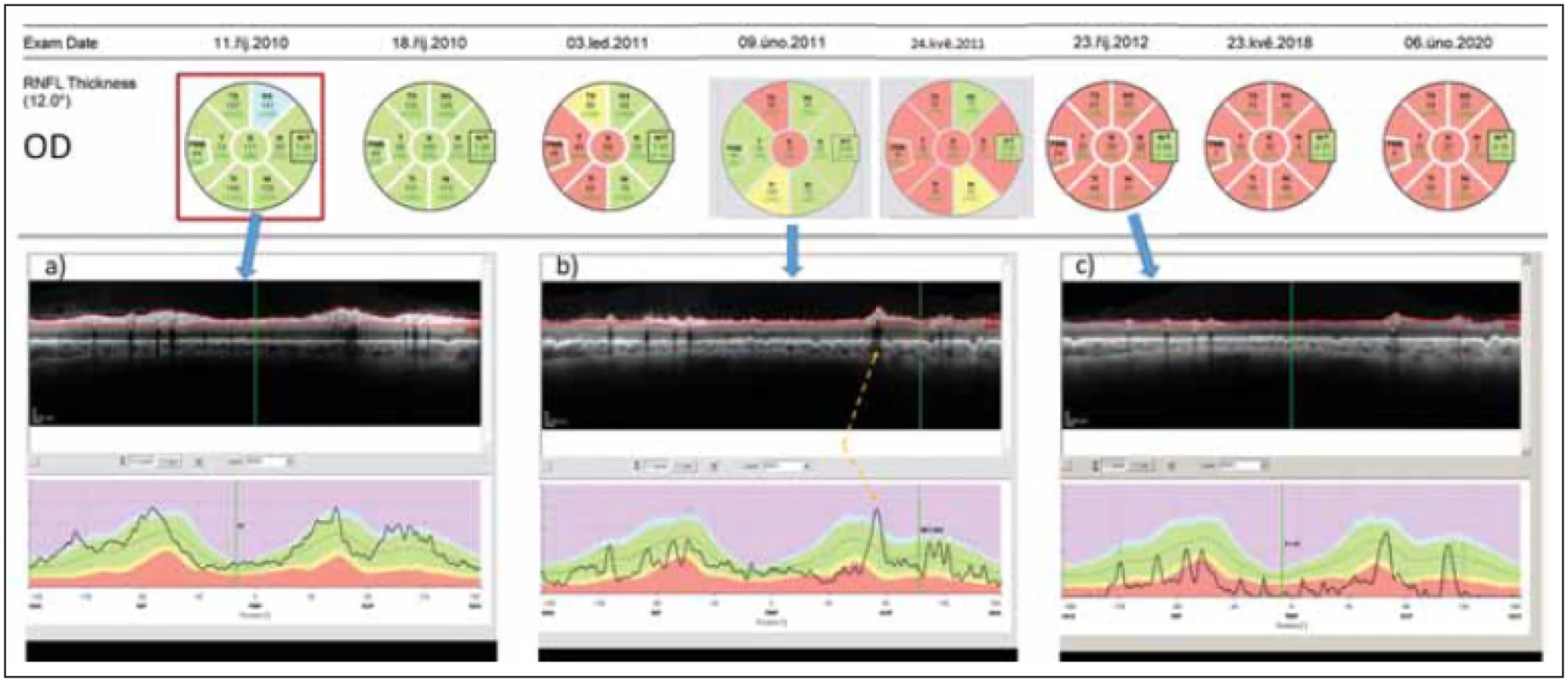
RNFL – retinal nerve fi ber layer
Fig. 3. Optical coherence tomography assessment of macula in a patient with optic neuritis in neuromyelitis optica spectrum
disorders. The thickness of retinal layers is color-coded to the right of each map. The fi rst column shows the measurement of TMV, the
middle column shows the thickness of NFL, and the thickness of GCL is in the column on the right. The fi rst assessment was performed
in October 2017 shortly after the fi rst symptoms of optic neuritis and reveals peripapillary edema (blue arrows) aff ecting the NFL and
TMV (results in the fi rst row). The assessment performed six weeks later shows thinning of GCL and decrease of peripapillary edema
(results in the second row). The fi nal assessment shown was performed in June 2019 and shows loss of NFL and GCL in all macular
segments and related decrease of TMV.
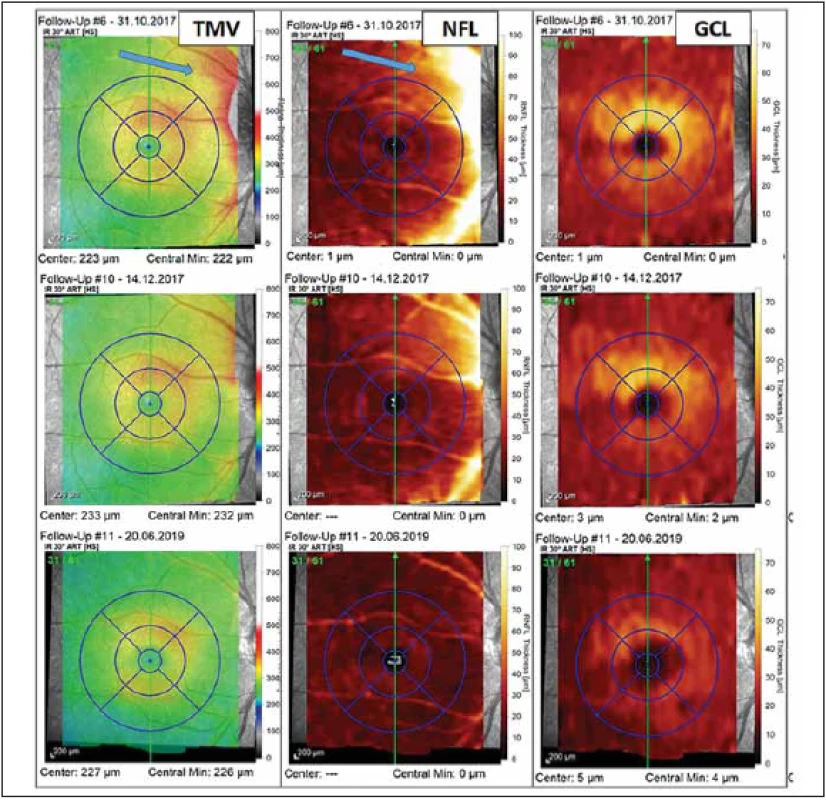
GCL – ganglion cell layer; NFL – nerve fi ber layer in macula; TMV – total macular volume
Mikrostrukturální změny u NMOSD bez ON
V očích pacientů s NMOSD, u nichž neproběhl zánět ani v jednom očním nervu (NON-NMOSD), nedochází ke snižování pRNFL, a proto byly tyto oči dlouho považovány za nepostižené. Průměrná tloušťka pRNFL je v NON-NMOSD očích hraničně vyšší, avšak nedosahuje nad horní hranici normy pro věk a pohlaví pacienta (vlastní data) [18]. Vysvětlení pro toto pozorování zatím není známo, ale může souviset s poruchou homeostázy vody u NMOSD. Existují i další důkazy, že sítnice u NON-NMOSD očí není zcela nepostižená.
Oertel et al ukázali, že objem GCIPL v NON-NMOSD očích je nižší než u zdravých kontrol (0,60 ± 0,05 vs. 0,63 ± 0,04 mm3; p = 0,016), a to i v případě, že do kohorty zahrnuli jen pacienty, kteří neměli postižení ani na jednom oku (ON u NMOSD často postihuje i chiasma, což by mohlo měření ovlivnit). Mírný úbytek vrstvy GCIPL byl naměřen i během 3letého longitudinálního sledování [21,22].
ON u NMOSD je destruktivnější než ON u RS
Naši představu o mechanizmu poškození sítnice u NMOSD odvozujeme od známých charakteristik lézí v CNS. Autoprotilátky proti AQP4 překročí hematoencefalickou bariéru (o spouštěcím mechanizmu porušení bariéry se vedou debaty) [23], reagují s transmembránovými akvaporinovými kanály astrocytů objímajících kapiláry, aktivují komplement a spustí cytotoxickou reakci s formováním membrány atakujícího komplexu. V procesu se také uplatňuje protilátkově zprostředkovaná buněčná cytotoxická reakce proti astrocytům. V CNS do místa zánětu vycestují na podkladě chemotaxe další buňky imunitního systému (eozinofily, neutrofily a monocyty/makrofágy), které způsobí sekundární poranění oligodendrocytů a neuroaxonální poranění. Geneze postižení sítnice u NMOSD se (oproti CNS) liší na několika úrovních. Za prvé je namířena nejen proti astrocytům, ale také proti Müllerovým buňkám. Na zvířecím modelu bylo ukázáno, že k autoimunitní reakci v oku nemusí být nutně přítomen komplement [24]. Vazba AQP4-IgG na astrocyty CNS vede k internalizaci AQP4, poruše transportu vody, edému astrocytů a zánětu [25]. Ačkoliv byl tento jev prokázán na astrocytech CNS, dokážeme si představit, že stejný efekt by byl pro citlivé buňky sítnice toxický. Müllerovy buňky jsou nejen strukturální oporou sítnice a zajišťují metabolizmus vody, ale také chrání neurony před nadměrnou expozicí glutamátu. Přesný mechanizmus postižení sítnice u NMOSD není zcela objasněn.
Destruktivnost procesu u pacientů s AQP4--IgGpozNMOSD je dána topografickým vztahem Müllerových buněk a astrocytů sítnice ke gangliovým buňkám [26]. Plochá těla astrocytů sítnice (exprimují AQP4, stejně jako v CNS) se nachází na povrchu vrstvy RNFL a jejich výběžky se proplétají v celé vrstvě RNFL. Těla Müllerových buněk sídlí ve vnitřní jaderné vrstvě (INL), prochází celou sítnicí a jejich výběžky tvoří vnitřní a zevní limitující membránu sítnice. Müllerovy buňky jsou v sítnici mimo jiné zodpovědné za metabolizmus vody a jejich stěna je bohatá na kanály AQP4. Axony gangliových buněk jsou tedy obklopeny buňkami, které bohatě exprimují AQP4, a při aktivaci zánětu u NMOSD jsou vystaveny plošné destrukci [23].
Patofyziologie NMOSD je předmětem intenzivního studia a její částečné pochopení již přineslo úspěšné terapeutické strategie [27–29].
Klinický význam OCT u NMOSD
Správná diagnóza u první ON v životě je kritická pro správnou volbu léčebné strategie a záchranu zraku. OCT je unikátním nástrojem, který nám umožňuje neinvazivně studovat změny ve vrstvách sítnice a odlišit vzorec postižení typický pro ON u NMOSD a u RS. První vyšetření OCT je vhodné provést již na počátku příznaků ON. V tu chvíli sice ještě nemůžeme hodnotit vzorec ztráty vrstev, ale získáme tím důležité výchozí měření stavu obou očí. Pokud jde o první ON a je skutečně postiženo jen jedno oko (u NMOSD je často postiženo chiasma), tak můžeme porovnávat tloušťku sítnice v postiženém a nepostiženém oku. V dalších týdnech jsou změny RNFL v postiženém oku maskovány pomalu ustupujícím peripapilárním otokem. Vyšetření OCT mezi 2. a 3. měsícem od počátku příznaků ON u NMOSD již odhalí pokles vrstvy RNFL v peripapilární oblasti ve více než jen v temporálním segmentu.
Grantová podpora
Podpořeno projektem Progres Q27/LF1.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
MUDr. Jana Lízrová Preiningerová, Ph.D.
Neurologická klinika a Centrum klinických neurověd
1. LF UK a VFN v Praze
Kateřinská 30
128 08 Praha
e-mail: jana.lizrova@vfn.cz
Sources
1. Monteiro ML, Fernandes DB, Apostolos-Pereira SL et al. Quantification of retinal neural loss in patients with neuromyelitis optica and multiple sclerosis with or without optic neuritis using Fourier-domain optical coherence tomography. Invest Ophthalmol Vis Sci 2012; 53 (7): 3959–3966. doi: 10.1167/iovs.11-9324.
2. Mealy MA, Wingerchuk DM, Greenberg BM et al. Epidemiology of neuromyelitis optica in the United States: a multicenter analysis. Arch Neurol 2012; 69 (9): 1176–1180. doi: 10.1001/archneurol.2012.314.
3. Sato DK, Callegaro D, Lana-Peixoto MA et al. Distinction between MOG antibody-positive and AQP4 antibody-positive NMO spectrum disorders. Neurology 2014; 82 (6): 474–481. doi: 10.1212/WNL.0000000000000101.
4. Probstel AK, Rudolf G, Dornmair K et al. Anti-MOG antibodies are present in a subgroup of patients with a neuromyelitis optica phenotype. J Neuroinflammation 2015; 12 : 46. doi: 10.1186/s12974-015-0256-1.
5. Zamvil SS, Slavin AJ. Does MOG Ig-positive AQP4-seronegative opticospinal inflammatory disease justify a diagnosis of NMO spectrum disorder? Neurol Neuroimmunol Neuroinflamm 2015; 2 (1): e62. doi: 10.1212/NXI.0000 000000000062.
6. Merle H, Olindo S, Bonnan M et al. Natural history of the visual impairment of relapsing neuromyelitis optica. Ophthalmology 2007; 114 (4): 810–815. doi: 10.1016/j.ophtha.2006.06.060.
7. Ratchford JN, Quigg ME, Conger A et al. Optical coherence tomography helps differentiate neuromyelitis optica and MS optic neuropathies. Neurology 2009; 73 (4): 302–308. doi: 10.1212/WNL.0b013e3181af78b8.
8. Schneider E, Zimmermann H, Oberwahrenbrock T et al. Optical coherence tomography reveals distinct patterns of retinal damage in neuromyelitis optica and multiple sclerosis. PLoS One 2013; 8 (6): e66151. doi: 10.1371/journal.pone.0066151.
9. Park KA, Kim J, Oh SY. Analysis of spectral domain optical coherence tomography measurements in optic neuritis: differences in neuromyelitis optica, multiple sclerosis, isolated optic neuritis and normal healthy controls. Acta Ophthalmol 2014; 92 (1): e57–e65. doi: 10.1111/aos.12215.
10. Wingerchuk DM, Hogancamp WF, O‘Brien C et al. The clinical course of neuromyelitis optica (Devic‘s syndrome). Neurology 1999; 53 (5): 1107–1114. doi: 10.1212/wnl. 53.5.1107.
11. Matiello M, Lennon VA, Jacob A et al. NMO-IgG predicts the outcome of recurrent optic neuritis. Neurology 2008; 70 (23): 2197–2200. doi: 10.1212/01.wnl.0000303817.82134.da.
12. Jitprapaikulsan J, Chen JJ, Flanagan E et al. Aquaporin-4 and myelin oligodendrocyte glycoprotein autoantibody status predict outcome of recurrent optic neuritis. Ophthalmology 2018; 125 (10): 1628–1637. doi: 10.1016/j.ophtha.2018.03.041.
13. Sotirchos ES, Filippatou A, Fitzgerald KC et al. Aquaporin-4 IgG seropositivity is associated with worse visual outcomes after optic neuritis than MOG-IgG seropositivity and multiple sclerosis, independent of macular ganglion cell layer thinning. Mult Scler 2019 : 1352458519864928. doi: 10.1177/1352458519864928.
14. Sato DK, Nakashima I, Takahashi T et al. Aquaporin-4 antibody-positive cases beyond current diagnostic criteria for NMO spectrum disorders. Neurology 2013; 80 (24): 2210–2216. doi: 10.1212/WNL.0b013e318296ea08.
15. de Seze J, Blanc F, Jeanjean L et al. Optical coherence tomography in neuromyelitis optica. Arch Neurol 2008; 65 (7): 920–923. doi: 10.1001/archneur.65.7.920.
16. Merle H, Olindo S, Donnio A et al. Retinal peripapillary nerve fiber layer thickness in neuromyelitis optica. Invest Ophthalmol Vis Sci 2008; 49 (10): 4412–4417. doi: 10.1167/iovs.08-1815.
17. Nytrova P, Kleinova J, Lizrova Preiningerova J et al. Neuromyelitis optica a poruchy jejího širšího spektra – retrospektivní analýza klinických a paraklinických nálezů. Cesk Slov Neurol N 2015; 78/111 (1): 72–77. doi: 10.14735/amcsnn201572.
18. Fernandes DB, Raza AS, Nogueira RG et al. Evaluation of inner retinal layers in patients with multiple sclerosis or neuromyelitis optica using optical coherence tomography. Ophthalmology 2013; 120 (2): 387–394. doi: 10.1016/j.ophtha.2012.07.066.
19. Oertel FC, Kuchling J, Zimmermann H et al. Microstructural visual system changes in AQP4-antibody-seropositive NMOSD. Neurol Neuroimmunol Neuroinflamm 2017; 4 (3): e334. doi: 10.1212/NXI.0000000000000334.
20. Shen T, You Y, Arunachalam S et al. Differing structural and functional patterns of optic nerve damage in multiple sclerosis and neuromyelitis optica spectrum disorder. Ophthalmology 2019; 126 (3): 445–453. doi: 10.1016/j.ophtha.2018.06.022.
21. Wingerchuk DM, Banwell B, Bennett JL et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015; 85 (2): 177–189. doi: 10.1212/WNL.0000000000001729.
22. Oertel FC, Havla J, Roca-Fernandez A et al. Retinal ganglion cell loss in neuromyelitis optica: a longitudinal study. J Neurol Neurosurg Psychiatry 2018; 89 (12): 1259–1265. doi: 10.1136/jnnp-2018-318382.
23. Zeka B, Lassmann H, Bradl M. Muller cells and retinal axons can be primary targets in experimental neuromyelitis optica spectrum disorder. Clin Exp Neuroimmunol 2017; 8 (Suppl 1): 3–7. doi: 10.1111/cen3.12345.
24. Felix CM, Levin MH, Verkman AS. Complement-independent retinal pathology produced by intravitreal injection of neuromyelitis optica immunoglobulin G. J Neuroinflammation 2016; 13 (1): 275. doi: 10.1186/s12974-016-0746-9.
25. Hinson SR, Romero MF, Popescu BF et al. Molecular outcomes of neuromyelitis optica (NMO) -IgG binding to aquaporin-4 in astrocytes. Proc Natl Acad Sci U S A 2012; 109 (4): 1245–1250. doi: 10.1073/pnas.1109980108.
26. Levin MH, Bennett JL, Verkman AS. Optic neuritis in neuromyelitis optica. Prog Retin Eye Res 2013; 36 : 159–171. doi: 10.1016/j.preteyeres.2013.03.001.
27. Bradl M, Reindl M, Lassmann H. Mechanisms for lesion localization in neuromyelitis optica spectrum disorders. Curr Opin Neurol 2018; 31 (3): 325–333. doi: 10.1097/WCO.0000000000000551.
28. Mader S, Kumpfel T, Meinl E. Novel insights into pathophysiology and therapeutic possibilities reveal further differences between AQP4-IgG - and MOG-IgG-associated diseases. Curr Opin Neurol 2020; 33 (3): 362–371. doi: 10.1097/WCO.0000000000000813.
29. Chen T, Lennon VA, Liu YU et al. Astrocyte-microglia interaction drives evolving neuromyelitis optica lesion. J Clin Invest 2020; 130 (8): 4025–4038. J Clin Invest 2020; 130 (8): 4025–4038.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2020 Issue supplementum 1
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Memantine Eases Daily Life for Patients and Caregivers
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
-
All articles in this issue
- Editorial
- Historie neuromyelitis optica a onemocnění jejího širšího spektra, vývoj diagnostických kritérií
- Neuromyelitis optica – imunopatogenetické mechanizmy
- Epidemiologie, klinický obraz a průběh onemocnění u neuromyelitis optica a onemocnění jejího širšího spektra
- Nálezy na magnetické rezonanci u neuromyelitis optica a onemocnění jejího širšího spektra
- Laboratorní vyšetření u neuromyelitis optica a onemocnění jejího širšího spektra
- Využití optické koherenční tomografie u neuromyelitis optica a onemocnění jejího širšího spektra
- Evokované potenciály u neuromyelitis optica a spektra ochorení neuromyelitis optica
- Diferenciální diagnostika neuromyelitis optica a onemocnění jejího širšího spektra
- Terapie relapsů u neuromyelitis optica a onemocnění jejího širšího spektra
- Chronická a symptomatická léčba neuromyelitis optica a onemocnění jejího širšího spektra
- Specifika onemocnění ze širšího spektra neuromyelitis optica u dětí
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Nálezy na magnetické rezonanci u neuromyelitis optica a onemocnění jejího širšího spektra
- Laboratorní vyšetření u neuromyelitis optica a onemocnění jejího širšího spektra
- Epidemiologie, klinický obraz a průběh onemocnění u neuromyelitis optica a onemocnění jejího širšího spektra
- Diferenciální diagnostika neuromyelitis optica a onemocnění jejího širšího spektra
