68Ga-DOTATOC
68Ga-DOTATOC
The radiopharmaceutical 68Ga-DOTATOC represents the latest radiopharmaceutical in the diagnosis of a neuroendocrine tumor with somatostatin receptor overexpression. Technological and economic difficulties of preparing and quality control of the radiopharmaceutical limit its use to specialised departments. Background of the department with rich experience with radiopharmaceuticals for positron emission tomography allows handling more difficult 68Ga-radiopharmacy and may increase and improve the care of oncology patients.
Keywords:
68Ga-DOTATOC – radiopharmacy – neuroendocrine tumors
Authors:
Michal Budinský; Petr Vyšinský; Stanislav Synek; Beatrix Bencsiková; Iveta Selingerová; Zdeněk Řehák
Published in:
Čes. slov. Farm., 2021; 70, 136-141
Category:
Original Article
doi:
https://doi.org/https://doi.org/10.5817/CSF2021-4-136
Overview
Radiofarmakum 68Ga-DOTATOC představuje nejnovější registrované radiofarmakum k diagnostice neuroendokrinních nádorů se zvýšenou expresí somatostatinových receptorů. Technologická a ekonomická náročnost přípravy a hodnocení jakosti radiofarmaka omezuje jeho možné použití pouze na specializovaná pracoviště. Zázemí pracoviště s bohatou zkušeností s přípravou radiofarmak pro pozitronovou emisní tomografii umožňuje zvládnout i náročnější galliovou - 68Ga radiofarmacii a může tím rozšířit a zkvalitnit péči o onkologické pacienty.
Klíčová slova:
68Ga-DOTATOC – radiofarmacie – neuroendokrinní nádory
Úvod
Neuroendokrinní nádory (NEN) představují poměrně vzácnou heterogenní skupinu zhoubných nádorů. Společným znakem těchto nádorů jsou obvykle dobře vyjádřené somatostatinové receptory (SSTR). U člověka rozlišujeme pět podtypů SSTR (SSTR1–SSTR5), všechny jsou spřažené s G-proteinem (GPCR)1, 2). NEN vykazují expresi více než jednoho podtypu receptorů, nejčastěji jsou zastoupeny podtypy SSTR1–SSTR3 a SSTR5, podtyp SSTR4 je zastoupen minoritně3). Nejčastějšími lokalizacemi NEN jsou gastrointestinální trakt, slinivka břišní, plíce a močové cesty. Z méně častých lokalizací NEN jsou to mj. kůže a vaječníky4). V evropské populaci se incidence NEN uvádí 3 až 4/100 000/rok, s lepší diagnostikou roste také incidence. Většina pacientů má dobrou prognózu přežití, proto je také prevalence desetinásobná proti incidenci 35 až 40/100 000. Podle údajů Národního onkologického registru (NOR) tvoří NEN asi 1,6 % všech zhoubných novotvarů5).
K zobrazení SSTR jsou využívána analoga somatostatinu, radiofarmaka značená galliem-68 (68Ga-DOTATOC, 68Ga-DOTANOC a 68Ga-DOTATATE), indiem-111 (111In-Octreoscan), případně techneciem-99m (99mTc-Tektrotyd) nebo iodem-123 (123I-Octreotid)6), lišící se afinitou k jednotlivým podtypům SSTR. Tato radiofarmaka se primárně vážou na SSTR2, mohou se však lišit silou vazby. 68Ga-DOTATOC vykazuje afinitu k SSTR5, 68Ga-DOTANOC vykazuje afinitu k SSTR5 a méně SSTR3, 68Ga-DOTATATE pouze na SSTR27).
K diagnostice NEN metodou pozitronové emisní tomografie v kombinaci s výpočetní tomografií (PET/ CT), popř. s magnetickou rezonancí (PET/MR) je v České republice radiofarmakum 68Ga-DOTATOC jediným registrovaným léčivým přípravkem. 68Ga-DOTATOC PET/CT vyšetření proti scintigrafickému vyšetření 111Inpentetreotidem (111In-Octreoscan) má vyšší senzitivitu (96 % proti 86 %) a výrazně vyšší i specificitu (93 % proti 50 %)8). Lze jej využít jako metodu volby k diagnostice, lokalizaci a sledování pacientů s NEN9). Využití tohoto radiofarmaka popisuje obrázek 1 (68Ga-DOTATOC vyšetření PET/CT vyšetření u 55leté ženy). I přes registraci kitu pro přípravu radiofarmaka SOMAkit TOC (Advanced Accelerator Applications, Saint Genis Pouilly, Francie) a radionuklidového generátoru Galliapharm (Eckert & Ziegler Radiopharma GmbH, Berlín, Německo) je však jeho dostupnost problematická a omezena na pár pracovišť, která jsou schopna pro své pacienty toto radiofarmakum zajistit.
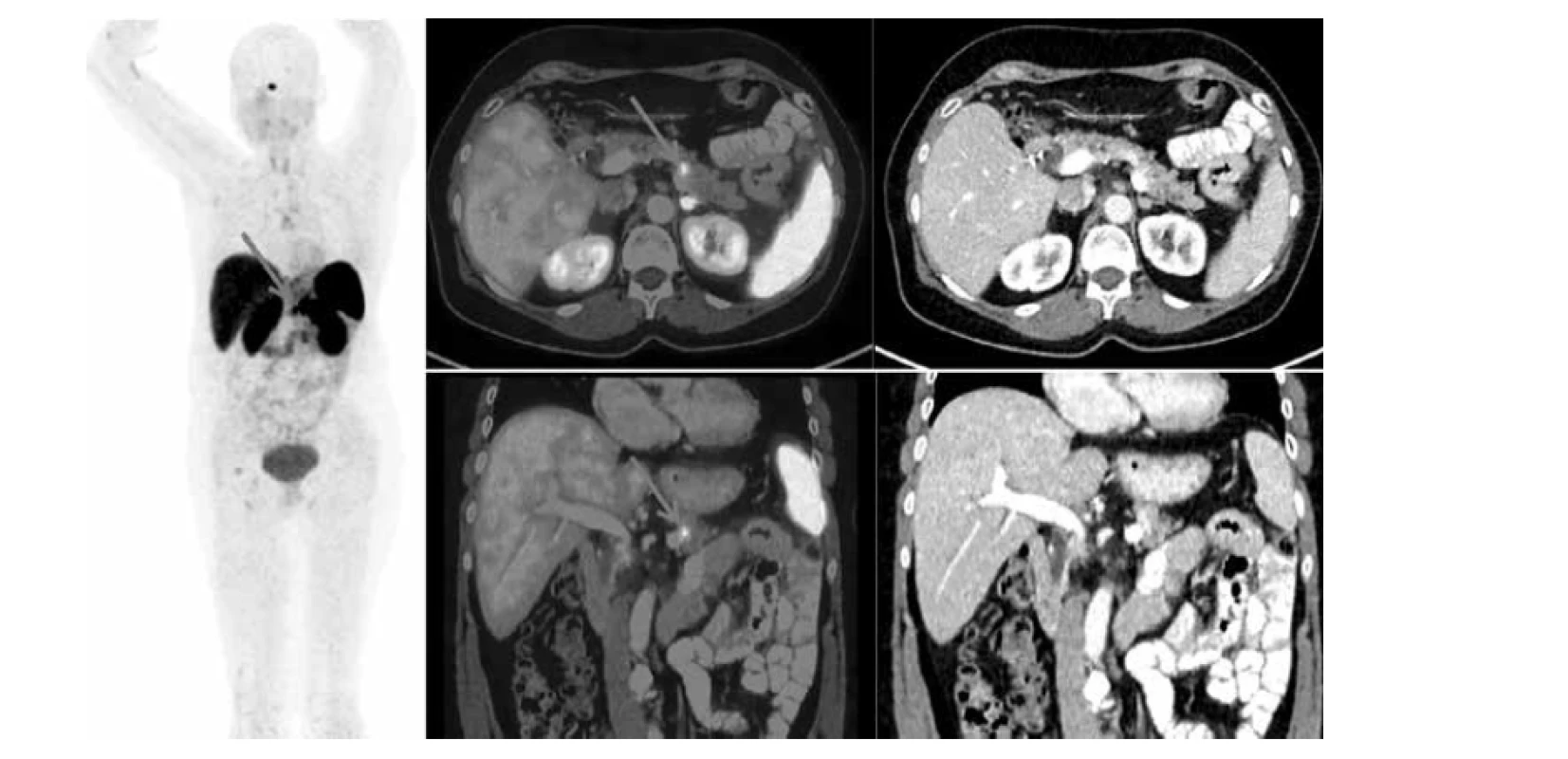
Cílem tohoto sdělení je popsat nejen samotnou přípravu a hodnocení jakosti radiofarmaka 68Ga-DOTATOC v obecné rovině, ale také zhodnotit technologické zkušenosti s tímto radiofarmakem, včetně vyhodnocení profesní expozice ionizujícímu záření (IZ) farmaceutického personálu na pracovišti Ústavní lékárny Masarykova onkologického ústavu v Brně.
Pokusná část
Příprava radiofarmaka
Jako zdrojový materiál pro přípravu radiofarmaka je využit radionuklid gallium-68 v podobě [68Ga]chloridu gallitého v prostředí kyseliny chlorovodíkové získaný elucí registrovaného radionuklidového generátoru Galliapharm 1,48 GBq pomocí sterilního roztoku ultračisté 0,1M kyseliny chlorovodíkové a dále peptid edotreotid dostupný v podobě registrovaného léčivého přípravku SOMAkit TOC. SOMAkit TOC je dodáván ve formě kitu obsahujícího dvě injekční lahvičky – injekční lahvička obsahující 40 μg edotreotidu a injekční lahvička obsahující 1 ml reakčního pufru.
Radionuklidové značení nosičových struktur pomocí [68Ga]chloridu gallitého je velmi citlivé na přítomnost stopových nečistot kovů. Aby se minimalizovaly stopové nečistoty kovů, lze používat spotřební materiál (injekční jehly) s prokázanou odolností vůči zředěné kyselině (acidorezistentní nebo potažené silikonem).
Pro zajištění čistoty radionuklidového generátoru se doporučuje pravidelná eluce sterilním roztokem ultračisté 0,1M kyseliny chlorovodíkové. Pokud generátor nebyl používán po 3 a více dní, v koloně se nahromadí volné ionty radioizotopu germania-68. Doporučuje se proto 7–24 hodin před následující provozní elucí kolonu jednorázově propláchnout. Při každé eluci je z kolony vypláchnuto malé množství izotopu germania-68. Kontaminace radioizotopem germaniem-68 nesmí překročit 0,001 % eluované aktivity gallia-68. Pro zajištění co nejnižší kontaminace je třeba generátor proplachovat alespoň jednou za pracovní den. Při pravidelném proplachování generátoru by měla kontaminace po 12 měsíců zůstat pod 0,001 %.
Aktivita uvedená na signatuře generátoru je vyjádřena jako hodnota aktivity radioizotopu germania-68, jaké bylo dosaženo v den kalibrace (12 : 00 SEČ). Dostupná aktivita radioizotopu gallia-68 závisí na aktivitě germania-68 v době eluce a času, který uplynul od předchozí eluce. Generátor v plně rovnovážném stavu generuje více než 60 % gallia-68 při eluci 5 ml sterilního roztoku ultračisté 0,1M kyseliny chlorovodíkové. Výtěžek (obr. 2) postupně klesá, jak se postupně rozpadá mateřský radionuklid germanium-68. Analogicky postupně klesá i výtěžek při syntéze radiofarmaka (obr. 3).
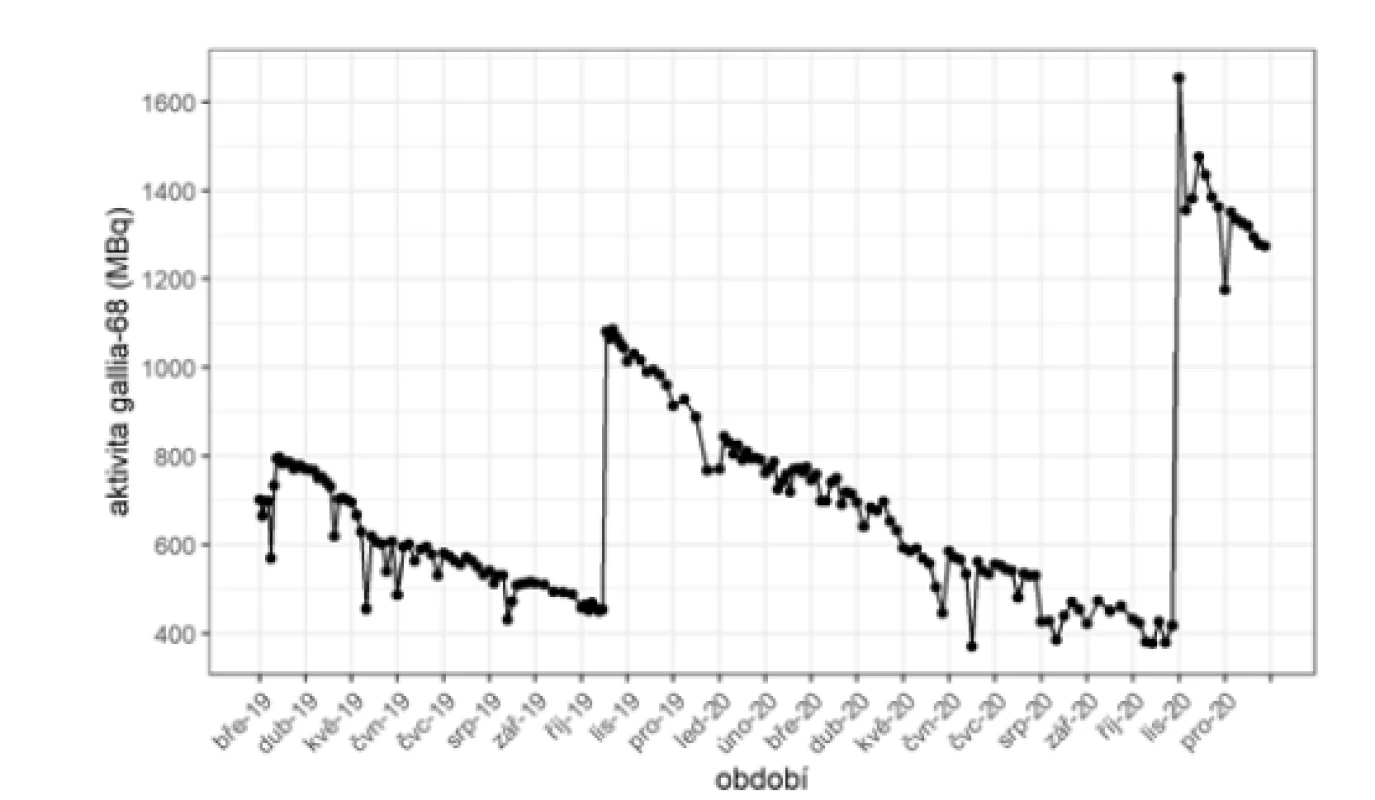
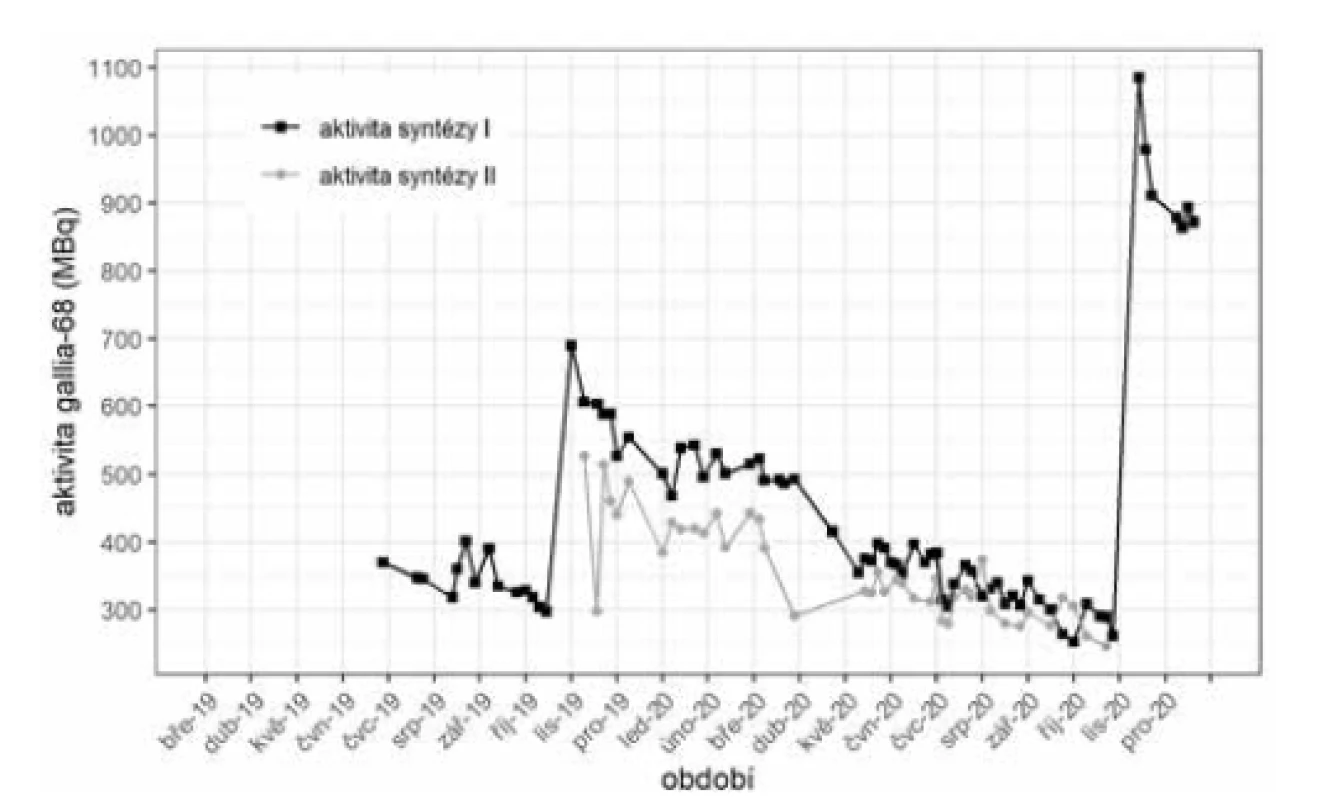
Příprava roztoku edotreotidu značeného galliem-68 probíhá dle požadavků souhrnu údajů o přípravku (SPC) za aseptických podmínek v souladu s požadavky správné radiofarmaceutické praxe. Představuje operace v podobě eluce radionuklidového generátoru do lahvičky s peptidem, úpravu vlastností reakčního roztoku přidáním pufru, jeho zahřátí a následné zchlaze ní. Takto získaný roztok je podroben hodnocení jakosti v podobě hodnocení vzhledu, pH a efektivity značení a následně je přípravek propuštěn k aplikaci.
Z injekční lahvičky s práškem edotreotidu se odtrhne uzávěr a povrch lahvičky se otře antiseptikem k dezinfekci povrchu, uzávěr se nechá oschnout. Aby byl v injekční lahvičce během značení udržován atmosférický tlak, septum injekční lahvičky se propíchne odvětrávací jehlou opatřenou sterilním filtrem.
Z injekční lahvičky s reakčním pufrem se odtrhne uzávěr a povrch jejího uzávěru se otře antiseptikem k dezinfekci povrchu, uzávěr se nechá oschnout. Pomocí injekční stříkačky s minimálním mrtvým prostorem se odebere objem 0,5 ml reakčního pufru.
K lahvičce s práškem edotreotidu se pomocí sterilní jehly potažené silikonem a membránového filtru připojí výstupní linka radionuklidového generátoru. Generátor se propláchne pomocí pumpy 5 ml sterilního roztoku ultračisté 0,1M kyseliny chlorovodíkové přímo do injekční lahvičky, a zajistí se tak rekonstituce prášku v eluátu. Na konci eluce se odpojí generátor od injekční lahvičky vytažením jehly z pryžového septa a ihned se přidá 0,5 ml reakčního pufru, který je připravený v injekční stříkačce. Odstraní se jehla s odvětrávacím filtrem.
Pomocí manipulačních kleští se přesune injekční lahvička do otvoru ve varném hnízdě vytemperovaném na 95 °C. Injekční lahvička se ponechá při teplotě 95 °C po dobu minimálně 7 minut (maximálně však 10 minut) bez jakéhokoliv pohybu nebo míchání.
Po vyjmutí z varného hnízda se injekční lahvička nechá vychladnout 10 minut při laboratorní teplotě.
Hodnocení jakosti radiofarmaka
U připraveného radiofarmaka se zkontroluje vzhled, hodnota pH a efektivita značení.
Vzhled radiofarmaka se hodnotí vizuální kontrolou. Roztok musí být čirý bez viditelných částic.
Hodnota pH se hodnotí pomocí indikátorových proužků k měření pH. Na indikátorový proužek se nanese injekční stříkačkou kapka vzorku. Požadovaná hodnota pH je v rozsahu 3,2–3,8.
Efektivita značení se hodnotí metodami tenkovrstvé chromatografie. Stanovuje se množství koloidního gallia-68 a množství volného 68Ga3+. Jako stacionární fáze se využívá chromatografický papír se skleněnými vlákny iTLC-SG (Agilent Technologies, Santa Clara, USA) nastříhaný na proužky 1 x 12 cm. Pro stanovení koloidního gallia-68 se používá jako mobilní fáze roztok octanu amonného (77 g/l) ve vodě smísený s methanolem v poměru 1 : 1 v/v. Pro stanovení volného 68Ga3+ se používá jako mobilní fáze 0,1M vodný roztok citronanu sodného upravený pomocí kyseliny chlorovodíkové na pH = 5.
Vyvíjecí komory iTLC se připraví nalitím mobilních fází do výšky 3–4 mm. Analyzovaný vzorek radiofarmaka se nanese na proužek chromatografického papíru pomocí injekční stříkačky 1 cm od okraje a vloží se do vyvíjecí komory. Po dosažení čela 1 cm od horního okraje se proužek chromatografického papíru vyjme z kolony, osuší a následně analyzuje s využitím iTLC skeneru.
Maximální množství nečistot je do 3 % v podobě koloidního gallia-68 a do 2% v podobě volného 68Ga3+.
Příprava injekční dávky pro pacienta
Po propuštění radiofarmaka k aplikaci je radiofarmakum rozplněno do stíněné injekční stříkačky s využitím instrumentálního zařízení μDDS-A (Tema Sinergie, Faenza, Itálie). Připravená injekční stříkačka s radiofarmakem je opatřena signaturou a spolu s průvodním listem otevřeného radionuklidového zdroje je předána k aplikaci.
Výsledky
Výsledky hodnocení jakosti radiofarmaka
Výsledky hodnocení jakosti radiofarmaka popisují grafy na obrázcích 4, 5 a 6 – hodnocení jakosti radiofarmaka.
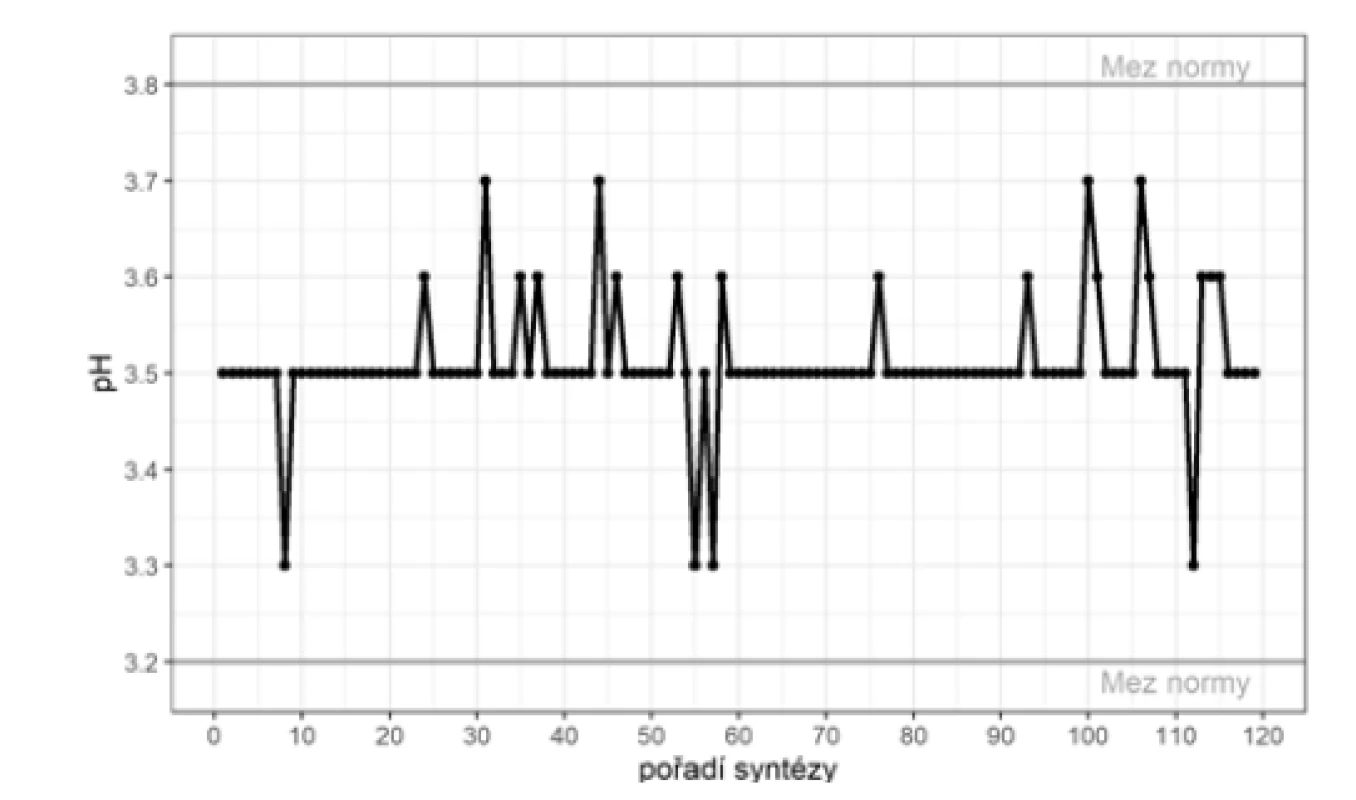
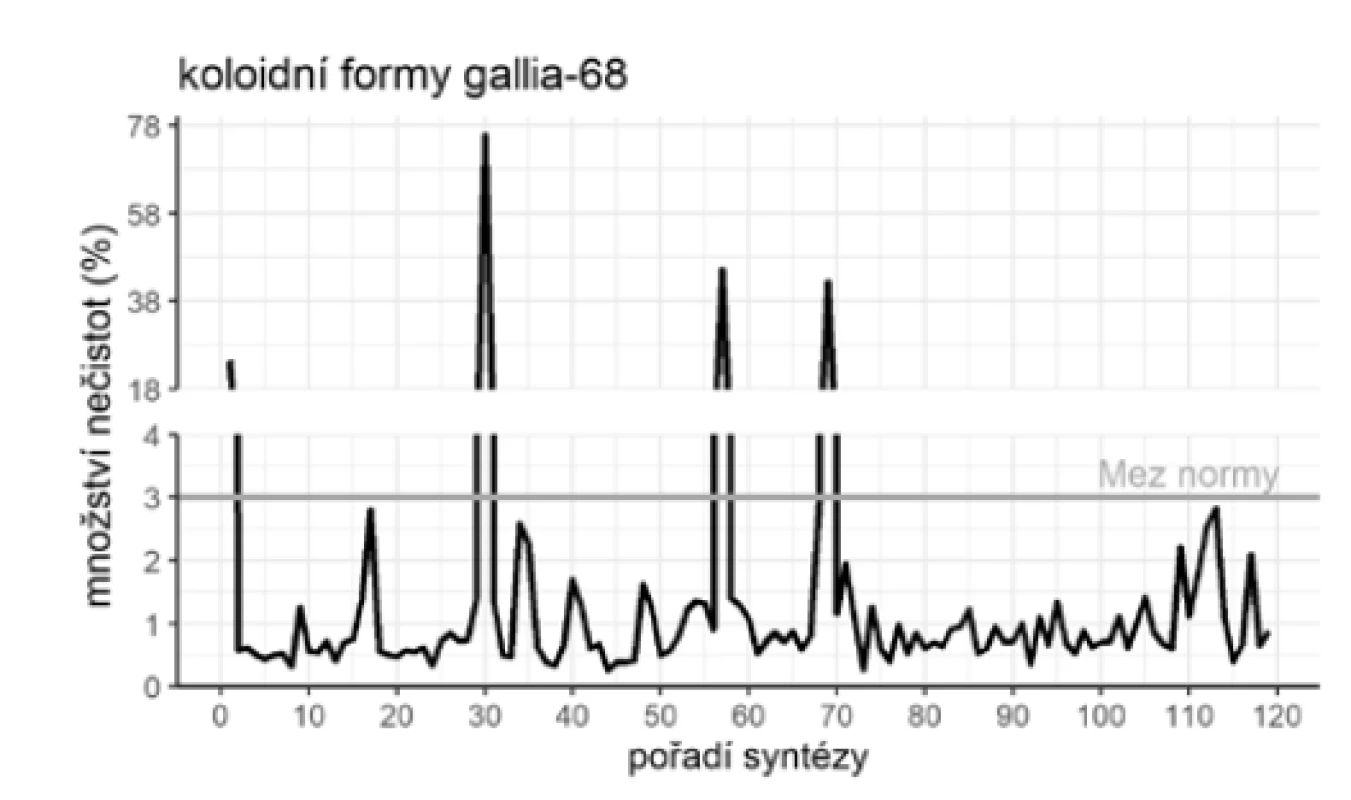
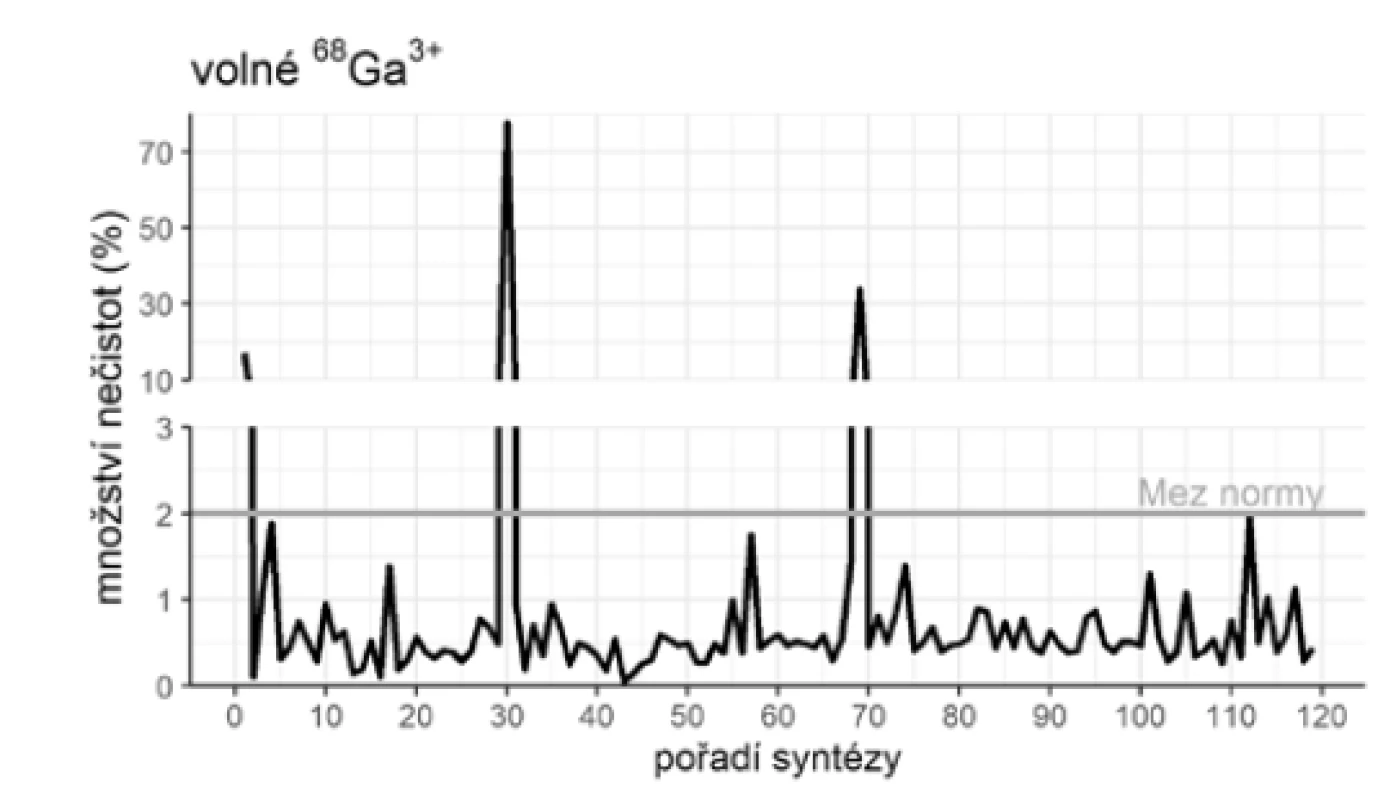
Z celkem 119 syntéz tohoto radiofarmaka nebylo na základě hodnocení jakosti ve čtyřech případech (3,36 %) radiofarmakum propuštěno k aplikaci. Ve třech případech byly souhlasně nevyhovující oba druhy nečistot – koloidní gallium-68 i volné 68Ga3+. Při 1. syntéze bylo stanoveno 24,58 % koloidního gallia-68 a 17,07 % volného 68Ga3+, při 30. syntéze 75,78 % koloidního gallia-68 a 77,45 % volného 68Ga3+, při 69. syntéze 42,35 % koloidního gallia-68 a 33,81 % volného 68Ga3+. U 57. syntézy bylo nevyhovující množství koloidního gallia-68 v množství 45,20 %, množství volného 68Ga3+ bylo stanoveno 1,75 %, což je v mezích normy. U těchto čtyř neúspěšných syntéz bylo provedeno šetření příčin neshody. Prostudováním protokolu přípravy a kontroly radiofarmaka nebyla zjištěna žádná zjevná příčina, která by vedla k neúspěšné syntéze radiofarmaka. Konzultace problematiky s produktovým specialistou výrobce a distribuce také nepřinesla zjištění zjevné příčiny neshody. Vzhledem k neúspěšnému šetření příčin neshody nebylo možné přijmout žádná nápravná opatření, která by umožnila předcházet případné neshodě tohoto charakteru při dalších syntézách. Lze se pouze domnívat, že možnými příčinami neshody mohl být vadný kit pro přípravu radiofarmaka z výroby, možné nedodržení teplotního řetězce při nakládání s kitem pro přípravu radiofarmaka nebo přítomnost kovů z radionuklidového generátoru nebo použitého spotřebního materiálu. Lze také uvažovat lidský faktor při syntéze radiofarmaka.
Výsledky dozimetrie farmaceutického personálu
Zařazení nového radiofarmaka do běžného provozu s sebou přináší pochopitelné úvahy nad expozicí personálu IZ, zvláště pak v případě, jedná-li se o technologicky náročnější přípravu a hodnocení jakosti radiofarmaka, což příprava 68Ga-radiofarmak bezesporu je. Syntéza 68Ga-DOTATOC z kitu pro přípravu radiofarmaka SOMAkit TOC neumožňuje využít plnou instrumentaci pro zajištění kompletní přípravy s cílem redukovat kontakt radiofarmaceutického personálu s radiofarmakem ve smyslu optimalizace radiační ochrany. Tyto systémy sice existují, jejich dostupnost a možnost využití pro přípravu radiofarmaka je však problematická. Jedná se o zařízení typu KitLab (Eckert & Ziegler Radiopharma GmbH, Berlín, Německo) a Morgana (Tema Sinergie, Faenza, Itálie). Možnost využití těchto systémů limituje i omezená rozměrová a funkční kompatibilita mezi laminárním boxem a systémem pro automatizovanou přípravu. Dostupnější jsou moduly pro syntézu radiofarmaka cestou výroby, avšak požadavky na správnou výrobní praxi jsou pro většinu pracovišť nukleární medicíny prakticky nesplnitelné.
Vzhledem k nemožnosti využít plnou instrumentaci pro přípravu radiofarmaka 68Ga-DOTATOC lze očekávat u farmaceutického personálu nárůst hodnot expozice v prstové dozimetrii. Jelikož příprava radiofarmaka probíhá v prostředí stíněného laminárního boxu pro přípravu pozitronových radiofarmak (NMC 1/50 DSI, Tema Sinergie, Faenza, Itálie), je nárůst hodnot expozice v celotělové dozimetrii nepravděpodobný.
Pro sledování osobních dávek jsou využívány prstové termoluminiscenční dozimetry a celotělové osobní dozimetry OSL InLight Model2 (oba Landauer, Glenwood, USA), poskytovatelem služby osobní dozimetrie je VF, a.s. Černá Hora. Výsledky dozimetrie jsou vyjádřeny jako osobní dávkové ekvivalenty Hp(10) a Hp(0,07). Z veličiny Hp(10) a stanovené energie fotonů je vypočítána efektivní dávka E, veličina Hp(0,07) udává ekvivalentní dávku HT na prsty. Z osobních dávek jednotlivých pracovníků jsou vypočítány kolektivní dávky skupiny pracovníků za sledovaná období.
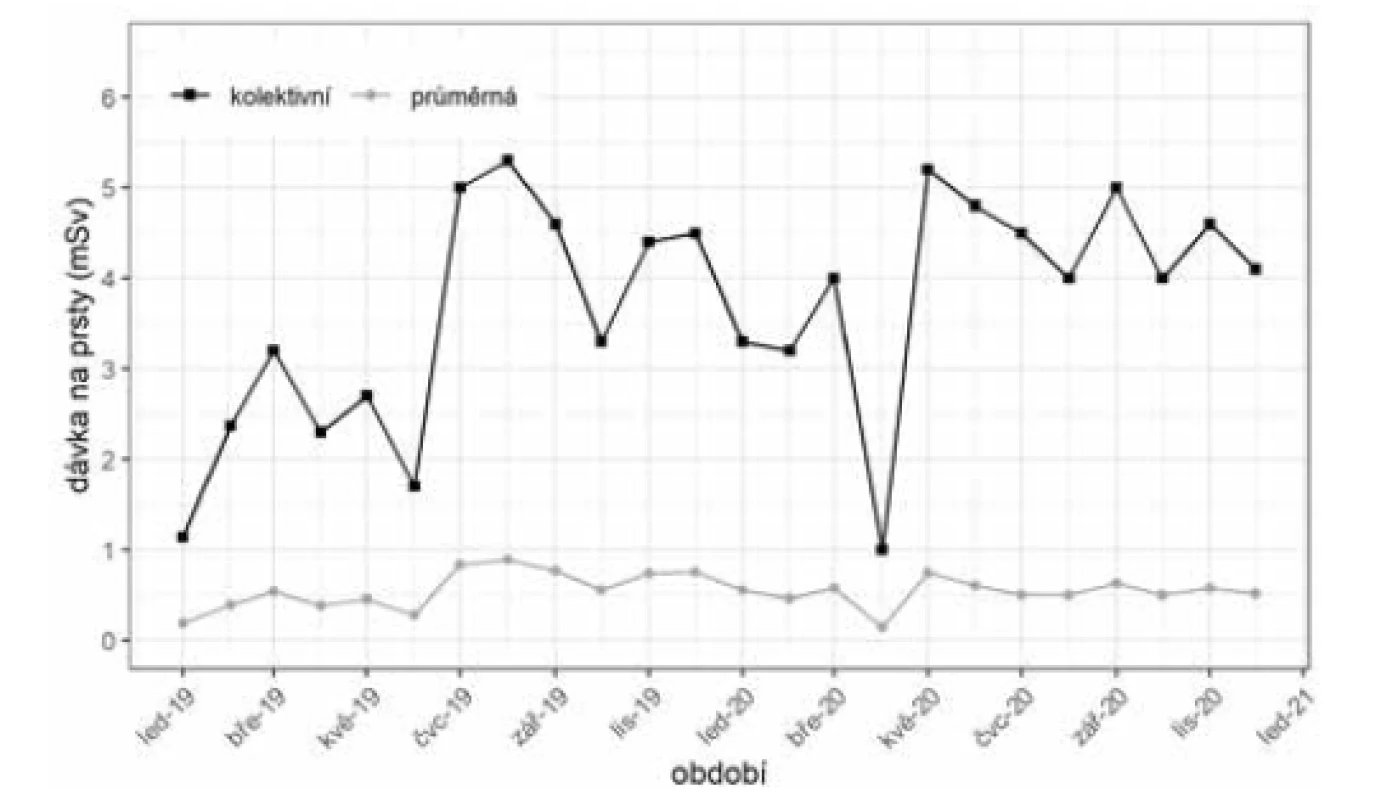
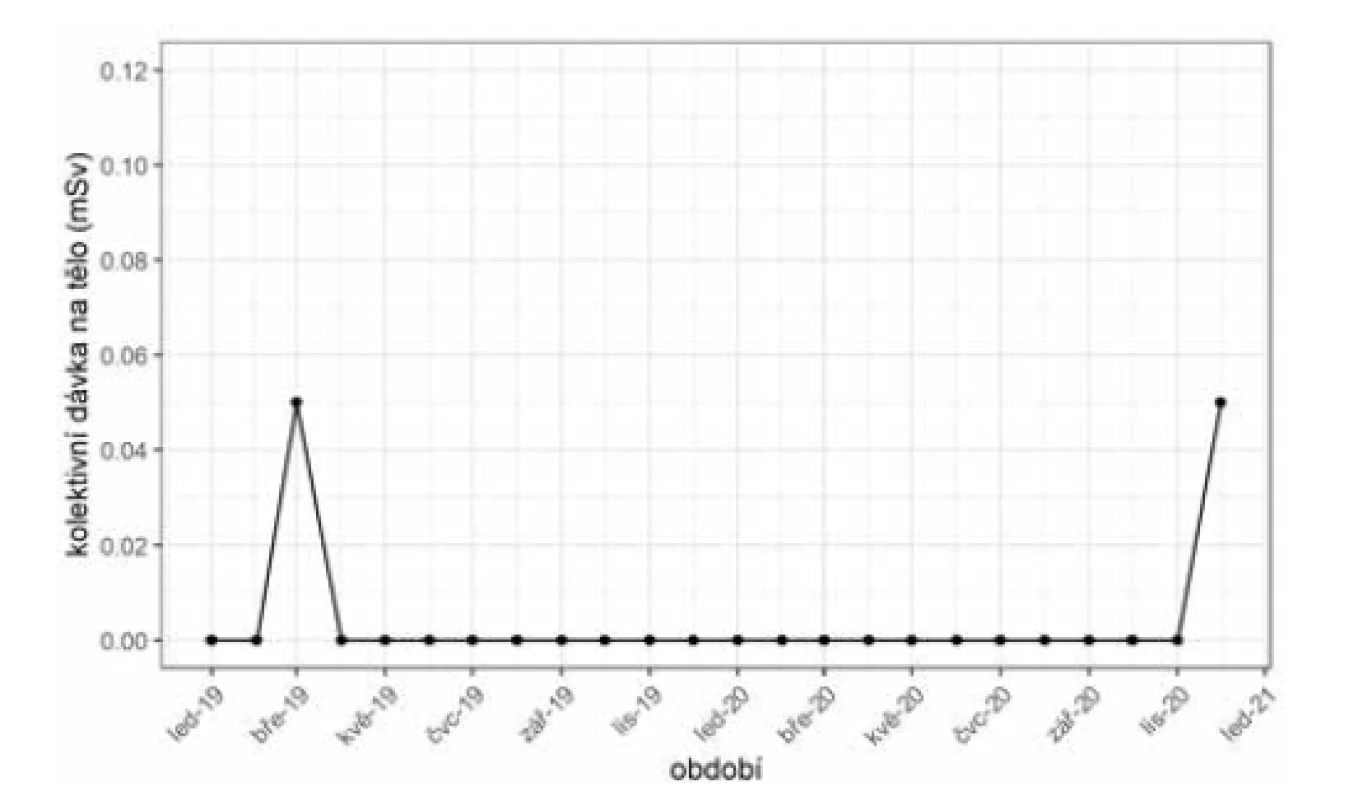
Výsledky prstové a celotělové dozimetrie ukazují grafy na obrázcích 7 a 8. V grafech je zaznamenána dozimetrie za období leden 2019 až prosinec 2020. Z výsledků je patrné navýšení hodnot expozice v prstové dozimetrii, které koresponduje s termínem zařazení syntézy 68Ga-DOTATOC do běžného provozu oddělení (červen 2019) a s postupným nárůstem počtu příprav tohoto radiofarmaka v následujících měsících. Trend postupného nárůstu v prstové dozimetrii je přechodně pozastaven v dubnu 2020 z důvodu ochromení provozu v důsledku rozvoje první vlny pandemie COVID-19. V celotělové dozimetrii nedošlo k žádným negativním změnám a až na výjimky (březen 2019 a prosinec 2020) odpovídají výsledky nulovým hodnotám celotělové expozice.
Diskuze
Příprava radiofarmak značených galliem-68 je ve srovnání s konvenčními radiofarmaky značenými techneciem - 99m a indiem-111 náročnější. Dostupnost radionuklidu gallia-68 získaného elucí registrovaného radionuklidového generátoru a peptidu edotreotidu k radionuklidovému značení v podobě registrovaného kitu pro přípravu radiofarmaka umožňuje při vybavení pracoviště technologií pro přípravu radiofarmak pro PET i toto radiofarmakum poměrně snadno připravit. I přes obavy spojené s náročností všech činností spojených s přípravou a hodnocením jakosti tohoto radiofarmaka lze s časovým odstupem vyhodnotit tyto obavy jako přehnané a úspěšnost syntézy radiofarmaka v našich podmínkách dosahuje 96,64 %. Při porovnání našich výsledků s výsledky z jiných pracovištích je úspěšnost jejich syntézy ještě vyšší a dosahuje 98,23 %10) a 97,96 %11).
Ve výsledcích prstové dozimetrie je patrný nárůst o 0,63 mSv za jednu syntézu a hodnocení jakosti tohoto radiofarmaka. Studie z jiného pracoviště zaznamenává za jednu syntézu a hodnocení jakosti hodnotu 0,31 mSv12). Kromě využití peristaltické pumpy pro automatizovanou eluci generátoru by se nabízela jako nástroj optimalizace radiační ochrany i další instrumentace přípravy, ta je však v současné době v našich podmínkách jen těžko dostupná.
Závěr
Radiofarmaka značená galliem-68 s afinitou k SSTR mají své místo v diagnostice metodou PET. 68Ga-DOTA-peptidy, které jsou v zahraničí používány již řadu let, jsou pro nás stále ještě relativně nová a prakticky málo prozkoumaná radiofarmaka. Jejich dostupnost snižuje nejen technologická náročnost přípravy a hodnocení jakosti těchto radiofarmak, ale i finanční náročnost vybavení pracoviště potřebnou technologií a v neposlední řadě také cena samotného radiofarmaka. Z těchto důvodů budou tato nová radiofarmaka i v budoucnosti pro většinu českých pracovišť prakticky nedostupná. Také vzácnost tohoto onemocnění povede k centralizaci těchto přípravků na pár vybraných pracovišť pro větší spádovou oblast, a umožňuje tak alespoň částečně zajistit toto radiofarmakum pro potřeby diagnostiky NEN.
Po stránce radiofarmaceutické technologie se příprava a hodnocení jakosti radiofarmaka 68Ga-DOTATOC po pár úvodních syntézách stává rutinní záležitostí s úspěšností syntézy přes 96 %. Z hlediska expozice IZ dochází k nárůstu expozice v prstové dozimetrii, kdy jedna syntéza představuje navýšení dávky o 0,63 mSv, v celotělové dozimetrii vliv na možné navýšení osobních dávek nepozorujeme.
I přes zmíněné komplikace je MOÚ prvním pracovištěm v České republice, které toto radiofarmakum zařadilo do rutinního provozu a nabízí jej svým pacientům v rámci diagnostiky NEN. Jedná se však zatím o dílčí krok v péči o pacienty s NEN. Teprve zapojení těchto radiofarmak jako součást teranostiky pak umožní další posun v boji s NEN. To je však hudbou (snad blízké) budoucnosti.
Střet zájmů: žádný.
Došlo 30. dubna 2021 / Přijato 29. června 2021
PharmDr. Michal Budinský, P. Vyšinský, S. Synek
Masarykův onkologický ústav, Ústavní lékárna
Žlutý kopec 7, 656 53 Brno
e-mail: budinsky@mou.cz
B. Bencsiková
Masarykův onkologický ústav, Klinika komplexní onkologické péče,
Brno
I. Selingerová
Masarykův onkologický ústav, Oddělení laboratorní medicíny, Brno
Z. Řehák
Masarykův onkologický ústav, Oddělení nukleární medicíny, Brno
Sources
1. Patel Y. C. Somatostatin and its receptor family. Frontiers in Neuroendocrinology 1999; 20(3), 157–198.
2. Patel Y. C., Strikant C. B. Somatostatin receptors. Trends Endocrinol Metab. 1997; 8(10), 398–405.
3. Papotti M., Bongiovanni M., Volante M., Allia E., Landolfi S., Helboe L., Schindler M., Cole S. L., Bussolati G. Expression of somatostatin receptor types 1–5 in 81 cases of gastrointestinal and pancreatic endocrine tumors: a correlative immunohistochemical and reverse - transcriptase polymerase chain reaction analysis. Virchows arch. 2002; 440(5), 461–175.
4. Vítek P. Neuroendokrinní nádory, in Onkologie v klinické praxi. Standardní přístupy v diagnostice a léčbě vybraných zhoubných nádorů. Praha: Mladá fronta 2019.
5. Sedláčková E., Bajčiová V., a kol. Epidemiologie NEN ve světe a v ČR, registry. In: Neuroendokrinní nádory. Praha: Maxdorf 2016.
6. Wang L., Tang K., Zhang Q., Li H., Wen Z., Zhang H. Somatostatin Receptor-Based MoleculaImaging and Therapy for Neuroendocrine Tumors. Biomed Res Int. 2013; 2013, 102819.
7. Pauwels E., Cleeren F., Bormans G., Deroose C. M. Somatostatin receptor PET ligands – the next generation for clinical practice. Am. J. Nucl. Med. Mol. Imag. 2018; 8(5), 311–331.
8. Gabriel M., Decristoforo C., Kendler D., Dobrozemsky G., Heute D., Uprimny C., Kovacs P., Guggenberg E., Bale R., Virgolini I. J. 68Ga-DOTA-Tyr3-Octreotide PET in neuroendocrine tumors: comparison with somatostatin receptor scintigraphy and CT. J. Nucl. Med. 2007; 48, 508–518.
9. Bencsiková B., Řehák Z., Budinský M., Hejnová R., Kozáková Š., Kiss I., Demlova R., Svoboda M. 68Ga - DOTA-TOC PET/CT vyšetření u pacienta s gastroenteropankreatickým neuroendokrinním nádorem – první vyšetření v České republice. Klin. Onkol. 2019; 32(5), 390–392.
10. Monaharan P., Lamarca A., Navalkissoor S., Calero J., Chan P. S, Julyan P., Sierra M., Caplin M., Valle J. Safety, tolerability and clinical implementation of „ready-to-use“ 68gallium-DOTA0-Tyr3-octreotide (68Ga-DOTATOC) (SomaKIT TOC) for injection in patients diagnosed with gastropancreatic neuroendocrine tumors (GEP-NETs). ESMO Open. 2020; 5, e000650.
11. Calero J. Kits or synthesis modules? A review of both strategies. Ga-68 for beginners. London: UKRG 2018.
12. Murby B. Radiation risk assessment. Ga-68 for beginners. London: UKRG 2018.
Labels
Pharmacy Clinical pharmacologyArticle was published in
Czech and Slovak Pharmacy

2021 Issue 4
-
All articles in this issue
- Specifický charakter léčiv a hodnota léčiv
- Postavení vitaminu D v primární a sekundární prevenci u ortopedických pacientů
- 68Ga-DOTATOC
- Farmaceutické špecifiká v latinskej dizertačnej tlači De phthisi (O tuberkulóze) z roku 1679 od slovenského lekára Matúša Palumbiniho
- Česká farmacie 150 let pod křídly odborné společnosti
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- About the journal
Most read in this issue
- 68Ga-DOTATOC
- Postavení vitaminu D v primární a sekundární prevenci u ortopedických pacientů
- Specifický charakter léčiv a hodnota léčiv
- Farmaceutické špecifiká v latinskej dizertačnej tlači De phthisi (O tuberkulóze) z roku 1679 od slovenského lekára Matúša Palumbiniho
