Chirurgická léčba Crohnovy choroby
Crohn's Disease Surgery
Surgery of Crohn’s disease is an important part of the general treatment algorithm. The role of surgery is changing with the development of conservative procedures. The recent years have seen the return to early treatment of patients with Crohn’s disease. Given the character of the disease and its intestinal symptoms, a specific approach to these patients is necessary, especially regarding the correct choice of surgery. The paper focuses on the luminal damage of the small and large intestine including complications of the disease. We describe the individual indications for a surgical solution, including the choice of anastomosis or multiple / repeated surgeries.
Key words:
anastomosis – complications – Crohn's disease – resection – surgery
:
Zdeněk Kala 1; Filip Marek 1; Vlastimil A. Válek 2; Daniel Bartušek 2
:
Chirurgická klinika LF MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Zdeněk Kala, CSc.
1; Radiologická klinika LF MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Vlastimil A. Válek, CSc., MBA
2
:
Vnitř Lék 2014; 60(7-8): 617-623
:
100th Birthday - prof. Z. Mařatka
Chirurgická léčba Crohnovy choroby je významnou součástí celkového léčebného algoritmu. Postavení chirurgie se mění s rozvojem konzervativních postupů. V posledních letech je návrat k časné léčbě pacientů s Crohnovou chorobou. Vzhledem k charakteru onemocnění a střevního postižení je vyžadován specifický přístup k těmto pacientům zejména ve správné volbě operačního přístupu. Článek je zaměřen na luminální postižení tenkého a tlustého střeva včetně komplikací choroby. Popisujeme jednotlivé indikace operačního řešení včetně volby anastomózy či vícedobého operačního řešení.
Klíčová slova:
anastomóza – Crohnova choroba – chirurgie – komplikace – resekce
Úvod
V době popsání Crohnovy choroby jako regionální ileitidy Crohnem, Ginzburgem a Oppenheimerem v roce 1932 byla považována chirurgická kompletní resekce za jedinou kurativní metodu tohoto onemocnění [1]. Vzhledem k vysoké morbiditě a letalitě se chirurgická léčba v dalších letech přesunula k bypassovým operacím. I přes nižší procento pooperačních komplikací se tento trend ukázal být slepou cestou vzhledem k rozvoji infikovaných mukokél a neoplastických změn v ponechaných úsecích. Vzhledem k tomuto faktu se chirurgická léčba vrátila zpět k resekčním zákrokům na tenkém i tlustém střevě. V posledních 3 dekádách se i díky rozvoji konzervativních metod léčby posouvá chirurgie k ještě záchovnějším postupům, jako jsou segmentální resekce, strikturoplastiky, perkutánní drenáže abscesů, endoluminální dilatace striktur [2]. Zejména v posledních letech je posun k miniinvazivním výkonům s rozvíjející se technikou laparoskopických operací.
Chirurgie je důležitou součástí managementu léčby Crohnovy choroby. Studie ukazují, že 70–90 % pacientů si v některé fázi léčby vyžádá chirurgickou intervenci. U pacientů s ileocékálním postižením je pravděpodobnost chirurgického výkonu 75% po 5 letech od vzniku potíží a až 90% po 10 letech. U postižení tenké kličky je procento operovaných pacientů nižší: 50 % po 5 letech a 70 % po 10 letech [3].
Chirurgická léčba je indikována v případě nemožnosti či selhání konzervativní léčby a v léčbě komplikací. S rozvojem medikamentózních postupů, v poslední době zejména biologické terapie, přichází operační řešení v pozdějších stadiích onemocnění. Tento fakt je důsledkem vyššího rizika chirurgických komplikací zejména u pacientů po dlouhodobé kortikoterapii, imunosupresivní či biologické léčbě. V poslední době je stále více diskutována problematika časné chirurgické léčby zejména v ileocékální oblasti s následnou biologickou terapií.
Mezi nejčastější příznaky vyžadující operační řešení patří:
- nedostatečná odpověď na medikamentózní a nutriční terapii – zejména pokud při progresi zánětlivého onemocnění dochází ke zhoršení průjmů s významným váhovým úbytkem.
- stenózy – dle závažnosti stenózy se liší i klinické příznaky od občasných pocitů plnosti a křečí až po setrvalý subileózní stav, který může za nepříznivých okolností dospět do ileózního stavu s úplnou střevní obstrukcí.
- abscesy nebo píštěle – jedním z častých příznaků agresivní perforující formy Crohnovy choroby je tvorba nitrobřišních (mezikličkové, malá pánev, stěna břišní) či perianálních abscesů. V případě přitažení postiženého úseku u perforující formy dochází k tvorbě fistulací (enterokutánní, enteroenterické, enterokolické či enterovezikální). Léčba komplikací Crohnovy choroby je většinou obtížná a vyžaduje multidisciplinární přístup a dostatečnou konzervativní přípravu a léčbu před provedením operačního zákroku, jak bude zmíněno níže.
- kancerogeneze – fulminantě probíhající forma Crohnovy choroby po 8–10 letech významně zvyšuje riziko vzniku adenokarcinomu v postiženém úseku, zejména v oblasti tlustého střeva. Na základě klinických zkušeností jsou dlouhodobě postižené úseky s četnými pseudopolypy, zejména u pacientů na víceleté imunosupresivní terapii, indikovány k resekčnímu zákroku preventivně.
- akutní stavy – velmi často se u pacientů při fulminantím průběhu léčba komplikuje krvácením, obstrukcí, toxickým megakolon či perforací vyžadující akutní operační řešení.
Luminální postižení tenkého střeva
Symptomatická stenóza ilea a ileocékální oblasti
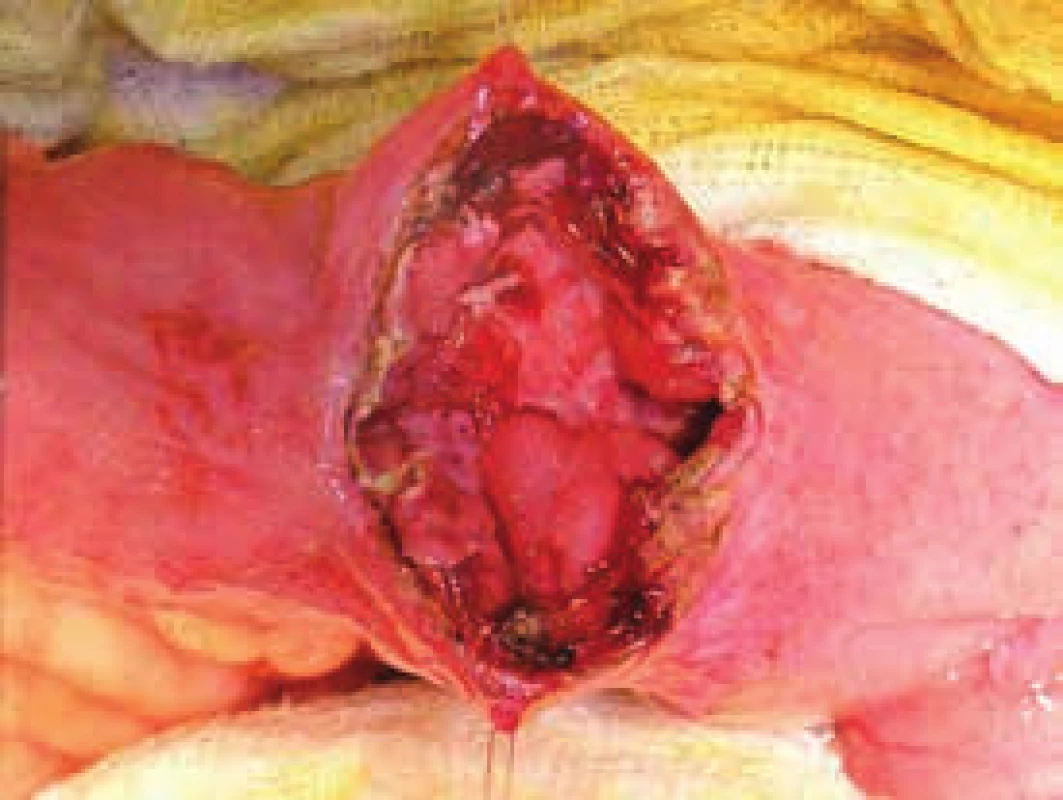
Ileocékální resekce a resekce ilea je nejčastěji prováděnou operací pro diagnózu luminální Crohnovy choroby. Primární operační řešení by mělo být zvažováno u pacientů s přetrávajícími obstrukčními symptomy po iniciální kortikoidní terapii. V ileocékální oblasti je ke zvážení i primární operační řešení bez předchozí medikamentózní terapie u pacientů s významnými symptomy obstrukce, ale bez známek aktivity onemocnění [4,5]. Dlouhodobé studie ukazují, že pacienti po operačním zákroku v této lokalitě mají 50% šanci, že již nebude v budoucnosti nutná další chirurgická léčba [6,7], obr. 1.
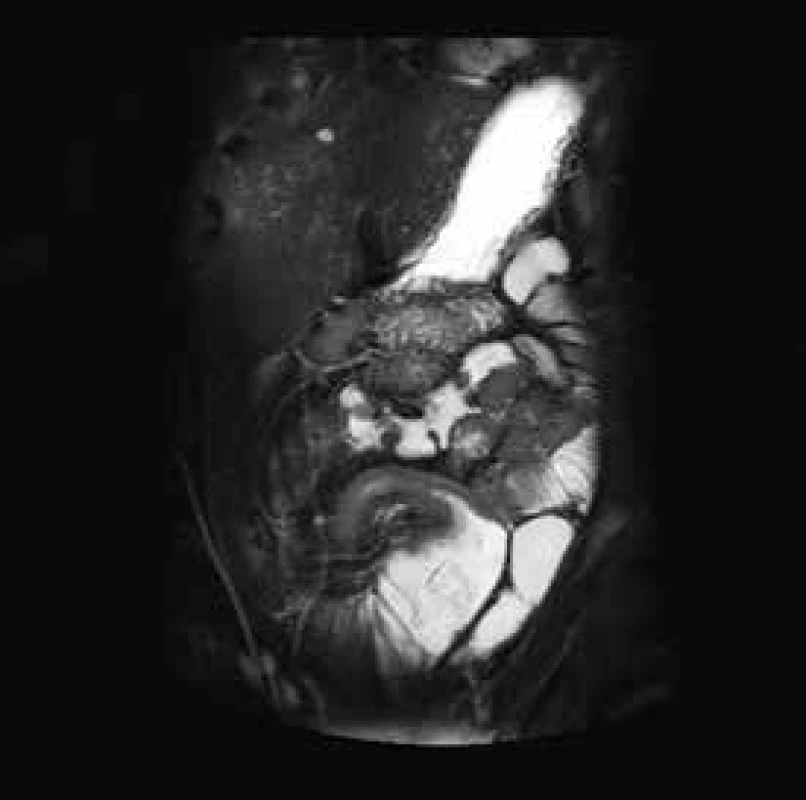
Laparoskopie vs otevřená chirurgie
V literatuře převažují retrospektivní a nerandomizované studie zabývající se touto problematikou u Crohnovy choroby. Nicméně 2 rozsáhlé metaanalýzy 14 a 15 studií ukazují na výhody v pooperačním období u pacientů operovaných laparoskopicky. Výhody zahrnují zejména dřívější obnovení peristaltiky, kratší hospitalizaci a nižší pooperační morbiditu [8,9]. Eshuis v roce 2008 publikoval 10leté sledování pacientů po laparoskopicky asistovaných a otevřených výkonech a dospěl k závěru, že u obou sledovaných skupin není z dlouhodobého hlediska rozdíl v rekurenci Crohnovy choroby vyžadující následnou intervenci [10]. Nesporný je kosmetický efekt, a to zejména u mladších pacientek. Vzhledem k vysokému procentu následných operací pro Crohnovu chorobu v dalších letech léčby je laparoskopický přístup vhodný i z pohledu nižšího rizika rozsáhlých srůstů a nižšího rizika incizionálních hernií. Podle našich zkušeností z laparoskopického přístupu profitují zejména pacienti s ileocékálním postižením bez nálezu fistulací a abscesů, výkon musí provádět chirurgické pracoviště se zkušenostmi s laparoskopickou kolorektální chirurgií.
Technika anastomózy
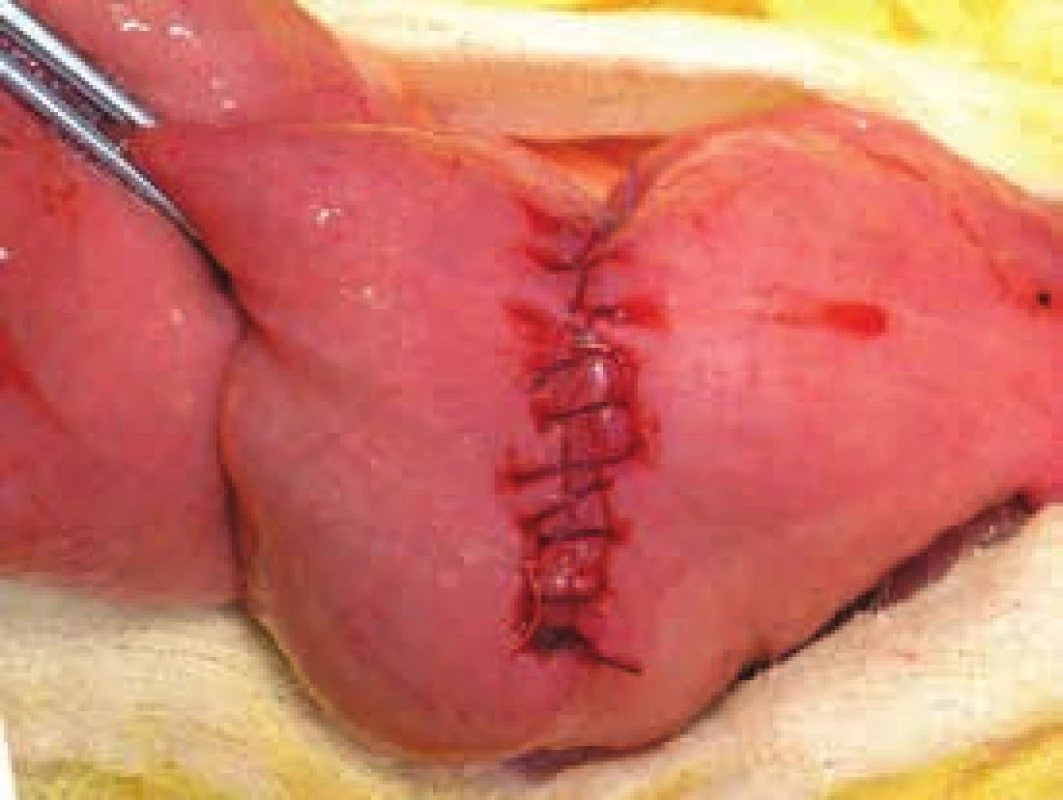
Vzhledem k časté rekurenci Crohnovy choroby v oblasti anastomózy byla právě tato důležitá fáze operace podrobena četným analýzám. V minulosti bylo zlatým standardem provedení ručně šité anastomózy konec ke konci z obavy vzniku recidivy ve slepě uzavřených pahýlech střeva. Důležitost šířky anastomózy právě pro již zmíněnou rekurenci v místě anastomózy nebo těsně před ní byla zmíněna v několika studiích již v 90. letech minulého století [11–13]. Similis v roce 2007 prezentoval výsledky metaanalýzy 8 komparativních studií publikovaných mezi lety 1992 a 2005 porovnávající výsledky výše zmíněných anastomóz, tedy koncem ke konci a staplerovou anastomózu stranou ke straně. Do metaanalýzy bylo zahrnuto 712 anastomóz u 661 pacienta. Výsledky ukázaly, že end-to-end anastomóza se pojí s vyšším rizikem insuficience anastomózy ve smyslu anastomického leaku a celkových pooperačních komplikací. Nebyl prokázán statisticky významný vyšší výskyt rekurence Crohnovy choroby v terénu této anastomózy [14]. Na našem pracovišti je preferována široká side-to-side ručně šitá či staplerová anastomóza na základě zkušeností s nižším výskytem insuficience anastomózy a zejména nižším výskytem pooperačních subileózních stavů (obr. 2).
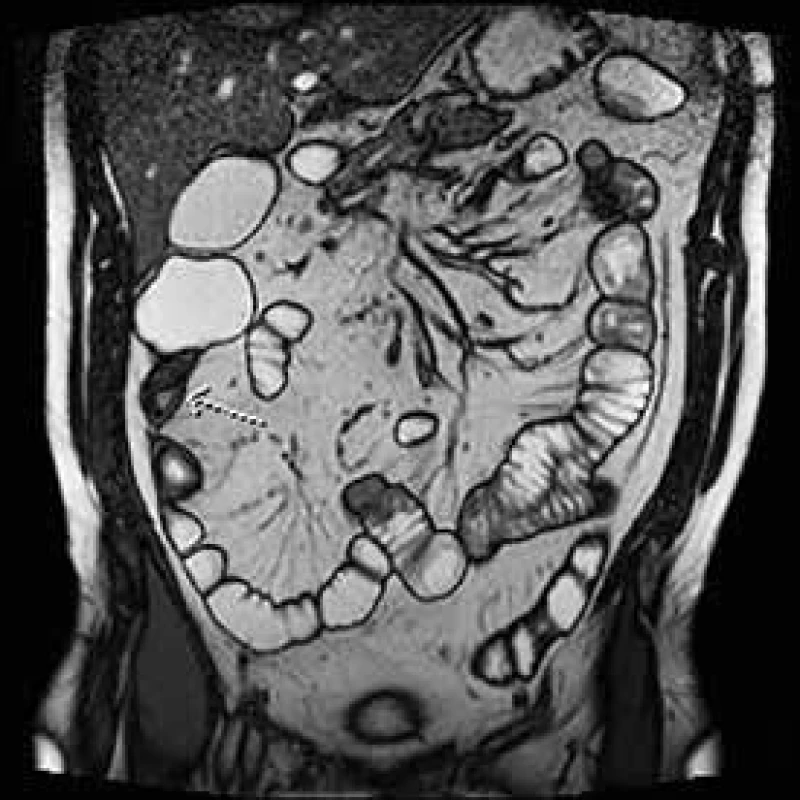
Perforující formy luminální Crohnovy choroby
Do perforujících forem zahrnujeme zejména píštěle a abscesy. Jedná se o agresivní formu Crohnovy choroby, která vyžaduje aktivní přístup jak konzervativní léčby, tak léčby chirurgické. Pokud je management léčby ideální, pak je riziko rekurence shodné jako u nekomplikovaných crohnovských stenóz. V terapii komplikovaných forem hraje významnou roli i intenzivní medicína a odborně vedená nutriční léčba. Perianální postižení je samostatnou kapitolou vyžadující odlišný přístup než luminální choroba.
Konkomitantní abscesy
Aktivní forma choroby může být spojena s tvorbou abscesů, které mohou být lokalizované jak v malé pánvi, retroperitoneu, tak i mezikličkově, kde jsou většinou součástí zánětlivých pseudotumorů. V těchto případech je velmi častá přítomnost píštělí a abscesů současně. V literatuře nejsou k dispozici recentní randomizované studie, na základě kterých by šlo doporučit ideální léčebný plán. Nicméně dle dřívějších prací a klinických zkušeností je dosahováno nejlepších výsledků operační léčby, pokud je abscesová formace léčena v první době antibiotickou léčbou a perkutánní drenáží. Ne každá abscesová kolekce, zejména pokud je součástí zánětlivého pseudotumoru, vyžaduje drenáž. Ve velkém procentu vystačíme s antibiotickou léčbou. Kultivace z těchto abscesů bývají při následné operační revizi ve většině případů sterilní. Pokud si klinický stav vynutí drenáž, pak preferujeme perkutánní přístup – CT navigovaně či pod ultrazvukovou kontrolou s následným skiaskopickým nástřikem drénované kolekce. Invazivnější alternativou je při technických komplikacích či nedostupnosti intervenčního radiologa chirurgická drenáž. Další léčebná strategie se odvíjí od klinických projevů onemocnění. Pokud jsou známky obstrukce s predilatací střeva či subjektivní potíže zejména ve smyslu křečí či pocitu nafouknutí a škroukání v dutině břišní, pak zvažujeme chirurgický výkon. V opačném případě je prostor pro nechirurgickou medikamentózní léčbu Crohnovy choroby. V mezidobí mezi drenáží a ATB terapií abscesové kolekce je vhodné ponechat „bowel rest“ s plnou parenterální výživou za pravidelných kontrol zánětlivé aktivity onemocnění a monitorace vnitřního prostředí. V tomto období je nutné stabilizovat nutriční stav pacienta.
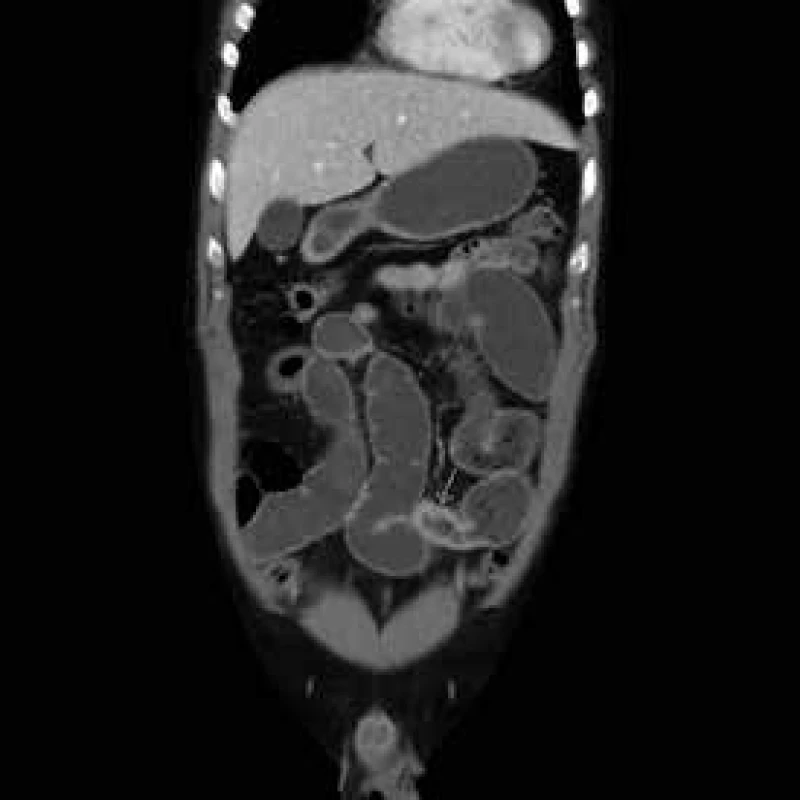
V literatuře se často uvádí termín odložená chirurgické resekce. Jednoznačný konsensus na délce odložení nebyl vysloven. Na našem pracovišti preferujeme odklad resekčního zákroku minimálně 6 týdnů po zavedení konzervativní léčby abscedující formy. Před operačním výkonem opakujeme USG střev a CT břicha k objektivizaci rozsahu a aktivity onemocnění. CT břicha je nutné k posouzení vztahu k okolním strukturám, a to zejména k ureterům, které mohou být u některých pacientů iatrogenně poraněny s nutností složité rekonstrukce s možnými doživotními následky pro operovaného pacienta. V případě přitažení či úzkého vztahu crohnovského infiltrátu k uvedeným strukturám zavádíme peroperačně cévku do ureteru, kterou v případě nekomplikovaného průběhu po skončení operace extrahujeme. Výše zmíněný odstup operačního řešení od léčby akutního stavu Crohnovy choroby zvyšuje významně šanci na resekci s primární anastomózou. Tento postup není rigidním doporučením, je třeba se řídit klinickým průběhem onemocnění a přístup individualizovat a aktuálně přehodnocovat. Pokud pacient při septických komplikacích dospěje do akutní operační revize s nutností akutní resekce zejména při průkazu střevní perforace, pak je většinou zvolen dvoudobý operační postup s obnovením kontinuity ve druhé době. V případě tohoto postupu vzhledem k riziku pooperačních srůstů a vysokému riziku břišní katastrofy při obtížné adheziolýze zvažujeme obnovení kontinuity spíše v intervalu měsíců [15–17], obr. 3.
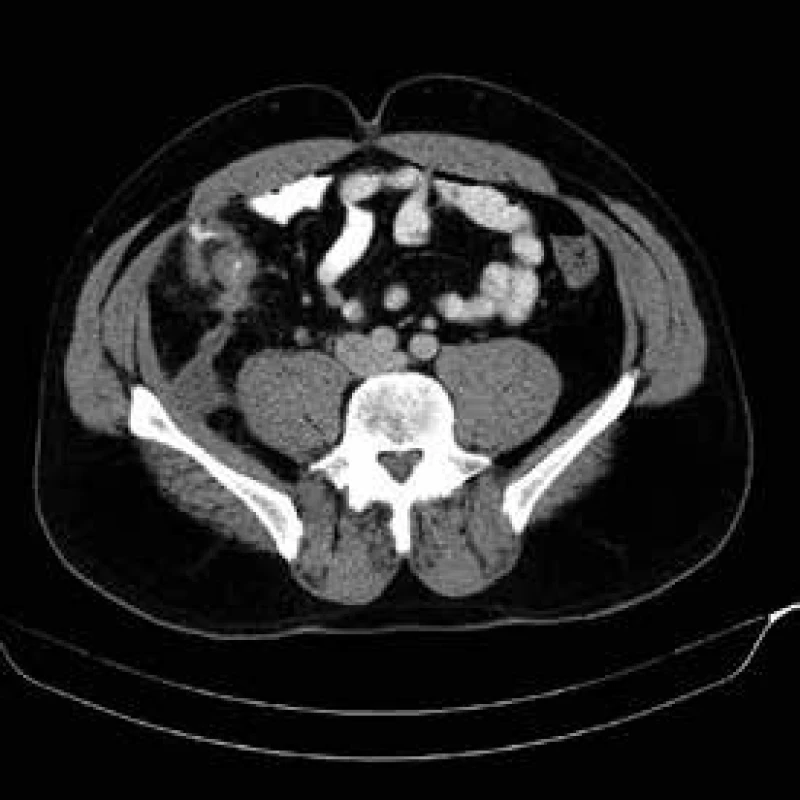
Fistulující formy
Většina píštělí asociovaných s Crohnovou chorobou je klasifikována jako píštěle vnitřní. Bouhnick uvádí, že pouze 17 % píštělí je ve formě enterokutánních či kolokutánních, vaginálních nebo perineálních. Zbytek je tvořen píštělemi vnitřními – enteroenterálními, enterokolickými a enterovezikálními [18]. Jednotlivé typy fistulací vyžadují odlišný přístup chirurga. Zevní píštěle řešíme drenáží s následnou excizí celého průběhu píštěle „en bloc“ s postiženou částí tenkého či tlustého střeva po zklidnění aktivity zánětlivého postižení. Enterovaginální postižení je raritní a je řešeno ve spolupráci s gynekologem. Problematika enteroenterálních fistulací je často svázána s mezikličkovými abscesy a potom je jejich řešení shodné, jak již bylo popsáno výše v části o konkomitantních abscesech. Po zklidnění již při operační revizi často dříve na zobrazovacích metodách popisované mezikličkové fistulace ve skutečnosti nenacházíme. Jedná se již jen o konvoluty kliček s fibrózní reakcí v okolí. Enterokolické píštěle jsou nejčastěji zastoupené píštělí ileosigmoideální. Ve většině případů se jedná o dolichosigma přitažené k zánětlivě postiženému úseku tenké kličky. Tento stav řešíme resekcí postiženého úseku ilea či ileocekální resekcí s přešitím ústí píštěle do sigmatu či drobnou klínovitou resekcí sigmatu. Zcela výjimečně se jedná o primární segmentální postižení sigmatu fistulující do okolí. Zde je potom indikace k segmentální resekci v místě postiženého sigmatu. Zcela nepodkročitelným vyšetřením před operačním řešením je recentní koloskopie, která pomáhá diagnostikovat slizniční změny na sigmatu. Samotnou píštěl se většinou koloskopicky daří vizualizovat málokdy, je ale důležitá k posouzení mukózního postižení v daném úseku [19]. Zcela odlišná je situace u enterovezikálních píštělí. V těchto případech cystoskopické vyšetření v předoperačním období nepožadujeme a řídíme se peroperačním nálezem. Fistulaci do močového měchýře excidujeme a stěnu močového měchýře přešíváme ve dvou vrstvách dle zvyklostí v urologické operativě. Po tomto zákroku ponecháváme permanentní močový katétr po dobu minimálně 7 dnů [20].
Chronické stenózy tenké kličky
Segmentální stenózy tenkého střeva jsou jedním z typických projevů Crohnovy choroby. Zobrazení postižení tenkého střeva se liší dle zvyklostí pracoviště od klasické enteroklýzy, přes CT střev k MR enterografii. Na specializovaných pracovištích je metodou volby USG střev v rukou zkušeného radiodiagnostika. Počet stenóz a jejich délka se mohou lišit, stejně tak se může jednat o skip léze při postižení v ileocékální oblasti či na tlustém střevě. Většina autorů doporučuje provádět strikturoplastiky u stenóz kratších 10 cm [21–23], obr. 4–6. V případě vícečetných striktur v krátkém úseku tenkého střeva je indikována segmentální resekce, spíše než četné strikturoplastiky, a to za podmínky, že nehrozí syndrom krátkého střeva. Aktivní crohnovský zánět, flegmóna stěny, mukózní krvácení či podezření na neoplazii je kontraindikací k provedení strikturoplastiky. Otázka rizika rekurence při porovnání strikturoplastiky a resekce není zcela jednoznačně dořešena [24,25]. Strikturoplastiky v oblasti tlustého střeva jsou kontraindikovány (obr. 7).
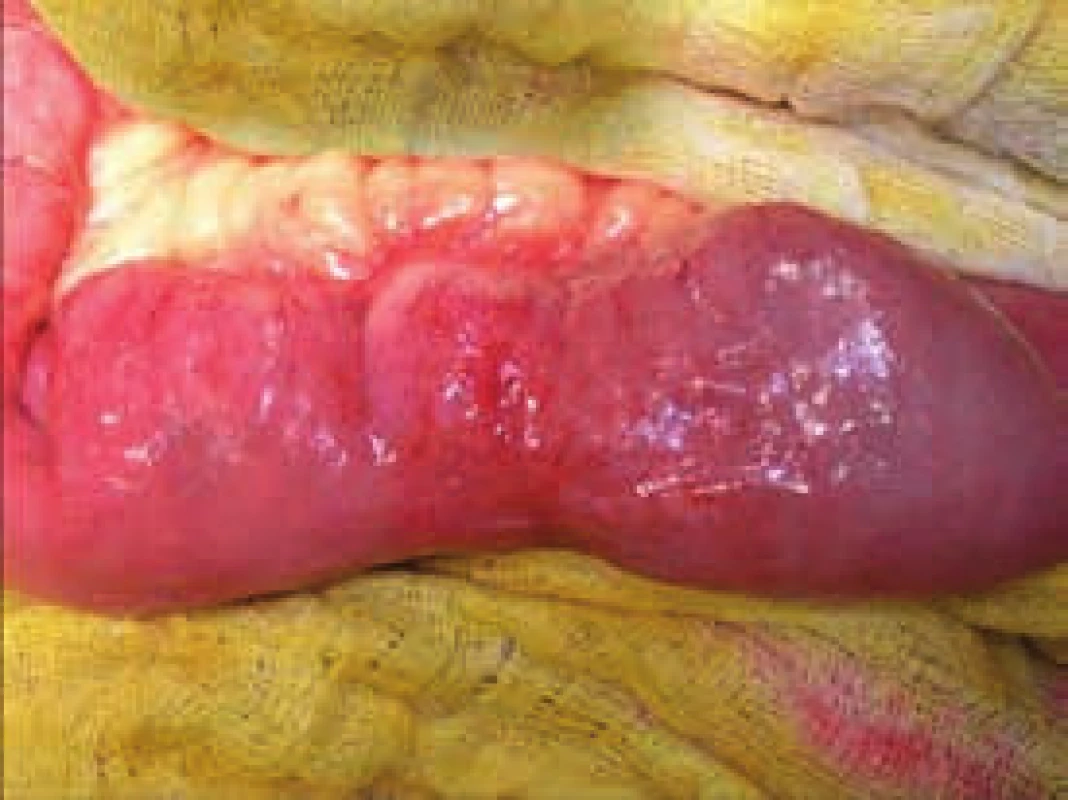
Birminghamská kritéria pooperačních komplikací
Yamamota et al z Univerzitní nemocnice v Birminghamu zpracovali výsledky 1 008 anastomóz u 566 operací pro Crohnovu chorobu. Ze statistického zpracování výsledků se podařilo definovat rizikové faktory pro rozvoj pooperačních komplikací [32].
Birminghamská kritéria:
- albumin nižší než 30 g/l
- předoperační léčba kortikoidy
- peroperačně objevený absces
- peroperačně objevená píštěl
Riziko komplikací vychází z počtu peroperačně zjištěných kritérií:
- přítomnost 0 kritéria 5 %
- přítomnost 1 kritéria 14 %
- přítomnost 2 kritérií 16 %
- přítomnost 3 kritérií 29 %
- přítomnost 4 kritérií 50 %
V případě výskytu 2 a více kritérií u jednoho pacienta je ke zvážení vícedobé operační řešení, tzn. resekční zákrok se stomií v první době vzhledem k vysokému riziku při hojení anastomózy s obnovením kontinuity s časovým odstupem.
Luminální postižení tlustého střeva
Chirurgický přístup k operativě nespecifických zánětů střevních se liší pro postižení tenkého a tlustého střeva. Je to dáno zejména odlišným cévním zásobením, které má vliv na vyšší procento komplikací v oblasti tlustého střeva. Při postižení tenké kličky máme obavy z četných či rozsáhlých resekcí zejména pro riziko rozvoje syndromu krátkého střeva. Problematice tlustého střeva dominuje snaha o provedení operace šetřící sfinktery s maximálním oddálením trvalého střevního vývodu. Symptomatika pacientů s postižením tlustého střeva je také odlišná, spíše se připodobňuje pacientům s ulcerózní kolitidou. Ileokolické fistulace jsme popsali již v problematice tenkého střeva, abscesové kolekce jsou u tlustého střeva méně časté, jedná se spíše o zánětlivé prosáknutí střevních závěsů a presakrálního prostoru u postižení rekta a anoperineální oblasti.
Operační řešení je indikováno vždy až po vyčerpání intenzivní konzervativní léčby. Ve srovnání s minulými lety operujeme pacienty v pozdějších stadiích onemocnění s rozvojem anti-TNFα terapie. Dlouhotrvající imunosupresivní terapie a biologická léčba udržují pacienty v uspokojivém klinickém stavu po dobu mnoha roků, ale narůstá riziko neoplazie. Další indikací k operačnímu řešení jsou akutní stavy. Jedná se zejména o krvácení a rozvoj toxického megakolon. Méně často operujeme pacienty pro perforaci. V akutních stadiích je nejčastěji indikována subtotální kolektomie s ponecháním pahýlu rekta a vyvedením terminální ileostomie. Vzhledem k obtížnějšímu odlišení ulcerózní kolitidy a crohnovské kolitidy velmi často operujeme pod diagnózou indeterminované kolitidy. Poté dle výsledku definitivní histologie volíme typ obnovení kontinuity, který se zásadně liší u jednotlivých typů nespecifických střevních zánětů.
Segmentální postižení kolon
Limitované postižení kolon je možné řešit segmentální resekcí kolon. U segmentální resekce je v literatuře popisované vyšší riziko lokální rekurence v porovnání se subtotální kolektomií [26–28]. I přes toto vyšší riziko volíme segmentální resekci jako metodu první volby v porovnání se založením trvalé stomie v první době v případě proktokolektomie.
Multisegmentální postižení kolon
Pokud se jedná o 2 krátká segmentální postižení na obou koncích kolon, tak je ke zvážení provedení 2 segmentálních resekcí. I přes vyšší riziko insuficience anastomózy při vícečetné kolické resekci je tento typ operace metodou volby při nekomplikovaném peroperačním průběhu. V případě vyššího počtu stenóz či delších úseků postižení jsou indikovány rozsáhlejší resekční zákroky. Výjimečně se jedná o pravostrannou hemikolektomii, která je spíše indikovaná u rozsáhlejšího ileocékálního postižení s přechodem na colon ascendens. Shodná je situace na levé části tračníku. Nejčastějším výkonem pro multisegmentální či extenzivní postižení je subtotální kolektomie. Pokud se jedná o selhání konzervativní terapie s plánovanou elektivní operací, pak je často možno provést primární ileorektální anastomózu při histologicky ověřené chorobě. V případě akutních operací je nejčastějším výkonem subtotální kolektomie se slepým uzávěrem pahýlu rekta a vyvedením terminální ileostomie. Dle stavu rekta v pooperačním období volíme odloženě ve druhé době buď obnovení kontinuity ileorektoanastomózou nebo nutnost abdominoperineální amputace rekta s ponecháním terminální ileostomie jako trvalé řešení.
Kontroverzní je obnovení kontinuity proktektomií s vytvořením ileoanálního J pouche – IPAA (ileal pouch-anal anastomosis). Většina studií s IPAA zahrnuje i podskupinu s Crohnovou chorobou. Jedná se o retrospektivní analýzy, které ukazují selhání pouche až v 50 % [29–31]. Při následném odstranění pouche je resekována velká část ilea, což může vyústit v syndrom krátkého střeva v případě nutnosti dalších resekčních zákroků na tenkém střevě. Jsou pracoviště, která IPAA u pacientů s Crohnovou chorobou s absencí perianálního postižení provádějí se souhlasem pacienta, který je informován o vysokém riziku selhání pouche. Na našem pracovišti IPAA pro Crohnovu chorobu neprovádíme.
Závěr
Problematika operací pro nespecifické střevní záněty je značně odlišná od operačních postupů pro nádorová onemocnění tenkého a tlustého střeva. Operační taktika a indikační rozvaha má velký vliv na krátkodobé pooperační výsledky a zejména na dlouhodobý výskyt rekurence choroby. Důležitá je vzájemná spolupráce s gastroenterologem řídícím medikamentózní léčbu a radiodiagnostikem zajišťujícím zobrazovací metody k objektivizaci probíhajícího onemocnění. S rozvojem konzervativních medikamentózních metod v posledních letech dochází k operačnímu řešení u komplikovanějších pacientů s rozsáhlým onemocněním. Z tohoto důvodu je vhodné koncentrovat takto komplikované pacienty do center specializovaných na chirurgickou léčbu nespecifických střevních zánětů.
prof. MUDr. Zdeněk Kala, CSc.
zkala@fnbrno.cz
Chirurgická klinika LF MU a FN Brno, pracoviště Bohunice, Brno
www.chirurgiebrno.cz
Doručeno do redakce 28. 5. 2014
Sources
1. Crohn BB, Ginsburg L, Oppenheimer GD. Regional ileitis: A pathological and clinical entity. JAMA 1932; 99(16): 1323–1329.
2. Heuman R, Boeryd B, Bolin T et al. The influence of disease at the margin of resection on the outcome of Crohn´s desease. Br J Surg1983; 70(9): 519–521.
3. Fazio VW, Wu JS. Surgical therapy for Crohn´s disease of the colon and rectum. Surg Clin North Am 1997; 77(1): 197–210.
4. Vermeire S, Van Assche G, Rutgeerts P. The role of C-reactive protein as an inflammatory marker in gastrointestinal diseases. Nat Clin Pract Gastroenterol hepatol 2005; 2(12): 580–586.
5. Solem CA, Loftus jr. EV, Tremaine WJ et al. Correlation of C-reactive protein with clinical, endoscopic, histologic, and radiographic activity in inflammatory bowel disease. Inflamm Bowel Dis 2005; 11(8): 707–712.
6. Cullen G, O’toole A, Keegan D et al. Long-term clinical results of ileocecal resection for Crohn’s disease. Inflamm Bowel Dis 2007; 13(11): 1369–1373.
7. Aratari A, Papi C, Leandro G et al. Early versus late surgery for ileo-caecal Crohn´s disease. Aliment Pharmacol Ther 2007; 26(10): 1303–1312.
8. Tilney HS, Constantinides VA, Heriot AG et al. Comparison of laparoscopic and open ileocecal resection for Crohn´s disease: a metaanalysis. Surg Endosc 2006; 20(7): 1036–1044.
9. Lesperance K, Marin MJ, Lehmann R et al. National trends and outcomes for the surgical therapy of ileocolonic Crohn´s disease: a population-based analysis of laparoscopis vs. open approaches. J Gastrointest Surg 2009; 13(7): 1251–1259.
10. Eshuis EJ, Polle SW, Slors JF et al. Long-termi surgical recurrence, morbidity, quality of life, and body image of laparoscopic assisted vs. open ileocolic resection for Crohn´s disease: a comparative study. Dis Colon Rectum 2008; 51(6): 858–867.
11. Hashemi M, Novell JR, Lewis AA. Side-to-side stapeled anastomosis may delay recurrence in Crohn´s disease. Dis Colon Rectum 1998; 41(10): 1293–1296.
12. Yamamoto T, Bain IM, Mylonakis E et al. Stapeled functional end-to-end anastomosis versus sutured end-to-end anastomosis after ileocolonic resection in Crohn disease. Scand J Gastroenterol 1999; 34(7): 708–713.
13. Ikeuchi H, Kusunoki M, Yamamura T. Long-term results of stapeled and hand-sewn anastomoses in patients with Crohn´s disease. Dig Surg 2000; 17(5): 493–496.
14. Similis C, Purkayastha S, Yamamoto T et al. A meta-analysis comparing conventional end-to-end anastomosis vs. other anastomotic configurations after resection in Crohn´s disease. Dis Colon Rectum 2007; 50(10): 1674–1687.
15. Gervais DA, Hahn PF, O´Neill MJ et al. Percutaneous abscess drainage in Crohn disease: technical success and short - and long-term outcomes during 14 years. Radiology 2002; 222(3): 645–651.
16. Garcia JC, Persky SE, Bonis PA et al. Abscesses in Crohn´s disease: outcome of medical versus surgical treatment. J Clin Gastroenterol 2001; 32(5): 409–412.
17. Yamaguchi A, Matsui T, Sakurai T. The clinical characteristics and outcome of intraabdominal abscess in Crohn´s disease. J Gastroenterol 2004; 39(5): 441–448.
18. Bouhnik Y, Panis Y. Therapeutic strategies of fistulous Crohn’s disease: medical or surgical treatment? Gastroenterol Clin Biol 2003; 27(Suppl 3): S98-S103.
19. Young-Fadok TM, Wolff BG, Meagher A et al. Surgical Management of ileosigmoid fistulas in Crohn´s disease. Dis Colon Rectum 1997; 40(5): 558–561.
20. Solem CA, Loftus jr. EV, Tremaine W et al. Fistulas to the urinary system in Crohn´s disease: clinical features and outcomes. Am J Gastroenterol 2002; 97(9): 2300–2305.
21. Sampietro GM, Sartani A, Danelli P. Stricturoplasty in the surgical treatment of complicated Crohn´s disease. Ann Ital Chir 2000; 74(6): 659–663.
22. Shatari T, Clark MA, Yamamoto T. Long stricturoplasty is as safe and effective as short stricturoplasty in small-bowel Crohn´s disease. Colorectal Dis 2004; 6(6): 438–441.
23. Tichansky D, Cagir B, Yoo E et al. Stricturoplasty for Crohn´s disease: metaanalysis. Dis Colon Rectum 2000; 43(7): 911–919.
24. Yamamoto T, Fazio VW, Tekkis PP. Safety and efficacy of stricturoplasty for Crohn´s disease: a systematic review and metaanalysis. Dis Colon Rectum 2007; 50(11): 1968–1986.
25. Fichera A, Lovadina S, Rubin M et al. Patterns and operative treatment of recurrent Crohn´s disease. a prospective longitudinal study. Surgery 2006; 140(4): 649–654.
26. Allan A, Andrews H, Hilton CJ. Segmental colonic resection is an appropriate operation for short skip lesions due to Crohn´s disease in the colon. World J Surg 1989; 13(5): 611–664.
27. Maartense S, Dunker MS, Slors JF et al. Laparoscopic-assisted versus open ileocolic resection for Crohn´s disease: a randomised trial. Ann Surg 2006; 243(2): 143–149.
28. Yamamoto T, Bain IM, Mylonakis E et al. Stapled functional end-to-end anastomosis versus sutured end-to-end anastomosis after ileocolonic resection in Crohn´s diesease. Scand J Gastroenterol 1999; 34(7): 708–713.
29. Panis Y, Poupard B, Nemeth J. Ileal pouch/anal anastomosis for Crohn´s disease. Lancet 1996; 347(9005): 854–857.
30. de Oca J, Sanchez-Santos R, Rague JM. Long-term results of ileal pouch-anal anastomosis in Crohn´s disease. Inflamm Bowel Dis 2003; 9(3): 171–175.
31. Mylonakis E, Allan RN, Keighley MR. How does pouch construction for a final diagnosis of Crohn´s disease compare with ileoproctostomy for established Crohn´s proctocolitis? Dis Colon Rectum 2001; 44(8): 1137–1142.
32. Yamamoto T, Allan RN, Keighley MR. Risk factors for intra-abdominal sepsis after surgery in Crohn´s disease. Dis Colon Rectum 2000; 43(8): 1141–1145.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2014 Issue 7-8
-
All articles in this issue
- Effect of the liquid milk nutritional supplement with enhanced content of whey protein on the nutritional status of the elderly
- Celiac disease in adult patients with type 1 diabetes mellitus
- Acute pancreatitis – Validation of Revised Atlanta Classification on 159 patients and prognostic factors
- Genetics and pharmacogenetics of osteoporosis
- Importance of lymphangiogenesis and ultrastructure of lymphatic capillaries in metastasis of malignant melanoma
- What is new in heart failure with preserved ejection fraction within last five years?
- Specifics of diabetes mellitus in women
- Osteoporosis and bone alterations in celiac disease in adults
- Education model at the Clinic of Internal Medicine of the Faculty Hospital Motol Prague – Our experience with local education project for young physicians on postgraduate education
-
Zdeněk Mařatka and his share in the founding of the Czech Gastroenterological Society and its journal.
Gastroenterological Society in Czech and Slovac republics - Crohn's Disease Surgery
- Advances in diagnosis and therapy of inflammatory bowel diseases
- Biological therapy in women with inflammatory bowel disease during pregnancy
- Crohn’s disease – etiopathogenetic factors
- Etiology and pathogenesis of inflammatory bowel diseases
- History of surgical treatment of non-specific inflammatory bowel diseases
- Epidemiology of dyspepsia
- Management of patients with dyspepsia
- Endoscopic classification of colon and rectal neoplasias
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Endoscopic classification of colon and rectal neoplasias
- Acute pancreatitis – Validation of Revised Atlanta Classification on 159 patients and prognostic factors
- Crohn's Disease Surgery
- Management of patients with dyspepsia
