Geriatrický nemocný v onkologii
Geriatric patient in oncology
At the beginning of the article there are mentioned the stages of human life breakdown and breakdown of senior age by stages approximately corresponding to functional efficiency. Attention is paid to a specific geriatric regime respecting the differences of senior age. Article emphasizes the role of comprehensive geriatric assessment including evaluation of psychological changes and social aspects in accordance to optimal geriatric approach. Diagnostic strategy and oncology treatment in terms of prognosis and expected goals are also described. There are discussed the specifics of diseases in elderly patients in the cancer context. Present work reviews the differences between calendar and biological age with possibility to segregate seniors and to avoid inadequate palliative care. Finally, the author discusses the aspects of supportive care for seniors and polypharmacotherapy with its potential risk.
Keywords:
functional geriatric examination – palliative care – polypharmacotherapy – specific geriatric regime – supportive care – specifics of diseases in elderly patients
Authors:
Hana Matějovská Kubešová
Authors‘ workplace:
Klinika interní, geriatrie a praktického lékařství LF MU a FN Brno, pracoviště Bohunice, přednostka prof. MUDr. Hana Matějovská Kubešová, CSc.
Published in:
Vnitř Lék 2014; 60(Suppl 2): 46-53
Category:
70th Birthday - prof. MUDr. Jiří Vorlíček, CSc.
Overview
V úvodu článku je připomenuto členění lidského života na věkové etapy a dále členění seniorského věku podle etap přibližně odpovídajících funkční zdatnosti. Pozornost je věnována specifickému geriatrickému režimu jako metodě respektující odlišnosti seniorského věku. Je zdůrazněna role komplexního geriatrického vyšetření včetně posouzení psychických změn a sociálních aspektů při optimalizaci přístupu ke staršímu nemocnému z hlediska strategie diagnostiky a léčby onkologických onemocnění vzhledem k prognóze nemocného a očekávanému cíli u konkrétního nemocného. V kontextu onkologického onemocnění je pojednáno i o specificích chorob ve vyšším věku, je řešen rozdíl mezi kalendářním a biologickým věkem nemocných z hlediska možné segregace seniorů a neadekvátně paliativního přístupu. V závěru článku jsou diskutovány aspekty podpůrné péče u seniorů a polyfarmakoterapie s jejími možnými riziky.
Klíčová slova:
funkční geriatrické vyšetření – paliativní péče – podpůrná péče – polyfarmakoterapie – specifický geriatrický režim – specifika chorob ve stáří
Úvod
Současná geriatrická medicína usiluje o co nejdelší zachování přiměřené tělesné a duševní aktivity, odvrácení ztráty soběstačnosti a zlepšení prognózy seniorů v případě onemocnění. Má tedy intervenčně preventivní charakter a podporuje úspěšné zdravé stárnutí. Náplní a cílem moderní geriatrie jako medicínského oboru je zvládání modifikovaného klinického obrazu chorob a zdravotně-sociálních problémů seniorů s následným prodloužením let aktivního života a udržení funkčních kapacit co nejdéle.
Dnes je za počátek stáří vesměs považován věk 65 let a o vlastním stáří se hovoří od 75 roků. Z tohoto pojetí je odvozeno i současně nejčastěji užívané členění stáří:
- věk 65–74 let – mladí senioři (young old), orientačně dominuje problematika penzionování, volného času, aktivit, seberealizace
- věk 75–84 let – staří senioři (old old), problematika adaptace, tolerance zátěže, specifického stonání, osamělosti; Věk nad 75 roků, kdy začíná stáří v užším slova smyslu, se jeví jako zlomový bod ontogeneze, kdy dochází k rozvoji významnějších změn spojovaných s fyziologickým stárnutím
- věk 85 let a více – dlouhověcí senioři (oldest old) bývá vyčleňován jako samostatná kategorie pro vysoký počet výskytu křehkých seniorů a vysoké riziko možnosti vzniku náhlé závislosti; Součástí této skupiny jsou však také senioři, jimž se vyhnuly závažnější zdravotní komplikace ať již z důvodu celoživotního zdravého stylu či genetické predispozice [1–3].
Demografická prognóza české populace do budoucnosti předpokládá vzestup počtu seniorů na dvojnásobek, z dnešních 1 500 000 na 3 000 000 osob. Očekává se další prodloužení střední délky života až o 4 roky u obou pohlaví, tedy ze současných 76 let na 80 let u mužů a z 81 let na 85 let u žen. Počet osob ve staří nad 65 roků věku bude tvořit 30–33 % celé populace, počet osob starších 80 let se do roku 2050 ztrojnásobí (graf).
![Analýza současné demografické situace a prognóza pro rok 2050 [4]](https://pl-master.mdcdn.cz/media/image/5c4d68d91d993b8c168609dafe83075c.png?version=1537794170)
Podobně jako ve společnosti dochází také k významnému stárnutí klientely zdravotnických zařízení – k tzv. geriatrizaci medicíny. Následkem tohoto stavu je nutno modifikovat přístup ke starším nemocným. Souhrnně je tento změněný přístup nazýván specifickým geriatrickým režimem. Tato skutečnost se významně prolíná do všech odvětví medicíny – a to první linií počínaje a nejrůznějšími specializacemi konče [5].
Specifický geriatrický režim zahrnuje:
- individualizovanou – konkrétnímu nemocnému přiměřenou diagnostiku a terapii s cílem zlepšení kvality života
- léčebnou rehabilitaci v rozsahu potřebném pro zachování/obnovení soběstačnosti
- aktivní přístup celého multidisciplinárního týmu se zaměřením na zlepšení soběstačnosti
- sociální práci s cílem vytvoření podmínek dovolujících návrat do domácího prostředí
Z uvedeného přístupu profituje zejména starší pacient ohrožený specifickými riziky:
- atypickým průběhem více chorob vzájemně se ovlivňujících
- možností vzniku časné poruchy orgánové funkce vyčerpáním funkční rezervy (plíce, ledviny atd)
- rozvojem imobilizačního syndromu
- ztrátou soběstačnosti
- maladaptací na změny
- věkovou diskriminací (ageizmus) [3,5]
Základním nástrojem zhodnocení reálného stavu nemocného je komplexní geriatrické vyšetření, jehož výsledky jsou využívány v rozhodovacím procesu diagnostiky a terapie u konkrétního nemocného. Komplexní geriatrické vyšetření se zabývá fyzickým stavem, psychickým stavem a sociálními podmínkami nemocného.
Funkční geriatrické vyšetření
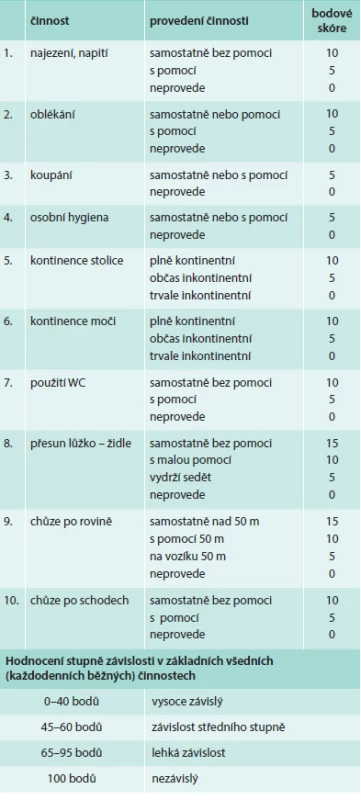
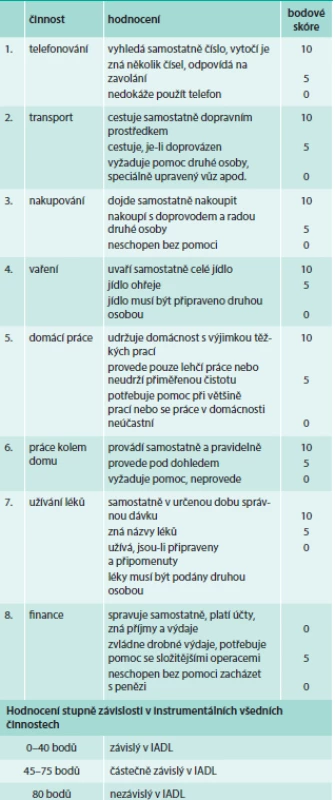
Zhodnocení soběstačnosti z pohledu nutnosti pomoci zvenčí k udržení adekvátní kvality života seniora je nejčastěji prováděno dnes stále šířeji zaváděnými testy ADL (activities of daily living) a IADL (instrumental activities of daily living), tab. 1 a 2. Výsledky obou testů vyjádří míru závislosti nemocného, tedy zda a jakou asistenci zvenčí nemocný potřebuje.
Posouzení psychického stavu
Psychický stav seniora může zásadním způsobem ovlivnit výsledek léčebných snah – např. depresivní nemocný se méně snaží, vyhýbá se rehabilitaci, vynechává medikaci a podobně, a může tak dospět k podstatně horším výsledkům léčby. Vyhodnocení psychického stavu zahrnuje jednak vyšetření paměťových funkcí – nejčastěji je používán test MMSE (mini mental state examination), tab. 3 [6].

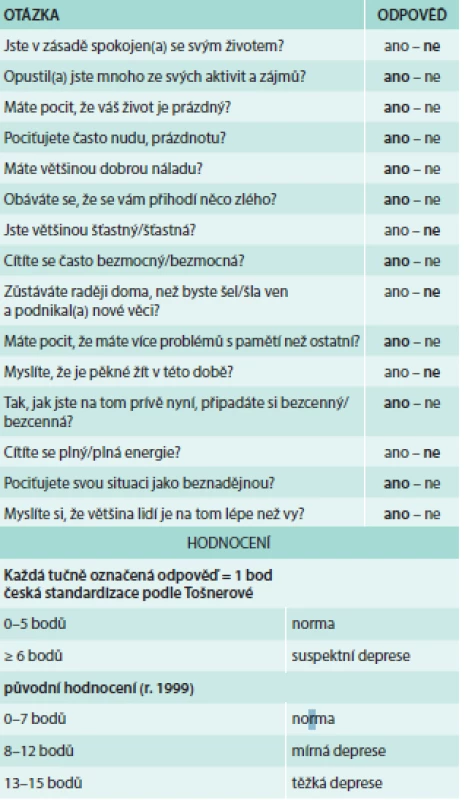
Dalším aspektem, který vyhodnocujeme, je přítomnost deprese, která je u starších nemocných často přehlížena nebo považována za „běžný smutek“. K testování slouží škála deprese podle Sheikha-Yesavage, jejímž výsledkem je vyhodnocení přítomnosti a závažnosti deprese (tab. 4) [7].
Psychický stav seniora může doznat i velmi náhlých, ale přechodných změn v případě amentně-delirantních stavů, jejichž příčinou je nejčastěji dehydratace, počínající infekci či iontové dysbalance. Tyto stavy ale po svém odeznění nemají u většiny nemocných dlouhodobější vliv na stav kognice.
Sociální diagnostika
Musí být u geriatrických nemocných velmi podrobná a mnohdy rozhoduje o dalších postupech léčby a rehabilitace. Nejdůležitější je získat přehled o dosud využívaných sociálních službách, o reálných podmínkách v bydlišti nemocného a dále o schopnostech, možnostech a ochotě příbuzných či jiných pečovatelů poskytnout náležitou péči. Podle zjištěných fakt se odvíjí plánování další péče doma, v léčebně dlouhodobě nemocných či v ústavu sociální péče. Plánování propuštění je pro seniory i jejich pečovatele velmi prospěšnou záležitostí, protože v mezidobí mezi odezněním akutní fáze onemocnění a propuštěním z nemocnice mají pečovatelé šanci se seznámit s nutnými úkony a pod dohledem nemocničního personálu se zacvičit v jejich provádění, případně provést náležité úpravy v domácnosti seniora.
Nedílnou součástí plánovaného propuštění je vazba na agentury domácí péče či mobilní hospicové péče, které naváží na léčebnou péči aplikovanou za hospitalizace, dále pomáhají v zaškolení pečovatelů a v řešení případných dalších zdravotních komplikací [9].
Specifické rysy chorob ve stáří
Vzájemným působením – stárnutí na jedné a choroby na druhé straně vznikají specifika chorob ve stáří. K zvláštnostem onemocnění ve vyšším věku patří:
- multimorbidita – souběžná přítomnost více onemocnění u jednoho jedince buď bez příčinné souvislosti, nebo chorob navzájem se kauzálně podmiňujících.
- vzájemná podmíněnost zdravotní a sociální situace – každá změna zdravotního stavu staršího člověka může významně ovlivňovat jeho sociální vztahy a naopak.
- zvláštnosti klinického obrazu chorob ve stáří:
- mikrosymptomatologie – minimální příznaky choroby („fenomén ledovce“)
- monosymptomatologie nebo oligosymptomatologie – ojedinělé z běžně se vyskytujících příznaků, pokud se nemoc objevila ve středním nebo mladším věku
- vzdálené příznaky – v popředí klinického obrazu jsou symptomy, které odpovídají potížím jiného orgánu než je základní onemocnění; obvykle se jedná o 2 nejkřehčí orgány seniorského organizmu – srdce a mozek (např. zmatenost jako první příznak urosepse)
- sklon k chronicitě – i u chorob v mladším a středním věku typicky akutních, navíc je ve stáří i vyšší riziko úmrtí
- sklon ke komplikacím – buď typu „řetězová reakce“ (jedna nemoc vyvolává druhou) nebo jde o komplikaci, která k ní nemá přímý vztah („fenomén vytěsnění“)
- delší doba rekonvalescence [1,3]
Vlastní symptomatologie základního onemocnění bývá nenápadná. Klinickému obrazu obvykle dominují projevy nespecifické a univerzální ze sekundární dekompenzace mozkové činnosti. Patří k nim obvykle univerzální neurologicko-psychiatrická symptomatologie podmíněná hypoperfuzí (hypoxií) mozku (TIA, delirium atp). Mozek seniora bývá postižen degenerativními či vaskulárními změnami a reaguje na změny obvykle jako první orgán.
Mezi příčinami morbidity ve stáří zaujímají přední místo choroby kardiovaskulárního systému podmíněné aterosklerózou (AS), jako ICHS, IM, angina pectoris, CMP, TIA, ICHDKK (AS je přítomna až u 90 % osob starších 75 roků věku). Ve stáří jsou rovněž časté choroby pohybového ústrojí, smyslových orgánů, nádory, úrazy, choroby respiračního (CHOPN), gastrointestinálního (biliární a jiné potíže) a urogenitálního systému (u mužů prostata, u žen gynekologické orgány). Časté jsou i cukrovka, duševní a nervové choroby. Jejich současná na sobě mnohdy nezávislá koexistence je typická právě pro stařeckou multimorbiditu.
Pro kvalitu života seniora není rozhodující přítomnost samotné choroby (nebo více nemocí), ale stupeň disability, tj. funkčního postižení, ke kterému ve svém důsledku vede. Plná soběstačnost přitom může být zachována i v přítomnosti mnoha chorob současně.
Senioři jsou obecně vulnerabilnější onemocněními a rovnováha jejich orgánové homeostázy je značně křehká. Klinickým obrazem selhání adaptace na bázi chronického stresu ve stáří je geriatrický maladaptační syndrom. Stresor je obvykle v psychosociální oblasti a jeho klinická manifestace nastává nejčastěji v kardiovaskulární oblasti (IM, CMP) nebo ve zhoršení imunity (bronchopneumonie) [10].
Jak již bylo uvedeno, nemoci a chorobné stavy ve stáří se vyznačují četnými zvláštnostmi. Nemoci ve stáří mají tendenci se kumulovat a vzájemně potencovat. V geriatrické medicíně je typická vícerozměrnost. Nemocného jako bio-psycho-sociální jednotku je třeba ve stáří chápat daleko více holisticky (tj. celostně), než v mladších věkových obdobích, a to jak z pohledu etiopatogeneze choroby, tak i každodenní klinické praxi.
Uvedené problémy somatické, psychické a sociální se ve vzájemné interakci vyznačují „obtížnou léčitelností“, chronickým průběhem s progresí a relativně nepříznivou prognózou. Nemocnému a jeho okolí přinášejí mnoho jen velmi obtížně zvladatelných situací a problémů a vyžadují i odlišný přístup umožňující zlepšení zdravotního stavu nebo alespoň udržení stávající soběstačnosti a akcentující návrat do domácího prostředí.
Senior a onkologické onemocnění
Počátek diagnostiky onkologických onemocnění u starších nemocných může být značně opožděný většinou pro určité váhání nemocného v rozhodnutí, kdy se vydat k lékaři. Samotné diagnostické procedury mohou následovat jedna po druhé také se zpožděními danými souběžně probíhajícími chorobami. Tímto způsobem může mnohdy dojít k promeškání vhodné periody, v níž by nemocný byl ještě schopen podstoupit i agresivnější typy onkologické terapie s vyšší nadějí na uspokojivý výsledek. Na druhé straně mnoho seniorů je schopných zvládnout celý proces diagnostiky a komplexní onkologické terapie překvapivě hladce.
V rozhodování o strategii onkologické terapie seniora obecně hraje roli mnoho faktorů. S prodlužující se střední dobou života se senioři dožívají svých duplicit i triplicit nádorů – po předchozí absolvované onkologická léčba musíme předpokládat nižší míru funkčních rezerv nemocného. Je otázkou, jaký postup vyšetření volit a s jakým očekávaným dopadem na volbu léčebné strategie – zvláště v případech, v nichž je zřejmé, že nebude možno léčit kauzálně, ztrácí stanovení přesné diagnózy za cenu zatěžování nemocného svůj význam.
Naopak někdy napomohou k časné diagnostice patologické stavy, které mohou být varovnými znameními počátečních fází malignity – flebotrombóza vzniklá za nejasných okolností, nově vzniklá „alergie“, která může být kožním projevem paraneoplazie, recidivující infekce, nejasná anemizace, hypochromie, vysoká sedimentace erytrocytů, neklesající aktivita CRP, neklesající sérová koncentrace D-dimerů, hemoptýza, subfebrilie. Cílené pátrání po malignitě při těchto stavech může vést k velmi časné diagnóze samozřejmě s vysokou šancí pro daného seniora.
Vlastní rozhodování o léčebné strategii může být ve stáří ovlivněno také mnoha faktory. Např. rozdílem mezi biologickým a kalendářním věkem, sociálními vlivy, při nichž senior mnohdy myslí více na svého nemohoucího partnera a odmítá další vyšetření či hospitalizaci a v neposlední řadě vlivem příbuzných a blízkých, jejichž rady mohou seniora na jedné straně pozitivně motivovat, ale také způsobit např. odmítnutí zásadní diagnostické procedury.
Mnohdy se setkáváme s tendencí segregovat starší nemocné od modernějších nákladných, i když efektivních vyšetřovacích a léčebných metod. Dalším nepříznivým trendem je považovat seniory příliš brzy za neschopné absolvovat adekvátní terapii a přistupovat k jejich chorobám mnohdy neadekvátně paliativně.
Hlavní oblasti podpůrné terapie u seniorů
Funkční rezerva kardiovaskulárního aparátu může zkomplikovat situace, v nichž je žádoucí docílit vyššího obratu tekutin, jako je prehydratace při podání některých typů chemoterapie, snaha o snížení osmotické zátěže při sepsi apod. Nejčastějším projevem objemového přetížení oběhu je dušnost až po obraz plicního edému, u léčených hypertoniků není výjimkou vzestup krevního tlaku až do hodnot hypertenzní krize. Při současné hypoproteinemii se obvykle objevují gravitační edémy [11].
Důsledky radioterapie a chemoterapie mohou u staršího nemocného nabýt intenzivnějších rozměrů s velmi pomalou regresí a jsou obvykle příčinou prodlužování intervalů mezi jednotlivými aplikacemi. Použití např. růstových faktorů ke zkrácení neutropenie po chemoterapii se u staršího nemocného nemusí vzhledem k nízké funkční rezervě krvetvorby setkat s očekávaným efektem [12].
Infekční komplikace vzniklé u seniorů obecně, ale i u seniorů s nádorovým onemocněním mohou mít neobvyklou symptomatologii – slabost dolních končetin, pády, synkopy, „celkové zhoršení stavu“, nepřijímání stravy a tekutin, delirantní stavy. Tím může být odvedena pozornost od problému hlavního, tedy akutní infekce. Akutní stav u seniora vyžaduje vždy akutní řešení – čím hlouběji necháme seniora propadnout do vznikající komplikace, tím déle potom trvá její léčení a snižují se šance nemocného na uspokojivý výsledek. Fulminance infekcí je ve vyšším věku vyšší včetně rychlého vzniku septického šoku a rychlejšího propadu do těžké malnutrice, renálního selhání a dysbalancí. Terapie širokospektrými antibiotiky zavedená nejprve empiricky a později případně upravená podle výsledků kultivací je nevyhnutelná, znamená však vyšší hrozbu přidružení se infekce patogenem Clostridium difficile – u velmi vyčerpaného seniora vysokého věku i s možností fatálního zakončení [13,14].
Poruchy výživy jsou v seniorském věku velmi časté – nejčastěji v podobě hypoproteinemie, byť na první pohled se senior jako malnutriční nemusí jevit. Dlouhodobé upřednostňování převážně sacharidové stravy pro její snadnou přípravu, snadnou stravitelnost a také nižší ekonomickou náročnost může vést u seniora k obezitě, nicméně s nedostatkem bílkovin, vitaminů, minerálů a stopových prvků – tedy k obezitě malnutriční. Malnutrice samotná potom znamená závažný rizikový faktor vzniku dekubitů a dalších nehojících se ran, zvyšuje riziko infekčních komplikací a zpomaluje postup rehabilitace [15,16].
Vnímání bolesti není ve stáří sníženo a bolest by neměla být okolím vnímána jako nutný doprovodný příznak samotného vyššího věku. Senioři často neprezentují bolest – jsou na její určitou hladinu přivyklí. Navíc může sdělení údajů o přítomnosti bolesti a její intenzitě bránit přítomnost kognitivní poruchy. Používané škály bolesti většinou nejsou přizpůsobené starším nemocným a nemocný s demencí nemusí být schopen pochopit práci se škálou. V tom případě se soustředíme na druhotné projevy bolesti – neklid, zrychlení tepové frekvence, zvýšení krevního tlaku, zhoršení chuti k jídlu, zhoršení spánku. I u nemocného bez kognitivního deficitu může vnímání bolesti a její prezentace navenek ovlivňovat ve smyslu pozitivním i negativním psychické rozpoložení a sociální situace nemocného [17].
V léčbě bolesti u seniorů se řídíme obecnými pravidly stupnice WHO, je však nutno předpokládat změny farmakokinetiky a farmakodynamiky podávaných analgetik. Obecně je možno v seniorské populaci pozorovat nejspíše pro vysoký výskyt osteoartrózy a spondylartrózy nadužívání nesteroidních antirevmatik, z nichž většina je dnes volně dostupných. Výskyt vedlejších účinků analgetik je v seniorské populace vyšší – nejčastěji v podobě rizika gastrointestinálního krvácení, renálního selhání či dekompenzace hypertenze.
Skupina opioidů je ovšem u nemocných vyššího věku využívána nedostatečně stejně jako u nemocných mladších věkových skupin. Ve snaze o zachování přiměřené kvality života bychom u onkologických nemocných vyššího věku při neúspěchu nebo limitované účinnosti neopioidních analgetik nebo slabých opioidů neměli se zahájením terapie silnými opioidy váhat. Aktuálně dostupné náplasťové formy zajistí postupné uvolňování a jsou výhodné u nemocných s kognitivní poruchou se sníženou mírou kompliance. Naopak oblíbený a upřednostňovaný tramadol vyvolává velmi často stavy zmatenosti a poruchy kinetiky trávicího traktu, a je proto u seniorské populace nevhodný [18].
Rizika polyfarmakoterapie
Přibývající počet chorob ve stáří vede ke zvyšování počtu užívaných léků. Hlavním rizikem užívání vyššího počtu druhů léků je nárůst výskytu nežádoucích účinků léčby. Při průměrném počtu 6 užívaných druhů léků musíme očekávat výskyt nežádoucích účinků u každého desátého nemocného. Z hlediska lékových interakcí je nutno kalkulovat exponenciální nárůst, tedy při zvažovaném průměrném počtu 6 užívaných druhů léků musíme očekávat okolo 40–50 lékových interakcí, i když samozřejmě zdaleka ne všechny možné interakce jsou klinicky závažné. Za nejzávažnější nutno považovat interakce warfarinu, perorálních antidiabetik, benzodiazepinů, prednisonu, digoxinu, které při podávání současně s dalšími léčivy mohou podstatným způsobem ovlivnit jejich účinnost či výskyt nežádoucích vedlejších účinků.
Mnoha studiemi je ovšem prokázáno, že čím vyšší počet léků nemocný užívá, tím vyššího počtu chyb se dopouští, a tím více klesá jeho kompliance.
Součet, či možná spíše součin těchto vlivů potom dává známý fakt, že až 28 % hospitalizací seniorů je způsobeno chybami v užívání léků nebo nežádoucími účinky medikace nebo lékovými interakcemi [19].
Rizika farmakoterapie starších nemocných vyplývající z přidružených chorob a dysability
Přítomnost přidružených chorob zvyšuje zásadním způsobem riziko výskytu lékových interakcí, a to jednak interakce lék vs lék, ale také interakce lék vs choroba či lék vs strava. Z pohledu nežádoucích interakcí nejrůznějšího druhu byla vypracována kritéria hodnocení léků [20,21] a na základě jejich použití vznikl seznam léků nevhodných pro seniory, z nichž však mnohé jsou v rutinní praxi běžně používány jednak z neznalosti, ale také proto že za ně dosud není adekvátní náhrada [22].
Dysabilita ovlivňuje negativním způsobem komplianci starších nemocných – senzorické postižení vede k chybám v dávkování léků – chybně přečtené lékové schéma, motorické postižení může např. znemožnit otevření lahvičky s lékem či rozsypání léku. Kognitivní porucha vede často buď k vynechání dávky léků – nemocný se domnívá, že léky již užil, nebo častěji k užití dvojí dávky protože nemocný se domnívá, že léky toho dne ještě neužil.
Sociální faktory ovlivňující farmakoterapii starších nemocných
Sociální faktory mohou ovlivnit farmakoterapii starších nemocných v kladném i záporném smyslu. I těžce dysaptibilní nemocný s mnoha chorobami a deficity může mít bezchybnou farmakoterapii zajištěnou spolupracující rodinou či jiným zodpovědným pečovatelem. Naopak osaměle žijící senior s jen drobným kognitivním deficitem může vlivem jedné malé, nicméně mnohokrát opakované chyby v medikaci dospět až např. k těžkému předávkování léku.
K sociálním faktorům musíme započítat také finanční náročnost medikace a, bohužel, si musíme uvědomit opakovaně prokázaný fakt, že nejhorší komplianci je možno očekávat u léků s nejvyšším doplatkem.
Selfmedication/samoléčení – volně dostupné léky
Věková skupina pacientů v rozmezí 60–75 let tvoří 15 % populace, ale tato skupina se podílí 33 % na konzumaci léků na předpis a na 40 % léků volně prodejných. Téměř 60 % seniorů nakupuje vitaminy, 30 % seniorů nesteroidní antirevmatika (NSA) a 43 % seniorů analgetika. Pokud si představíme konkrétní volně prodejné preparáty, jedná se ve skupině nesteroidních antirevmatik o nejrůznější firemní názvy ibuprofenu, u analgetik o paracetamol, případně i přežívající kompozitní preparáty. Jen velmi nízké procento seniorů je schopno odlišit název generický a firemní, a proto mnohdy dochází ke zdvojování a ztrojování téhož generika pod různými firemními názvy u jednoho nemocného.
Volně prodejné léky je tedy nutno považovat za podstatnou složku medikace nemocného a brát jejich nežádoucí účinky a interakce v úvahu při pátrání po příčinách záhadných zhoršení zdravotního stavu. Nemocní o užívání volně prodejných medikamentů často mlčí z obav z nelibosti ošetřujícího lékaře, ale také proto, že sami senioři nepovažují užívání medikamentu za podstatné, protože ho neužívají nijak pravidelně, a navíc je označen jako potravní doplněk. Přehled o významném vlivu volně prodejných medikamentů poskytuje údaj o podílu tržeb v lékárnách – nemocniční lékárny udávají 20–30 % prodeje bez receptu, zatímco lékárny na exponovaných místech pěších zón až 80 %.
Naši pozornost vyžadují produkty rostlinné, protože k těm se řada nemocných obrací jako k „zaručeně přírodním, a tudíž neškodným“. Je však známo, že produkty rostlinného původu mohou být kontaminovány pesticidy, v případě čajů plísněmi, složení těchto produktů je velmi nekonstantní a kolísá podle složení půdy, na které daná rostlina vyrostla. Prakticky každý rostlinný produkt je mnohasložkový, tedy jeho vlivem narůstá právě riziko interakcí s předepsanou léčbou a pravděpodobnost vyššího výskytu nežádoucích účinků.
Zvláště u seniorů s onkologickým onemocněním může být tendence k samoléčení velmi vysoká i vlivem snahy rodiny a blízkých podpořit proces léčby.
Z hlediska psychologického přístupu se snažíme o podporu nemocného se zachováváním obecných pravidel zvládání zátěžových situací, u seniorské populace se však můžeme setkat s jistou limitací motivace k dalšímu boji s chorobou. Studie na toto téma přinášejí mnohdy překvapivá zjištění – některé situace považují senioři za „horší než smrt“. Je to zejména život na přístrojích, který je nepřijatelný pro 60 % seniorů, ztráta mentálních schopností pro 40 %, přítomnost stálé bolesti by nesneslo 33 %, smrt oproti stavu být trvalou zátěží pro rodinu by upřednostnilo 33 % seniorů a smrt oproti ztrátě soběstačnosti 24 %. Respektování těchto názorů může přístup k nemocnému poněkud zkomplikovat, nicméně vlídný, chápavý a pozorný přístup ke staršímu onkologickému nemocnému se snahou o zachování jeho důstojnosti nepochybně vždy povede k významnému zlepšení kvality jeho života.
Závěrem
- se zvyšujícím se věkem se zvyšuje pravděpodobnost onkologického onemocnění, duplicit, triplicit
- i v seniorském věku je šance na časnou diagnostiku nádoru
- dobře připravený senior v dobrém stavu výživy je schopen absolvovat i náročnější diagnostické a terapeutické postupy
- podpůrná terapie je u seniorů komplikovanější z hlediska rizik polyfarmakoterapie
- komplikace léčby u seniorů jsou častější a závažnější, rekonvalescence je pomalejší
- senioři akceptují vývoj nemoci vyrovnaněji
prof. MUDr. Hana Matějovská Kubešová, CSc.
hkubes@med.muni.cz
Klinika interní, geriatrie a praktického lékařství LF MU a FN Brno
www.fnbrno.cz
Doručeno do redakce 25. 9. 2014
Přijato po recenzi 7. 10. 2014
Sources
1. Kalvach Z, Zadák Z, Jirák R et al. Gerontologie a geriatrie. Grada Publishing-Avicenum: Praha 2005. ISBN 80–247–0548–6.
2. Kalvach Z, Zadák Z, Jirák R et al. Geriatrické syndromy a geriatrický pacient. Grada Publishing: Praha 2008. ISBN 978–80–247–2490–4.
3. Topinková E. Geriatrie pro praxi. Galén: Praha 2005. ISBN 80–7262–365–6.
4. Demografické ročenky. Český statistický úřad. Dostupné z WWW: <http://www.czso.cz/csu/redakce.nsf/i/obyvatelstvo_lide>.
5. Weber P et al. Minimum z klinické gerontologie. NCO NZO: Brno 2000. ISBN 80–7013–314–7.
6. Folstein MF, Folstein SE, McHugh PR. Mini-mental state. A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res 1975; 12(3): 189–198.
7. Sheikh JI, Yesavage JA, Brooks JO 3rd et al. Proposed factor structure of the Geriatric Depression Scale. Int Psychogeriatr 1991; 3(1): 23–28.
8. Kubešová H, Holík J, Weber P et al. Spotřeba léčiv v seniorské populaci a rizika polyfarmakoterapie ve stáří. Čas Lék Čes 2006; 145(9): 708–711.
9. Sláma O. Palliative and hospice care in the Czech Republic and in Europe. Klin Onkol 2009; 22(4): 183–185.
10. Hegyi L, Cagán S. Geriatric maladaptation syndrome. Vnitř Lék 1994; 40(5): 325–328.
11. Matějovská Kubešová H. Akutní stavy u starších onkologicky nemocných. In: Akutní stavy v geriatrii. Galén: Praha 2009 : 215–219. ISBN 978–80–7262–620–5.
12. Weber P, Hrubanová J, Meluzínová H et al. Anemia in elderly an important diagnostic and therapeutic problem in geriatric medicine. Advances gerontology 2009; 22(4): 662–666.
13. Kubešová H. Úskalí infekčních komplikací ve stáří. Česká geriatrická revue 2008; 6(1): 6–13.
14. Bielaková K, Weber P, Matějovská Kubešová H et al. Onemocnění vyvolané Clostridium difficile u geriatrických nemocných. Čas Lék Čes 2011; 150(6): 334–338.
15. Kubešová H, Weber P. Poruchy příjmu potravy ve stáří. Interní medicína pro praxi 2008; 10(2): 64–68.
16. Meluzínová H, Weber P, Kubešová H et al. Dekubitus – komplexní pohled geriatra. Interní medicína pro praxi 2007; 9(11): 499–506.
17. Bielaková K, Matějovská Kubešová H, Weber P. Léčba bolesti u geriatrických pacientů – známe jejich úskalí? Geriatrie a gerontologie 2012; 1(2): 91–94.
18. Kubešová H, Weber P, Polcarová V et al. Léčba opioidy ve stáří a možnosti minimalizace rizik léčby. Bolest 2006; 3(3): 153–158.
19. Topinková E, Mádlová P, Weber P et al. Inappropriate prescribing in geriatric patients at hospital admission as determined by STOPP/START criteria. European Geriatric Medicine 2010; 1(Suppl 1): S79.
20. Beers MH, Ouslander JG, Rollingher I et al. Explicit criteria for determining inappropriate medication use in nursing home residents. Arch Intern Med 1991; 151(9): 1825–1832.
21. STOPP and START: New Criteria for Drug Therapy in the Elderly. STOPP START Toolkit supporting Medication review. Dostupné z WWW: <http://www.eldercarerxconsultants.com/StopStartArticle.aspx>.
22. Fialová D, Topinková E, Ballóková A et al. Expertní konsenzus ČR 2012 v oblasti léčiv a lékových postupů potenciálně nevhodných ve stáří. Klinická farmakologie a farmacie 2013; 27(1): 18–28.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2014 Issue Suppl 2
-
All articles in this issue
- Testikulární zhoubné nádory – jsme snad u konce cesty?
- Dispenzarizace nemocných po léčbě karcinomu prsu, kolorekta a prostaty
- Diferenciální diagnostika eozinofilie
- Klinické hodnocení nových léčiv u vzácných diagnóz v onkologii – současná situace v Evropě a u nás
- Paliativní péče a chronické srdeční selhání
- Vývoj a současná funkčnost informační základny české onkologické péče
- O bolesti trochu jinak
- Nové antibiotiká: potrebujeme nové molekuly, alebo nové stratégie?
- Geriatrický nemocný v onkologii
- Nové náhledy na roli lidského papilomaviru v léčbě nádorů hlavy a krku
- Ph-negativní myeloproliferativní onemocnění s trombocytemií ve světle účinku léčby přípravkem Thromboreductin® v datech registru ke konci roku 2013
- Diabetes mellitus a zhoubné nádory
- Paliativní medicína a dobrá smrt
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Diferenciální diagnostika eozinofilie
- Paliativní medicína a dobrá smrt
- Dispenzarizace nemocných po léčbě karcinomu prsu, kolorekta a prostaty
- Ph-negativní myeloproliferativní onemocnění s trombocytemií ve světle účinku léčby přípravkem Thromboreductin® v datech registru ke konci roku 2013
