Guidelines EAU pro léčbu zakřivení penisu
:
E. Wespes; K. Hatzimouratidis; I. Eardley; F. Giuliano; D. Hatzichristou; I. Moncada; A. Salonia; Y. Vardi
:
Urol List 2013; 11(1): 65-77
© European Association of Urology 2012
1. ÚVOD
Zakřivení penisu může být vrozená anomálie, ale může se vyvinout i v průběhu mužova života. Vrozené zakřivení penisu je v těchto guidelines považováno za samostatnou patologii u dospělé populace bez současného výskytu jakékoli další abnormality (např. v močové trubici). Pro informace týkající se vrozeného zakřivení penisu u dětských pacientů doporučujeme čtenáři sedmou kapitolou EAU Guidelines pro pediatrickou urologii s názvem Vrozená penilní kurvatura.
Získané zakřivení penisu je důsledkem La Peyronieho onemocnění (označováno v tomto dokumentu jako Peyronieho onemocnění), choroby pojmenované po francouzském lékaři, Francois Gigot de La Peyronie (1743), ačkoli to nebyl první lékař, který toto onemocnění popsal [1].
2. METODOLOGIE
Členové panelu provedli systémový průzkum literatury v rámci databáze Medline. V kontrolovaném slovníku databáze MeSH se pro Peyronieho onemocnění užívá speciální termín „indurace penisu“, databáze neobsahuje termín pro „vrozené zakřivení penisu“. Při vyhledávání vhodných článků tedy byla vyhledávána v MeSH hesla „vrozené abnormality“, „penis/abnormality“ a „muž“ a heslo „vrozené zakřivení penisu“ ve vyhledávači. Vzhledem k tomu, že se jedná o první guidelines zabývající se touto problematikou, byly vybrány všechny vhodné články publikované do ledna 2012. Celkem bylo nalezeno 48 článků týkajících se vrozeného zakřivení penisu a 1 200 článků týkajících se Peyronieho onemocnění. Členové panelu hodnotili všechny záznamy a vybrali články s nejvyšší úrovní důkazů. V případě některých dílčích témat však jsou k dispozici pouze důkazy nízké úrovně.
2.1 Úroveň důkazu a stupeň doporučení
Úroveň jednotlivých důkazů a stupně doporučení užívaná v těchto guidelines odpovídají definicím uvedeným v tab. 1 a 2. Cílem tohoto systému je zprostředkovat transparentní vztah mezi dostupnými důkazy a příslušným doporučením.

Při klasifikaci doporučení není souvislost mezi úrovní důkazu a stupněm doporučení zcela automatická. Důkaz publikovaný v RCT nemusí být automaticky hodnocen jako doporučení stupně A, pokud jsou publikované výsledky nekonzistentní nebo jsou shledány metodologické nedostatky. A naopak, absence důkazů vyšší úrovně nevylučuje udělení doporučení stupně A, pokud lze konkrétní důkaz podpořit rozsáhlými klinickými zkušenostmi nebo konsenzem odborníků. Existují výjimky v případě, že nelze provést průkazné studie, například z etických nebo jiných důvodů, a nejednoznačná doporučení jsou považována za užitečná.
Podobné případy jsou v textu označeny hvězdičkou jako „povýšení hodnocení na základě konsenzu panelu odborníků“. Kvalitu příslušných vědeckých důkazů je třeba při volbě příslušného stupně uvážit v kontextu benefitů, limitací, preferencí a nákladů [3–5].
Autoři EAU Guidelines neprovádí analýzu nákladů ani systematicky nehodnotí preference na lokální/národní úrovni. Autoři uvádí tuto informaci pouze v případě, že je k dispozici.
2.2 Vývoj publikace
Jedná se o novou publikaci, která byla před vydáním zaslepeně recenzována. Standardní postup bude zahrnovat každoroční hodnocení nových publikací zabývajících se touto problematikou a následnou aktualizaci guidelines. Spolu s tímto dokumentem je k dispozici jeho zkrácená verze. Všechny publikace jsou k dispozici zdarma na stránkách Evropské urologické asociace (EAU) Uroweb (http://www.uroweb.org/guidelines/online-guidelines/).
2.3 Prohlášení o potenciálním střetu zájmů
Prohlášení o potenciálním střetu zájmů jednotlivých členů panelu je k dispozici na webových stránkách EUA http://www.uroweb.org/guidelines/online-guidelines/.
3. VROZENÉ ZAKŘIVENÍ PENISU
3.1 Epidemiologie a patofyziologie
Penilní kurvatura je vzácné onemocnění: jedna ze studií uvádí méně než 1% incidenci [6], zatímco jiná studie uvádí, že se jedná o častější onemocnění o prevalenci 4–10 % při absenci hypospadie [7]. Vrozené zakřivení penisu nemá žádnou zřejmou příčinu. Jediná studie, která zkoumá ultrastrukturu tuniky albuginea, prokázala přítomnost zesílených a fragmentovaných kolagenových vláken a úplnou absenci vláknité struktury s přeměnou na elektronově denzní, fibrózní, granulomatózní materiál s nahromaděným elastinem [8].
3.2 Vyšetření pacienta
Vrozené zakřivení penisu lze obvykle diagnostikovat pouze na základě odebrání lékařské a sexuální anamnézy. Fyzikální vyšetření penisu ve ztopořeném stavu je užitečné pro popis zakřivení a vyloučení dalších patologií [9]. Erektilní funkce je normální, v případě významného zakřivení však může být narušená.
3.3 Léčba
V rámci medikamentózní léčby vrozeného zakřivení penisu byla vyzkoušena pouze aplikace androgenů, která však u dospělých pacientů nevedla k žádnému zlepšení [10]. Z tohoto důvodu je pro léčbu této choroby indikována pouze operační léčba. Operační léčba vrozeného zakřivení penisu je obvykle založena na stejných principech jako léčba Peyronieho onemocnění (detailní popis viz další kapitola), u dospělých pacientů však může být indikována kdykoli. Je zajímavé, že většina případů operační léčby Peyronieho onemocnění byla poprvé popsána u pacientů trpících vrozeným zakřivením penisu [11]. Při operaci se využívá téměř výhradně technika plikace, která dosahuje vysoké míry účinnosti (67–97 %) [12–14]. Operační technika s implantací kožního štěpu byla popsána pouze u malého vzorku pacientů, a neumožňuje tedy vyvodit žádné závěry [15].
Závěry
Vrozené zakřivení penisu lze obvykle diagnostikovat pouze na základě lékařské a sexuální anamnézy. Fyzikální vyšetření penisu ve ztopořeném stavu je užitečné pro popis zakřivení a vyloučení dalších patologií (úroveň důkazu: 3).
Jedinou terapeutickou možností je operační léčba, jež může být u dospělých pacientů indikována kdykoli. Při operaci se využívá téměř výhradně technika plikace, která dosahuje vysoké míry úspěšnosti (úroveň důkazu: 3).
4. PEYRONIEHO ONEMOCNĚNÍ
4.1 Epidemiologie, patofyziologie a přirozený vývoj
K dispozici máme pouze minimum údajů týkajících se epidemiologie Peyronieho onemocnění, uvádí se 0,4–9% míra prevalence [16–22]. Příčina vzniku této choroby není známa, obvyklou hypotézou je poranění tuniky albuginea (opakované mikrovaskulární poranění nebo trauma) [23]. Na počátku Peyronieho onemocnění je akutní zánětlivý proces. Pro akutní zánět je typická zvýšená proliferace fibroblastů v tunice albuginea, z nichž některé proliferují do myofibroblastů, s nadměrným ukládáním kolagenu, a přetrvávající fragmentace fibrinu a elastinu. Dlouhotrvající zánětlivý proces vede k přetváření pojivové tkáně a vzniku denzního fibrózního plaku [23–25]. Vznik plaku může vést k zakřivení penisu, jež může v závažných případech zabránit proniknutí do vaginy. Mezi nejčastější komorbidity a rizikové faktory patří diabetes, hypertenze, poruchy lipidového profilu, ischemická kardiopatie, erektilní dysfunkce, kouření a nadměrná konzumace alkoholu [21,22,26,27].
Dupuytrenova kontraktura se vyskytuje častěji u pacientů s Peyronieho onemocněním a postihuje 9–39 % pacientů [18,28–30], zatímco u 4 % pacientů s Dupuytrenovou kontrakturou je přítomno Peyronieho onemocnění [28]. Dosud však není zřejmé, zda tyto faktory přispívají k patofyziologii Peyronieho onemocnění, nebo nikoli. Ačkoli patogenezi této choroby bude teprve nutné prokázat, mladší muži a běloši mají vyšší riziko Peyronieho onemocnění po radikální pánevní operaci, např. radikální prostatektomii [31]. Peyronieho onemocnění může mít chronickou i progresivní povahu a rozlišují se dvě fáze [32]: první – akutní zánětlivá fáze, která může být spojena s bolestivostí penisu v ochablém stavu nebo bolestivou erekcí a projevy „měkkého“ uzlíku/plaku a zakřivením penisu. V druhé – fibrotické – fázi dochází ke vzniku tvrdého hmatného plaku, který může být kalcifikován, což vede ke stabilizaci onemocnění. Očekává se, že v průběhu času dojde ke zhoršení onemocnění u 30–50 % pacientů a stabilizaci u 47–67 % pacientů. Spontánní zlepšení bylo zaznamenáno pouze u 3–13 % pacientů [27,33,34]. Ke zmírnění zakřivení dochází s vyšší pravděpodobností v prvním stadiu onemocnění spíše než později, kdy již došlo k vytvoření plaku, který byl významně kalcifikován [35]. Bolest uvádí 35–45 % pacientů během první fáze onemocnění [36]. U 90 % mužů dojde postupně k vymizení bolesti, obvykle během prvních 12 měsíců po vypuknutí onemocnění [33,34].
Kromě fyziologických a funkčních změn penisu trpí postižení muži rovněž značným psychickým dyskomfortem. Validované dotazníky zaměřené na psychické zdraví prokázaly, že 48 % mužů s Peyronieho onemocněním má depresi mírného až středního stupně, vyžadující psychiatrické vyšetření [37].
Závěry
Peyronieho onemocnění je poruchou pojivové tkáně, pro niž je charakteristický vznik fibrotické léze nebo plaku v tunice albuginea, jež následně způsobuje deformaci penisu (úroveň důkazu: 2).
Role souvisejících komorbidních stavů a rizikových faktorů (např. diabetes, hypertenze, abnormální lipidový profil a Dupuytrenova kontraktura) v rámci patogeneze Peyronieho onemocnění není dosud známa (úroveň důkazu: 3).
Rozlišují se dvě fáze onemocnění: první – akutní zánětlivá fáze (bolestivá erekce, „měkký“ uzlík/plak), v druhé – fibrotické/kalcifikační – fázi dochází ke vzniku tvrdého hmatného plaku (stabilizace onemocnění) (úroveň důkazu: 2).
Spontánní vymizení onemocnění není běžné (3–13 % případů) a u většiny pacientů dojde k progresi (30–50 %) nebo stabilizaci onemocnění (47–67 %). Bolest se obvykle vyskytuje během počátečního stadia onemocnění, ale u většiny mužů postupně vymizí (úroveň důkazu: 3).
4.2 Vyšetření pacienta
Cíl prvního vyšetření spočívá ve zjištění symptomů a délky jejich trvání (bolest při erekci, hmatné uzlíky, zakřivení, délka penisu, tvrdost a obvod penisu) a posouzení stavu erektilní funkce. Dále je nezbytné zaznamenat dyskomfort, jež symptomy pacientovi způsobují, a výskyt potenciálních rizikových faktorů pro vznik erektilní dysfunkce a Peyronieho onemocnění. Pro sběr údajů byl navržen speciální dotazník, tento validovaný instrument je vhodný pro klinickou praxi [38]. Zásadní význam má skutečnost, zda je onemocnění stále v aktivním stadiu, neboť tato informace podmiňuje farmakoterapii a načasování operačního výkonu. Aktivní onemocnění je pravděpodobně přítomno u pacientů, u nichž symptomy přetrvávají teprve po krátkou dobu, trpí bolestí při erekci nebo zaznamenali nedávnou změnu v zakřivení penisu. Často je obtížné definovat konec zánětlivé fáze, obvykle se jako relevantní kritéria stabilizace onemocnění uvádějí vymizení bolestivosti a stabilizace zakřivení přetrvávající po dobu alespoň tří měsíců. V této fázi lze doporučit operační léčbu, pokud je indikována (viz kap. 4.4.4 Operační léčba zakřivení penisu) [33].
Vyšetření je zahájeno běžným vyšetřením močopohlavních cest a pokračuje vyšetřením rukou a chodidel pro detekci potenciální Dupuytrenovy kontraktury nebo plantární fasciální fibromatózy (Ledderhose onemocnění) [34]. Při vyšetření penisu se obvykle zjišťuje přítomnost hmatného uzlíku nebo plaku. Je vhodné vyšetřit penis po celé jeho délce. V současné době neexistuje žádný standardizovaný přístup, doporučuje se však měřit penis v maximálně nataženém stavu na dorzální straně od báze až po jeho špičku [34]. Velikost plaku se měří na ztopořeném penisu, neexistuje však žádná souvislost mezi velikostí plaku a stupněm zakřivení [35]. Délka penisu ve ztopořeném stavu je důležitý údaj, neboť má přímý vliv na volbu léčby [39]. Sami pacienti obvykle uvádějí změnu v obvodu penisu. Erektilní funkci lze hodnotit pomocí validovaných instrumentů, jako např. IIEF (International Index of Erectile Function) [40]. Je však třeba zdůraznit, že IIEF nebyl validován přímo pro využití u pacientů s Peyronieho onemocněním. Erektilní dysfunkce se vyskytuje u pacientů s Peyronieho onemocněním poměrně často (> 50 %), je však nutné rozlišit počátek dysfunkce (před rozvinutím Peyronieho choroby, nebo po něm). Erektilní dysfunkce je zpravidla způsobena poruchou cévního zásobení penisu [27,35]. Přítomnost erektilní dysfunkce může mít vliv na terapeutický postup [41].
Měření velikosti plaku pomocí ultrazvuku je nepřesná metoda, která závisí na vyšetřujícím, a nedoporučuje se tedy pro běžnou klinickou praxi [42]. Duplexní ultrazvukové vyšetření může být nezbytné pro stanovení vaskulárních parametrů [41] (viz rovněž kap. 2.5.3.3 a tab. 3 v EAU Guidelines pro léčbu sexuální dysfunkce). Dále je nezbytné objektivní měření zakřivení penisu ve ztopořeném stavu, což může zajistit pacient sám doma vyfotografováním vlastního ztopořeného penisu při přirozené erekci (preferovaná možnost) nebo s asistencí pomocí testu s užitím vakuově asistované erekce nebo pomocí injekční aplikace vazoaktivní látky [38].
![Výsledky operační léčby Peyronieho onemocnění (údaje z různých nekomparativních studií) [108,110–136,138,139].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/b48c97f1b5e7a61cf5512093406c54bf.png)
Doporučení guidelines pro vyšetření pacientů s Peyronieho onemocněním
Lékařská a sexuální anamnéza u pacientů s Peyronieho onemocněním musí zahrnovat následující informace: délku trvání onemocnění, přítomnost bolesti penisu, změny v deformaci penisu, obtíže při pronikání do vaginy v důsledku deformace penisu a přítomnost erektilní dysfunkce (úroveň důkazu / stupeň doporučení: 2/B).
Fyzikální vyšetření musí zahrnovat následující: vyšetření hmatných uzlíků, měření délky penisu a rozsahu zakřivení (fotografie penisu, erekce navozené pomocí vakuového zařízení nebo medikamentózně) a identifikaci jakéhokoli dalšího souvisejícího onemocnění (Dupuytrenova kontraktura, plantární fasciální fibromatóza) (úroveň důkazu / stupeň doporučení: 2/B).
Měření velikosti plaku pomocí ultrazvuku je nepřesná metoda, která závisí na vyšetřujícím, a nedoporučuje se tedy pro běžnou klinickou praxi (úroveň důkazu / stupeň doporučení: 3/C).
Duplexní ultrazvukové vyšetření je nezbytné pro stanovení vaskulárních parametrů souvisejících s erektilní dysfunkcí (úroveň důkazu / stupeň doporučení: 2/B).
4.3 Neoperační léčba
Konzervativní léčba Peyronieho onemocnění je primárně zaměřena na léčbu onemocnění v časném stadiu, kdy jsou přítomny symptomy a plak není silně fibrotický a není kalcifikován [34,43]. V této fázi se doporučuje několik možností: perorální farmakoterapie, injekce preparátu přímo do léze a další topické terapie, jimž se věnuje tato kapitola (tab. 1). Role konzervativní léčby u mužů se stabilním/chronickým onemocněním nebyla dosud stanovena [32,44]. Evropská agentura pro hodnocení lékařských přípravků dosud neschválila jediný preparát pro léčbu Peyronieho onemocnění. Pouze parabenzoát draselný (Potaba) FDA označila jako „potenciálně účinný“ při léčbě Peyronieho onemocnění. Výsledky studií zaměřených na konzervativní léčbu Peyronieho onemocnění jsou často protichůdné, a neumožňují tak stanovit doporučení pro běžnou každodenní léčbu. Tento fakt je zapříčiněn metodologickými nedostatky v podobě nekontrolovaných studií, malého počtu pacientů podstupujících léčbu, krátké doby sledování a rovněž rozdílnými výslednými parametry [44]. Výsledky týkající se účinnosti konzervativní léčby u určité populace pacientů v rámci počáteční (zánětlivé) a pozdější (fibrotické) fáze onemocnění nejsou zatím k dispozici.
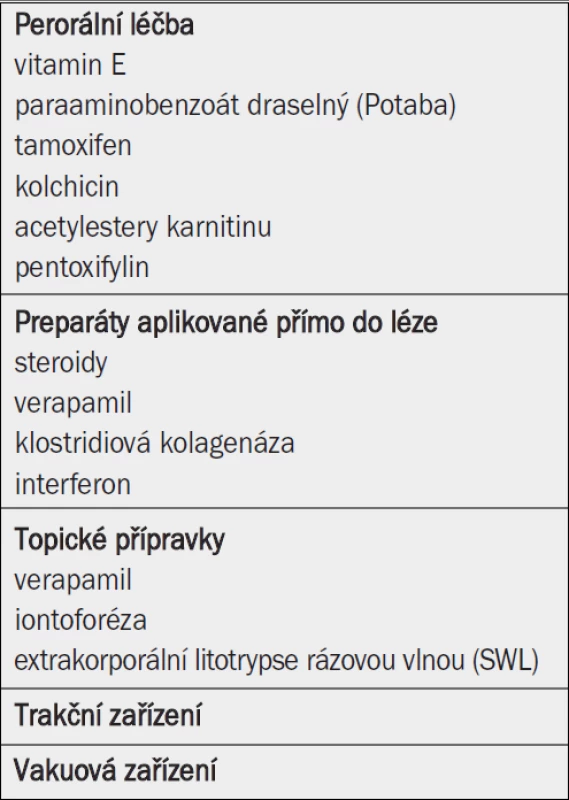
4.3.1 Perorální léčba
4.3.1.1 Vitamin E
Vitamin E (tokoferol, látka rozpustná v tucích, jež účinkuje jako přírodní antioxidant, který likviduje volné radikály vznikající během přeměny energie) většina urologů předepisuje v dávkování 400 UI jednou nebo dvakrát denně, a to díky snadné dostupnosti, nízké ceně a bezpečné aplikaci vitaminu [45]. Navzdory hypotézám o jeho potenciální roli v rámci léčby Peyronieho onemocnění [46] neprokázala dvojitě zaslepená, placebem kontrolovaná, zkřížená studie významný dopad této látky na deformaci penisu ani velikost plaku [47].
4.3.1.2 Paraaminobenzoát draselný (Potaba)
Předpokládá se, že paraaminobenzoát draselný vykazuje antifibrotický účinek prostřednictvím zvýšené absorpce kyslíku tkání, zvýšením sekrece glykosaminoglykanů a posílením aktivity monoamin oxidáz [48]. Role této látky v rámci léčby Peyronieho onemocnění vychází z předběžných studií, které uvádějí zmírnění zakřivení penisu, zmenšení velikosti plaku a bolesti penisu během erekce [49]. V prospektivní, dvojitě zaslepené kontrolní studii zahrnující 41 pacientů s Peyronieho onemocněním vedla aplikace paraaminobenzoátu draselného (12 g/den po dobu 12 měsíců) k významnému zmírnění bolesti penisu, neměla však žádný dopad na jeho zakřivení ani velikost plaku [50]. Jiná prospektivní, randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie zahrnující 103 pacientů s Peyronieho onemocněním popisuje při aplikaci paraaminobenzoátu draselného (4 × 3 g/den po dobu 12 měsíců) významné zmenšení velikosti plaku, ovšem nulový účinek na zakřivení a bolest penisu [51]. Již existující zakřivení zůstává však při aplikaci paraaminobenzoátu draselného stabilizováno, což nasvědčuje tomu, že by tento preparát mohl působit preventivně před dalším zhoršováním zakřivení. Vedlejší účinky spojené s léčbou zahrnují nevolnost, anorexii, pruritus, úzkosti, zimnici, studený pot, pocit zmatení a obtíže při koncentraci. Nebyl však zaznamenán výskyt žádných závažných vedlejších účinků.
4.3.1.3 Tamoxifen
Tamoxifen je nesteroidní antagonista receptoru estrogenu. Jeho předpokládaný účinek v rámci léčby Peyronieho onemocnění spočívá v modulaci sekrece TGFb1 fibroblasty. Předběžné studie uvádějí, že tamoxifen (20 mg 2× denně po dobu tří měsíců) zmírňuje bolest penisu, zakřivení penisu a zmenšuje velikost plaku [52]. Placebem kontrolovaná, randomizovaná studie (zahrnující pouze 25 pacientů s onemocněním v pozdějším stadiu, průměrná délka trvání 20 měsíců) užívající stejný léčebný protokol však neprokázala žádné významné zmírnění bolestivosti, zakřivení ani zmenšení velikosti plaku u mužů s Peyronieho onemocněním [53].
4.3.1.4 Kolchicin
Kolchicin se běžně užívá pro léčbu akutní fáze dny. Pro léčbu Peyronieho onemocnění byl tento preparát zvolen na základě svého protizánětlivého účinku [54]. Předběžné výsledky u 24 mužů ukazují, že polovina mužů (0,6–1,2 mg denně po dobu 3–5 měsíců) zaznamenala zlepšení bolestivé erekce i zakřivení penisu. Ke zmenšení velikosti plaku (nebo jeho vymizení) došlo u 50 % mužů [55]. Jiná studie zahrnující 60 mužů (kolchicin 0,5–1 mg denně po dobu 3–5 měsíců, se zvýšením dávky až na 2 mg 2× denně) uvádí vymizení bolesti penisu u 95 % pacientů a zmírnění zakřivení penisu u 30 % pacientů [54]. Podobné výsledky uvádí jiná nekontrolovaná retrospektivní studie zahrnující 118 pacientů. Autoři dospěli k závěru, že nejčastější formou deformace penisu je zakřivení na laterální straně, jež se po aplikaci kolchicinu přesouvá na dorzální stranu [56]. Mezi vedlejší účinky spojené s aplikací kolchicinu patří potíže související s gastrointestinálním traktem (nevolnost, zvracení, průjem), jež lze zmírnit při podávání s pouze postupným zvyšováním dávky [54]. Kombinovaná šestiměsíční aplikace vitaminu E a kolchicinu (600 mg/den a 1 mg každých 12 hod) u pacientů s Peyronieho onemocněním v časném stadiu vedla k významnému zmenšení velikosti plaku a zmírnění zakřivení, ale nikoli ke zmírnění bolesti (ve srovnání s aplikací ibuprofenu 400 mg/den po dobu šesti měsíců) [57].
4.3.1.5 Acetylestery karnitinu
Ačkoli konkrétní mechanizmus účinku acetylesterů karnitinu u pacientů s Peyronieho onemocněním není znám, předpokládá se, že může snižovat hladinu kalcia v endoteliálních buňkách [58], což může vést k supresi proliferace fibroblastů a tvorby kolagenu, a tedy redukci penilní fibrózy. V randomizované, dvojitě zaslepené studii bylo 48 pacientů s Peyronieho onemocněním v časném stadiu rando-mizováno k aplikaci acetyl-L-karnitinu (1 g 2× denně) nebo tamoxifenu (20 mg 2× denně). Po třech měsících byl acetyl-L-karnitin významně účinnější než tamoxifen s ohledem na redukci bolesti i zakřivení a zpomalení progrese onemocnění, nikoli však s ohledem na zmenšení velikosti plaku (oba preparáty způsobily významné zmenšení velikosti plaku) [59]. Aplikace tamoxifenu je spojena s výrazně větším výskytem vedlejších účinků. Kombinovaná aplikace verapamilu přímo do léze (10 mg 1× týdně po dobu 10 týdnů) s propionyl-l-karnitinem (2 g/3 měsíce) vedla k významně větší redukci velikosti plaku a progrese onemocnění než kombinovaná aplikace verapamilu přímo do léze a tamoxifenu (40 mg/den) po dobu tří měsíců [60].
4.3.1.6 Pentoxifylin
Pentoxifylin je nespecifický inhibitor fosfodiesterázy, který způsobuje downregulaci TGFb1 a podporuje fibrinolytický účinek [61]. Zvýšení hladiny oxidu dusnatého může mít navíc prospěšný účinek v rámci prevence progrese Peyronieho onemocnění a zvratu fibrózy [62]. Předběžné údaje jedné kazuistiky nasvědčují tomu, že aplikace pentoxifylinu (400 mg 3× denně po dobu šesti měsíců) vede ke zmírnění zakřivení penisu a jasnějšímu ultrazvukovému zobrazení plaku [62]. Jiná studie zahrnující 62 pacientů s Peyronieho onemocněním ukazuje, že šestiměsíční aplikace pentoxifylinu vede ke stabilizaci nebo redukci obsahu vápníku v plaku [63].
4.3.1.7 Inhibitory fosfodiesterázy 5 (PDE5i)
Indikace PDE5i při léčbě Peyronieho onemocnění vychází z výsledků studií na zvířecích modelech, které ukazují, že tato agens mohou snižovat poměr kolagen/hladká svalovina a kolagen III/I a zvyšovat index apoptózy plaku [64]. Retrospektivní, kontrolovaná studie ukazuje, že každodenní aplikace tadalafilu (2,5 mg po dobu šesti měsíců) vedla ke statisticky významnému (p < 0,05) ústupu zjizvení septa u 69 % pacientů oproti pouhým 10 % v kontrolní skupině (bez léčby). Do této studie však byli zařazeni pacienti s izolovaným zjizvením septa bez prokázané deformace penisu [65]. PDEi tedy nelze v současné době doporučit pro léčbu Peyronieho onemocnění.
4.3.2 Aplikace preparátu přímo do léze
Další terapeutickou možností je injekční aplikace látky přímo do plaku na penisu, jež umožňuje lokální podání konkrétní látky zajišťující její vyšší koncentraci v plaku. Pomocí této metody je však obtížné zajistit aplikaci účinné látky do cílové oblasti.
4.3.2.1. Steroidy
Předpokládá se, že steroidy aplikované přímo do léze účinkují bráněním zánětlivého prostředí zodpovědného za progresi plaku prostřednictvím inhibice fosfolipázy A2 a suprese imunitní reakce a omezením syntézy kolagenu [66]. Malé nerandomizované studie testující účinek steroidů uvádějí zmenšení velikosti penilního plaku a vymizení bolesti [67,68]. Jediná jednoduše zaslepená, placebem kontrolovaná studie testující aplikaci betamethasonu přímo do léze neprokázala žádné statisticky významné změny deformace penisu, velikosti plaku ani bolesti během erekce [69]. Vedlejší účinky zahrnují atrofii tkáně, ztenčení kůže a imunitní supresi [67].
4.3.2.2 Verapamil
Aplikace verapamilu (antagonista kalciového kanálu) do léze u pacientů s Peyronieho onemocněním vychází z in-vitro údajů, které prokazují transport molekul extracelulární matrix, zahrnující kolagen, fibronektin a glykosaminoglykany spolu se současným zvýšením aktivity kolagenázy, modifikací zánětlivé odpovědi v časném stadiu onemocnění a inhibicí proliferace fibroblastů v plaku [70,71]. Řada studií uvádí, že injekce verapamilu přímo do léze může způsobovat významné zmírnění zakřivení penisu i zmenšení objemu plaku [72–76]. Tyto výsledky nasvědčují tomu, že injekci verapamilu (technika s provedením většího množství vpichů, 10 mg verapamilu v 10ml roztoku, aplikováno po celém objemu plaku každé dva týdny, celkem 12 po sobě jdoucích aplikací) lze doporučit pro léčbu akutní fáze Peyronieho onemocnění bez kalcifikací nebo chronického plaku a stabilizaci progrese onemocnění a potenciální redukci deformace penisu, dosud však chybí ověření ve větších, placebem kontrolovaných studiích [72]. Výskyt vedlejších účinků není častý (4 %) a jedná se pouze o drobné komplikace jako nevolnost, mírné bolesti hlavy, bolest penisu a ekchymóza [72]. Jediná randomizovaná, placebem kontrolovaná studie však nezaznamenala žádné statisticky významné rozdíly s ohledem na velikost plaku, zakřivení penisu, bolest penisu během erekce ani změkčení plaku [77]. Kazuistiky prokázaly, že nižší věk a větší počáteční zakřivení penisu představují predikátory příznivého výsledku [78].
4.3.2.3 Klostridiová kolagenáza
Klostridiová kolagenáza je chromatograficky očištěný bakteriální enzym, jenž selektivně napadá kolagen – primární složku plaku u mužů s Peyronieho onemocněním [79–81]. Injekce klostridiové kolagenázy byly schváleny FDA pro léčbu Dupuytrenovy kontraktury s podobným mechanizmem účinku [82]. Prospektivní, randomizovaná, placebem kontrolovaná, dvojitě zaslepená studie srovnávající vliv aplikace očištěné klostridiové kolagenázy do léze (6 000–14 000 jednotek) na velikost plaku a deformaci penisu vs placeba v podobě fyziologického roztoku uvádí 36% celkovou odpověď (vs 4% odpověď v placebo větvi; p < 0,007) [79]. Pacienti však byli sledováni pouze po dobu tří měsíců. U pacientů s plakem o menší velikosti a zakřivením < 60° bylo dosaženo ještě lepších výsledků. Účinnost injekce kolagenázy do léze (tři injekce klostridiové kolagenázy 10 000 U/0,25 cm3/injekce, aplikováno po dobu 7–10 dnů a následně 7–10 dnů po třech měsících) hodnotí placebem nekontrolovaná studie s krátkou dobou sledování zahrnující pouze malou populaci pacientů s Peyronieho onemocněním [81]. I přes metodologické nedostatky prokázala studie významné zmenšení úhlu zakřivení, šířky i délky plaku oproti výchozímu stavu. Nejčastější vedlejší účinky zahrnovaly bolest penisu, kontuze a ekchymózu.
4.3.2.4 Interferon
Bylo prokázáno, že interferon a2b snižuje proliferaci fibroblastů, tvorbu extracelulární matrix a tvorbu kolagenu z fibroblastů a zlepšuje hojení plaku in vitro [83]. Injekce interferonu přímo do léze (5 × 106 jednotek interferonu a2b v 10 ml fyziologického roztoku, 2× týdně po dobu 12 týdnů) ve srovnání s placebem významně zmenšuje zakřivení penisu, velikost i hustotu plaku a zmírňuje bolestivost [84,85]. Vedlejší účinky zahrnují myalgii, artralgii, sinusitidu, horečku a symptomy připomínající chřipku; všechny lze účinně léčit pomocí nesteroidních protizánětlivých preparátů před aplikací interferonu.
4.3.3 Topická léčba
4.3.3.1 Topická aplikace verapamilu
Malá, randomizovaná, placebem kontrolovaná studie uvádí, že topická aplikace verapamilu (15% gel aplikovaný topicky do těla penisu 2× denně) vedla k významnému zmírnění zakřivení penisu, zmenšení velikosti plaku a zmírnění bolesti penisu [86]. Výsledek se dále významně zlepšil po devíti měsících (ve srovnání se stavem po třech měsících), což nasvědčuje tomu, že delší interval terapie může mít velký význam. V současné době však neexistuje dostatek údajů, které by prokazovaly, že topická aplikace verapamilu umožňuje dosáhnout adekvátní hladiny aktivní složky v tunice albuginea [87].
4.3.3.2 Iontoforéza
Cílem iontoforézy (též označované jako transdermální elektromotivní aplikace preparátu nebo elektromotivní aplikace (EMDA)) je snaha o překonání překážek lokální aplikace léčiv. Nekontrolované studie uvádějí slibné výsledky v doménách zmírnění zakřivení penisu, zmenšení plaku a zmírnění bolesti během erekce [88–90]. Randomizovaná, dvojitě zaslepená, kontrolovaná studie zaznamenala při aplikaci 5 mg verapamilu a 8 mg dexamethasonu pomocí iontoforézy statisticky významné zlepšení zakřivení i velikosti plaku [91]. Jiná randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie testující iontoforézu s aplikací 10 mg verapamilu však nezjistila statisticky signifikantní zlepšení zakřivení penisu [92]. Tato metoda není spojena s výskytem žádných významných vedlejších účinků.
4.3.3.3 Extrakorporální litotrypse rázovou vlnou (SWL)
Mechanizmus účinku SWL při léčbě Peyronieho onemocnění nebyl zatím stoprocentně objasněn, existují však dvě hypotézy. Podle první SWL přímo narušuje a přetváří penilní plak. Druhá hypotéza tvrdí, že vytvářením tepla SWL podporuje vaskularitu této oblasti, což vede k zánětlivé reakci zvyšující aktivitu makrofágů, díky čemuž dochází k lýze nebo dokonce k resorpci plaku [93].
Většina nekontrolovaných studií však neprokázala u pacientů s Peyronieho onemocněním významné zlepšení [94–96]. Prospektivní, randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie testující účinnost čtyř epizod SWL týdně (při každém sezení aplikováno 2 000 cílených rázových vln) zaznamenala významné zlepšení pouze v doméně bolesti penisu [97].
4.3.3.4 Trakční zařízení
Vyvíjení trvalé trakce u pacientů s Dupuytrenovou kontrakturou zvyšuje aktivitu degradačních enzymů [98], což zpočátku oslabuje tažnou sílu a v konečném důsledku vede k rozpouštění plaku. Po tomto procesu následuje zvýšení hladiny nově syntetizovaného kolagenu [98]. Tento koncept byl testován v nekontrolované studii zahrnující 10 pacientů s Peyronieho onemocněním (extendér FastSize Penile Extender byl aplikován jako jediná léčebná metoda po dobu 2–8 hod/den po dobu šesti měsíců) [99].
U všech mužů došlo ke zmírnění zakřivení o 10°–45°, průměrně se zakřivení zmírnilo o 33 % (rozmezí: 51–34°). Délka nataženého penisu se zvětšila o 0,5–2,0 cm, obvod ztopořeného penisu o 0,5–1,0 cm. U čtyř z pěti mužů došlo rovněž ke korekci závěsného efektu.
Nevyskytly se žádné vedlejší účinky (kožní změny, ulcerace, hypestezie ani redukce rigidity penisu). Jiná nekontrolovaná studie zahrnující 15 pacientů s Peyronieho onemocněním a zakřivením < 50° (extendér Andropenis byl aplikován po alespoň 5 hod/den po dobu šesti měsíců) však uvádí minimální zmenšení zakřivení penisu (4°, nebylo dosaženo efektu zvětšení). Průměrná velikost nataženého penisu se po šesti měsících zvětšila o 1,3 cm a délka penisu v ochablém stavu o 0,83 cm [100].
4.3.3.5 Vakuová zařízení
Princip aplikace vakuových zařízení je stejný jako v případě trakčních zařízení. Účinnost vakuových zařízení hodnotí nekontrolovaná studie (studii dokončilo 31 pacientů) [101]. Pacienti užívali vakuové zařízení 10 min 2× denně v průběhu 12 týdnů a zaznamenali významné zmírnění bolesti penisu (p = 0,012) a významné prodloužení délky penisu v nataženém stavu (p = 0,029) v průměru o 0,5 cm. 67 % pacientů zaznamenalo zlepšení zakřivení penisu, 10 % pacientů pozorovalo zhoršení a u 23 % mužů nedošlo k žádné změně. Polovina pacientů byla s výsledkem spokojena a druhá polovina podstoupila operační korekci zakřivení.
Doporučení guidelines pro neoperační léčbu Peyronieho onemocnění
Konzervativní léčba Peyronieho onemocnění je zaměřena primárně na léčbu onemocnění v časném stadiu. Dále je možností volby pro pacienty, kteří nejsou vhodnými kandidáty pro chirurgický výkon, a pacienty, kteří operační léčbu neakceptují (stupeň doporučení: 3C).
Perorální aplikace paraaminobenzoátu draselného může vést k významné redukci velikosti penilního plaku a zmírnění bolesti penisu a stabilizaci zakřivení (úroveň důkazu / stupeň doporučení: 1b/B).
Aplikace verapamilu přímo do léze může vést k významné redukci zakřivení penisu i objemu plaku (úroveň důkazu / stupeň doporučení: 1b/C).
Aplikace klostridiové kolagenázy přímo do léze může vést k významnému zmenšení úhlu zakřivení, šířky i délky plaku (úroveň důkazu / stupeň doporučení: 2b/C).
Aplikace interferonu přímo do léze může vést k redukci zakřivení penisu, velikosti i hustoty plaku a bolesti (úroveň důkazu / stupeň doporučení: 1b/B).
Topická aplikace verapamilu ve formě 15% gelu může vést k redukci zakřivení penisu i velikosti penilního plaku (úroveň důkazu / stupeň doporučení: 1b/B).
Aplikace 5 mg verapamilu a 8 mg dexamethasonu pomocí iontoforézy může vést k redukci zakřivení penisu i velikosti penilního plaku (úroveň důkazu / stupeň doporučení: 1b/B).
Extrakorporální litotrypse rázovou vlnou nevede ke zmenšení zakřivení penisu ani velikosti plaku, a neměla by tedy být indikována s tímto záměrem; tato metoda však může vést ke zmírnění bolesti (úroveň důkazu / stupeň doporučení: 1b/B).
Penilní trakční a vakuová zařízení mohou způsobovat zmírnění deformace penisu a prodloužení penisu (úroveň důkazu: 3C).
Doporučení proti
Aplikace steroidů přímo do léze nevede k významné redukci zakřivení penisu, zmenšení velikosti plaku ani zmírnění bolesti. Tuto léčbu tedy nelze doporučit (úroveň důkazu / stupeň doporučení: 1b/B).
Perorální aplikace vitaminu E a tamoxifenu nevede k významné redukci zakřivení penisu, zmenšení velikosti plaku ani zmírnění bolesti; tato léčba by tedy neměla být indikována s tímto záměrem (úroveň důkazu / stupeň doporučení: 2b/B).
Nelze doporučit ani další perorální preparáty (acetylestery karnitinu, pentoxyfilin) (úroveň důkazu / stupeň doporučení: 3/C).
4.4 Operační léčba
Ačkoli u většiny pacientů povede konzervativní léčba Peyronieho onemocnění k vymizení bolestivé erekce, pouze u malého procenta mužů dojde k významnějšímu narovnání penisu. Cíl operační léčby spočívá v korekci zakřivení, jež umožní dosažení uspokojivého pohlavního styku [102]. Operační léčba je indikována pouze u pacientů, u nichž je onemocnění stabilizováno po dobu alespoň tří měsíců, někteří autoři doporučují dokonce interval 6–12 měsíců [103]. Před podepsáním informovaného souhlasu by měl být pacient informován o potenciálních cílech a rizicích operace. Pacientovi je třeba vysvětlit zejména rizika v podobě možného zkrácení penisu, vzniku erektilní dysfunkce, znecitlivění penisu, vzniku recidivy, potenciálně hmatných uzlíků a stehů pod kůží a možnost provedení obřízky během operace [32].
Při léčbě vrozeného zakřivení penisu i Peyronieho onemocnění rozlišujeme dva hlavní typy rekonstrukčních technik: operaci vedoucí ke zkrácení penisu, anebo naopak jeho prodloužení [104]. Technika se zkrácením penisu spočívá v provedení Nesbitovy klínovité resekce a plikace na konvexní straně penisu. Technika s prodloužením penisu se provádí naopak na konkávní straně a vyžaduje užití štěpu. Cílem je minimalizace rizika zkrácení penisu, k němuž dojde při Nesbitově technice nebo plikaci tuniky albuginea nebo korekci složitějších deformací. Obnažení penisu se současným provedením obřízky (v rámci prevence fimózy po výkonu) představuje standardní přístup při všech typech operace [104].
Nejnovější údaje však nasvědčují tomu, že provedení obřízky není vždy nezbytné. U mužů, kteří mají před výkonem normální předkožku, není obřízka nutná [105]. U mužů s Peyronieho onemocněním a erektilní dysfunkcí, kteří nereagují na medikamentózní léčbu, je vhodné zvážit operační korekci zakřivení se současnou implantací penilní protézy [106]. Volba nejvhodnější léčby závisí na délce penisu, závažnosti zakřivení a stavu erektilní funkce, včetně odpovědi na farmakoterapii v případě erektilní dysfunkce [32]. Při rozhodování o léčbě je rovněž nutné zohlednit pacientova očekávání od operace. V současné době neexistují žádné standardizované dotazníky pro hodnocení výsledku operace [102]. K dispozici máme pouze minimum údajů z kvalitních prospektivních studií, ve většině případů se jedná o údaje nízké úrovně. Většina dat vychází z retrospektivních studií (obvykle nekomparativních a nerandomizovaných) nebo je založena na názoru odborníků [32,107].
4.4.1 Techniky se zkrácením penisu
Nesbit v roce 1965 jako první popsal techniku odstranění elipsovitých segmentů tuniky albuginea naproti neelastickému korporálnímu segmentu při léčbě vrozeného zakřivení penisu [11]. O čtrnáct let později se tato technika stala úspěšnou metodou léčby rovněž pro pacienty s Peyronieho onemocněním [108]. Tato technika spočívá v povedení 5–10mm příčné eliptické excize tuniky albuginea nebo přibližně 1 mm na každých 10° zakřivení [104]. Celkově dosahuje Nesbitova technika vynikajících krátkodobých i dlouhodobých výsledků. U více než 80 % pacientů je dosaženo úplného narovnání penisu [109]. Recidiva deformace a penilní hypestezie se vyskytují velmi vzácně (přibližně 10 %) a riziko vzniku erektilní dysfunkce po výkonu je minimální [104,110]. Nejčastěji uváděným výsledkem Nesbitovy operace je zkrácení penisu [110]. U přibližně 85 % pacientů však bylo popsáno zkrácení o pouhých 1–1,5 cm, jež ovšem ve většině případů není příčinou sexuální dysfunkce [108,111]. Pacienti obvykle subjektivně vnímají zkrácení penisu rozsáhlejší, než je ve skutečnosti [109,110]. Doporučuje se tedy zaznamenat údaj o délce penisu před výkonem a po rekonstrukci, bez ohledu na užitou techniku. Dosud byla popsána pouze jediná modifikace Nesbitovy techniky – excize části tloušťky stěny tuniky albuginea namísto tradiční klínovité excize tuniky albuginea [112]. Plikace je obvykle založena na stejných principech jako Nesbitova technika, ale její provedení je snazší. Starší publikace plikaci uvádějí jako modifikaci Nesbitovy techniky. Plikace spočívá v provedení jedné nebo vícečetné podélné incize na konvexní straně penisu s užitím Heineke-Miculicz principu, případně se plikace provádí bez incize [113–118]. Další modifikace se označuje jako 16bodová technika, při níž se užívá minimální tah. Technika se provádí v lokální anestezii [119]. Užívání nevstřebatelné sutury snižuje riziko recidivy zakřivení. Výsledky a spokojenost pacientů s výsledkem jsou srovnatelné s Nesbitovou technikou [104]. Dosud byla popsána řada modifikací a údaje nemají dostatečnou úroveň, aby bylo možné vyzdvihnout konkrétní variantu proti ostatním.
4.4.2 Techniky s prodloužením penisu
Při tomto druhu technik se provádí incize na kratší (konkávní) straně tuniky, díky čemuž se tato strana prodlouží a vytvoří defekt v tunice albuginea, který je překryt štěpem. Odstranění plaku však může v důsledku žilního úniku vést ke vzniku erektilní dysfunkce [120]. Devine a Horton jako první popsali v roce 1974 užití kožního štěpu [121]. Od této doby byla popsána řada technik a vyzkoušeny nejrůznější materiály (tab. 2) [122–136]. Ideální materiál pro vytvoření štěpu však dosud bohužel nebyl stanoven. Techniky s užitím štěpu jsou spojeny se vznikem erektilní dysfunkce u 25 % pacientů. Navzdory vynikajícím počátečním výsledkům byla u 17 % pacientů v důsledku kontrakce štěpu a dlouhodobého selhání nutná opakovaná operace [137].

Žilní štěpy nabízejí teoretickou výhodu kontaktu dvou endoteliálních ploch, pakliže je štěp fixován ke kavernózní tkáni nacházející se pod ním. Nejčastěji se užívá žíla saphena nebo dorzální penilní žíla [104]. V druhém případě se vyhneme provádění sekundární incize pro získání štěpu. Po operaci s užitím žilního štěpu se uvádí následující komplikace: zakřivení penisu (20 %), zkrácení penisu (17 %) a vznik hernie v místě štěpu (5 %) [122–124].
Tunika vaginalis má minimální cévní zásobení, umožňuje snadné odebrání štěpu a vzhledem k nízkým metabolickým nárokům má minimální tendenci se kontrahovat [126].
Při užití kožních štěpů dochází běžně ke kontrakci materiálu, což může vést k recidivě zakřivení (35 %), progresivnímu zkrácení penisu (40 %) a nutnosti opakovat operaci u 17 % pacientů po deseti letech [138]. Užívání štěpu perikardia zemřelého pacienta (Tutoplast®) dosahuje dobrých výsledků díky kombinaci vynikající roztažitelnosti do všech směrů a elasticity o 30 % [129]. V retrospektivním telefonickém dotazníku uvedlo 44 % pacientů, že u nich došlo k recidivě zakřivení (ačkoli většina z nich mohla nadále uskutečnit úspěšný pohlavní styk) a byli s výsledkem spokojeni [129,138]. Bylo prokázáno, že submukóza tenkého střeva (SIS, xenogenní štěp na bázi kolagenu získaný z vrstvy submukózy tenkého střeva prasete) podporuje regeneraci tkáně a růst endoteliálních buněk. Submukóza tenkého střeva funguje jako lešení pro podporu angiogeneze, migraci a diferenciaci hostitelských buněk, díky čemuž se nakonec cizí tkáň svou strukturou i funkcí podobá tkáni původní. Tento materiál se úspěšně užívá pro korekci závažné chordy a Peyronieho onemocnění, bez vzniku významnějších kontrakcí nebo histologických alterací, k dispozici je však pouze minimum údajů [133]. Incize tuniky s použitím štěpu nabízí vynikající modalitu pro muže se zakřivením > 60°, pacienty s deformací ve tvaru přesýpacích hodin a dobrou erektilní funkcí, kteří jsou ochotni podstoupit vyšší riziko vzniku erektilní dysfunkce po výkonu [139]. Mezi nepříznivé prognostické faktory patří předoperační erektilní dysfunkce, užívání štěpů větší velikosti, věk > 60 let a zakřivení na ventrální straně [106]. Ačkoli ve srovnání s Nesbitovou technikou nebo plikací je tento typ operace spojen s významně nižším rizikem zkrácení penisu, toto riziko stále hrozí a je třeba pacienta náležitě upozornit [104]. Pacientům s Peyronieho onemocněním, kteří podstoupili operační léčbu, se doporučuje užívání penilních extendérů v intervalech 8–12 hodin (denně), protože tato metoda představuje účinný a bezpečný způsob prevence zkrácení penisu [140].
4.4.3 Penilní protéza
Implantace penilní protézy je obvykle vyhrazena pro léčbu Peyronieho onemocnění u mužů s erektilní dysfunkcí, zejména u jedinců, kteří nereagují na aplikaci inhibitorů fosfodiesterázy 5 (PDE5i) [104]. Existují různé typy penilních protéz, nejúčinnějších výsledků však lze u těchto pacientů dosáhnout implantací inflatabilní penilní protézy [141]. Většina pacientů s mírně až středně závažným zakřivením může očekávat vynikající výsledek již pouhým zavedením cylindru. U pacientů se závažnější deformací se provádí operační „remodelace“ penisu přes nafouknutý cylindr (který je manuálně ohnut na opačné straně zakřivení penisu po 90 sekund, často je doprovázen hlasitým prasknutím) [142,143].
V případě, že je finální zakřivení < 30°, nedoporučuje se další léčba vzhledem k tomu, že penilní protéza funguje jako tkáňový expandér a během několika měsíců umožní kompletní korekci zakřivení [142]. Ačkoli u většiny pacientů je tato technika účinná, u některých jedinců může být pro dostatečné napřímení penisu nutné provedení Nesbitovy/plikační techniky nebo excize/incize plaku a užití štěpu [144,146].
Riziko komplikací není v tomto případě (infekce, malformace atd.) vyšší než v běžné populaci. U pacientů, u nichž byla nutná „modelace“ penisu přes nafouknutou protézu, bylo zaznamenáno malé riziko perforace močové trubice (3 %) [143].
4.4.4 Terapeutický algoritmus
Volba nejvhodnější operační techniky pro korekci zakřivení penisu závisí na následujících proměnných, které jsou hodnoceny před operací: délce penisu, stupni zakřivení a stavu erektilní funkce. V případě zakřivení < 60° je zkrácení penisu přijatelné a obvykle je indikována Nesbitova nebo plikační technika; ve většině případů se jedná o vrozené zakřivení penisu. V případě zakřivení > 60° nebo složité deformace nebo jestliže má pacient s dobrou erektilní funkcí (ať již díky farmakoterapii nebo přirozeně) významně zkrácený penis, je možné doporučit implantaci štěpu. U pacientů s erektilní dysfunkcí, u nichž nezabírá medikamentózní léčba, je nejvhodnější volbou implantace inflatabilní protézy, ať již provedeme další korekci penisu, nebo nikoli (modelaci, plikaci nebo dokonce implantaci štěpu plus protézy). Terapeutický algoritmus je znázorněn na schématu 1.

Tab. 3 uvádí výsledky různých chirurgických technik. Je třeba zdůraznit, že operační léčba Peyronieho onemocnění nebyla hodnocena v žádné randomizované, kontrolované studii. Riziko vzniku erektilní dysfunkce je pravděpodobně vyšší při technikách s prodloužením penisu [32,104]. Recidivující zakřivení je důsledkem buď brzkého provedení výkonu před dostatečnou stabilizací onemocnění, opakované aktivace onemocnění po jeho předchozí stabilizaci, nebo užití vstřebatelné sutury, jež ztratila svoji pevnost před tím, než efekt sutury převzaly fibrotické změny [104]. Z tohoto důvodu se doporučuje užívání pouze nevstřebatelné sutury nebo pomalu se vstřebávající sutury. Při užívání nevstřebatelné sutury je nutné, aby byl uzel zanořen, abychom předešli nepříjemnému dráždění kůže penisu, čemuž lze předcházet rovněž užitím pomalu se vstřebávajících stehů [110]. Znecitlivění penisu je potenciální riziko jakéhokoli výkonu vyžadujícího mobilizaci dorzálního neurovaskulárního svazku. Ve většině případů se jedná o neuropraxii, která je způsobena pohmožděním dorzálních senzorických nervů. Vzhledem k tomu, že většina deformací se vyskytuje na dorzální straně, tato komplikace se nejčastěji objevuje při technikách s prodloužením penisu (a implantací štěpu) u mužů s dorzální deformací [104].
Doporučení Guidelines pro operační léčbu zakřivení penisu
Operační léčba je indikována v případě, že je Peyronieho onemocnění stabilizováno po dobu alespoň tří měsíců (není přítomna bolest a nedochází k dalšímu zhoršování deformace), k čemuž obvykle dochází dvanáct měsíců od objevení symptomů a nástupu potíží při pohlavním styku (úroveň důkazu / stupeň doporučení: 3/C).
Před výkonem je třeba zohlednit délku penisu, závažnost zakřivení, erektilní funkci (včetně reakce na medikamentózní léčbu u pacientů s erektilní dysfunkcí) a očekávání pacienta (úroveň důkazu / stupeň doporučení: 3/C).
Techniky se zkrácením tuniky, zejména plikace, jsou léčbou první volby při léčbě vrozeného zakřivení penisu a Peyronieho onemocnění u mužů s penisem o adekvátní délce, zakřivením < 60° a absencí specifických deformací (deformace ve tvaru přesýpacích hodin, závěsný efekt) (úroveň důkazu / stupeň doporučení: 2b/B).
Techniky s implantací štěpů jsou léčbou první volby při léčbě Peyronieho onemocnění u mužů s penisem o nedostatečné délce, zakřivením > 60° a specifickými deformacemi (deformace ve tvaru přesýpacích hodin, závěsný efekt) (úroveň důkazu / stupeň doporučení: 2b/B).
Implantace penilní protézy s dodatečnou úpravou, či bez ní (modelace, plikace, implantace štěpu) se doporučuje pro léčbu Peyronieho onemocnění u mužů s erektilní dysfunkcí, která nereaguje na medikamentózní léčbu (úroveň důkazu / stupeň doporučení: 2b/B).
6. ZKRATKY UŽITÉ V TEXTU
Tento seznam neobsahuje nejběžnější zkratky.
EAU – Evropská urologická asociace
EMDA – transdermální elektromotivní aplikace léku nebo elektromotivní aplikace léku
SWL – litotrypse rázovou vlnou
IIEF – mezinárodní index erektilní funkce
MeSH – Medical Subject Headings
PDE5i – inhibitory fosfodiesterázy typu 5
Sources
1. Musitelli S, Bossi M, Jallous H. A brief historical survey of “Peyronie’s disease”. J Sex Med 2008; 5(7): 1737–1346.
2. Oxford Centre for Evidence-Based Medicine Levels of Evidence (May 2009). Produced by Phillips B, Ball C, Sackett D et al since November 1998. Updated by Jeremy Howick March 2009.
3. Atkins D, Best D, Briss PA et al. GRADE Working Group. Grading quality of evidence and strength of recommendations. BMJ 2004; 328(7454): 1490.
4. Guyatt GH, Oxman AD, Vist GE et al. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ 2008; 336(7650): 924–926.
5. Guyatt GH, Oxman AD, Kunz R et al. GRADE Working Group. Going from evidence to recommendations. BMJ 2008; 336(7652): 1049–1051.
6. Yachia D, Beyar M, Aridogan IA et al. The incidence of congenital penile curvature. J Urol 1993; 150 (5 Pt 1): 1478–1479.
7. Montag S, Palmer LS. Abnormalities of penile curvature: chordee and penile torsion. ScientificWorldJournal 2011; 11 : 1470–1478.
8. Darewicz B, Kudelski J, Szynaka B et al. Ultrastructure of the tunica albuginea in congenital penile curvature. J Urol 2001; 166(5): 1766–1768.
9. Baskin LS, Duckett JW, Lue TF. Penile curvature. Urology 1996; 48(3): 347–356.
10. Catuogno C, Romano G. Androstanolone treatment for congenital penile curvature. Eur Urol 2001; 39 (Suppl 2): 28–32.
11. Nesbit R. Congenital curvature of the phallus: Report of three cases with description of corrective operation. J Urol 1965; 93 : 230–232.
12. Bar Yosef Y, Binyamini J, Matzkin H et al. Midline dorsal plication technique for penile curvature repair. J Urol 2004; 172 (4 Pt 1): 1368–1369.
13. Hayashi Y, Kojima Y, Mizuno K et al. Modified technique of dorsal plication for penile curvature with or without hypospadias. Urology 2002; 59(4): 584–586.
14. Ebbehoj J, Metz P. Congenital penile angulation. Br J Urol 1987; 60(3): 264–266.
15. Badawy H, Morsi H. Long-term followup of dermal grafts for repair of severe penile curvature. J Urol 2008; 180 (4 Suppl): 1842–1845.
16. Schwarzer U, Sommer F, Klotz T et al. The prevalence of Peyronie’s disease: results of a large survey. BJU Int 2001; 88(7): 727–730.
17. Rhoden EL, Teloken C, Ting HY et al. Prevalence of Peyronie’s disease in men over 50-y-old from Southern Brazil. Int J Impot Res 2001; 13(5): 291–293.
18. Mulhall JP, Creech SD, Boorjian SA et al. Subjective and objective analysis of the prevalence of Peyronie’s disease in a population of men presenting for prostate cancer screening. J Urol 2004; 171 (6 Pt 1): 2350–2353.
19. La Pera G, Pescatori ES, Calabrese M et al. Peyronie’s disease: prevalence and association with cigarette smoking. A multicenter population-based study in men aged 50-69 years. Eur Urol 2001; 40 : 525–530.
20. Kumar B, Narang T, Gupta S et al. A clinico-aetiological and ultrasonographic study of Peyronie’s disease. Sex Health 2006; 3(2): 113–118.
21. Lindsay MB, Schain DM, Grambsch P et al. The incidence of Peyronie’s disease in Rochester, Minnesota, 1950 through 1984. J Urol 1991; 146(4): 1007–1009.
22. Sommer F, Schwarzer U, Wassmer G et al. Epidemiology of Peyronie’s disease. Int J Impot Res 2002; 14(5): 379–383.
23. Devine CJ Jr., Somers KD, Jordan SG et al. Proposal: trauma as the cause of the Peyronie’s lesion. J Urol 1997; 157 : 285–290.
24. Jarow JP, Lowe FC. Penile trauma: an etiologic factor in Peyronie’s disease and erectile dysfunction. J Urol 1997; 158(4): 1388–1390.
25. Gonzalez-Cadavid NF, Rajfer J. Mechanisms of Disease: new insights into the cellular and molecular pathology of Peyronie’s disease. Nat Clin Pract Urol 2005; 2(6): 291–297.
26. Rhoden EL, Riedner CE, Fuchs SC et al. A cross-sectional study for the analysis of clinical, sexual and laboratory conditions associated to Peyronie’s disease. J Sex Med 2010; 7 (4 Pt 1): 1529–1537.
27. Kadioglu A, Tefekli A, Erol B et al. A retrospective review of 307 men with Peyronie’s disease. J Urol 2002; 168(3): 1075–1079.
28. Carrieri MP, Serraino D, Palmiotto F et al. A case-control study on risk factors for Peyronie’s disease. J Clin Epidemiol 1998; 51(6): 511–515.
28. Deveci S, Hopps CV, O’Brien K et al. Defining the clinical characteristics of Peyronie’s disease in young men. J Sex Med 2007; 4(2): 485–490.
30. Bjekic MD, Vlajinac HD, Sipetic SB et al. Risk factors for Peyronie’s disease: a case-control study. BJU Int 2006; 97(3): 570–574.
31. Tal R, Heck M, Teloken P et al. Peyronie’s disease following radical prostatectomy: incidence and predictors. J Sex Med 2010; 7(3): 1254–1261.
32. Ralph D, Gonzalez-Cadavid N, Mirone V et al. The management of Peyronie’s disease: evidencebased 2010 guidelines. J Sex Med 2010; 7(7): 2359–2374.
33. Gelbard MK, Dorey F, James K. The natural history of Peyronie’s disease. J Urol 1990; 144(6): 1376–1379.
34. Mulhall JP, Schiff J, Guhring P. An analysis of the natural history of Peyronie’s disease. J Urol 2006; 175(6): 2115–2118.
35. Bekos A, Arvaniti M, Hatzimouratidis K et al. The natural history of Peyronie’s disease: an ultrasonography-based study. Eur Urol 2008; 53(3): 644–650.
36. Pryor JP, Ralph DJ. Clinical presentations of Peyronie’s disease. Int J Impot Res 2002; 14 : 414–417.
37. Nelson CJ, Diblasio C, Kendirci M et al. The chronology of depression and distress in men with Peyronie’s disease. J Sex Med 2008; 5(8): 1985–1990.
38. Levine LA, Greenfield JM. Establishing a standardized evaluation of the man with Peyronie’s disease. Int J Impot Res 2003; 15 (Suppl 5): S103–S112.
39. Greenfield JM, Lucas S, Levine LA. Factors affecting the loss of length associated with tunica albuginea plication for correction of penile curvature. J Urol 2006; 175(1): 238–241.
40. Rosen RC, Riley A, Wagner G et al. The international index of erectile function (IIEF): a multidimensional scale for assessment of erectile dysfunction. Urology 1997; 49(6): 822–830.
41. Kadioglu A, Tefekli A, Erol H et al. Color Doppler ultrasound assessment of penile vascular system in men with Peyronie’s disease. Int J Impot Res 2000; 12(5): 263–267.
42. Porst H, Vardi Y, Akkus E et al. Standards for clinical trials in male sexual dysfunctions. J Sex Med 2010; 7 (1 Pt 2): 414–444.
43. Hellstrom WJ, Bivalacqua TJ. Peyronie’s disease: etiology, medical, and surgical therapy. J Androl 2000; 21(3): 347–354.
44. Muller A, Mulhall JP. Peyronie’s disease intervention trials: methodological challenges and issues. J Sex Med 2009; 6(3): 848–861.
45. Shindel AW, Bullock TL, Brandes S. Urologist practice patterns in the management of Peyronie’s disease: a nationwide survey. J Sex Med 2008; 5(4): 954–964.
46. Scott WW, Scardino PL. A new concept in the treatment of Peyronie’s disease. South Med J 1948; 41(2): 173–177.
47. Pryor JP, Farell CF. Controlled clinical trial of Vitamin E in Peyronie’s disease. Prog Reprod Biol 1983; 9 : 41–45.
48. Griffiths MR, Priestley GC. A comparison of morphoea and lichen sclerosus et atrophicus in vitro: the effects of para-aminobenzoate on skin fibroblasts. Acta Derm Venereol 1992; 72(1): 15–18.
49. Zarafonetis CJ, Horrax TM. Treatment of Peyronie’s disease with potassium para-aminobenzoate (potaba). J Urol 1959; 81(6): 770–772.
50. Shah PJR, Green NA, Adib RS et al. A multicentre double-blind controlled clinical trial of potassium para-amino-benzoate (POTABA1) in Peyronie’s disease. Progr Reprod Biol Med 1983; 9 : 61–67.
51. Weidner W, Hauck EW, Schnitker J. Potassium paraaminobenzoate (POTABA) in the treatment of Peyronie’s disease: a prospective, placebo-controlled, randomized study. Eur Urol 2005; 47(4): 530–535.
52. Ralph DJ, Brooks MD, Bottazzo GF et al. The treatment of Peyronie’s disease with tamoxifen. Br J Urol 1992; 70(6): 648–651.
53. Teloken C, Rhoden EL, Grazziotin TM et al. Tamoxifen versus placebo in the treatment of Peyronie’s disease. J Urol 1999; 162(6): 2003–2005.
54. Kadioglu A, Tefekli A, Koksal T et al. Treatment of Peyronie’s disease with oral colchicine: long-term results and predictive parameters of successful outcome. Int J Impot Res 2000; 12(3): 169–175.
55. Akkus E, Carrier S, Rehman J et al. Is colchicine effective in Peyronie’s disease? A pilot study. Urology 1994; 44(2): 291–295.
56. Akman T, Sanli O, Uluocak N et al. The most commonly altered type of Peyronie’s disease deformity under oral colchicine treatment is lateral curvature that mostly shifts to the dorsal side. Andrologia 2011; 43(1): 28–33.
57. Prieto Castro RM, Leva Vallejo ME, Regueiro Lopez JC et al. Combined treatment with vitamin E and colchicine in the early stages of Peyronie’s disease. BJU Int 2003; 91(6): 522–524.
58. Netticadan T, Yu L, Dhalla NS et al. Palmitoyl carnitine increases intracellular calcium in adult rat cardiomyocytes. J Mol Cell Cardiol 1999; 31(7): 1357–1367.
59. Biagiotti G, Cavallini G. Acetyl-L-carnitine vs tamoxifen in the oral therapy of Peyronie’s disease: a preliminary report. BJU Int 2001; 88(1): 63–67.
60. Cavallini G, Biagiotti G, Koverech A et al. Oral propionyl-l-carnitine and intraplaque verapamil in the therapy of advanced and resistant Peyronie’s disease. BJU Int 2002; 89(9): 895–900.
61. Shindel AW, Lin G, Ning H et al. Pentoxifylline attenuates transforming growth factor-beta1 - stimulated collagen deposition and elastogenesis in human tunica albuginea-derived fibroblasts part 1: impact on extracellular matrix. J Sex Med 2010; 7(6): 2077–2085.
62. Brant WO, Dean RC, Lue TF. Treatment of Peyronie’s disease with oral pentoxifylline. Nat Clin Pract Urol 2006; 3(2): 111–115.
63. Smith JF, Shindel AW, Huang YC et al. Pentoxifylline treatment and penile calcifications in men with Peyronie’s disease. Asian J Androl 2011; 13(2): 322–325.
64. Ferrini MG, Kovanecz I, Nolazco G et al. Effects of long-term vardenafil treatment on the development of fibrotic plaques in a rat model of Peyronie’s disease. BJU Int 2006; 97(3): 625–633.
65. Chung E, Deyoung L, Brock GB. The role of PDE5 inhibitors in penile septal scar remodeling: assessment of clinical and radiological outcomes. J Sex Med 2011; 8(5): 1472–1477.
66. Tranchant C, Braun S, Warter JM. Mechanism of action of glucocorticoids: role of lipocortins. Rev Neurol (Paris) 1989; 145(12): 813–818.
67. Desanctis PN, Furey CA Jr. Steroid injection therapy for Peyronie’s disease: a 10-year summary and review of 38 cases. J Urol 1967; 97(1): 114–116.
68. Winter CC, Khanna R. Peyronie’s disease: results with dermo-jet injection of dexamethasone. J Urol 1975; 114(6): 898–900.
69. Cipollone G, Nicolai M, Mastroprimiano G et al. Betamethasone versus placebo in Peyronie’s disease. Arch Ital Urol Androl 1998; 70(4): 165–168.
70. Roth M, Eickelberg O, Kohler E et al. Ca2+ channel blockers modulate metabolism of collagens within the extracellular matrix. Proc Natl Acad Sci U S A 1996; 93(11): 5478–5482.
71. Mulhall JP, Anderson MS, Lubrano T et al. Peyronie’s disease cell culture models: phenotypic, genotypic and functional analyses. Int J Impot Res 2002; 14(5): 397–405.
72. Levine LA, Goldman KE, Greenfield JM. Experience with intraplaque injection of verapamil for Peyronie’s disease. J Urol 2002; 168(2): 621–625.
73. Anderson MS, Shankey TV, Lubrano T et al. Inhibition of Peyronie’s plaque fibroblast proliferation by biologic agents. Int J Impot Res 2000; 12 (Suppl 3): S25–S31.
74. Rehman J, Benet A, Melman A. Use of intralesional verapamil to dissolve Peyronie’s disease plaque: a long-term single-blind study. Urology 1998; 51(4): 620–626.
75. Bennett NE, Guhring P, Mulhall JP. Intralesional verapamil prevents the progression of Peyronie’s disease. Urology 2007; 69(6): 1181–1184.
76. Cavallini G, Modenini F, Vitali G. Open preliminary randomized prospective clinical trial of efficacy and safety of three different verapamil dilutions for intraplaque therapy of Peyronie’s disease. Urology 2007; 69(5): 950–954.
77. Shirazi M, Haghpanah AR, Badiee M et al. Effect of intralesional verapamil for treatment of Peyronie’s disease: a randomized single-blind, placebo-controlled study. Int Urol Nephrol 2009; 41(3): 467–471.
78. Moskovic DJ, Alex B, Choi JM et al. Defining predictors of response to intralesional verapamil injection therapy for Peyronie’s disease. BJU Int 2011; 108(9): 1485–1489.
79. Gelbard MK, James K, Riach P et al. Collagenase versus placebo in the treatment of Peyronie’s disease: a double-blind study. J Urol 1993; 149(1): 56–58.
80. Ehrlich HP. Scar contracture: cellular and connective tissue aspects in Peyronie’s disease. J Urol 1997; 157(1): 316–319.
81. Jordan GH. The use of intralesional clostridial collagenase injection therapy for Peyronie’s disease: a prospective, single-center, non-placebo-controlled study. J Sex Med 2008; 5(1): 180–187.
82. Hurst LC, Badalamente MA, Hentz VR et al. Injectable collagenase clostridium histolyticum for Dupuytren’s contracture. N Engl J Med 2009; 361(10): 968–979.
83. Duncan MR, Berman B, Nseyo UO. Regulation of the proliferation and biosynthetic activities of cultured human Peyronie’s disease fibroblasts by interferons-alpha, -beta and -gamma. Scand J Urol Nephrol 1991; 25(2): 89–94.
84. Kendirci M, Usta MF, Matern RV et al. The impact of intralesional interferon alpha-2b injection therapy on penile hemodynamics in men with Peyronie’s disease. J Sex Med 2005; 2(5): 709–715.
85. Hellstrom WJ, Kendirci M, Matern R et al. Single-blind, multicenter, placebo controlled, parallel study to assess the safety and efficacy of intralesional interferon alpha-2B for minimally invasive treatment for Peyronie’s disease. J Urol 2006; 176(1): 394–398.
86. Fitch WP 3rd, Easterling WJ, Talbert RL et al. Topical verapamil HCl, topical trifluoperazine, and topical magnesium sulfate for the treatment of Peyronie’s disease - a placebo-controlled pilot study. J Sex Med 2007; 4(2): 477–484.
87. Martin DJ, Badwan K, Parker M et al. Transdermal application of verapamil gel to the penile shaft fails to infiltrate the tunica albuginea. J Urol 2002; 168(6): 2483–2485.
88. Di Stasi SM, Giannantoni A, Capelli G et al. Transdermal electromotive administration of verapamil and dexamethasone for Peyronie’s disease. BJU Int 2003; 91(9): 825–829.
89. Riedl CR, Plas E, Engelhardt P et al. Iontophoresis for treatment of Peyronie’s disease. J Urol 2000; 163(1): 95–99.
90. Tuygun C, Ozok UH, Gucuk A et al. The effectiveness of transdermal electromotive administration with verapamil and dexamethasone in the treatment of Peyronie’s disease. Int Urol Nephrol 2009; 41(1): 113–118.
91. Di Stasi SM, Giannantoni A, Stephen RL et al. A prospective, randomized study using transdermal electromotive administration of verapamil and dexamethasone for Peyronie’s disease. J Urol 2004; 171(4): 1605–1608.
92. Greenfield JM, Shah SJ, Levine LA. Verapamil versus saline in electromotive drug administration for Peyronie’s disease: a double-blind, placebo controlled trial. J Urol 2007; 177(3): 972–975.
93. Husain J, Lynn NN, Jones DK et al. Extracorporeal shock wave therapy in the management of Peyronie’s disease: initial experience. BJU Int 2000; 86(4): 466–468.
94. Strebel RT, Suter S, Sautter T et al. Extracorporeal shockwave therapy for Peyronie’s disease does not correct penile deformity. Int J Impot Res 2004; 16(5): 448–451.
95. Hauck EW, Hauptmann A, Bschleipfer T et al. Questionable efficacy of extracorporeal shock wave therapy for Peyronie’s disease: results of a prospective approach. J Urol 2004; 171(1): 296–299.
96. Srirangam SJ, Manikandan R, Hussain J et al. Long-term results of extracorporeal shockwave therapy for Peyronie’s disease. J Endourol 2006; 20(11): 880–884.
97. Palmieri A, Imbimbo C, Longo N et al. A first prospective, randomized, double-blind, placebo controlled clinical trial evaluating extracorporeal shock wave therapy for the treatment of Peyronie’s disease. Eur Urol 2009; 56(2): 363–369.
98. Bailey AJ, Tarlton JF, Van der Stappen J et al. The continuous elongation technique for severe Dupuytren’s disease. A biochemical mechanism. J Hand Surg Br 1994; 19(4): 522–527.
99. Levine LA, Newell M, Taylor FL. Penile traction therapy for treatment of Peyronie’s disease: a singlecenter pilot study. J Sex Med 2008; 5(6): 1468–1473.
100. Gontero P, Di Marco M, Giubilei G et al. Use of penile extender device in the treatment of penile curvature as a result of Peyronie’s disease. Results of a phase II prospective study. J Sex Med 2009; 6(2): 558–566.
101. Raheem AA, Garaffa G, Raheem TA et al. The role of vacuum pump therapy to mechanically straighten the penis in Peyronie’s disease. BJU Int 2010; 106(8): 1178–1180.
102. Montorsi F, Adaikan G, Becher E et al. Summary of the recommendations on sexual dysfunctions in men. J Sex Med 2010; 7(11): 3572–3588.
103. Kendirci M, Hellstrom WJ. Critical analysis of surgery for Peyronie’s disease. Curr Opin Urol 2004; 14 : 381–388.
104. Langston JP, Carson CC 3rd. Peyronie disease: plication or grafting. Urol Clin North Am 2011; 38 : 207–216.
105. Garaffa G, Sacca A, Christopher AN et al. Circumcision is not mandatory in penile surgery. BJU Int 2010; 105(2): 222–224.
106. Mulhall J, Anderson M, Parker M. A surgical algorithm for men with combined Peyronie’s disease and erectile dysfunction: functional and satisfaction outcomes. J Sex Med 2005; 2(1): 132–138.
107. Smith JF, Walsh TJ, Lue TF. Peyronie’s disease: a critical appraisal of current diagnosis and treatment. Int J Impot Res 2008; 20(5): 445–459.
108. Pryor JP, Fitzpatrick JM. A new approach to the correction of the penile deformity in Peyronie’s disease. J Urol 1979; 122(5): 622–623.
109. Pryor JP. Correction of penile curvature and Peyronie’s disease: why I prefer the Nesbit technique. Int J Impot Res 1998; 10(2): 129–131.
110. Ralph DJ, al-Akraa M, Pryor JP. The Nesbit operation for Peyronie’s disease: 16-year experience. J Urol 1995; 154(4): 1362–1363.
111. Savoca G, Trombetta C, Ciampalini S et al. Long-term results with Nesbit’s procedure as treatment of Peyronie’s disease. Int J Impot Res 2000; 12(5): 289–2893.
112. Rehman J, Benet A, Minsky LS et al. Results of surgical treatment for abnormal penile curvature: Peyronie’s disease and congenital deviation by modified Nesbit plication (tunical shaving and plication). J Urol 1997; 157(4): 1288–1291.
113. Lemberger RJ, Bishop MC, Bates CP. Nesbit’s operation for Peyronie’s disease. Br J Urol 1984; 56(6): 721–723.
114. Sassine AM, Wespes E, Schulman CC. Modified corporoplasty for penile curvature: 10 years’ experience. Urology 1994; 44(3): 419–421.
115. Licht MR, Lewis RW. Modified Nesbit procedure for the treatment of Peyronie’s disease: a comparative outcome analysis. J Urol 1997; 158(2): 460–463.
116. Yachia D. Modified corporoplasty for the treatment of penile curvature. J Urol 1990; 143(1): 80–82.
117. Essed E, Schroeder FH. New surgical treatment for Peyronie disease. Urology 1985; 25(6): 582–587.
118. Ebbehoj J, Metz P. New operation for “krummerik” (penile curvature). Urology 1985; 26(1): 76–78.
119. Gholami SS, Lue TF. Correction of penile curvature using the 16-dot plication technique: a review of 132 patients. J Urol 2002; 167(5): 2066–2069.
120. Dalkin BL, Carter MF. Venogenic impotence following dermal graft repair for Peyronie’s disease. J Urol 1991; 146(3): 849–851.
121. Devine CJ Jr, Horton CE. Surgical treatment of Peyronie’s disease with a dermal graff. J Urol 1974; 111(1): 44–49.
122. Montorsi F, Salonia A, Maga T et al. Evidence based assessment of long-term results of plaque incision and vein grafting for Peyronie’s disease. J Urol 2000; 163(6): 1704–1708.
123. Kadioglu A, Tefekli A, Usta M et al. Surgical treatment of Peyronie’s disease with incision and venous patch technique. Int J Impot Res 1999; 11(2): 75–81.
124. El-Sakka AI, Rashwan HM, Lue TF. Venous patch graft for Peyronie’s disease. Part II: outcome analysis. J Urol 1998; 160 (6 Pt 1): 2050–2053.
125. Hatzichristou DG, Hatzimouratidis K, Apostolidis A et al. Corporoplasty using tunica albuginea free grafts for penile curvature: surgical technique and long-term results. J Urol 2002; 167(3): 1367–1370.
126. Das S. Peyronie’s disease: excision and autografting with tunica vaginalis. J Urol 1980; 124(6): 818–819.
127. Gelbard MK, Hayden B. Expanding contractures of the tunica albuginea due to Peyronie’s disease with temporalis fascia free grafts. J Urol 1991; 145(4): 772–776.
128. Cormio L, Zucchi A, Lorusso F et al. Surgical treatment of Peyronie’s disease by plaque incision and grafting with buccal mucosa. Eur Urol 2009; 55(6): 1469–1475.
129. Taylor FL, Levine LA. Surgical correction of Peyronie’s disease via tunica albuginea plication or partial plaque excision with pericardial graft: long-term follow up. J Sex Med 2008; 5(9): 2221–2228.
130. Burnett AL. Fascia lata in penile reconstructive surgery: a reappraisal of the fascia lata graft. Plast Reconstr Surg 1997; 99(4): 1061–1067.
131. Fallon B. Cadaveric dura mater graft for correction of penile curvature in Peyronie disease. Urology 1990; 35(2): 127–129.
132. Leungwattanakij S, Bivalacqua TJ, Yang DY et al. Comparison of cadaveric pericardial, dermal, vein, and synthetic grafts for tunica albuginea substitution using a rat model. BJU Int 2003; 92(1): 119–124.
133. Knoll LD. Use of porcine small intestinal submucosal graft in the surgical management of Peyronie’s disease. Urology 2001; 57(4): 753–757.
134. Bokarica P, Parazajder J, Mazuran B et al. Surgical treatment of Peyronie’s disease based on penile length and degree of curvature. Int J Impot Res 2005; 17(2): 170–174.
135. Faerber GJ, Konnak JW. Results of combined Nesbit penile plication with plaque incision and placement of Dacron patch in patients with severe Peyronie’s disease. J Urol 1993; 149 (5 Pt 2): 1319–1320.
136. Egydio PH, Lucon AM, Arap S. A single relaxing incision to correct different types of penile curvature: surgical technique based on geometrical principles. BJU Int 2004; 94(7): 1147–1157.
137. Kadioglu A, Akman T, Sanli O et al. Surgical treatment of Peyronie’s disease: a critical analysis. Eur Urol 2006; 50(2): 235–248.
138. Chun JL, McGregor A, Krishnan R et al. A comparison of dermal and cadaveric pericardial grafts in the modified Horton-Devine procedure for Peyronie’s disease. J Urol 2001; 166(1): 185–188.
139. Chung E, Clendinning E, Lessard L et al. Five-year follow-up of Peyronie’s graft surgery: outcomes and patient satisfaction. J Sex Med 2011; 8(2): 594–600.
140. Taylor FL, Levine LA. Peyronie’s Disease. Urol Clin North Am 2007; 34(4): 517–534.
141. Montorsi F, Guazzoni G, Barbieri L et al. AMS 700 CX inflatable penile implants for Peyronie’s disease: functional results, morbidity and patient-partner satisfaction. Int J Impot Res 1996; 8(2): 81–85.
142. Wilson SK. Surgical techniques: modeling technique for penile curvature. J Sex Med 2007; 4(1): 231–234.
143. Wilson SK, Delk JR 2nd. A new treatment for Peyronie’s disease: modeling the penis over an inflatable penile prosthesis. J Urol 1994; 152(4): 1121–1123.
144. Carson CC. Penile prosthesis implantation in the treatment of Peyronie’s disease. Int J Impot Res 1998; 10(2): 125–128.
145. Montague DK, Angermeier KW, Lakin MM et al. AMS 3-piece inflatable penile prosthesis implantation in men with Peyronie’s disease: comparison of CX and Ultrex cylinders. J Urol 1996; 156(5): 1633–1635.
146. Chaudhary M, Sheikh N, Asterling S et al. Peyronie’s disease with erectile dysfunction: penile modelling over inflatable penile prostheses. Urology 2005; 65(4): 760–764.
Labels
Paediatric urologist UrologyArticle was published in
Urological Journal

2013 Issue 1
-
All articles in this issue
- The role of phosphodiesterase inhibitors in urology in treatment of erectile dysfunction
- Tadalafil in the treatment of LUTS/BPH and ED
- Varicocele and the signification of its repair
- Laparoscopis nephrectomy for atrophic kidney with serious infectious episode
- Simultaneous ipsilateral native nephrectomy with kidney transplantation for the patiens with polycystic kidney disease
- Retroperitoneal laparoscopic nephrectomy for the patients undergoing peritoneal dialysis
- Preliminary experience with transperitoneal laparoendoscopic single-site radical nephrectomy using a home-made single-port device in China
- A review of current practices and controversies in the use of indwelling ureteric stents
- Does early following PCNL lead to trapped stones in the tract: Myth or reality
- Patient preferences for advanced urological techniques: A guide to future surgical developments?
- Bipolar plasma vaporization of prostate for symptomatic large benign prostatic enlargement: two-year clinical results
- Gender as a factor influencing clinico-pathological parameters and prognosis of renal cell carcinoma
- EAU Guidelines on penile curvature
- Urological Journal
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Varicocele and the signification of its repair
- EAU Guidelines on penile curvature
- A review of current practices and controversies in the use of indwelling ureteric stents
- Tadalafil in the treatment of LUTS/BPH and ED

