-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Totální pankreatektomie a její současné místo v léčbě onemocnění pankreatu
Total pancreatectomy and its current place in the treatment of pancreatic diseases
Total pancreatectomy (TP) is a surgical procedure indicated selectively for patients with benign and malignant disease. In the case of malignancy, TP is indicated electively for multifocal or advanced disease, mostly for chronic pancreatitis after a non-effective primary operation. TP is indicated as “salvage surgery” in cases of acute postoperative pancreatitis or in situations where it is not possible to complete the elective partial resection. With respect to survival and quality of life, the outcomes of TP patients are comparable to those of patients who have undergone partial resection. The exclusion of patients who have a high probability of not profiting from TP is still a problem. The aim of this review is to inform gastroenterologists about the current place of TP in the treatment of malignant and benign pancreatic diseases. A multidisciplinary team and a surgeon played key roles in all cases.
Key words:
pancreatic cancer – chronic pancreatitis – total pancreatectomy – multidisciplinary team
The author declares he has no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
6. 9. 2016Accepted:
18. 9. 2016
Autoři: M. Ryska
Působiště autorů: Chirurgická klinika 2. LF UK a ÚVN – VFN v Praze
Vyšlo v časopise: Gastroent Hepatol 2016; 70(5): 408-412
Kategorie: Gastrointestinální onkologie: přehledová práce
prolekare.web.journal.doi_sk: https://doi.org/10.14735/amgh2016408Souhrn
Totální pankreatektomie (TP) je výkonem, který je indikován pro benigní a maligní onemocnění pankreatu selektivně. U plánovaných výkonů v případě multifokální či rozsáhlé malignity, u chronické pankreatitidy většinou po provedeném primárním operačním výkonu, který nevedl k terapeutickému úspěchu. Z akutní indikace je TP prováděna jako tzv. salvage surgery u akutní pooperační pankreatitidy či v situacích, kdy nelze dokončit plánovanou parciální resekci. Výsledky v přežívání a hodnocení kvality života jsou obdobné jako u parciálních resekcí. Problémem zůstává identifikace nemocných, kteří s vysokou pravděpodobností z TP profitovat nebudou. Cílem souhrnného sdělení je informovat gastroenterologickou veřejnost o současném místu TP u maligních i benigních onemocnění slinivky břišní. Klíčové místo v rozhodnutí provést TP náleží multidisciplinárnímu týmu a v některých případech peroperačně chirurgovi.
Klíčová slova:
karcinom pankreatu – chronická pankreatitida – totální pankreatektomie – multidisciplinární týmÚvod
Parciální resekční výkon na pankreatu u malignity může být potenciálně kurativní v podobě radikální pankreatoduodenektomie, levostranné pankreatektomie či centrální resekce žlázy. U benigních onemocnění, především u konzervativně nezvládnutelné těžké chronické pankreatitidy, může být vedle drenážních duodenum-záchovných výkonů účinnou léčebnou metodou ke zmírnění obtíží nemocného a současně i k odstranění komplikace, např. stenózy duodena, distálního žlučovodu či důsledků levostranné portální hypertenze.
Odstranění celé žlázy – totální pankreatektomie (TP) – je v uvedeném portfoliu operačních výkonů považováno i dnes za výkon spíše výjimečný, i když její indikace se v průběhu posledních let významně změnila. Peroperační mortalita resekčních výkonů a TP v posledním období významně klesla. Je tak možné vysledovat i změnu v indikacích k TP [1–6].
Současný literární přehled o TP pro benigní či maligní onemocnění slinivky břišní získaný pomocí databáze PubMed za léta 2009–2015 obsahuje 772 fulltextových přehledných a původních sdělení. U malignit se jednotlivá sdělení týkají především indikací [2,5,6], časných a pozdních komplikací [3], přežívání v závislosti na základním onemocnění a kvalitě života (QoL – quality of life) [1,4]. U benigních onemocnění se autoři věnují především po TP navazující autotransplantaci Langerhansových ostrůvků v prevenci pooperačního diabetu, a to zejména u nemocných s chronickou pankreatitidou [7].
Historická poznámka
Zatímco prvenství v provedení parciálního resekčního výkonu na slinivce je připisováno německému chirurgovi Kauschovi z roku 1912, až Whipple se ve 30. letech 20. století postaral o jeho širší publicitu [8], a to nehledě na vysokou pooperační úmrtnost dosahující 50 %. Původně několikadobý výkon byl teprve v roce 1941 Trimblem technicky uzpůsoben na výkon jednodobý. Kazuistické sdělení popisující TP pro karcinom publikoval v Annals of Surgery o dva roky později Rockey [9]. Výkon byl v té době nepochybně podmíněn „velkou odvahou“ operatéra, nicméně jeho provedení se zásadně neliší od současného.
Přínos TP pro pacienta s onemocněním pankreatu poprvé systematicky analyzovali na skupině 65 nemocných s odstupem 30 let až Ihse et al [10]. Největším problémem překvapivě nebylo očekávané „inzulinové kóma“, ale časné chirurgické komplikace. Časná letalita výkonu přesahující 20 % byla brzdou širšímu klinickému uplatnění. Tu se podařilo významně snížit až v 90. letech 20. století, kdy Trede [11] v sestavě 52 TP z celkového počtu 285 resekovaných zaznamenal v časném pooperačním období pouze tři exity (5,8 %). Na základě nízké časné letality blížící se parciálním resekčním výkonům poukazovali protagonisté TP na její výhody s ohledem na poměrně vysoký výskyt multifokálního šíření karcinomu, jeho šíření do okrajů resekční linie a na možnost provést adekvátnější lymfadenektomii. Někteří chirurgové si u TP cenili především vyloučení rizika fatální pooperační pankreatitidy a dehiscence pankreatické anastomózy s rozvojem život ohrožujících pankreatických píštělí. Úvahy se týkaly i benigních indikací, zejména chronické pankreatitidy a rizika přehlédnutí karcinomu při tzv. neidentifikovatelných masách [12]. Naproti tomu skeptici poukazovali na pooperační rozvoj tzv. brittle diabetes a absenci trávicích enzymů. U chronické pankreatitidy zdůrazňovali nepřiměřenost tak rozsáhlého výkonu z benigní indikace [13].
Pozornost zaslouží práce Willeta [14], který upozornil na 51% výskyt pozitivity resekční plochy s tím, že v případě její negativity u parciální resekce pro karcinom lze dosáhnout pětiletého přežití u 22 % operovaných. Zajímavým údajem nejen podpořil výhodu TP, ale studií předstihl o více než 10 let pozoruhodnou práci Verbeke [15]. Ta prokázala pomocí tzv. Leedského protokolu zpracování resekátu slinivky mikroskopicky pozitivní okraje u 85 % parciálně resekovaných nemocných. V případě negativního nálezu, tj. R0 resekce stanovené touto metodou, se 80 % pacientů dožilo pěti let po operaci [16].
Současné indikace TP
Je třeba zdůraznit, že TP by měla být prováděna výběrově. Důkazem toho je nejen absence standardní indikace k TP u karcinomu jako součásti doporučených postupů [17], ale zejména platného rozdělení nemocných na základě předoperačního stagingu na resekabilní, borderline resekabilní a neresekabilní z důvodů lokální pokročilosti či metastatického postižení. Toto rozdělení určuje provedení parciálního resekčního výkonu s potenciálním radikálním a kurativním cílem, nikoli indikací k TP. I u nemocných s benigním onemocněním pankreatu je indikace TP zvažována s ještě větší opatrností, a to s ohledem na potenciální problémy v pozdním pooperačním období (obtížně zvládnutelné hypoglykemické stavy).
Indikace optimálního léčebného postupu u pacienta s onemocněním pankreatu musí být stanovena v rámci multidisciplinárního týmu (MDT) – radiolog, gastroenterolog, patolog chirurg, onkolog – a to na pracovišti s vysokou frekvencí těchto nemocných. Pracoviště musí nejen rutinně zvládat komplexní péči o tyto nemocné, ale mít schopnost reagovat na pravidelně prováděné audity výsledků a rozborů komplikací. Chirurg v tomto týmu nese odpovědnost nejen za časný výsledek resekčního výkonu, ale často v očích pacienta a jemu blízkých i za délku přežívání a QoL [18].
Indikace TP u maligního onemocnění pankreatu
V současné době je v souladu s literárními údaji [17] i s vlastními zkušenostmi [19,20] resekce pro maligní onemocnění pankreatu indikována u 15–20 % nemocných. Z tohoto počtu se v 10–12 % jedná o TP. Ta je v rámci MDT indikována elektivně, a to a) primárně, b) původně jako výkon resekční (ten je na základě peroperačního nálezu chirurgem konvertován na TP), c) u malé části nemocných je k TP přistoupeno urgentně – jako k výkonu „salvage surgery“ pro život ohrožující akutní pooperační pankreatitidu či pankreatickou píštěl typu C [1,5,21].
Do první skupiny v současné době zahrnujeme pacienty, u kterých předpokládáme maligní nebo potenciálně maligní postižení slinivky v rozsahu přesahujícím možnosti parciální resekce – intraduktální papilární mucinózní neoplazie, multifokální neoplazie ostrůvků, syndrom familiárního pankretického karcinomu. Dalšími indikacemi jsou nemocní s lokálně pokročilým nebo multifokálním karcinomem, rozsáhlým neuroendokrinním tumorem nebo metastatickým postižením žlázy (např. při karcinomu ledviny).
Ve druhé skupině se chirurg rozhoduje provést TP v případě většího rozsahu postižení, než bylo prezentováno na MDT, v případě peroperačního pozitivního odečtu resekční linie patologem a v posledním období u nemocných s vysokým rizikem vzniku pooperační pankreatické píštěle – jedná se o nemocné s tzv. soft tissue a filiformním ductus pancreaticus, kteří jsou ohroženi vysokým rizikem vzniku dehiscence pankreatické anastomózy v časném pooperačním období [2,3].
Indikace TP u benigního onemocnění pankreatu
Pravděpodobně i po 20 letech lze souhlasit s názorem Russella [22], že TP je indikována u nemocného s chronickou pankreatitidou jedině při konsenzu pacienta, gastroenterologa a chirurga. A to na základě selhání medikamentózní a endoskopické léčby, na základě přetrvávajících neztlumitelných bolestí či při absenci efektu předchozího chirurgického výkonu. Většinou se jedná o předchozí drenážní výkony podle Freye nebo Begera, dříve prováděné longitudinální anastomózy jsou dnes považovány až na výjimky za neúčinné. Indikace TP je zvažována i u skupiny nemocných s hereditární pankretitidou a při endoskopicky neodstranitelných konkrementech v průběhu ductus pancreaticus. Za „výhodu“ může být při indikaci k TP považována přítomnost na inzulinu závislého diabetu, a to zejména s ohledem na hodnocení QoL pooperačně [4,22].
V posledním období existují pracoviště, která zejména u mladých nemocných s chronickou pankreatitidou spojují TP s autotransplantací Langerhansových ostrůvků [7]. Jedná se o technicky náročnou přípravu buněčného substrátu, který je v průběhu operace nebo těsně po ní aplikován do portálního řečiště pacienta. U nás první zprávu o použití autotransplantace po TP u pěti nemocných, nikoli však s chronickou pankreatitidou, ale s karcinomem slinivky, publikoval Kočík [23].
TP – poznámka k chirurgickému výkonu
Vlastní provedení výkonu bývá v souladu se standardně uváděným operačním postupem a snahou o minimalizaci peroperační krevní ztráty. A v případě malignity s adekvátní lymfadenektomií [24,25]. TP může být pro chirurga v resekční fázi při angioinvazivitě maligního ložiska či tvrdém zánětlivém peripankreatickém infiltrátu při chronické pankreatitidě, zejména po předchozích operacích, technicky obtížným výkonem. Významná portální hypertenze může dokonce provedení výkonu znemožnit. Právě krevní ztráta je považována za nezávislý nepříznivý faktor pooperačního vývoje. Naproti tomu rekonstrukční fáze je ve srovnání s parciálním výkonem jednodušší.Absence pankreatodigestivní anastomózy nebo slepé sutury pankreatického remnantu vylučuje vznik obávané pankreatické píštěle. Ve většině případů je TP spojena se splenektomií, a to v rámci onkologické radikality či z důvodu nemožnosti zachovat nepoškozenou slezinnou žílu.
Chirurg při TP může zprvu postupovat izolací duodena s hlavou pankreatu – např. při původně plánované pankreatoduodenektomii s následnou konverzí na TP, nebo vyjme preparát en bloc (obr. 1). Podstatná je bezpečnost výkonu, snaha o onkologickou radikalitu a minimální krevní ztráta. V případě cévní resekce je vhodné provádět rekonstrukci s co nejmenší časovou prodlevou [24].
Obr. 1. Totální pankreatektomie u nemocného s IPMN – resekát. Fig. 1. Total pancreatectomy in patients with IPMN – the biopsy. 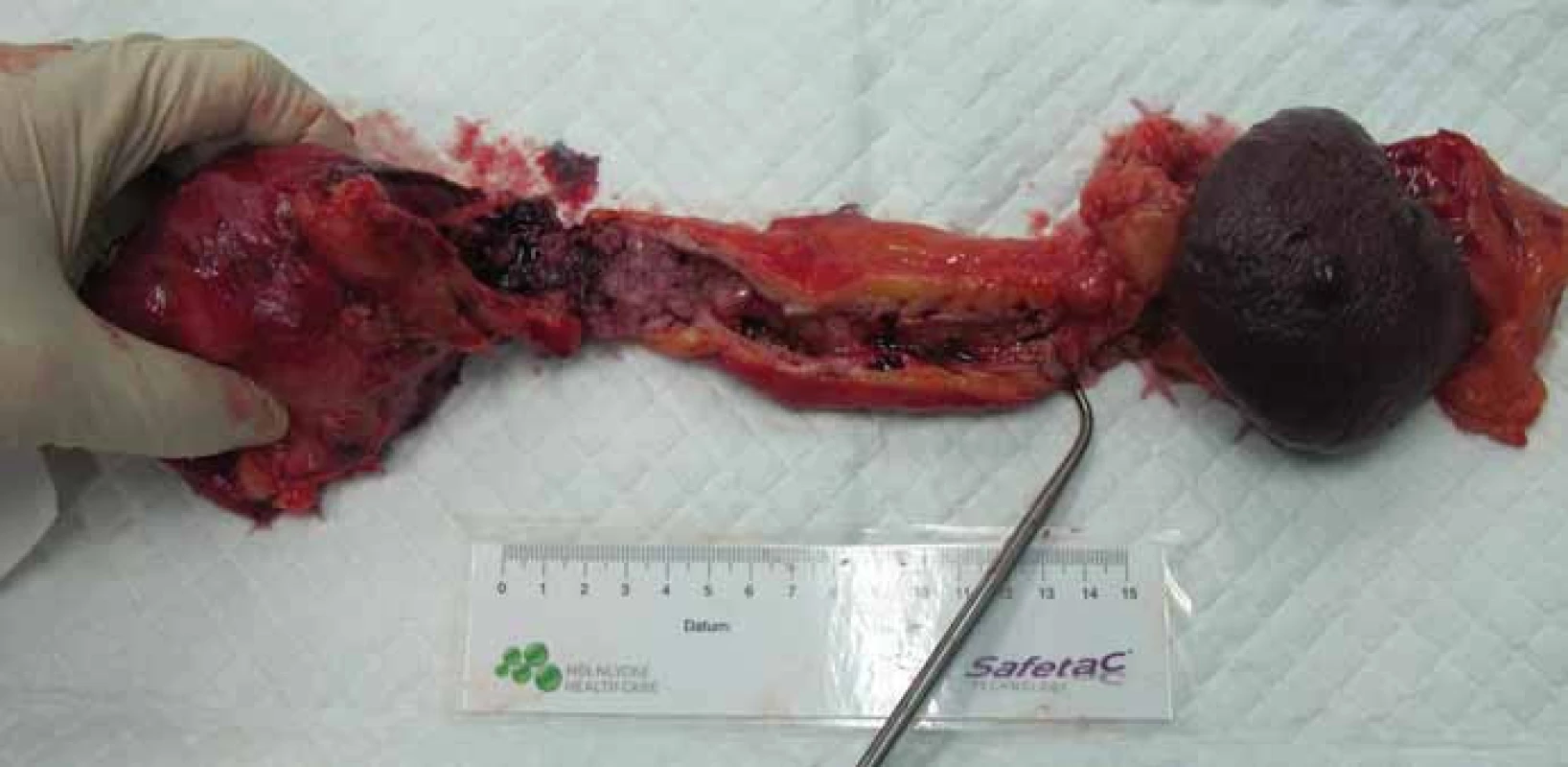
Preventivní podávání antibiotik je omezeno pouze na dobu operace. Vhodné je při operaci zavést nazojejunální sondu k časné enterální výživě. U pacienta musí být pečlivě sledována pooperační hladina glykemie.
Současné výsledky TP
Z analýzy 434 provedených TP pro primární maligní nádor pankreatu z let 2001–2012 Hartwig et al [3] vyvozují, že TP je spojeno s mediánem přežívání 24,4 měsíce – v případě benigního nálezu s pětiletým přežíváním 93,8 %, v případě duktálního adenokarcinomu 15,2 %. Hospitalizační letalita, tj. úmrtnost do 90. pooperačního dne, dosáhla v této sestavě 7,8 % s tím, že nezávislými rizikovými faktory byla krevní ztráta přesahující 2 000 ml, operační čas delší než 420 min a arteriální resekce. Almond et al [2] uvádějí u elektivní skupiny 12,5% časnou pooperační letalitu s tím, že nejčastější pooperační komplikací byla sepse a pooperační krvácení. V populační studii National Cancer Database uvádí Johnston et al [6] časnou letalitu 9,3 %. Nicméně se jedná o údaj do 30. pooperačního dne. Velmi nízkou časnou letalitu TP na sestavě 147 nemocných uvádí Müller (4,8 %) [26].
V naší sestavě 37 nemocných (z celkového počtu 41) z let 2009–2015 s elektivně provedenou TP dosáhla časná pooperační letalita měřená do 90. pooperačního dne 9,8 %. Neprokázali jsme závislost časné pooperační letality na definitivním nálezu patologa [21].
V případě urgentní indikace pro akutní pooperační pankreatitidu, kdy TP představuje de facto kompletizaci výkonu, tj. konverzi primárního parciálního výkonu na totální odstranění žlázy, se pooperační letalita pohybuje v rozmezí 11–55 % [5]. Ze čtyř našich urgentně operovaných zemřeli dva pacienti časně pooperačně [21].
Při vyloučení zemřelých v časném pooperačním období a nemocných, u kterých byla TP pro malignitu spojena s cévní rekonstrukcí, je pětileté přežívání po TP shodné s přežíváním po parciálním resekčním výkonu. Časná pooperační letalita je však vyšší zhruba dvojnásobně – u parciálních resekcí se na specializovaných pracovištích pohybuje mezi 2 a 4 % [2–4]. Nicméně obě skupiny nemocných nejsou srovnatelné. Skupina TP je stran časných výsledků operace znevýhodněna okolnostmi, pro které byla parciální resekce považována za nedostatečnou nebo neproveditelnou (rozsah postižení, technická náročnost apod.). Randomizaci pacientů provést nelze. U TP z indikace chronické pankreatitidy je vhodné hodnotit výsledky léčby s větším časovým odstupem [27].
Výskyt pooperačních komplikací po TP se pohybuje mezi 25 a 69 % [1,26]. Ve srovnání s parciální resekcí pankreatu, ať se jedná o pankreatoduodenektomii s hrozbou insuficience pankreatodigestivní anastomózy nebo o levostrannou pankreatektomii s nebezpečím úniku pankreatické šťávy ze slepé sutury ponechané části pankreatu, vytvoření pankreatické píštěle nehrozí. Pokud rozdělíme pooperační komplikace, tak „chirurgické“ je nutné řešit u 25–37 % a „interní“ u 15–37 % nemocných po TP s tím, že s nutností provést relaparotomii musíme počítat zhruba v 10–17 % [3,26]. Podobně jako u pankreatoduodenektomie, prodlouženou dobu vyprazdňování žaludku můžeme zaznamenat u téměř 20 %, nitrobřišní a ranné infekce u 18 % a pooperační krvácení u 7 % nemocných. Větší incidence komplikací se v časném pooperačním období vyskytuje u nemocných v souvislosti s přidruženou cévní resekcí. Průměrná doba hospitalizace nemocných po TP se neliší od pacientů po resekčním výkonu.
Pooperační vznik tzv. brittle diabetes s potenciálním těžko ovlivnitelným výskytem hypoglykemických stavů je nadále předmětem diskuzí. Asi u 60 % nemocných je jedním z příznaků rozvoje karcinomu pankreatu porucha glukózové tolerance, asi ve 20 % vznikne diabetes mellitus (DM) 2. typu po resekčním výkonu. Chronická pankreatitida toto procento zvyšuje [28]. TP je jednoznačně příčinou pooperačního diabetu a pacienti po tomto výkonu jsou srovnáváni s nemocnými s DM 1. typu [2] s obdobnými změnami hodnot glykovaného hemoglobinu (HbA1c) a odpovídajícími komplikacemi. Horší výsledky vykazují nemocní, u kterých byla TP provedena pro chronickou pankreatitidu [29]. Pooperační dispenzarizace musí být proto vedena i tímto směrem.
QoL po TP hodnotí pacient paralelně s délkou přežívání. Nehledě na používání neporovnatelných hodnot získaných generickými (SF 36) a specifickými (většinou EORTC QLQ-C30, modul PAN 26) dotazníky lze zaznamenat, že QoL nemocných po TP a po parciálních resekčních výkonech se významně neliší [1,4,27].
Závěr
TP je v současné době výkonem, který má srovnatelnou pooperační letalitu a morbiditu s parciálními resekčními výkony. Jeho indikace, podobně jako u resekčních výkonů, podléhá multioborovému týmu, a to na pracovištích specializovaných na komplexní léčbu onemocnění pankreatu. Provedení TP automaticky neznamená ve srovnání s parciálním resekčním výkonem „onkologickou radikalizaci“ léčby. U části pacientů však totální odstranění žlázy umožňuje radikální výkon provést. Cenou je vznik pooperačního diabetu srovnatelného s DM 1. typu. TP zůstává i nadále výkonem selektivním, který má své místo v chirurgické léčbě onemocnění slinivky břišní.
Podpořeno MO1012.
Autor deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 6. 9. 2016
Přijato: 18. 9. 2016
prof. MUDr. Miroslav Ryska, CSc.
Chirurgická klinika 2. LF UK a ÚVN – VFN
U Vojenské nemocnice 1200
169 02 Praha 6
miroslav.ryska@uvn.cz
Zdroje
1. Watanabe Y, Ohtsuka T, Matsunage T et al. Long-term outcomes after total pancreatectomy: special reference to survivors’ living conditions and quality of life. World J Surg 2015; 39 (5): 1231–1239. doi: 10.1007/s00268-015-2948-1.
2. Almond M, Roberts KJ, Hodson J et al. Changing indications for a total pancreatectomy: perspectives over a quarter of a century. HPB (Oxford) 2015; 17 (5): 416–421. doi: 10.1111/hpb.12365.
3. Hartwig W, Gluth A, Hinz U et al. Total pancreatectomy for primary pancreatic neoplasms. Ann Surg 2015; 261 (3): 537–546. doi: 10.1097/SLA.0000000000000791.
4. Epelboym I, Winner M, DiNorcia J et al. Quality of life in patiens after total pancreatectomy is comparable with quality of life in patiens who undergo a partial pancreatic resection. J Surg Res 2014; 187 (1): 189–196. doi: 10.1016/j.jss.2013.10.004.
5. Nentwich MF, El Gammal AT, Lemcke T et al. Salvage completion pancreatectomies as damage control for post-pancreatic surgery complications: a single-center retrospective analysis. World J Surg 2015; 39 (6): 1550–1556. doi: 10.1007/ s00268-015-2969-9.
6. Johnston WC, Hoen HM, Cassera MA et al. Total pancreatectomy for pancreatic ductal adenocarcinoma: review of the National Cancer Data Base. HPB (Oxford) 2016; 18 (1): 21–28. doi: 10.1016/j.hpb.2015.07.009.
7. Fazlalizadeh R, Moghadamyeghaneh Z, Demirjian AN et al. Total pancreatectomy and islet autotransplantation: a decade nationwide analysis. World J Transplant 2016; 6 (1): 233–238. doi: 10.5500/wjt.v6.i1. 233.
8. Whipple AO, Parsons WB, Mullins CR. Treatment of carcinoma of ampulla of vater. Ann Surg 1935; 102 (4): 763–779.
9. Rockey EW. Total pancreatectomy for carcinoma: case report. Ann Surg 1943; 118 (4): 603–611.
10. Ihse I, Lilja P, Arnesjö B et al. Total pancreatectomy for cancer. An appraisal of 65 cases. Ann Surg 1977; 186 (6): 675–680.
11. Trede M, Schwall G. The complications of pancreatectomy. Ann Surg 1988; 207 (1): 39–47.
12. Martin RF, Rossi RL. Pancreatoduodenectomy with or without pylorus preservation. In: Beger HG, Warshaw AL, Buchler ME et al. The Pancreas. Oxford: Blackwell Science 1998 : 863–869.
13. Andrén-Sanberg A, Ihse I. Factors influencing survival after total pancreatectomy in patients with pancreatic cancer. Ann Surg 1983; 198 (5): 605–610.
14. Willet CG, Lewandrowski K, Warshaw AL et al. Resection margins in carcinoma of the head of the pancreas. Implications for radiation therapy. Ann Surg 1993; 217 (2): 144–148.
15. Verbeke CS, Leitch D, Menon KV et al. Redefining the R1 resection in pancreatic cancer. Br J Surg 2006; 93 (10): 1232–1237.
16. Verbeke CS, Menon KV. Redefining resection margin status in pancreatic cancer. HPB (Oxford) 2009; 11 (4): 282–289. doi: 10.1111/j.1477-2574.2009.00055.x.
17. Ducreux M, Cuhna AS, Caramella C et al. Cancer of the pancreas: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2015; 26 (Suppl 5): v56–v68. doi: 10.1093/annonc/ mdv295.
18. Ryska M, Dušek L, Pohnán R et al. Kvalita života je důležitým faktorem indikační rozvahy u nemocných s karcinomem pankreatu. Multicentrická prospektivní studie. Rozhl Chir 2012; 91 (4): 199–208.
19. Ryska M, Rudis J. Pancreatic fistula and postoperative pancreatitis after pancreatoduodenectomy for pancreatic cancer. Hepatobiliary Surg Nutr 2014; 3 : 268–275.
20. Ryska M. Předoperační staging u nemocného s karcinomem pankreatu. Gastroent Hepatol 2015; 69 (6): 525–529. doi: 10.14735/amgh2015525.
21. Ryska M, Rudiš J, Bělina F et al. Totální pankreatektomie. Retrospektivní klinická studie. RvCH 2016. In press.
22. Russell RC. Surgical failures – total pancreatectomy. In: Beger HG, Warren RS, Büchler MW et al. The Pancreas. Oxford: Blackwell Science 1998; 877–885.
23. Kocik M, Lipar K, Saudek F et al. Pancreatic islet autotransplantation after com - pletion pancreatectomy for pancreatic fistula after hemipancreatoduodenectomy for carcinoma. Transplant Proc 2014; 46 (6): 1996–1998. doi: 10.1016/j.trans - proceed.2014.06.009.
24. Kulu Y, Schmied BM, Werner J et al. Total pancreatectomy for pancreatic cancer: indications and operative technique. HPB (Oxford) 2009; 11 (6): 469–475. doi: 10.1111/j.1477-2574.2009.00085.x.
25. Tol JAMG, Gouma DJ, Bassi C et al. Definition of a standard lymphadenectomy in surgery for pancreatic ductal adenocarcinoma: a consensus statement by the International Study Group on Pancreatic Surgery (ISGPS). Surgery 2014; 156 (3): 591–600. doi: 10.1016/j.surg.2014.06. 016.
26. Müller MW, Friess H, Kleeff J et al. Is there still a role for total pancreatectomy? Ann Surg 2007; 246 (6): 966–974.
27. Behrman SW, Mulloy M. Total pancreatectomy for the treatment of chronic pancreatitis: indications, otcomes, and recommendations. Am Surg 2006; 72 (4): 297–302.
28. Wu JM, Ho TW, Kuo TC et al. Glycemic change after pancreaticoduodenectomy: a population-based study. Medicine (Baltimore) 2015; 94 (27): e1109. doi: 10.1097/MD.0000000000001109.
29. Jethwa P, Sodergren M, Lala A et al. Diabetic control after total pancreatectomy. Dig Liver Dis 2006; 38 (6): 415–419.
Štítky
Detská gastroenterológia Gastroenterológia a hepatológia Chirurgia všeobecná
Článek Gastrointestinální onkologieČlánek Zpráva z odborné stážeČlánek Ursodeoxycholová kyselinaČlánek Správná odpověď na kvíz
Článok vyšiel v časopiseGastroenterologie a hepatologie
Najčítanejšie tento týždeň
2016 Číslo 5- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Gastrointestinální onkologie
- Vzácná komplikace ulcerózní kolitidy
- Současné principy screeningu kolorektálního karcinomu – od oportunního k populačnímu screeningovému programu
-
Mezioborová spolupráce ve screeningu kolorektálního karcinomu
Čekací doba na kolonoskopii - „Full-thickness“ endoskopická resekce lokální reziduální neoplazie v hepatální flexuře – videokazuistika
- Dlouhodobé výsledky po radikálních resekcích pro adenokarcinom žaludku
- SOUTĚŽ O DVĚ NEJLEPŠÍ PŮVODNÍ PRÁCE 2016
- Totální pankreatektomie a její současné místo v léčbě onemocnění pankreatu
- Modifikovaný FOLFIRINOX v léčbě karcinomu pankreatu – účinnost a toxicita
- Metastazující maligní melanom do trávicího traktu bez známého primárního ložiska
- „Watermelon stomach” jako první příznak cirhózy jater
- Vzácná komplikace koloskopie – cholelitiáza s komplikacemi
- Prehepatální portální hypertenze
- Extraezofageální a gastroezofageální reflux – vztah k astma bronchiale
- 48th Annual Meeting of the European Pancreatic Club in Liverpool, 6–9th July 2016
- Zpráva z odborné stáže
- Výběr z mezinárodních časopisů
- Kreditovaný autodidaktický test: gastrointestinální onkologie
- Ursodeoxycholová kyselina
- Správná odpověď na kvíz
- Gastroenterologie a hepatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Modifikovaný FOLFIRINOX v léčbě karcinomu pankreatu – účinnost a toxicita
- Prehepatální portální hypertenze
- Extraezofageální a gastroezofageální reflux – vztah k astma bronchiale
- Totální pankreatektomie a její současné místo v léčbě onemocnění pankreatu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



