-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Explantace stimulátoru nervus vagus odpovídající protokolu vyšetření magnetickou rezonancí
Surgical explantation of a vagal nerve stimulator according to the magnetic resonance imaging protocol
Aim: An overview of MRI in patients with implanted vagal nerve stimulator (VNS) and the method of surgical explantation of VNS, reflecting the MRI protocol allowing the subsequent MRI examination without significant limitations.
Patients and methods: MRI can also be safely performed in patients with the implanted VNS device. Head examination and body examination caudally from Th8 can be performed, but only local radiofrequency coils must be used. Before the MRI, the VNS system must be reprogrammed. If the patient has an explanted generator and the larger part of the electrode, the MRI of the entire body can be performed with any common MRI setting. This applies to a situation where after the explantation there is only a 2 - cm part of the electrode left – corresponding to the portion of the electrode on the vagal nerve with fixation anchors.
Results: From June 2016 to June 2018, we explanted a VNS with this approach in six patients. Post-operative course of all patients was without complications. Post-operative control was performed using neck X-ray and CT 3D imaging. Imaging methods showed that the remainder of the electrode on the vagal nerve electrode was ≤ 2 cm. Post-operatively, patients did not have swallowing difficulties, hoarseness or voice changes. Four patients have subsequently already undergone MRI without any difficulties or complications.
Conclusion: Surgical explantation of VNS according to the MRI protocol, leaving part of the electrode on the vagal nerve and omitting the complete preparation of the entire electrode on the nerve, reduces the risk of complications and shortens the duration of the operation. The patient can afterwards safely undergo the MRI of the entire body without any limitations in normal technical settings.
患者和方法:
在植入VNS装置的患者中,MRI也可以安全地进行。头部检查和身体检查可以从Th8尾部进行,但只能使用局部射频线圈。在MRI之前,VNS系统必须重新编程。如果患者有一个外植的发电机和电极的更大部分,整个身体的MRI可以在任何常见的MRI设置下进行。这适用于一种情况,即移植后仅剩下电极的2-cm部分—对应于带固定锚的迷走神经上的电极部分。
结果:
从2016年6月到2018年6月,我们用这种方法在6例患者中移植了VNS。所有患者术后均无并发症发生。术后对照采用颈部x线片和CT三维成像。成像方法显示,迷走神经电极上电极的剩余部分≤2cm。术后,患者没有吞咽困难,声音嘶哑或声音变化。四名病人其后已接受核磁共振检查,没有任何困难或并发症。
结论:
根据MRI协议进行VNS手术切除,将部分电极保留在迷走神经上,省去了整个神经电极的完整准备,降低了并发症的风险,缩短了手术时间。患者可以在正常的技术条件下安全的进行全身的MRI检查,没有任何限制。
关键词:
癫痫。磁共振成像。迷走神经刺激。装置移除
Keywords:
Epilepsy – vagal nerve stimulation – device removal
Autoři: M. Bláha 1; M. Tomášek 2; V. Suchánek 3; P. Marusič 2; J. Lisý 3; M. Tichý 1
Vyšlo v časopise: Cesk Slov Neurol N 2019; 82(2): 183-188
Kategorie: Původní práce
prolekare.web.journal.doi_sk: https://doi.org/10.14735/amcsnn2019183Souhrn
Cíl: Přehled možností provedení MR u pacientů s implantovaným vagovým stimulátorem (vagal nerve stimulator; VNS) a způsob chirurgické explantace VNS odpovídající MR protokolu a umožňující následné vyšetření MR bez výrazných omezení.
Soubor a metodika: MR vyšetření je možné provést i u pacientů s implantovaným VNS. Lze provést vyšetření hlavy a těla kaudálně od Th8. Musí však být použita pouze lokální radiofrekvenční cívka a před MR musí být generátor VNS přeprogramován. Pokud má pacient generátor a větší část elektrody explantovány, lze provést MR v oblasti celého těla jakýmkoliv MR nastavením. To platí pro situaci, kdy po explantaci zůstane nejvýše 2cm část elektrody – což odpovídá části elektrody na vagovém nervu s fixačními kotvičkami.
Výsledky: Od června 2016 do června 2018 jsme explantovali VNS výše uvedeným způsobem u šesti pacientů. Pooperační průběh u všech pacientů byl bez významných komplikací. Pooperační kontrolu jsme provedli pomocí RTG krku a CT 3D zobrazení. Zobrazovací metody ukázaly ponechanou část elektrody na n. vagus ≤ 2 cm. Pooperačně pacienti neměli polykací obtíže, chrapot ani změnu hlasu. Čtyři pacienti následně po zhojení rány již podstoupili MR bez jakýchkoliv obtíží či komplikací.
Závěr: Explantace VNS odpovídající MR protokolu s ponecháním části elektrody na n. vagus, tedy vynecháním kompletní preparace celé elektrody na nervu, snižuje riziko komplikací a zkracuje dobu operačního zákroku. Pacientovi můžeme následně bezpečně provádět MR celého těla bez omezení v běžných technických nastaveních.
Klíčová slova:
epilepsie – stimulace nervus vagus – explantace
Úvod
Stimulace vagového nervu je paliativní metodou léčby pacientů s refrakterní fokální i generalizovanou epilepsií. První implantace vagového stimulátoru (vagal nerve stimulator; VNS) byla provedena v USA v roce 1988 [1] a metoda byla schválena ke klinickému použití U. S. Food and Drug Administration v roce 1997 po klinických studiích bezpečnosti a účinnosti [2,3]. První implantace VNS v ČR se uskutečnila již v roce 1997. V současné době (k 18. září 2018) bylo v naší republice již implantováno 894 VNS u 604 pacientů [4]. To znamená 604 primoimplantací a 290 opakovaných operací u těchto pacientů – výměna generátoru při vybití baterie nebo pro malfunkci generátoru či elektrody.
Snížení frekvence nebo intenzity záchvatů vede ke zlepšení kvality života asi u 2/ 3 pacientů s VNS a s prodlužující se dobou od implantace je snížení počtu záchvatů výraznější [2,3,5 – 10]. Pacientů s VNS postupně v ČR přibývá. I tito pacienti mohou potřebovat během svého života vyšetření pomocí MR. Ať už pro onemocnění nesouvisející s jejich základní diagnózou epilepsie nebo pro nové posouzení vhodnosti resekční operace. V prvním případě se může jednat o nutné vyšetření při degenerativním postižení páteře, při nádorovém onemocnění nebo stále častěji o vyšetření velkých kloubů po úraze nebo při pokročilé artróze. V druhém případě pak rozvoj neurodiagnostických metod, a hlavně metody mapování stereotakticky zavedenými hlubokými mozkovými elektrodami, dnes umožní naplánovat resekční výkon u většího spektra pacientů, než tomu bylo před lety [11 – 15]. U pacientů s VNS, zvláště nebylo-li dosaženo výrazného zlepšení, je tedy možné s odstupem let provést nové posouzení vhodnosti resekční operace a vyšetřit je jako možné kandidáty resekční operace. MR patří k základním vyšetřovacím metodám před epileptochirurgickým výkonem.
Protokol výrobce vagového stimulátoru firmy LivaNova, Inc. – dříve Cyberonics, Inc. (Londýn, Velká Británie) – pro MR vyšetření u VNS z roku 2016 umožňoval toto provést ve dvou různých základních klinických situacích [16]. V případě implantovaného VNS je možné vyšetření hlavy a těla kaudálně od Th8, musí však být použita pouze lokální radiofrekvenční (RF) cívka a před MR musí být generátor VNS přeprogramován. Pokud má pacient generátor a větší část elektrody explantovány, lze provést MR v oblasti celého těla jakýmkoliv MR nastavením. To platí pro situaci, kdy po explantaci zůstane pouze 2 cm dlouhá část elektrody, což odpovídá části elektrody na vagovém nervu s fixačními kotvičkami. Novelizovaný protokol z října 2017 je poměrně složitý [17]. Rozděluje implantované systémy VNS na dvě skupiny – A a B. Do skupiny A patří modely 105, 106 a 1 000 – s implantovaným generátorem nad IV. žebrem. Ostatní modely – 100C, 101, 102, 102R, 103, 104 nebo modely 105, 106, 1 000 – s generátorem níže než IV. žebro řadíme do skupiny B. Pro skupinu B platí stejná omezení, jaká jsou v Protokolu z roku 2016. Skupina A může být vyšetřována stejně jako skupina B a navíc ve speciálních situacích se může použít celotělová RF vysílací cívka (body coil), avšak při rozšíření „zakázané“ zóny od C7 do L3. Prakticky lze tedy u pacientů s modelem 105 a 106 navíc vyšetřit pomocí MR pouze pánev. V další části práce tak budeme popisovat omezení a nastavení pro skupinu B, kam můžeme zařadit i zbytek stimulátorů, pokud nebudeme vyžadovat vyšetření pánve.
Explantaci VNS zvažujeme v případě jeho klinické neúčinnosti či pouze nevýznamného efektu na epileptické záchvaty. Důležitý je postoj pacienta. Na jedné straně spektra jsou pacienti, kteří chtějí „všechno pryč“, a naopak na druhé straně pacienti, kteří už nechtějí žádnou operaci. Při posuzování indikace k explantaci VNS jsou jistě podstatné i věk pacienta a jeho přidružené choroby – pravděpodobnost, že bude potřebovat vyšetření MR v budoucnu, je v řadě případů vysoká.
Explantaci VNS je možné provést kompletně (vynětí generátoru a celé elektrody) nebo částečně. Explantace generátoru v podklíčkové oblasti je technicky poměrně snadná. Preparace a explantace elektrody v krční oblasti je již technicky obtížnější a může být zatížena i komplikacemi. Ponechání části elektrody přímo na vagovém nervu sníží riziko léze n. laryngeus recurrens a poranění jugulární žíly [16 – 18]. Pokud ponecháme elektrodu na vagovém nervu v délce 2 cm a méně podle zde popsaného protokolu, pacientovi můžeme bezpečně provést MR celého těla bez jiných omezení v běžných technických nastaveních [16,17,19 – 21].
Soubor a metodika
Vyšetření MR u pacientů s implantovaným funkčním VNS
Pro provádění MR u pacientů s implantovaným funkčním VNS je nutná součinnost epileptologa, lékaře a laboranta MR. Vyšetření je možné provést mimo oblast uložení VNS – zelená zóna (obr. 1). Generátor a elektroda systému VNS nesmí být vystaveny RF poli. Při tomto vyšetření je nutné použít lokální RF cívky jako zdroj RF pole. Lze tedy provést MR vyšetření hlavy, lokte, zápěstí, kolen a kotníků. Jako zdroj RF pole nesmí být použita celotělová cívka ani RF cívka v lehátku pacienta. Do prostoru MR se nesmí přinést ani programovací zařízení ani magnet pacienta.
Obr. 1. Vyšetření MR u pacientů s implantovaným funkčním vagovým stimulátorem. MR je možné provést v zelené zóně a s použitím lokálních radiofrekvenčních (RF) cívek. V šedé zóně se MR nesmí provádět.
Fig. 1. MRI in patients with an implanted vagal nerve stimulator. MRI can be safely performed in the green zone with local radiofrequency (RF) coils. Gray area is the MRI exclusion zone.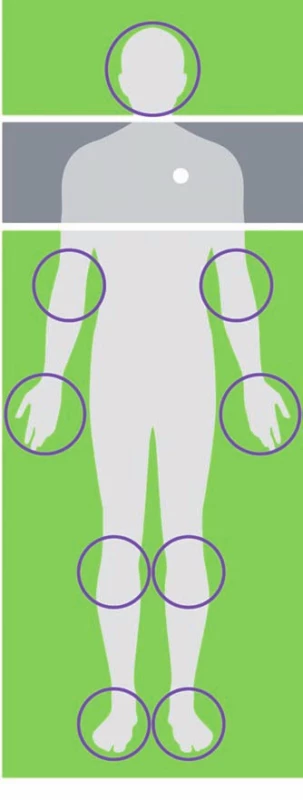
Postup před provedením MR
- Pomocí programovacího systému se provede systémová diagnostika VNS a zaznamenají nastavené parametry stimulace:
- přeprogramují se parametry stimulačního proudu pro Normal mode i Magnet mode – Output current i Magnet current (mA): 0,0;
- u AspireSR Model 106 se v AutoStim mode nastaví:
- AutoStim current (mA): 0,0 a detekce tachykardie (tachycardia detection) OFF;
- kontrola programátorem, zda přednastavené parametry byly adekvátně uloženy;
- pacient je poučen, aby nahlásil bolest, dyskomfort nebo pocit tepla v oblasti krku či hrudníku při vyšetření laborantovi MR, který může vyšetření zastavit.
Postup po provedeném MR
- Pomocí programovacího systému se provede systémová diagnostika VNS;
- pokud došlo k resetování základních dat generátoru, vloží se znovu sériové číslo, identifikační údaje pacienta a datum implantace;
- naprogramují se zpět stimulační parametry;
- kontrola impedance elektrody a adekvátního uložení přednastavených parametrů.
Vyšetření MR u pacientů s nefunkčním VNS či částečně explantovaným systémem (pokud zůstává > 2 cm elektrody)
Možnosti a omezení vyšetření MR jsou stejné jako v předchozím případě při funkčním VNS. Vyšetření MR je možné provést s lokální RF cívkou mimo oblast uložení VNS – hlava, lokty, zápěstí, kolena a kotníky. Nelze použít jako zdroj RF pole celotělovou cívku ani RF cívku v lehátku pacienta. Nemusí se pomocí programátoru odlišně nastavovat generátor, pacient se poučí, aby nahlásil bolest, dyskomfort nebo pocit tepla v oblasti krku nebo hrudníku při vyšetření laborantovi MR, který může vyšetření ukončit.
Vyšetření MR u pacientů s explantovaným systémem dle výše uvedeného protokolu (zůstává ≤ 2 cm elektrody na vagovém nervu)
U těchto pacientů je možné provést MR vyšetření celého těla. Jako zdroj RF pole se dá použít lokální, celotělová i lehátková cívka. Neměl by být překročen gradient magnetického pole 720 gauss/ cm a specifická míra absorbce pro vyšetření hlavy 3,2 W/ kg (obr. 2). Tyto hodnoty nejsou při běžných vyšetřeních na 1,5 a 3Teslových přístrojích překračovány. Měření na fantomech a zkušenosti s pacienty jsou zatím pouze s uzavřenými MR, a proto je doporučováno provádět vyšetření pouze na tomto typu přístroje [16,17,19 – 21].
Obr. 2. Přípustné parametry a konfigurace MR vyšetření pro různé klinické situace. RF – radiofrekvenční; SAR – specifická míra absorbce; VNS – stimulátor vagového nervu
Fig. 2. Permitted MRI configurations and modes for different clinical situations. RF – radiofrequency; SAR – specific absorption rate; VNS – vagal nerve stimulator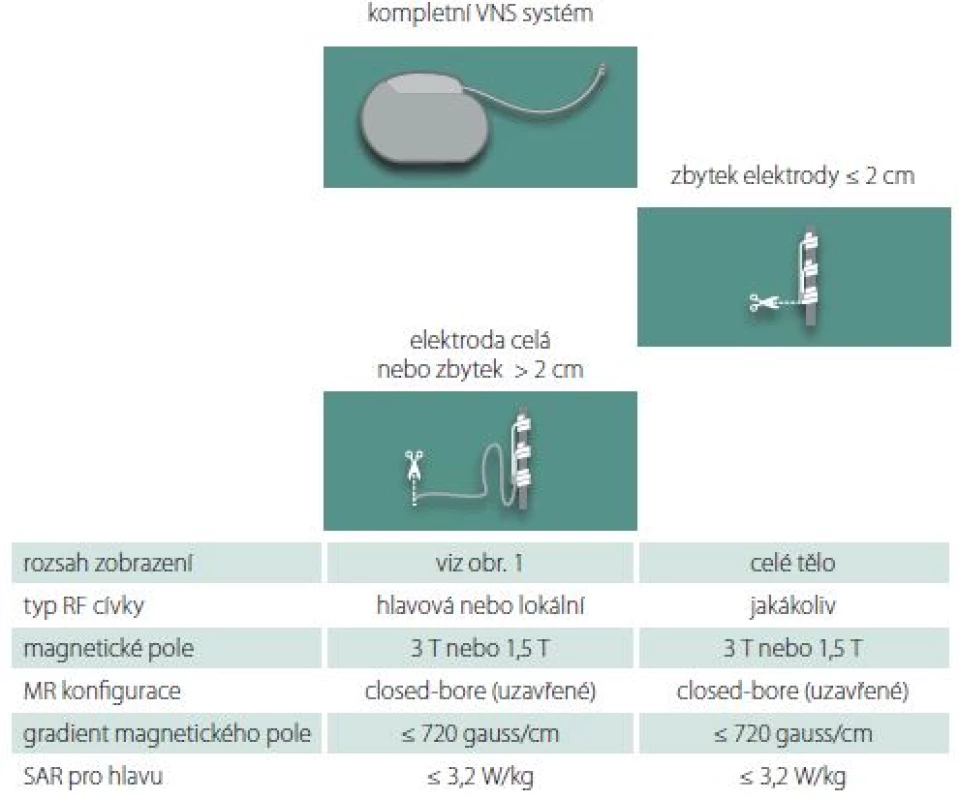
Explantace VNS
Cílem této operace je vynětí implantovaného hardwaru – generátoru, elektrody a fixačních plochých křidélek – s ponecháním distální části elektrody přímo na vagovém nervu s třemi fixačními kotvičkami. Operaci provádíme v celkové anestezii v poloze pacienta na zádech s vytočenou hlavou doprava. Snažíme se využít původní jizvy na hrudníku a krku. Explantace generátoru je technicky poměrně snadná. Riziko komplikací je malé, nejčastěji může dojít k pooperačnímu hematomu v místě kapsy generátoru, bez nutnosti re-intervence. Pokud jsou kapsa a mrtvý prostor větší, ponecháváme na pooperační období drenážní systém Mini-Redon (B. Braun Medical Inc., Bethlehem, PA, USA). Vyjmutí elektrody v tunelizované části přes klíček a na distální straně krku může vyžadovat pomocnou kožní incizi, pokud jde o starší elektrodu, která se při extrakci trhá a nelze ji vyjmout v jednom kuse. Preparace elektrody v krční oblasti je již technicky obtížnější a může být zatížena i komplikacemi. Pro snazší orientaci v jizevnatém terénu provádíme všem pacientům předoperační RTG krku. Ten nám ukáže počet implantovaných fixačních křidélek i počet a velikost jednotlivých smyček elektrody. V původní jizvě na krku lze poměrně snadno nalézt povrchově uloženou část elektrody a fixační křidélka. Po odstranění všech fixačních křidélek provedeme preparaci v jizvě do prostoru mezi karotidou a jugulární žílou pod mikroskopem směrem k první fixační kotvičce na nervu (je umístěna nejvíce kaudálně na vagovém nervu, na elektrodě je však nejvíce proximálně). Druhou, méně častou možností je postupovat po elektrodě kaudálně, kde se stáčí do poslední smyčky a míří kraniálně k první fixační kotvičce na vagovém nervu. Tato metoda disekce postupem po elektrodě v celé její délce je mnohem obtížnější než přímý přístup k nervově cévnímu svazku s vyhledáním kotviček na nervu. Manipulace s nervem by měla být co nejmenší, protože na rozdíl od primoimplantace je nerv již fixován jizvou. Elektrodu ustřihneme u napojení na tuto první kotvičku, což ponechá na vagovém nervu část elektrody ≤ 20 mm dlouhou s ponechanými třemi fixačními kotvičkami (první kotvička je pouze fixační, další dvě jsou RTG kontrastní s elektrickými kontakty) (obr. 3). Uvolněnou a vypreparovanou elektrodu v krční ráně vyjmeme a zkontrolujeme celistvost. Podle velikosti rány a krvácení i zde můžeme použít drenážní systém Mini-Redon. Pacienta můžeme propustit do domácího ošetřování první nebo druhý pooperační den. Před dimisí je vhodné provést RTG krku k potvrzení adekvátní explantace elektrody (obr. 4). Kontrolní RTG krku ukáže ponechanou malou rovnou část elektrody na vagovém nervu, je vidět druhá a třetí kotvička s kontakty. První fixační kotvička je RTG nekontrastní. Pokud byla elektroda odstřižena těsně před začátkem první kotvičky, je zbytek elektrody na vagovém nervu dlouhý 20 mm – jak jsme ověřili provedením CT u prvních dvou pacientů (obr. 5). Měření vzdálenosti na prostém RTG snímku krku je nepřesné.
Obr. 3. Zbytek elektrody ponechaný na vagovém nervu. Kotvička na obrázku dole je pouze fixační a je RTG nekontrastní.
Fig. 3. The remainder of the electrode left on the vagal nerve. Lower anchor is only for fixation and is from X-ray non-contrast material.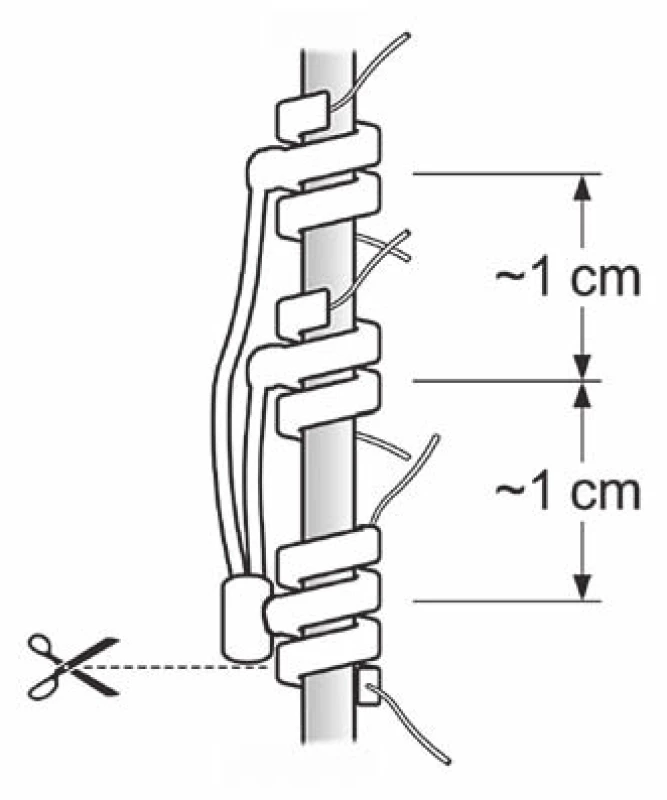
Obr. 4. Pooperační RTG s ponechaným zbytkem elektrody na vagovém nervu.
Fig. 4. Postoperative X-ray with the remainder of the electrode on the vagal nerve.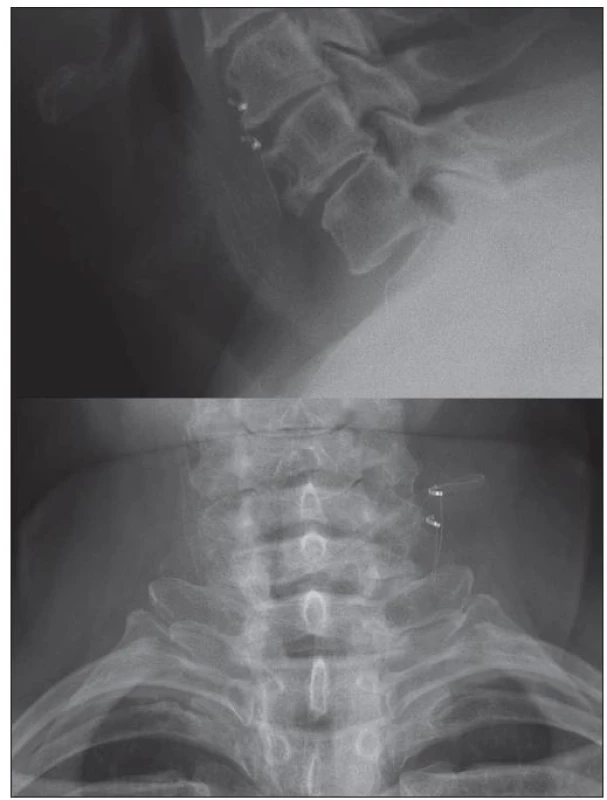
Obr. 5. Pooperační CT s ponechaným zbytkem elektrody na vagovém nervu.
Fig. 5. Postoperative CT with the remainder of the electrode on the vagal nerve.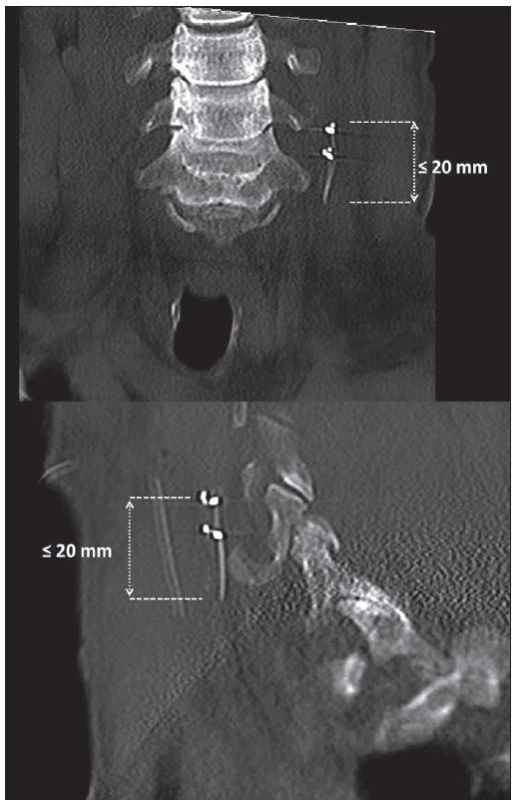
Výsledky
Od června 2016 do června 2018 jsme explantovali VNS výše uvedeným protokolem u šesti pacientů. Jednalo se o čtyři muže a dvě ženy – průměrný věk 38,5 ± 10 let. Vagový stimulátor měli zaveden 12,8 ± 3,7 let. Pětkrát jsme explantovali celý systém – tedy generátor a elektrodu až k odstupu první kotvičky. Jeden z pacientů měl již generátor a část elektrody vyjmuty na jiném pracovišti a explantovali jsme tedy úsek elektrody o délce asi 5 cm, také k odstupu první kotvičky. Pooperační průběh u všech pacientů byl bez komplikací. Pooperační kontrolu pro potvrzení adekvátního odstranění hardwaru jsme provedli pomocí bočního a předozadního RTG krku a u prvních dvou pacientů pomocí 3D zobrazení CT. Zobrazovací metody ukázaly ponechanou část elektrody na n. vagus ≤ 2 cm. Pooperačně pacienti neměli polykací obtíže, chrapot ani změnu hlasu. Čtyři pacienti následně po zhojení rány již podstoupili MR bez jakýchkoliv obtíží. Protože se jednalo o novou klinickou situaci, u třech pacientů při prvním vyšetření MR osobně dohlíželi radiolog a neurochirurg. Během vyšetřování i po něm jsme u pacientů nezaznamenali bolest, dyskomfort, teplo ani polykací obtíže. Z těchto čtyř pacientů již tři podstoupili resekční epileptochirurgický výkon.
Diskuze
Asi u jedné třetiny pacientů s implantovaným VNS není významný efekt na snížení frekvence nebo intenzity záchvatů, a tím tedy nedochází ke zlepšení kvality života [2,3,5 – 10]. U těchto pacientů je možno zvažovat explantaci VNS. Při rozhodování o tomto operačním výkonu jistě hraje velkou roli i riziko možných komplikací. Z tohoto hlediska by nejbezpečnějším výkonem bylo odstranění generátoru v podklíčkové oblasti a částečné vynětí elektrody tunelované podkožně do oblasti krku. Při tomto výkonu bychom odstranili části systému, které jsou na pacientovi viditelné a hmatné. Zbytek elektrody by však v budoucnu pacienta limitoval pro provedení MR. Výkonem naopak s nejvyšším rizikem komplikací je totální odstranění celého systému. Tento typ operace může být nutný v případě infekce nebo při výměně nefunkční elektrody. Preparace v oblasti jugulární žíly může vést k peroperačnímu krvácení a mobilizace elektrody a fixačních kotviček z vagového nervu k pooperační přechodné nebo permanentní dysfunkci tohoto nervu [18,22 – 26]. Incidence paralýzy hlasivek po revizní operaci v oblasti vagového nervu je vyšší (3 %) než u primoimplantací, ale u většiny pacientů dochází ke spontánnímu zotavení. Trvalá paralýza nastává u < 1 % pacientů po re-operacích [22,26]. Explantace VNS podle MR protokolu s ponecháním části elektrody na vagovém nervu, tedy vynecháním kompletní preparace celé elektrody na nervu, snižuje riziko komplikací a zkracuje dobu operačního zákroku. Pacientovi můžeme následně bezpečně provádět MR celého těla bez omezení v běžných technických nastaveních. Jakékoliv komplikace vyplývající z ponechání 20mm části elektrody na vagovém nervu nejsou podle současné odborné literatury zatím známy. V našem souboru šesti pacientů se zdá být tento postup přínosný. Operace je kratší, vyhneme se ne snad technicky obtížné, nýbrž spíše pro operatéra nepříjemné fázi odpreparování a sloupávaní kotvících kotviček od vagového nervu, kterou tak dobře známe při výměnách poškozených elektrod u respondérů vagové terapie. V našem souboru šesti explantací jsme nezaznamenali žádnou peroperační ani pooperační komplikaci a následné vyšetření MR u čtyř pacientů proběhlo velmi dobře. Tři pacienti po explantaci VNS touto metodou byli již indikováni k resekčnímu epileptochirurgickému výkonu a podstoupili jej.
Závěr
U pacientů s implantovaným VNS lze provést vyšetření pomocí MR podle výše zmíněných protokolů, s určitými omezeními v nastavení a mimo oblast uloženého stimulátoru. Při vyšetření je nutná součinnost epileptologa, lékaře a laboranta MR. Explantaci VNS je vhodné zvážit v případě jeho klinické neúčinnosti – podstatné jsou věk pacienta, jeho přidružené choroby, postoj pacienta k další operaci, možná indikace k resekční epileptochirurgické operaci a odhad nutnosti MR vyšetření nyní a v budoucnosti. Explantace systému VNS s ponecháním elektrody na n. vagus v délce 2 cm podle zde popsaného protokolu snižuje riziko komplikací a umožňuje následně provádět vyšetření pomocí MR bez speciálních opatření a omezení.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Přijato k recenzi: 11. 10. 2018
Přijato do tisku: 5. 2. 2019
MUDr. Martin Bláha, Ph.D.
Neurochirurgická klinika dětí a dospělých
2. LF UK a FN Motol
V Úvalu 84
150 06 Praha
e-mail: drmartinblaha@yahoo.com
Zdroje
1. Penry JK, Dean JC. Prevention of intractable partial seizures by intermittent vagal stimulation in humans: preliminary results. Epilepsia 1990; 31 (Suppl 2): S40 – S43.
2. Ben-Menachem E, Mañon-Espaillat R, Ristanovic R et al. Vagus nerve stimulation for treatment of partial seizures: 1. A controlled study of effect on seizures. First International Vagus Nerve Stimulation Study Group. Epilepsia 1994; 35(3): 616 – 626.
3. Ramsay RE, Uthman BM, Augustinsson LE et al. Vagus nerve stimulation for treatment of partial seizures: 2. Safety, side effects, and tolerability. First International Vagus Nerve Stimulation Study Group. Epilepsia 1994; 35(3): 627 – 636.
4. Cardion s. r. o. Databáze pacientů. Brno 2018.
5. Spanaki MV, Allen LS, Mueller WM et al. Vagus nerve stimulation therapy: 5-year of greater outcome at a university-based epilepsy center. Seizure 2004; 13 : 587 – 590.
6. DeGiorgio CM, Schachter SC, Handforth A et al. Prospective long term study of vagus nerve stimulation for the treatment of refractory seizures. Epilepsia 2000; 41(9): 1195 – 1200.
7. Chrastina J, Novak Z, Zeman T et al. Single-center long-term results of vagus nerve stimulation for epilepsy: A 10 – 17 year follow-up study. Seizure 2018; 59 : 41 – 47. doi: 10.1016/ j. seizure. 2018. 04. 022.
8. Englot DJ, Rolston JD, Wright CW et al. Rates and predictors of seizure freedom with vagus nerve stimulation for intractable epilepsy. Neurosurgery 2016; 79(3): 345 – 353. doi: 10.1227/ NEU.0000000000001165.
9. Reid SA. Surgical technique for implantation of the neurocybernetic prosthesis. Epilepsia 1990; 31(Suppl 2): S38 – S39.
10. Kuba R, Brázdil M, Kalina M et al. Vagus nerve stimulation: longitudinal follow-up of patients treated for 5 years. Seizure 2009; 18(4): 269 – 274. doi: 10.1016/ j.seizure.2008.10.012.
11. Kovac S, Vakharia VN, Scott C et al. Invasive epilepsy surgery evaluation. Seizure 2017; 44 : 125 – 136. doi: 10.1016/ j.seizure. 2016.10.016.
12. Ryvlin P, Cross JH, Rheims S. Epilepsy surgery in children and adults. Lancet Neurol 2014; 13(11): 1114 – 1126. doi: 10.1016/ S1474-4422(14)70156-5.
13. Wang ZI, Jones SE, Jaisani Z et al. Voxel-based morphometric magnetic resonance imaging (MRI) postprocessing in MRI-negative epilepsies. Ann Neurol 2015; 77(6): 1060 – 1075. doi: 10.1002/ ana.24407.
14. Hanáková P, Horák O, Ryzí M et al. Identifikace dětských pacientů s farmakorezistentní epilepsií a výběr kandidátů nefarmakologické terapie. Cesk Slov Neurol N 2018; 81/ 114(2): 180 – 184. doi: 10.14735/ amcsnn2018180.
15. Serletis D, Bulacio J, Bingaman W et al. The stereotactic approach for mapping epileptic networks: a prospective study of 200 patients. J Neurosurg 2014; 121(5): 1239 – 1246. doi: 10.3171/ 2014.7.JNS132306.
16. Cyberonics, Inc. MRI Guidelines for VNS Therapy®. [online]. Available from URL: http:/ / www.cardion.cz/ data/ mri-kompatibilita/ vns-terapie.pdf.
17. LivaNova, PLC. MRI with the VNS Therapy® System. [online]. Available from URL: https:/ / us.livanova.cyberonics.com/ healthcare-professionals/ prescribing-information.
18. Giordano F, Zicca A, Barba C et al. Vagus nerve stimulation: surgical technique of implantation and revision and related morbidity. Epilepsia 2017; 58 (Suppl 1): 85 – 90. doi: 10.1111/ epi.13678.
19. Gorny KR, Bernstein MA, Watson RE. 3 Tesla MRIof patiens with a vagus nerve stimulator: initial experience using a T/ R head coil under controlled conditions. J Magn Reson Imaging 2010; 31(2): 475 – 481. doi: 10.1002/ jmri. 22037.
20. de Jonge JC, Melis GI, Gebbink TA et al. Safety of dedicated brain MRI protokol in patiens with a vagus nerve stimulator. Epilepsia 2014; 55(11): e112 – e115. doi: 10.1111/ epi.12774.
21. Rösch J, Hamer HM, Mennecke A et al. 3 T-MRI in patients with pharmacoresistant epilepsy and a vagus nerve stimulator: a pilot study. Epilepsy Res 2015; 110 : 62 – 70. doi: 10.1016/ j.eplepsyres.2014.11.010.
22. Kahlow H, Olivecrona M. Complications of vagal nerve stimulation for drug-resistant epilepsy: a single center longitudinal study of 143 patients. Seizure 2013; 22(10): 827 – 833. doi: 10.1016/ j.seizure.2013.06.011.
23. Couch JD, Gilman AM, Doyle WK. Long-term expectations of vagus nerve stimulation: a look at battery replacement and revision surgery. Neurosurgery 2016; 78(1): 42 – 46. doi: 10.1227/ NEU.0000000000000985.
24. Révész D, Rydenhag B, Ben-Menachem E. Complications and safety of vagus nerve stimulation: 25 years of experience at a single center. J Neurosurg Pediatr 2016; 18(1): 97 – 104. doi: 10.3171/ 2016.1.PEDS15534.
25. Rijkers K, Berfelo MW, Cornips EM et al. Hardware failure in vagus nerve stimulation therapy. Acta Neurochir (Wien) 2008; 150(4): 403 – 405. doi: 10.1007/ s00701-007-1492-7.
26. Aalbers MW, Rijkers K, Klinkenberg S et al. Vagus nerve stimulation lead removal or replacement: surgical technique, institutional experience, and literature overview. Acta Neurochir (Wien) 2015; 157(11): 1917 – 1924. doi: 10.1007/ s00701-015-2547-9.Štítky
Detská neurológia Neurochirurgia Neurológia
Článok vyšiel v časopiseČeská a slovenská neurologie a neurochirurgie
Najčítanejšie tento týždeň
2019 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Neuromultivit v terapii neuropatií, neuritid a neuralgií u dospělých pacientů
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Roztroušená skleróza mozkomíšní, těhotenství, mateřství a kojení
- Intradurálne extramedulárne nádory chrbtice
- Roztroušená skleróza mozkomíšní, úloha střevní mikrobioty v poškozujícím zánětu
- Genetické a neurobiologické aspekty komorbidního výskytu poruch autistického spektra a epilepsie
- Roztroušená skleróza a těhotenství z pohledu gynekologa – možnosti asistované reprodukce
- Hraje leptin roli v rozvoji intrakraniálních meningeomů?
- Srovnávací studie pacientů s myastenií České a Slovenské republiky
- Moderní mikrochirurgie jako trvalé, bezpečné a šetrné řešení nekrvácejících mozkových výdutí
- Explantace stimulátoru nervus vagus odpovídající protokolu vyšetření magnetickou rezonancí
- Obecné pohyby a neurologický vývoj raného věku u dětí s novorozeneckou hypoglykemií
- Srovnání kosmetického efektu krátkého podélného a příčného kožního řezu při karotické endarterektomii
- Změny v obsahu esenciálních a stopových prvků v lidských degenerujících meziobratlových ploténkách nekorespondují s klinickým stavem pacientů
- Jak náhrada extracelulárního sodíku ovlivňuje distribuci rychlosti vedení periferním nervem u krysy
- Rychlá diagnostika chemokinu CXCL13 v mozkomíšním moku u pacientů s neuroboreliózou
- Aneuryzmatické subarachoidální krvácení v těhotenství – úspěšný kliping po selhání koilingu
- Extra-intrakraniální bypass iniciovaný rehabilitačním lékařem pro kognitivní deterioraci
- Traumatické pseudoaneuryzma arterie temporalis superficialis
- Klíšťová meningitida komplikovaná kardioembolickým intraluminálním trombem v krkavici a mozkovou mrtvicí
- Genetika nervosvalových onemocnění
- Analýza dat v neurologii LXXIV. - Neparametrický Spearmanův koeficient korelace
- Recenze knih
- Doc. Vladimír Škorpil, 100 let od narození zakladatele naší elektromyografie
- Česká a slovenská neurologie a neurochirurgie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Intradurálne extramedulárne nádory chrbtice
- Rychlá diagnostika chemokinu CXCL13 v mozkomíšním moku u pacientů s neuroboreliózou
- Genetika nervosvalových onemocnění
- Roztroušená skleróza a těhotenství z pohledu gynekologa – možnosti asistované reprodukce
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



