-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Je koncept vaskulární demence trvale udržitelný?
Autori: doc. MUDr. Martin Vališ, Ph.D.; Fean
Pôsobisko autorov: Neurologická klinika LF UK a FN Hradec Králové
Vyšlo v časopise: Cesk Slov Neurol N 2020; 83(2): 141
Kategória: Kontroverze
Při hledání odpovědi na tuto otázku bude nutné připomenout si v úvodu několik základních pojmů a, jelikož článek není určen jen odborníkům zabývajícím se problematikou kognitivních poruch a demencí, stručně zrekapitulovat odkud se tento pojem vlastně vzal a co koncept vaskulární demence v současné době obnáší. Pro komplexnější pochopení toho, proč nám způsobuje tolik komplikací jak v diagnostice, tak v terapii, tato zdánlivě jasná a jednoduchá diagnóza.
Již v 17. století anglický lékař Thomas Willis jako první zmiňuje tzv. paralytickou demenci a ve svých zápisech uvádí, že „pozoroval více nemocných, u nichž se po onemocnění mozku objevila duševní tupost, poruchy paměti, stupidita a nakonec paralýza, což mohl zpravidla předvídat“. O více než 200 let později Otto Binswanger a Alois Alzheimer poprvé přesně makroskopicky a histologicky popsali vaskulární demenci jako spektrum změn mozku, tvořených lakunárními ikty, status cribrosus, arteriosklerotickými změnami, perivaskulární gliózou, graduální atrofií mozkové kůry, charakterizované jejími laminárními nekrózami a mikroinfarkty. Na základě studií prací obou výše jmenovaných autorů oddělil Emil Kraepelin od skupiny presenilních a senilních demencí nozologickou jednotku arteriosklerotická psychóza, následně v roce 1974 použil Vladimir Hachinski pojem multiinfarktová demence a od roku 1985 se v literatuře začíná objevovat název vaskulární demence, za jehož autora je pokládán Carlo Loeb [1].
Vaskulární demence nepatří mezi primárně neurodegenerativní onemocnění, jedná se o heterogenní skupinu syndromů (tab. 1), pro které je společný kognitivní deficit a vaskulární etiologie. Četností výskytu se řadí na druhé, resp. třetí místo po Alzheimerově demenci, společně s demencí s Lewyho tělísky. Mívá schodovitě postupný ráz nebo relapsy či chronicky progresivní ráz a stanovení konečné diagnózy může být svízelné, protože existuje několik diagnostických kritérií (Mezinárodní klasifikace nemocí a přidružených zdravotních problémů [MKN-10], Diagnostic and Statistical Manual of Mental Disorders [DSM], National Institute of Neurological Disorders and Stroke-Association Internationale pour la Recherche et l'Enseignement en Neurosciences [NINDS-AIREN], State of California Alzheimer's Disease Diagnostic and Treatment Centers [ADDTC]), které nejsou vždy vzájemně kompatibilní [2]. Za vaskulární demenci ve své čisté formě považujeme takovou tíži kognitivní dysfunkce, která je provázena zhoršenou autonomií pacienta a nemocný nemá příznaky kognitivního postižení jiné etiologie. V klinické praxi se však častěji setkáváme s demencí smíšenou (většinou se jedná o kombinaci vaskulární demence a Alzheimerovy nemoci), což definujeme jako stav, kdy má pacient s neurodegenerativním onemocněním větší rozsah cévního postižení mozku, než je obvyklé a je zároveň předpoklad, že souvisí s kognitivními poruchami [3].
Tab. 1. Klinicko-patologické dělení 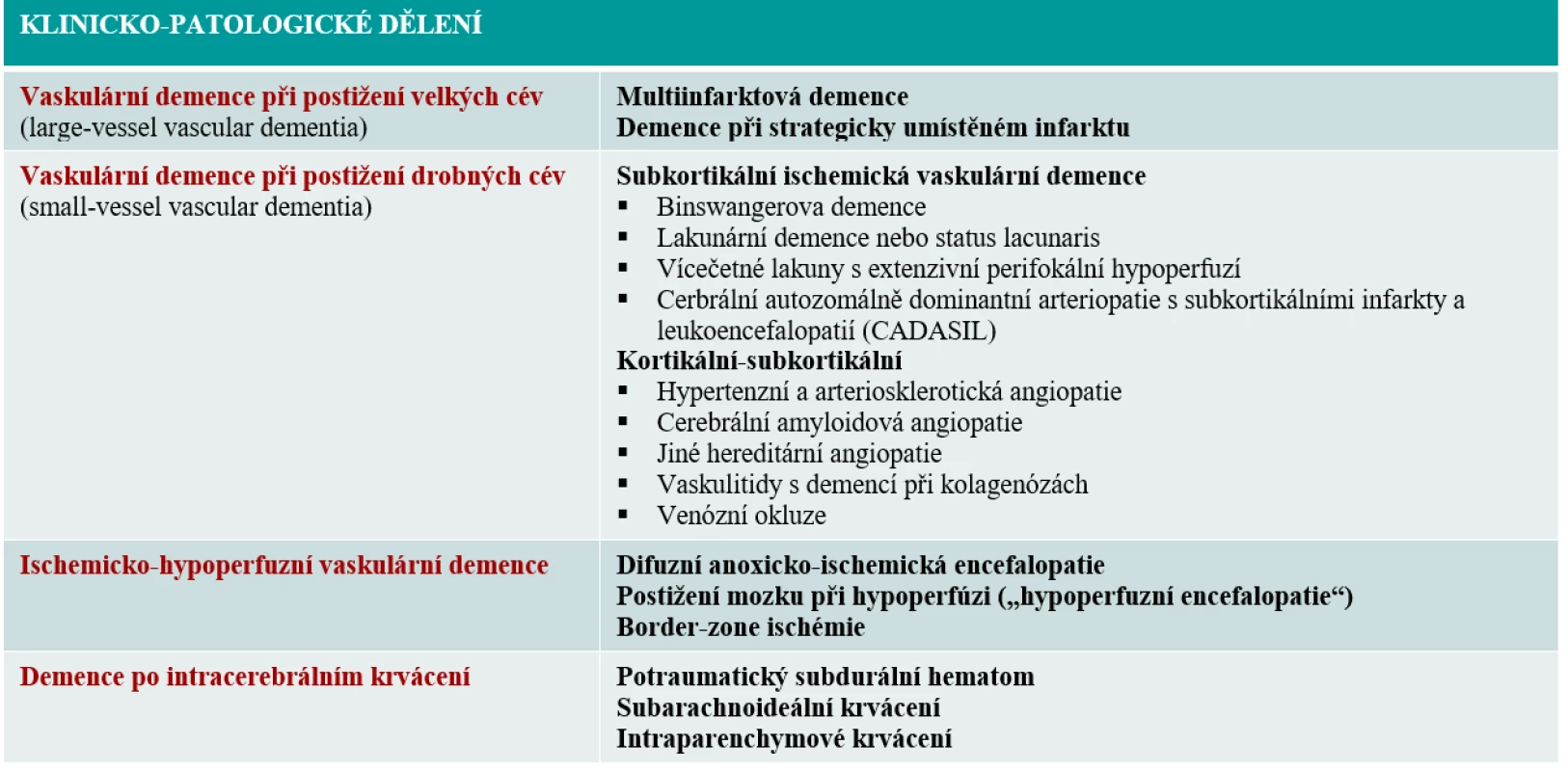
K odlišení vaskulárních od neurodegenerativních demencí se často užívá poměrně jednoduché a dobře známé Hachinského ischemické škály, přičemž skóre ≥ 7 z celkových 18 bodů svědčí pro suspektní vaskulární demenci. I když od doby vzniku Hachinského škály v roce 1974 došlo k významnému technickému rozvoji a dostupnost moderních zobrazovacích metod včetně funkčního zobrazení mozku a využití radiofarmak nepochybně přispěla k pokroku zejména ve vědeckovýzkumné oblasti, provedení těchto vyšetření vyžaduje racionální indikaci [4]. Amyloid PET umožňující stanovení denzity beta-amyloidových neuritických plak v šedé hmotě mozku in vivo není k rutinnímu diagnostickému využití a kromě finanční náročnosti může nemalé komplikace představovat dodržení přesného časového intervalu kvůli dovozu radiofarmak (flutemetamol, florbetaben, florbetapir) ze zahraničí, který je spojen s velkými ztrátami způsobenými rychlým radioaktivním rozpadem. V této souvislosti je nutné zdůraznit, že Hachinského škála není o moc horší a je významně levnější než negativní amyloid PET.
Kauzální terapie kognitivní deteriorace cévního původu dodnes neexistuje – vasodilatancia, nootropika a antioxidanty efekt neprokázaly, inhibitory acetylcholinesterázy a memantin mají podle výsledků provedených klinických studií pouze mírný efekt s nejistým klinickým významem, dostupná data nepodporují jejich široké využití v léčbě a jejich úhrada z prostředků zdravotního pojištění v ČR není schválena. Proto je veškeré terapeutické úsilí zaměřeno především na důsledné ovlivňování vaskulárních rizikových faktorů (nediagnostikovaná / nekorigovaná arteriální hypertenze, diabetes mellitus, dyslipidémie, obezita, kouření, ischemická choroba srdeční, fibrilace síní) a sekundární prevenci ischemických iktů (antihypertenziva, statiny, kompenzace diabetu, antiagregace / antikoagulace dle etiologie při prokázaném cerebrálním infarktu, endarterektomie) [2,4].
Dnes nám v praxi dělá problém zejména heterogenita vaskulárních demencí, nezřetelné hranice mezi jednotlivými skupinami, kdy stejná osoba může být klasifikována do různých kategorií a absence univerzálně přijatelného názvosloví. Velmi důležitá je i skutečnost, že ne každá demence po iktu je vaskulární, i když je třeba podotknout, že po prvním iktu je 5× vyšší riziko rozvoje demence (vaskulární, demaskování dosud „němé“ Alzheimerovy demence, smíšená demence) v příštích 12 měsících a 2× větší v dalších letech ve srovnání s běžnou populací. Vzhledem k tomu, že populace stárne a osoby starší 80 let představují ve většině evropských zemí nejrychleji rostoucí věkovou kohortu, představuje demence významný nejen medicínský, ale i socioekonomický problém a mluví se o ní jako o celosvětové epidemii 21. století. Není proto překvapením, že v posledních letech jsme svědky intenzivního neurobiologického a molekulárně genetického výzkumu. Koncept vaskulární demence se tak pořád vyvíjí, projevují se snahy o globální konsenzus diagnostických kritérií, přibývá vědomostí o patofyziologických podkladech a rizikových faktorech, probíhají klinické studie s cílem vývoje nových léků a zdokonalují se zobrazovací techniky. Právě pokroky v oblasti zobrazovacích metod a laboratorní diagnostiky umožňují její rozpoznání v daleko větší míře a mnohdy i časněji, než tomu bylo v uplynulých desetiletích. Velká pozornost je v současnosti věnována biomarkerům, zvláště mikroRNA (ribonukleová kyselina), která sehrává důležitou úlohu v patogenezi iktu a miR-409-3p, miR-502-3p, miR486-5p, miR-451 již byly identifikovány jako biomarkery pro vaskulární demenci při postižení drobných cév. Aktivace nebo suprese exprese mikroRNA tak může v budoucnu představovat důležitý cíl pro léčbu a prevenci vaskulárních demencí. Kromě toho se zkoumají potenciální biomarkery zánětlivé odpovědi, biomarkery poškození mozkové tkáně či biomarkery koagulace a mnoho dalších. Vedle sporadických případů vaskulární demence byla identifikována i řada monogenně podmíněných poruch a předmětem výzkumu jsou dnes genové interakce, kombinace polymorfismů a endofenotypy... [5,6]
Medicína se sice neustále posouvá mílovými kroky k neuvěřitelným výsledkům a možnostem, nicméně zůstává mnoho sporných situací a otázek na které zatím neznáme odpovědi. Aktuálně je trendem, nejen v neurologii, ale ve všech oborech snaha o stále častěji zdůrazňovaný maximálně individualizovaný přístup k léčbě, optimalizaci terapeutických a diagnostických postupů u konkrétního pacienta s využitím moderních informačních metod. Perspektivy personalizované medicíny jsou v dalším rozvoji farmakogenetických prediktivních ukazatelů a propojování klinické praxe s genomovými, epigenomickými, transkriptomickými či proteomickými údaji a jejich provázání s dalšími biomarkery onemocnění. V medicíně není nic úplně černobíle, a i díky tomu můžeme diskutovat na poli kontroverzí. Musíme pracovat s tím co máme a pravdou je, že koncept vaskulární demence je to jediné, co teď máme k dispozici. Otázkou zůstává, zda vůbec lze vytvořit všeobecně aplikovatelná diagnostická kritéria onemocnění s širokým etiopatogenetickým podkladem a pestrým klinickým obrazem. Někteří proto preferují vytvoření diagnostických kritérií pro jednotlivé subtypy vaskulární demence. Osobně si myslím, že tento koncept udržitelný je, jistě ale potřebuje revizi a aktualizaci. Jestli to tak opravdu bude a udrží se trvale, nám ukáže až čas.
doc. MUDr. Martin Vališ, Ph.D., FEAN
Neurologická klinika
LF UK a FN Hradec Králové
Zdroje
1. Wolters FJ, Ikram MA. Epidemiology of vascular dementia. Arterioscler Thromb Vasc Biol 2019; 39(8): 1542–1549. doi: 10.1161/ATVBAHA.119.311908.
2. O'Brien JT, Thomas A. Vascular dementia. Lancet 2015; 386(10004): 1698–1706. doi: 10.1016/S0140-6736(15)00463-8.
3. Custodio N, Montesinos R, Lira D et al. Mixed dementia: a review of the evidence. Dement Neuropsychol 2017; 11(4): 364–370. doi: 10.1590/1980-57642016dn11-040005.
4. Jaul E, Meiron O. Systemic and disease-specific risk factors in vascular dementia: diagnosis and prevention. Front Aging Neurosci 2017; 9 : 333. doi: 10.3389/fnagi.2017.00333.
5. Manso-Calderon R. Genetics in vascular dementia. Future Nurol 2019; 14(1), FNL5. doi: 10.2217/fnl-2018-0027.
6. Cipollini V, Troili F, Giubilei F. Emerging biomarkers in vascular cognitive impairment and dementia: from pathophysiological pathways to clinical application. Int J Mol Sci 2019; 20(11): 2812. doi: 10.3390/ijms20112812.
Štítky
Detská neurológia Neurochirurgia Neurológia
Článek Poměr fosforylovaného tau proteinu k beta amyloidu v likvoru predikuje pozitivitu amyloidové PETČlánek Chirurgická léčba benigních neurogenních tumorů mediastina – analýza 7letého souboru pacientůČlánek Dopis redakciČlánek Komentář redakceČlánek Prof. Mraček oslavil 90 letČlánek Odešla MUDr. Olga Baudyšová
Článok vyšiel v časopiseČeská a slovenská neurologie a neurochirurgie
Najčítanejšie tento týždeň
2020 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Neuromultivit v terapii neuropatií, neuritid a neuralgií u dospělých pacientů
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Cévní morfologie, symptomy, diagnostika a léčba ischemických příhod mozkového kmene
- Je koncept vaskulární demence trvale udržitelný?
- Je koncept vaskulární demence trvale udržitelný? NE
- Je koncept vaskulární demence trvale udržitelný? Komenář
- Mezinárodní klasifikace bolestí hlavy (ICHD-3) – oficiální český překlad
- Schwannóm extrakraniálnej časti trojklanného nervu
- Chirurgická léčba mozkových metastáz
- Cavum septi pellucidi, cavum vergae a cavum veli interpositi
- Poměr fosforylovaného tau proteinu k beta amyloidu v likvoru predikuje pozitivitu amyloidové PET
- Provocative factors and treatment response in juvenile myoclonic epilepsy – experience from a tertiary epilepsy center
- Chirurgická léčba benigních neurogenních tumorů mediastina – analýza 7letého souboru pacientů
- Transkraniální sonografie mediotemporálního laloku u pacientů s Alzheimerovou demencí
- Endarterektomie zevní karotické tepny
- Vestibulární funkce u pacientů s kochleárním implantátem
- Cystická hydatidóza mozečku – vzácná kazuistika
- A case of late brachial plexopathy after chemotherapy and radiotherapy
- Spontaneous vaginal extrusion of the distal catheter of a ventriculoperitoneal shunt
- Opakovaná trombektómia u pacienta so zriedkavou kombináciou etiologických faktorov
- Dopis redakci
- Komentář redakce
- Prof. Mraček oslavil 90 let
- Odešla MUDr. Olga Baudyšová
- K jubileu profesorky Soni Nevšímalové
- Česká a slovenská neurologie a neurochirurgie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Cavum septi pellucidi, cavum vergae a cavum veli interpositi
- Cévní morfologie, symptomy, diagnostika a léčba ischemických příhod mozkového kmene
- Mezinárodní klasifikace bolestí hlavy (ICHD-3) – oficiální český překlad
- Chirurgická léčba mozkových metastáz
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



