-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Klinické studie ukončené, přednesené nebo publikované v poslední době
Autoři: J. Špinar; J. Vítovec; L. Špinarová
Vyšlo v časopise: Kardiol Rev Int Med 2005, 7(1): 25-27
Kategorie: Klinické studie
SENIOR (Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors with Heart Failure)
Eur Heart J 2005; 26(3): 215–225.
Studie SENIOR (Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors with Heart Failure) 225 měla za cíl zhodnotit účinek nebivololu na morbiditu a mortalitu starších pacientů s chronickým srdečním selháním bez ohledu na ejekční frakci.
Studie byla randomizovaná, dvojitě zaslepená, multicentrická, mezinárodní a hodnotila podávání nebivololu ve srovnání s podáváním placeba u starších pacientů se srdečním selháním na optimální standardní terapii. Vstupním kritériem byl věk nad 70 let a srdeční selhání definované jako hospitalizace pro městnavé srdeční selhání v posledních 12 měsících, nebo ejekční frakce levé komory nižší než 35 % při hodnocení v posledních 6 měsících. Vylučovacími kritériem bylo: změna medikace srdečního selhání v posledních 6 týdnech, změna kardiovaskulární medikace 2 týdny před randomizací, nekorigovaná chlopenní vada, kontraindikace podávání betablokátorů (TF pod 60/min, systolický tlak pod 90 mmHg), významné jaterní nebo ledvinové postižení, cévní mozková příhoda v posledních 3 měsících, plánovaná koronární intervence nebo jiné závažné onemocnění, které by snížilo přežívání během studie.
Podávání nebivololu bylo zahájeno dávkou 1,25 mg denně za postupné titrace přes 2,5mg a 5mg dávku na cílovou dávku 10 mg. Dávka byla zvyšována po 1–2 týdnech. Po fázi titrace následovala udržovací fáze, během níž byly návštěvy ve 4. a 6. měsíci po randomizaci a dále po 3 měsících. Minimální doba sledování byla 12 měsíců.
Primárním cílem byl kombinovaný parametr celkové mortality nebo kardiovaskulární hospitalizace. Sekundárním cílem byla celková mortalita, kombinace celkové mortality a hospitalizace z jakékoliv příčiny, celková hospitalizace, kardiovaskulární hospitalizace, kombinovaný parametr kardiovaskulární mortalita nebo hospitalizace z kardiovaskulární příčiny, funkční kapacita NYHA a 6minutový walk–test.
Výsledky: Celkem bylo zařazeno 2 135 pacientů z 11 zemí. Česká republika zařadila 312 pacientů. 7 pacientů bylo ze studie vyřazeno. Celkem bylo hodnoceno 2 128 pacientů, 1 067 ve skupině s nebivololem a 1 061 v placebové skupině. Pacienti se nelišili v žádném základním parametru.
Průměrná doba trvání byla 21 měsíců, ve skupině nebivololu 1 863 pacientských let a 1 839 pacientských let v placebové skupině.
Průměrná udržovací dávka byla 7,7 mg v nebivololové skupině a 8,5 mg v placebové skupině. Dávku rovnou nebo vyšší než 5 mg dosáhlo 80 % pacientů ve skupině užívající nebivolol a 87 % pacientů ve skupině užívající placebo. Dávka 10 mg byla dosažena v nebivololové skupině u 68 % a v placebové u 80 % pacientů. Předčasné ukončení studie z jakéhokoliv jiného důvodu než úmrtí činilo u nebivololu 27 % a u placeba 25 %.
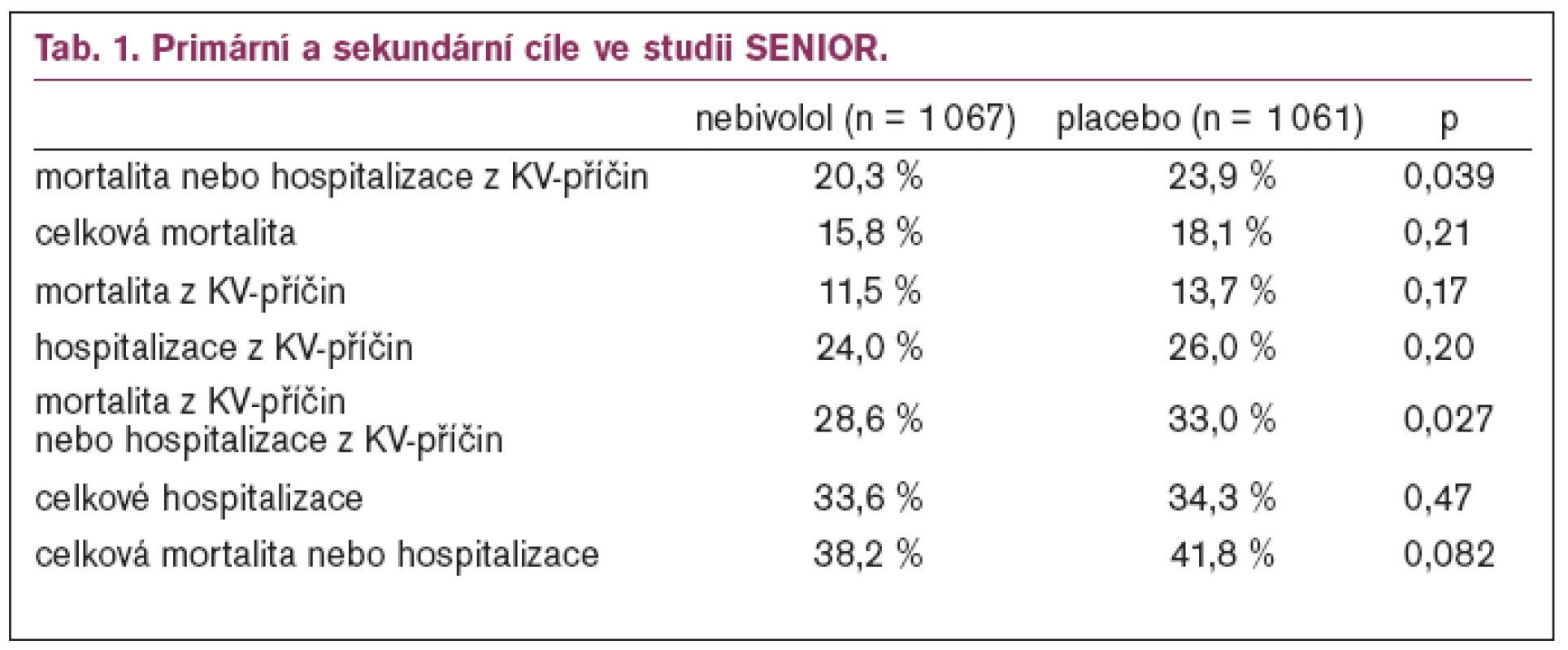
Primární cíl – kombinace úmrtí nebo hospitalizace z kardiovaskulárních příčin – byl ve skupině s nebivololem 31,1 % vs 35,3 % u placeba (p < 0,039). Snížení absolutního rizika je 4,2%, což představuje potřebu léčit (NNT) 24 pacientů po dobu 21 měsíců k zabránění události (tab. 1).
Výsledky primárního cíle byly podobné v jednotlivých podskupinách: pohlaví, věk, ejekční frakce, diabetes mellitus nebo předchozí srdeční infarkt. Nebyla zde žádná statistická závislost, že by některý z těchto faktorů ovlivnil příznivý efekt nebivololu.
Celková mortalita se ve skupině nebivololu a placeba nelišila: 15,8 % vs 18,1 %, p< 0,21 (tab. 1).
Náhlá smrt se vyskytla ve skupině nebivololu v 36 % a v placebové skupině ve 48 %.
Při hodnocení vedlejších účinků nebyly nalezeny rozdíly , vyjma těch účinků, které jsou spojeny s podáváním betablokátorů: vyšší výskyt bradykardie a snížení výskytu anginy pectoris nebo nestabilní anginy. Bradykardie jako důvod ukončení studie byla přítomna u 18 pacientů ve skupině s nebivololem a u 4 na placebu.
Studie SENIOR zavzala starší pacienty, kteří jsou v lékových studiích opomíjeni. Příznivý vliv léčby se začal u pacientů léčených nebivololem projevovat již po 6 měsících a dále se prohluboval. Pacienti ve studii SENIOR lépe odrážejí populaci pacientů s chronickým srdečním selháním, která je tvořena právě staršími pacienty, protože je známo, že incidence srdečního selhání s věkem narůstá.
Dalším novým krokem bylo zahrnutí pacientů se zachovalou funkcí levé komory a srdečním selháním. O této skupině pacientů je velmi málo údajů a právě jejich počet s přibývajícím věkem narůstá. Ve studii SENIOR byl prokázán příznivý efekt nebivololu jak na pacienty s nízkou, tak zachovalou ejekční frakcí levé komory. Nebivolol by mohl být prospěšný pro pacienty se srdečním selháním bez ohledu na ejekční frakci.
Význam studie SENIOR rozšiřuje podání betablokátorů i na populaci pacientů starší než 70 let a je první velkou randomizovanou prospektivní studií, která přináší pozitivní výsledky s podáváním betablokátoru u pacientů se zachovalou systolickou funkcí.
PEACE (Prevention of Events with Angiotensin Converting Enzyme InhibitionTrial)
N Engl J Med 2004; 351 : 2058–2068.
PEACE (Prevention of Events with Angiotensin Converting Enzyme Inhibition Trial) je multicentrická, randomizovaná dvojitě zaslepená klinická studie, srovnávající léčbu ACEI – trandolaprilem ve srovnání s podáváním placeba u nemocných s prokázanou ICHS, bez známek srdečního selhání s ejekční frakcí nad 0,4 (PEACE). Nemocní nesměli mít nekontrolovanou hypertenzi, labilní diabetes mellitus či kreatinin > 177 μmol/l).
Studie testovala, zda se potvrdí hypotéza (primárnícíl studie), předpokládající účinnost ACEI (ve srovnání s placebem) u nízko rizikových pacientů s prokázanou ICHS na snížení úmrtí z kardiovaskulárních příčin či snížení vzniku nefatálního infarktu myokardu.
Sekundárním cílem studie byl složený cíl: kardiovaskulární úmrtí, nefatální IM a koronární revaskularizace. Do studie bylo zahrnuto 8 290 nemocných (plánováno bylo 14 100, ale v říjnu 1997 po zařazení 1 548 nemocných steering committee rozhodla o snížení na 8 100). Také v tu dobu byl původní primární cíl změněn na sekundární.
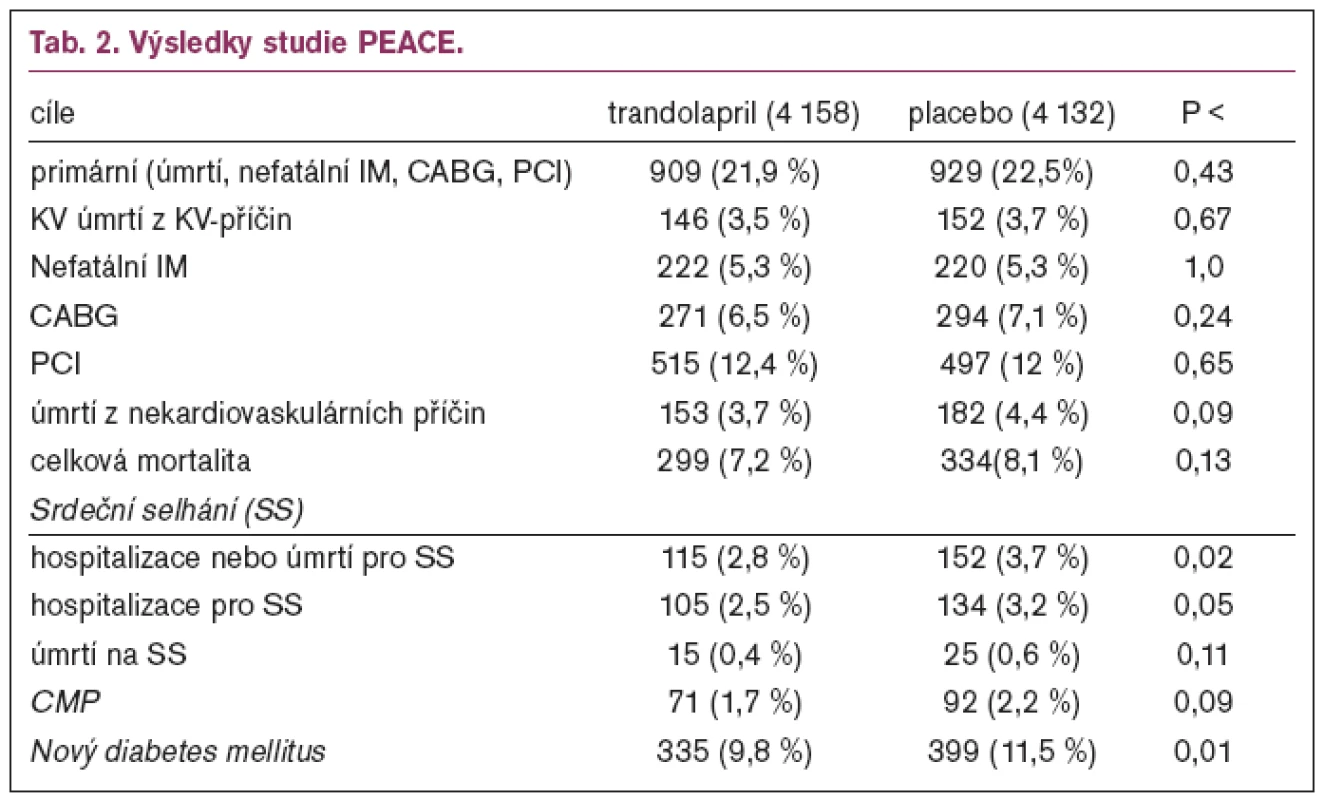
Zařazovací kritéria byla věk 50 a více let, ICHS dokumentovaná infarktem myokardu, aortokoronárním bypassem (CABG) nebo koronární angioplastikou (PTCA) před více než 3 měsíci, či stenózou nejméně 1 koronární tepny nad 50 %. Ejekční frakce nad 40 %, normální kinetikou levé komory při ventrikulografii či echokardiografickém vyšetření. Nemocný musel tolerovat léčbu ACE–inhibitorem v run–in–fázi s více než 80% adherencí k léčbě. Dávka trandolaprilu byla titrována dle tolerance do 4 mg .Výsledky studie PEACE ukazuje tab. 2.
Z tabulky je patrné, že nebyl pozorován efekt na snížení primárního cíle, na celkovou mortalitu nebo na nový infarkt myokardu. Byl pozorován významný trend na snížení cévních mozkových příhod, statisticky významné snížení hospitalizací či úmrtí na srdeční selhání a statisticky významné snížení výskytu nového diabetes mellitus.
Výsledky studie PEACE byly pro mnohé zklamáním, poněvadž se očekával podobný efekt na kardiovaskulární příhody jako ve studiích HOPE nebo EUROPA.
Nezanedbatelným výsledkem studie PEACE je snížení nového výskytu diabetes mellitus z 11,5 % na placebu na 9,8 % na aktivní léčbě (p = 0,01), což je snížení o 17 %. Toto potvrzuje výsledky studie HOPE, v níž ramipril proti placebu snížil výskyt nového diabetes mellitus o 34 %, nebo výsledky studie ALLHAT, v níž lisinopril snížil výskyt nového diabetes mellitus o 43 % proti chlortalidonu a o 20 % proti amlodipinu.
CAMELOT – Effect of antihypertensive agents on cardiovascular events inpatients with coronary disease and normal blood pressure
JAMA 2004; 292 : 2217–26.
Studie CAMELOT je dvojitě zaslepená, multicentrická studie, která srovnává účinek amlodipinu (10 mg) nebo enalaprilu (20 mg) oproti placebu u nemocných s ischemickou chorobou srdeční a průměrnou hodnotou krevního tlaku v oblasti normálního až optimálního krevního tlaku. Celkem bylo zařazeno 1 991 nemocných s angiograficky dokumentovanou ischemickou chorobou srdeční a vstupním diastolickým krevním tlakem < 100 mmHg. Celkem 274 nemocným byl proveden intravaskulární ultrazvuk (IVUSG) pro kontrolu účinku léčby.
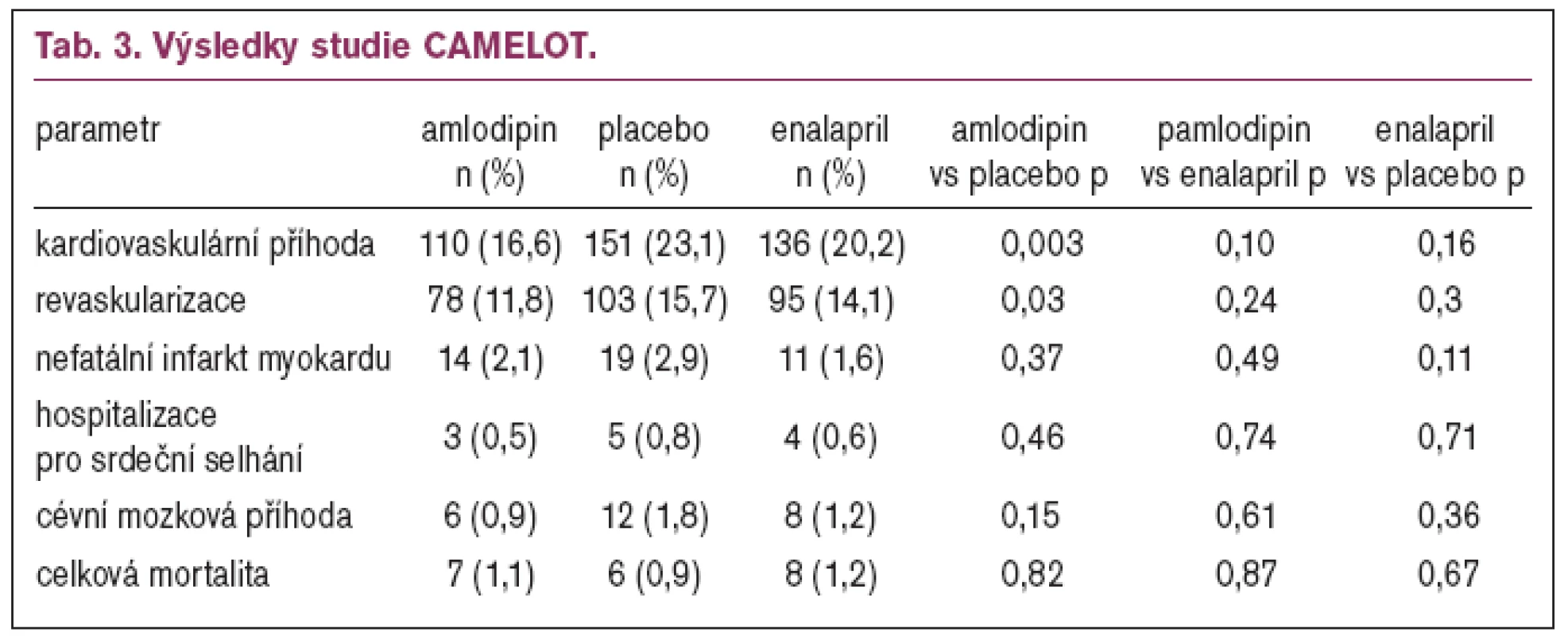
Krevní tlak stoupl u placeba o 0,7/0,6 mmHg; po amlodipinu poklesl o 4,8/2,5 mmHg, po enalaprilu o 4,9/2,4 mmHg (p < 0,001 pro aktivní léčbu vs. placebo). Doba sledování byla 2 roky. Hlavní výsledky ukazuje tabulka 3.
U nemocných, kteří podstoupili vyšetření IVUSG se průměrný ateromový objem (PAV = percent atheroma volume) zhoršil o 0,5 % po amlodipinu, 0,8 % po enalaprilu a 1,3 % po placebu, což nedosáhlo statistické významnosti. U pacientů s TKs nad průměrem byla progrese PAV po amlodipinu 0,2 % a po placebu 2,3 % (p = 0,02). Všechny ostatní podskupiny nedosáhly statistické významnosti.
Studie CAMELOT ukázala na poměrně významný pokles kardiovaskulárních příhod u nemocných se stabilní ischemickou chorobou srdeční a normálním krevním tlakem. Počet nemocných, které bylo třeba léčit amlodipinem vs placebo, aby se zabránilo 1 kardiovaskulární příhodě byl 16. Ukazuje se, že současná doporučení pro kontrolu hypertenze u nemocných s ischemickou chorobou srdeční nejsou dostatečná a že bychom krevní tlak měli snižovat mnohem více než na hodnoty 149/90 mmHg.
Mechanizmus pozitivního účinku amlodipinu na kardiovaskulární příčiny u stabilní ischemické choroby srdeční není zcela znám. Vzhledem k tomu, že největší účinek spočíval v nutnosti revaskularizace, je pravděpodobné, že se projevil antiischemický účinek amlodipinu, který je všeobecně doporučovaným antianginózním lékem. Oproti tomu enalapril, přestože snížil krevní tlak stejně jako amlodipin, nemá pravděpodobně antianginózní účinek. Ve studii CAMELOT byla (z dosud publikovaných velkých klinických studií zaměřených na ischemickou chorobu srdeční) antihypertenziva amlodipin a enalapril podávána nemocným s nejnižším krevním tlakem. Systolický krevní tlak byl o 10 mmHg nižší než ve studiích HOPE či EUROPA.
Studie CAMELOT je třetí v souvislé řadě klinických studií (po studiích ALLHAT a VALUE), jež neprokazují v přímém srovnání větší účinek látek blokujících systém renin–angiotenzin (ACEI či AIIA) ve srovnání s amlodipinem.
prof. MUDr Jindřich Špinar, CSc., FESC1
prof. MUDr. Jiří Vítovec, CSc.2
MUDr. Lenka Špinarová, Ph.D.2
1Interní kardiologická klinika, FN Brno–Bohunice
2I. interní kardioangiologická klinika, FN U sv. Anny, Brno
Štítky
Detská kardiológia Interné lekárstvo Kardiochirurgia Kardiológia
Článek Aortální stenóza
Článok vyšiel v časopiseKardiologická revue – Interní medicína
Najčítanejšie tento týždeň
2005 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Intermitentní hladovění v prevenci a léčbě chorob
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Praktické aspekty a novinky ve farmakologické léčbě arytmií
- Trimetazidin v léčbě anginy pectoris a ostatních forem ICHS
- Renesance antialdosteronik v soudobé kardiologii
- Klinické studie ukončené, přednesené nebo publikované v poslední době
- Michael Aschermann et al. Kardiologie. Praha: Galén 2004. 1540 s. ISBN 8072622900
- Doporučení diagnostických a léčebných postupů u arteriální hypertenze – verze 2004
- Srdce v obraze lidových rčení
- Srdeční infarkt a změny počasí – další možné souvislosti
- Aortální stenóza
- Rehabilitace po infarktu myokardu
- Professor Medicinae Internae, Jiří Widimský
- Tomáš Baťa, podpůrce moderních trendů ve zdravotní péči, se zařadil mezi dlouhověké
- Kardiologická revue – Interní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Aortální stenóza
- Doporučení diagnostických a léčebných postupů u arteriální hypertenze – verze 2004
- Trimetazidin v léčbě anginy pectoris a ostatních forem ICHS
- Praktické aspekty a novinky ve farmakologické léčbě arytmií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy