-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Možnosti překonání rezistence k hormonální léčbě u pacientek s hormonálně dependentním metastatickým karcinomem prsu
Autoři: P. Tesařová
Působiště autorů: Onkologická klinika VFN v Praze a 1. LF UK, Praha
Vyšlo v časopise: Klin Onkol 2012; 25(6): 486-488
Kategorie: Aktuality v onkologii
Nejčastějším důvodem ztráty účinku hormonální terapie u hormonálně dependentního karcinomu prsu je rezistence k hormonální léčbě, primární nebo získaná. Ta znemožňuje použití dosavadní hormonální léčby. Překonání této rezistence je možné změnou hormonální léčby s jiným mechanizmem účinku, nebo kombinací hormonální terapie s mTOR (mammalian target of rapamycin) inhibitorem, který může obnovit citlivost nádoru k hormonální terapii, jak to prokázaly výsledky studie fáze III Bolero-2 (obr. 1) [1].
Obr. 1. Studie Bolero-2, lokální a centrální hodnocení PFS. 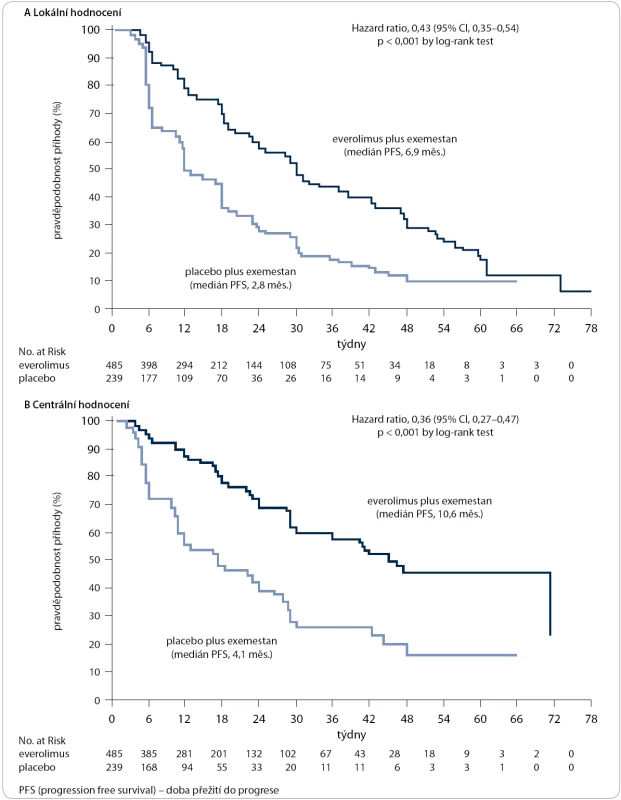
Stav hormonálních receptorů je prognostickým ukazatelem, ale i prediktivním faktorem odpovědi na hormonální léčbu. Všichni nemocní s hormonálně dependentním karcinomem prsu mohou z hormonální léčby profitovat.
Inhibitory aromatázy (AI) snižují hladiny cirkulujících estrogenů blokádou činnosti enzymu aromatázy, která konvertuje androgeny na estrogeny. Ve srovnání s tamoxifenem jsou v první linii metastatického karcinomu prsu účinnější. V metaanalýze randomizovaných studií porovnávajících AI s tamoxifenem v první linii metastatického karcinomu prsu bylo prokázáno statisticky lepší celkové přežití (RR 0,89, 95% CI 0,80–0,99), především v rámci léčby třetí generací inhibitorů. Také ale v druhé a dalších liniích ve srovnání s progestiny prokázaly AI třetí generace lepší celkové přežití (RR 0,86, 95% CI 0,79–0,94) [2]. Jiné metaanalýzy ale přínos pro celkové přežití nepotvrdily.
Není zcela jasno ani v případě zkřížené rezistence mezi nesteroidními a steroidními AI. Praxe vypadá tak, že se většinou v první linii indikují nesteroidní inhibitory aromatázy (anastrozol a letrozol) a teprve po jejich selhání inhibitor steroidní – exemestan. Exemestan se odlišuje od neesteroidních inhibitorů ireverzibilní blokádou aromatázy.
Téměř 50 % nemocných s hormonálními receptory je primárně rezistentních k hormonální léčbě, v průběhu terapie pokročilého karcinomu prsu se téměř všechny nemocné dopracují k rezistenci získané. Mechanizmem této rezistence je pravděpodobně aberantní metabolická signalizace přes fosfatidylinozitol 3-kinázu (PI3K)–Akt cestou mTOR aktivace. Přibývá informací o úzké interakci mezi ER signální cestou a mTOR aktivací. Substrát mTOR komplexu 1 (mTORC1), nazývaný S6 kináza1 fosforyluje a tím aktivuje funkční doménu 1 ER, která je zodpovědná za aktivaci receptoru nezávislou na ligandě.
Everolimus je inhibitor mTOR (mammalian target of rapamycin), který je v současné době používán v léčbě pokročilého karcinomu ledviny a neresekovatelných nebo metastatických neuroendokrinních nádorů pankreatu. Everolimus je esterový analog rapamycinu a je podobně jako rapamycin, inhibitorem proteinkinázy mTOR, multifunkční kinázy zprostředkující signální transdukci, jež se podílí na přenosu proliferačních stimulů a urychlení buněčného přechodu z fáze G1 do fáze S. V buňce se váže na imunoglobulin Fk vážící protein 12 (FKBP-12), a tak vzniká imunosupresivní komplex, který inhibuje aktivaci mTOR a klíčovou regulační kinázu. Dochází k inhibici T lymfocytů a proliferace způsobené stimulací cytokiny (IL-2, IL-4, and IL-15), dochází také ke snížení produkce protilátek. V preklinických modelech prokázal everolimus v kombinaci s inhibitorem aromatázy synergickou inhibici proliferace a indukci apoptózy.
Studie BOLERO-2
V randomizované studii fáze 2 byl porovnáván neoadjuvantně podaný everolimus s letrozolem proti letrozolu samotnému u pacientů s nově diagnostikovaným ER pozitivním karcinomem prsu, odpověď na kombinaci byla vyšší než na letrozol samotný. Studie fáze III The Breast Cancer Trials of Oral Everolimus-2 (BOLERO-2) měla posoudit účinnost a bezpečnost kombinace everolimu a exemestanu u pacientů s ER pozitivním karcinomem prsu, který nebyl již citlivý k léčbě nesteroidními inhibitory aromatázy. Everolimus a exemestan versus placebo a exemestan v poměru 2 : 1 byly podávány 724 pacientkám s hormonálně dependentním pokročilým karcinomem prsu, které progredovaly nebo recidivovaly při léčbě nesteroidními inhibitory aromatázy v adjuvanci či pro pokročilý karcinom prsu. Populace byla stratifikovaná podle přítomnosti nebo nepřítomnosti viscerálních metastáz a podle senzitivity na předchozí hormonální léčbu.
Primárním cílem studie byla doba do progrese (progression free survival – PFS). Sekundárním cílem bylo celkové přežití (overall survival – OS), procento odpovědí a bezpečnost.
Studie byla dobře vyvážená. Medián věku byl 62 let, u 56 % pacientek byly diagnostikovány viscerální metastázy a 84 % mělo hormonálně dependentní karcinom. Předchozí léčba obsahovala letrozol nebo anastrozol (100 %), tamoxifen (48 %), fulvestrant (16 %) a chemoterapii (68 % – v léčbě časného i metastatického karcinomu prsu, 25 % pouze v léčbě metastatického karcinomu prsu). Nejčastější toxicitou stupně 3 a 4 byla stomatitida (8 % v kombinovaném rameni vs 1 % v rameni s exemestanem a placebem), anémie (6 % vs 1 %), dušnost (4 % vs 1 %), hyperglykemie (4 % vs 1 %), únava (4 % vs 1 %) a pneumonitida (3 % vs 0 %). V rámci finální analýzy byl medián PFS hodnocen lokálními investigátory jako 7,8 měsíce ve skupině léčené everolimem a exemestanem a 3,2 měsíce ve skupině léčené exemestanem a placebem, HR = 0,45 (95% CI: 0,38–0,54) p < 0,0001. Kombinovaná léčba tedy snižovala riziko progrese o 55 %. Podle centrálního hodnocení byl v uvedených dvou skupinách pacientek medián PFS 11 měsíců a 4,1 měsíců (HR = 0,38 (95% CI: 0,31–0,48), p < 0,0001 (viz obr. 1) [1].
Studie Bolero-2 tedy potvrdila, že everolimus v kombinaci se steroidním inhibitorem aromatázy zlepšuje dobu do progrese u pacientek s lokálně pokročilým nebo metastatickým karcinomem prsu, u kterých došlo k relapsu nebo progresi onemocnění po předchozí léčbě nesteroidními inhibitory aromatázy letrozolem a anastrozolem. Tyto závěry dokazují, že everolimus bude pravděpodobně nová a zajímavá terapeutická možnost pro pacienty s metastatickým karcinomem prsu.
Kazuistika
Pacientka E.D. narozená v roce 1937 se na naší klinice léčila od roku 1993 pro lobulární ER pozitivní karcinom prsu T1cN1M0. Absolvovala ablaci prsu s exenterací axily, 6krát adjuvantní chemoterapii CMF (cyklofosfamid, fluorouracil a metotrexát) a 5letou léčbu tamoxifenem. V roce 2004 absolvovala scintigrafii skeletu na základě bolestí v bederní krajině, která prokázala mnohočetné metastázy ve skeletu. V dubnu 2004 zahájila léčbu letrozolem a perorálním bisfosfonátem. V únoru 2006 se ale bolesti znovu vrátily, došlo k elevaci markerů a progresi kostního nálezu. Nemocná až do června 2006 úspěšně reagovala na léčbu faslodexem, pak se ale na ultrazvuku objevilo metastatické postižení jater, pro které zahájila od července 2006 léčbu capecitabinem spolu s intravenózním zolendronátem, ale už v květnu 2008 musela být terapie z důvodů progrese v játrech změněna na perorální navelbin a v dubnu 2010 paclitaxel týdně. Nemocná byla léčena ambulantně, byla celkově ve velmi dobrém stavu, bez větších bolestí, s dobrou výkonností, přesto se ale už v listopadu 2010 objevila nová ložiska v játrech a nemocnou jsme zařadili do studie s eribulin mesylátem. V průběhu terapie došlo k parciální remisi v játrech, ale v září 2011 musela studii pro progresi opustit. U těžce předléčené nemocné, která ale byla v dobrém celkovém stavu, jsme měli možnost vyzkoušet kombinovanou terapii exemestan s everolimem. Léčbu pacientka velmi dobře tolerovala, došlo k promptnímu snížení markerů, úplnému ústupu ascitu a stabilizaci nálezu v játrech. Léčba byla v březnu 2012 komplikovaná aftosní stomatitidou stupně 3 s erozivní gastropatií, slizničním krvácením do zažívacího traktu a anémií, vyžadující krevní převody. Stav se ale zcela upravil, opět jsme se vrátili k zavedené kombinační léčbě s redukcí dávky everolimu na 5 mg denně. Léčba probíhá dosud ambulantně, došlo k dlouhodobé stabilizaci stavu, nemocná má minimální obtíže v podobě bolestí ve skeletu po námaze. Pacientka má velmi pomalu progredující, hormonálně dependentní metastatický karcinom prsu, s kterým žije v dobré kvalitě života 8 let. Everolimus spolu s exemestanem užívá 12 měsíců s uspokojivým efektem ve skeletu i v játrech a k terapii dochází nadále jen ambulantně.
Rezistence k cílené léčbě bude pravděpodobně ještě dlouho problém, který bude trápit onkology i jejich pacienty. Nicméně teprve pochopení pravděpodobných mechanizmů jejího vzniku, nám snad do budoucna pomůže zvolit takovou terapii, která prodlouží účinek cílené léčby generalizovaných pacientek s karcinomem prsu co nejdéle. Kombinovaná léčba exemestan s everolimem splňuje zcela naše požadavky na ideální paliativní léčbu, je totiž dostatečně účinná i u předléčených nemocných a přitom jim nijak zásadně nezhoršuje kvalitu života.
doc. MUDr. Petra Tesařová, CSc.
Onkologická klinika VFN v Praze
a 1. LF UK
U Nemocnice 2
128 08 Praha 2
e-mail: petra.tesarova@vfn.cz
Obdrženo/Submitted: 15. 11. 2012
Zdroje
1. Baselga J, Campone M, Piccart M et al. Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer. N Engl J Med 2012; 366(6): 520–529.
2. Gennari A, Conte P, Rosso R et al. Survival of metastatic breast carcinoma patients over a 20-year period: a retrospective analysis based on individual patient data from six consecutive studies. Cancer 2005; 104(8): 1742–1750.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek Klinický registr CORECT
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2012 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Když se ve střevech děje něco nepatřičného...
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
-
Všetky články tohto čísla
- Klinická onkologie slaví 25. výročí
- Molekulární podstata Waldenströmovy makroglobulinemie
- Prečo sú mitochondrie vhodné ciele pre liečbu rakoviny
- Hodnocení jaterní funkce v onkologické praxi
- EML4-ALK fúzní gen u pacientů s plicním karcinomem: biologie, diagnostika a cílená terapie
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Výsledky léčby mozkových tumorů stereotaktickou radioterapií a radiochirurgií
- Profil pacientů s nádory léčených na pohotovosti referenčního střediska nádorové péče v jižní Brazílii
- Proteiny rezistence a chemorezistence u pacientek s karcinomem ovaria
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Paraneoplastický neurologický syndrom u 64letého pacienta s malobuněčným karcinomem plic – kazuistika
- Vzpomínka na MUDr. Vladimíra Spurného, CSc.
- Prof. MUDr. Rostislav Vyzula, CSc., již a teprve šedesátiletý
- Klinický registr CORECT
- Možnosti překonání rezistence k hormonální léčbě u pacientek s hormonálně dependentním metastatickým karcinomem prsu
- Aprepitant a pruritus – komentář k článku
- Informace z České onkologické společnosti
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Hodnocení jaterní funkce v onkologické praxi
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



