-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Sledování pacientek léčených tamoxifenem pro karcinom prsu
Follow-up in patients on tamoxifen
Tamoxifen is the most frequently used drug in hormonal treatment of breast cancer. Follow-up of patients on tamoxifen is controversial and it has no universal guidelines. We analyze a group of 74 patients on tamoxifen indicated for hysteroscopy for abnormal ultrasonography (USG; 71.6%), abnormal uterine bleeding (AUB; 6.8%), abnormal USG and AUB (10.8%), or other indications (10.8%). Histological examination revealed four times (5.4%) simple non-atypical hyperplasia, six times (8.1%) endometrial polyp with simple non-atypical hyperplasia, and one time (1.4%) well differentiated endometroid endometrial carcinoma, other findings (85.1%) were atrophic, proliferative, and secretory endometrium or atrophic endometrial polyp. Ultrasound was not significant for endometrial pathology. 46% patients with AUB had clinically relevant endometrial pathology comparing to 11.5% clinically relevant pathologies in asymptomatic patients. We show a high rate of false positivity of USG and the importance of AUB as a symptom of endometrial pathology in our patient series. The examination at the beginning of the treatment and its dynamic changes during follow-up are important. USG is a basic diagnostic method of follow-up, hysteroscopy is the best diagnostic and therapeutical method for any endometrial pathology.
Key words:
breast cancer – tamoxifen – hormonal treatment – ultrasonography – hysteroscopy
Autoři: as. MUDr. Jiří Bouda, Ph.D. 1; MUDr. Jiří Štěpán 1; MUDr. Tomáš Svoboda 2; doc. MUDr. Zdeněk Rokyta, CSc. 1
Působiště autorů: Gynekologicko-porodnická klinika LF UK a FN Plzeň 1; radioterapeutické oddělení FN Plzeň 2
Vyšlo v časopise: Prakt Gyn 2006; 10(2): 60-63
Souhrn
Tamoxifen je nejčastěji užívaným lékem při hormonální léčbě karcinomu prsu. Mezi jeho vedlejší účinky patří častý výskyt patologií endometria. Sledování pacientek léčených tamoxifenem je problematické a jednotný postup neexistuje. Analyzujeme soubor 74 pacientek léčených tamoxifenem pro karcinom prsu a indikovaných k hysteroskopii pro abnormální ultrazvukový nález (71,6 %), abnormální děložní krvácení (ADK; 6,8 %), kombinaci abnormálního USG a ADK (10,8 %) a z jiných důvodů (10,8 %). Z histologického vyšetření jsme zaznamenali 4krát (5,4 %) prostou hyperplazii bez atypií, 6krát (8,1 %) korporální polyp s prostou hyperplazií bez atypií a 1krát (1,4 %) dobře diferencovaný endometrální endometroidní adenokarcinom, ostatní nálezy (85,1 %) tvořilo atrofické endometrium, proliferační či sekreční endometrium či atrofický korporální polyp. Ultrazvukové vyšetření prováděné před výkonem nebylo signifikantní pro patologii endometria. Mezi pacientkami s abnormálním děložním krvácením mělo klinicky významný histologický nález 46 % pacientek, zatímco mezi asymptomatickými pouze 11,5 %. V souboru dokumentujeme vysokou míru falešně pozitivních ultravzvukových nálezů a význam abnormálního děložního krvácení jako symptomu intrauterinní patologie. Důležité je vstupní vyšetření při zahájení léčby a sledování dynamiky změn. Ultrazvuk je základní diagnostickou metodou follow-up, hysteroskopie je pak suverénní diagnostickou i terapeutickou metodou k řešení patologií endometria.
Klíčová slova:
karcinom prsu – tamoxifen – hormonální léčba – ultrasonografie – hysterektomieÚvod
Karcinom prsu je nejčastějším zhoubným onemocněním žen v České republice. Každoročně tímto nádorem onemocní přes 5 000 pacientek (r. 2002 : 5 378 žen, incidence 102,7/100 000 žen, mortalita 37,5/100 000 žen). Jedná se o nádor hormonálně dependentní, a tak je jednou z léčebných modalit také hormonální léčba. Tato bývá indikována u tumorů s pozitivitou hormonálních receptorů jak v premenopauze, tak i postmenopauze. Dosud nejčastějším preparátem využívaným v těchto indikacích je tamoxifen. Je to selektivní modulátor estrogenových receptorů s antiestrogenními účinky v prsní žláze a vnitřní estrogenní aktivitou, projevující se například na endometriu. Účinek preparátu je však komplexní a zahrnuje také inhibici růstových faktorů, indukci antiproliferativních faktorů a přímý cytostatický efekt na nádorové buňky [1]. Další preparáty, které se užívají v obdobných indikacích, jsou inhibitory aromatázy, a to jak nesteroidní (Femara, Arimidex), tak steroidní (Aromasin). Jinou variantou trvalého či časově limitovaného hormonálního ovlivnění onemocnění je chirurgická či radiační kastrace nebo léčba GnRH-analogy či různé kombinace výše uvedených metod.
Problémem při sledování pacientek léčených tamoxifenem je obtížná interpretace ultrazvukového nálezu. Existuje pestrá škála doporučení, jak pacientky sledovat a léčit případné patologie endometria.
Pacientky a metody
Předmětem předkládaného retrospektivního souboru je 74 pacientek, u nichž byla na našem pracovišti v letech 2001-2004 provedena hysteroskopie v souvislosti s užíváním tamoxifenu při léčbě karcinomu prsu. Ve sledovaném období bylo provedeno celkem 1 614 hysteroskopií, pacientky léčené tamoxifenem tedy tvořily 4,6 % indikací k hysteroskopii. U sledovaných pacientek jsme analyzovali indikaci k výkonu, ultrazvukový a hysteroskopický nález, histologický nález, dobu užívání tamoxifenu. Cílem bylo na základě analýzy souboru navrhnout doporučení k optimálnímu follow-up.
Výsledky
U 53 pacientek (71,6 %) byl indikací k hysteroskopii abnormální USG-nález, u 8 (10,8 %) abnormální USG-nález a abnormální děložní krvácení (ADK), u 5 (6,8 %) ADK a u 8 (10,8 %) pacientek byla indikace jiná (graf 1). Věk pacientek se pohyboval mezi 33 a 83 lety, s mediánem 62 let. V souboru jsme zaznamenali 33krát atrofické endometrium (44,6 %), 27krát (36,5 %) atrofický (cystický) korporální polyp, 3krát (4,1 %) proliferační či sekreční endometrium, 4krát (5,4 %) prostou hyperplazii bez atypií, 6krát (8,1 %) korporální polyp s prostou hyperplazií bez atypií a 1krát (1,4 %) dobře diferencovaný endometrální endometroidní adenokarcinom (graf 2). Průměrná doba užívání tamoxifenu byla 3,1 roku.
Graf 1. Indikace k hysteroskopii 
USG-nález hodnotil výšku, strukturu a ohraničení endometria. Výška endometria se pohybovala od 3 do 37 mm, s mediánem 11 mm. 28 pacientek (37,8 %) mělo endometrium do 8 mm, dalších 18 pacientek mezi 9-12 mm (24,3 %) a zbylých 28 pacientek (37,8 %) nad 13 mm. Korelaci mezi USG-nálezem (při hodnocení pouze výšky endometria) a histologií uvádí tab.
Tab. 1. Korelace ultrazvukového a histologického nálezu. 
Diskuse
Pro follow-up pacientek užívajících tamoxifen byla navržena celá řada postupů [1-7]. Při rozvaze o optimálním sledování uživatelek tamoxifenu je třeba vycházet z frekvence a závažnosti jednotlivých patologických stavů a výtěžnosti příslušných diagnostických metod.
Léčba tamoxifenem je obyčejně dlouhodobá a mezi dokumentovanými vedlejšími účinky je stimulace endometria s tvorbou polypů [8], hyperplazie endometria [9] i endometrálního karcinomu. Při dlouhodobém užívání je relativní riziko onemocnění karcinomem endometria u uživatelek tamoxifenu 2,2-7,5krát vyšší než u běžné populace [10-12]. Zda má tento karcinom (tamoxifen-induced endometrial carcinoma) odlišné biologické chování a jinou prognózu je sporné [10,12,13]. Když se však sečte relativní riziko recidivy karcinomu prsu, nádoru v kontralaterálním prsu a karcinomu endometria, je benefit užívání tamoxifenu nesporný. V souboru jsme zaznamenali pouze 1 karcinom (1,4 %), 4krát prostou hyperplazii (5,4 %) a 6krát hyperplastický polyp (8,1 %), zbylých 85,1 % nálezů tvořilo atrofické endometrium, atrofický polyp či proliferační nebo sekreční endometrium. Operační řešení atrofických polypů je diskutabilní [2]. Distribuce histologických nálezů v souboru je v souladu s jinými studiemi [2,6,7,14,15].
Základním diagnostickým nástrojem je ultrazvuk. Někteří autoři doporučují USG-vyšetření 1-2krát ročně [5,6]. Obvyklým nálezem při vyšetření je zesílené, nepravidelné, „cystické“ endometrium. Změny jsou často soustředěny v subendometriální zóně, bez postižení epitelu. Samotný nález vyššího endometria není signifikantní a vede k nadměrnému množství falešně pozitivních nálezů a zbytečným invazivním zákrokům [7,14-16]. Někteří autoři [2,5,14,15,17] uvádějí 8-9 mm hranici jako spolehlivou k vyloučení hyperplazie endometria a endometrálního adenokarcinomu. Specificitu ultrazvuku zvyšuje vyšetření dvojím kontrastem, čili hysterosonografie [14,18]. Distribuce USG-nálezů v našem souboru odpovídala údajům publikovaným v literatuře [2,7], strukturální změny jsou při jednoduchém vyšetření vaginální sondou u pacientek s tamoxifenem obtížně interpretovatelné [2]. Vezmeme-li jako hraniční výši endometria 8 mm, pak abnormální či patologický histologický nález (hyperplazie endometria, hyperplastický polyp či adenokarcinom) mělo v souboru 7,1 % pacientek, ve skupině s endometriem 9-12 mm 11,1 % pacientek, ve skupině nad 13 mm 14,3 % pacientek (tab).
Někteří autoři [1] preferují sledování pacientek cytologií endometria, kterou považují za jednoduchou a ekonomicky efektivní metodu s uspokojivou senzitivitou i specificitou vyšetření. Jiní považují [2,6] za jedinou signifikantní metodu hysteroskopii.
V našem souboru mělo 13 (17,6 %) pacientek ADK, což je obdobné jako v jiných studiích [2]. V této skupině mělo 6 pacientek (46 %) histologický nález hyperplazie endometria, hyperplastického polypu či endometrálního adenokarcinomu. Ve skupině asymptomatických pacientek (61 pacientek, 82,4 %) mělo výše uvedené histologické nálezy pouze 7 pacientek (11,5 %). Když vydělíme pacientky s hyperplazií, hyperplastickým polypem či karcinomem, mělo ADK 6 z 11 pacientek (54,5 %). Mnozí autoři [7] považují ADK za nejdůležitější znak hyperplazie či karcinomu a kliniky asymptomatické ženy dále nevyšetřují.
Obr. 1. USG – cystická atrofie při léčbě tamoxifenem. 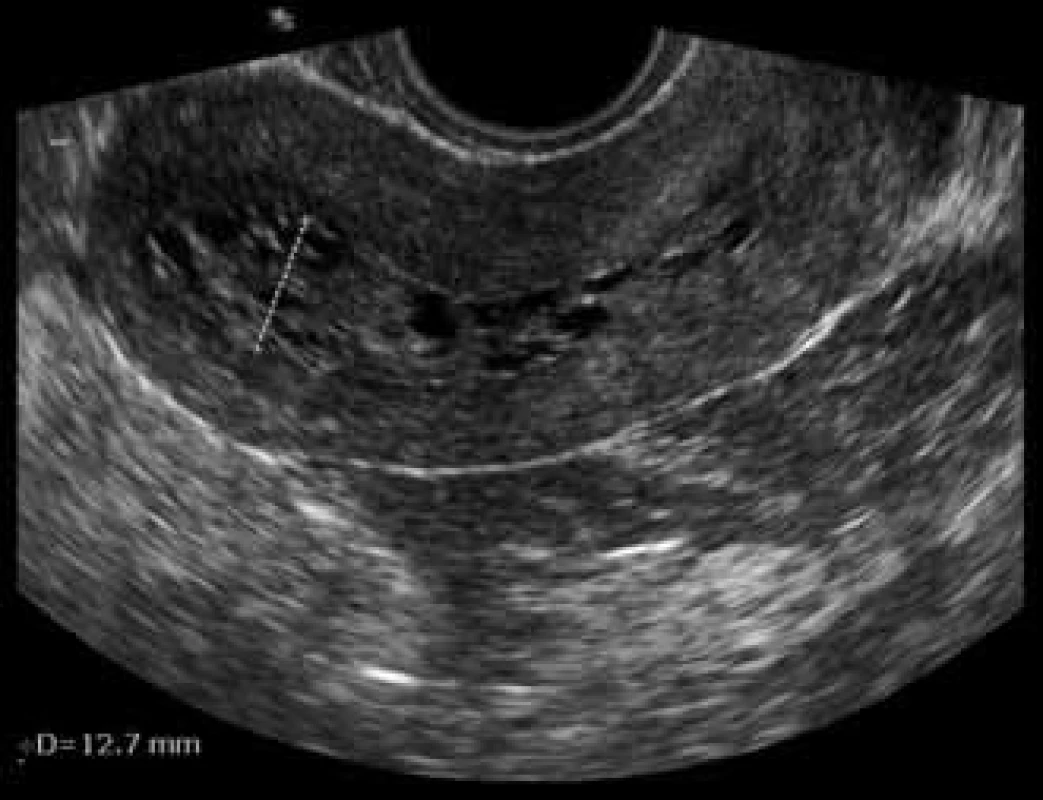
Obr. 2. Hysteroskopický nález korporálního polypu při léčbě tamoxifenem. 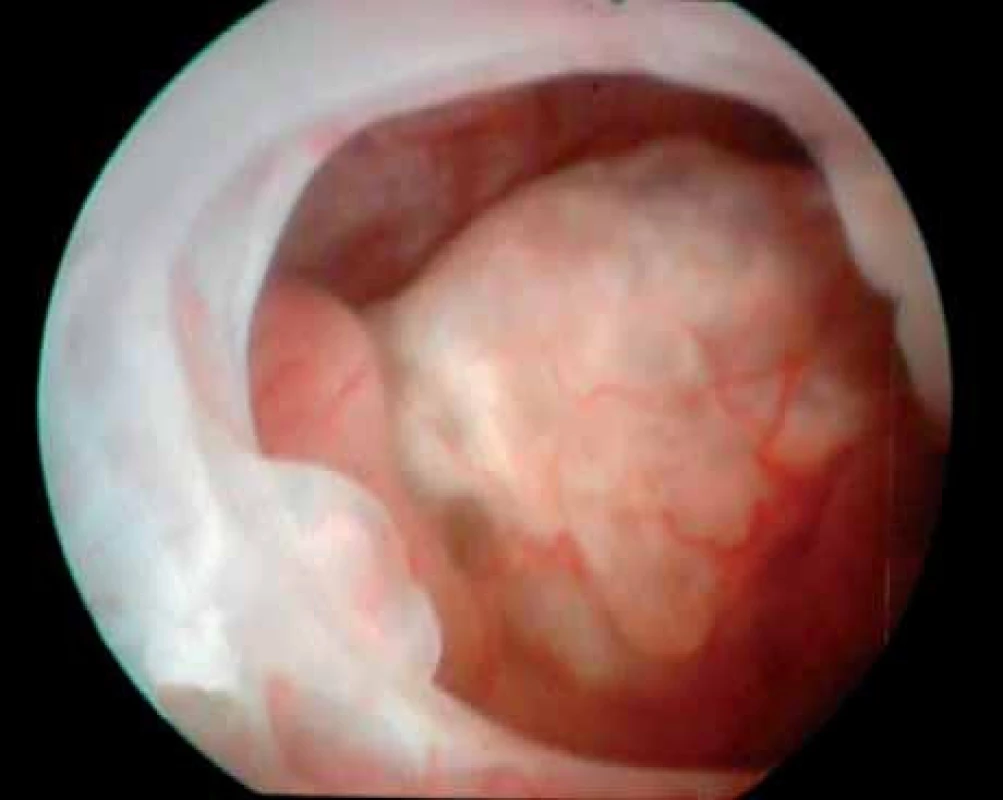
Obr. 3. Hysteroskopický nález cystické atrofie při léčbě tamoxifenem. 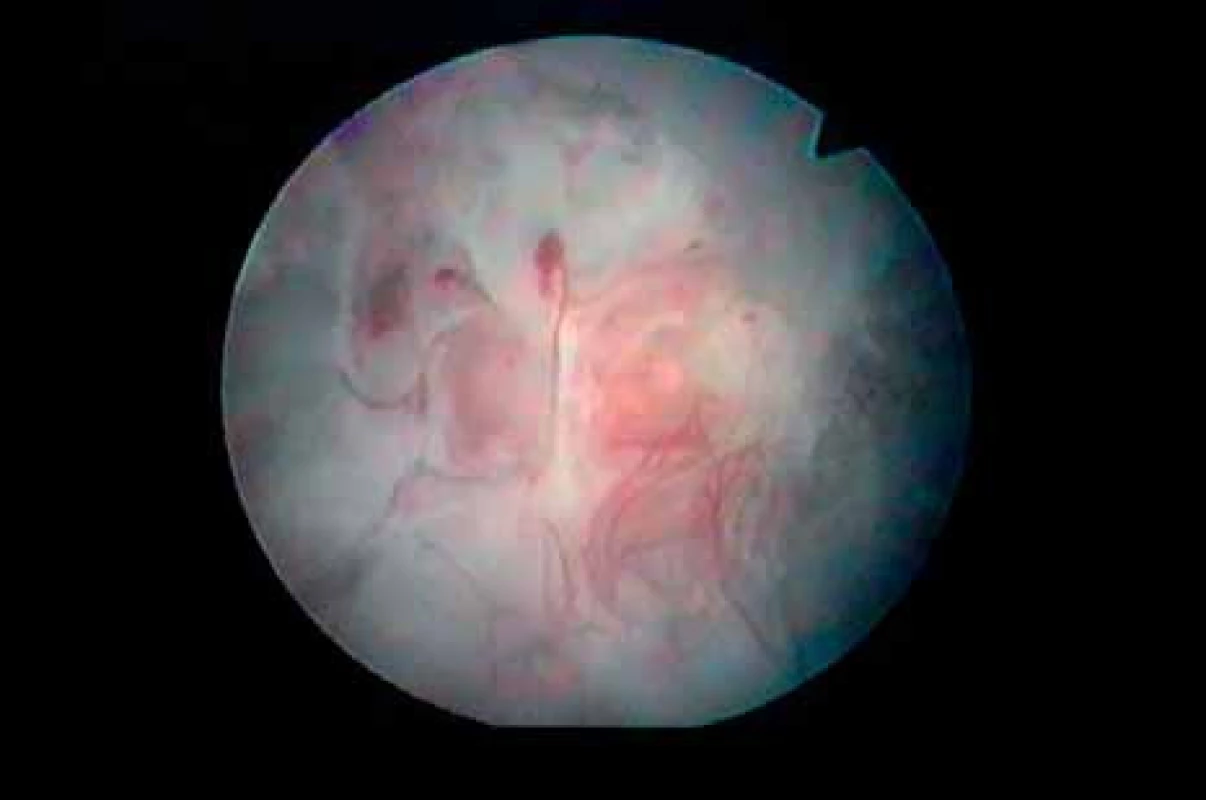
Závěr
Jednoznačné doporučení, jak postupovat při sledování uživatelek tamoxifenu, neexistuje. Sami se řídíme následujícími zásadami:
- Každá pacientka užívající tamoxifen by měla mít při zahájení léčby minimálně komplexní gynekologické vyšetření zahrnující ultrazvukové vyšetření vaginální sondou. V tomto bodě je důležitá informovanost a spolupráce indikujícího lékaře.
- Při jakémkoli abnormálním nálezu provádíme hysteroskopii a řešíme eventuální patologii endometria. Při abnormálním vstupním nálezu dáváme do úvahy změnu preparátu.
- V dalším sledování postačuje komplexní gynekologické vyšetření včetně ultrazvuku 1krát ročně, za signifikantní považujeme pouze zřetelnou změnu od úvodního nálezu či přítomnost abnormálního děložního krvácení. V těchto případech provádíme hysteroskopii.
- U referovaných pacientek bez relevantního vstupního vyšetření na počátku léčby považujeme za indikované k dalšímu vyšetření (hysteroskopii) pouze pacientky klinicky symptomatické či pacientky s výší endometria nad 10-12 mm. U pacientek s endometriem hraniční výše je možné uvažovat o doplnění hysterosonografií.
Kontroverze při sledování pacientek užívajících tamoxifen vyřeší patrně až širší zavedení jiných preparátů se stejnou léčebnou účinností a absencí výše zmíněných vedlejších účinků.
1as. MUDr. Jiří Bouda, Ph.D.
1MUDr. Jiří Štěpán
2MUDr. Tomáš Svoboda
1doc. MUDr. Zdeněk Rokyta, CSc.
1Gynekologicko-porodnická klinika LF UK a FN Plzeň
2radioterapeutické oddělení FN Plzeň
Zdroje
Labi FL, Meggiorini ML, Nusiner MP et al. Cytologic endometrial surveillance in tamoxifen-treated women. Eur J Gynaecol Oncol 2002; 23 : 537-539.
2. Giorda G, Crivellari D, Veronesi A et al. Comparison of ultrasonography, hysteroscopy, and biopsy in the diagnosis of endometrial lesions in postmenopausal tamoxifen-treated patients. Acta Obstet Gynecol Scand 2002; 81 : 975-980.
3. Yuce K, Tuncer ZS, Onculoglu C et al. Reproductive tract pathology in asymptomatic women treated with tamoxifen. Eur J Gynaecol Oncol 2001; 22 : 466-468.
4. Lhomme C, Pautier P, Zagame L et al. Endometrial surveillance of women on tamoxifen. Gynecol Obstet Fertil 2003; 31 : 647-656.
5. Burkart C, Wight E, Pok J et al. Ultrasound endometrium follow-up during tamoxifen treatment: Really not reliable or useful after all? Ultraschall Med 2001; 22 : 136-142.
6. Zarbo G, Caruso G, Zammitti M et al. The effects of tamoxifen therapy on the endometrium. Eur J Gynaecol Oncol 2000; 21 : 86-88.
7. Gerber B, Krause A, Muller H et al. Effects of adjuvant tamoxifen on the endometrium in postmenopausal women with breast cancer: a prospective long-term study using transvaginal ultrasound. J Clin Oncol 2000; 18 : 3464-3470.
8. Ismail SM. Pathology of endometrium treated with tamoxifen. J Clin Pathol 1994; 47 : 827-833.
9. Neven P, De Muylder X, Van Belle Y et al. Longitudinal hysteroscopic follow-up during tamoxifen treatment. Lancet 1998; 351 : 36.
10. Fornander T, Rutqvist LE, Cedermark B, et al. Adjuvant tamoxifen in early breast cancer: occurrence of new primary cancers. Lancet 1989; 1 : 117-120.
11. Rutqvist LE, Mattsson A. Cardiac and thromboembolic morbidity among postmenopausal women with early-stage breast cancer in a randomized trial of adjuvant tamoxifen. The Stockholm Breast Cancer Study Group. J Natl Cancer Inst 1993; 85 : 1398-1406.
12. Fisher B, Costantino JP, Redmond CK et al. Endometrial cancer in tamoxifen-treated breast cancer patients: findings from the National Surgical Adjuvant Breast and Bowel Project (NSABP) B-14. J Natl Cancer Inst 1994; 86 : 527-537.
13. Magriples U, Naftolin F, Schwartz PE et al. High-grade endometrial carcinoma in tamoxifen-treated breast cancer patients. J Clin Oncol 1993; 11 : 485-490.
14. Valenzano M, Bertelli GF, Costantini S et al. Transvaginal ultrasonography and hysterosonography to monitor endometrial effects in tamoxifen-treated patients. Eur J Gynaecol Oncol 2001; 22 : 441-444.
15. Fung MF, Reid A, Faught W et al. Prospective longitudinal study of ultrasound screening for endometrial abnormalities in women with breast cancer receiving tamoxifen. Gynecol Oncol 2003; 91 : 154-159.
16. Gardner FJ, Konje JC, Brown L et al. Uterine surveillance of asymptomatic postmenopausal women taking tamoxifen. Climacteric 1998; 1 : 180-187.
17. Suh-Burgmann EJ, Goodman A. Surveillance for endometrial cancer in women receiving tamoxifen. Ann Intern Med 1999; 131 : 127-135.
18. Richenberg J CP. Ultrasound of the Uterus. In: Callen PW (ed). Ultrasound in Obstetrics and Gynecology. 4th ed. Philadelphia: WB Saunders 2000 : 841-842.
Štítky
Detská gynekológia Gynekológia a pôrodníctvo Reprodukčná medicína
Článok vyšiel v časopisePraktická gynekologie
Najčítanejšie tento týždeň
2006 Číslo 2- Ne každé mimoděložní těhotenství musí končit salpingektomií
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Je „freeze-all“ pro všechny? Odborníci na fertilitu diskutovali na virtuálním summitu
- Mýty a fakta ohledně doporučení v těhotenství
-
Všetky články tohto čísla
- Slovo úvodem
- Edukační kazuistika
- Efekt aplikace kortikoidů na dopplerovskou velocimetrii a plod
- Hereditární angioedém v těhotenství
- Sledování pacientek léčených tamoxifenem pro karcinom prsu
- Léze žlázového epitelu cervixu
- Tumor malé pánve u gynekologické pacientky – raritní případ benigního nádoru apendixu: kazuistika
- Klinický význam HPV-testu
- Karcinom pochvy
- Klinickobiochemické vyšetrenia a gravidita
- Pupečníková krev: slibný zdroj krvetvorných buněk pro transplantace
-
Autorská soutěž praktické gynekologie
O nejlepší článek v roce 2006 - Karcinom prsu a vulvy
-
Celostátní konference České gynekologické a porodnické společnosti ČLS JEP a Sdružení soukromých gynekologů ČR
Seminář porodních asistentek
Brno, 26.–28. května 2006
- Praktická gynekologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Tumor malé pánve u gynekologické pacientky – raritní případ benigního nádoru apendixu: kazuistika
- Karcinom pochvy
- Sledování pacientek léčených tamoxifenem pro karcinom prsu
- Léze žlázového epitelu cervixu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



