-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Roztroušená skleróza a dysfunkce dolních močových cest. Možnosti diagnostiky, potřeba léčby a sledování
MULTIPLE SCLEROSIS AND LOWER URINARY TRACT DYSFUNCTION. METHODS OF DIAGNOSTICS; TREATMENT AND FOLLOW-UP REQUIREMENTS
Based on data in literature almost 97% patients with multiple sclerosis suffer from lower urinary tract dysfunction. The impairment concerns both filling and emptying bladder function. Multiple sclerosis, among other diseases, is an underlying condition for neurogenic lower urinary dysfunction, which significantly impair patients’ quality of life. Currently there is a lack of any clearly defined criteria for MS patient care, especially in patients with advanced MS.
Key words:
multiple sclerosis, neurogenic urinary tract dysfunction, urinary incontinence
Autoři: G. Varga *; D. Pacík
Působiště autorů: Urologická klinika FN Brno LF MU Brno *
Vyšlo v časopise: Urol List 2012; 10(1): 56-62
Souhrn
Podle literárních zdrojů postihují dysfunkce dolních močových cest až 97 % pacientů s roztroušenou sklerózou (RS). Poškození se týká jak jímací, tak evakuační funkce močového měchýře. Roztroušená skleróza patří mezi nemoci podmiňující rozvoj neurogenně podmíněných dysfunkcí dolních močových cest, které zásadním negativním způsobem zasahují do kvality života postižených osob. Doposud však chybí jasně stanovená pravidla péče o pacienty s RS, zvláště pro pacienty s pokročilou formou RS.
Klíčová slova:
roztroušená skleróza, neurogenní dysfunkce močových cest, močová inkontinenceRoztroušená skleróza (RS) je chronické zánětlivé onemocnění centrálního nervového systému (CNS), které vede jak k demyelinizaci nervových vláken, tak k jejich přímé ztrátě. Toto záludné onemocnění je v naší zeměpisní šířce nejčastější (!) příčinou invalidity mladších věkových skupin z neurologických příčin [1]. Na celém světě postihuje 2,5 mil. lidí. RS je dnes jednoznačně řazena mezi autoimunitní zánětlivé onemocnění, přičemž cílovými antigeny pro autoimunitní agresi jsou antigeny myelinové pochvy, která obaluje nervová vlákna CNS. Prvním zdokumentovaným případem RS byl Augustus d’Esté (1794–1848), vnuk Jiřího III., krále Anglie, a bratranec královny Viktorie. Onemocnění se u něho objevilo ve 28 letech a prezentovalo se optickou neuritidou, paraparézou, mikčními potížemi a impotencí [2]. Jedná se o první dochovaný případ s typickým průběhem onemocnění včetně urologické symptomatologie.
EPIDEMIOLOGIE ROZTROUŠENÉ SKLERÓZY
Na epidemiologii tohoto onemocnění se podílí řada faktorů, které nejsou ještě doposud kompletně zmapované. Nejvyšší výskyt RS je v mírném pásmu severní polokoule. Je pozorovaná značná mezirasová a etnická variabilita prevalence onemocnění. RS se prakticky vyhýba Eskymákům, Japoncům a Laponcům. Nízký výskyt lze pozorovat i u afroamerické populace a indiánů. Tam, kde se toto onemocnění přesto vyskytuje, lze většinou vypátrat předka euroidní rasy, nejčastěji skandinávských předků. To poukazuje i na genetické faktory v epidemiologii s polygenním typem dědičnosti. Prevalence RS v ČR činí 100–150/100 tis. obyvatel. Vyskytuje se v poměru 2 : 1 v neprospěch žen, s prvními příznaky nejčastěji ve 2.–4. dekádě života. Mezi vyvolávající faktory, které u geneticky predisponovaného jedince vedou k rozvoji prvních příznaků, patří infekce, stres, hormonální změny (po porodu, menarché), kouření aj. Ložisko demyelinizace přitom může vzniknout v kterékoli oblasti mozku i míchy, z čeho také vyplývá i velká variabilita příznaků [1].
TYPY A PRŮBĚH ROZTROUŠENÉ SKLERÓZY
Průběh onemocnění RS lze obecně rozdělit na benigní, tedy dlouhotrvající remitentní průběh pozorovaný asi u 10–15 % pacientů, který je dán schopností imunitního systému včasně reagovat supresorickými mechanizmy. Lze ho hodnotit pouze retrospektivně, bez možnosti jakékoli predikce. Maligní průběh je charakterizován rychlým nárůstem neurologického deficitu s rozsáhlým poškozením axonů i oligodendrocytů v místě zánětlivých ložisek, tzv. placích [1].
Podle průběhu dělíme RS na typy:
- remitentní-relabující (80–85 % pacientů): onemocnění probíhá v atakách a následných remisích. Období remise může být bezpříznakové, pokud ataka nezanechala neurologický deficit. Polovina pacientů během prvních 10 let onemocnění přejde do sekundárně progresivního stadia
- sekundární progresivní: dochází k pozvolnému nárůstů neurologického deficitu, většinou již trvalého charakteru s relapsy/bez nich, které již nemají tak dramatický průběh jako u remitentního typu
- primárně progresivní (10–15 % pacientů): již od samého počátku je patrný pozvolný nárůst neurologického deficitu s dominující centrální (spastickou) paraparézou dolních končetin a častějším výskytem u mužů kolem 40. roku věku
- klinicky izolovaný syndrom (CIS): první ataka, která je na základě paraklinických vyšetření (magnetická rezonance, vyšetření likvoru) podezřelá z budoucího rozvoje RS (graf 1)
Graf 1. Graf znázorňující průběh jednotlivých typů RS (převzato z www.zdn.cz). 
ETIOPATOGENEZE
RS, jak již bylo zmíněno, je onemocnění charakterizované vznikem mnohočetných zánětlivých ložisek v bíle hmotě CNS. Jedná se o složitý autoimunitní proces iniciovaný autoagresivními T-lymfocyty proti myelinovým antigenům. Tímto procesem dochází k aktivaci celé kaskády imunitních dějů s multicelulární účastí a s produkcí mnoha cytokinů a chemokinů, které vedou k poškození myelinu [1]. I když se tzv. plaky demyelinizace mohou vyskytovat kdekoli v CNS, predilekční oblastí je cervikální segment míšní a hlavně laterální kortikospinální a retikulospinální dráhy, které se podílí na inervaci detruzoru a vnějšího svěrače uretry [3].
Nejcennějším vyšetřením v diagnostice RS je nukleární magnetická rezonance (NMR), která potvrdí přítomnost plaků demyelinizace v CNS až u 70–95 % pacientů s typickou klinickou symptomatologii [4–6].
UROLOGICKÁ PROBLEMATIKA ROZTROUŠENÉ SKLERÓZY
Závažnost urologického aspektu tkví v tom, že až více než 80 % pacientů postižených RS trpí určitým stupněm neurogenně podmíněné dysfunkční mikce. U pacientů s dobou onemocnění trvající více než 10 let se přítomnost urologické symptomatologie objeví dokonce až v 96 % případů [3,7,8].
Postižení pacienti udávají nejen problémy s močením (LUTS), ale i úzce související potíže se stolicí, které tak negativním způsobem zasahují do kvality života osob trpících RS [9]. Sociální a psychologický aspekt močové inkontinence, která zasahuje do kvality života této komunity pacientů, by se neměl podceňovat, protože právě sociální izolace a ztráta sebedůvěry jsou ve skupině těchto pacientů typickým nálezem. Khan et al při zjišťovaní subjektivního vnímaní závažnosti jednotlivých poruch relevantních pro postižené RS demonstrovali, že až 94 ze 101 pacientů hodnotilo „močovou funkci“ jako „vysoce problematickou“ [10]. Nejen z pohledu matematika, ale i laika, se jedná o vysoké číslo.
Cílem neurologické a urologické veřejnosti je proto snaha najít vhodnou strategii pro zhodnocení onemocnění, která by byla jakýmsi vodítkem v plánovaní adekvátního postupu léčby a péče o pacienta s RS [11,12].
Na odborných fórech Společnosti pro sexuální, urologickou a střevní dysfunkci u pacientů s RS (SUBDIMS – „Sexual, Urological and Bowel Dysfunction In Multiple Sclerosis Group“) se opakovaně zdůrazňuje požadavek sjednocení urologického managementu podle pravidel „evidence--based-medicine“ (EBM), zvláště pro pacienty s pokročilou formou RS. Mezinárodní multidisciplinární kolektiv expertů v čele s Ridderem a se podílel na přehledu dostupné literatury zabírající se problematikou konzervativního managementu dysfunkcí DMC a byl konfrontován se značnou variabilitou diagnosticko-terapeutických postupů a s nedostatkem doporučení pro klinickou praxi [13]. Tato práce se stala základem k další iniciativě, která by měla vést ke zlepšení urologické péče o pacienty zejména s pokročilou formou RS.
CHARAKTERISTIKA NEUROGENNÍHO MĚCHÝŘE U RS
Podle etiologické klasifikace se RS řadí mezi získaná netraumatická onemocnění, která se podílí na rozvoji neurogenně podmíněných dysfunkcí dolních močových cest (NDMC). Typ dysfunkce závisí od lokalizace plaků demyelinizace v CNS. Jak již bylo zmíněno, i přes jejich predilekční lokalizaci v cervikálním míšním segmentu se mohou vyskytovat prakticky kdekoli v CNS [1]. Zvláště pak v případě primárně a sekundárně progresivního typu RS. Doposud chybí důkazy pro potvrzení hypotézy, že dynamika patofyziologických změn CNS v průběhu nemoci koreluje i s dynamikou, resp. se změnou jednoho typu NDMC na druhý. Protože neurologický nález je v případě primární a sekundární progresivní RS charakterizovaný postupným zhoršováním, lze usuzovat, že i urodynamický nález se může v průběhu nemoci změnit. Délka trvání RS signifikantně koreluje s výskytem a závažností dysfunkce dolních močových cest (DMC) [10,11]. Není vyloučené, že původní spinální nebo supraspinální léze časem zprogreduje do sakrální nebo subsakrální léze charakterizované již jiným typem NDMC [14]. Léčba, která zpočátku pacientovi zabírá, se tak může časem projevit jako neúčinná nebo dokonce může situaci ještě zhoršovat.
Ve včasném stadiu RS dominují symptomy urgence, urgentní inkontinence a frekvence způsobené neurogenní hyperaktivitou detruzoru (NDO). Prevalence tohoto typu dysfunkce je v literárních zdrojích uváděná v rozmezí 37–99 %. Obstrukční symptomatologie z důvodů detruzorosfinkterické dyssynergie (DSD) se vyskytuje u 34–79 % pacientů a v 25 % případech se můžeme setkat s chronickou retencí močovou. Současná koexistence jímací (iritační symptomatologie) a evakuační (obstrukční symptomy) poruchy byla zjištěna u 59 % mužů a 51 % žen [10]. Jejím urodynamickým podkladem může být kombinace NDO + DSD, která může vést ke zvýšení intravezikálního tlaku a následnému rozvoji vezikoureterálního refluxu (VUR). I přes fakt, že deteriorace horních cest močových v případě RS se zdá být nižší než v případě traumatického míšního postižení, je potřebné věnovat lidem (a zvláště mužům) s touto kombinací speciální pozornost [13,15].
DIAGNOSTIKA
Metody ke stanovení typu NDMC a močové inkontinence u pacientů s RS se prozatím řídí doporučením Evropské urologické asociace (EAU) pro léčbu neurogenních dysfunkcí močových cest [16]. Pozůstávají z klinického vyšetření včetně anamnézy a zhodnocení mikčního diáře, urodynamických studií (cystometrie + EMG, videourodynamika, uroflowmetrie, PQ studie) a zobrazovacích metod (ultrazvukové vyšetření ledvin a měchýře, mikční cystouretrografie, event. nefrogram). Před jakýmkoli funkčním vyšetřováním je však bez pochybností nutné shromáždit veškeré základní údaje, které se použijí při další interpretaci NDMC [16,17].
Anamnéza
Cílem obecné anamnézy je shromáždit informace o délce trvání RS, jejím typu a průběhu, o koexistenci dalších neurologických, případně kongenitálních anomálií, o předchozích urologických onemocněních a jejich léčbě. Důležitá je také farmakologická anamnéza k zjištění možného vlivu užívané medikace na funkci dolních močových cest (DMC). V gynekologické anamnéze se zaměřujeme na počet a způsob vedení porodů, menstruační a sexuální funkci. Dále je třeba zhodnotit i střevní funkci, která je inervačně propojena s mikční. Významné je zaměřit se na faktory životního stylu, jako je kouření, konzumace alkoholu a drog. Ve speciální anamnéze dokumentujeme příznaky a symptomy, které pacienta přinutily navštívit specializované vyšetření. Je potřebné zaznamenat symptomy související jak s jímací, tak i s evakuační funkcí DMC, dále nástup a povahu NDMC. Je vhodné srovnat současný stav mikce se stavem před samotným vznikem NDMC a dále dokumentovat časovou asociaci vzniku mikčních potíží a RS. Velmi důležité jsou údaje o projevech močové inkontinence, způsobu a typu močení jako i samotné vnímaní močení. Mikční deníky poskytují cenné informace o počtu mikcí, frekvenci denního a nočního močení, počtu nucení na močení, objemech mikčních porcí, epizodách inkontinence, bilanci tekutin a umožňují zhodnotit i případnou noční polyurii.
Fyzikální vyšetření
Obecné fyzikální vyšetření klade důraz na zhodnocení mentálního a fyzického stavu pacienta. Těžká porucha mobility, zvýšený svalový spazmus, těžká mentální porucha, kognitivní poruchy, celková slabost a přítomnost těžkých komplikací jsou údaje, na které je potřeba zaměřit naši pozornost, protože určují další léčebnou strategii. Palpací hodnotíme zevní genitál, perineální kůži, dolní polovinu břicha a zad, dále prostatu, hodnotíme stav pánevního dna a případně pokles pánevních orgánů. Jako součást obecného neurofyziologického vyšetření lze provést specifické testy ke zhodnocení motorických a senzorických funkcí trupu, končetin a nohou. Je však nutné podotknout, že většina pacientů s RS již přichází do urologické ambulance s neurologickým nálezem, který nám poskytuje veškeré potřebné informace o postižení inervace. Přesto se neivazivními speciálními testy můžeme zaměřit na vyšetření aktivity sakrálního reflexu a kožní citlivosti v perineálních dermatomech. Vyšetřujeme citlivost perianogenitální oblasti, tonus análního sfinkteru, volní kontrakce análního sfinkteru a pánevního dna.
Laboratorní testy a paraklinické metody
Nedílnou součástí je i chemické a mikroskopické vyšetření moči, rozbor krve a zobrazovací vyšetření, jako je ultrazvuk ledvin a měchýře, postmikční reziduum, RTG, popřípadě magnetická rezonance (NMR) [17]. NMR CNS má své opodstatnění asi u 9 % pacientů s RS, u kterých jsou mikční potíže prvním symptomem vedoucím k potvrzení diagnózy RS [18].
Obr. 1. Šipky označují mnohočetná ložiska demyelinizace lokalizovaná periventrikulárně a v oblasti postranních komor mozku u pacientky s primárně progresivní formou RS. 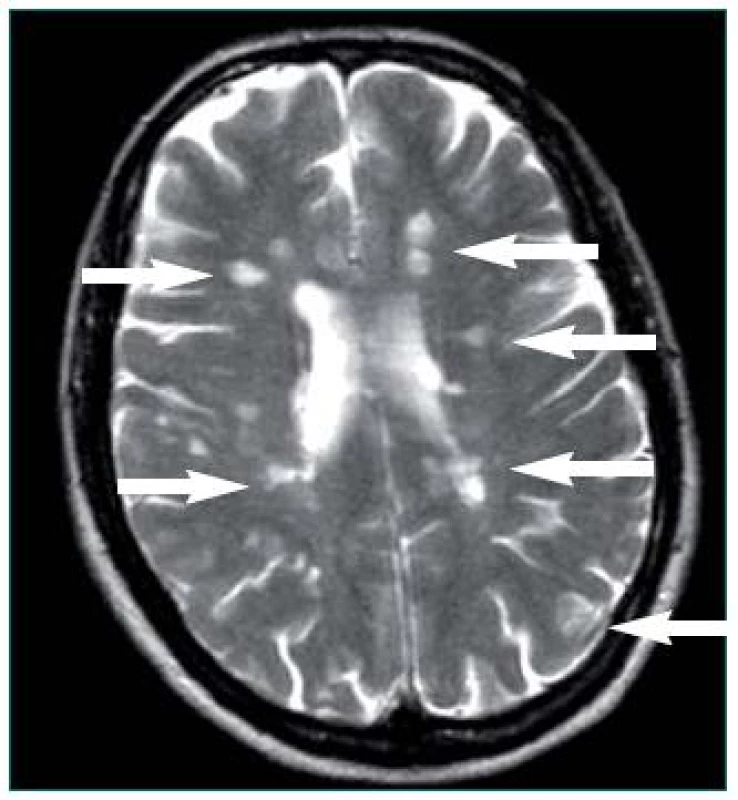
Urodynamické vyšetření (UD)
Klasické urodynamické techniky nám umožňují získat mnoho funkčních parametrů u pacientů s neurogenním měchýřem a umožňují objektivní zhodnocení dysfunkce DMC. Podle doporučení EAU pro klinickou praxi je před zahájením UD vyšetření nutné vyprázdnit rektální ampulu. Minimálně 48 hod před vyšetřením je nutné vysadit léky ovlivňující funkci DMC [16]. Všechny nálezy UD vyšetření je nutné podrobně zaznamenat a zhodnotit na základě doporučení a standardů Mezinárodní společnosti pro kontinenci (ICS) a kriticky zhodnotit jakýkoli zdroj artefaktů během vyšetření. Součásti UD vyšetření je:
- Mikční diář, jak již o něm bylo zmíněno v odstavci o anamnéze, se doporučuje k zhodnocení stavu DMC. Je vhodné pacienta poučit o záznamu alespoň 2–3 dnů [16].
- Uroflowmetrie (UFM) a měření postmikčního rezidua (PVR) je neinvazivní metoda k posouzení funkčního stavu mikce. Je nutné ho provést před invazivním UD vyšetřením a doporučuje se vyšetření opakovat 2–3× [16]. Velkým přínosem jsou také při dispenzarizaci a hodnocení efektu léčby.
- Plnicí cystometrie (CSM) zaznamenává chování detruzoru během plnicí fáze. Nejlepších výsledků dosahuje v kombinaci s měřením intravezikálního tlaku během mikční fáze nebo s videourodynamickým vyšetřením [16].
- Měření DLPP (Detrusor Leak Point Pressure) umožňuje hodnotit riziko poškození HMC. Hodnota nad 40 cm H2O je spojena s vysokým rizikem postižení HMC [20]. V případě RS je však toto riziko minimální a pohybuje se pod 1 %.
- Manometricko-průtoková studie (PQ studie) zhodnocuje souhru detruzoru, sfinkteru a pánevního dna během močení. Nejlepších výsledků lze dosáhnout její kombinací s videourodynamickým vyšetřením. Většina typu obstrukcí, které vznikají následkem NDMC, jsou zapříčiněny nerelaxující uretrou nebo nerelaxujícím hrdlem měchýře [16]. PQ studie hodnotí hlavně mechanickou obstrukci, u pacientů s NDMC má pouze omezený význam.
- Elektromyografie (EMG) zaznamenává aktivitu zevního uretrálního svěrače, periuretrální příčné svaloviny, análního svěrače a příčně pruhované svaloviny pánevního dna. Při UD vyšetření je EMG pomůckou k zhodnocení schopnosti pacienta ovládat svalovinu pánevního dna. V průběhu mikční fáze lze rozpoznat přítomnost DSD.
- Profilometrie uretry má při diagnostice NDMC pouze omezenou roli [21].
- Videourodynamické vyšetření představuje standardní metodu vyšetřování NDMC [16].
Nezodpovězena zůstává otázka přínosu urodynamického vyšetření u pacientů s RS. I přesto, že riziko poškození horních močových cest u RS se zdá nižší než u pacientů s míšní lézí, je potřebné věnovat speciální pozornost pacientům (speciálně mužům) s neurogenní detruzorovou hyperaktivitou v kombinaci s DSD [8]. Elegantní studie Giannantoniho ukázala, že komplikace horních močových cest (HMC) signifikantně korelují s délkou trvání RS, s maximem amplitudy detruzorových kontrakcí a s poškozením pyramidových drah. V jeho studii nebyla prokázána korelace poškození HMC s typem RS nebo dokonce s hodnotou EDSS (Expanded Disability Status Scale) [23]. Již několik let se objevují práce, které uvažují o možnosti použít odlišné diagnosticko-terapeutické postupy, než je tomu v případě transverzálních míšních lézí. Krhut et al publikovali jednoduchý diagnosticko-léčebný algoritmus v případě dysfunkcí DMC u RS, kdy na základě symptomů a zhodnocení PVR byli pacienti stratifikováni do několika léčebných skupin. Ke kompletnímu UD vyšetření byli indikovaní pouze ti pacienti, kteří nezareagovali na zavedenou terapii [24]. Toto schéma lze použít v běžné urologické ambulanci v rámci prvního kontaktu s pacientem s RS, ale přesto se domníváme, že primárně by skupina těchto pacientů měla být již od počátku vzniku urologických potíží vedena ve specializovaných centrech (urodynamických poradnách) zabývajících se danou problematikou. Poškození HMC nemusí být způsobeno pouze vezikoureterálním refluxem, ale i hypertrofií detruzoru, která může vést k vezikoureterální obstrukci [13]. Závažnost případné subvezikální obstrukce a hodnotu detruzorového tlaku během mikce lze bezpečně určit pouze kompletním UD vyšetřením, které se doposud považuje za zlatý standard v diagnostickém algoritmu.
Speciální testy
Speciální testy jako „ledový test“ (test ledovou vodou) nebo betanecholový test nemají v případě RS větší význam.
Neurofyziologické testy
Speciální vyšetřovací metody mohou být doplňkem neurologického, resp. neuro-fyziologického vyšetření. Některé testy podle ICS lze považovat prozatím za experimentální [25]. Jejich výtěžnost se uplatňuje v neurologické praxi, pro urologické potřeby u pacientů s RS je prakticky nulová. Jedná se o:
- EMG svaloviny pánevního dna, análního sfinkteru
- měření latence bulbokavernozního reflexu (experimentální metoda)
- motorické evokované potenciály
- studie nervového vedení n. pudendus
- somatosenzorické evokované potenciály
- epidurální záznam spinálních evokovaných potenciálů (experimentální metoda)
- extradurální záznam aferentní nervové aktivity ze sakrálních kořenů (experimentální metoda)
- test sympatikové kožní odpovědi (experimentální metoda)
LÉČBA
Léčba neurogenně podmíněných dysfunkcí DMC u pacientů s RS je primárně konzervativní. V případě již pokročilé formy RS je založena spíše na tradici než na důkazech, které jsou shromážděny z literatury orientované z převážné většiny na traumatické postižení míchy. Většina center nevyužívá v péči o tyto pacienty žádný strukturovaný přístup nebo se řídí jenom interními limitovanými doporučeními [10]. Terapeutické principy se dnes prozatím řídí doporučením Evropské urologické asociace (EAU) na základě výsledku UD vyšetření [16]. Obecně platí poučka z doporučení EAU a Mezinárodní společnosti pro kontinenci (ICS), že primárním cílem léčby je ochrana horních močových cest, zlepšení močové inkontinence, zlepšení kvality života a podle možností obnova normální funkce DMC [16,25].
Rehabilitace
Posilování pánevního dna, tak jak ho prezentoval Kegel v roce 1948 pro léčbu stresové inkontinence, se osvědčilo jako účinná léčba LUTS u pacientů s RS, kdy došlo ke zlepšení symptomů a potlačení DO [26,27]. Lucio et al v prospektivní randomizované studii potvrdili účinnost posilování PD jako „sólo“ léčby u žen s remitentní formou RS. Autoři dosáhli zmírnění LUTS, snížení počtu epizod inkontinence a redukce počtu vložek a také snížení nykturií ve srovnání s kontrolní skupinou [28].
Podobných výsledků bylo dosaženo i při zhodnocovaní výsledku elektrostimulace svalstva pánevního dna jako i elektrostimulace sakrálních dermatomů u pacientů s RS s detruzorovou hyperaktivitou [29,30].
Opakovaná transkraniální magnetická stimulace motorické oblasti kortexu indukuje déle trvající modulaci spinální excitability. Proto tato metoda, prozatím experimentální, představuje do budoucna potenciální možnost léčby NDMC [31]. U 9 z 10 pacientů s RS, kteří si stěžovali na potíže s močením, došlo po aplikaci této metody ke zlepšení mikční fáze a k signifikantní redukci PVR [32].
Konzervativní management
Anticholinergika a čistá intermitentní selfkatetrizace (ČIK) jsou považovány za základ urologické péče o pacienty ve včasném stadiu RS. Přesto se během progrese onemocnění můžeme potkat s mnoha interferujícími faktory, které komplikují průběh ČIK. Důležitá je optimalizace schématu ČIK, která může významně redukovat frekvenci inkontinence [33]. U pacientů s míšním traumatem bylo prokázáno, že až 50 % žen zanechalo ČIK z důvodu přetrvávající inkontinence [34]. Ztráta motoriky horních končetin, nedostatečná abdukce dolních končetin nebo porucha kognitivních funkcí v průběhu progrese RS jsou dalšími faktory, které znemožňují průběh ČIK [13].
Kondomové urinaly se často používají jako pohodlné řešení inkontinence, ale je potřebné myslet na možnost maskování vysokotlakového močového měchýře. Proto jako permanentní řešení by se měly používat až po UD vyšetření u pacientů s optimální evakuací močového měchýře.I přes riziko infekce a kožních problémů může být jejich dlouhodobé užívaní užitečné u vybraných pacientů v pokročilém stadiu RS [13].
Permanentní katetrizace by teoreticky měla být určena pro ty pacienty, u kterých selhaly všechny možné terapeutické metody. De Ridder retrospektivním přehledem literárních zdrojů zjistil, že pouze 28 % pacientů s pokročilou RS mělo permanentní katetrizaci jako trvalé řešení NDMC nebo inkontinence (40 % permanentní katétr, 60 % epicystotomie) [13]. Je mylnou představou, že permanentní katetrizace poskytuje ochranu před deteriorací HMC, protože rozhodujícím faktorem pro tuto komplikaci je intravezikální, resp. detruzorový tlak, ne objem nebo kapacita měchýře [23]. Neurogenní měchýř se může kontrahovat kolem balonku katétru, a vysoký intravezikální tlak tak může stále vyvolat VUR [35]. Studie dále prokázaly, že dlouhodobá katetrizace způsobuje různé komplikace, jako je uretrální trauma a krvácení, uretritida, uretrokutánni fistula jako důsledek nevhodně zvoleného kalibru katétru, urolitiáza, akutní a chronická infekce močových cest, eroze meatu a sfinkteru, inkompetence hrdla měchýře a karcinom měchýře [36]. Proto se u pacientů s NDMC doporučuje odstranit permanentní katétr, co nejdříve to situace dovolí, a přejít na jinou metodu derivace moči, tedy ČIK. Z hlediska snížení rizika febrilních epizod mohou z dočasného nočního zavedení permanentního balonkového katétru profitovat pacienti na intermitentní katetrizaci s přetrvávajícími nočními úniky. Pokud je však dlouhodobá katetrizace nevyhnutelná, měly by se upřednostňovat silikonové katétry, nebo katétry potažené hydrogelovou vrstvou [37]. Z hlediska léčby infekcí se v současnosti akceptuje, že bakteriurie by se v průběhu chronické katetrizace měla léčit jen v případě klinické symptomatologie, jakou je cystalgie, horečka, hematurie, náhle obtékaní katétru nebo zvýšení elasticity. Výše uvedené platí i přes fakt, že se jedná o skupinu s imunokopromitovaným stavem [13].
FARMAKOTERAPIE
Současná farmakoterapie NDMC poskytuje pro urologa dostatečné spektrum více či méně účinných selektivních preparátů. V případě NDMC se jedná o léčbu symptomatickou a je doplňkem ostatních terapeutických metod. Jejím cílem je ovlivnit detruzorovou hyperaktivitu, neurogenní sfinkterovou deficienci nebo posílit evakuační schopnost měchýře, a to právě na základě výsledku UD vyšetření. V případě perzistující NDO lze postupnou titrací použít i vysoké dávky anticholinergik, pokud pacient dobře toleruje vedlejší účinky preparátu.
Noční polyurie a nykturie mohou být léčeny desmopresinem v podobě perorálního lyofilizátu [38]. Před zavedením této léčby se musí brát v úvahu riziko vodní intoxikace a hyponatremie. Pre-vencí této komplikace jsou pravidelné kontroly iontů v séru, adekvátní restrikce tekutin a použití nižších terapeutických dávek [39]. Kontraindikací léčby jsou těžké poruchy kognitivních funkcí, které znemožňují validně zhodnotit příjem tekutin a spolupráci pacienta v průběhu léčby.
Alternativou k anticholinergní terapii je aplikace botulotoxinu (Btx), která si v ČR doposud nenašla stabilní místo v léčbě NDMC. Krhut et al prezentoval výsledky aplikace Btx do detruzoru u pacientů s NDMC a v dílčím souboru 9 pacientů s RS byla spokojenost s výsledkem léčby dosažena u všech 9 (100 %). Rovněž u všech 9 (100 %) pacientek se podařilo dosáhnout plné kontinence. Došlo k nárůstu cystometrické kapacity z 178,2 na 462,2 ml a snížení detruzorového tlaku z 52,2 na 10,4 cm H2O. Délka trvání účinku léčby byla 12,3 (8–15) měsíců [40].
I s intravezikální instalací kapsaicinu se dosáhlo významné redukce DO u 80 % pacientů s RS trvající po dobu 6 měsíců [42]. Již dříve se však kapsaicin nahradil resiniferatoxinem, který způsobuje menší bolestivost během aplikace. V současnosti je dostupný jako studijní lék jenom v několika centrech.
V současnosti probíhá intenzivně výzkum účinků marihuany (kanabisu), která může ovlivnit řadu symptomů RS, jako je spasticita, tremor, únava, bolest a mikční potíže. Počáteční výsledky však naznačují spíše subjektivní než objektivní zlepšení v mnoha symptomech RS [42]. Studuje se bezpečnost aplikace preparátů např. ve formě sublingválního spreje nebo orální medikace, ale již nyní je jisté, že současné užívaní rostlinných extraktů se bude ubírat cestou vývoje více specifických syntetických kanbinoidů [43].
CHIRURGICKÁ LÉČBA
Je jen pár literárních citací týkajících se chirurgické léčby dysfunkcí DMC u pacientů s RS. V případě vyčerpaní a selhání konzervativních metod se však lze ještě uchýlit k využití této varianty. Přesto je potřebné chirurgickou léčbu zvažovat přísně individuálně s přihlédnutím na handicap pacienta, možné komplikace související s výkonem, kvalitu života a samozřejmě přání pacienta. Nejdůležitějším faktorem při zvažovaní chirurgické léčby je prognóza ad vitam. Je potřebné myslet na fakt, že se jedná o imunokompromitované pacienty, pro které je jakákoli intervence spojena s obrovskou zátěží pro organizmus i pro samotný průběh RS.
Pacienti s netraumaticky získanou NDMC s refrakterní detruzorovou hyperaktivitou (DO) mohou profitovat z neuromodulace pomocí sakrální stimulace, která byla popsána i u pacientů s RS [44]. Přesto je ji vhodné navrhnout pacientům se stabilní formou RS a informovat je, že průběh neuromodulace může být narušen dalším vývojem, resp. případnou progresí jejich onemocnění. Obecně platí, že pacienti s nekompletní míšní lézí traumatického nebo netraumatického původu mohou z neuromodulace těžit na rozdíl od kompletní léze míšní nebo syndromu kaudy [44].
Z denervačních procedur se literatura zmiňuje o sakrální rizotomii předních a/nebo zadních kořenů (sakrální deaferentace, SDAF). Tato metoda může být zvažována také v případě refrakterní DO u pacientů, kteří nejsou schopni podstoupit současnou elektrostimulaci předních sakrálních kořenů (progresivní forma RS, pacienti neschopní dojít na toaletu) [46].
Sporadická data se v literatuře objevují i na využití augmentační ileocystoplastiky. Zachoval et al publikovali v r. 2003 výsledky této metody v souboru 9 pacientů (7 žen, 2 muži) s refrakterní DO. 7 pacientů mělo remitentní a 2 pacienti sekundárně progresivní průběh RS. Pooperačně, během 6 - až 19měsíčního sledování, bylo pozorováno zlepšení ve všech sledovaných parametrech (nárůst kapacity, pokles Pdet, subjektivní zlepšení, zlepšení skóre QoL). 6 pacientů (2 již předoperačně) provádělo ČIK [46]. Autoři hodnotili tuto metodu jako efektivní a bezpečnou, pokud se indikuje uváženě. Zajisté by bylo zajímavé sdělení autora o této skupině pacientů, zda případnou progresí RS (pokud nastala) došlo i ke změně urologického managementu, zvláště ve skupině se sekundárně progresivní RS.
ZÁVĚR
Péče o pacienty s neurogenní dysfunkcí dolních močových cest představuje jednu z nejobtížnějších oblastí urologické praxe. V případě pokročilé formy RS je doposud založena spíše na tradici než na „evidence-based-medicine“. Většina těchto důkazu totiž pochází z literatury orientované na míšní poranění. Špatně zvolený postup při diagnostice a léčbě těchto dysfunkcí vede k výraznému zhoršení kvality života pacientů, kteří jsou již stigmatizováni samotnou RS. Proto je třeba přistupovat ke každému pacientovi s RS individuálně a, pokud možno, je orientovat spíše do center zabývajících se danou problematikou. Doufejme, že trvale probíhající pokrok ve výzkumu neuropatofyziologie RS a neurogenních mikčních poruch zaručí pacientům s tímto záludným onemocněním do budoucna vést ničím nerušený život. Role SUBDIMS do té doby je jasná: vytvořit guidelines s jasně stanoveným managementem pro tuto specifickou skupinu pacientů.
MUDr. Gabriel Varga, FEBU
Urologická klinika FN Brno LF MU Brno
Jihlavská 20, 625 00 Brno
gabrielvarga@hotmail.com
Zdroje
1. Havrdová E. Roztroušená skleróza míšní. In: Neuroimunologie. Praha: Maxdorf 2001.
2. Landtblom AM, Fazio P, Fredrikson S et al. The first case history of multiple sclerosis: Augustus d'Este (1794-1848). Neurolgical Sciences 2010; 31(1): 29–33.
3. Zachoval R. Mikční dysfunkce u pacientů s roztroušenou sklerózou. In: Krhut J et al. Neurourologie. Praha: Nakladatelství Galén 2005.
4. Bielekova BM, Kadom NM et al. MRI as a marker for disease heterogeneity in multiple sclerosis. Neurology 2005, 11(65): 1071.
5. Chard, D, Miller D. Is multiple sclerosis a generalized disease of the central nervous system? An MRI perspective. Curr Opin Neurol 2009; 22(3): 214–218.
6. Rovaris M, Barkhof F, Calabrese M et al. MRI features of benign multiple sclerosis: Toward a new definition of this disease phenotype. Neurology 2009; 72(19): 1693–1701.
7. Koldewijn EL, Hommes OR, Lemmens WA et al. Relationship between lower urinary tract abnormalities and disease related parameters in multiple sclerosis. J Urol 1995, 154(1): 169–173.
8. Litwiller SE, Frohman EM, Zimmern PE. Multiple sclerosis and the urologist. J Urol 1999; 161(3): 743–757.
9. Krogh K, Christensen P. Neurogenic colorectal and pelvic floor dysfunction. Best Pract Res Clin Gastroenterol 2009; 23(4): 531–543.
10. de Seze M, Ruffion A, Dennys P et al. The neurogenic bladder in multiple sclerosis: review of the literature and proposal of management guidelines. Mult Scler 2007; 13(13): 915–928.
11. Khan F, Pallant JF, Shea TL et al. Multiple sclerosis: prevalence and factors impacting bladder and bowel function in an Australian community cohort. Disabil Rehabil 2009; 31(19): 1567–1576.
12. Borello-France D, Dusi J, O'Leary M et al. Test-retest reliability of the Urge-Urinary Distress Inventory and Female Sexual Function Index in women with multiple sclerosis. Urol Nurs 2008; 28(1): 30–35.
13. DeRidder D, Ost D, Van der AF et al. Conservative bladder management in advanced multiple sclerosis. Mult Scler 2005; 11(6): 694–699.
14. Varga G, Hajný M, Pacík D et al. Korelace urodynamického nálezu a nálezu na magnetické rezonanci u pacientů s dysfunkční mikcí v důsledku sklerózy multiplex. Čes Urol 2007; 11(1): 37.
15. Lemack GE, Frohman E, Ramnarayan P. Women with voiding dysfunction secondary to bladder outlet dyssynergia in the setting of multiple sclerosis do not demonstrate significantly elevated intravesical pressures. Urology 2007; 69(5): 893–897.
16. Stöhrer M, Castro-Diaz D, Chartier-Kastler E et al. EAU Guidelines on Neurogenic Urinary Tract Dysfunction. In: EAU Guidelines.
17. Stohrer M, Goepel M, Kondo A et al. The standardization of terminology in neurogenic lower urinary tract dysfunction with suggestions for diagnostic procedures. Neurourol Urodyn 1999; 18(2): 139–158.
18. Fowler CJ. Bladder dysfunction in multiple sclerosis: causes and treatment. Int. MS Journal. 1996; 1 : 4.
19. Hanuš T. A Value of Urodynamic for Patients with Neurogenic Lower Urinary Tract Dysfunctions. Textbook ESU Course Functional Disorders of the Urinary Tract; an update 2001; 21–28.
20. Bruschini H, Almeida FG, Srougi M. Upper and lower urinary tract evaluation of 104 patients with myelomeningocele without adequate urological management. World J Urol 2006; 24(2): 224–228.
21. Lose G, Griffiths D, Hosker G et al. Standardisation of urethral pressure measurement: Report from the Standardisation Sub-Committee of the International Continence Society. Neurourol Urodyn 2002; 21(3): 258–260.
22. van Waalwijk van Doorn E, Anders K, Khullar V et al. Standardisation of ambulatory urodynamic monitoring: Report of the Standardisation Comittee of the Internationla Continence Society for Ambulatory Urodynamic Studies. Neurourol Urodyn 2000; 19(2): 113–125.
23. Giannantoni A, Scivoletto G, Di Stasi SM et al. Urological dysfunctions and upper urinary tract involvement in multiple sclerosis patients. Neurourol Urodyn 1998; 17(2): 89–98.
24. Krhut J, Hradílek P, Mainer K et al. Nové schéma v diagnostice a terapii dysfunkcí dolních močových cest u pacientů s roztroušenou sklerózou. Urologie pro praxi 2005 : 209–212.
25. Wyndaele JJ, Kovindha A, Madersbacher H et al. Neurologic Urinary and Faecal Incontinence. In: Incontinence, 4th Edition, Abrams P, Cardozo L, Khoury S, Wein A (eds.) Plymouth: Health Publication Ltd., 2009 : 793–960.
26. McClurg D, Ashe RG, Marshall K et al. Comparison of pelvic floormuscle training electromyography biofeedback, and neuromuscular electrical stimulation for bladder dysfunction in people with multiple sclerosis: a randomized pilot study. Neurourol Urodyn 2006; 25(4): 337–348.
27. De Ridder D,Vermeulen C, Ketelaer P et al. Pelvic floor rehabilitation in multiple sclerosis. Acta Neurol Belg 1999; 99(1): 61–64.
28. Lucio AC et al. Pelvic Floor Muscle Training in the Treatment of Lower Urinary Tract Dysfunction in women with Multiple Sclerosis. Neurourol Urodyn 2010; 29(8): 1410–1413.
29. McClurg D et al. Neuromuscular Electrical Stimulation and the treatment of Lower Urinary Tract Dysfunction in Multiple Sclerosis – A Double Blind, Placebo Controlled, Randomised Clinical Trial. Neurourol Urodyn 2008; 27(3): 231–237.
30. Fjorback MV, Van Rey FS, Rijkhoff NJ et al. Electrical stimulation of sacral dermatomes in multiple sclerosis patients with neurogenic detrusor overactivity. Neurourol Urodyn 2007; 26(4): 525–530.
31. Baumer T, Lange R, Liepert J et al. Repeated premotor rTMS leads to cumulative plastic changes of motor cortex excitability in humans. Neuroimage 2003; 20(1): 550–560.
32. Centonze D, Petta F, Versace V et al. Effects of motor cortex rTMS on lower urinary tract dysfunc-tion in multiple sclerosis. Mult Scler 2007; 13(2): 269–271.
33. De Ridder D, Van Poppel H, Baert L et al. From time dependent intermittent self-catheterization to volume dependent self-catheterization in multiple sclerosis using the PCI 5000 bladdermanager. Spinal Cord 1997; 35(9): 613–616.
34. Timoney AG, Shaw PJ. Urological outcome in female patiens with spinal cord injury: the effectiveness of intermittent catheterization. Paraplegia 1990; 28(9): 556–563.
35. Jamil F, Williamson M, Ahmed YS et al. Natural-fill urodynamics in chronically catheterized patients with spinalcord injury. BJU Int 1999; 83(4): 396–399.
36. Wall BM, Dmochowski RR, Malecha M et al. Inducible nitric oxide synthase in the bladder of spinal cord injured patients with a chronic indwelling urinary catheter. J Urol 2001; 165(5): 1457–1461.
37. Ozawa H, Uematsu K, Ohmori H et al. [Long-term usefulness and safety of the contemporary balloon catheter]. Zasshi 2005; 96(5): 541–547.
38. Valiquette G, Herbert J, Maede-D’Alisera P. Desmopressin in the management of nocturia in patients with multiple sclerosis. A double-blind, crossover trial. Arch Neurol 1996; 53(12): 1270–1275.
39. Odeh M, Oliven A. Coma and seizures due to severe hyponatremia and water intoxication in an adult with intranasal desmopressin therapy for nocturnal enuresis. J Clin Pharmacol 2001; 41(5): 582–584.
40. Krhut J et al Výsledky léčby neurogenních dysfunkcí dolních cest močových aplikací botulinum-toxinu do detruzoru. Čes Urol 2007; 11(3): 77–81.
41. De Ridder D, Chandiramani V, Dasgupta P et al. Intravesical capsaicin as a treatment for refractory detrusor hyperreflexia: a dual center study with long-term follow up. J Urol 1997; 158(6): 2087–2092.
42. Zajicek J, Fox P, Sanders H et al. Cannabinoids for treatment of spasticity and other symptoms related to multiple sclerosis (CAMS study): multicentre randomised placebo-controlled trial. Lancet 2003; 362(9395): 1517–1526.
43. Duran M, Laporte JR, Capella D. News about therapeutic use of cannabis and enclocannabinoid system. Med Clin 2004; 122(10): 390–398.
44. Chartier-Kastler EJ, Ruud Bosch JL, Perrigot M et al. Long-term results of sacral nerve stimulation (S3) for the treatment of neurogenic refraktory urge incontinence related to detrusor hyperreflexia. J Urol 2000; 164(5): 1476–1480.
45. Hohenfellner M, Pannek J, Botel U et al. Sacral bladder denervation for treatment of detrusor hyperreflexia and autonomic dysreflexia. Urology 2001; 58(1): 28–32.
46. Zachoval R, Piťha J, Medová E et al. Augmentation cystoplasty in patients with multiple sclerosis. Urol Int 2003; 70(1): 21–26.
Štítky
Detská urológia Urológia
Článek Slovo úvodem
Článok vyšiel v časopiseUrologické listy
Najčítanejšie tento týždeň
2012 Číslo 1- Vyšetření T2:EGR a PCA3 v moči při záchytu agresivního karcinomu prostaty
- Lék v boji proti benigní hyperplazii prostaty nyní pod novým názvem Adafin
-
Všetky články tohto čísla
- Slovo úvodem
- Souvislost mezi testosteronem a karcinomem prostaty
- Nádory prostaty a varlat u české a světové populace
- Aktivní sledování malých tumorů ledviny
- Radiofrekvenční ablace nádorů ledvin
- Současné principy a terapeutické koncepty pro retrográdní intrarenální odstranění urolitiázy
- Role profylaxe antibiotiky při léčbě vezikoureterálního refluxu
-
Laparoskopická operace pánevního dna
Část I – laparoskopická kolposuspenze
Část II – laparoskopická kolpopexe - Roztroušená skleróza a dysfunkce dolních močových cest. Možnosti diagnostiky, potřeba léčby a sledování
- Jaká je skutečnost srovnání konvenčního a roboticky asistovaného přístupu k radikální prostatektomii? Je oprávněné platit vyšší cenu?
- Nykturie u geriatrické populace a její důsledky, jaké jsou možnosti jejího ovlivnění, co je možné, co reálné a co smysluplné?
- Nežádoucí účinky antimuskarinik na centrální nervový systém
- Popis a klasifikace komplikací po urologických chirurgických výkonech:Ad hoc hodnocení a doporučení EAU Guidelines
- Urologické listy
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Souvislost mezi testosteronem a karcinomem prostaty
- Nežádoucí účinky antimuskarinik na centrální nervový systém
-
Laparoskopická operace pánevního dna
Část I – laparoskopická kolposuspenze
Část II – laparoskopická kolpopexe - Radiofrekvenční ablace nádorů ledvin
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



