-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Silový trénink u nemocných po akutním infarktu myokardu se sníženou ejekční frakcí levé komory srdeční
Power training at the patients after acute myocardial infarction with decreased left ventricular ejection fraction
Intention of the work:
Cardiovascular rehabilitation programme is an important and indivisible part of care of the patients after acute myocardial infarction. The basis of the rehabilitation programme in patients at rehabilitation phase II is an anaerobic training recently combined with the training with power moves. The submitted work addresses the evaluation of the training safety in patients with decreased left ventricular ejection fraction (EF).Patients and methods:
The authors have involved 109 patients (18 women, 91 men) in the age of 58 ± 9 years (median 58 years) to the ambulantory controlled rehabilitation programme. 11 patients (10 %) had an induced myocardial ischaemia at the entry load test. 34 patients (32 %) had decreased EF < 50 % (38 ± 6 %, median 41 %). The time from the development of myocardial infarction to the initiation of rehabilitation was 31 ± 7 days (median 29 days), at the patients after aortal coronary bypass it was 45 ± 19 days (median 33 days). Before and after rehabilitation the patients had echocardiographically determined left ventricular EF and there was made a spiroergometry with determination of peak oxygen intake (pVO2). They attended the rehabilitation programme 3 times a week during 8 weeks. There was made an aerobic exercise at the pulse frequency corresponding 60 pVO2 and 14 days later it was supplemented with power exercises. Patients with normal EF made power exercises at 50% 1 RM level (one repetition maximum), the patients with decreased EF started at the value of 30% 1-RM intending to reach the values of 50% 1-RM.Results:
In both subgroups of the patients the rehabilitation programme led to a significant increase of pVO2, load tolerance and training load tolerance, no significant differences between the subgroups were observed. In the subgroup with decreased EF the EF values moderately improved (38 ± 6 % versus 45 ± 6 %, p < 0.007). Before the rehabilitation, total muscular power was moderately but not significantly decreased in the subgroup with decreased EF (p < 0.09). In both subgroups the total power significantly increased (p < 0.0001) without mutual difference, total power increase was higher in the subgroup with decreased EF (p < 0.004. The relationship among total power, EF and pVO2 was not found, but there exists a correlation to the age before rehabilitation (r = –0.43, p < 0.003) and after rehabilitation (r = –0.41, p < 0.001).Conclusion:
Isometric exercise in patients after accute myocardial infarction is safe, it did not led to the development of myocardial ischemia, haemodynamic changes or arrhytmia. The authors initiate the ambulatory rehabilitation programme within 3–4 weeks after the development of accute myocardial infarction involving the power exercises after 2 weeks of initial aerobic training.Key words:
accute myocardial infarction – rehabilitation – power exercise
Autoři: L. Elbl 1; V. Chaloupka 1; I. Tomášková 1; F. Jedlička 1; S. Nehyba 1; P. Kala 2; J. Schildberger 2; M. Poloczek 2; Š. Chaloupková 3; M. Hudcová 3
Působiště autorů: Oddělení funkčního vyšetřování FN Brno, pracoviště Bohunice, přednosta: doc. MUDr. Václav Chaloupka, CSc. 1; Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC 2; Oddělení rehabilitace FN Brno, pracoviště Bohunice, přednosta prim. MUDr. Jana Roubalová 3
Vyšlo v časopise: Vnitř Lék 2005; 51(1): 41-47
Kategorie: Původní práce
Souhrn
Cíl práce:
Kardiovaskulární rehabilitační program je důležitou a nedílnou součástí péče o nemocné po akutním infarktu myokardu. Základem rehabilitačního programu u nemocných ve druhé fázi rehabilitace je aerobní trénink, který je v poslední době kombinován se cvičením se silovými prvky. Předložená práce se zaměřuje na vyhodnocení bezpečnosti tohoto tréninku u nemocných se sníženou ejekční frakcí (EF) levé komory.Pacienti a metody:
Autoři zařadili do ambulantního řízeného rehabilitačního programu 109 nemocných (18 žen, 91 mužů) ve věku 58 ± 9 let (medián 58 let). 11 nemocných (10 %) mělo při vstupním zátěžovém testu indukovanou ischemii myokardu, 34 nemocných (32 %) mělo sníženou EF < 50 % (38 ± 6 %, medián 41 %). Doba od vzniku infarktu myokardu do zahájení rehabilitace byla 31 ± 7 dní (medián 29 dní), u nemocných po aortokoronárním bypassu 45 ± 19 dní (medián 33 dní). Nemocní měli před a po rehabilitaci echokardiograficky stanovenou EF levé komory a byla provedena spiroergometrie se stanovením vrcholového příjmu kyslíku (pVO2). Rehabilitační program absolvovali 3krát týdně po dobu 8 týdnů. Bylo provedeno aerobní cvičení při tepové frekvenci odpovídající 60 % pVO2 a po 14 dnech doplněno o silová cvičení. Pacienti s normální EF prováděli silová cvičení na úrovni 50 % 1-RM (one repetition maximum), pacienti se sníženou EF zahájili na hodnotě 30 % 1-RM s cílem dosáhnout hodnoty 50 % 1-RM.Výsledky:
V obou podskupinách nemocných vedl rehabilitační program k významnému zvýšení pVO2, zátěžové tolerance i tréninkové zátěžové tolerance, přičemž nebyly pozorovány významné rozdíly mezi podskupinami. V podskupině se sníženou EF došlo k mírnému zlepšení hodnot EF (38 ± 6 % vs 45 ± 6 %, p < 0,007). Celková svalová síla před rehabilitací byla mírně, ale nevýznamně snížena v podskupině se sníženou EF (p < 0,09). V obou podskupinách došlo k významnému nárůstu celkové síly (p < 0,0001) bez vzájemného rozdílu, přičemž přírůstek celkové síly byl vyšší v podskupině se sníženou EF (p < 0,004). Nebyl nalezen vztah mezi celkovou sílou, EF a pVO2, ale existuje korelace k věku před rehabilitací (r = –0,43; p < 0,003) a po rehabilitaci (r = –0,41; p < 0,001).Závěr:
Izometrické cvičení u nemocných po akutním srdeční infarktu se sníženou EF je bezpečné, nevedlo ke vzniku ischemie myokardu, hemodynamických změn nebo arytmie. Ambulantní rehabilitační program autoři zahajují do 3–4 týdnů od vzniku akutního srdečního infarktu a silová cvičení zařazují po 2 týdnech úvodního aerobního tréninku.Klíčová slova:
akutní infarkt myokardu – rehabilitace – silové cvičeníÚvod
Kardiovaskulární rehabilitační program je důležitou a nedílnou součástí péče o nemocné po akutním infarktu myokardu (IM). Rehabilitační program představuje komplexní přístup k nemocnému, zahrnující problematiku fyzické aktivity a sekundární prevence ischemické choroby srdeční [11]. Dnes je prokázáno, že rehabilitace pozitivně ovlivňuje morbiditu a mortalitu nemocných po IM [24].
Základem rehabilitačního programu u nemocných ve II. fázi rehabilitace po přestálém akutním IM je aerobní trénink [16]. Na druhé straně je nutno si uvědomit, že u většiny z nás v průběhu běžných denních aktivit spíše převládají činnosti se silovými prvky, tedy s dominující izometrickou prací svalů. Myšlenka zavést cvičení s rezistenčními prvky do rehabilitačního procesu není nová. Nicméně použití silových prvků se dlouho nedoporučovalo z obav provokace ischemie a arytmogenního účinku v souvislosti s velmi náhlým a poměrně velkým nárůstem krevního tlaku (TK), který doprovází izometrickou práci svalů. Dodnes není zcela jasný vliv silového cvičení na proces remodelace levé komory srdeční (LK) [4,10,19]. Některé práce prokázaly, že tyto obavy nejsou opodstatnělé [6,26]. Cvičení se silovými prvky bylo zařazeno i u nemocných s chronickým srdečním selháváním [7,20].
Většina publikovaných prací zaměřených na rehabilitaci nemocných po IM hodnotí výsledky aerobního programu [18]. Studií zabývajících se vyhodnocením silového cvičení je poměrně méně. V naší předchozí práci jsme vyhodnotili význam a bezpečnost silového tréninku po akutním IM v obecné rovině a s ohledem na věk nemocných [17]. Předložená práce navazuje na toto sdělení z roku 2000 a věnuje pozornost přínosu a bezpečnosti tréninku se silovými prvky u nemocných se sníženou ejekční frakcí levé komory (EF), kteří byli zařazeni do ambulantního řízeného rehabilitačního programu po prvním akutním IM v období let 2002–2003.
Soubor nemocných
Soubor nemocných tvoří 109 jedinců po prodělaném prvním IM ve věku (58 ± 9 let, medián 58 let, 26–80). Zařadili jsme 18 žen a 91 mužů. 34 nemocných (32%) mělo sníženou EF LK pod 50% (38 ± 6%, medián 41%, 28–48). Charakteristika obou podskupin je shrnuta v tab. 1. Celkem 11 nemocných (10%) mělo při vstupním vyšetření diagnostikovánu přítomnost ischemie při zátěžovém testu. 5 nemocných bylo v podskupině se sníženou EF a 6 mělo normální klidovou hodnotu EF. Nemocní se sníženou systolickou funkcí byli ve funkční klasifikaci NYHA I-III. Dle očekávání bylo v této skupině více nemocných s infarktem myokardu přední stěny (p < 0,0001) a ošetřených chirurgickou revaskularizací (p < 0,02). Průměrná doba zařazení pacienta do rehabilitačního programu od vzniku akutního IM byla 31 ± 7 dní (medián 29 dní, 13–44) u nemocných léčených PTCA. U pacientů, kteří se podrobili kardiochirurgickému zákroku, byla doba delší, 45 ± 19 dní (medián 33 dní, 23–68).
Tab. 1. Charakteristika podskupin. 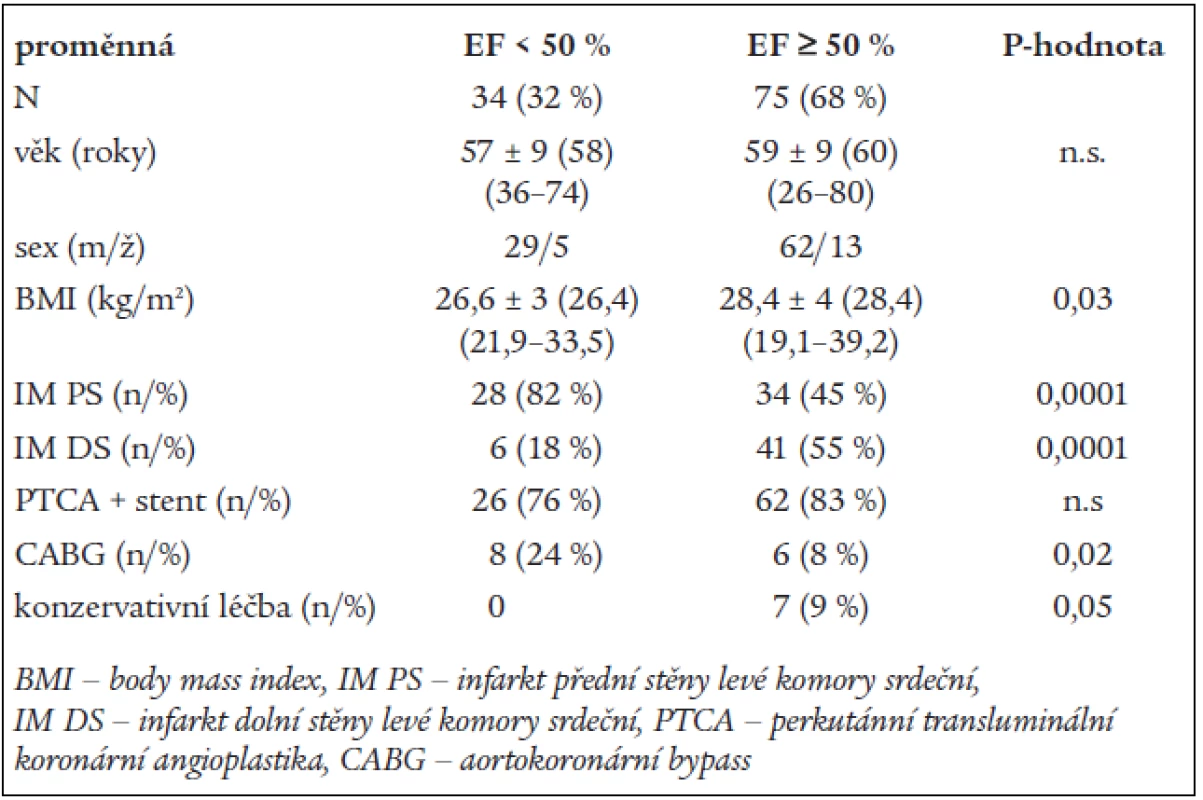
Metodika
Metodiku rehabilitačního programu jsme již opakovaně zveřejnili na jiném místě [17,22]. Aerobní cvičení probíhá na ergometrech při tepové frekvenci (TF) odpovídající 60% vrcholového příjmu kyslíku (pVO2). Silové cviky zařazujeme po 2 týdnech od zahájení programu a provádíme je na posilovacím zařízení BASIC Kettler. Před zahájením silového cvičení provedeme vyšetření krevního tlaku (TK) izometrickým zátěžovým testem pomocí ručního balonkového dynamometru. Pokud je reakce TK fyziologická (< 180/120 mm Hg), stanovíme pro každý cvik maximální zátěž, kterou je pacient schopen 1krát bez pomoci překonat (1-RM). Nemocní s normální EF cvičí na hodnotě 50% 1-RM, u nemocných se sníženou EF začínáme na hodnotě 30% 1–RM a cílem je dosáhnout 50% 1-RM. U těchto nemocných je během silového cvičení trvale sledován EKG-záznam na monitoru. Pro silové cvičení používáme sestavu 3 cviků: A – vzpírání zátěže dopředu, B – posilování nohou sounož a C – stahování zátěže. Zátěž, se kterou pacient cvičí, je vyjádřena v kg a součtem jednotlivých cviků získáme celkovou sílu [17].
Pacienti byli vyšetřeni před a po absolvování rehabilitačního programu echokardiograficky (ATL 3000 HDI) a pomocí 2rovinné Simpsnovy metody byla stanovena EF LK.
Spiroergometrické vyšetření (přístroj Oxycon Delta Jaeger) bylo taktéž provedeno před a po rehabilitačním programu. Provedli jsme rampový test 20 W/1 min. do subjektivního maxima či vzniku symptomů. Stanovili jsme hodnotu pVO2 pro vyhodnocení tréninkového efektu a hodnotu anaerobního prahu (ventilační anaerobní práh) pro určení tréninkové TF.
Statistická analýza dat
Předložené výsledky jsou uvedeny jako průměr + 1 SD, relativní četnost, interval a medián. Naměřené ukazatele před a po rehabilitačním programu byly srovnány párovým a nepárovým Studentovým t-testem. Vztahy mezi proměnnými jsme vyhodnotili lineární regresní analýzou. Neparametrické hodnoty byly testovány χ2-testem. Hodnoty p < 0,05 byly považovány za statisticky významné. Použili jsme statistický program NCSS 6.0 (Number Cruncher Statistical Systems, USA).
Výsledky
Ejekční frakce levé komory srdeční
Hodnota EF LK byla u nemocných s normálními hodnotami 60 ± 4% (medián 60%, 50–68) a nebyla rehabilitačním programem ovlivněna (60 ± 5%, medián 60%, 55–71, n.s.). U nemocných se sníženou klidovou EF byla hodnota 38 ± 6% (medián 41%, 28–48) a po rehabilitaci došlo ke zvýšení na hodnotu 45 ± 6% (medián 47%, 36–56, p < 0,007). Rozdíl v hodnotách EF před a po rehabilitaci byl mezi oběma podskupinami statisticky významný (p < 0,0001).
Spiroergometrie
Ukazatelé zátěžového vyšetření jsou shrnuty v tab. 2. Z tab. 2 je patrné, že vrcholový příjem kyslíku je před rehabilitací významně nižší v podskupině se sníženou EF LK. Obě podskupiny vykazují statisticky významné zlepšení pVO2 po rehabilitaci (p < 0,0001), přičemž v tomto ukazateli není statisticky významný rozdíl mezi podskupinami. Taktéž tolerance zátěže je po rehabilitaci v obou podskupinách významně zvýšena oproti vstupním hodnotám (p < 0,0001) a opět bez statisticky významného rozdílu mezi podskupinami pacientů.
Tab. 2. Změny zátěžových ukazatelů (spiroergometrie). 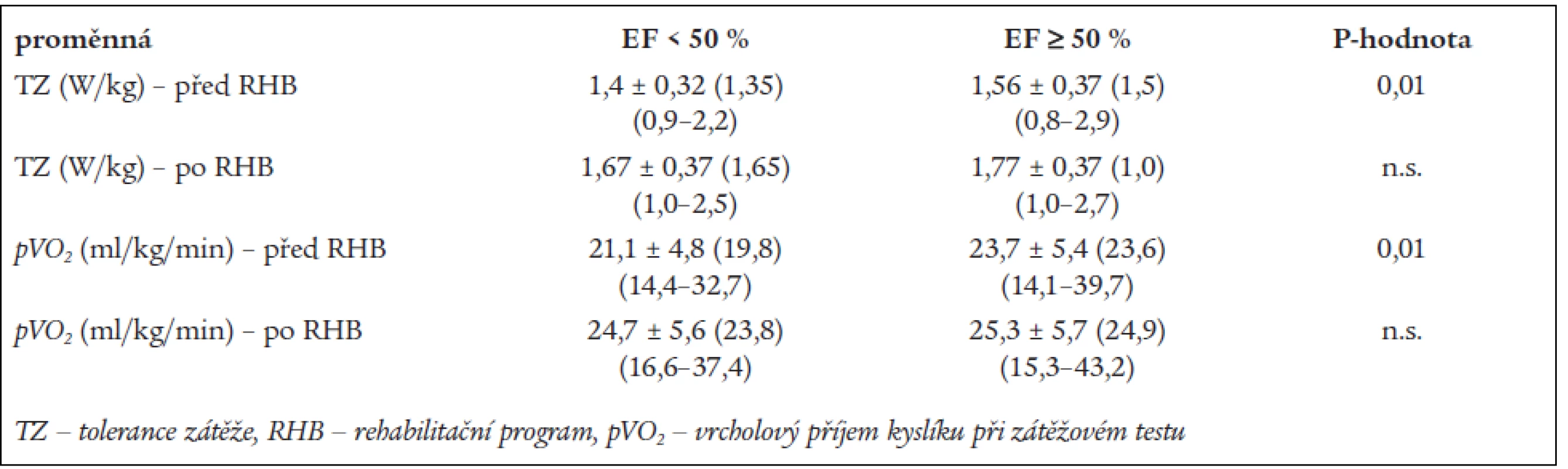
Aerobní cvičení
V tab. 3 jsou shrnuty hodnoty tréninkové zátěžové tolerance na úrovni TF odpovídající 60% pVO2 na závěr rehabilitačního programu, hodnoty TF a TK. Z tab. 3 vyplývá, že není patrný signifikantní rozdíl v toleranci zátěže, se kterou nemocní ukončili program, pacienti s normální EF mají vyšší tlakovou odpověď na aerobní kondiční cvičení.
Tab. 3. Oběhové parametry při aerobním tréninku na závěr rehabilitačního programu. 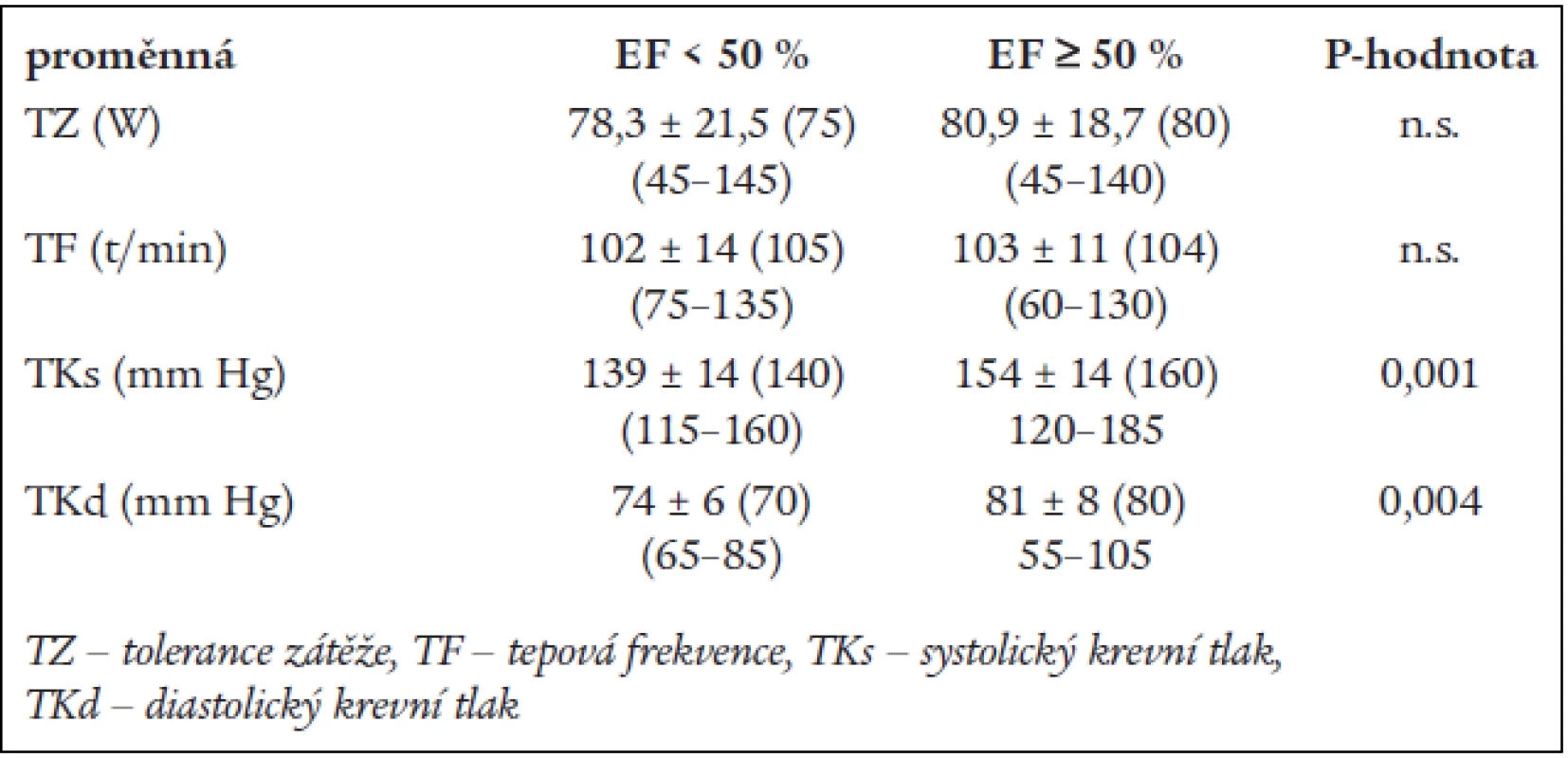
Silové cvičení
V tab. 4 jsou srovnány hodnoty zátěže v kilogramech u jednotlivých cviků a celková síla na začátku a konci rehabilitačního programu. Z tab. 4 je patrné, že v obou podskupinách dochází v významnému zlepšení celkové síly (A + B + C). Hodnota celkové síly nebyla před rehabilitací u nemocných se sníženou EF významně nižší, byl jen naznačen trend k nižší hodnotě (p < 0,09). Po ukončení rehabilitace nebyl rozdíl mezi skupinami nemocných, přičemž nárůst celkové síly vyjádřený v absolutní i relativní hodnotě je dokonce statisticky významně vyšší v podskupině se sníženou EF LK (graf).
Tab. 4. Srovnání jednotlivých cviků silového cvičení a celkové síly v podskupinách. 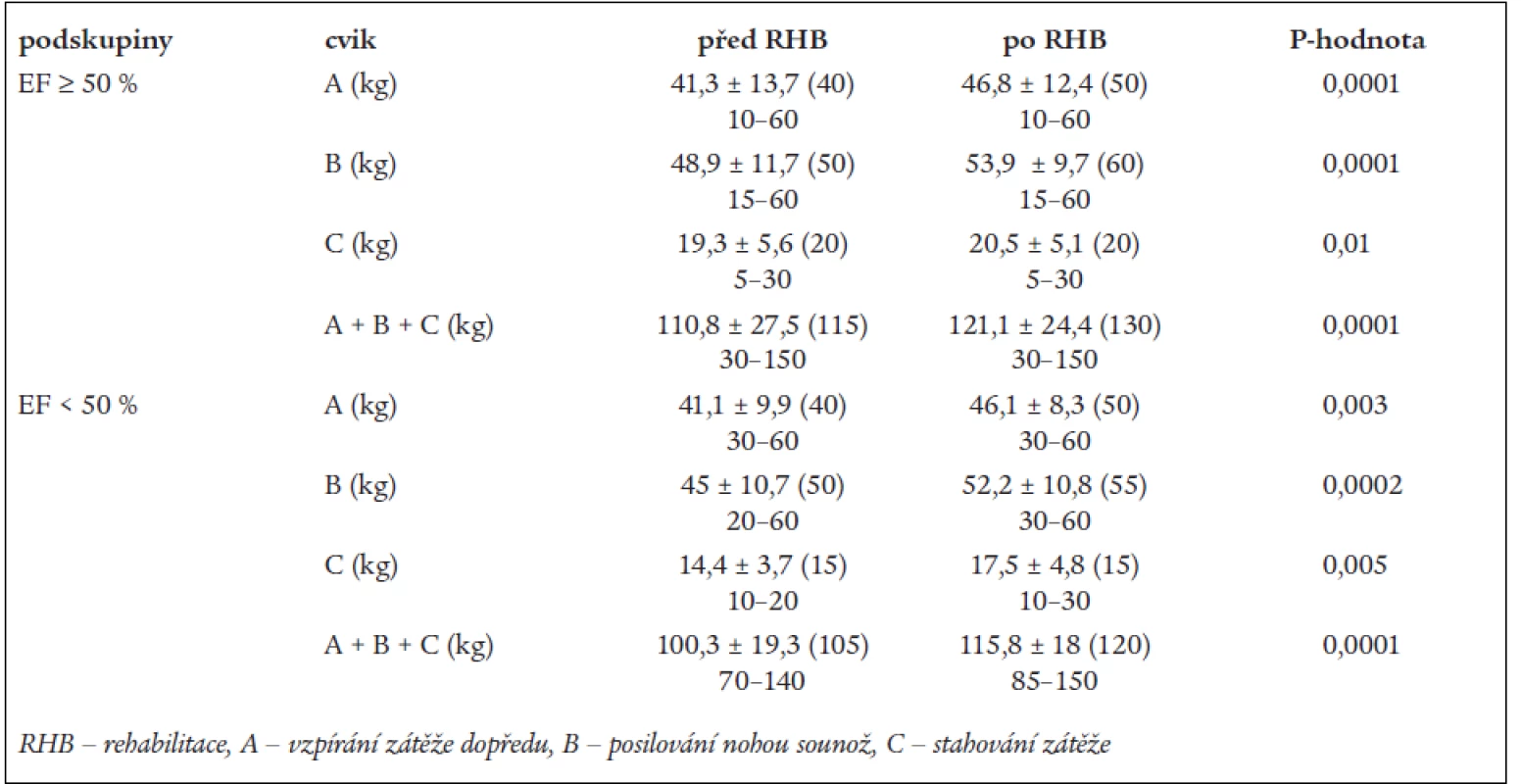
Graf. Srovnání změny celkové síly po rehabilitaci v podskupinách. 
Hodnoty jsou vyjádřeny mediánem zvýšení celkové síly k kilogramech a v % přírůstku oproti vstupním hodnotám. Vedlejší účinky silového cvičení
Během provádění silových cviků jsme nezaznamenali u žádného nemocného výskyt závažných poruch srdečního rytmu ani výskyt stenokardií. Všichni nemocní absolvovali předepsaná cvičení po celou dobu rehabilitačního programu. U nemocných se sníženou EF bylo silové cvičení ukončeno na úrovni 50% 1-RM.
Regresní analýza dat
Nalezli jsme významný negativní vztah mezi celkovou silou a věkem nemocných před rehabilitací (r = –0,43, p < 0,003) i po jejím ukončení (r = –0,41, p < 0,01). Vztah mezi ejekční frakcí LK, pVO2 a celkovou silou byl volný. Vztah mezi EF a pVO2 byl pro celou skupinu volný a nesignifikantní. Totéž platilo i pro analýzu v podskupině se sníženou EF.
Diskuse
Aerobní cvičení je integrovanou součástí rehabilitační péče o nemocné po srdečním infarktu. Je prokázáno, že vede ke zlepšení zátěžové tolerance, fyzické kondice, k ústupu anginózních potíží, dušnosti a únavy. Pozitivně ovlivňuje kvalitu života nemocného, vede ke změnám životního stylu a podílí se na eliminaci rizikových faktorů v rámci sekundární prevence ICHS. Fyzický trénink po IM snižuje kardiovaskulární morbiditu a mortalitu až o 20–25% [24].
Jedním z hlavních cílů rehabilitace po srdečním infarktu je umožnit pacientovi pokud možno co nejrychlejší návrat do denního života, zvládnout fyzickou aktivitu odrážející jeho pracovní, osobní, sportovní zátěž. Řada denních aktivit je spjata s fyzickou činností, u níž dominuje silová práce. Již v roce 1970 poukázali Clausen et al na potřebu upravit rehabilitační cvičení u pacientů se srdečními chorobami tak, aby opravdu odráželo fyzické aktivity jejich běžného dne [5].
Zařazení silového tréninku do rehabilitačního procesu kardiaků je doporučováno až v posledních 10–12 letech. Do guidelines ASCM (American College of Sport Medicine) a AHA (American Heart Association) byl zařazen teprve v roce 1990. Aerobní cvičení, které významně pozitivně ovlivní kardiopulmonální a oběhové funkce, ovlivní taktéž rizikové faktory ICHS. Silové cvičení vede ke zvýšení svalové síly, vytrvalosti a svalové hmoty. Má obdobný pozitivní vliv jako aerobní cvičení na zvýšení denzity kostní tkáně, ovlivňuje pozitivně metabolizmus glukózy, vede ke snížení procenta tukové tkáně, pozitivně ovlivňuje spektrum lipidů v séru, zvyšuje bazální metabolizmus [23].
Silové cvičení významně neovlivní klidovou tepovou frekvenci, systolický a diastolický krevní tlak. Silové cvičení o střední až vyšší intenzitě prováděné 2–3krát týdně vede ke zvýšení pVO2 a doby trvání aerobní zátěže prováděné na kole nebo chůzí. Toto zvýšení bylo prokázáno jak v kombinaci s aerobním cvičením, tak i při samostatném silovém cvičení [2,3,9,21,26].
Problémem byla otázka bezpečnosti silového cvičení u nemocných se srdečním onemocněním, především po IM. Vlastní „izometrická zátěž“ vede k významnému zvýšení systolického i diastolického tlaku, mírnému zvýšení TF a stažlivosti LK. Periferní cévní rezistence se podstatně nemění, mírně se zvýší minutový srdeční objem na úkor vyšší TF, zvýší se index srdeční práce. V důsledku zvýšení systolického tlaku se zvyšuje i endsystolické napětí stěny LK, zvyšuje se spotřeba kyslíku myokardem. Tyto změny mají kontinuální lineární charakter v průběhu trvání zátěže a upravují se rychle ad integrum po jejím přerušení. U nemocných se stenózou koronární tepny test vyvolá regionální poruchu funkce LK v oblasti zásobené touto tepnou, a proto byl dlouho používán jako jednoduchý diagnostický test ICHS ve spojení s invazivními i neinvazivními vyšetřovacími metodami [15]. Náhlé hemodynamické změny a změny krevního tlaku mohou vyvolat regionální ischemii, anginu pectoris a arytmie. Rizikovou skupinu představují především nemocní po předním Q-infarktu [19].
Bezpečnost silového tréninku u zdravých jedinců prokázal Gordon et al. Ve skupině 6 653 zdravých jedinců ve věku 20–69 let, kteří cvičili na úrovni 1-RP, nevyvolalo silové cvičení srdeční komplikace [12]. Bezpečnost silového cvičení byla prokázána i u nemocných s mírnou hypertenzí [13].
U nemocných se srdečním onemocněním je silové cvičení prováděno obvykle na úrovni 40–60% 1-RM. Invazivním měřením krevního tlaku bylo zjištěno, že při této zátěži se hodnoty TK pohybují v akceptovatelných rozmezích, a jeho výkyvy by tedy neměly mít vliv na vznik arytmií [14].
Zvýšení svalové síly a výkonnosti se výrazněji neliší, použijeme-li cvičení s vyšší intenzitou (80% 1-RM) oproti středně těžké zátěži (30–40% 1-RM). Při této zátěži je též nižší dvojprodukt (systolický tlak × TF) oproti aerobnímu cvičení. V důsledku zvýšení diastolického krevního tlaku při silovém cvičení, snížení žilního návratu, a tím zmenšení enddiastolického objemu LK může naopak dojít ke zlepšení prokrvení subendokardiální oblasti, což může vysvětlovat minimální výskyt ischemických změn či arytmií při takto definovaném silovém cvičení [9].
Rizikovou skupinu pro silové cvičení představují nemocní se systolickou dysfunkcí LK. Daub et al nezařadili z bezpečnostních důvodů do silového cvičení nemocné s EF pod 35% nebo s nálezem rozsáhlého Q-infarktu přední stěny dle EKG [6]. Na druhé straně Adams et al provedli silové cvičení u nemocných po IM s výrazně sníženou EF 24 ± 8%. Dokázali, že tito nemocní profitují ze silového cvičení stejně jako skupina se středním a nízkým rizikem na úrovni střední až vysoké intenzity cvičení (60–80% 1–RM) a bez přítomnosti vedlejších nežádoucích účinků [1].
V naší práci jsme u nemocných se sníženou EF z bezpečnostních důvodů začali na nižším stupni silového zatížení a při dobré toleranci jsme dosáhli srovnatelného maxima 50% 1-RM se skupinou s normální EF. Nález nižší celkové síly, i když nesignifikantní, u nemocných se sníženou EF LK před rehabilitací nedáváme do přímé souvislosti se srdečním postižením. Tomu odpovídá i zjištěný vztah jen k věku pacientů. Domníváme se, že velkou roli ve stanovení a interpretaci tohoto ukazatele hraje i fyzická kondice pacientů do období před vznikem akutní koronární příhody. Důležitý je ale fakt, že silové cvičení přispělo k výraznému zvýšení celkové síly těchto pacientů a výsledek po rehabilitaci je srovnatelný s pacienty bez poškozené funkce LK. Stejný výsledek je patrný i u vyhodnocení aerobního cvičení.
Ne u všech nemocných zachytíme projevy ischemie při silovém cvičení EKG-monitorováním, stejně tak nemusí dojít ke vzniku anginy pectoris. Ischemie může být němá nebo dojde jen k vyvolání poruchy kinetiky stěny LK, která výše uvedeným příznakům předchází a klinické projevy by se objevily až při vyšším zatěžování. Proto je nezbytné před zahájením silového cvičení provést zátěžový test. Pacienti, kteří při testu dosáhnou více než 5–6 MET (metabolických ekvivalentů) bez průkazu ischemie, závažné arytmie či dysfunkce LK, mohou být zařazeni do silového tréninku [23]. V naší studii jsme identifikovali 10% nemocných, kteří měli při zátěžovém testu projevy ischemie myokardu. U všech byla podle charakteru koronarografického nálezu indikována konzervativní léčba a při zátěžovém testu bylo dosaženo > 5 MET. Tito nemocní absolvovali kombinovaný trénink bez problémů.
Vyšší věk není limitací pro silové cvičení po srdečním infarktu. Bylo prokázáno, že u nemocných ve věku nad 60 let a především u starších žen je silové cvičení vhodné a tato forma rehabilitace je bezpečná [8,17,25].
Důležitým aspektem je doba, kdy můžeme s časným tréninkem v rámci fáze II po propuštění z nemocnice začít. V tomto směru nemusí být naše výsledky plně srovnatelné se zahraničními, kde citované práce mají často charakter pilotních studií. V našem případě se stal ambulantní řízený rehabilitační program standardním přístupem v léčbě a sekundární prevenci ICHS u nemocných po akutním IM léčeném v naší nemocnici. Medián doby od vzniku akutního IM po zařazení do rehabilitace na našem pracovišti se nachází na dolní hranici ve srovnání s jinými pracovišti, kde se pohybuje mnohdy z „bezpečnostních“ důvodů od 4 až 6 týdnů až po několik měsíců po akutní koronární příhodě. Tento fakt ovlivňuje i skutečnost, že v mnoha případech pacienti nerehabilitují v centrech pod odborným vedením, ale v domácím prostředí [11]. I tak považujeme medián doby zařazení do rehabilitace za poměrně dlouhý, ale odráží jen naše kapacitní možnosti a dobu potřebnou na provedení vstupních testů. Zahájení silového cvičení za 14 dní po úvodním samostatném aerobním cvičení považujeme za optimální. Výjimku tvoří nemocní po kardiochirurgickém zákroku, které posuzujeme individuálně a silová cvičení odkládáme s ohledem na proces hojení po sternotomii a přítomnost dalších pooperačních komplikací.
Mezi kontraindikace silového cvičení patří nestabilní angina pectoris, srdeční selhávání ve funkční klasifikaci NYHA IV, projevy ischemie a dysfunkce LK při zátěži menší než 5 MET, klidová hypertenze s hodnotami TK ≥ 160/100 mm Hg, přítomnost závažných arytmií [23]. U nemocných s tlakovou hyperreakcí při izometrické zátěži (TK ≥ 180/120 mm Hg) a normálními hodnotami TK v klidu silové cvičení provádíme ale na hodnotách nižších 30% 1-RM. Další postup je taktéž závislý na úpravě antihypertenzní léčby [17].
Závěr
Závěrem můžeme konstatovat, že kombinovaný aerobní trénink se silovými prvky u nemocných po akutním infarktu je bezpečný. Je vhodný i u nemocných se sníženou ejekční frakcí. Nevedl ke vzniku nežádoucích hemodynamických změn, arytmií a stenokardií. Byl dobře tolerován u nemocných s prokázanou ischemií myokardu zátěžovým testem. Snažíme se zahájit rehabilitační program do 3–4 týdnů po vzniku srdečního infarktu a silová cvičení zařazujeme po 14 dnech aerobního tréninku.
Práce vznikla za podpory výzkumného záměru Ministerstva zdravotnictví České republiky 00065269705
doc. MUDr. Lubomír Elbl, CSc.
www.fnbrno.cz
e-mail: lelbl@fnbrno.cz
Doručeno do redakce: 24. 2. 2004
Přijato po recenzi: 2. 4. 2004
Zdroje
1. Adams KJ, Barnard KL, Swank AM et al. Combined High-Intensity Strength and Aerobic Training in Diverse Phase II Cardiac Rehabilitation Patients. J Cardiopulmonary Rehabil 1999; 19 : 209–215.
2. Ades PA, Ballor DL, Ashikaga T et al. Weight training improves walking endurance in healthy elderly persons. Ann Intern Med 1996; 124 : 568–572.
3. Beniamini Y, Rubenstein JJ, Faigenbaum AD et al. High-Intensity Strength Training of Patients Enrolled in an Outpatient Cardiac Rehabilitation Program. J Cardiopulmonary Rehabil 1999; 19 : 8–17.
4. Cannistra LB, Davidoff R, Picard MH et al. Moderate-High Intensity Exercise Training after Myocardial infarction: Effect on Left Ventricular Remodeling. J Cardiopulmonary Rehabil 1999; 19 : 373–380.
5. Clausen JP, Trap-Jensen J, Lassen NA. The effects of training on the heart rate during arm and leg exercise. Scand J Clin Lab Invest 1970; 26 : 295–301.
6. Daub WD, Knapik GP, Black WR. Strenght training early after myocardial infarction. J Cardiopulmonary Rehabil 1996; 16 : 100–108.
7. DeLagardelle C, Feiereisen P, Autier P et al. Strength/endurance training versus endurance training in congestive heart failure. Med Sci Sports Exerc 2002; 34 : 1868–1872.
8. Fragnolli-Mum K, Savage PD, Ades PA. Combined Resistive–Aerobic Training in Older Patients With Coronary Artery Disease Early After Myocardial Infarction. J Cardiopulmonary Rehabil 1998; 18 : 416–420.
9. Franklin BA, Bonzheim K, Gordon S et al. Resistance training in cardiac rehabilitation. J Cardiopulmonary Rehabil 1991; 11 : 99–107.
10. Giannuzzi P, Tavazzi L, Temporelli PL et al. Long-Term Physical Training and Left Ventricular Remodeling After Anterior Myocardial Infarction: Results of the Exercise in Anterior Myocardial Infarction (EAMI) Trial. J Am Coll Cardiol 1993; 22 : 1821–1829.
11. Giannuzi P, Saber H, Bjornstad H et al. Secondary prevention through cardiac rehabilitation. Eur Heart J 2003; 24 : 1273–1278.
12. Gordon NF, Kohl HV, Pollock ML et al. Cardiovascular safety of maximal strength testing in healthy adults. Am J Cardiol 1995; 76 : 851–853.
13. Harris KA, Holly RG. Physiological response to circuit weight training in borderline hypertensive subjects. Med Sci Sport Exerc 1987; 19 : 246–252.
14. Haslam DR, McCarteny SN, McKelvie RS et al. Direct measurement of arterial blood pressure during formal weightlifting in cardiac patients. J Cardiopulmonary Rehabil 1988; 8 : 213–225.
15. Chaloupka V, Žák J. Význam izometrické zátěže v echokardiografické diagnostice ischemické choroby srdeční. Vnitř Lék 1984; 30 (4): 313–323.
16. Chaloupka V, Vaněk P, Juráň F et al. Nemocniční, posthospitalizační a lázeňská rehabilitace u nemocných s ICHS. Cor Vasa 1998; (40): K243–K251.
17. Chaloupka V, Elbl L, Nehyba S. Silový trénink u nemocných po infarktu myokardu. Vnitř Lék 2000; 46 (12): 829–834.
18. Chaloupka V, Elbl L, Nehyba S et al. Pohybová aktivita u nemocných s kardiovaskulárním onemocněním. Kardiol Rev 2003; 1 : 16–19.
19. Jugdutt BI, Michorowski BL, Kappagoda CT et al. Exercise training after Q wave myocardial infarction: Importance of regional ventricular function and topography. J Am Coll Cardiol 1988; 12 : 362–372.
20. Jančík J, Svačinová H, Dobšák P et al. Kombinovaný trénink u nemocných se systolickou dysfunkcí levé komory srdeční. Vnitř Lék 2003; 4 (49): 280–284.
21. McCartney N, McKelvie RS, Martin J et al. Weight-training-induced attenuation of the circulatory response of older males to weight lifting. J Appl Physiol 1993; 74 : 1056–1060.
22. Nehyba S, Chaloupka V, Elbl L. Rehabilitační péče o nemocné po prodělaném srdečním infarktu. Prakt Lék 1995; 6 (75): 272–273.
23. Pollock ML, Franklin BA, Balady GJ et al. Resistance Exercise in Individuals With and Without Cardiovascular Disease. Bebefits, Rationale, Safety, and Prescription. An Advisory From the Committee on Exercise, Rehabilitation, and Prevention, Council on Clinical Cardiology, American Heart Association. Circulation 2000; 101 : 828–833.
24. Oldridge NB, Guyatt GH, Fischer ME et al. Cardiac rehabilitation after myocardial infarction: combined experience of randomised clinical trials. JAMA 1988; 260 : 954–950.
25. Parker DN, Hubter GR, Treuth MS et al. Effects of Strength Training on Cardiovascular Responses During a Submaximal Walk and a Weight-Loaded Walking Test in Older Females. J. Cardiopulmonary Rehabil 1996; 16 : 56–62.
26. Stewart KJ, McFarland LD, Weinhofer JJ et al. Safety and efficacy of weight training soon after acute myocardial infarction. J. Cardiopulmonary Rehabil 1998; 18 : 37–44.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Slovo nakladateleČlánek Odkaz sira Williama OsleraČlánek Jan Lebl, Štěpánka Průhová et al. Abeceda diabetu. Příručka pro děti, mladé dospělé a jejich rodičeČlánek MyokarditidyČlánek ÚvodníkČlánek Metabolický syndrom a sympatický nervový systém: je obstrukční spánková apnoe klíčem k pochopení?Článek Hypertenze a hyperurikemie
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2005 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Co dělat při intoleranci statinů?
-
Všetky články tohto čísla
- Slovo nakladatele
- Jaterní postižení při deficitu alfa−1−antitrypsinu
- Akutní myokarditida manifestující se obrazem transmurálního infarktu myokardu provázená akutním renálním selháním
- Význam centralizace péče o nemocné s akutním krvácením do horní části trávicího traktu
- Za profesorem MUDr. Stanislavem Havelkou
- Otevřený dopis Jiřímu Vorlíčkovi
- Bioekvivalenční studie s novými antihypertenzivy
- Komentář k Doporučení American Heart Association/American College of Cardiology Foundation pro léčbu warfarinem
- Odkaz sira Williama Oslera
- Jan Lebl, Štěpánka Průhová et al. Abeceda diabetu. Příručka pro děti, mladé dospělé a jejich rodiče
- Jiří Vítovec, Jindřich Špinar et al. Farmakoterapie kardiovaskulárních onemocnění
- Petr Cetkovský et al. Intenzivní péče v hematologii
- Individuální výběr nemocných pro silový trénink po akutním infarktu myokardu se sníženou ejekční frakcí levé komory
- Viktor Chrobok, Jaromír Astl, Pavel Komínek et al. Tracheostomie a koniotomie, techniky, komplikace a ošetřovatelská péče
- Anna Jedličková. Antimikrobiální terapie v každodenní praxi
- David Cibula, Luboslav Stárka, Jana Vrbíková et al. Syndrom polycystických ovarií
- Tomáš Skalický, Vladislav Třeška, Jiří Šanjdauf et al. Chirurgie jater
- Zpráva o kurzu Hot topics in internal medicine, Alicante, Španělsko, 16.–22. 10. 2004
- Myokarditidy
- Myelodysplastický syndrom v novém tisíciletí. Jak klasifikovat a jak léčit nemocné?
- Efekt a tolerancia kombinovanej liečby fludarabinom s cyklofosfamidom u chorých s chronickou lymfocytovou leukémiou
- Naše zkušenosti s novou organizací péče o nemocné s akutním krvácením do horní části trávicího traktu
- Silový trénink u nemocných po akutním infarktu myokardu se sníženou ejekční frakcí levé komory srdeční
- Úvod do problematiky metabolického syndromu
- Metabolický syndrom a sympatický nervový systém: je obstrukční spánková apnoe klíčem k pochopení?
- Diabetes mellitus a metabolický syndrom
- Hypertenze jako součást metabolického syndromu
- Úvodník
- Obezita a metabolický syndrom
- Dyslipidemie u metabolického syndromu
- Hypertenze a hyperurikemie
- Role pohybové léčby a tělesné zdatnosti v prevenci a léčbě metabolického syndromu
- Akutní infarkt myokardu u pacienta s anamnézou infekční endokarditidy
- Extramedulární plazmocytom štítné žlázy - vzácná příčina solitární uzlové strumy s hypertyreózou
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Jaterní postižení při deficitu alfa−1−antitrypsinu
- Myelodysplastický syndrom v novém tisíciletí. Jak klasifikovat a jak léčit nemocné?
- Hypertenze a hyperurikemie
- Myokarditidy
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



