-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Zmeny v lipoproteínovom spektre pri končatinovo- cievnej ischemickej chorobe
Changes in lipoprotein spectrum in patients with the diagnosis of extremito-vascular ischemic disease
New method of lipoprotein determination on polyacrylamid gel with Lipoprint LDL system quantifies non atherogenic and atherogenic plasma lipoproteins, including small dense LDL, the potent atherogenic lipoprotein subpopulations. According to majority of non atherogenic versus atherogenic lipoprotein in the whole lipoprotein spectrum, this method distinguishes a non atherogenic lipoprotein profile phenotype A from an atherogenic lipoprotein profile phenotype B. Definitely, the contribution of this method is focusing on the atherogenic lipoprotein profile phenotype B in 80% of patients with an extremito ‑ vascular ischemic disease and on the existence of control subgroup of normolipemic subjects with an atherogenic lipoprotein profile (7% of probands of control group). These persons represent a risk population. Till now, the facilities for identifying of these “normolipemic persons at risk” are limited.
Key words:
atherogenic lipoproteins – atherogenic vs non atherogenic lipoprotein profile
Autoři: S. Oravec; A. Dukát; P. Gavornik; M. Čaprnda; O. Reinoldová
Působiště autorů: II. interná klinika Lekárskej fakulty UK Bratislava, Slovenská republika, prednosta prof. MU Dr. Andrej Dukát, CSc., FESC
Vyšlo v časopise: Vnitř Lék 2010; 56(6): 620-623
Kategorie: 65. narozeniny vedoucího redaktora časopisu Vnitřní lékařství prim. MUDr. Petra Svačiny
Souhrn
Metóda delenia lipoproteínov na polyakrylamidovom géli Lipoprint LDL systém kvantifikuje neaterogénne a aterogénne lipoproteíny plazmy, včítane malých denzných LDL, silne aterogénných lipoproteínov. Podľa prevahy neaterogénnych alebo aterogénnych lipoproteínov v lipoproteínovom spektre metóda identifikuje neaterogénny lipoproteínový profil fenotyp A a aterogénny lipoproteínový profil fenotyp B. Prínosom metódy je upozornenie na existenciu aterogénneho lipoproteínového profilu fenotyp B u 80 % pacientov s končatinovo ‑ cievnou ischemickou chorobou, ale aj na jestvovanie kontrolnej podskupiny normolipemikov s aterogénnym lipoproteínovým profilom (7 % probandov kontrolnej skupiny). Ide o rizikovú populáciu. Možnosti identifikácie týchto „rizikových normolipemikov“ sú zatiaľ obmedzené.
Kľúčové slová:
aterogénne lipoproteíny – aterogénny vs neaterogénny lipoproteínový profilÚvod
V ostatnom čase nanovo narastá záujem lipidológov a klinických pracovníkov o identifikovanie lipoproteínových entít v lipoproteínovom spektre plazmy, ktorých prítomnosť v relevantných množstvách poškodzuje endotelové bunky, navodzuje dysfunkciu endotélia a spolu iniciuje spustenie multifaktoriálneho procesu degeneratívnych zmien v cieve, čoho dôsledkom je vznik ateromatóznych cievnych plakov. Ide o aterogénne lipoproteíny [1]. Ich početné zastúpenie v plazme charakterizuje lipoproteinového spektrum, fenotyp B [5,6]. V ňom sa nachádzajú malé denzné lipoproteíny nízkej hustoty (mdLDL) vo zvýšených koncentráciách a spoluúčastnia sa pri vzniku ischemického cievneho poškodenia [2 – 4]. Pri nízkom zastúpení aterogénnych lipoproteínov v lipoproteinovom spektre dostávame obraz neaterogénneho lipoproteínového profilu, fenotyp A [5,6].
Míľnikom v analýze a využitia v dia-gnostike porúch metabolizmu lipoproteinov sa stala elektroforetická metóda delenia lipoproteínov na polyakrylamidovom géli (PAGE), systémom Lipo-print LDL [7 – 10]. Umožňuje analyzovať 12 lipoproteínových subpopulácií: VLDL, IDL 1 – 3, LDL 1 – 7, HDL.
Elektroforéza lipoproteínov
-
kvantitatívne vyhodnocuje:
a) aterogénne (VLDL, IDLc IDLb a LDL 3 – 7, tzv. malé denzné LDL)
b) neaterogénne lipoproteínové entity (IDLa, HDL)
c) lipoproteíny s neistou aterogenitou (LDL 1 – 2) - určuje neaterogénny vs aterogénny lipoproteínový profil, fenotyp A a fenotyp B
Aterogénny lipoproteínový profil je charakterizovaný prítomnosťou aterogénnych lipoproteínov veľmi nízkej hustoty (VLDL), intermediárnej hustoty (IDLc a IDLb) a malých denzných lipoproteínov nízkej hustoty (mdLDL) vo vysokých koncentráciách. V prípade tzv. malých denzných LDL (tab. 1), „small dense LDL“, ide o silne aterogénne subpopulácie LDL [1], ktoré migrujú v oblasti LDL 3 – 7. Ako ich názov naznačuje, sú menšie, s priemerom menším než 26,5 nm, resp. 265 Angströmov a flotujú v hustotnom rozmedzí d = 1,048 – 1,065 g/ ml, t.j. vyššom než LDL 1, LDL 2. Na deliacom polyakrylamidovom géli (PAG) ich možno identifikovať ako jemné pásy na anodickej strane gélu, hneď za HDL frakciou, ktorá putuje na čele delených lipoproteínov.
Pacienti a metódy
V našej klinickej štúdii bolo vyšetrených 100 pacientov s novozistenou, klinicky manifestnou diagnózou končatinovo - cievnej ischemickej choroby (KICH). Súbor tvorilo 55 mužov a 45 žien, (priemerný vek žien 52,5 ± 14,0, priemerný vek mužov 56,0 ± 11,0) v klaudikačom štádiu C2a, proximálny typ (AP), prvé štádium (P1) s dyslipidémiou. Pacienti boli exfajčiari.
Diagnostika ochorenia sa vykonala na základe anamnézy, základného a funkčného fyzikálneho vyšetrenia (polohový námahový test podľa Ratschowa v modifikácii podľa Linharta). Z pomocných vyšetrení sa určoval členkovo - brachiálny index [11,12].
V plazme sa testovala koncentrácia celkového cholesterolu (TC), triacylglycerolov (TAG), určilo kvantitatívne zastúpenie aterogénnych a neaterogénnych lipoproteínov a fenotyp lipoproteínového profilu: neaterogénny fenoty A vs aterogénny fenotyp B.
Kontrolnú skupinu tvorilo 150 normolipemických probandov bez klinických a laboratórnych známok ochorenia kardiovaskulárneho systému.
Krv sa odobrala po 12 - hodinovom lačnení a získala sa EDTA - K2 plazma, ktorá sa použila na analýzu bioche-mických parametrov.
Celkový cholesterol sa analyzoval enzymatickou metódou CHOD - PAP a stanovila sa jeho koncentrácia v plazme (Roche, SRN), triacylglyceroly sa analyzovali enzymatickou metódou a stanovila ich koncentrácia v plazme (Roche, SRN).
K určeniu lipoproteínového profilu sa použil System Lipoprint LDL, firma Quantimetrix, CA, USA, ktorý simultánne analyzoval 12 lipoproteínových tried a ich subpopulácií. Koncentrácia lipoproteínov systémom Lipoprint LDL sa vyjadrila obsahom cholesterolu v jednotlivých lipoproteínových triedach, resp. entitách: napr. VLDL - cholesterol. Prínosom metódy je kvantitatívne hodnotenie aterogénnych lipoproteínov plazmy, včítane malých denzných LDL (mdLDL), ktorú predstavujú subpopulácie LDL 3 – 7.
Prostanoidy: Prostacyklín (PGI2), resp. jeho chemicky stabilná forma, 6 - keto - PGF1α, a tromboxan A2 (TxA2),resp. jeho chemicky stabilná forma, tromboxan B2 (TxB2), sa analyzovali v plazme, metódou ELISA (DGR, USA).
V našej štúdii sa zaviedol výpočet Skóre Aterogénneho Rizika (SAR), čo predstavuje pomer neaterogénnych a aterogénnych lipoproteínov plazmy. SAR nad 10,8 deklaruje neaterogénne lipoproteínové spektrum, hodnota pod 9,8 aterogénne lipoproteínové spektrum. Hodnota medzi 9,8 – 10,8 je interval šedej zóny.
K štatistickému vyhodnoteniu nameraných hodnôt sa použil nepárový Studentov t test.
Cieľ práce
Zmapovať zastúpenie aterogénnych lipoproteínov, určiť fenotyp lipoproteínového profilu u pacientov s diagnózou končatinovo - cievnej ischemickej choroby (KICH) a analýzou prostanoidov v plazme hodnotiť integritu cievneho endotelu.
Výsledky
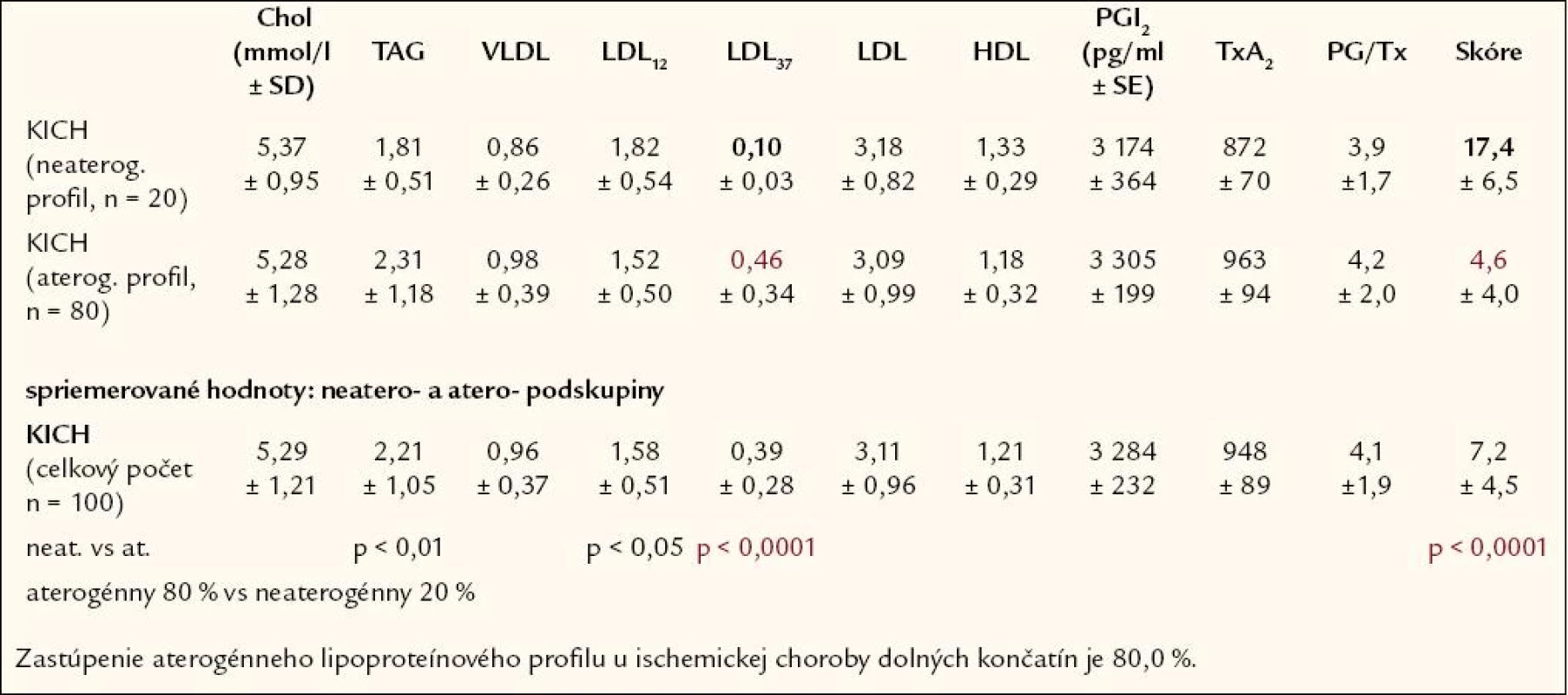
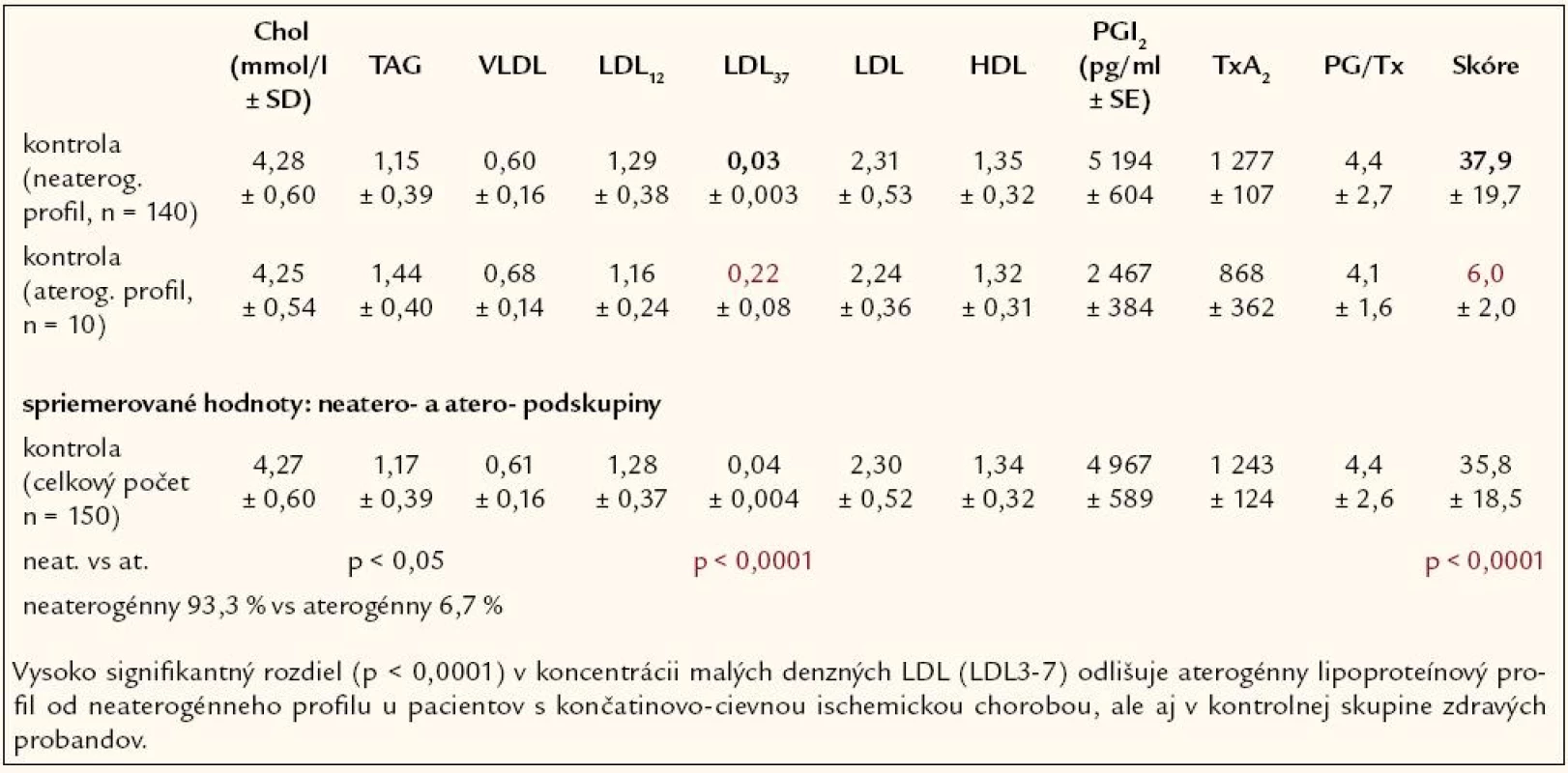
Hodnoty biochemických parametrov neaterogénny vs aterogénny lipopro-teínový profil, u pacientov s KICH popisuje tab. 2 a u kontrolnej skupiny tab. 3.
Vysoko signifikantný rozdiel (p << 0,0001) v koncentrácii malých denz-ných LDL (LDL3 - 7) odlišuje aterogénny lipoproteínový profil od neaterogénneho profilu u pacientov s končatinovo - cievnou ischemickou chorobou, ale aj v kontrolnej skupine zdravých probandov (tab. 4).
Tab. 4. Hodnoty biochemických parametrov, kontrolná skupina vs pacienti s končatinovo- cievnou ischemickou chorobou. 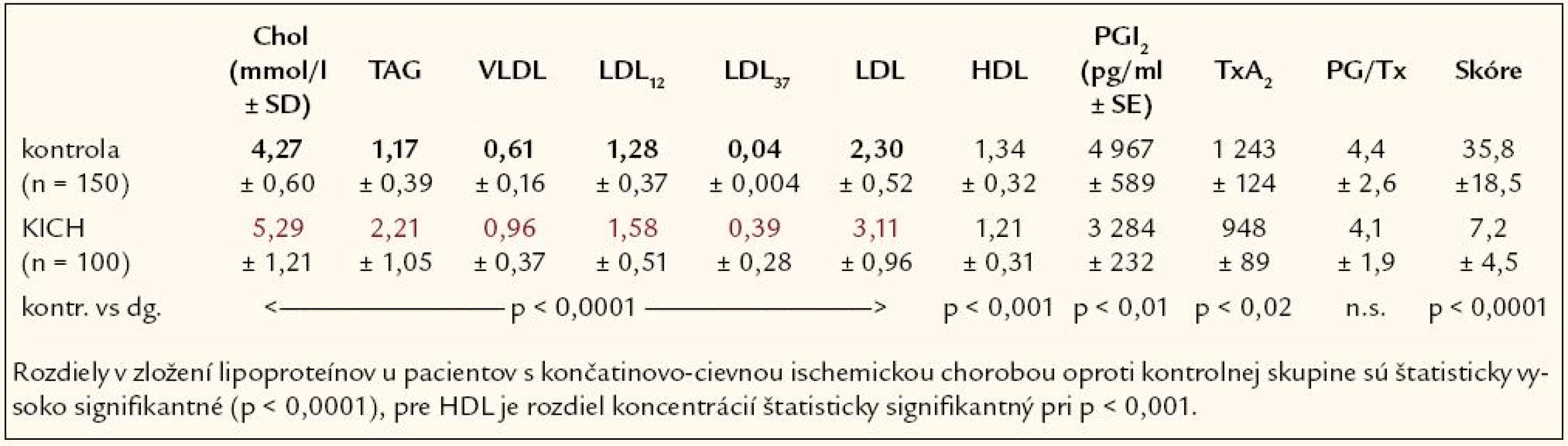
Rozdiely v zložení lipoproteínov u pacientov s končatinovo - cievnou ischemickou chorobou oproti kontrolnej skupine sú štatisticky vysoko signifikantné (p < 0,0001), pre HDL je rozdiel koncentrácií štatisticky signifikantný pri p < 0,001.
Diskusia
Nová diagnostická metóda elektroforetického delenia lipoproteínov na polyakrylamidovom géli identifikovala aterogénny lipoproteínový profil u 80 % pacientov s končatinovo - cievnou ischemickou chorobou (KICH), čo je v súlade s klinickým obrazom silnej aterogénnej aktivity u vyšetrovaných osôb s KICH [13,14]. Vysoko signifikantné rozdiely medzi kontrolnou skupinou a skupinou pacientov s KICH zaznamenávame pri všetkých lipidových a lipoproteínových parametroch.
Metóda prekvapivo odhaľuje aj prítomnosť aterogénneho profilu lipoproteínov u kontrolnej skupiny zdravých probandov a rozdeľuje kontrolnú skupinu na dve podskupiny:
a) s aterogénnym
b) s neaterogénnym lipoproteínovým profilomTo, čo ich odlišuje, je rozdiel v koncentrácii mdLDL, ktorý je vysoko štatisticky signifikantný (p < 0,0001). Temer 7% podskupina zdravých probandov kontrolnej skupiny s aterogénnou konštelácie lipoproteínov dáva podnet k sprís-neniu kritérií výberu probandov pri tvorbe kontrolnej skupiny.
V predkladanej štúdii sa analyzovala koncentrácia prostacyklínu (PGI2) a tromboxanu A2 (TxA2) v plazme, ako index miery dysfunkcie endotelu [15]. Intaktný endotel je charakterizovaný neporušenou endotelovou sekréciou prostanoidov, vyjadrenou pomerom molárnej koncentrácie PGI2/ TxA2, a predstavuje hodnotu 1,5 a vyššiu. Hodnoty koncentrácie prostacyklínu a tromboxanu kontrolnej skupiny a pacientov s KICH sú zhrnuté v tab. 2 – 4. Endotelová sekrécia prostanoidov u pacientov s KICH oproti kontrolnej skupine je znížená (p < 0,01, resp. p < 0,02) a potvrdzuje dysfunkciu endotelu u vyšetrovaných pacientov. Rovnakou mierou je porušená syntéza (a tým aj sekrécia) oboch prostanoidov: prostacyklínu aj tromboxanu, takže pomer PGI2/ TxA2 = 4,1 u testovaných pacientov nie je signifikantne odlišný od pomeru prostacykín/ tromboxan = 4,4 u kontrolnej skupiny.
Ako ďalší parameter na testovanie aterogenity lipoproteínového profilu sme novo zaviedli „Skóre Aterogénneho Rizika“ (SAR). Ide o index, ktorý porovnáva množstvo neaterogénnych a aterogénnych lipoproteínov v celom lipoproteínovom spektre. Ako vidieť v tab. 2 – 4, jeho informatívna hodnota je porovnateľná s testovanými subpopuláciami LDL 3 – 7 = mdLDL. Ako sa uvádza v tab. 2 – 4, rozdiely v skóre aterogénneho rizika medzi aterogénnym a neaterogénnym lipoproteínovým profilom v skupine pacientov, ale aj v rámci kontrolnej skupiny: aterogénna vs neaterogénna subskupina, sú štatisticky vysoko signifikantnné (p < 0,0001). Širšie použitie SAR v klinickej praxi vyžaduje ďalšie testovania v klinických štúdiách.
doc. MUDr. Stanislav Oravec, CSc.
www.nspr.sk
e-mail: stanislavoravec@yahoo.comDoručeno do redakce: 31. 5. 2010
Zdroje
1. Superko HR. Lipoprotein subclasses and atherosclerosis. Front Biosci 2001; 6: D355 – D365.
2. Berneis KK, Krauss RM. Metabolic origins and clinical significance of LDL heterogeneity. J Lipid Res 2002; 43 : 1363 – 1379.
3. Packard CJ. Triacylglycerol ‑ rich lipoproteins and the generation of small dense low ‑ density lipoprotein. Biochem Soc Trans 2003; 31 : 1066 – 1069.
4. Shoji T, Hatsuda S, Tsuchikura S et al. Small dense low ‑ density lipoprotein cholesterol concentration and carotid atherosclerosis. Atherosclerosis 2009; 202 : 582 – 588.
5. Austin MA, King MC, Vranizan KM et al. Atherogenic lipoprotein phenotype. A proposed genetic marker for coronary heart disease risk. Circulation 1990; 82 : 495 – 506.
6. Van J, Pan J, Charles MA et al. Atherogenic lipid phenotype in a general group of subjects. Arch Pathol Lab Med 2007; 131 : 1679 – 1685.
7. Hoefner DM, Hodel SD, O’Brien JF et al. Development of a rapid quantitative method for LDL subfraction with use of the Quantimetrix Lipoprint LDL system. Clin Chem 2001; 47 : 266 – 274.
8. Oravec S. Nová laboratórno ‑ medicínska pomoc v diagnostike dyslipoproteínemií a kardiovaskulárnych ochorení: Identifikácia LDL podskupín. Med Milit Slov 2006; 8 : 28 – 32.
9. Oravec S. Identifikácia subpopulácií LDL triedy – Aktuálny prínos v diagnostike porúch metabolizmu lipoproteínov a ochorení kardiovaskulárneho systému. Med Milit Slov 2006; 8 : 32 – 34.
10. Oravec S. Nové perspektívy v diagnostike porúch metabolizmu lipoproteínov – prínos v interpretácii výsledkov. Med Milit Slov 2007; 9 : 42 – 45.
11. Gavorník P. Etiopatogenéza a nová klinicko‑etiologicko‑anatomicko‑patologická (CEAP) klasifikácia končatinovej choroby. Interní Med 2010; 10 : 115 – 123.
12. Gavorník P. Všeobecná angiológia. Angiologická propedeutika. Cievne choroby. Bratislava: Vydavateľstvo Univerzity Komenského 2001.
13. Hirsch AT, Haskal ZJ, Hertzer NR et al. ACC/ AHA 2005 Guidelines for the management of patients with peripheral arterial disease. J Am Coll Cardiol 2006; 47 : 1239 – 1312.
14. Norgren L, Hiatt WR, Dormandy JA et al. Inter ‑ society consensus for the management of peripheral arterial disease. Int Angiol 2007; 26 : 81 – 157.
15. Vakkilainen J, Mäkimattila S, Seppälä ‑ Lindroos A et al. Endothelial dysfunction in men with small LDL particles. Circulation 2000; 102 : 716 – 721.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2010 Číslo 6- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Plicní hypertenze – neobvyklá komplikace syndromu bakteriálního přerůstání – editorial
- Existuje diurnální variabilita big endotelinu a NT‑proBNP u nemocných s těžkým chronickým srdečním selháním?
- Normalizovaný smoothness index a parametrický populační RDH index telmisartanu u pacientů s čerstvě zjištěnou hypertenzí a metabolickým syndromem
- Esenciální trombocytemie a jiné myeloproliferace s trombocytemií léčené Thromboreductinem. Výstupy z databáze Registru k 1. čtvrtletí roku 2010
- Plicní hypertenze – neobvyklá komplikace hemolýzy a syndromu bakteriálního přerůstání
- XXIX. dni mladých internistov Slovenska a České republiky v Martině
- Prim. MU Dr. Petr Svačina – významné životní jubileum
- Můj život s prim. MU Dr. Petrem Svačinou
-
Hyperlipoproteinemie a dyslipoproteinemie I.
Klasifikace, diagnostika, kardiovaskulární, kardiometabolické a reziduální riziko - Registr BRNO 2: farmakoterapie po infarktu myokardu
- Odlišné průběhy recidivující anebo multisystémové formy histiocytózy z Langerhansových buněk u dospělých osob – popis 22 případů z jednoho pracoviště
- Sepse a septický šok u onkologických a imunokompromitovaných pacientů – diagnostika, terapie
- Psychologický náhled na problémy onkologických pacientů a ošetřujícího týmu
- Preventivní podání antibiotik a probiotik u těžké akutní pankreatitidy
- Přínos jednotlivých zobrazovacích metod pro diagnostiku a sledování aktivity mnohočetného myelomu
- Příspěvek k hodnocení sérových hladin vybraných biologických působků u monoklonální gamapatie nejistého významu a v jednotlivých klinických stadiích mnohočetného myelomu
- Kontinuálne monitorovanie tkanivovej glukózy
- Význam senzitivity baroreflexu pre stratifikáciu kardiovaskulárneho rizika u hypertonikov
- Prevencia a liečba končatinovocievnej ischemickej choroby
- Zmeny v lipoproteínovom spektre pri končatinovo- cievnej ischemickej chorobe
- Vysoké školy musí mít nejen kvalitní výuku, ale také účinnou kontrolu kvality znalostí a schopností studentů (produktů) vysoké školy
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Sepse a septický šok u onkologických a imunokompromitovaných pacientů – diagnostika, terapie
-
Hyperlipoproteinemie a dyslipoproteinemie I.
Klasifikace, diagnostika, kardiovaskulární, kardiometabolické a reziduální riziko - Esenciální trombocytemie a jiné myeloproliferace s trombocytemií léčené Thromboreductinem. Výstupy z databáze Registru k 1. čtvrtletí roku 2010
- Odlišné průběhy recidivující anebo multisystémové formy histiocytózy z Langerhansových buněk u dospělých osob – popis 22 případů z jednoho pracoviště
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy