-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Změna spektra supraventrikulárních tachyarytmií indikovaných ke katetrové ablaci – editorial
Autoři: R. Lábrová
Působiště autorů: Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC
Vyšlo v časopise: Vnitř Lék 2011; 57(6): 523-528
Kategorie: Editorialy
Pařízek P et al. Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií. Vnitř Lék 2011; 57(6): XXX–XXX.
Supraventrikulární tachyarytmie (SVT) jsou všechny poruchy srdečního rytmu, v jejichž mechanizmu figurují srdeční tkáně nad úrovní Hisova svazku, Tawarových ramének a srdečních komor. SVT se obvykle projevují rychlou, pravidelnou nebo nepravidelnou srdeční frekvencí. Objevují se v závislosti na věku, pohlaví a přidružených chorobách [1]. Dnešní poznatky o mechanizmu vzniku a způsobu udržování SVT pocházejí z oblasti buněčné elektrofyziologie a z klinických elektrofyziologických studií při programované elektrické stimulaci srdce [2,3]. Stanovení mechanizmu tachyarytmie je nutné pro zvolení správné terapie.
Účinnost léčby SVT byla donedávna neuspokojivá. Připadala v úvahu pouze léčba antiarytmiky, která je úspěšná asi ve 30–50 % [4]. Farmakologická terapie jednak slouží k verzi SVT na sinusový rytmus a jednak má zabránit dalším paroxyzmům tachyarytmie. Akutní farmakologická verze atrioventrikulární nodální reentry tachykardie (AVNRT) a atrioventrikulární reentry tachykardie (AVRT) u přítomných síňokomorových akcesorních drah je většinou účinná, ale snaha vertovat flutter síní I. typu na sinusový rytmus je převážně bez efektu. Další možností verze je nefarmakologická léčba, např. jícnová stimulace síní, při níž stimulační elektrodou zavedenou do jícnu stimulujeme levou síň rychlejší frekvencí, než je frekvence síní vlastní SV tachyarytmie, tzv. overdriving nebo elektrická kardioverze, kdy arytmii rušíme výbojem stejnosměrného proudu o vysokém napětí v krátkodobé celkové analgosedaci. Účinnost antiarytmik k zabránění recidivy paroxyzmů SVT je většinou nízká. Zvláště flutter a fibrilace síní velmi často recidivuje a často se musí ponechat jako základní rytmus pouze s antiarytmickým ovlivněním AV převodu, abychom docílili přiměřené frekvence komor, a tím zabránili vzniku tachykardické kardiomyopatie s dysfunkcí levé komory. Antiarytmická léčba je u většiny nemocných se strukturálním postižením myokardu omezená a problematická a je nutné také myslet na možnost vedlejších účinků. Mezi nejzávažnější vedlejší účinky patří i proarytmogenní efekt antiarytmika, který se pohybuje mezi 0 a 10 % a zvyšuje se závažností strukturálního onemocnění srdce [5]. Farmakoterapie v zabránění recidiv SVT je vlastně léčbou paliativní.
Velký rozvoj invazivního elektrofyziologického vyšetření (EFV) s pomocí programované stimulace srdce vedl k odhalení mechanizmů vzniku a udržení SVT. Příčinou vzniku arytmií je ve většině případů srdeční onemocnění, jehož morfologie připravuje tzv. arytmogenní substrát. Tento arytmogenní substrát je oblast strukturálně, ale především elektricky abnormní myokard, který je odpovědný za vznik a udržování arytmie. Arytmogenní substrát je vrozený, to je případ akcesorní spojky s různě rychlým vedením či paralelní dráhy v oblasti AV uzlu, nebo získaný. Akutní a často reverzibilní substrát může být pouze na úrovni membrán, uveďme např. modulaci membránových vlastností katecholaminy, nervovými vlivy, toxiny, hypoxií či minerálovou dysbalancí, nebo na úrovni tkáně, to je např. zánět, nekróza či trauma. Chronický substrát je častější, příkladem je fibróza, anizotropie nebo hypertrofie svalových vláken srdce.
Mechanizmus supraventrikulárních tachyarytmií je v zásadě dvojí. Prvním typem mechanizmu je porucha vzniku elektrického impulzu a dává podklad pro vznik fokální (ložiskové) tachyarytmie. Vzniká na podkladě urychlené či abnormní automacie nebo na podkladě spuštěné aktivity. Druhým nejobvyklejším mechanizmem vzniku tachyarytmií je reentry mechanizmus (kroužení vzruchu), který vzniká poruchou vedení elektrického vzruchu. Představuje opakovanou nevyhasínající aktivaci určitého okrsku myokardu, sebeudržující elektrický obvod, který opakovaně depolarizuje okolní tkáň. Tachyarytmie, které ve svém mechanizmu využívají stabilní reentry okruh nebo vycházejí z ohraničeného ložiska, mají většinou zcela pravidelnou síňovou aktivitu a označujeme je jako arytmie monomorfní [6,7]. Toto poznání potom umožnilo zavedení invazivní nefarmakologické terapie – katetrové ablace při léčbě tachyarytmií – do klinické praxe.
V posledních 25 letech dochází k velkému rozvoji této nefarmakologické léčby SVT. Perkutánní transvenózní katetrová ablace se používá k léčbě tachyarytmií od roku 1980. Nejdříve se při ní používal stejnosměrný proud o vysokém napětí, což byl vlastně intrakardiální elektrický výboj. Od roku 1987 se k ablaci užívá radiofrekvenční (RF) energie, která má oproti užívání stejnosměrného proudu velké výhody. Nevyžaduje celkovou anestezii, nezpůsobuje barotrauma a aplikace RF energie je lépe řiditelná do patologického elektrofyziologického místa. Řiditelným katetrem se v srdci aplikuje RF energie a způsobí drobnou koagulační nekrózu myokardu, která se hojí homogenní jizvou. Tím se vlivem tepla přeruší patologická elektrická vodivost v srdci, a dojde tak k definitivnímu vyléčení arytmií. U některých arytmií se používá katetr s hrotem chlazeným infuzí fyziologického roztoku a dovoluje vytvoření hlubších lézí, a tím dojde k rychlejšímu dosažení úspěšné RFA, např. ke vzniku obousměrného bloku na kavotrikuspidálním istmu u flutteru síní I. typu [8].
První radiofrekvenční katetrová ablace (RFA) byla provedena v klinické praxi v roce 1987 prof. Borggrefem u WPW syndromu – pravostranné atrioventrikulární přídatné dráhy, v roce 1989 prof. Kuckem u levostranné dráhy, v témže roce také u atrioventrikulární nodální reentry tachykardie (AVNRT), v roce 1992 u flutteru síní I. typu a síňové tachykardie, v roce 1994 Haïssaguerrem u fibrilace síní.
AVNRT jedna z nejčastějších SV tachyarytmií, je typickou reentry tachyarytmií, jejímž podkladem je dualita vedení v oblasti AV uzlu, ve většině případů způsobená přítomností pomalé a rychlé dráhy, které se liší rychlostmi vedení a refrakteritami. Při RFA pomalé dráhy u AVNRT se zavádí ablační katetr do posteroseptální oblasti – mezi ústí koronárního sinu a trikuspidálním anulem. Pokud v tomto místě nedochází k přerušení vedení pomalé dráhy, posunuje se ablační katetr směrem midseptálně, směrem k Hisovu svazku, inferiorně od apexu Kochova trojúhelníku. Někdy je optimální místo k úspěšné RF ablaci kolem ústí, v ústí nebo i pod ústím koronárního sinu. Optimální poloha ablačního katetru se hledá za sinusového rytmu pod RTG kontrolou, síňový potenciál je frakcionovaný, po něm následuje ostrý potenciál pomalé dráhy (obr. 1, 2). Potenciál pomalé dráhy v ablačním katetru předchází potenciál Hisova svazku z vyšetřovacího katetru asi o 34 ± 13 ms. Během aplikace RF energie v místě pomalé dráhy vzniká pomalý junkční rytmus. Další aplikace RF energie se potom provádí za komorové stimulace, při které se sleduje nepoškozené retrográdní vedení rychlou dráhou. Pokud vzniká rychlý a nepravidelný junkční rytmus, místy i s aberací, potom pravděpodobně neovlivňujeme parietální buňky, ale již kompaktní AV uzel, kdy hrozí úplná AV blokáda a je nutné aplikaci RF energie rychle ukončit a hledat optimálnější a bezpečnější místo. Během aplikace RF energie tedy dochází většinou ke kompletnímu přerušení antegrádně vedoucí pomalé dráhy, kdežto retrográdní vedení rychlé dráhy zůstává zachováno. Po úspěšné RFA již tachykardie není stimulačně vyvolatelná, ani po 20 min od poslední aplikace RF energie. Po úspěšné RF ablaci pomalé dráhy zůstává nezměněn AH interval, nezměněno retrográdní vedení z komory na síň a refrakterita. Není změněn ani prográdní Wenckebachův bod.
Obr. 1. RFA typické AVNRT, intrakardiální záznam potenciálu pomalé dráhy v místě aplikace RF energie. HRA – horní pravá síň, HBE – Hisův svazek, RVA – pravá komora, CS – koronární sinus, ABL – intrakardiální záznam z ablačního katetru: A – síňová aktivita, ostrý potenciál pomalé dráhy, V – komorová aktivita, H – aktivita Hisova svazku. 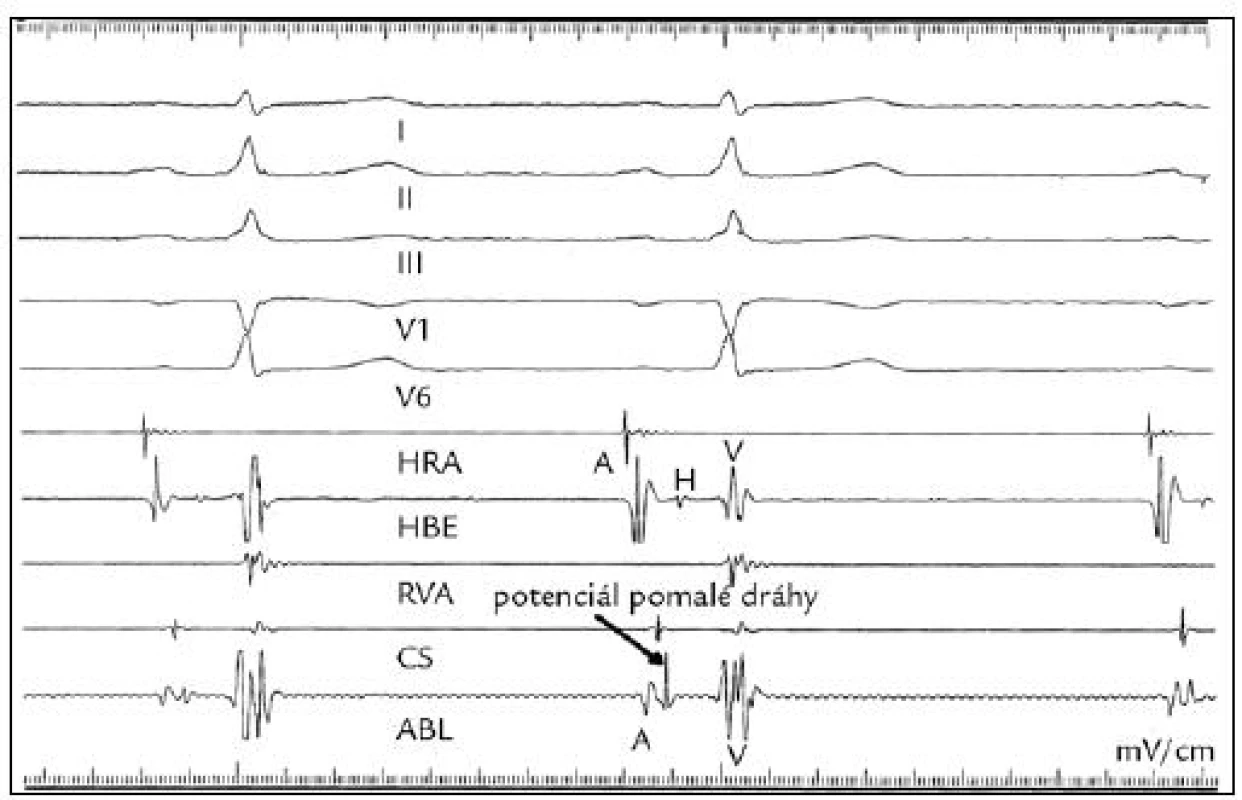
Obr. 2. RTG RFA typické AVNRT. Projekce předozadní (AP). Záznam uložení vyšetřovacích a ablačního katetru v srdci při RF ablaci pomalé dráhy. HRA – horní pravá síň, HIS – Hisův svazek, CS – koronární sinus, RVA – hrot pravé komory, ABL – ablační katetr v oblasti pomalé dráhy. 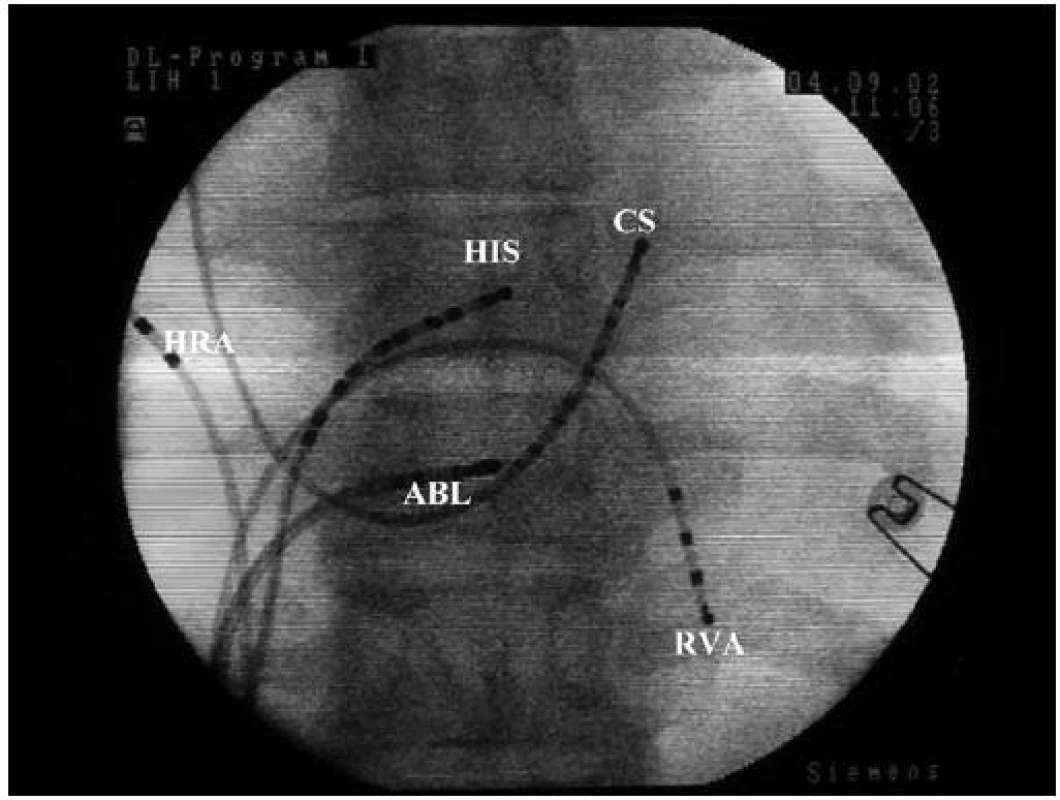
Atrioventrikulární akcesorní dráhy patří k častým indikacím k RFA. U Wolfova-Parkinsonova-Whiteova syndromu lze stanovit diagnózu již z přítomnosti preexcitace – δ vlny a srdeční osy na povrchovém 12svodovém EKG. Z povrchového EKG lze poměrně přesně určit i lokalizaci akcesorní spojky. V roce 1994 bylo na základě zkušeností z elektrofyziologických vyšetření a ablačních výkonů publikováno nové dělení akcesorních drah. U pravostranných drah se rozlišuje lokalizace dle mapování kolem trikuspidálního anulu, u levostranných drah potom při mapování mitrálního anulu.
Skryté akcesorní dráhy, které vedou pouze retrográdně, nemají přítomnou preexcitaci na EKG, takže se při sinusovém rytmu neodhalí. Jejich přítomnost se může odhadnout ze záznamu ortodromní AVRT, kdy se zjišťuje síňová aktivita za QRS komplexem, většinou delší než 100 ms.
Až při mapování během elektrofyziologického vyšetření je určen počet akcesorních drah, jejich uložení a to, která dráha se podílí na reentry okruhu při AVRT. Někdy se nám po úspěšné RF ablaci jedné dráhy odkryje vedení další dráhou s vyvolatelnou druhou AVRT.
K endokardiálnímu mapování pravostranných akcesorních drah se zavádí ablační katetr přes v. femoralisl. dx. Ablační katetr je řiditelný 4polární, obvykle se 4mm typem koncové elektrody. Většinou se mapuje a provádí RFA ze síňového aspektu trikuspidálního prstence. Pokud nedojede k přerušení vodivosti dráhy, mapuje se z komorového aspektu trikuspidálního prstence.
Pokud je zjevná preexcitace na povrchovém EKG, mapuje se při sinusovém rytmu proti maximální preexcitaci na povrchovém EKG. Hledá se nejpředčasnější antegrádní komorová aktivace a nejkratší síňokomorový (AV) interval v ablačním katetru, protože v tomto místě je přídatná dráha ablačnímu katetru nejblíže. Řídíme se podle RTG polohy a intrakardiálního záznamu. Pokud je zjištěna latentní preexcitace nebo skrytá retrográdně vedoucí akcesorní dráha, potom se mapuje při paroxyzmální AVRT nebo při stimulaci z hrotu pravé komory a v ablačním katetru hledáme nejčasnější retrográdně převedenou síňovou aktivitu a nejkratší komorosíňový (VA) interval. Někdy se podaří v mapovacím katetru zaznamenat potenciál akcesorní dráhy. Dráhy, které se nachází u pacienta v oblasti posteroseptální, nemusí být vždy přístupné z endokardu. Většinou jsou při nástřiku koronárního sinu kontrastní látkou zjištěny divertikly koronárního sinu či jiné anomálie. A proto je také někdy nutná aplikace radiofrekvenční energie do koronárního sinu.
Pokud je zjištěna při základním EFV přítomnost akcesorní atrioventrikulární dráhy vlevo, provádí se Seldingerovou metodou punkce a. femoralisl. dx. a potom se ablační mapovací katetr zavádí retrográdně přes aortu do levé komory. V poslední době se preferuje transseptální přístup, kdy se katetr zavedený do levé síně lépe řídí do optimální polohy a může se mapovat na síňové straně mitrálního prstence.
Technika mapování a hledání optimálního místa k aplikaci radiofrekvenční energie je stejná jako u pravostranných atrioventrikulárních drah pouze s tím rozdílem, že mapujeme na komorovém, event. síňovém aspektu mitrálního anulu.
Po úspěšné radiofrekvenční ablaci akcesorní atrioventrikulární dráhy dochází k přerušení vedení této dráhy, normalizuje se antegrádní i retrográdní převod a zmizí δ vlna na povrchovém EKG (obr. 3, 4). Antidromní či ortodromní AVRT je při kontrolním EFV po zákroku nevyvolatelná, ani po 20 min od poslední aplikace RF energie.
Obr. 3. RFA WPW syndromu, akcesorní spojky levé laterální. Během aplikace RF energie, dochází k přerušení vodivosti akcesorní dráhy, na povrchovém EKG vymizí δ vlna, normalizuje se PQ interval. V koronárním sinu – CS 1,2 je odskok síňového a komorového potenciálu. HRA – horní pravá síň, HBE – potenciály z Hisova svazku, CS – koronární sinus, USER – ablační katetr. 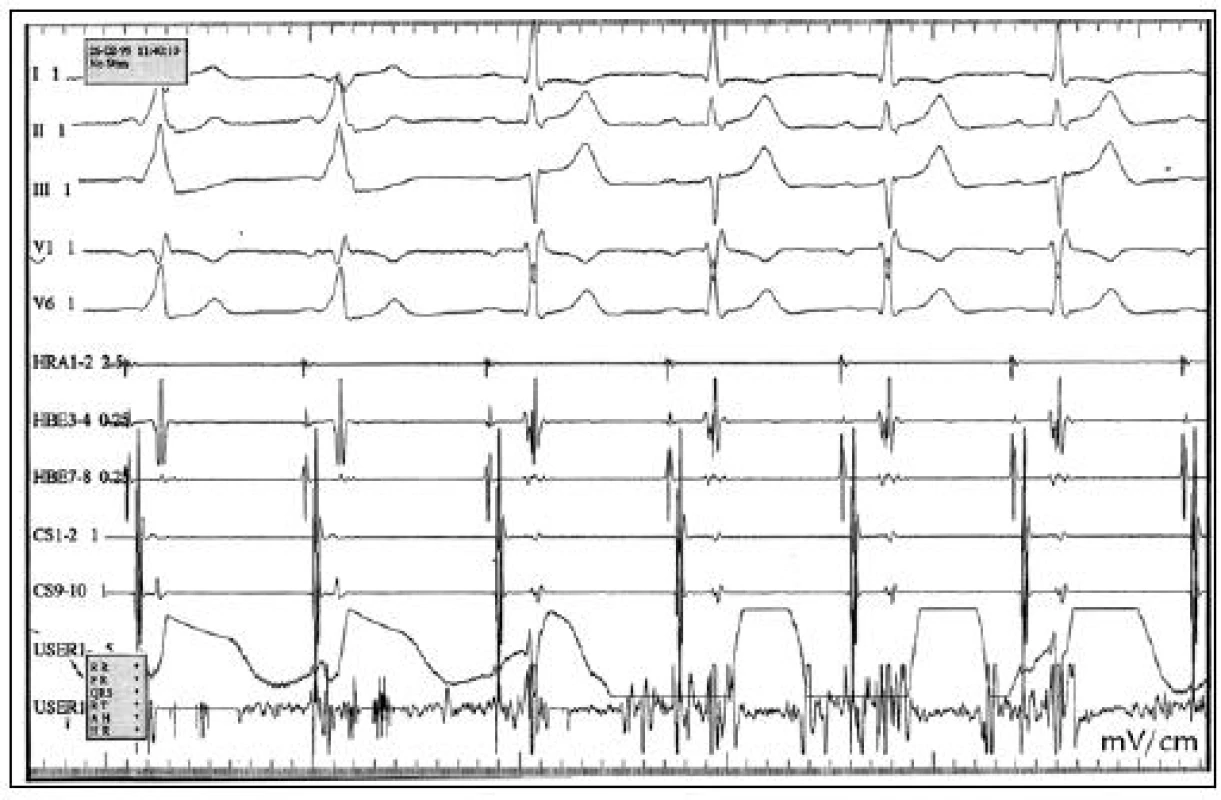
Obr. 4. RTG snímek RFA akcesorní dráhy levé laterální. Projekce pravá šikmá (RAO). Vyšetřovací a ablační katetr při mapování v oblasti mitrálního prstence. HRA – horní pravá síň, HIS – Hisův svazek, RVA – hrot pravé komory, CS – koronární sinus, ABL – ablační katetr, retrográdně zavedený přes a. femoralis l. dx. 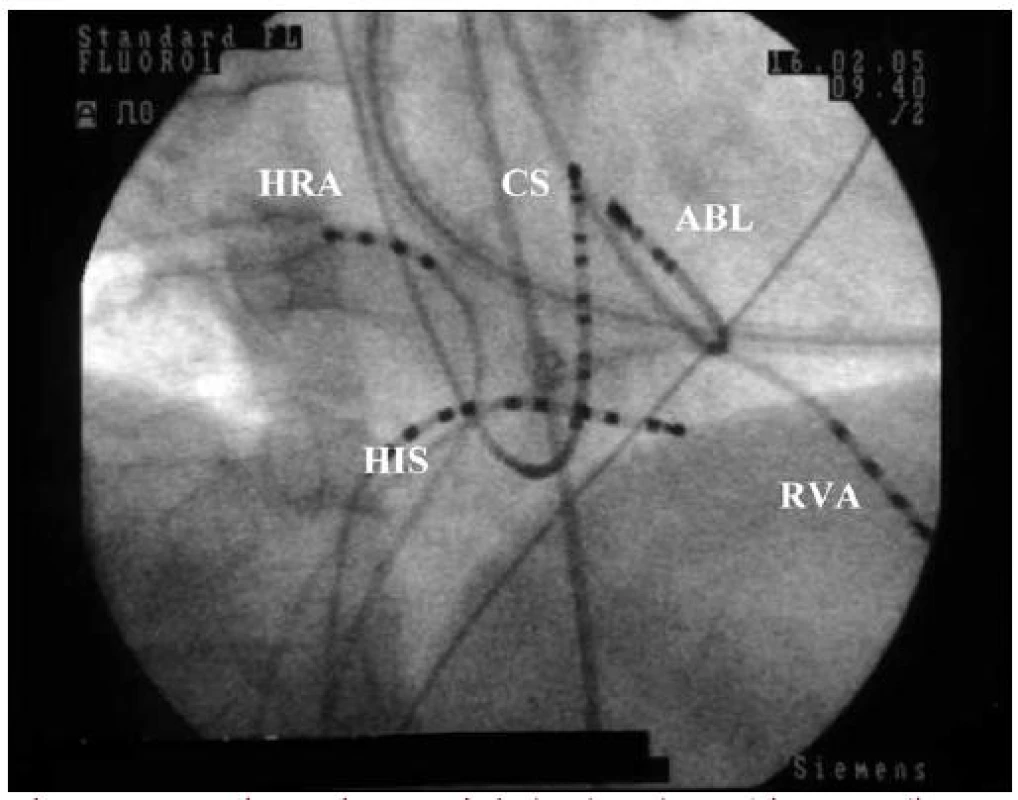
Flutter síní I. typu se stává v poslední době již nejčastější indikací k RFA. U RF ablace flutteru síní I. typu jednoznačně převažuje anatomický přístup, při kterém se vytváří lineární léze napříč můstkem, istmem mezi dolní konkavitou trikuspidálního prstence a ústím dolní duté žíly, což je nejužší místo makroreentry okruhu. V některých případech se event. rozšiřuje o další linii trikuspidální anulus – koronární sinus či koronární sinus – dolní dutá žíla. RFA se provádí za běžícího flutteru síní nebo při sinusovém rytmu za stimulace z obou stran istmu, tzn. z koronárního sinu na jedné straně nebo na druhé straně z distální části Halo katetru, který obkružuje pravou síň. Během aplikace RF energie dochází ke zmenšení nebo rozštěpu místního potenciálu a nakonec k přerušení flutteru síní (obr. 5, 6). Cílovým stavem úspěšné RFA je obousměrná blokáda v oblasti istmu, o které se přesvědčíme stimulací z obou stran kavotrikuspidálního istmu. Po úspěšné RFA je flutter síní programovanou stimulací síní nevyvolatelný.
Obr. 5. RFA flutteru síní I. typu. Během aplikace RF energie dochází k ukončení flutteru síní I. typu a vzniká sinusový rytmus. Následuje dokončení bidirekcionálního bloku v oblasti kavotrikuspidálního istmu. CS – koronární sinus, HBE – Hisův svazek, MRA – halo katetr, RVA – pravá komora, USER – ablační katetr. 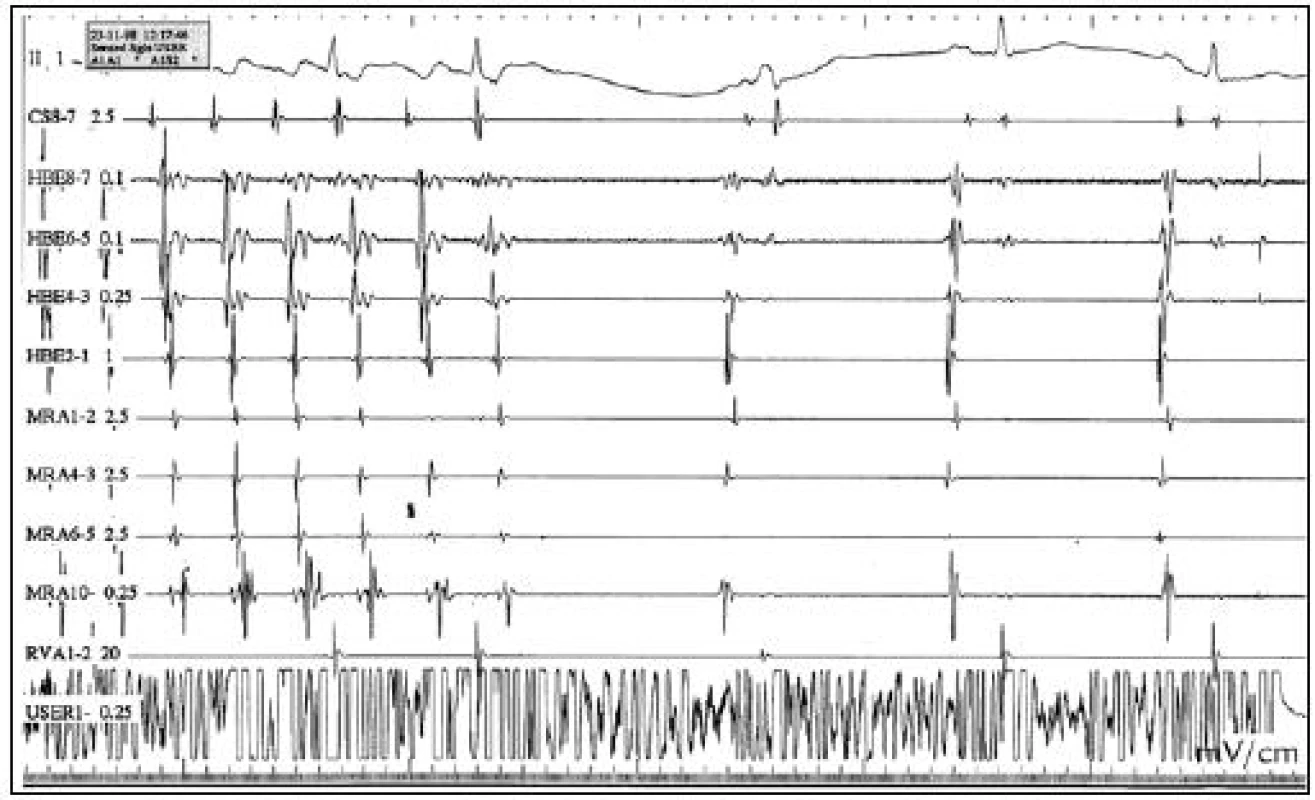
Obr. 6. RTG snímek RFA flutteru síní I. typu. Levá šikmá projekce (LAO). Umístění vyšetřovacích katetrů a ablačního katetru v srdci u flutteru síní I. typu. HAL – duodekapolární halo katetr v pravé síni, HIS – Hisův svazek, CS – koronární sinus, ABL – ablační katetr v oblasti kavotrikuspidálního istmu. 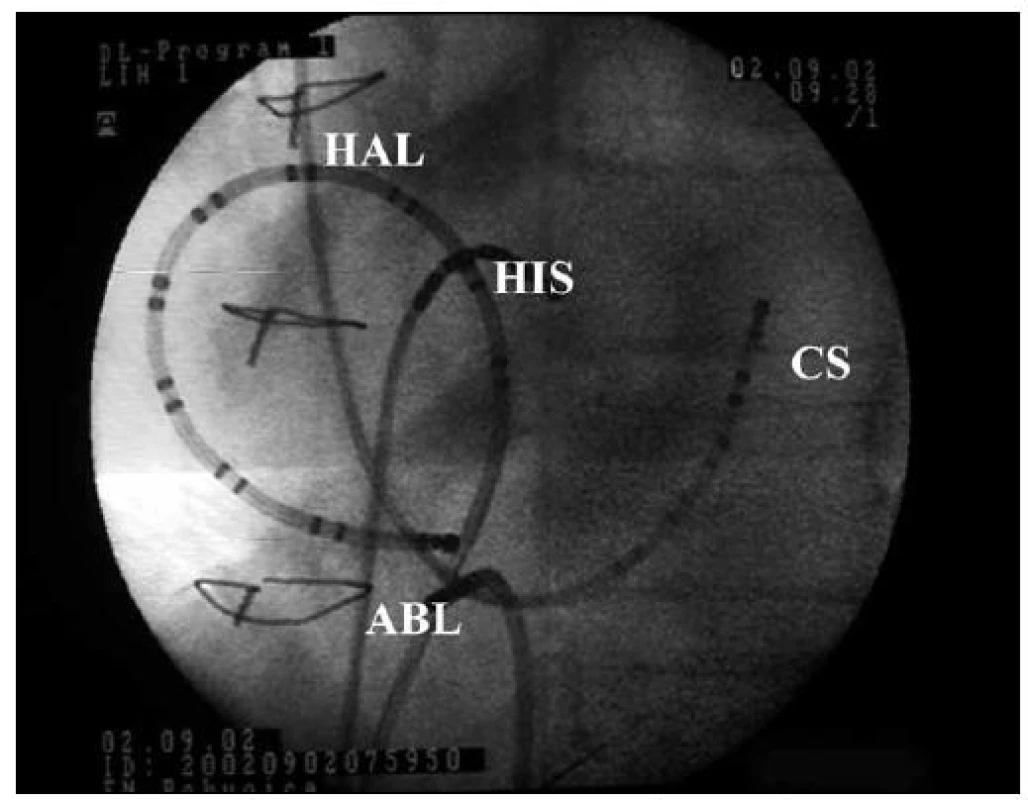
RFA flutteru síní ale nepotlačí paroxyzmy již dříve dokumentované fibrilace síní, a to zvláště u pacientů se zvětšenou levou síní. Pokud má pacient v dokumentaci oba typy arytmie, potom se většinou provádí RFA obou arytmií zároveň.
V současné době se u většiny SVT – u flutteru síní I. typu, AVNRT, akcesorních drah a síňové tachykardie, jak doporučují autoři Pařízek et al v publikaci Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií – provádí katetrová ablace již jako léčebná metoda první volby. Dlouhodobá úspěšnost RFA AVNRT, akcesorních drah a flutteru síní I. typu je vysoká, mezi 98–99 %, u síňové tachykardie, která je zastoupena menším počtem pacientů, je 89 %. Celkový výskyt komplikací byl 2,9 %.
Na našem pracovišti, Interní kardiologické klinice LF MU a FN Brno, pracovišti Bohunice, jsme v letech 1995–2010 provedli celkem 2 154 katetrových ablací. Během tohoto období se měnilo jednak spektrum ablačních výkonů, jednak jejich průběh a výsledky. Spektrum indikací k RF ablacím ovlivnily lepší znalosti o mechanizmu arytmií, novější technologie i větší zkušenosti katetrizujících lékařů. Spektrum výkonů se rozšířilo o levosíňové a komorové tachykardie.
Od září 2004 se na Interní kardiologické klinice LF MU a FN Brno, pracovišti Bohunice provádí RF ablace paroxyzmální formy fibrilace síní. Dále se provádí i cirkumferenční ablační linie kolem pravostranných a levostranných plicních žil a kontroluje se elektrická izolace plicních žil u paroxyzmální formy FS.
Od roku 2006 se provádí u symptomatických pacientů s perzistující či dlouhodobě perzistující fibrilací síní komplexní ablace v levé síni pomocí trojrozměrného mapování systémem CARTO nebo je užívána integrace trojrozměrné elektroanatomické mapy systémem CARTO nebo NAVEX s rekonstrukcí levé síně a plicních žil pomocí počítačové tomografie [9–11].
Dlouhodobá úspěšnost RFA AVNRT a akcesorních drah se blíží 100%, u flutteru síní I. typu je 99% a u síňových tachykardií 93%. U paroxyzmální formy fibrilace síní se úspěšnost pohybuje mezi 80–89 %. Celkový počet komplikací je nízký – 2,6 %.
V prvních letech ablačních výkonů byly nejčastěji indikovány k invazivnímu řešení AVNRT, které byly zastoupeny mezi 40–60 %, kolem 25–35 % akcesorní dráhy (obr. 7–9). V roce 2005 se stal nejčastější arytmií indikovanou k RFA flutter síní I. typu, který představoval 35 % všech výkonů, AVNRT se dostala v indikacích na 2. místo, tvořila 28 %, akcesorní dráhy 18 % a fibrilace síní se dostala na 4. místo, tvořila 14 %. V roce 2009 se stává fibrilace síní již druhou nejčastější indikací k RFA za typickým flutterem síní. V roce 2010 je stále nejčastější indikací k RFA flutter síní I. typu, tvoří 35 %, na 2. místě je fibrilace síní s 26 %, AVNRT s 20 % a akcesorní dráhy s 9 %. Předpokládá se, že v krátké době se fibrilace síní stane nejčastěji indikovanou arytmií a odsune flutter síní I. typu na 2. místo, a to protože podle epidemiologických studií se v následujících 50 letech má zvýšit počet pacientů s fibrilací síní 2,5–5krát.
Obr. 7. Spektrum RFA 1997. Obr. 7–9 ukazují změnu spektra indikací ke katetrové ablaci na IKK FN Brno v průběhu období 1995–2010. AVNRT – atrioventrikulární nodální reentry tachykardie, AV uzel – neselektivní ablace AV uzlu s implantací kardiostimulátoru, fokální ST – fokální síňová tachykardie, KT – komorová ektopie a komorová tachykardie. 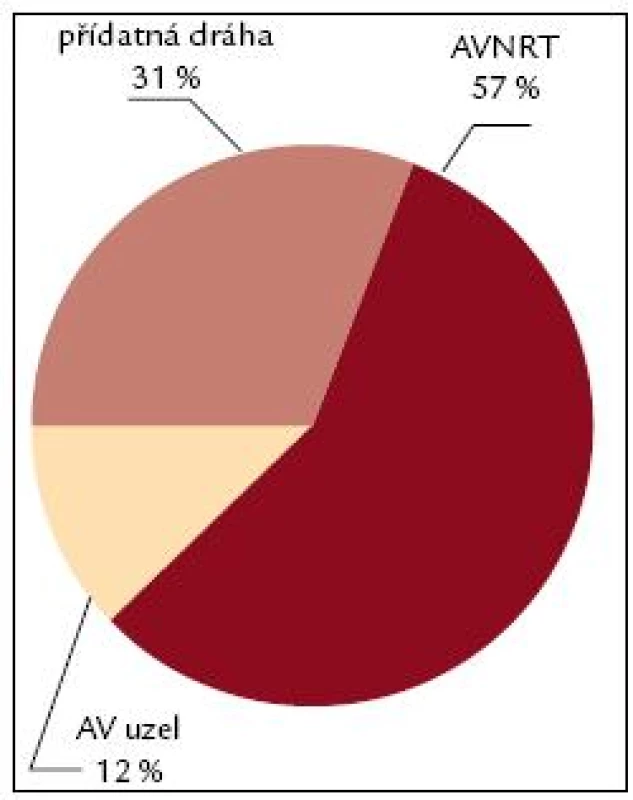
Obr. 8. Spektrum RFA 2005. Vysvětlivky viz. obr. 7. 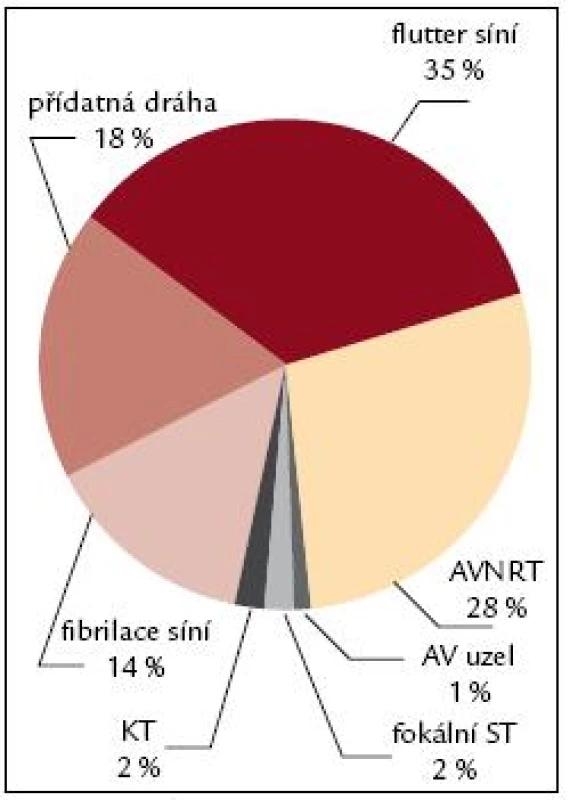
Obr. 9. Spektrum RFA 2010. Vysvětlivky viz. obr. 7. 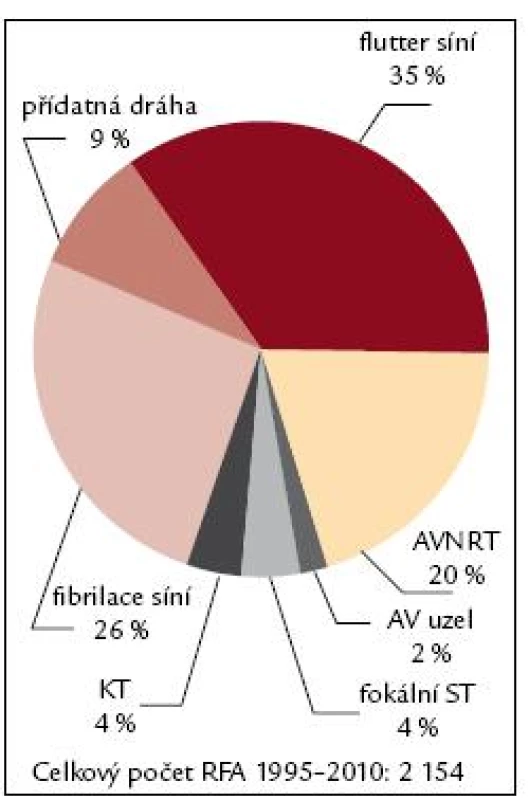
Podle guidelines Evropské kardiologické společnosti z roku 2010 se u pacientů s paroxyzmální formou fibrilace síní může doporučit RFA – izolace plicních žil již po jednom neúčinném antiarytmiku, nebo dokonce podle individuálního zvážení se může u této formy fibrilace síní navrhnout RFA jako léčebná metoda první volby [12].
To znamená, že je metoda aplikována v době, kdy ještě nedochází k významné strukturální a mechanické remodelaci síní a je největší předpoklad úspěšného výkonu. Po úspěšné ablaci se potom pacient dostává v rámci rizika tromboembolie na úroveň zdravého člověka.
V brzké době očekáváme úpravu v indikacích ke katetrové ablaci u fibrilace síní i v doporučeních České kardiologické společnosti.
I u novějšího spektra výkonů dochází k postupnému snižování délky výkonů, radiační zátěže, stoupá úspěšnost a klesá počet komplikací. Léčba RF ablací je pacienty dobře tolerována a u většiny SVT je již indikována jako léčebná metoda první volby. Úspěšná RFA vede k definitivnímu vyléčení arytmií. Po úspěšné RFA jsou většinou pacienti bez chronické antiarytmické a antikoagulační terapie a výrazně se jim zlepšuje kvalita života.
doc. MUDr. Růžena Lábrová, Ph.D.
www.fnbrno.cz
e-mail: labrova@seznam.cz
Zdroje
1. Baine WB, Yu W, Weis KA. Trends and outcomes in the hospitalization of older Americans for cardiac conduction disorders or arrhythmias, 1991–1998. J Am Geriatr Soc 2001; 49 : 763–770.
2. Blomström-Lundqvist C, Scheinman MM, Aliot ME et al. ACC/AHA/ESC Guidelines for the management of patients with supraventricular arrhythmias. A report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines. EHJ 2003; 24 : 1857–1897.
3. Fiala M. Doporučené postupy pro diagnostiku a léčbu supraventrikulárních tachyarytmií. Cor Vasa 2005; 47 (9 Suppl): 18–39.
4. Wanless RS, Anderson K, Joy M et al. Multicenter comparative study of the efficacy and safety of sotalol in the profylactic treatment of patients with paroxysmal supraventricular tachyarrhythmias. Am Heart J 1997; 133 : 441–446.
5. Tendera M, Wnuk-Wojnar AM, Kulakowski P et al. Efficacy and safety of dofetilide in the prevention of symptomatic episode of paroxysmal supraventricular tachycardia: a 6 month double-blind comparison with propafenone and placebo. Am Heart J 2001 : 142 : 93–98.
6. Garson A, Smith RT, Moak JP et al. Atrial automatic ectopic tachycardia in children. In: Tuboul P, Waldo AL (eds). Atrial Arrhythmias: Current Concepts and Management. St. Louis. Mo: Mosby Year Book 1990, 282–287.
7. Chen SA, Chiang CE, Yang CJ et al. Sustained atrial tachycardia in adult patients. Electrophysiologic characteristics, pharmacological response, possible mechanisms, and effects of radiofrequency ablation. Circulation 1994; 90 : 1262–1278.
8. Jaïs P, Shah DC, Haïssaguerre M et al. Prospective randomized comparison of irrigated-tip versus conventional-tip catheters for ablation of common flutter. Circulation 2000; 101 : 772–776.
9. Lábrová R. Fibrilace síní v době katétrové ablace. Vnitř Lék 2010; 56 : 871–879.
10. Lábrová R, Fiala M, Toman O et al. Radiofrekvenční katetrová ablace paroxyzmální fibrilace síní konvenční metodou, bezprostřední a dlouhodobé výsledky. Vnitř Lék 2008; 54 : 953–960.
11. Lábrová R, Špinar J. Katetrizační ablace fibrilace síní. Kardiol Rev 2008; 10 : 103–110.
12. European Heart Rhythm Association; European Association for Cardio-Thoracic Surgery, Camm AJ, Kirchhof P, Lip GY et al. Guidelines for the management of atrial fibrillation. The Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010; 31 : 2369–2429.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Brugada syndromČlánek Primární jaterní karcinoid
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2011 Číslo 6- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Změna spektra supraventrikulárních tachyarytmií indikovaných ke katetrové ablaci – editorial
- Brugada syndrom: syndrom vzácný, ale zákeřný – editorial
- Primární jaterní karcinoid – editorial
- Vplyv dlhodobej glykemickej kompenzácie na zmeny v lipidovom profile detí a adolescentov s diabetes mellitus 1. typu
- Účinnost a bezpečnost podávání moxonidinu u pacientů s metabolickým syndromem (klinické hodnocení O.B.E.Z.I.T.A.)
- Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií
- Brugada syndrom
- Senioři a kardiovaskulární medikace
- Infekční endokarditida – klíčová včasná diagnóza
- Úspěšná léčba Erdheimovy-Chesterovy nemoci chemoterapií obsahující 2-chlorodeoxyadenozin. Popis dvou případů a přehled literatury
- Primární jaterní karcinoid
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Brugada syndrom
- Primární jaterní karcinoid
- Senioři a kardiovaskulární medikace
- Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



