-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Nádor srdce manifestující se náhlou srdeční smrtí
Heart tumor manifesting as a sudden cardiac death
Cardiac tumors are rare. They can be divided into primary and secondary. Primary tumors are benign or malignant. The diagnostics is based on imaging techniques. Therapy is surgical on the first place, followed by chemotherapy and radiotherapy in case of malignant tumors. Prognosis of benign tumors is favourable. We present a case report of a patient dying suddenly after hospital admission on for malignant ventricular arrhythmia. Gradually we revealed a nehodgkin lymphoma infiltration of the heart as the structural fundament of this arrhythmia.
Key words:
cardiac tumors – malignant arrhythmias – nehodgkin lymphoma
Autoři: L. Koten 1; P. Salajka 2
Působiště autorů: Interní klinika IPVZ Praha a Krajské nemocnice T. Bati, a. s., Zlín, přednosta prim. MUDr. Jiří Latta 1; Patologicko-anatomické oddělení Krajské nemocnice T. Bati, a. s., Zlín, přednostka prim. MUDr. Dagmar Dolinská 2
Vyšlo v časopise: Vnitř Lék 2012; 58(9): 674-678
Kategorie: Kazuistiky
Souhrn
Nádory srdce se vyskytují vzácně. Dělí se na primární a sekundární. Primární pak na benigní a maligní. V diagnostice hrají hlavní roli zobrazovací metody. Terapie je na prvním místě chirurgická, u maligních pak následovaná chemoterapií a radioterapií. Prognóza benigních nádorů je příznivá. Práce popisuje případ pacienta umírajícího na maligní komorovou arytmii. Postupně se prokázalo, že jejím strukturálním podkladem je nádorová infiltrace myokardu buňkami nehodgkinského lymfomu.
Klíčová slova:
nádory srdce – maligní arytmie – nehodgkinský lymfomÚvod
Nádorová onemocnění srdce jsou co do výskytu v populaci velmi vzácná, pro konkrétního nemocného však mohou mít zcela devastující následky. Srdeční nádory se podle původu dělí na primární a sekundární (metastatické). Podle biologické povahy se pak primární nádory rozdělují na benigní a maligní.
Incidence primárních nádorů srdce je do 0,03 %, prevalence do 0,02 % [1]. Přibližně 75 % primárních nádorů je benigních, přičemž asi 1/2 z nich tvoří myxomy. Primární nádory většinou rostou intrakavitálně a převážně jsou lokalizovány v levé předsíni, čímž ovlivňují hemodynamiku v levém srdci a mohou být časně diagnostikovány [2]. Naproti tomu sekundární nádory jsou až 100krát častější. Jsou reprezentovány buď metastázami při generalizaci nádorového onemocnění, nebo jde o přímé prorůstání tumoru z okolních struktur či cestou velkých žil [3]. Většinou se jedná o karcinomy, sarkomy a lymfomy [1]. Srdeční metastázy zřídka rostou intrakavitálně, neinterferují s tokem krve, a proto bývají diagnostikovány později [2]. Zvláštní skupinu tvoří nádorové postižení perikardu označované jako tzv. karcinomatózní perikarditida [3]. Primárním nádorem je zde nejčastěji karcinom plic, prsu a hematologické malignity [3].
Průběh a projevy nádorového onemocnění srdce jsou závislé na povaze nádoru a na jeho lokalizaci. Srdeční nádor se může klinicky manifestovat jen celkovými nespecifickými příznaky. Mezi ně patří zejména ztráta tělesné hmotnosti, bolest na hrudi, dušnost, horečka, z laboratorních pak vysoká sedimentace, anémie, trombocytopenie. Mezi specifické projevy nádoru srdce patří arytmie při lokální invazi nádoru. Dále pak srdeční selhání v případě náhrady funkčního myokardu neoplastickou hmotou [1,2]. Nádor se může rovněž klinicky projevit jako plicní embolie nebo orgánový infarkt při embolizaci fragmentů nádoru anebo trombů uvolněných z povrchu nádoru do systémového či plicního řečiště. Velká část nádorů se však projeví v hemodynamice nemocného při interferenci nádorových hmot s chlopenním aparátem nebo při obstrukci přítoku či odtoku krve ze srdce [4]. Tak se může i relativně malý, biologicky benigní nádor stát pro pacienta „maligním“ svou lokalizací. Nádorové postižení perikardu se může projevit perikardiálním výpotkem nebo i tamponádou. Nádory však mohou být i zcela klinicky němé a jsou pak náhodným pitevním nálezem.
V diagnostice nádorového onemocnění srdce hrají zásadní roli zobrazovací metody. Na prvním místě je to echokardiografické vyšetření, dále pak výpočetní tomografie a magnetická rezonance, případně i pozitronová emisní tomografie. Nálezy na skiagramu hrudníku jsou zpravidla nespecifické [4]. Srdeční nádor se jen vzácně projeví jako kardiomegalie na skiagramu [1]. V případě zachycení metastatického postižení plicního parenchymu je nutno pomýšlet i na sekundární postižení srdce, neboť až u 20 % pacientů s generalizovaným nádorovým onemocněním může být touto chorobou zasaženo i srdce [4].
Na EKG nemá nádorové onemocnění srdce žádný specifický projev. Může být příčinou extrasystol, arytmií nebo blokád při zasažení srdečního převodního systému [5].
Invazivní vyšetření, jako jsou katetrizace nebo angiografie, již v současné době nejsou metodami první volby a často bývají při diagnostice plně nahrazovány výše uvedenými obrazovými metodami. Výjimku tvoří perikardiocentéza, kdy může být nádorové postižení perikardu prvně diagnostikováno až při cytologickém vyšetření aspirované tekutiny. Podezření na maligní povahu onemocnění by měly vzbudit zejména opakovaně nebo rychle se tvořící srdeční výpotky, pro jejichž tvorbu není jiné klinické vysvětlení.
Definitivní diagnostické určení nádoru bývá na základě patologického rozboru vzorku získaného z endomyokardiální biopsie nebo pooperačně.
Nejčastějším benigním primárním nádorem srdce je myxom. Dále do této skupiny patří fibrom, lipom, rabdomyom a paraganliom. Většinu primárních maligních nádorů srdce tvoří sarkomy [3].
Sekundární srdeční metastázy bývají nejčastěji u bronchogenního karcinomu, karcinomu prsu, maligního melanomu, karcinomu žaludku a kolorekta [3]. Žádný nádor nemetastazuje výhradně do srdce [4]. Nádor se do srdce dostává buď přímým prorůstáním (nádory plic, mediastina, jícnu), nebo jako nádorový trombus cestou dolní duté žíly (nádor ledvin, jater), případně cestou plicních žil (nádory plic). Daleko nejčastěji je to však metastaticky, hematogenně či lymfogenně [3].
Terapie benigních nádorů je na prvním místě chirurgická s cílem odstranění maximálního objemu nádoru. U maligních nádorů je pak kardiochirugický výkon ještě doplněn adjuvantní chemoterapií a radioterapií. Extrémním příkladem kardiochirugického řešení inoperabilního srdečního nádoru je transplantace srdce [4]. Sekundární srdeční nádory jsou léčeny systémovou chemoterapií nebo radioterapií, paliativní chirurgické odstranění sekundárního tumoru však může vést ke zmírnění symptomů a prodloužení života [2,4].
V případě maligního perikardiálního výpotku je na místě systémová chemoterapie a intraperikardiální aplikace fluorouracilu, tetracyklinu a radioaktivního zlata. Při přetrvávajícím výpotku je třeba provést chirurgickou fenestraci perikardu [4].
Prognóza benigních nádorů srdce je velmi dobrá. Jejich chirurgické odstranění zpravidla vede k úplnému vyléčení pacienta. Někdy však mohou, zejména myxomy, recidivovat. V tomto případě se často jedná o familiárně podmíněný výskyt [4]. Ačkoliv z primárních nádorů srdce je jen 25 % maligních, jejich prognóza je velmi špatná, neboť v době diagnózy jsou už u více než 1/2 přítomny vzdálené metastázy [3,4]. Chirurgické řešení, stejně tak i radioterapie a chemoterapie jsou většinou jen paliativní. Totéž platí i pro sekundární nádorová onemocnění srdce.
Popis případu
60letý muž s anamnézou cévní mozkové příhody, po non-Q infarktu myokardu anteroextenzivně (1989), s hyperlipidemií, bývalý kuřák byl přivezen RZP pro synkopu. Pacient byl hospitalizován před rokem na neurologickém oddělení naší nemocnice pro cévní mozkovou příhodu. Tehdy byl komplexně vyšetřen včetně echokardiografického vyšetření, RTG snímku a základní laboratoře. Nálezy byly bez hrubé patologie. V celkově dobrém stavu byl pacient propuštěn do domácí péče.
Nyní byl nemocný nalezen příbuznými ve večerních hodinách doma v bezvědomí. Před příjezdem RZP se spontánně probral. Lékařem RZP byla dokumentována hypotenze (TK 95/60 mm Hg), na EKG pravidelná arytmie se širokými QRS komplexy (obr. 1) – hodnoceno jako setrvalá komorová tachykardie. Do léčby byl podán bolus amiodaronu (300 mg i.v.) a krystaloidy (1/1 FR 500 ml i.v.). Pacient byl transportován na koronární jednotku.
Obr. 1. EKG záznam z monitoru na místě zásahu zachycující tachykardii se širokým QRS komplexem. 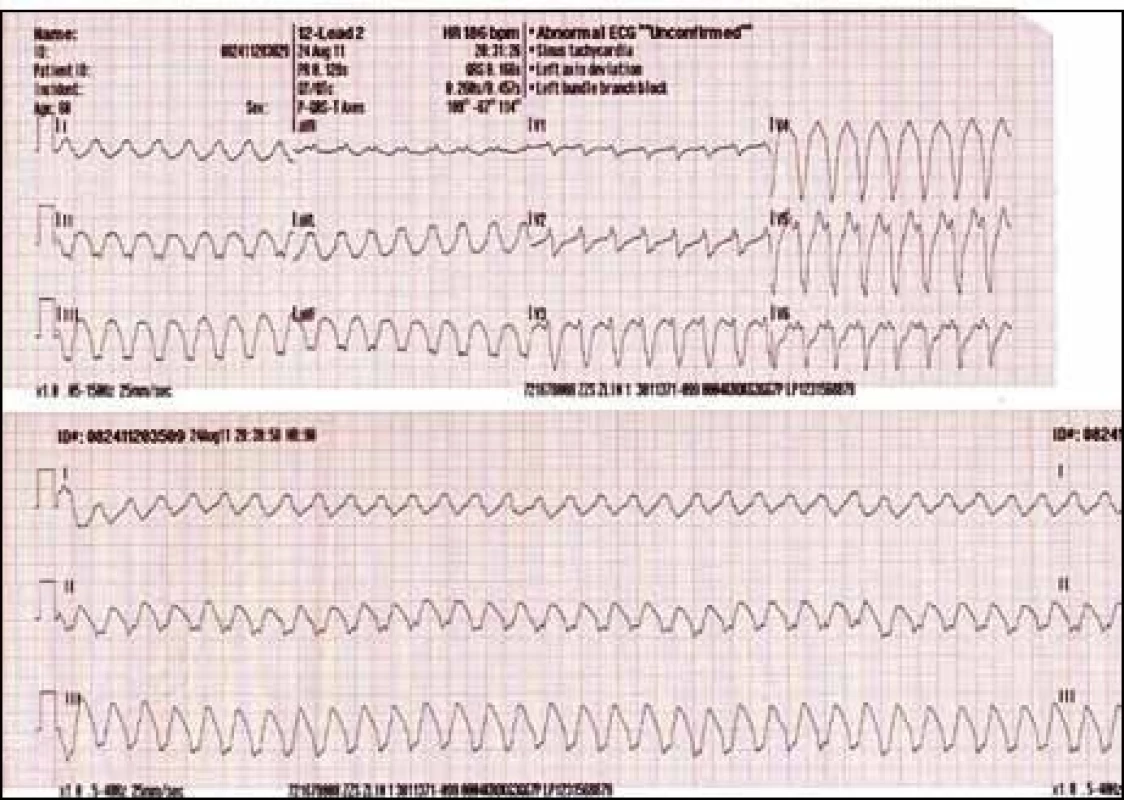
Při přijetí měl pacient TK 108/70 mm Hg, TF 180/min. Nemocný byl při vědomí, popíral dušnost, stenokardie, udal ale, že se posledních 6 měsíců cítí velmi unaven, má nechutenství a nedobrovolně zhubnul 20 kg, k lékaři však nešel. Na EKG při přijetí perzistovala setrvalá komorová tachykardie o TF 180/min. Aplikace amiodaronu byla bez efektu, proto byl v krátké celkové anestezii elektrickou kardioverzí obnoven sinusový rytmus. Poté na EKG byly nespecifické repolarizační změny inferolaterálně (obr. 2). Bylo pokračováno v podávání amiodaronu venózně.
Obr. 2. EKG záznam po elektrické kardioverzi. 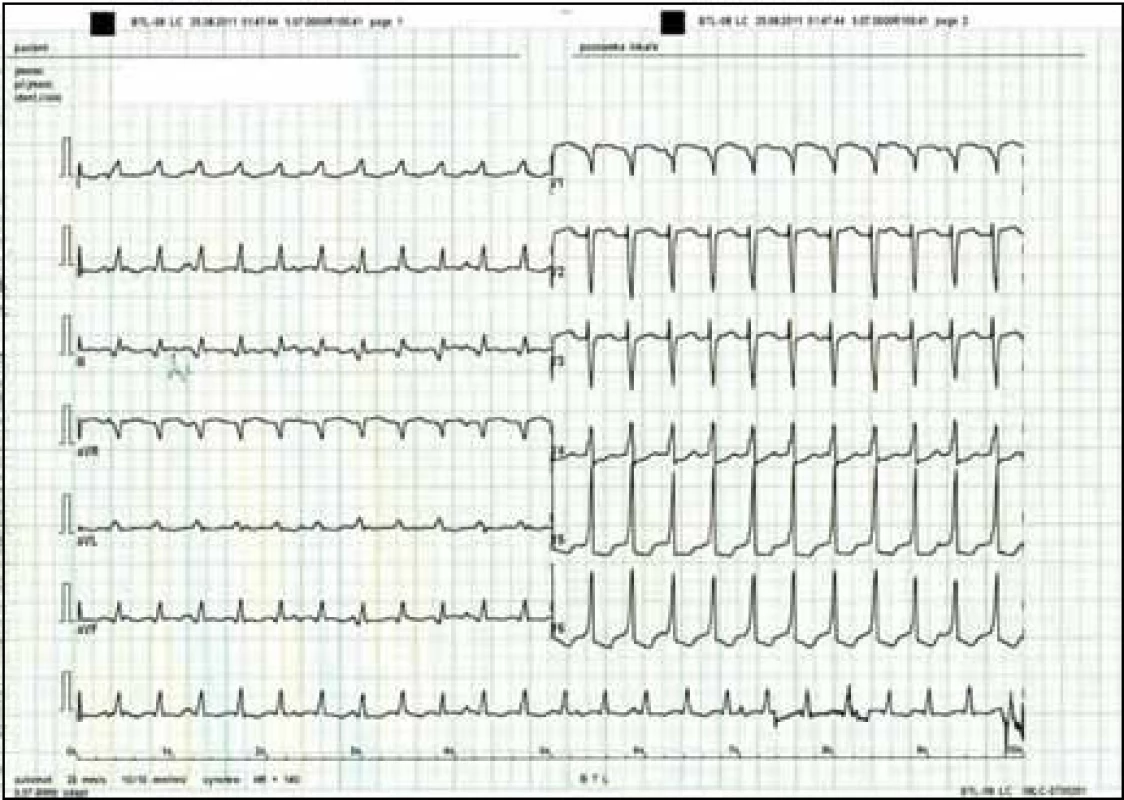
Mezitím byl proveden RTG nitrohrudních orgánů vleže: srdeční stín hraniční velikosti, bez známek městnání, v plicním parenchymu byly zobrazeny 2 ložiskové stíny v pravém dolním plicním poli o průměrech 25 a 40 mm a vlevo v dolním plicním poli další stín o průměru 30 mm. Nález byl hodnocen jako metastatický rozsev (obr. 3). V laboratoři byla oproti poslední hospitalizaci mírná normochromní normocytární anémie, hyperurikemie, jinak bylo základní vyšetření v normě. Nemocný byl vyšetřen echokardiograficky, kdy byla zjištěna výrazně ztluštělá stěna levé komory (IVSd 26 mm, LVPWd 21 mm) s nehomogenní odrazivostí, levá komora difuzně těžce hypokinetická, kdy lépe pohyblivý byl jen hrot a bazální segmenty, EF LK 20 % (obr. 4 a 5). Za zadní stěnou LK byl zaznamenán perikardiální výpotek (9 mm v diastole). Ostatní nález při echokardiografickém vyšetření bez významné patologie. Zároveň bylo provedeno i orientační ultrazvukové vyšetření břicha, které prokázalo velké (12 × 10 cm) hypoechogenní ložisko pravé ledviny destruující horní pól pravé ledviny a vrůstající do dolní duté žíly.
Obr. 3. Zadopřední snímek nitrohrudních orgánů. 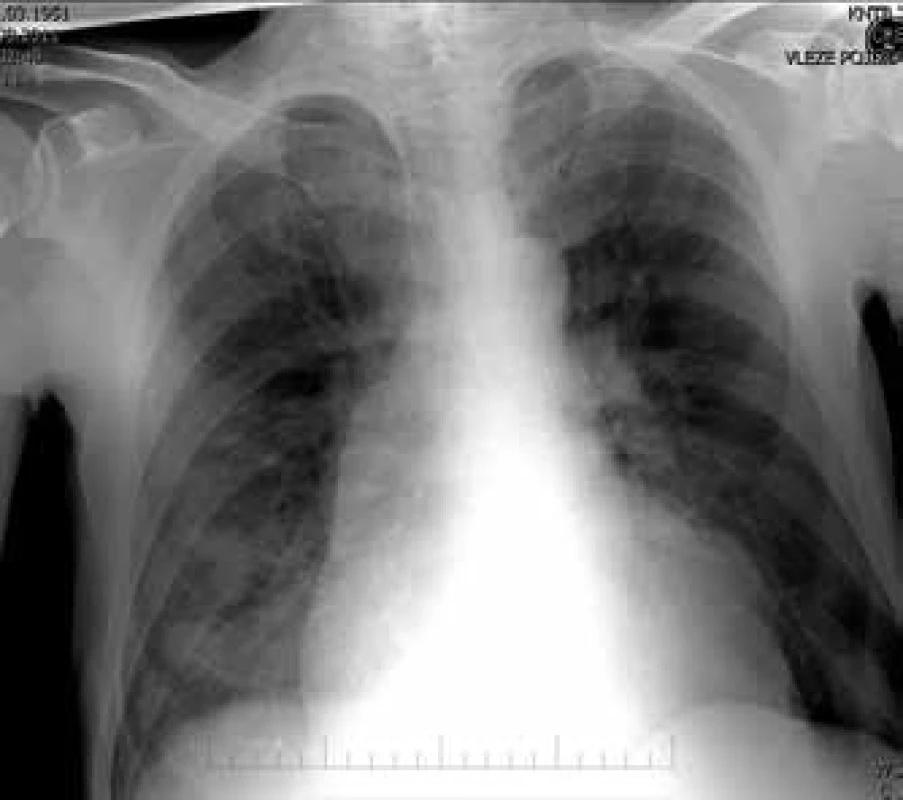
Obr. 4. Snímek z echokardiografického vyšetření zobrazující hypertrofovanou levou komoru – parasternální projekce na krátkou osu. 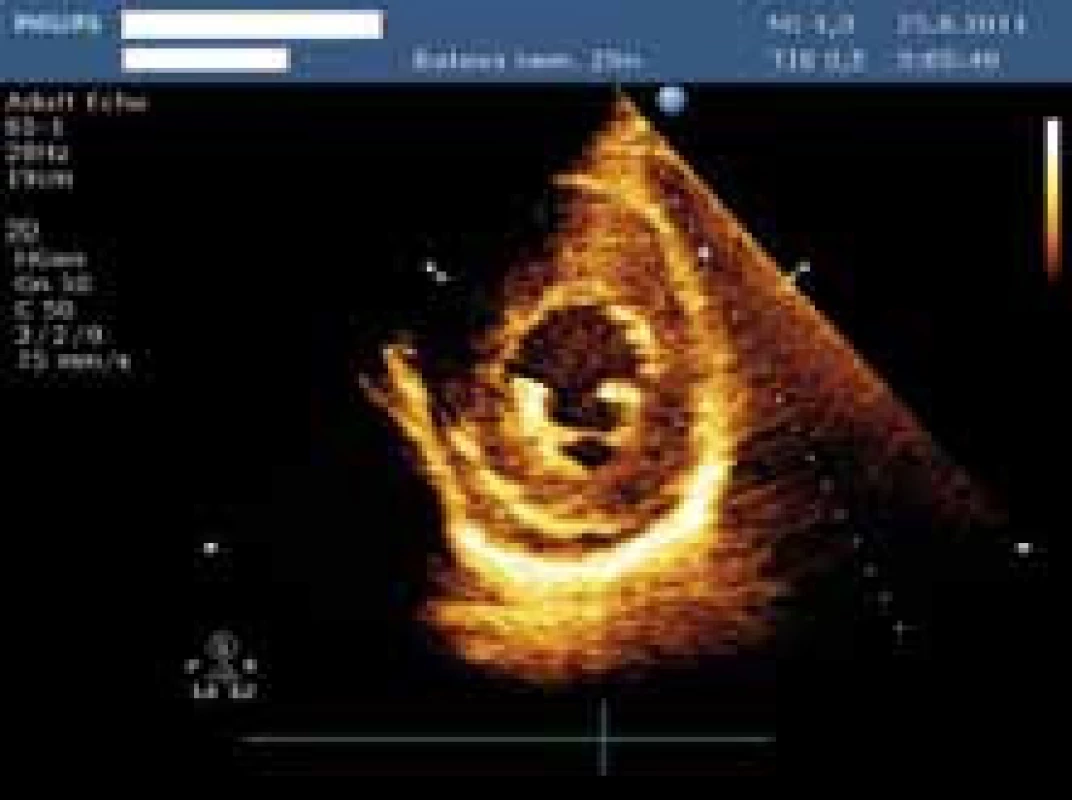
Obr. 5. Snímek z echokardiografického vyšetření zobrazující hypertrofovanou levou komoru – apikální dvoudutinová projekce. 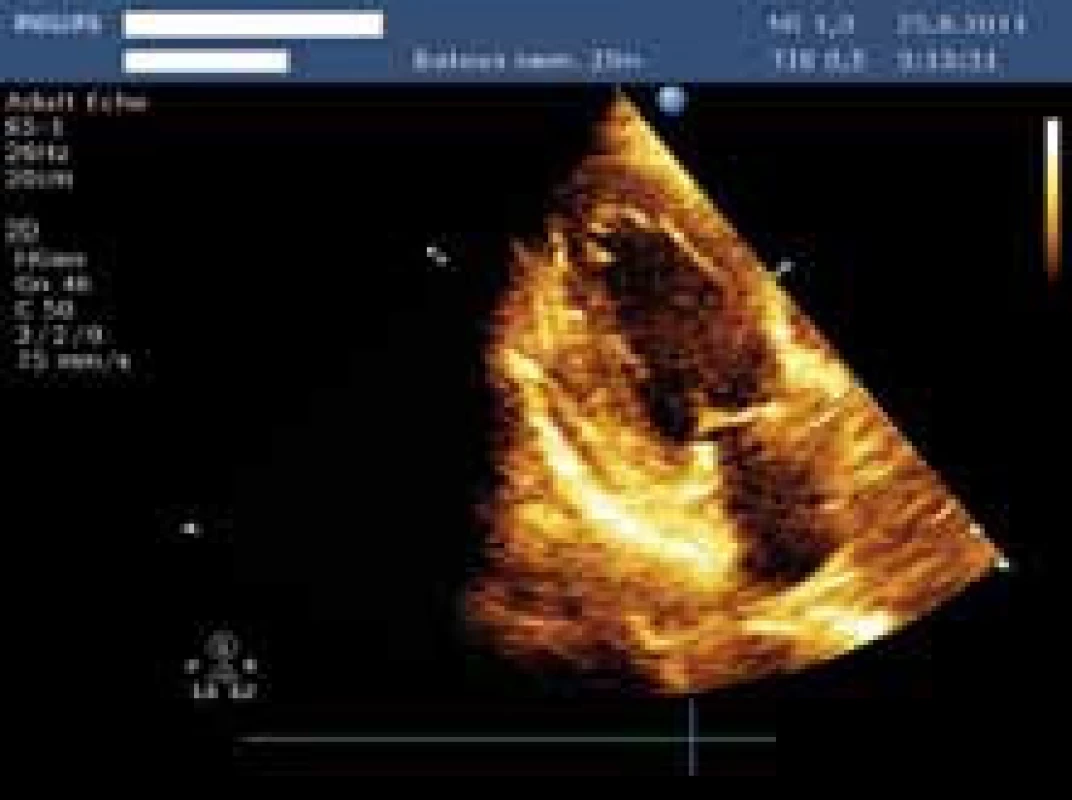
V terapii bylo pokračováno v podávání amiodaronu. Na EKG se po několika hodinách opět objevil běh setrvalé komorové tachykardie, pacient byl znovu elektricky defibrilován. Poté se na monitoru střídala sinusová tachykardie a flutter síní s rychlým převodem na komory. Ke kontrole frekvence byl přidáván metoprolol bolusově. Za 16 hod od přijetí byla na EKG opět setrvalá komorová tachykardie ústící do asystolie. Životní funkce pacienta se již nepodařilo obnovit.
Byla indikována patologicko-anatomická pitva: diagnostikován tumor levé ledviny o velikosti 12 × 9 × 6 cm, další ložisko v oblasti pravé nadledviny velikosti 10 × 10 × 8 cm expandující do pravého laloku jater. Zjištěna difuzní infiltrace myokardu ztlušťující stěny komor až na 17 mm (LK) a septum až 20 mm. Hrot levé komory byl relativně ušetřen, infiltráty se vyskytovaly více vpravo (obr. 6). Histochemicky se jednalo o nehodgkinský tumor – nejpravděpodobněji z plášťových buněk (obr. 7 a 8).
Obr. 6. Pitevní preparát srdce. 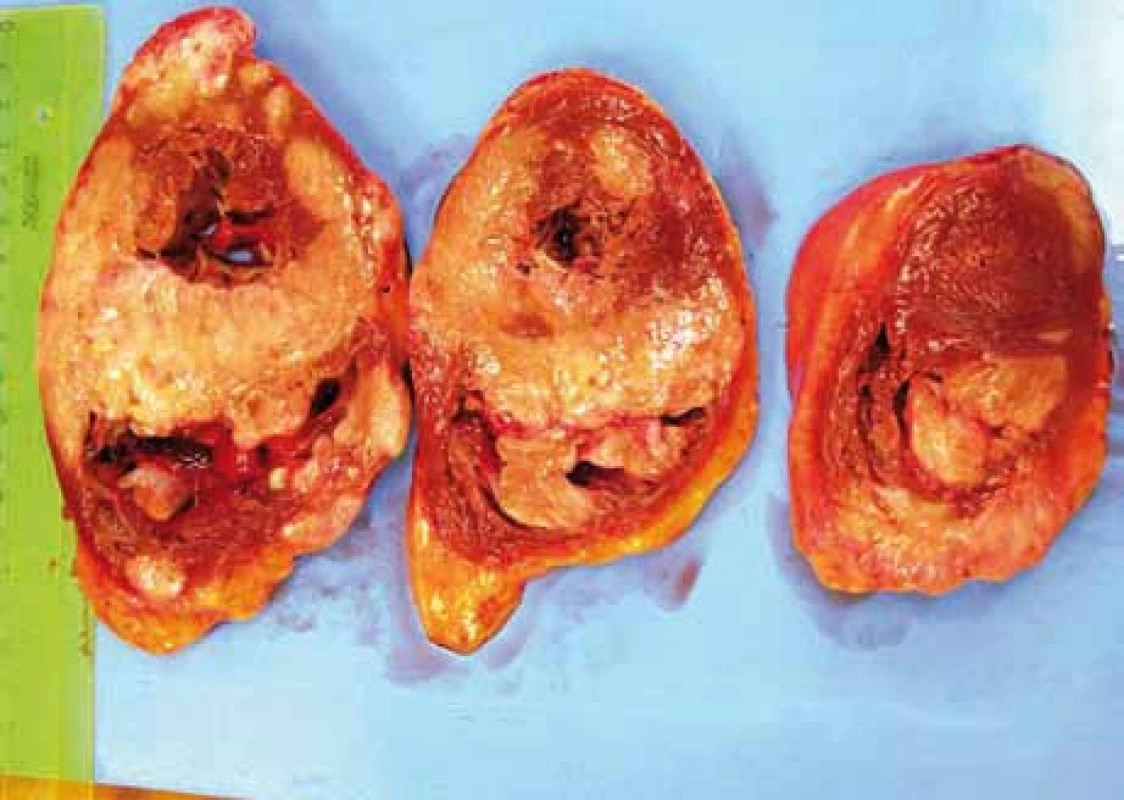
Obr. 7. Mikropreparát z myokardu zobrazující srdeční tkáň infiltrovanou lymfocyty. Barvení hematoxylin-eozin. 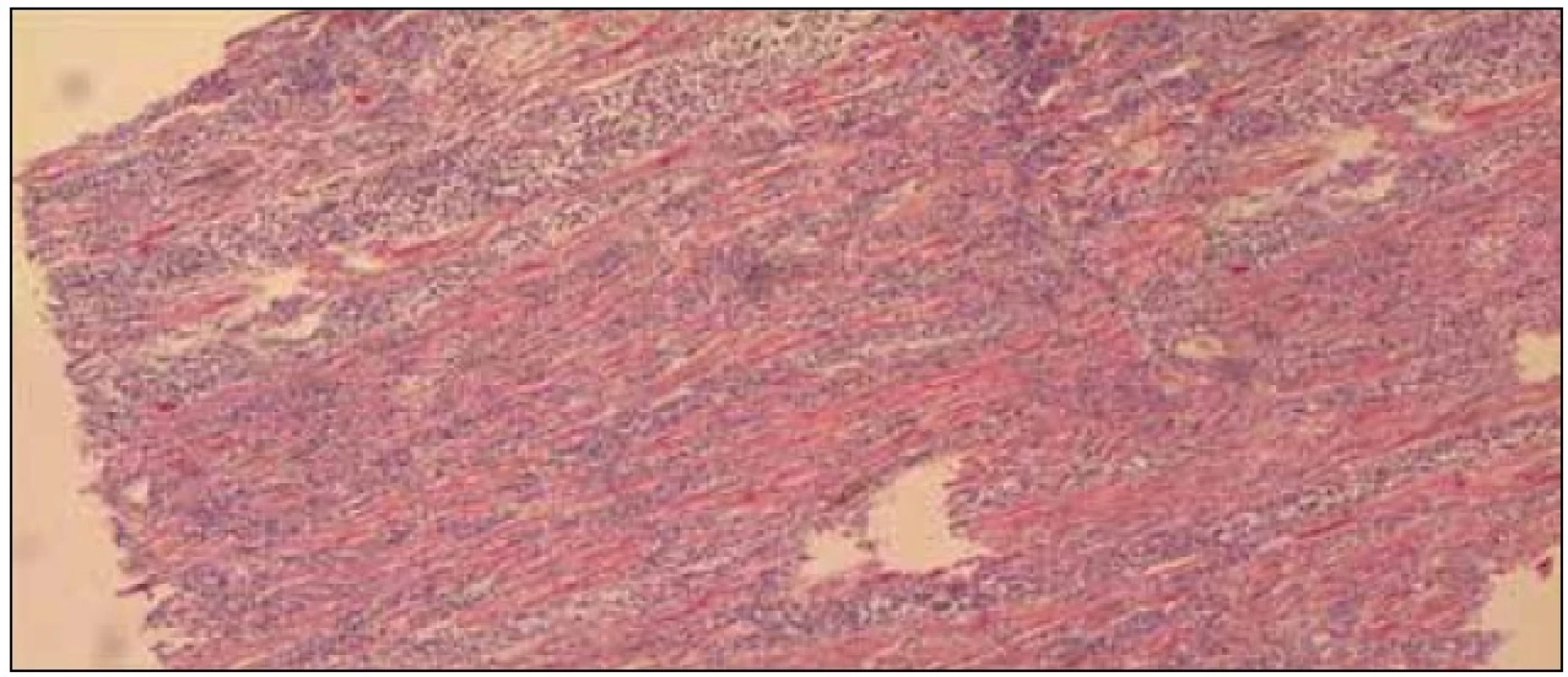
Obr. 8. Leukocyte common antigen (LCA) pozitivní buňky infiltrující myokard. 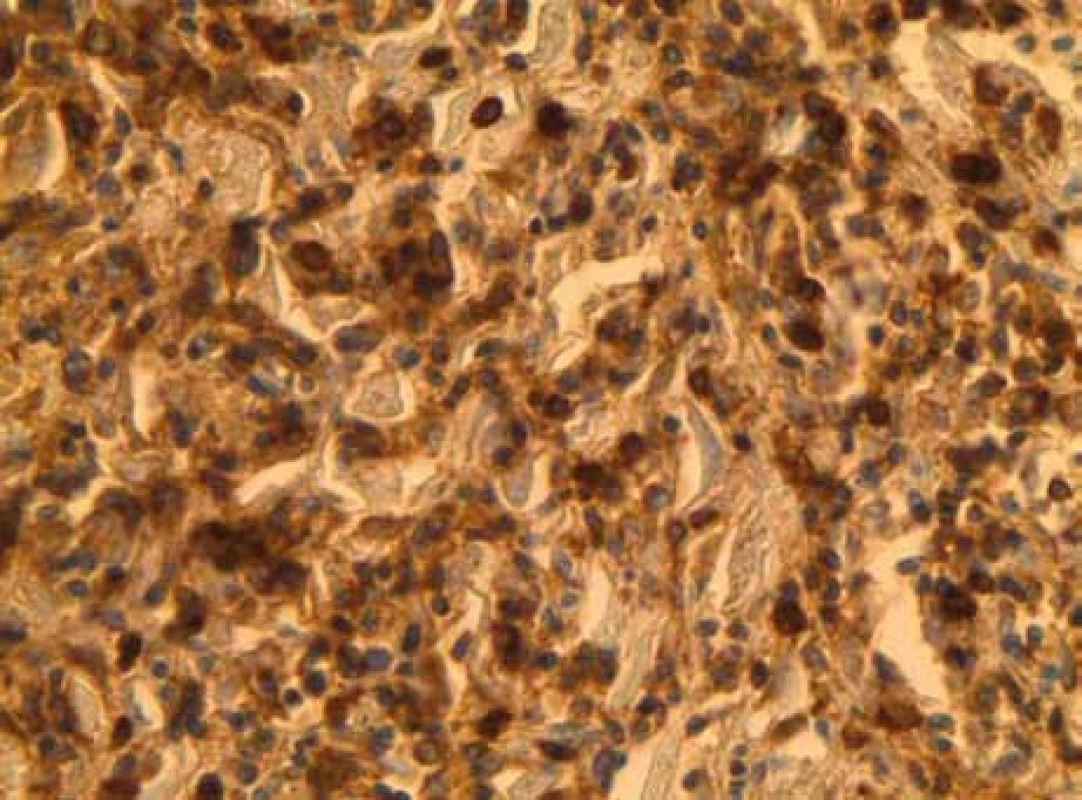
Diskuze
Sekundární postižení srdce se vyskytuje u 15–20 % osob s generalizovaným tumorem [3,4]. Metastatické postižení srdce může být difuzní, mnohouzlové nebo jednouzlové [3]. Naše práce se od jiných [6] odlišuje tím, že shodou náhod jsme měli k dispozici výsledky vyšetření z předchozí hospitalizace před rokem a nyní možnost je srovnat se základními vyšetřeními proveditelnými na koronární jednotce u lůžka pacienta. Perakutní průběh případu a oběhová nestabilita nemocného však neumožňovaly podrobnější diagnostiku ani léčbu.
V laboratoři jsme nově dokumentovali normochromní normocytární anémii, nižší byly hodnoty transamináz, lipidového spektra a albuminu. Na skiagramu hrudníku došlo k rozšíření srdečního stínu (obr. 3), které bylo dáno nádorovou infiltrací myokardu a přítomným perikardiálním výpotkem.
Při echokardiografickém vyšetření během hospitalizace na neurologii byl nález fyziologický s normálními rozměry (IVSd 12 mm, LVPWd 10 mm) i s normální funkcí LK (EF LK 65 %). Za rok došlo ke zdvojnásobení tloušťky stěn (IVSd 26 mm, LVPWd 21 mm) a poklesu systolické funkce na 20 %.
Tato hlavní morfologická změna se odrazila i na EKG. Na grafu získaném před rokem je PQ 0,16 s, QRS 0,08, QT 0,36, osa QRS –30°, ST úseky izoelektrické, negativní T vlny ve svodech II, III, VF, V4–6, přechodová zóna ve V3. Kmit S ve V3 dosahoval 8 mV. Na EKG nyní po kardioverzi je PQ prodlouženo na 0,2 s, QRS na 0,1 s, QT 0,36, nově deviace osy QRS doprava se vznikem levého zadního hemibloku, nově nesignifikantní 1 mV deprese ST ve svodech V4–5, polarita vln T se nezměnila, přechodová zóna se přesunula do V4. Prodloužení převodních intervalů a změnu elektrické osy lze vysvětlit změněnými elektrickými vlastnostmi neoplastické tkáně.
Na EKG došlo sice k zásadnímu nárůstu velikosti kmitu S ve V3 na 20 mV, voltážová kritéria pro hypertrofii levé komory podle obvyklých indexů však splněna nebyla (Cornell 21 mV, Sokolow-Lyon 17 mV, McPhie 31 mm, Lewis 1 mm). Právě nesoulad mezi jasnou hypertrofií stěn levé komory při echokardiografickém vyšetření a jejím chybění na elektrokardiogramu vždy vzbuzuje podezření na restriktivní kardiomyopatii [6], infiltrativní postižení myokardu – nejčastěji při amyloidóze, střádavých onemocněních, ale právě i při nádorové infiltraci.
Výše popsané regionální poruchy kinetiky a těžká deprese systolické funkce mají jasné vysvětlení v přeměně myokardu v nádorovou tkáň. Jak ukazují řezy srdcem, lze i makroskopicky rozpoznat, že funkční myokard zůstal zachován jen v hrotu a bazálních segmentech.
Předložená kazuistika je případem sekundárního nádorového onemocnění srdce, kdy jako primární ložisko byl označen nehodgkinský lymfom z oblasti horního pólu levé ledviny. V našem případě šlo v úzkém smyslu slova o prvozáchyt tohoto závažného onemocnění, byť se toto již více než 1/2 roku u nemocného projevovalo nechutenstvím, únavou a zejména váhovým úbytkem. Ambulantně byl rovněž před 1/2 rokem proveden EKG Holter, kdy byly zjištěny četné SVES, krátké paroxysmy supraventrikulární tachykardie, četné monomorfní KES, z nichž některé v kupletech a bigeminické vazbě. Maligní arytmie tehdy zaregistrovány nebyly. Tento záznam je ex post plně v souladu s nálezy pozorovanými při nádorovém postižení srdce [2,5].
Přestože byl pacient před rokem po propuštění z neurologie objektivně zdráv a paraklinická vyšetření v normě, za zhruba 1/2 roku se u něj začaly objevovat první příznaky závažného onemocnění. Tyto varující příznaky jej bohužel nepřiměly k návštěvě praktického lékaře, což vedlo k pozdní diagnóze onemocnění a k nevyhnutelně špatnému konci. Ačkoliv je prognóza lymfomů obecně špatná, lze spekulovat, že by časnější odhalení tohoto non--hodgkinského lymfomu mohlo vést k prodloužení života nemocného.
Závěr
Nádorová onemocnění srdce jsou obecně velmi vzácná. Vzhledem k tomu, že postihují ústřední orgán oběhu, je jejich nález u konkrétního pacienta zcela zásadní. Nádory srdce mohou život nemocného ohrožovat jednak svou povahou, jednak svou lokalizací. Čím časněji je nádor diagnostikován, tím může být prognóza pacienta příznivější. Klinické projevy srdečního nádoru mohou být buď orgánově specifické, nebo zcela nekonkrétní. Naše práce ukázala, jak důležitá je včasná analýza úplně nespecifických systémových projevů nádorového onemocnění. Přestože se možnosti diagnostiky velmi zlepšují a jsou stále dostupnější, vždy na prvním místě záleží na rozhodnutí a vůli nemocného. Bez tohoto zásadního atributu je pak veškerá snaha lékařů marná, což je i ústředním poselstvím námi popisovaného případu.
MUDr. Mgr. Lukáš Koten
www.bnzlin.cz
e-mail: koten@bnzlin.cz
Doručeno do redakce: 29. 1. 2012
Přijato po recenzi: 1. 5. 2012
Zdroje
1. Sheppard MN, Mohiaddin R. Tumors of the heart. Future Cardiol 2010; 6(2): 181–193.
2. Reynen K, Köckeritz U, Strasser RH. Metastases to the heart. Ann Oncol 2004; 15 : 375–381.
3. Šteiner I. Srdce a nádorová onemocnění. In: Vojáček J et al (eds). Klinická kardiologie. Hradec Králové: Nucleus 2009.
4. Táborská K, Linhart A. Nádory srdce In: Aschermann M et al (eds). Kardiologie. Praha: Galén 2004.
5. Daughenbaugh LA. Cardiomyopathy: an overview. J Nurse Pract 2007; 3 : 248–258.
6. Baratella MC, Calamelli S, D’Este D. Metastatic tumor of the heart: description of a case. J Cardiovasc Med (Hagerstown) 2011; 12 : 741–742.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2012 Číslo 9- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
- Splenektomie a sepse: pacienti musí být informováni o riziku, musí být vakcinováni a v určitých případech užívat profylakticky antibiotika
- Je možné snížit četnost závažných infekcí u pacientů po splenektomii?
- Leptospiróza
- Srovnání dvou metod dlouhodobého externího telemonitorování EKG po ablaci fibrilace síní
- Časný pohybový režim snižuje asymetrický dimetylarginin po transplantaci ledviny
- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
- Léková compliance – úskalí terapie revmatoidní artritidy?
- Peripartální život ohrožující krvácení – mezioborové konsenzuální stanovisko
- Upozornění na nebezpečí invazivních infekcí u splenektomovaných pacientů. Zkušenosti z FN Brno 2011
- Morbus Weil – kazuistika a princípy
- Nádor srdce manifestující se náhlou srdeční smrtí
- Naše zkušenosti s léčbou multicentrické plazmocelulární Castlemanovy choroby s projevy vaskulitidy – popis případu a přehled literatury
- Hyperventilační echokardiografie v diagnostice vazospastické anginy pectoris
- Aktuální poznatky o nových perorálních antikoagulanciích z Kongresu Evropské kardiologické společnosti v Mnichově (25.–29. 8. 2012)
- Zpráva o konání XVI. česko-slovenského hematologického a transfuziologického sjezdu a XIII. česko-slovenské konference laboratorní hematologie
- Prestižní cena pro jihočeské kardiocentrum
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
- Splenektomie a sepse: pacienti musí být informováni o riziku, musí být vakcinováni a v určitých případech užívat profylakticky antibiotika
- Upozornění na nebezpečí invazivních infekcí u splenektomovaných pacientů. Zkušenosti z FN Brno 2011
- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



