-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Studie RESOLUTE v České republice: inzulin glargin zlepšuje kompenzaci diabetu 2. typu u pacientů s dosud neuspokojivým výsledkem terapie kombinací inzulin detemir a perorální antidiabetika. Výsledky neintervenčního projektu RESOLUTE v České republice
RESOLUTE Study in the Czech Republic: insulin glargine improves the compensation of type 2 diabetes in patients with unsatisfactory results of therapy with a combination of insulin detemir and oral antidiabetics. Results of the non‑intervention RESOLUTE Project in the Czech Republic
Introduction:
The RESOLUTE was a multinational, non interventional, 6 month prospective observational project evaluating in clinical practice, whether patients with type 2 diabetes mellitus (T2DM) inadequately controlled with detemir in combination with oral anti‑diabetic drugs (OADs) may benefit from switching to glargine. In Czech Republic 200 patients, for whom the participating physician according to their own consideration, had decided to prescribe insulin glargine in replacement of insulin detemir, were included in this project.Objectives:
The primary endpoint was to assess the change in HbA1c over the 6 - month period in T2DM patients treated with insulin glargin after switch from insulin detemir. Secondary endpoints included the evaluation of the change in fasting plasma glucose, insulin dose, body weight over the 6-month period after starting insulin glargine , the evaluation of the number of hypoglycemia during the last month of therapy which each basal insulin and the frequency of adverse events (AE) during treatment with insulin glargine.Results:
Insulin glargine therapy resulted in a statistically significant improvement in compensation of diabetes characterized by a mean HbA1c decrease of about 0.82 (± 0.93) % (p < 0.001) and a mean decrease of recorded fasting glycemia about 1.91 (± 2.81) mmol/ l (p < 0.001). No significant change in the mean body weight was recorded during study [+0.12 (± 2.98) kg; p = NS]. The mean daily insulin glargine dose used at the end of the observation increased in comparison with last mean daily dose of insulin detemir [+2.99 (± 7.54) U; p < 0.001]. The improvement in glycemic control was accompanied by low risk of hypoglycemia. The percentage of patients with documented symptomatic (5.0%), nocturnal (2.5%) and severe (0%) hypoglycemia in the last month of glargine therapy was consistently lower compared with the last month of previous treatment with detemir (14.6%, 9.5% and 2.5%, respectively). Other adverse events were reported in 3.0% of patients on glargine therapy. No adverse events were considered as adverse event related to insulin glargin treatment. No serious adverse or no serious adverse events leading to treatment discontinuation or death were documented during the course of the study.Conclusion:
Under real‑life conditions, switching from insulin detemir to once ‑ daily insulin glargine in poorly controlled T2DM patients resulted in clinically relevant improvements in glycemic control without an increase in weight and hypoglycemia risk.Key words:
diabetes mellitus type 2 – insulin glargine – insulin detemir
Autori: M. Kvapil
Pôsobisko autorov: Interní klinika 2. lékařské fakulty UK a FN Motol Praha, přednosta prof. MU Dr. Milan Kvapil, CSc., MBA
Vyšlo v časopise: Vnitř Lék 2013; 59(9): 800-806
Kategória: Původní práce
Súhrn
Úvod:
Projekt RESOLUTE měl charakter mezinárodního, neintervenčního, prospektivního observačního projektu s délkou trvání 6 měsíců a měl za cíl zjistit v podmínkách běžné klinické praxe, zda pacienti s diabetem 2. typu (T2DM), jejichž onemocnění není dostatečně kontrolováno při léčbě inzulinem detemir v kombinaci s perorálními antidiabetiky, mohou mít prospěch z převedení na terapii inzulinem glargin.Metodika:
V České republice bylo do projektu RESOLUTE zařazeno celkem 200 pacientů, u kterých byla podle uvážení jejich lékaře zahájena léčba inzulinem glargin místo dosavadní léčby inzulinem detemir. Primárním cílem studie bylo zjištění změny HbA1c po 6 měsících od zahájení léčby inzulinem glargin. Sekundárními sledovanými parametry byla změna glykemie nalačno, změna tělesné hmotnosti během sledování, změna dávek inzulinu, počet hypoglykemických příhod a četnost všech nežádoucích příhod.Výsledky:
Při léčbě inzulinem glargin došlo ke statisticky významnému zlepšení kompenzace diabetu. Průměrná hodnota HbA1c poklesla o 0,82 (± 0,93) % (p < 0,001) a průměrná hladina glykemie nalačno poklesla o 1,91 (± 2,81) mmol/ l (p < 0,001). Změna tělesné hmotnosti nebyla v průběhu projektu statisticky významná [+0,12 (± 2,98) kg; p = NS]. Během sledování došlo k mírnému vzestupu průměrné denní dávky inzulinu glargin ve srovnání s poslední průměrnou denní dávkou inzulinu detemir [+2,99 (± 7,54) U; p < 0,001]. Zlepšení kompenzace diabetu bylo spojeno s nízkým rizikem hypoglykemie. Procento pacientů s dokumentovanou symptomatickou (5,0 %), noční (2,5 %) a závažnou hypoglykemií (0 %) bylo za poslední měsíc léčby s inzulinem glargin konzistentně menší ve srovnání s posledním měsícem léčby s inzulinem detemir (14,6 %; 9,5 %; 2,5 % pacientů). Nežádoucí příhody, jiné než hypoglykemie, byly zaznamenány u 3,0 % pacientů léčených glarginem a nebyly považovány za příhody příčinně související s podáváním inzulinu glargin. Závažné nežádoucí příhody ani nežádoucí příhody vedoucí k přerušení léčby nebo úmrtí nebyly během sledování hlášeny.Závěr:
Za podmínek běžné klinické praxe umožnil přechod z inzulinu detemir na inzulin glargin u nedostatečně kompenzovaných pacientů s T2DM intenzivnější kontrolu sledovaných parametrů kompenzace T2DM bez statisticky významného zvýšení tělesné hmotnosti a bez zvýšení rizika hypoglykemie.Klíčová slova:
diabetes mellitus 2. typu – inzulin glargin – inzulin detemirÚvod
Diabetes mellitus 2. typu (T2DM) je onemocnění, které je charakterizováno chronickou hyperglykemií v důsledku snížení senzitivity periferních tkání k inzulinu a omezenou funkcí Langerhansových ostrůvků [1]. Léčba tohoto onemocnění obvykle začíná změnami životního stylu a podáváním perorálních antidiabetik (PAD). Vzhledem k progresivnímu charakteru onemocnění a ztrátě funkce b - buněk potřebují pacienti často v určité fázi onemocnění zahájit terapii inzulinem pro dosažení nebo udržení cílových hladin HbA1c. Obvykle je cílem pro zahájení inzulinové terapie na základě patofyziologie T2DM kontrola glykemie nalačno [2]. Pro iniciaci inzulinoterapie se proto doporučuje zvolit bazální inzulin a přidat jej k léčbě PAD [3]. Zvoleným bazálním inzulinem může být inzulin typu NPH nebo dlouhodobě působící inzulinová analoga, inzulin glargin nebo inzulin detemir. Inzulin glargin je prvním inzulinovým analogem s dlouhodobým účinkem, který byl uveden do běžného užívání. Má předvídatelný a konstantní profil účinku s délkou trvání 24 hod. Podává se jednou denně, kdykoliv během dne, ale vždy ve stejnou dobu [4]. Inzulin detemir, v řadě další inzulinový analog s prodlouženým účinkem, který byl uveden do klinické praxe, má trvání účinku až 24 hod v závislosti na dávce, což umožňuje jeho podávání 1–2krát denně [5].
Bezpečnost a účinnost dlouhodobých inzulinových analog, která byla vyvinuta s cílem překonat limitace vyplývající z farmakokinetických parametrů humánního inzulinu, byla ve srovnání s inzulinem NPH hodnocena v mnoha randomizovaných klinických studiích. Metaanalýzy těchto studií nám potvrdily, že s inzulinovými analogy lze dosáhnout stejné úrovně kompenzace jako s NPH inzulinem, ale s významným snížením rizika hypoglykemie [6 – 8].
Při hodnocení dvou bazálních analog, na základě analýzy výsledků z publikovaných klinických studií realizovaných u pacientů s T2DM a dostupných zdrojů do ledna roku 2011, se výsledná kompenzace diabetu (glykemie nalačno, glykovaný hemoglobin), celkové riziko nočních a závažných hypoglykemií při srovnání s 1krát nebo 2krát denně podávaným detemirem a 1krát denně podávaným inzulinem glargin signifikantně nelišila. Léčba inzulinem detemir byla spojena s nižším hmotnostním přírůstkem, zatímco léčba inzulinem glargin vedla k celkovému snížení dávky bazálního inzulinu a omezení počtu reakcí v místě vpichu [9]. Výsledky nedávné klinické studie však ukázaly, že inzulin glargin více redukoval HbA1c ve srovnání s inzulinem detemir, když byly obě bazální analoga podávána po celou dobu sledování u pacientů s T2DM 1krát denně [10].
Zatímco výsledky randomizovaných klinických studií poskytují základ pro klinickou praxi, výsledky observačních studií nám ukazují, nakolik jsou výsledky randomizovaných klinických studií přenosné do každodenní praxe [11]. Observační studie, které byly realizované u pacientů se špatně kompenzovaným T2DM, ukázaly zlepšení hladin HbA1c při přechodu na inzulin glargin [12] nebo inzulin detemir [13].
Cílem předkládaného observačního projektu RESOLUTE (Real Life of Efficacy and Safety of Insulin Glargine in Patients with 2 Diabetes, Previously Treated with Insulin Detemir and Not Adequately Controlled) bylo zjistit v podmínkách běžné klinické praxe, zda pacienti se špatně kompenzovaným T2DM při léčbě inzulinem detemir ± PAD mohou mít užitek z převedení na léčbu inzulinem glargin ± PAD.
Metody
Design studie
RESOLUTE byla multinárodní, neintervenční, prospektivní studie s přibližnou délkou sledování pacientů 6 měsíců. Studie probíhala v 88 centrech a 5 zemích světa, mezi které se vedle Nizozemska, Polska, Ruska a Argentiny řadila také Česká republika. Projekt byl realizován v době mezi červnem roku 2010 a listopadem roku 2011. V souladu s neintervenčním charakterem projektu nebyl stanoven pevný režim návštěv. Data byla získávána od ambulantních pacientů v ambulancích, kde byla vedena jejich léčba diabetu. Za první návštěvu v rámci studie (vstupní návštěva) byla považována návštěva, při níž došlo k převedení pacienta na glargin, nebo návštěva, která následovala za méně než 4 týdny od zahájení léčby glarginem. Lékaři dále zaznamenávali údaje o vývoji stavu pacientů a kompenzaci diabetu přibližně za 3 a 6 měsíců od zahájení terapie inzulinem glargin.
Tato práce hodnotí výsledky u pacientů, kteří byli zařazeni do projektu v České republice.
Kritéria vstupu pro lékaře
Na projektu v České republice spolupracovalo celkem 40 lékařů, aktivně ordinujících ambulantních diabetologů z celého území České republiky, kteří souhlasili se svou účastí v tomto projektu a byli obeznámeni s protokolem studie (příloha 1).
Příloha 1. Projekt RESOLUTE. Seznam lékařů. 
Pro omezení možné chyby spojené s výběrem pacientů měl každý lékař zahrnout do projektu pacienty, kteří přicházeli k ošetření konsekutivně a kteří splnili kritéria pro vstup do projektu v následujících 6 měsících po iniciační návštěvě. Každý lékař mohl zařadit do projektu minimálně 3 a maximálně 20 pacientů.
Výběr pacientů
V rámci projektu bylo v České republice celkem sledováno 200 pacientů s diabetem 2. typu. Do studie mohli být zařazeni pacienti s diabetem 2. typu starší 18 let, kteří byli léčeni po dobu alespoň 3 měsíců inzulinem detemir ± PAD, jejichž HbA1c byl ≥ 7,0 % a < 10,0 % (DCCT) a kterým jejich ošetřující diabetolog předepsal inzulin glargin místo inzulinu detemir v posledních 4 týdnech před vstupní návštěvou nebo při vstupní návštěvě v souladu se souhrnem informací o přípravku (SPC) inzulin glargin. Vylučovací kritéria zahrnovala léčbu jiným inzulinem než detemirem před záměnou za inzulin glargin, potřebu jiného inzulinu než inzulinu glargin v době změny bazálního inzulinu a těhotenství v době vstupu do studie. Hodnocení účinnosti bylo provedeno u pacientů, kteří splnili vstupní kritéria pro zařazení do projektu a kteří projekt dokončili, tzn. u 199 pacientů. Hodnocení bezpečnosti bylo provedeno u všech 200 pacientů zařazených do projektu.
Studie probíhala v souladu se standardy pro sběr dat v klinických studiích definovaných Helsinskou deklarací, v souladu s českou legislativou a byla ohlášena Státnímu ústavu pro kontrolu léčiv (SÚKL) před jejím zahájením. Každý pacient podepsal před zahájením sběru dat písemný informovaný souhlas.
Primární a sekundární cíle
Primárním cílem studie bylo zjištění změny HbA1c po 6 měsících od zahájení léčby inzulinem glargin. Sekundárními sledovanými parametry byla změna glykemie nalačno (FPG), změna tělesné hmotnosti během sledování, změna dávek inzulinu, počet hypoglykemických příhod a četnost všech ostatních nežádoucích příhod.
Údaje byly získávány z výpovědí a záznamů pacientů a ze zdravotní dokumentace ošetřujících lékařů. Základní hodnotou pro HbA1c a pro glykemii nalačno (získanou při selfmonitoringu pacienta nebo laboratorní analýzou) byla poslední hodnota získaná před převedením na inzulin glargin. Počet epizod hypoglykemií byl zaznamenán v období 4 týdnů před zařazením do projektu a srovnáván s obdobím 4 týdnů před jednotlivými následnými kontrolami.
Dokumentovaná symptomatická hypoglykemie byla definována jako příhoda s klinickými symptomy, o níž se předpokládalo, že byla způsobena hypoglykemií a byla potvrzena naměřenou hodnotou glykemie ≤ 3,9 mmol/ l získanou při selfmonitoringu pacienta.
Vážná symptomatická hypoglykemie byla definována jako příhoda s klinickými symptomy, o kterých se předpokládalo, že jsou způsobeny hypoglykemií a které vyžadovaly pomoc jiné osoby pro aktivní podání cukru, glukagonu nebo jiného opatření a byla spojena s naměřením hodnoty glykemie < 2 mmol/ l nebo byla spojena s odezněním neurologických symptomů, které lze přisoudit obnově glykemie na normální hodnoty po perorálním podání sacharidu, po aplikaci glukagonu nebo po nitrožilním podání glukózy.
Noční hypoglykemie byla událost, která proběhla u pacienta během doby jeho spánku od doby večerního ulehnutí do ranního vstávání.
Dávkování inzulinu glargin během sledování u jednotlivých pacientů odpovídalo standardní praxi jejich ošetřujících lékařů.
Statistické zpracování
Analýzy byly provedeny ve statistickém programu SAS, verze 9.2 (SAS Institute, Inc., Cary, Severní Karolína, USA). Výsledky v této publikaci jsou prezentovány pro celou skupinu pacientů zařazených do projektu v České republice a v podskupinách v souladu s předchozím užíváním detemiru 1krát nebo 2krát denně a bez vzájemného porovnání mezi těmito podskupinami. Všechna data byla komentována a analyzována za použití metod deskriptivní statistiky. Pro hodnocení rozdílu od vstupních hodnot byl použit Wilcoxonův test. Pro hodnoty HbA1c a FPG byly kalkulovány oboustranné 95% intervaly spolehlivosti.
Prezentované výsledky jsou uvedeny jako průměrné hodnoty nebo jako průměrná hodnota (± směrodatná odchylka).
Výsledky
Demografické charakteristiky pacientů zařazených do projektu jsou uvedeny v tab. 1. Průměrný věk pacientů byl při zařazení do projektu 64 let s dobou trvání diabetu 9,0 roků. Průměrná vstupní tělesná hmotnost byla 90,8 kg a body mass index (BMI) 31,5 kg/ m2. Většinu pacientů tvořily ženy (52,3 %). Více pacientů užívalo původně inzulin detemir 1krát denně (n = 176; 88,4 %) a téměř všichni pacienti při vstupu do projektu užívali v kombinaci s bazálním inzulinem detemir alespoň 1 PAD (96,5 %). Tímto PAD byl zejména metformin (85,9 %) a/ nebo derivát sulfonylurey (63,3 %). Po změně bazálního analoga na inzulin glargin a během následné 6měsíční léčby zůstala tato terapie ve většině případů zachována. Stejné procento pacientů užívalo dále alespoň 1 PAD a metformin. Se změnou bazálního analoga se mírně snížil počet pacientů užívajících sulfonylureu (60,8 %).
Tab. 1. Demografická a vstupní charakteristika. 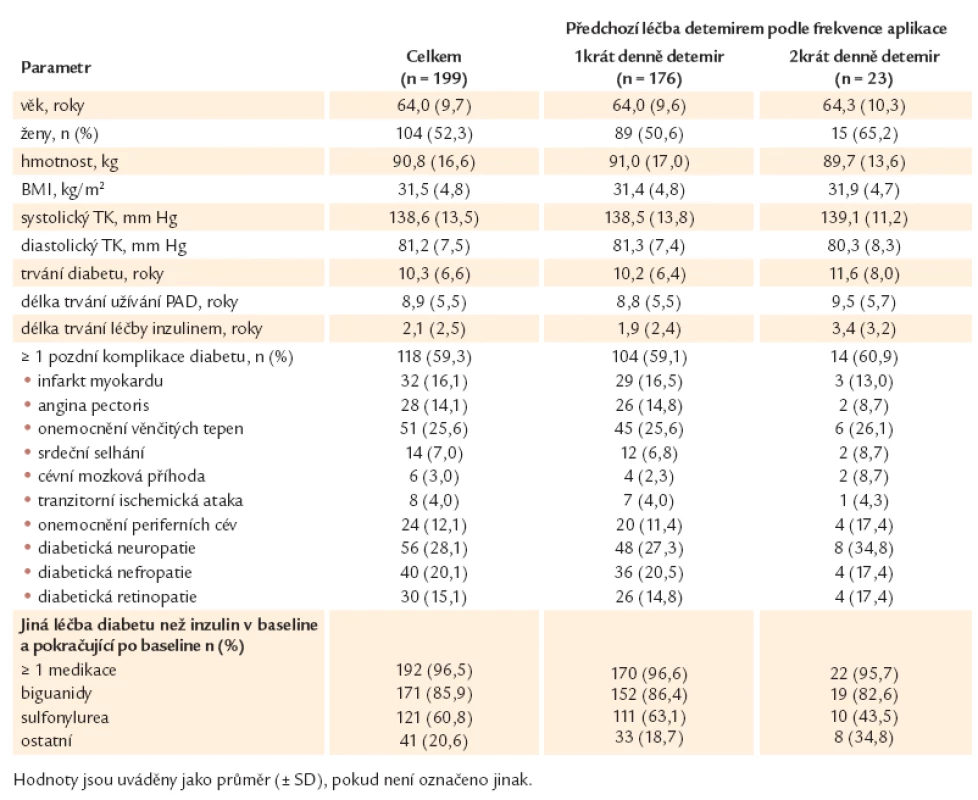
Mezi nejčastějšími důvody pro převedení pacientů na inzulin glargin patřily nedostatečná dosavadní kompenzace diabetu při léčbě detemirem, mnohočetná aplikace inzulinu během dne, nárůst hmotnosti a hypoglykemie během léčby s inzulinem detemir.
Kompenzace diabetu
V celé skupině pacientů převedené na inzulin glargin došlo ke snížení hladiny HbA1c (DCCT) z průměrné hodnoty 8,61 % při vstupu do studie na hodnotu 8,0 % a 7,79 % po 3 a 6 měsících léčby (graf 1A). Po 6 měsících tedy došlo k signifikantnímu absolutnímu poklesu průměrného HbA1c o 0,82 % (p < 0,001) s tím, že u pacientů, kteří původně užívali detemir 1krát denně, byl zaznamenán průměrný absolutní pokles HbA1c o 0,84 % (p < 0,001), a u pacientů, kteří původně užívali detemir 2krát denně o 0,67 % (p = 0,0113). Změny HbA1c v průběhu sledování jsou znázorněny na grafu 1.
Graf 1. Změna HbA<sub>1c</sub> (A) and FPG (B) v průběhu sledování. Hodnoty jsou uvedeny jako průměr. 
Hladina FPG se v celé skupině pacientů snížila z průměrné vstupní hodnoty 9,49 mmol/ l na 7,73 a 7,54 mmol/ l po 3 a 6 měsících léčby s inzulinem glargin (graf 1B). Průměrná FPG signifikantně poklesla po 6 měsících léčby s inzulinem glargin o 1,91 mmol/ l (p < 0,001) v celé skupině pacientů, resp. o 1,88 (p < 0,001) a 2,09 mmol/ l (p = 0,0012) u pacientů původně užívajících detemir 1krát a 2krát denně. Změny FPG v průběhu sledování jsou znázorněny na grafu 1.
Dávky bazálních analog v průběhu sledování
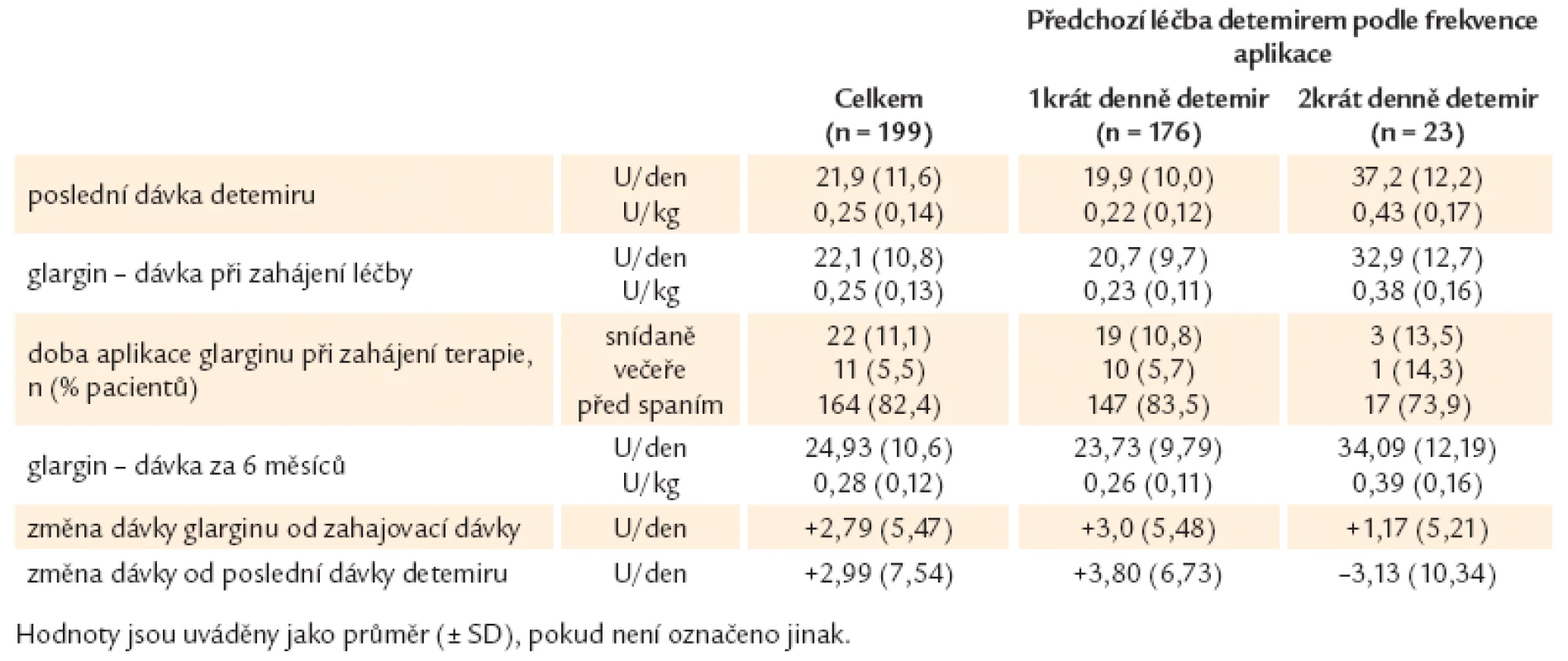
Průměrná denní dávka bazálního inzulinu glargin byla při hodnocení celé skupiny pacientů na konci 6měsíčního sledování mírně vyšší ve srovnání s poslední průměrnou dávkou inzulinu detemir o 2,99 U (p < 0,001). Při vztažení k hmotnosti pacientů byla dávka zvýšena o 0,03 U/ kg (p < 0,001). U pacientů původně užívajících detemir 1krát denně byl zaznamenán vzestup dávky o 3,8 U (p < 0,001), u pacientů původně užívajících detemir 2krát denně byl naopak zaznamenán statisticky nesignifikantní pokles dávky o 3,13 U (p = 0,3664). Bližší vývoj dávek aplikovaných inzulinů během sledování je uveden v tab. 2. Inzulin glargin byl podáván ve většině případů (99 %) 1krát denně, obvykle večer. Dva pacienti (1,0 %) užívali inzulin glargin 2krát denně, oba byli ze skupiny léčené původně detemirem 2krát denně.
Změny hmotnosti
Po 6 měsících užívání inzulinu glargin byl zaznamenán v celé skupině pacientů mírný statisticky nesignifikantní vzestup hmotnosti o 0,12 kg. Stejně tak tomu bylo ve skupině pacientů původně léčené detemirem 1krát denně, kde vzestup hmotnosti činil 0,21 kg (p = NS). Naopak u skupiny léčené původně detemirem 2krát denně byl zaznamenán statisticky nesignifikantní pokles hmotnosti o 0,56 kg.
Bezpečnost
Zlepšení kompenzace diabetu při léčbě s inzulinem glargin bylo spojeno s nižším výskytem hypoglykemických příhod. Hypoglykemickou příhodu zaznamenalo během posledního měsíce léčby s inzulinem glargin méně pacientů ve srovnání s předchozí léčbou inzulinem detemir.
Procento pacientů s alespoň 1 epizodou dokumentované symptomatické, noční nebo vážné hypoglykemie bylo během posledních 4 týdnů léčby s inzulinem glargin 5 %, 2,5 % a 0 % a s inzulinem detemir 14,6 %, 9,5 % a 2,5 %. Výskyt hypoglykemií je znázorněn na grafu 2.
Graf 2. Hypoglykemie během posledních 4 týdnů při léčbě glarginem nebo detemirem. Procento pacientů s dokumentovanou hypoglykemií během posledních 4 týdnů terapie. 
U 6 pacientů (3 %) byly hlášeny během léčby s inzulinem glargin jiné nežádoucí příhody než hypoglykemie (v 50 % infekční etiologie). Žádná tato příhoda nebyla investigátorem považována za příhodu skutečně související s podáváním inzulinu glargin. Závažné nežádoucí příhody či nežádoucí příhody vedoucí k přerušení léčby nebo úmrtí nebyly během sledování hlášeny.
Diskuze
Výsledky observační klinické studie RESOLUTE v České republice ukazují, že pacientům s T2DM, kteří jsou špatně kompenzováni při léčbě PAD a inzulinem detemir, může záměna inzulinu detemir za inzulin glargin v klinické praxi statisticky signifikantně zlepšit kontrolu glykemie, aniž by došlo k významnějšímu zvýšení hmotnosti a ke zvýšení rizika hypoglykemií. Oba sledované parametry kompenzace diabetu (HbA1c a glykemie nalačno) byly po 6 měsících léčby inzulinem glargin statisticky signifikantně zlepšeny ve srovnání se stavem při předchozí léčbě inzulinem detemir. Tyto výsledky odpovídají výsledkům celého mezinárodního projektu RESOLUTE, kde byl zaznamenán po 6měsíční léčbě inzulinem glargin pokles HbA1c o 1,1 % a pokles glykemie nalačno o 2,1 mmol/ l [14].
Podobných výsledků jako ve studii RESOLUTE bylo nedávno dosaženo v klinické praxi v Dánsku, kdy byl přechod z inzulinu detemir na glargin spojen se zlepšením glykemické kompenzace a celkovým zlepšením stavu pacienta, navzdory mírnému zvýšení BMI [16].
Na rozdíl od výsledků klinických randomizovaných studií [15] nebyla při léčbě inzulinem glargin v projektu RESOLUTE zaznamenána výraznější změna hmotnosti. Ve skupině pacientů, kteří původně užívali detemir 2krát denně, byl zaznamenán s inzulinem glargin pokles hmotnosti o 0,56 kg, zatímco ve skupině pacientů, kteří užívali detemir původně 1krát denně, byl zaznamenán mírný vzestup hmotnosti < 0,2 kg, stejně jako v celém souboru pacientů. Tyto změny nebyly statisticky významné a nemohou být považovány ani za klinicky významné.
Zlepšení kompenzace diabetu bylo ve studii RESOLUTE v České republice dosaženo s mírným navýšením dávky inzulinu glargin, kdy konečná průměrná dávka inzulinu glargin byla zvýšena o 0,03 U/ kg hmotnosti ve srovnání s poslední průměrnou aplikovanou dávkou inzulinu detemir. Tento rozdíl je klinicky nevýznamný, v žádném případě nemůže vysvětlit zlepšení glykovaného hemoglobinu. Navýšení dávky je pod hranicí změny dávky, která je obvykle používána pro titraci u pacientů s diabetem 2. typu. Stejně tak se tento rozdíl neodrazil ve změně tělesné hmotnosti.
Důležitá je v tomto kontextu skutečnost, že zlepšení kompenzace diabetu nebylo spojeno v projektu RESOLUTE se zvýšením incidence dokumentovaných symptomatických, nočních a vážných hypoglykemií, jak bychom mohli předpokládat na základě výsledků klinických randomizovaných studií, ale že zlepšení kompenzace bylo spojeno se snížením incidence u všech těchto kategorií hypoglykemie a že výskyt hypoglykemií při léčbě s inzulinem glargin můžeme označit celkově za nízký, neboť nízké riziko hypoglykemie vytváří prostor pro dosažení těsné kompenzace diabetu a zvyšuje complianci a adherenci pacientů k léčbě.
Naše studie má stejně jako všechny observační studie svá omezení [8]. Navzdory svým omezením mohou ale observační studie poskytovat cenné informace, které vhodně doplňují výsledky randomizovaných klinických studií [9].
Přestože se zdá, že mezi skupinami pacientů léčenými původně 1 nebo více dávkami detemiru existují rozdíly, není možné z této skutečnosti vyvozovat závěry vzhledem k tomu, že tyto skupiny nebyly randomizovány.
Závěr
Lze shrnout, že za podmínek běžné klinické praxe byl přechod z inzulinu detemir v kombinaci s PAD na inzulin glargin u nedostatečně kompenzovaných pacientů s T2DM spojen se signifikantním zlepšením kompenzace diabetu bez zvýšení tělesné hmotnosti a s nízkou incidencí hypoglykemie.
Dnes můžeme konstatovat, že glargin je bazální inzulin s více než 10 lety klinických důkazů v léčbě diabetu a je bazálním inzulinem, který můžeme označit jako referenční dlouhodobě působící inzulinový analog s prokázanou kardiovaskulární bezpečností [17].
Tato studie byla sponzorována společností Sanofi.
prof. MU Dr. Milan Kvapil, CSc., MBA
www.fnmotol.cz
e‑mail: milan.kvapil@fnmotol.cz
Doručeno do redakce: 29. 4. 2013
Přijato po recenzi: 19. 7. 2013
Zdroje
1. Nathan DM, Buse JB, Davidson MB et al. Medical management of hyperglycaemia in type 2 diabetes mellitus: a consensus algorithm for the initiation and adjustment of therapy: a consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetologia 2009; 52 : 17 – 30.
2. Holman RR, Farmer AJ, Davies MJ et al. Three‑year efficacy of complex insulin regimens in type 2 diabetes. N Engl J Med 2009; 361 : 1736 – 1747.
3. Inzucchi SE, Bergenstal RM, Buse JB et al. Management of hyperglycaemia in type 2 diabetes: a patient ‑ centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia 2012; 55 : 1577 – 1596.
4. SPC přípravku Lantus [online]. SÚKL [cit. 22 – 12 – 2012]. Dostupné z: www.sukl.cz.
5. SPC přípravku Levemir [online]. SÚKL [cit. 22 – 12 – 2012]. Dostupné z: www.sukl.cz.
6. DeVries JH, Meneghini L, Barnett A et al. Pooled Hypoglycemia Event Rates With Inzulin Glargine Added to Metformin (IG ‑ M) from Treat ‑ to ‑ Target Type 2 Diabetes Mellitus (T2DM) Trials. Diabetes 2012; 61 (Suppl 1): A552 – A553.
7. Home PD, Fritsche A, Schinzel S et al. Meta‑analysis of individual patient data to assess the risk of hypoglycaemia in people with type 2 diabetes using NPH insulin or insulin glargine. Diabetes Obes Metab 2010; 12 : 772 – 779.
8. Mullins P, Sharplin P, Yki ‑ Jarvinen H et al. Negative binomial meta‑regression analysis of combined glycosylated hemoglobin and hypoglycemia outcomes across eleven Phase III and IV studies of inzulin glargine compared with neutral protamine Hagedorn inzulin in type 1 and type 2 diabetes mellitus. Clin Ther 2007; 29 : 1607 – 1619.
9. Swinnen SG, Simon AC, Holleman F et al. Inzulin detemir versus inzulin glargine for type 2 diabetes mellitus. Cochrane Database Syst Rev 2011: CD006383.
10. Effect of Insulin Detemir and Insulin Glargine on Blood Glucose Control in Subjects With Type 2 Diabetes (EFFICACY) [online] [cit. 26 – 11 – 2012]. Available from: http:/ / clinicaltrials.gov/ ct2/ show/ NCT00909480.
11. Ligthelm RJ, Borzi V, Gumprecht J et al. Importance of observational studies in clinical practice. Clin Ther 2007; 29 : 1284 – 1292.
12. Hajos TR, Pouwer F, de Grooth R et al. The longitudinal association between glycaemic control and health‑related quality of life following insulin therapy optimisation in type 2 diabetes patients. A prospective observational study in secondary care. Qual Life Res 2012; 8 : 1359 – 1365.
13. Meneghini L, Koenen C, Weng W et al. The usage of a simplified self ‑ titration dosing guideline (303 Algorithm) for insulin detemir in patients with type 2 diabetes – results of the randomized, controlled PREDICTIVE 303 study. Diabetes Obes Metab 2007; 9 : 902 – 913.
14. Liverse AG, Rodriguez M, Czupryniak L et al. Glycaemic control of Type 2 diabetics with insulin glargine in everyday practice: Type 2 diabetic patients poorly controlled on insulin detemir therapy benefit from switching to insulin glargine. Diabetes Stoff Herz 2013; 22 : 141 – 147.
15. Rosenstock J, Davies M, Home PD et al. A randomised, 52‑week, treat ‑ to ‑ target trial comparing insulin detemir with insulin glargine when administered as add ‑ on to glucose‑lowering drugs in insulin‑naive people with type 2 diabetes. Diabetologia 2008; 51 : 408 – 416.
16. Veneman TF, Storms FEMG, Eland IA et al. From insulin detemir to glargine: Effect on glycemic control and psychological wellbeing in patients with diabetes mellitus type 2 in daily practice. J Diabetes Mellitus 2012; 2 : 101 – 108.
17. The ORIGIN trial investigators. Basal insulin and cardiovascular and other outcomes in dysglycemia. N Engl J Med 2012; 367 : 319 – 328.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2013 Číslo 9- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Využití natriuretických peptidů v diagnostice hypertrofie levé komory u obézních hypertoniků s metabolickým syndromem – editorial
- Jak zlepšit adherenci k lékovému režimu u klinicky komplexních polymorbidních seniorů? Editorial
- Vede fyzická aktivita při přerušení dodávky inzulinu inzulinovou pumpou u pacientů s diabetem 1. typu ke klinicky významným změnám?
- Využití natriuretických peptidů v diagnostice hypertrofie levé komory srdeční u obézních hypertoniků s metabolickým syndromem
- Význam stanovení kardiálních biomarkerů ve stratifikaci a sledování nemocných s AL‑ amyloidózou – zkušenosti jednoho centra
- Hodnocení vybraných ukazatelů apoptózy a angiogeneze u chronické lymfocytární leukemie
- Compliance starších nemocných s kognitivní poruchou
- Studie RESOLUTE v České republice: inzulin glargin zlepšuje kompenzaci diabetu 2. typu u pacientů s dosud neuspokojivým výsledkem terapie kombinací inzulin detemir a perorální antidiabetika. Výsledky neintervenčního projektu RESOLUTE v České republice
- Food intake regulation – 1st part
- Doporučení České endokrinologické společnosti pro léčbu Cushingova syndromu v dospělosti
- Cold agglutinin disease – no response to glucocorticoids and rituximab, what treatment is best for the 3rd line of therapy? Case report and review of the literature
- Regionální migrující osteoporóza – diferenciálně diagnostický problém
- Nová data a indikace pro sulodexid
-
ERS 2013
Duální bronchodilatace aneb Ve dvou (se) to lépe táhne - Dabigatran – klinická zkušenost z více než dvou miliónů pacientoroků
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Cold agglutinin disease – no response to glucocorticoids and rituximab, what treatment is best for the 3rd line of therapy? Case report and review of the literature
- Food intake regulation – 1st part
- Nová data a indikace pro sulodexid
- Doporučení České endokrinologické společnosti pro léčbu Cushingova syndromu v dospělosti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy