Porovnání přínosu FGM a CGM pro jednotlivé klinické situace u pacientů s diabetes mellitus 1. typu
Comparison of the benefits of FGM and CGM for different clinical scenarios in patients with type 1 diabetes mellitus
Rapid fluctuations of blood glucose in DM type 1 require precise and user friendly devices for selfmonitoring. This paper describes principles and differences between continuous (CGM) and flash (FGM) glucose monitoring, particular advantages and disadvantages, including overview of published studies.
Keywords:
continuous glucose monitoring – CGM – flash glucose monitoring – FGM – type 1 diabetes mellitus – glycemic variability – hypoglycaemia
:
Krčma M.
:
1. interní klinika FN PLzeň
:
Kardiol Rev Int Med 2019, 21(1): 29-32
Vysoká variabilita glykemie u diabetes mellitus 1. typu vyžaduje přesné a jednoduše použitelné nástroje pro selfmonitoring. Článek popisuje principy a rozdíly fungování přístrojů pro kontinuální (CGM) a okamžitou (FGM) monitoraci glykemie, vč. výhod a nevýhod pro jednotlivé klinické situace, a shrnutí publikovaných klinických studií.
Klíčová slova:
kontinuální monitorace glykemie – CGM – okamžitá monitorace glykemie – FGM – diabetes mellitus 1. typu – glykemická variabilita – hypoglykemie
Diabetes mellitus (DM) a zejména diabetes mellitus 1. typu (DM1) je onemocnění, u něhož nacházíme relativně rychlé kolísání glykemie v krvi. Nediabetický organizmus řeší homeostázu glukózy rychlými změnami vlastní sekrece inzulinu a glukagonu (a některých dalších hormonů) v závislosti na hladině glukózy. U inzulin dependentních diabetiků se s jistou nadsázkou stává regulátorem mozek pacienta, senzorem nějaké zařízení k měření glykemie (typicky glukometr) a akčními členy ruka s inzulinovým perem a s kostkou cukru.
Znalost své glykemie a optimálně i znalost dostatečného počtu hodnot předcházejících, aby se dalo uvažovat o trendu, je pro diabetika zásadní. Osobní glukometr je docela mladé zařízení; první byl na trh uveden v r. 1987 a i přesto, že se měnily používané metody měření z fotometrických na elektrochemické, což umožnilo snížit potřebu objemu kapilární krve na necelou tisícinu mililitru, zůstal princip stejný do dnešní doby. Vždy je nutné získat kapku krve vpichem do podkoží (prstu, předloktí), tu nasát speciálním testovacím proužkem, v němž proběhne reakce a několik sekund čekat na zobrazení aktuální změřené hladiny na displeji.
Dobrá kompenzace DM je přímo úměrná počtu měření a tato závislost trvá až do počtu 10–13 měření glukometrem denně. Odhlédneme-li od ceny testovacích proužků, samotná bolestivost a nepraktičnost invazivních měření podnítila hledání jiných cest monitorace. První systém kontinuální monitorace byl schválen americkým Úřadem pro kontrolu potravin a léčiv v r. 1999. Principem není měření koncentrace glukózy v kapilární krvi, jako u běžných glukometrů, ale v intersticiální tekutině v podkoží. Kanyla senzoru, která nese enzymy potřebné pro měření, je zavedena několik milimetrů do podkožní tkáně. Koncentrace glukózy je o něco opožděna za glykemií z krve, v závislosti na rychlosti změny glykemie kolem 5–13 min [1]. Vývoj rozdělil kontinuální senzory na dvě velké skupiny – kontinuální monitory glykemie (continuous glucose monitoring – CGM) a okamžité monitory glykemie (flash glucose monitoring – FGM). Obě platformy se liší spíše způsobem nakládání s naměřenými daty než technickým principem.
Kontinuální monitorace glykemie
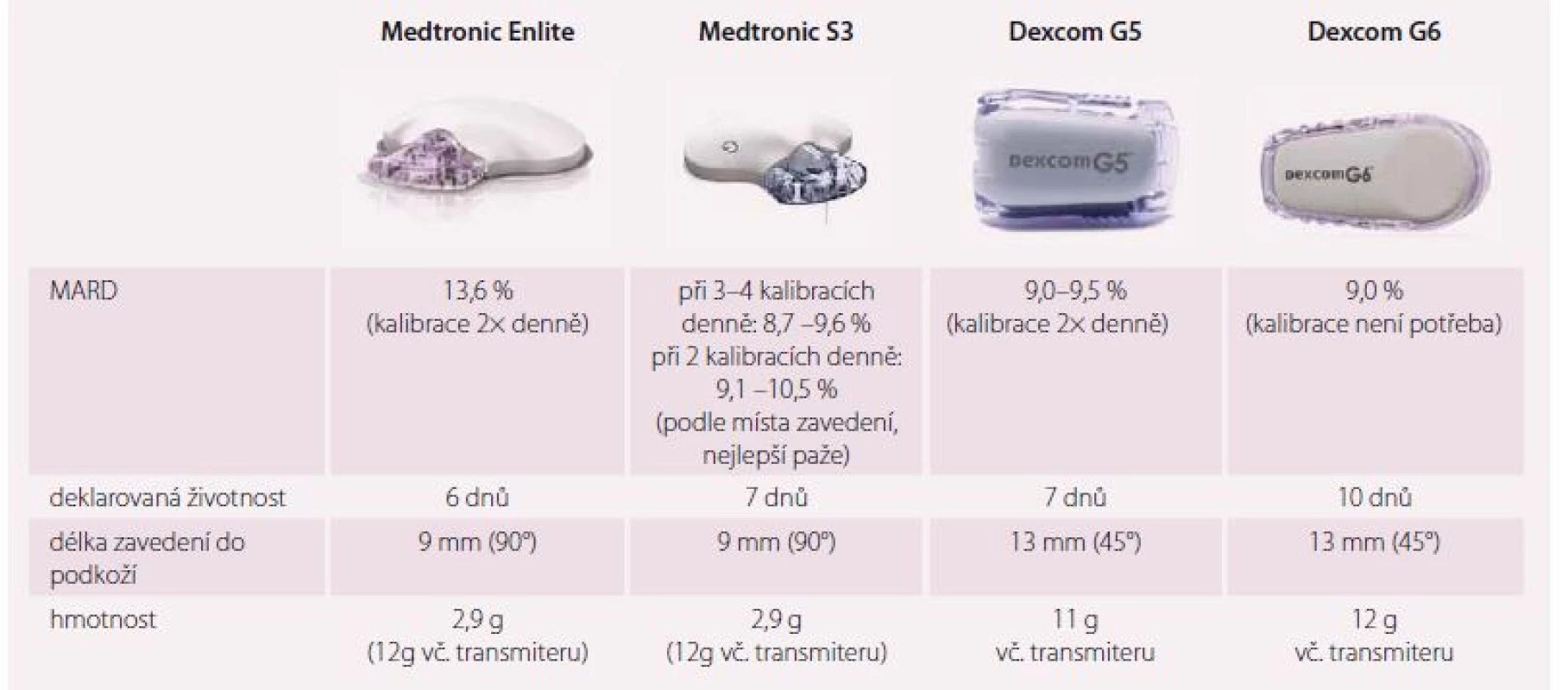
Hlavní součástí CGM je senzor s cca 6–7denní životností, připojený k transmitteru s celkovou hmotností zhruba 7–11 g dle konkrétního typu. Je možno ho zavést do podkoží tam, kde je dostatek tkáně (paže, ramena, boky, břicho, hýždě, stehna). Naměřená data se přenáší bezdrátovým přenosem (bluetooth) do zobrazujícího zařízení, kterým může být inzulinová pumpa nebo mobilní telefon. Většinu senzorů je potřeba kalibrovat pomocí klasického glukometru, 2× denně v době, kdy nedochází k prudké změně glykemie. Na trh se blíží i senzor bez nutnosti kalibrace (Dexcom G6), nicméně dosavadní uživatelské zkušenosti hovoří o vhodnosti kalibrace i v tomto případě. Kontinuální senzory poskytují hladinu glukózy každých 5 min, hlavní výhodou proti ostatním typům měření je znalost nejen okamžité hodnoty, ale i trendu a použití alarmů při překročení nastavené rychlosti změny glykemie nebo nastavené hodnoty. Aktuální přehled v ČR dostupných (nebo chystaných) zařízení ukazuje tab. 1. Data pocházejí z materiálů výrobců a nezávislých studií, především přehledné shrnující práce z letošního roku [2,3].
Efektivita CGM u diabetiků 1. typu byla v minulosti prokázána řadou prací s velmi konzistentními výsledky, za všechny zmíním randomizovanou českou studii COMISAIR [4], která během roční léčby vstupně relativně dobře kompenzovaných pacientů dosáhla použitím kontinuální monitorace zlepšení glykovaného hemoglobinu z 67 mmol/ mol na 54 mmol/ mol, ať už byla senzorová technologie přidána k inzulinové pumpě nebo intenzifikovanému režimu (MDI). Samotný převod z intenzifikovaného režimu na inzulinovou pumpu (bez CGM) v této studii zlepšil kompenzaci pacientů pouze o 5 mmol/ mol.
Využití CGM léčby zůstává limitováno na určitou podskupinu diabetiků 1. typu; dle dat z T1D Exchange registru, se počet pacientů léčených za pomocí senzorové technologie zvýšil ze 7 % (2010–2012) na 30 % (2016 –2018). Sledovaný soubor pacientů zahrnoval především děti a mladé diabetiky (56 % pod 18 let věku).
Okamžitá monitorace glykemie
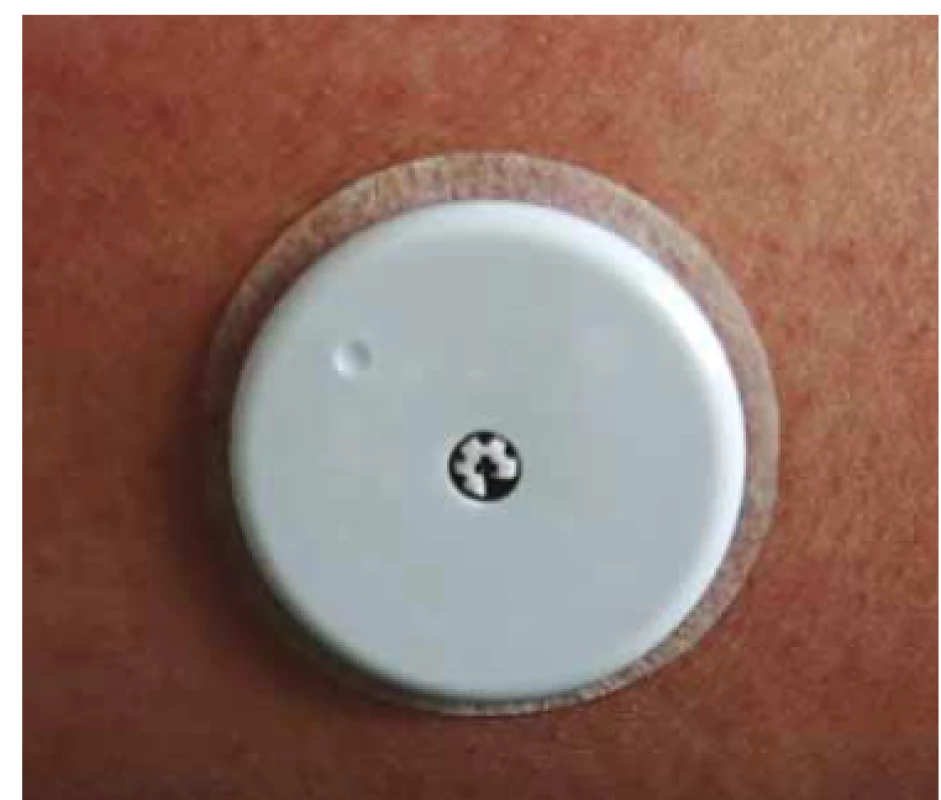
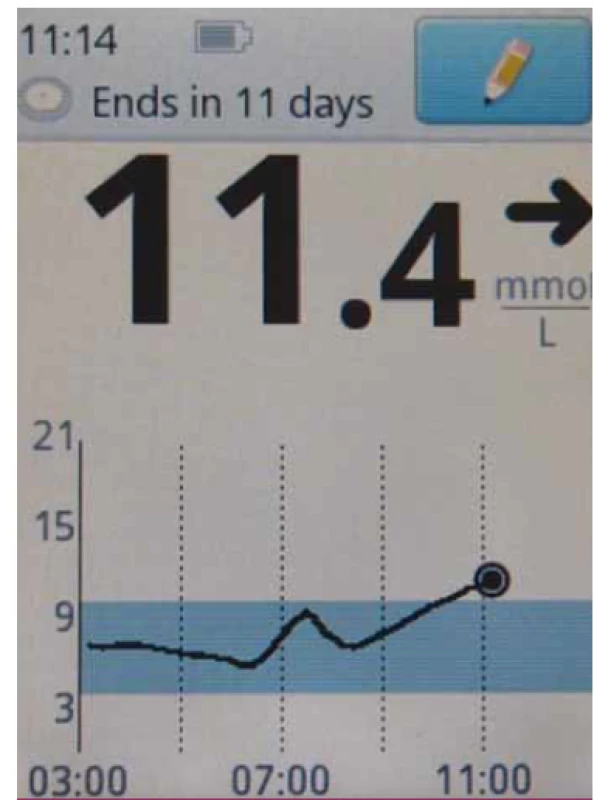
Technický princip je podobný, jde také o senzor, jehož elektronika je nalepena na kůži (u Freestyle Libre (tab. 2, obr. 1, 2), jediného dostupného zástupce v ČR, pouze na kůži paže), s vláknem kolmo zasahujícím do podkoží. Životnost senzoru je 14 dnů. Senzor poskytuje data každých 15 min a přenáší je do čtečky pomocí NFC technologie s dosahem několika cm; při každém naskenování dat je potřeba přejet čtečkou v blízkosti senzoru a načtou se data z posledních 8 hod. Starší data senzor přepisuje. Čtečka má paměť na 90 dnů záznamu a zároveň slouží jako glukometr pro klasické testovací proužky. První senzory Libre byly dostupné v září 2014 v sedmi zemích EU a postupně se pokrytí rozšiřuje; aktuálně je technologie Libre dostupná ve 46 zemích, ve 33 má částečnou nebo plnou úhradu ze zdravotního pojištění u diabetiků 1. typu a ve 21. zemích u diabetiků 2. typu, s různými indikačními kritérii a omezujícími podmínkami [2].

Masový rozmach FGM dokonce vedl v ČR k převisu poptávky nad nabídkou a způsobil několikaměsíční výpadek čteček, který se firmě podaří nejspíše vyřešit v dubnu letošního roku. Situace dle mého názoru ilustruje, jak velký přelom FGM technologie znamená; naši pacienti získávají přístroj s řadou funkcí kontinuálního monitoru, ale se složitostí glukometru a významně menší bolestivostí měření. Další rozšíření této technologie v ČR lze očekávat koncem roku, kdy nové úhradové podmínky sníží doplatky pacientů na nulu.
Hodně se diskutuje o přesnosti FGM a o možnosti jeho kalibrace. Zatím není výrobcem doporučena, nicméně analýza několika desítek pacientů [5] ukazuje, že existují systematické chyby u jednotlivých pacientů – určitá část vykazuje proti měření glukometrem nižší a mnohem menší část systematicky vyšší hodnoty. Zde by jistě kalibrace zpřesnila měření. Obdobné výsledky přinesla nezávislá analýza 39 pacientů s DM1, kde by se průměrná odchylka (MARD) 12,3 % dala při korekci systematické bias (a tedy při individuální kalibraci na konkrétního pacienta) snížit na 9,2 % [6]. Částečně zřejmě pomůže plánovaná změna výrobního postupu senzoru, kdy bude výrobní linka kalibrovat každý senzor nezávisle, lze očekávat i dle předběžných informací výrobce MARD 9,5 %. Přesnost FGM záleží na dni měření. První den většinou senzor glykemii podhodnocuje a teprve od 2. dne začíná měřit zcela přesně, proto bývá uváděna MARD zvlášť za 14 dnů a zvlášť za 1. den.
První kvalitní studií kvantifikující efekt FGM u diabetiků 1. typu byla studie IMPACT [7], která zařadila 167 výborně kompenzovaných diabetiků 1. typu (glykovaný Hb ≤ 58 mmol/ l) s dobou trvání nemoci > 5 let. Vyřazeni byli pacienti se syndromem nevnímání hypoglykemie. Pacienti byli randomizováni 1 : 1 do FGM větve a větve s klasickým selfmonitoringem glukometrem. Během 6 měsíců studie nedošlo ke změně dlouhodobé kompenzace měřené glykovaným hemoglobinem, v intervenované skupině se prodloužil čas v cílovém rozmezí (3,9–10,0 mmol/ l) o 0,9 hod/ den a snížil se čas strávený v hypoglykemii < 3,9 mmol/ l) z 3,44 hod/ den na 1,86 hod/ den. Pacienti ve skupině s FGM se skenovali zhruba 15× denně, v kontrolní skupině měli pacienti v průměru 5,5 měření glukometrem denně. Před randomizací byl průměrný počet měření glukometrem reportovaný pacienty 5,2× denně.
V loňském roce byla publikována roční observační studie z reálné praxe u 120 diabetiků 1. typu, kteří používali výhradně FGM (v kombinaci s intenzifikovaným inzulinovým režimem) a byli lékařsky kontrolováni v obvyklých 3měsíčních intervalech [8]. Předchozí frekvence selfmonitoringu – necelá 3 měření denně – se zvýšila na necelých 9 skenů denně a kompenzace DM se zlepšila z vstupních 69 mmol/ mol glykovaného hemoglobinu na 63 mmol/ mol po 1 roce. Mírně narostl počet lehkých hypoglykemií ze 17 měsíčně na 24 měsíčně, přičemž lehká hypoglykemie byla definována jako glykemie < 3,9 mmol/ l bez ohledu na symptomy. Těžká hypoglykemie se během ročního sledování nevyskytla. Nezměnila se celková denní dávka inzulinu, ale došlo k snížení dávky bazálu a navýšení prandiálního inzulinu, změna byla nejvyšší u pacientů s horší kompenzací.
Ještě lepší výsledky ukázala výrobcem podpořená analýza dat z let 2014–2017 z téměř 51 tisíc čteček FGM [9]. Bylo analyzováno více než 279 tisíc senzorů. Uživatelé se skenovali v průměru 14× (10–20×) denně, přitom došlo k poklesu průměrného glykovaného hemoglobinu z 64 na 50 mmol/ mol, adekvátní měrou se zvýšil čas v cílovém rozmezí glykemie 3,9–10 mmol/ l z 12 na 16,8 hod během dne. Poklesl počet hypoglykemií ve všech sledovaných pásmech. V této studii nemáme žádné informace o předchozím selfmonitoringu pacientů.
Efektivita CGM a FGM
Technologie FGM je relativně nová a přímých srovnávacích dat máme poměrně málo. Nepřítomnost alarmů může handicapovat FGM především v hypoglykemické oblasti. První randomizované srovnání vysoce rizikové populace (Gold skóre > 4 nebo čerstvá anamnéza těžké hypoglykemie) bylo publikováno jako I HART CGM studie před 2 lety [10], kdy byla u 40 pacientů s dlouhotrvajícím DM (21–36 let) randomizovaně zvolena léčba FGM vs. CGM. Během 8 týdnů sledování nedošlo u výborně kompenzovaných nemocných (glykovaný Hb 48–63 mmol/ mol) ke změně kompenzace DM. Skupina léčená CGM snížila více procento času stráveného v hypoglykemickém rozmezí, a to ve všech sledovaných oblastech (např. pro glykemii < 3,3 mmol/ l před CGM 4,5 % času, s CGM 2,4 %), u skupiny léčené FGM čas v hypoglykemii zůstal stejný (6,7 vs. 6,8 %).
Návazné sledování, kdy byly obě skupiny pacientů léčené otevřeným CGM, bylo publikováno v loňském roce [11]. Ve skupině, která přešla z FGM na CGM, došlo k významné redukci času stráveného v hypoglykemii (< 3,3 mmol/ l) z 6,8 % času na 1,5 % času. Prodloužil se čas v cílovém rozmezí glykemie (3,9–10,0 mmol/ l) z 60 na 67 %. Ve skupině, která zůstala na CGM, k dalším změnám nedošlo.
Obě technologie mají některé společné problémy. Jedním z nich jsou lokální reakce, iritační dermatitida nebo otlaky. Výskyt alergických reakcí se hrubě odhaduje do 5 % pacientů, zkušenosti z našeho pracoviště jsou obdobné.
Diabetes mellitus 2. typu
Jednoduchost použití a nižší náklady proti CGM svádí k použití FGM i u dlouhotrvajícího DM 2. typu (DM2) s vyčerpanou sekrecí inzulinu, jehož principy léčby se v mnohém podobají DM1. Studie REPLACE [12] zařadila 224 pacientů randomizovaných 2 : 1 k léčbě FGM vs. klasický selfmonitoring, šlo o pacienty léčené intenzifikovaným inzulinovým režimem nebo inzulinovou pumpou, kompenzace byla průměrná (glykovaný Hb 73 ± 11 mmol/ mol). Pacienti neabsolvovali zvláštní edukaci na FGM. Intervenovaná skupina prakticky nepoužívala glukometr, počet skenů byl zhruba 8× denně, tedy o něco méně než u diabetiků 1. typu v předešlých studiích. Kontrolní skupina měla v průměru 3,8 měření glukometrem denně. Během 6 měsíců studie nedošlo k významné změně glykovaného hemoglobinu celkově, ve skupině mladších pacientů pod 65 let věku vedla léčba FGM k malému statisticky významnému zlepšení kompenzace (proti kontrolní skupině < 3,5 mmol/ mol). Změnil se čas strávený v hypoglykemii (o 0,47 hod/ den v glykemii < 3,9 mmol/ l) při léčbě FGM. Dalším rozdílem bylo zlepšení kvality života měřené dotazníkem DTSQ v intervenční skupině.
V loňském roce byla publikována i farmakoekonomická studie ze Švédska, která využila data ze studie REPLACE, aby namodelovala užití FGM v porovnání s běžnými glukometry. Zjednodušeně, léčba FGM poskytovaná po dobu 40 let svým účinkem na pokles počtu hypoglykemií i při nezměněné kompenzaci DM2 prodlužuje život v plném zdraví (QALY) o 0,56 roku. Cena tohoto prodloužení (29 762 € / QALY) je pod hranicí považovanou ve Švédsku za nákladově únosnou (38 894 € / QALY). V ČR ani jeden ze systémů kontinuální či okamžité monitorace nemá u pacientů s DM2 úhradu ze zdravotního pojištění.
Kterou technologii, pro kterého pacienta?
Při výběru technologické léčebné modality je potřeba na prvním místě zvažovat individuální preferenci a dovednosti pacienta. Dle mého subjektivního pohledu, technologie CGM se svou kalibrací, možností/ nutností pohledu na glykemii jako kontinuální proměnnou a nikoli izolovanou hodnotu, akcentací trendů a alarmů při rychlých změnách glykemie, bude vhodnější více pro technicky gramotné jedince (nebo rodiče), kteří jsou ochotni DM věnovat hodně systematické práce. Naproti tomu na FGM lze pohlížet jako na nebolestivý a poměrně jednoduchý glukometr, s benefitem znalosti glykemií á 15 min v předchozích 8 hod od skenování, nehrozí zde únava z alarmů a „vyrušování“ DM z běžného života.
Na druhém místě stojí otázka, co od monitoringu žádáme? Výborně kompenzovaný pacient, frekventně se měřící glukometrem, který řeší především prevenci a léčbu hypoglykemií při fyzické aktivitě, bude zřejmě více profitovat z kontinuální monitorace, zejména, bude-li ji používat v kombinaci s inzulinovou pumpou s prediktivními algoritmy (PLGM) vypínání (či v budoucnu úpravy) bazální dávky. Pacient se syndromem nevnímání hypoglykemie je také adeptem kontinuální monitorace – alarmy (event. PLGM) jsou to, co ho dělí od těžkých hypoglykemií. Nakonec i studie IMPACT právě diabetiky neschopné vnímat hypoglykemii nezařazovala. Děti, kde do dávkování inzulinu zasahují rodiče, a kde není 100% compliance s častým skenováním, jsou také spíše kandidáty na léčbu CGM, obdobně jako sportovci, kde při neobvyklé a velké fyzické zátěži jsou alarmy rychlosti změny glykemie nezastupitelné [13].
Naproti tomu hůře kompenzovaný pacient, jemuž v kvalitním používání flexibilního režimu brání bolestivost a nepohodlnost měření glykemie z kapky krve, a kde snaha zkompenzovat diabetes naráží na limitovaný čas se cukrovkou zabývat, bude z monitorace FGM profitovat. Složitější CGM by jej mohl zbytečně odradit.
Na třetím místě jsou finance. Technologie FGM přináší pacientovi (a zdravotnímu systému) nižší náklady, v současné době je doplatek pacienta na senzory 800 Kč měsíčně, jednorázová investice do čtečky je 400 Kč. CGM s sebou přináší náklady zhruba o 1/3–1/2 vyšší. V případě, že nemáme jiné závažnější rozhodovací kritérium, je na místě zvažovat i finanční nákladnost.
Doručeno do redakce: 17. 3. 2019
Přijato po recenzi: 19. 3. 2019
MU Dr. Michal Krčma, Ph.D.
Sources
1. Schmelzeisen-Redeker G, Schoemaker M, Kirchsteiger H et al. Time Delay of CGM sensors. J Diabetes Sci Technol 2015; 9(5): 1006–1015. doi: 10.1177/ 1932296815590154.
2. Avari P, Reddy M, Oliver N. Is it possible to constantly and accurately monitor blood sugar levels, in people with Type 1 diabetes, with a discrete device (non-invasive or invasive)? Diabet Med 2019. Epub ahed of print. doi: 10.1111/ dme.13942.
3. Christiansen MP, Garg SK, Brazg R et al. Accuracy of a fourth-generation subcutaneous continuous glucose sensor. Diabetes Technol Ther 2017; 19(8): 446–456. doi: 10.1089/ dia.2017.0087.
4. Šoupal J, Petruželková L, Flekač M et al. Comparison of different treatment modalities for type 1 diabetes, including sensor-augmented insulin regimens, in 52 weeks of follow-up: a COMISAIR Study. Diabetes Technol Ther 2016; 18(9): 532–538. doi: 10.1089/ dia.2016.0171.
5. Koide K, Azuma K, Nojima J et al. Practical guidance for treatment of patients with diabetes using flash glucose monitoring: a pilot study. Diabetol Metab Syndr 2018; 10(1): 63. doi: 10.1186/ s13098-018-0364-z.
6. Staal O, Hansen H, Christiansen SC et al. Differences between flash glucose monitor and fingerprick measurements. Biosensors 2018; 8(4): E93. doi: 10.3390/ bios8040093.
7. Oskarsson P, Antuna R, Geelhoed-Duijvestijn P et al. Impact of flash glucose monitoring on hypoglycaemia in adults with type 1 diabetes managed with multiple daily injection therapy: a pre-specified subgroup analysis of the IMPACT randomised controlled trial. Diabetologia 2018; 61(3): 539–550. doi: 10.1007/ s00125-017-4527-5.
8. Paris I, Henry C, Pirard F et al. The new FreeStyle libre flash glucose monitoring system improves the glycaemic control in a cohort of people with type 1 diabetes followed in real-life conditions over a period of one year. Endocrinol Diabetes Metab 2018; 1(3): e00023. doi: 10.1002/ edm2.23.
9. Dunn TC, Xu Y, Hayter G et al. Real-world flash glucose monitoring patterns and associations between self-monitoring frequency and glycaemic measures: A European analysis of over 60 million glucose tests. Diabetes Res Clin Pract 2018; 137 : 37–46. doi: 10.1016/ j.diabres.2017.12.015.
10. Reddy M, Jugnee N, Anantharaja S et al. Switching from flash glucose monitoring to continuous glucose monitoring on hypoglycemia in adults with type 1 diabetes at high hypoglycemia risk: the extension phase of the I HART CGM study. Diabetes Technol Ther 2018; 20(11): 751–757. doi: 10.1089/ dia.2018.0252.
11. Reddy M, Jugnee N, El Laboudi A et al. A randomized controlled pilot study of continuous glucose monitoring and flash glucose monitoring in people with type 1 diabetes and impaired awareness of hypoglycaemia. Diabet Med 2018; 35(4): 483–490. doi: 10.1111/ dme.13561.
12. Haak T, Hanaire H, Ajjan R et al. Flash glucose-sensing technology as a replacement for blood glucose monitoring for the management of insulin-treated type 2 diabetes: a multicenter, open-label randomized controlled trial. Diabetes Ther 2017; 8(1): 55–73. doi: 10.1007/ s13300-016-0223-6.
13. Adolfsson P, Parkin CG, Thomas A et al. Selecting the appropriate continuous glucose monitoring system – a practical approach. Eur Endocrinol 2018; 14(1): 24. doi: 10.17925/ EE.2018.14.1.24.
Labels
Paediatric cardiology Internal medicine Cardiac surgery CardiologyArticle was published in
Cardiology Review

2019 Issue 1
-
All articles in this issue
- The most common causes of hospitalisation and death in patients with diabetes – results of the National Diabetology Registry
- Study DECLARE confirmed positive effect of dapagliflozin
- CANVAS – canagliflozin and cardiovascular or renal influence for diabetes mellitus type 2
- Diabetes mellitus and cancer – UPDATE
- Screening of asymptomatic carotid atherosclerosis in diabetic patients and its association with ankle-brachial index
- Comparison of the benefits of FGM and CGM for different clinical scenarios in patients with type 1 diabetes mellitus
- Could we soon have the final evidence of cardiovascular safety of DPP-4 inhibitors?
- Complex management of diabetic patients with membrovascular arterial disease and multiorganomultivascular disease
- Adherence to therapy in arterial hypertension
- The role of nebivolol in the treatment of cardiovascular diseases
- Cardiology Review
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Comparison of the benefits of FGM and CGM for different clinical scenarios in patients with type 1 diabetes mellitus
- The role of nebivolol in the treatment of cardiovascular diseases
- The most common causes of hospitalisation and death in patients with diabetes – results of the National Diabetology Registry
- Screening of asymptomatic carotid atherosclerosis in diabetic patients and its association with ankle-brachial index