-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Multianalytový přístup k diagnostice srdečních chorob technologií proteinových biočipů
Multi-marker approach in the diagnostics of cardiac diseases by protein biochip technology
Background.
Multi-marker approach is recommended for rapid diagnostics and risk stratification of acute coronary syndrome. We tested the analytical performance of protein biochip technology for determination cardiac markers.Methods. Analysis of cardiac markers:
CK-MB mass, cTnI, myoglobin, glycogen phosphorylase BB (GPBB), heart type of fatty acid binding protein (h-FABP) and carbonic anhydrase III (CAIII) was performed by system Evidence Investigator (Randox). Analytical parameters of Cardiac array were tested. The Evidence Investigator results were compared with Elecsys 2010 (Roche) CK-MB mass and myoglobin methods. Markers of myocardial injury were determined in 28 blood donors, 28 patients with acute myocardial infarction diagnosis and 21 patients after chemotherapy containing anthracyclines (monitoring of cardiotoxicity).Results.
The Passing-Bablok regression shows statistically significant differences in results. The reasons for these differences are poor standardization of methods and discrepancies between calibrations. New substances h-FABP and GPBB are promising early markers of acute myocardial infarction and diagnostic sensitivity of h-FABP would be better than myoglobin test. These markers can be useful for monitoring of cardiotoxicity of anthracyclines.Conclusions.
In future, the use of biochip technology in cardiology diagnostic represents an important challenge but it is a necessary standardization of immunochemical methods.Key words:
protein biochip, cardiac marker, cardiotoxicity, myocardial infarction.
Autoři: M. Vašatová 1; M. Tichý 1; Horáček Jm 2,3; R. Pudil 4; L. Horáková 4; V. Palička 1
Působiště autorů: Univerzita Karlova v Praze, LF a FN Hradec Králové, Ústav klinické biochemie a diagnostiky 1; Univerzita obrany Hradec Králové, Fakulta vojenského zdravotnictví, Katedra válečného vnitřního lékařství 2; Univerzita Karlova v Praze, LF a FN Hradec Králové, II. interní klinika, Oddělení klinické hematologie 3; Univerzita Karlova v Praze, LF a FN Hradec Králové, I. interní klinika 4
Vyšlo v časopise: Čas. Lék. čes. 2009; 148: 591-596
Kategorie: Původní práce
Souhrn
Východisko.
Multianalytový přístup je doporučován pro rychlou diagnostiku a stratifikaci rizika akutního koronárního syndromu. Testovali jsme analytickou vhodnost technologie proteinových biočipů pro stanovení kardiálních markerů.Metody. Analýza kardiálních markerů:
CK-MB mass, cTnI, myoglobinu, glykogen fosforylázy BB (GPBB), srdečního typu proteinu vázajícího mastné kyseliny (h-FABP) a karboanhydrázy III (CAIII) bylo provedeno systémem Evidence Investigator (Randox). Byly testovány analytické parametry soupravy Cardiac array. Výsledky získané systémem Evidence Investigator byly porovnány s hodnotami měřenými metodami na stanovení CK-MB mass a myoglobinu pro Elecsys 2010 (Roche). Markery poškození myokardu byly měřeny u 28 dárců krve, 28 pacientů s akutním infarktem myokardu a 21 pacientů po chemoterapii antracykliny (monitorování kardiotoxicity).Výsledky.
Passing-Bablokova regrese ukazuje statisticky významné rozdíly ve výsledcích. Důvodem těchto odchylek je nedostatečná standardizace metod a diskrepance mezi kalibracemi. Nové analyty h-FABP a GPBB jsou slibnými časnými markery akutního infarktu myokardu a diagnostická sensitivita h-FABP by mohla být vyšší než u myoglobinu. Tyto markery mohou být užitečné pro monitoring kardiotoxicity antracyklinů.Závěry.
Použití biočipové technologie v kardiologické diagnostice představuje výzvu do budoucna, ale bude nutná dokonalejší standardizace imunochemických metod.Klíčová slova:
proteinový biočip, kardiální marker, kardiotoxicita, infarkt myokardu.Úvod
V diagnostice akutních koronárních syndromů zaujímá stanovení biochemických markerů nekrózy myokardu důležité místo. U akutních koronárních syndromů bez elevace ST segmentů je jejich pozitivita známkou netransmurálního (nonQ) infarktu myokardu a umožňuje diagnostikovat nemocné s nestabilní anginou pectoris. Nově European Society of Cardiology, American College of Cardiology Foundation, American Heart Association a World Heart Federation publikovaly univerzální definici infarktu myokardu, ve které je přesně dáno použití biochemických markerů poškození myokardu. V první řadě jsou to srdeční troponiny pro průkaz nekrózy myokardu a pro diagnostiku reinfarktu je to stanovení myoglobinu a CK-MB mass (1, 2).
Současná biochemie nabízí možnosti stanovení více parametrů postižení myokardu současně. Tato tzv. multimarkerová strategie umožňuje stratifikaci rizika pacientů s akutními koronárními syndromy, například nestabilní anginou pectoris.
Tento přístup může být také užitečný i v jiných oblastech kardiologické diagnostiky – například při studiích kardiotoxicity léčiv (3) nebo při monitorování poškození myokardu účinkem radiofrekvenční katétrové ablace (4).
V posledních letech se rozšiřují poznatky o nových analytech, které by bylo možné využívat v kardiologické diagnostice, ale zatím nejsou součástí rutinní klinické praxe. Jde hlavně o BB izoenzym glykogen fosforylázy (GPBB) (5) a srdeční typ proteinu vázajícího mastné kyseliny (h-FABP) (6). Tyto látky by mohly hrát významnou roli jako časné markery ischémie nebo nekrózy myokardu v době, kdy ještě nelze očekávat pozitivitu troponinu, což má velký praktický význam pro akutní diferenciální diagnostiku nemocných vyšetřovaných pro bolesti na hrudi k vyloučení koronární etiologie obtíží.
FABP je cytoplazmatický protein účastnící se oxidace mastných kyselin. Strukturálně není vázán v buňkách a je schopen se velmi rychle uvolnit do krve. Jeho hladina signifikantně roste 1–3 hodiny po počátku infarktu myokardu, vrcholu dosahuje okolo 6.–8. hodiny a k normálu se vrací během 24–30 hodin. Jeho koncentrace je také vyšší během akutní ischémie. V lidském organismu bylo objeveno 9 subtypů FABP s různou tkáňovou lokalizací. Srdeční typ h-FABP může být použit jako časný diagnostický marker pro AIM s lepší senzitivitou a specificitou než myoglobin (6–8).
Glykogen fosforyláza je dimerický glykogenolytický enzym složený ze dvou identických podjednotek: GPBB (brain), GPLL (liver) a GPMM (muscle). Izoenzym BB je hlavní formou tvořenou v mozku a myokardu. Mnohem nižší koncentrace se vyskytují v leukocytech, krevních destičkách, slezině, játrech, ledvinách a dalších orgánech. Během ischémie myokardu je stimulována enzymatická aktivita GPBB a dochází ke změně v buněčné lokalizaci, z formy vázané na sarkoplazmatické retikulum na volný cytosolový enzym. Koncentrace GPBB roste okolo 3 hodin po nástupu bolesti na hrudi a vrcholu dosahuje přibližně po 6 hodinách. Tento enzym je schopen indikovat jak nekrotické poškození buněk myokardu, tak pouze ischemické procesy (5).
Karboanhydráza III (CAIII) je enzym přítomný v kosterním svalstvu, přičemž v myokardu se nevyskytuje. Z tohoto důvodu kombinované určení sérové hladiny CA III a myoglobinu zvyšuje diagnostickou specificitu a senzitivitu stanovení myoglobinu jako časného markeru pro AIM (9, 10).
Nový multianalytový přístup může pomoci v diagnostice různých kardiologických onemocnění. Cílem naší práce bylo testovat analytickou vhodnost použití Cardiac Array panelu pro přístroj Evidence Investigator (Randox), který je založený na technologii proteinových biočipů pro stanovení markerů poškození myokardu ve dvou klinických modelech: akutní infarkt myokardu s elevacemi ST segmentů, jako druhý model byla zvolena skupina pacientů s hematologickým onemocněním a současnou léčbou chemoterapií antracykliny s potenciální kardiotoxicitou.
Materiál a metody
Evidence Investigator™, biočipový analyzátor firmy Randox (Randox Laboratories Ltd., Velká Británie) umožňuje současné testování několika analytů z jednoho vzorku. Systém má proti klasickým imunochemickým technikám výhody zahrnující multiplexní přístup k analýze a možnost redukce objemů vzorku a reagencií.
Na přesně definovaných pozicích jsou na biočipu navázané protilátky proti jednotlivým analytům. Měření kardiálních markerů je založeno na principu sendvičové enzymoimunoanalýzy. Pro detekci protilátek je využívána chemiluminiscenční reakce peroxidu s luminolem, katalyzovaná křenovou peroxidázou. Luminiscence je cíleně snímána z jednotlivých ploch (spotů) na biočipu CCD kamerou. Zobrazovací technologie umožňuje kvantifikovat množství světla vycházejícího z jednotlivých reakčních ploch a software systému signály přepočítá na hodnotu koncentrací analytů ve vzorku.
Diagnostický panel Cardiac Array obsahuje dobře známé kardiální markery rutinně používané v klinické praxi: izoenzym kreatinkinázy CK-MB (CK-MB mass), myoglobin (MYO) a srdeční troponin I (cTnI) společně s novými analyty, jako jsou BB izoenzym glykogen fosforylázy (GPBB), srdeční typ proteinu vázajícího mastné kyseliny (h-FABP) či karboanhydráza III (CAIII).
Sérum je výrobcem upřednostňováno jako biologický materiál první volby pro stanovení na analyzátoru Evidence Investigator. Všechny koncentrace kardiálních markerů jsou udávány v μg/l. Devítibodová kalibrační závislost sestrojená výrobcem je součástí každého setu. Rozsah měření pro jednotlivé analyty je následující: CK-MB mass = 0,4–100 μg/l, MYO = 1,8–700 μg/l, GPBB = 1,97–290 μg/l, h-FABP = 0,15–150 μg/l, CAIII = 0,2–200 μg/l a cTnI = 0,18–50 μg/l.
Vnitřní kontrola kvality byla měřena na třech hladinách koncentrací pomocí kontrolních materiálů dodávaných výrobcem. Z naměřených výsledků kontroly kvality byla určena správnost (BIAS) a mezilehlá přesnost (reprodukovatelnost, Interassay CV) měření.
Pro porovnání biočipové technologie Evidence Investigator s rutinně užívanými metodami byla měřena skupina vzorků s širokým rozsahem měřených hodnot. Vzorky byly vybrány jak ze skupin dárců krve, tak od pacientů s různými kardiologickými diagnózami (n = 75). Výsledky testů pro CK-MB a MYO získané analýzou na biočipech byly srovnávány s odpovídajícími testy pro imunochemický analyzátor Elecsys 2010 (Roche). Ke zpracování dat byl použit statistický software MedCalc (Belgie).
Pro orientační ověření referenčních intervalů udávaných výrobcem jsme stanovili kardiální markery ve vzorcích sér od 28 dárců krve.
Klinické studie
Pro získání zkušeností s panelem kardiálních markerů na přístroji Evidence Investigator (Randox) bylo provedeno několik předběžných klinických studií. Jako příklad je uvedeno sledování kinetiky kardiálních markerů u pacientů s AIM a hodnocení kardiotoxicity cytostatické léčby u hematoonkologických pacientů.
V první skupině byly použity vzorky sér 28 pacientů (47–86 let, 21 mužů, 7 žen) s diagnózou AIM s elevacemi ST segmentů. Diagnóza byla stanovena podle pravidel doporučených Českou kardiologickou společností.
První odběr byl proveden do 6 hodin od vzniku bolestí na hrudi, druhý odběr 24 hodin po odběru prvním a třetí 5. den od přijetí pacienta k hospitalizaci. Byla sledována kinetika analytů v průběhu patologického procesu.
Kardiotoxicita onkologické léčby byla sledována u 21 pacientů (44 ± 10 let, 14 mužů, 7 žen) s akutní leukémií po chemoterapii antracykliny (kumulativní dávka 448,7 ± 91,3mg/m2). Přípravný režim představoval podání cyklofosfamidu (celková dávka 120 mg/kg, 60 mg/kg/den v tříhodinových intravenózních infuzích po 2 dny) společně s perorálním podáním busulfanu nebo celotělovým ozařováním. Tato léčba byla následována transplantací krvetvorných buněk. Kardiální markery byly měřeny před a 6, resp. 24 hodin po ukončení předtransplantačního režimu a dále 24 hodin a 14 dní po transplantaci krvetvorných buněk.
Vzorky do těchto studií byly získané ve Fakultní nemocnici v Hradci Králové. Krev byla odebrána žilním katétrem a do hodiny byla zpracována v laboratoři (centrifugace 5 min, 3500 otáček/min). Sérum bylo skladováno při -70 °C do analýzy. Projekt byl schválen etickou komisí FN a LF UK v Hradci Králové.
Výsledky
Správnost a mezilehlá přesnost (reprodukovatelnost) vypočtená z naměřených hodnot kontroly kvality je shrnuta v tabulce (tab. 1). Námi stanovené hodnoty jsou ve shodě s údaji výrobce ve všech parametrech kromě mezilehlé přesnosti u myoglobinu, kde jsme naměřili vyšší hodnoty variačního koeficientu (11,6–15,6 %) než udává výrobce (8,8–9,5 %).
Tab. 1. Výsledky hodnocení interní kontroly kvality pro Evidence Investigator Cardiac Array (Randox) (n = 10) 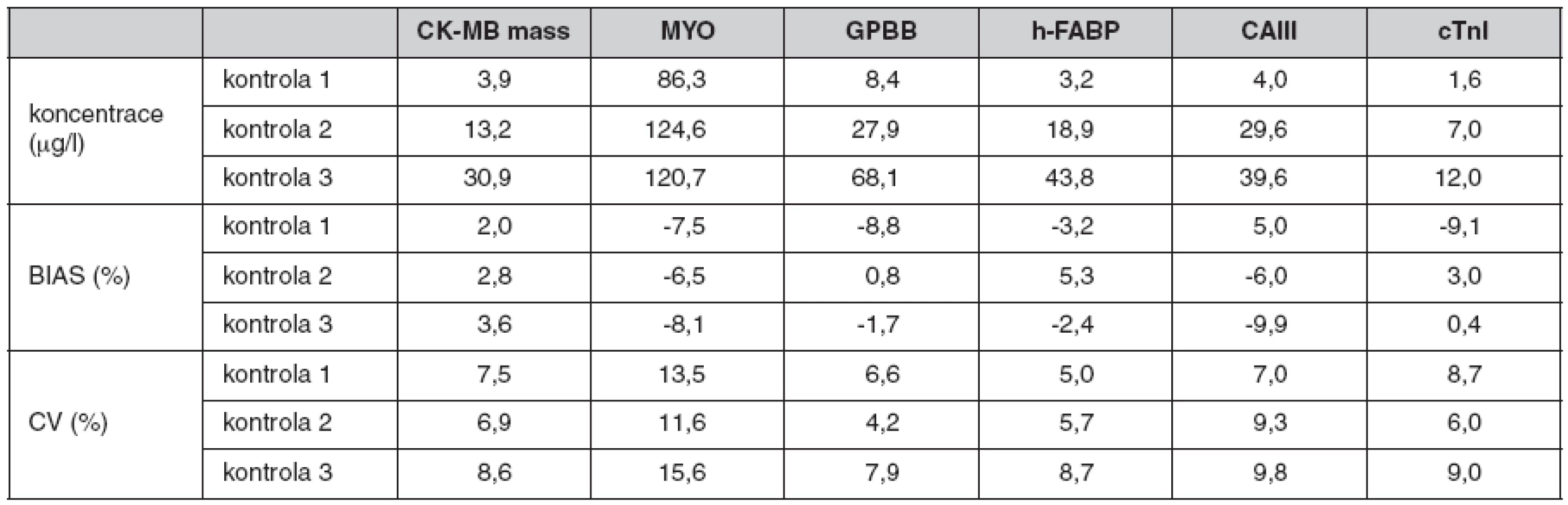
Na vybrané sérii vzorků bylo provedeno pro CK-MB mass a myoglobin porovnání výsledků naměřených systémem Evidence Investigator (Randox) a rutinně užívaným analyzátorem Elecsys 2010 (Roche). Výsledky měření jsou uvedeny v tabulce (tab. 2). K hodnocení výsledků byla použita Passing-Bablokova regrese. Výsledky měřené na obou systémech vykazovaly statisticky významné rozdíly. Rovnice regrese byly následující: Elecsys = 1,4232 Evidence + 0,4320 (korelační koeficient r = 0,9752) pro myoglobin (graf 1) a Elecsys = 2,0656 Evidence + 0,0946 pro CK-MB mass (r = 0,9748) (graf 2). Absolutní naměřené hodnoty jsou sice číselně nesrovnatelné, ale v rozlišení normálních a patologických koncentrací se metody téměř shodují (z 94,5 % u CK-MB mass a z 90,4 % u MYO). Z klinického hlediska je důležité sledování kinetiky kardiálních markerů. Z našich výsledků vyplývá, že pro kardiologickou diagnostiku lze použít metody obě, ale nelze kombinovat výsledky měření z jednotlivých analyzátorů mezi sebou. Tomu také odpovídá skutečnost, že jsou rozdílné hodnoty cut off udávané jednotlivými výrobci (Elecsys: CK-MB mass = 6,8 μg/l, MYO = 72,0 μg/l a Evidence Investigator: CK-MB mass = 3,9 μg/l, MYO = 59,0 μg/l).
Tab. 2. Porovnání biočipové technologie Evidence Investigator a rutinně používaného systému Elecsys 2010 (n = 75) 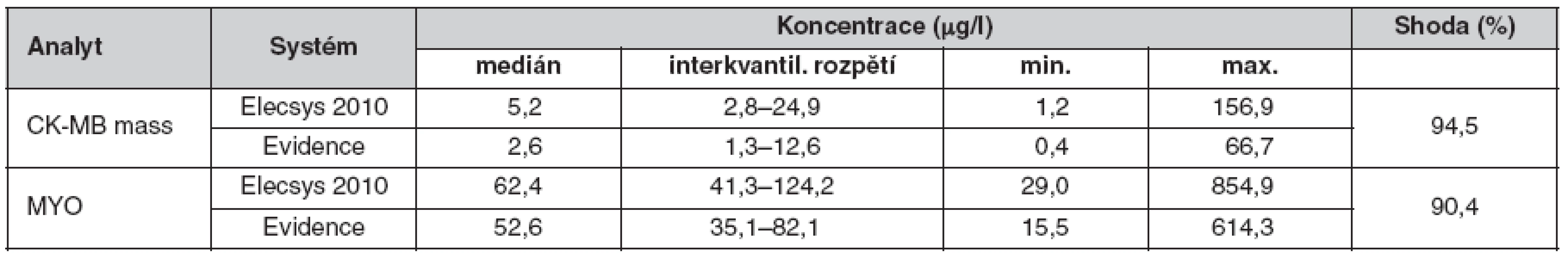
Graf 1. Passing-Bablokova regrese pro myoglobin Elecsys vs. Evidence Investigator Y = 1,4232 X + 0,4320 (95% CI směrnice: od 1,2985 do 1,5867 a 95% CI úseku: od -12,1281 do 5,6862) 
Graf 2. Passing-Bablokova regrese CK-MB mass Elecsys vs. Evidence Investigator Y = 2,0656 X + 0,0946 (95% CI směrnice: od 1,9238 do 2,1402 a 95% CI úseku: od -0,1761 do 0,3993) 
Pro ověření referenčních mezí udávaných výrobcem jsme stanovili hladiny kardiálních markerů u skupiny dárců krve (tab. 3). (Koncentrace jednotlivých analytů, které jsme naměřili v této skupině, přibližně odpovídají údajům o referenčních hodnotách výrobce.)
Tab. 3. Koncentrace kardiálních markerů ve skupině 28 dárců krve 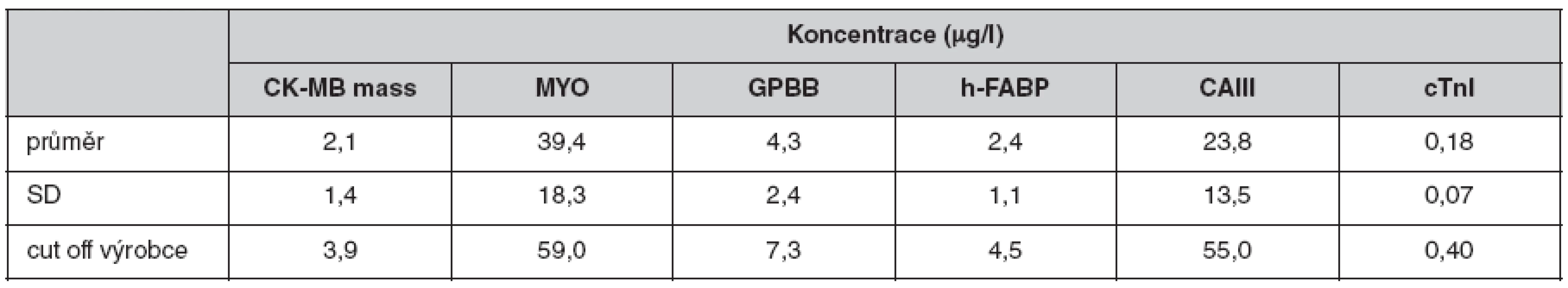
Klinické studie
Koncentrace kardiomarkerů naměřených ve skupině pacientů s diagnózou akutního infarktu myokardu jsou uvedeny v tabulce (tab. 4).
Tab. 4. Průměrné koncentrace kardiálních markerů ve skupině 28 pacientů s AIM 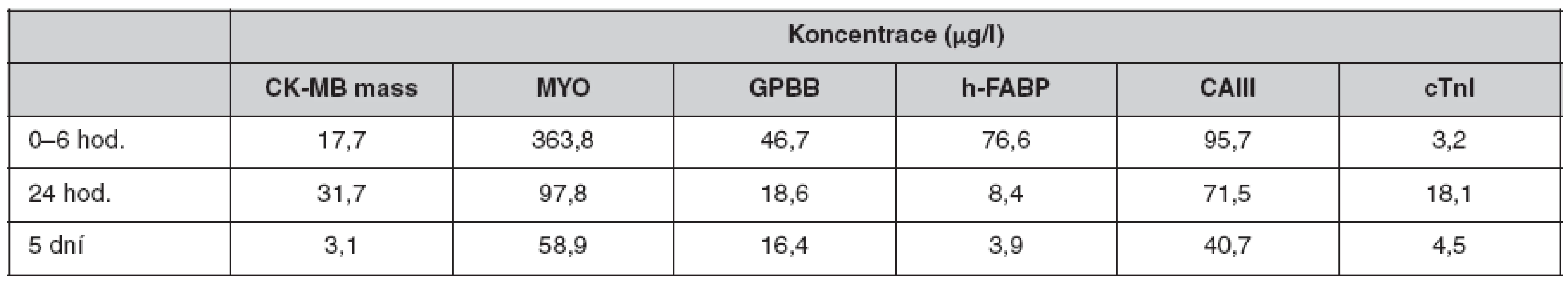
U všech 28 pacientů byla již při prvním odběru zvýšená koncentrace h-FABP a zároveň dosahovala maximální naměřené hodnoty. Při druhém odběru byla hladina h-FABP podstatně nižší a při třetím již byly všechny hodnoty v referenčních mezích. U myoglobinu byla při prvním odběru naměřena koncentrace nad cut off u 90 % pacientů (s maximem u 85 %). U 15 % pacientů byla maximální naměřená hladina při 2. odběru (po 24 hodinách). Obdobně jako h-FAPB se koncentrace myoglobinu velmi rychle navracely k normě. Hladina GPBB byla rovněž pozitivní u 90 % pacientů, ale maximální naměřené hodnoty bylo dosaženo pouze u 68 % z nich. Při 3. odběru (5. den) přetrvávala zvýšená hladina GPBB u 65 % pacientů. Z čehož lze usuzovat na pomalejší kinetiku GPBB ve srovnání s myoglobinem a h-FABP. Koncentrace CK-MB mass dosahovala maxima u 75 % pacientů při 2. odběru, přičemž u 3. odběru byly hladiny v 92 % případů v normě. Kardiální troponin I vzhledem ke své pomalé kinetice dosahoval u 20 % pacientů při 1. odběru dokonce koncentrací pod cut off, ale při 2. odběru už byla ve všech případech naměřena zvýšená hladina (u 95 % maximální hodnota).
Před hematoonkologickou léčbou byla u všech pacientů koncentrace kardiomarkerů v referenčních mezích. Přípravný režim před transplantací krvetvorných buněk vyvolal u 5 pacientů (24 %) zvýšení hladiny GPBB. U 2 pacientů (9 %) přetrvávala pozitivita ještě 14 dní po transplantaci, což může souviset s předchozí léčbou antracykliny jako projev chronické kardiotoxicity. U jednoho pacienta se zvýšila koncentrace h FABP po 14 dnech po transplantaci. Ostatní měřené kardiální markery (CK-MB mass, MYO a cTnI) zůstaly v referenčních mezích. Z tohoto lze usuzovat, že GPBB by mohla být možným citlivým markerem subklinické kardiotoxicity při podání hematoonkologické léčby.
Použité hodnoty cut-off pro jednotlivé kardiální markery jsou uvedeny v tabulce 3.
Diskuze
Pro diagnostiku poškození myokardu existuje v dnešní době široké spektrum biochemických markerů.
Stanovení kardiálních troponinů je doporučeno na prvním místě. I když je stanovení cTnT dobře standardizované, oba troponiny jsou v praxi využívány ve stejné míře, v Evropě vyšetřuje 51 % laboratoří cTnT a 49 % laboratoří cTnI (11). Neustálým problémem stanovení kardiálních troponinů zůstává nízká analytická citlivost metod. Jako cut off pro diagnostiku AIM je doporučována hodnota 99. percentilu zdravé populace stanovená s analytickou přesností (CV%) do 10 % (1). Toto kritérium většina souprav pro stanovení troponinu nesplňuje, i když v současné době již pronikají na trh soupravy s nižšími limity detekce a kvantifikace (high sensitivity troponin), kterými je možné měřit velmi nízké koncentrace troponinu s požadovanou přesností. Stanovení CK-MB mass je doporučeno pro diagnostiku infarktu myokardu pouze v případě, že není možné stanovení troponinů, zůstává však pro rychlou kinetiku markerem první volby při diagnostice reinfarktu. Analýza myoglobinu hraje hlavní roli v časných hodinách po vzniku infarktu myokardu pro svou vysokou negativní prediktivní hodnotu. Prakticky má ale frekvence jeho vyšetření v diagnostice akutního koronárního syndromu sestupný charakter (11).
Po shrnutí poznatků o kardiálních markerech je možné říci, že v mnoha případech je pro pacienta výhodnější komplexní pohled na biochemii kardiálních markerů. Biočipový analyzátor Evidence Investigator (Randox) je první analytický systém, který dovoluje simultánní stanovení klasických kardiomarkerů: troponinu I, myoglobinu a CK-MB mass a nových molekul: GPBB, h-FABP a CAIII, které nejsou zatím v diagnostice AIM rutinně používané.
Výsledky sledování analytických parametrů soupravy souhlasí s daty udávanými výrobcem kromě hodnot naměřených pro myoglobin. U myoglobinu jsme naměřili hodnoty variačního koeficientu vyšší (11,6–15,6 %) než udává výrobce (8,8–9,5 %). Na tuto skutečnost poukazují i další publikované práce (8, 12). Podle našich zkušeností problémem stanovení systémem Evidence investigator zůstává trvale hodnocení kontroly kvality.
Pro porovnání panelu Cardiac Array pro Evidence investigator (Randox) s klasickými imunochemickými postupy jsme vybrali analyzátor Elecsys 2010 (Roche). Získané výsledky z obou systémů vykazovaly statisticky významné rozdíly, jejichž důvodem je slabá standardizace metod a rozdíly v kalibracích metod. V současné době je tudíž pro každý systém potřeba hodnotit výsledky podle rozdílných hodnot cut off a samozřejmě je potřeba především individuálně sledovat trendy v růstu a poklesu koncentrací kardiomarkerů.
Klinická data získaná o nových kardiomarkerech ukazují, že h-FABP je v prvních hodinách po vzniku AIM citlivějším diagnostickým markerem než myoglobin. I když je h-FABP stejně jako myoglobin orgánově nespecifický, vyskytuje se v kosterním svalstvu v daleko menší míře než myoglobin. Jeho společné stanovení s myoglobinem zvyšuje diagnostickou specificitu testu. Vzhledem k odlišnému zastoupení obou proteinů v různých tkáních může být vypočtený poměr h FABP/MYO užitečný pro odlišení léze myokardu od poškození kosterního svalstva (6).
Karboanhydráza III je dalším markerem používaným k odlišení poškození myokardu od kosterního svalstva. Je to cytoplazmatický protein, který se tvoří pouze ve svalech příčně pruhovaných a nikoliv v myokardu. Dalo by se proto očekávat, že při AIM budou hladiny CAIII v normě. Námi naměřené výsledky ovšem ukazují, že se koncentrace CAIII u některých pacientů během AIM výrazně zvyšuje.
Sérová koncentrace GPBB u pacientů s AIM má v prvních hodinách podobnou kinetiku vzestupu jako myoglobin. Glykogen fosforyláza BB se zatím jeví jako možný časný marker budoucnosti.
U stanovení kardiotoxicity cytostatické léčby cyklofosfamidem se jeví jako použitelný marker glykogen fosforyláza BB, která vykazovala u 24 % pacientů vzestup hladin po podání přípravného režimu před transplantací krvetvorných buněk, a po ukončení léčby se vracela k normálním hodnotám.
Multiplexní analýza systémem Evidence Investigator je vhodná zatím zejména pro výzkumné účely. Nevýhodami tohoto poloautomatického systému zůstávají velký podíl manuální práce a nutnost sběru série vzorků. Firma již ale vyvinula automatický analyzátor, který umožňuje využívat technologii proteinových biočipů i pro statimová vyšetření.
Závěrem je možné říci, že současné stanovení více kardiálních markerů umožní komplexnější pohled na diagnostiku poškození myokardu a využití multiplexního přístupu zvyšuje diagnostickou senzitivitu a specificitu biočipového stanovení ve srovnání s jednotlivými testy. Z tohoto důvodu může být využití čipové technologie v některých situacích vhodné. Relativní nevýhodou však může být nutnost zpracování celého měřeného panelu bez možnosti výběru spektra analytů. Toto by mělo být v budoucnu vyřešeno úpravami panelu na žádost klinického pracoviště.
Zkratky
AIM – akutní infarkt myokardu
CAIII – karboanhydráza III
CCD – charge couple device
CK-MB mass – MB izoenzym kreatinkinázy (hmotnostní koncentrace)
cTnI – kardiální troponin I
cTnT – kardiální troponin T
GPBB – BB izoenzym glykogen fosforylázy
GPLL – LL izoenzym glykogen fosforylázy
GPMM – MM izoenzym glykogen fosforylázy
h-FABP – srdeční typ proteinu vázajícího mastné kyseliny
MYO – myoglobin
SD – směrodatná odchylka
95% CI – 95% konfidenční interval
Práce byla podpořena výzkumnými záměry MZO 00179906 a MSM 0021620817.
Adresa pro korespondenci:
RNDr. Martina Vašatová
ÚKBD LF UK a FN
Sokolská 581, 500 05 Hradec Králové
fax: +420 495 832 003, e-mail: ulrycmar@fnhk.cz
Zdroje
1. Thygesen K, Albert JS, White HD. Universal Definition of Myocardial Infarction. J Am Coll Cardiol 2007; 50 : 2173–2195.
2. Friedecký B, Engliš M, Franeková J, et al. Doporučení České společnosti klinické biochemie ke stanovení biochemických markerů poškození myokardu. Klin Biochem Metab 2008; 16 : 50–55.
3. Horacek JM, Tichy M, Pudil R, et al. Multimarker approach to evaluation of cardiac toxicity during preparative regimen and hematopoietic cell transplantation. Neoplasma 2008; 55 : 532–537.
4. Pudil R, Parizek P, Tichy M, et al. Use of the biochip microarray system in detection of myocardial injury cause by radiofrequency catheter ablation. Clin Chem Lab Med 2008; 46 : 1726–28.
5. Mair J. Glycogen phosphorylase isoenzyme BB to diagnose ischemic myocardial damage. Clin Chim Acta 1998; 272 : 79–86.
6. Pelsers MMAL, Hermes WT, Blaty JFC. Fatty acid-binding proteins as plasma markers of tissue injury. Clin Chim Acta 2005; 352 : 15–35.
7. Liao J, Chan CP, Cheung Y, et al. Human Heart-type fatty acid-binding protein for on-site diagnosis of early acute myocardial infarction. Int J Cardiol 2009; 133 : 420–423.
8. Mion MM, Novello E, Altinier S, et al. Analytical and clinical performance of a fully automated cardiac multi–markers strategy based on protein biochip microarray technology. Clin Biochem 2007; 40 : 1245–1251.
9. Vuori J, Huttunen K, Vuotikka P, et al. The use of myoglobin / carbonic anhydrase III ratio as marker for myocardial damage in patients with renal failure. Clin Chim Acta 1997; 265 : 33–40.
10. Beuerle JR, Azzazy HME, Styba G, et al. Characteristics of myoglobin, carbonic anhydrase III and the myoglobin/carbonic anhydrase III ratio in trauma, exercise and myocardial infarction patients. Clin Chim Acta 2000; 294 : 115–128.
11. Collinson P, Pulkki K, Suvisaari J, et al. How well do laboratories follow guidelines on cardiac markers? The Cardiac Marker Guideline Uptake in Europe Study. Clin Chem 2008; 54 : 448–449.
Štítky
Adiktológia Alergológia a imunológia Angiológia Audiológia a foniatria Biochémia Dermatológia Detská gastroenterológia Detská chirurgia Detská kardiológia Detská neurológia Detská otorinolaryngológia Detská psychiatria Detská reumatológia Diabetológia Farmácia Chirurgia cievna Algeziológia Dentální hygienistka
Článek Pandemic (H1N1) 2009Článek K marihuaně zcela legálněČlánek XXV. lékárnické dnyČlánek VII. Ningerovy dnyČlánek Spolek lékařů českýchČlánek KnihaČlánek LAUREÁTI NOBELOVY CENY
Článok vyšiel v časopiseČasopis lékařů českých
Najčítanejšie tento týždeň
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Průtoková cytometrie a její využití
- Děti v ohrožení metabolickým syndromem
- Pandemic (H1N1) 2009
- Multianalytový přístup k diagnostice srdečních chorob technologií proteinových biočipů
- Dodržování jednoduchých zásad zdravého životního stylu má klíčový vliv na prevenci chronických onemocnění
- K marihuaně zcela legálně
- Posuzování zdravotního stavu a pracovní schopnosti u onemocnění pohybového systému
- Efektivita léčby patologického hráčství – pilotní studie
- Mezinárodní konference Analytical Cytometry V
- Mezinárodní konference Analytical Cytometry V - pokračování
- Mezinárodní konference Analytical Cytometry V - pokračování
- Způsoby boje se stafylo-superantigenem
- Dermatologie patří mezi interní obory
- Surveillance a budoucnost epidemiologie
- XXV. lékárnické dny
- VII. Ningerovy dny
-
Současný stav hormonální terapie patologií menopauzy
Aktuální zpráva z 10. konference ČMAS ČLS JEP a SOM ČGPS ČLS JEP - Spolek lékařů českých
- Slavnostní předání Cen České lékařské společnosti JEP
- Šťastné a veselé – jenom aby!
- Kniha
- LAUREÁTI NOBELOVY CENY
- Časopis lékařů českých
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Posuzování zdravotního stavu a pracovní schopnosti u onemocnění pohybového systému
- Průtoková cytometrie a její využití
- Surveillance a budoucnost epidemiologie
- Děti v ohrožení metabolickým syndromem
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



