-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Olfaktoriální meningiomy – chirurgická léčba, její rizika a možnosti zachování čichu
Olfactory groove meningiomas – surgical treatment, surgical risks and sense of smell preservation
This review summarizes dysfunction of olfaction in patients with olfactory groove meningiomas (OGM). Clinical examination, including pre-operative and post-operative assessment of olfaction, is indispensable for the evaluation of the surgical outcome in patients with OGM. Review of a recent series of OGM documents showed a lack of the olfaction assessment in most of the studies. Psychophysical tests determining olfactory detection, discrimination and identification (e. g. University of Pennsylvania Smell Identification Test [UPSIT], The Single Staircase Odor Detection Threshold Test, Siffin’ Sticks Test) should be used to reveal olfactory dysfunction. Specialized examination techniques such as electro-olfactogram, olfactory evoked potentials and functional magnetic resonance imaging are being used in research. Standard treatment of OGM is a surgical resection. Controversy exists among the authors regarding the selection of a convenient surgical approach. Commonly, the uni-frontal and pterional approaches are being performed. Endoscopic resection, olfactory groove meningiomas, represents an alternative approach yet its indications are still limited. Postoperative olfaction preservation remains a difficult task even today.
Key words:
olfactory groove meningioma – skull base – olfaction – olfactory nerve
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři: M. Dedeciusová 1; M. Májovský 1; P. Fundová 2; V. Beneš 1; D. Netuka 1
Působiště autorů: Neurochirurgická a neuroonkologická klinika 1. LF UK a ÚVN Praha 1; Klinika otorhinolaryngologie a maxilofaciální chirurgie 3. LF UK a ÚVN Praha 2
Vyšlo v časopise: Cesk Slov Neurol N 2018; 81(1): 11-16
Kategorie: Přehledný referát
prolekare.web.journal.doi_sk: https://doi.org/10.14735/amcsnn201811Souhrn
Práce je zaměřena na poruchy čichu u pacientů s olfaktoriálními meningiomy (OGM). Přesné klinické vyšetření pacientů s OGM, včetně pre - a pooperačního zhodnocení čichu, je nezbytné pro hodnocení provedené chirurgické resekce. Článek poskytuje základní přehled recentních sérií OGM světových autorů. Jen malý zlomek z nich však dokumentuje přesné vyšetření čichu. Standardní vyšetření čichu by mělo stanovit čichovou detekci, diskriminaci a identifikaci pomocí jednoho z užívaných testů (např. University of Pennsylvania Smell Identification Test [UPSIT], The Single Staircase Odor Detection Treshold Test, Sniffin’ Sticks Test). Metodami vyšetření čichu, které jsou zatím využívány pro výzkum, zůstávají elektro-olfaktogram, čichové evokované potenciály a funkční magnetická rezonance. Zlatým standardem léčby OGM je chirurgická resekce. Volba vhodného operačního přístupu je stále kontroverzní a mezi jednotlivými autory nepanuje shoda. Nejčastěji se používá frontolaterální a pterionální přístup. Alternativou je endoskopická resekce, jejíž indikace jsou však omezené. Pooperační zachování čichu představuje zatím obtížný úkol.
Klíčová slova:
olfaktoriální meningiom – baze lební – čich – čichový nervÚvod
Olfaktoriální meningiomy (OGM) vyrůstají v oblasti lamina cribriformis a sutura frontosphenoidalis. Tvoří 4–13 % intrakraniálních meningiomů [1]. Během svého růstu zůstávají dlouho asymptomatické. Později komprimují nn. olfactorii, frontální laloky či chiasma opticum, což vede k nejčastějším klinickým symptomům, tj. hyposomii, kognitivnímu deficitu, mentálním změnám či poruše vizu [2,3]. První úspěšnou resekci OGM provedl v roce 1885 z levostranné frontální kraniotomie Francesco Durante [4]. Roku 1938 popsali Cushing a Eisenhardtová základní chirurgické principy resekce OGM [5]. V české literatuře nenacházíme publikaci, která by byla zaměřena pouze na OGM. Chirurgii baze lební vč. resekce nádorů zpracovali ve svém článku Sameš et al v roce 2013 [6]. V témže roce popsali endoskopickou endonazální resekci meningiomů baze lební Netuka et al [7]. I přes zvyšující se počet zahraničních publikací o OGM je volba optimálního operačního přístupu stále velmi kontroverzní. Recentní studie OGM navíc obvykle opomíjí přesné zhodnocení funkčních výsledků vč. vyšetření čichu, ačkoli trend v současné neurochirurgii je zcela opačný [8]. Příkladem jsou rozsáhlé recentní studie, které provedli např. Romani et al, Bitter et al a Palliny et al a které hodnotí čich pouze z anamnestických údajů pacientů [7]. Přesné vyšetření čichu lékařem ORL jedním z užívaných testů je ovšem esenciální k zhodnocení výsledků operace.
Klinický obraz
OGM zůstávají dlouho asymptomatické a klinicky se projevují až nádory větších rozměrů. Nejčastějšími symptomy jsou změny osobnosti, změny chování a bolesti hlavy. Tyto symptomy se vyskytují u 30–40 % pacientů [9]. Anosmie je diagnostikována ve 13–65 % případů, avšak jen ojediněle je vedoucím příznakem [8]. Méně časté jsou poruchy zraku a epileptické záchvaty [10].
Diagnostické vyšetřovací metody
Mezi nezbytné součásti vyšetření pacientů s OGM patří: anamnestický rozhovor, neurologické vyšetření, vyšetření čichu a v indikovaných případech vyšetření oční a neuropsychologické. Jednotlivá vyšetření jsou provedena i po operaci, aby mohl být zhodnocen funkční výsledek chirurgického zákroku.
Zobrazovací metody
Zlatým standardem v diagnostice OGM je MR. Výhodou MR je především přesné zobrazení topografických vztahů meningiomu k okolním neurovaskulárním strukturám (nn. optici, chiasma opticum, aa. cerebri anteriores, a. communicans anterior). Výhodou CT je zejména přesné zobrazení kostí. CT umožní zhodnocení hyperostóz, eroze baze lební i propagace OGM do paranazálních dutin [11]. Angiografické vyšetření, které dnes indikujeme jen zřídka, ukáže posun hlavních intrakraniálních tepenných kmenů a cévní zásobení tumoru. Chirurgicky významná je přítomnost nebo absence podílu větví vnitřní krkavice na cévním zásobení nádoru. Předoperační embolizace ethmoidálních arterií zásobujících meningiom může být přínosná u velkých nádorů. Při embolizaci je však nutné vážit riziko poškození vizu [12].
Oční vyšetření
Specializované oční vyšetření je vhodné u pacientů, kdy je na MR patrný kontakt meningiomu s chiasma opticum či zrakovými nervy. Vyšetřují se zraková ostrost, perimetr, oční pozadí a nitrooční tlak, jak to udávají např. Bassiouni, Gazzeri a další [13–16].
Neuropsychologické vyšetření
Při suspektní neuropsychologické alteraci je vhodné doplnit i vyšetření neuropsychologické. Psychická alterace se vyskytuje zejména u gigantických OGM. Například Gazzeri et al ve své studii hodnotí vliv bifrontálního přístupu při resekci OGM na kognitivní funkce pacientů. U všech pacientů byly kognitivní funkce vyšetřeny orientačně pomocí Mini-Mental State Examination (MMSE) před resekcí i po ní. Po operaci byly dále provedeny Brief psychiatric rating scale, Neuropsychiatric Inventory Test, Phonemic Verbal Fluency Test, Preferred Hand Test a Verbal Memory Test. Studie nepotvrdila předpokládaný negativní vliv bifrontálního přístupu na kognitivní funkce pacientů. Navíc v určitých případech došlo ke zlepšení kognitivních funkcí po zákroku [14].
Vyšetření čichu
Metody vyšetření čichu se dělí na subjektivní (prahové – detekce, nadprahové – identifikace a diskriminace) a objektivní (olfaktoriální evokované potenciály, elektro-olfaktogram, funkční MR).
Subjektivní metody, takzvané psychophysical olfactory tests, vyšetřují detekci, diskriminaci a identifikaci odorantů. Vyšetření detekce stanoví čichový práh, tj. nejnižší rozeznanou koncentraci odorantu. Nejznámějším používaným vyšetřením je The Single Staircase Odor Detection Treshold Test. Během testu je vyšetřovnané osobě prezentován čichový podnět (PEA vonící jako růže) ve stoupajících koncentracích. Diskriminace je schopnost rozlišení různých čichových podnětů v nadprahových koncentracích. Vyšetření využívá 32 párů vůní, z nichž 16 párů je shodných a 16 rozdílných. Pacient rozhoduje, zda jsou po sobě následující podněty shodné. Identifikace znamená schopnost správně odorant pojmenovat. Velmi často používaným testem čichové identifikace je University of Pennsylvania Smell Identification Test (UPSIT). Test se skládá z 40 různých vůní v mikrokrystalech nanesených na papíře. Vyšetřovaný vybírá vždy správnou ze čtyř možností. Kratší variantou je Pocket Smell Test (PST). K vyšetření detekce, identifikace a diskriminace je nejčastěji využíván Sniffin’ Sticks Test [17–19].
V recentních studiích OGM je čich vyšetřován výjimečně [8]. Většina studií udává pouze anamnestické údaje pacientů o přítomnosti hyposmie či anosmie [2,3,14–16,20–23]. Jak ukazuje např. studie Janga et al, anamnestické údaje odhalí jen těžkou poruchu čichu. Ve zmíněné studii uvedlo anamnesticky poruchu čichu 15 % pacientů, avšak vyšetření pomocí Sniffin’ Sticks prokázalo poruchu čichu u 67,5 % pacientů. Z větších studií dokumentují odborné všetření čichu lékařem ORL např. Bassiouni et al a Ciurea et al, ovšem neuvádí použitou testovací metodu [13,24]. V následujících odstavcích jsou podrobněji rozebrány studie Janga et al a Welge-Luessena et al, které jsou zaměřeny na čich u pacientů s OGM [25,26].
Jang et al publikovali retrospektivní sérii 40 OGM, která je zaměřena na čich a možnosti jeho zachování. Poruchu čichu anamnesticky uvedlo 15 % pacientů (6/ 40). Všichni pacienti byli následně před operací i po ní otestováni pomocí korejské verze Sniffin’ Sticks. Porucha čichu byla prokázána u 67,5 % pacientů (27/ 40). Anatomické zachování olfaktoriálních struktur se podařilo u 65 % pacientů (26/ 40), z toho v 19 případech bilaterálně a 7 případech unilaterálně. Funkčně byl však olfaktoriální aparát zachován pouze u 55 % pacientů (22/ 40). Dle výsledků této studie je pro zachování čichu po resekci meningiomu statisticky významná velikost nádoru, intaktnost čichu před operací a použitý operační přístup. Čich pacientů byl zachován po resekci 78,6 % nádorů menších než 4 cm. Oproti tomu pouze u 42,3 % pacientů s nádorem větším než 4 cm (p = 0,035). Normální čich po operaci mělo 84,6 % pacientů bez prokázené poruchy čichu před operací (11/ 13), ale pouze 40,7 % (11/ 27) pacientů, kteří měli hyposmii či anosmii již před operací (p = 0,016). Při frontolaterálním přístupu byl čich zachován u 71,4 %, zatímco u bifrontálního pouze v 36,8 % případů (p = 0,032) [25].
Dalším příkladem studie zaměřené na olfaktoriální funkce je retrospektivní série 12 OGM, kterou publikovali Welge-Luessen et al. U všech pacientů bylo provedeno před operací i po ní kompletní ORL vyšetření vč. vyšetření čichu pomocí Sniffin‘ Sticks. Před operací byli čtyři pacienti normosmičtí, dva bilaterálně hyposmičtí a šest ipsilaterálně anosmických (z nich čtyři anosmičtí i kontralaterálně, dva hyposmičtí kontralaterálně). Ve dvou případech bylo možné uchovat intaktní olfaktoriální aparát na straně nádoru, ale i v těchto případech byla po operaci prokázána funkční anosmie. Pooperační vyšetření čichu prokázalo kompletní anosmii u osmi pacientů a ipsilaterální anosmii u čtyř pacientů. U dvou pacientů bylo provedeno i měření olfaktoriálních evokovaných potenciálů (OEP) pomocí olfaktometru. Z této studie vyplývá, že vyšetření čichu má malý význam v diagnostice OGM. Dále, že pravděpodobnost zachování čichu je vyšší u nádorů menších než 3 cm a u pacientů s normosmií. A také, že zachování čichu na straně nádoru je extrémně obtížné bez ohledu na velikost nádoru a zvolený chirurgický přístup [26].
Mezi objektivní metody vyšetření čichu patří elektrofyziologické monitorování OEP, elektro-olfaktogram a funkční MR. Existují klinické studie a pokusy na zvířatech, které stimulovaly čichový epitel chemicky a následně snímaly OEP [27,28]. Stimulaci čichového epitelu sulfanem a následné snímání OEP uvádí ve své studii i Welge-Luessen et al [26]. Avšak přesné metody peroperačního monitorování OEP nebyly doposud popsány. Kvůli prolongované adhezi odorantů k čichovému epitelu nelze zajistit peroperačně konstantní podmínky stimulace. Alternativou je monitorování OEP vyvolaných elektrickou stimulací čichového epitelu, které popsali poprvé v roce 1996 Sato et al [29]. Elektrická stimulace dovoluje snadnou kvantifikaci intenzity stimulu i repetitivní stimulaci za konstatních podmínek. Studie měla dvě části. První z nich, experimentální, kdy autor monitoroval OEP u 25 psů. Ve druhé části byly zaznamenávány OEP u 10 pacientů, kteří podstoupili bifrontální či frontotemporální kraniotomii. Dle výsledků studie elektrická stimulace čichového epitelu vyvolá obvykle monofázické OEP snímatelné z olfaktoriálního traktu. Snímání OEP ze sklapu nebylo úspěšné. Obdobná stimulace nazální sliznice nevyvolala žádné OEP. Peroperační monitoring OEP by mohl pomoci snížít frekvenci anosmie způsobené peroperačním poškozením olfaktoriálního traktu. Přesné hodnoty indikující riziko poškození olfaktoriálního traktu nebyly zatím stanoveny. Dosud používaný 50% pokles amplitudy a prodloužení latence o 10 % je třeba ověřit v dalších studiích [29,30].
Záznamem receptorových potenciálů čichového epitelu vzniká elektro-olfaktogram. U člověka tuto metodu zatím nelze použít k hodnocení čichu. Receptorové potenciály lze v některých případech zaznamenat i u pacientů s anosmií, nebo dokonce po smrti pacienta [18,31].
Funkční MR (fMR) zobrazuje aktivaci čichových kortikálních oblastí, ale doposud neumožňuje čich vyšetřit. Hlavní přínos této metody je nyní v oblasti výzkumu. Příkladem takového využití je i studie, kterou provedli Fournel et al a která pomocí fMR zkoumá principy kódování čichu na kortikální úrovni. Studie ověřuje předpoklad podobnosti kódování chemických atributů v přední části piriformního kortexu a kódování atributů percepce v zadní části piriformního kortexu [32]. Berlin et al publikovali studii, která pomocí fMR dokumentuje odlišné zpracování čichového vjemu a zvýšenou aktivaci insuly u pacientů s obsedantně-kompulzivní poruchou [33].
Léčba olfaktoriálních meningiomů
Konzervativní postup
Observace je možná u malých incidentálně diagnostikovaných meningiomů. Symptomatické nádory dosahují obvykle větších rozměrů a chirurgická resekce je zpravidla jedinou terapeutickou metodou [11].
Chirurgická resekce
Historicky používané operační přístupy
V roce 1935 popsali Urban a Olivecrona unilaterální frontální kraniotomii. Tentýž přístup popsali o 3 roky později Cushing s Eisenhardtovou [5,34,35]. Součástí operačního přístupu byla i resekce části frontálního laloku, která umožnila lepší expozici nádoru. V roce 1938 popsal Dandy rozsáhlejší bifrontální kraniotomii s parciální frontální lobektomií [36]. Její různé variace dále popsali Tonnis a Morley a v éře mikrochirurgie Mac-Carty a Ojeman [37–40]. Pterionální přístup popsal Yasargil [34].
Současné operační přístupy
Mezi nejčastěji používané transkraniální přístupy v dnešní době patří přístup unifrontální, pterionální a bifrontální. Existují i přístupy rozšířené, např. orbitopterionální a modifikovaný orbitozygomatický nebo rozšířený transbazální přístup [16]. Alternativou jsou endoskopické endonazální přístupy, jejichž indikace jsou však limitovány [41,42]. Základní přehled sérií OGM světových autorů, vč. dosaženého procenta radikálních resekcí, morbidity, mortality i recidiv nádorů, shrnuje tab. 1 [2,3,13–16,20–23].
Pterionální přístup
Pterionální přístup je jedním z nejužívanějsích operačních přístupů k resekci OGM. Díky časné drenáži likvoru z karotické a prechiasmatické cisterny je možná menší retrakce frontálních laloků [2]. Přístup nepoškodí sinus frontalis, což snižuje riziko pooperační likvorey i infekcí [20]. Nespornou výhodou je i časná identifikace důležitých neurovaskulárních struktur, devaskularizace nádoru a uchování kontralaterálního olfaktoriálního nervu [20,43]. Oproti tomu možnou nevýhodou je užší pracovní úhel [23]. Pterionální přístup má v jednotlivých sériích poměrně nízkou morbiditu. V sérii publikované Turazzim el al se nevyskyla žádná komplikace [21]. Schaller et al ve své sérii uvádějí 4% morbiditu, kdy časný pooperační průběh komplikovalo krvácení v resekční dutině [20]. Nejčastější komplikací v sérii Guduka et al byly kontuze u 5,3 % pacientů [23]. Vyšší morbiditu udávají např. Bitter et al, kdy nejčastější komplikací byl v 8 % epileptický záchvat [2].
Laterální supraorbitální přístup
Jedná se o méně invazivní modifikaci pterionálního přístupu lokalizovanou více frontálně. Romaniho et al ve své sérii udávají jako nejčastější komplikaci likvoreu u 9 % pacientů [3].
Bifrontální přístup
Bifrontální přístup zajišťuje dokonalou expozici přední jámy lební. Usnadňuje radikální resekci, odstranění kostní hyperostózy i dekompresi optických nervů [44,45]. Knopp et al popisují i velmi dobré výsledky z hlediska zachování čichu, a to ve 100 % případů [46]. Hlavní nevýhodou přístupu je otevření sinus frontalis, retrakce frontálních laloků a pozdní identifikace neurovaskulárních struktur [15]. Jedná se o přístup invazivní, zatížený vyšší morbiditou a mortalitou. V sérii Spektra et al pooperační průběh nejčastěji, ve 14 % případů, komplikuje likvorea, dále v 9 % meningitida a v 9 % frontální kontuze [15]. Likvorea byla nejčastější komplikací i v sérii Gazzeriho et al u 5,5 % pacientů [14] a Bassiouni et al u 5,4 % pacientů [13]. Edém a krvácení nejčastěji komplikovaly pooperační průběh v sérii Nakamury et al v 15,2 %, resp. 10,9 % případů a v sérii Palliniho et al v 17,1 %, resp. 12,9 % případů [16,22].
Jednostranný frontální (frontolaterální) přístup
Jednostranný frontální přístup šetří kontralaterální frontální lalok, sinus sagitalis superior a omezuje retrakci mozku. Další výhodou je snadné odvrtání lamina cribriformis a odstranění invadující části tumoru [23]. Mezi nevýhody přístupu patří riziko likvorey, nutnost elevace ipsilaterálního frontálního laloku u velkých OGM, a tím i komprese přemosťujících žil [15].
Endoskopický endonazální transcribriformní přístup
Endoskopické endonazální přístupy jsou dnes preferovány k resekci extradurálních lézí a adenomů hypofýzy. Zlatým standardem léčby meningiomů přední jámy lební je však více než 30 let resekce transkraniální [47]. Endoskopický endonazální transcribriformní přístup je nejčastěji v rozsahu od crista gali k planum sphenoidale a mezi laminae papyraceae. Výhodou je časná devaskularizace nádoru, eliminace retrakce frontálních laloků a příznivý kosmetický výsledek. Snadné je i odstranění hyperostotické kosti a částí nádoru infiltrujících paranazální dutiny. Použití je limitováno laterální extenzí nádoru a omezenými možnostmi hemostázy [48]. Dalšími nevýhodami jsou poranění dutiny nosní a paranazálních sinů, riziko poškození čichu a vyšší riziko likvorey [49,50]. Přístup je možné použít u malých meningiomů s propagací do nosní dutiny u pacientů s anosmií. Ve své práci z roku 2015 Shin et al shrnují výsledky endoskopických resekcí 80 OGM. Nejčastější komplikací byla ve 26 % případů likvorea. Neurologický deficit se vyskytl u 8,8 % pacientů [51].
Stereotaktická radiochirurgie a radioterapie
Výhodou radiochirurgie je rychlý pokles dávky záření za hranicemi nádoru. Komplikacemi jsou bolesti hlavy, zhoršení edému i zrakový deficit. Některé studie prokazují, že po stereotaktické radiochirurgii a radioterapii je lokální kontrola nádoru shodná s resekcí Simpson grade I [52].
Radioterapie je rutinně používána u anaplastických meningiomů. Současně roste počet studií, jež podporují použití radioterapie i u meningiomů atypických. Je též vhodná u velkých meningiomů nebo meningiomů v blízkosti důležitých neurovaskulárních struktur u chirurgicky rizikových pacientů [53].
Diskuze
Čich zajišťuje ochranu před nebezpečnými faktory prostředí, podílí se na mezilidských vztazích a ovlivňuje naše stravovací zvyky. Uvážíme-li, že čichová centra jsou významně propojena s limbickým systémem, poškození čichu může vést k významným psychofyziologickým změnám [54]. Čichové kortikální oblasti se významně překrývají s oblastmi odpovědnými za sociální funkce. Emoční zpracování různých stimulů probíhá ve fylogeneticky starých limbických okruzích, které se původně vyvinuly pro zpracovávání čichových vjemů. Projekční čichové korové oblasti jsou rovněž nezbytné pro výběr vhodného partnera, emoce a strach (amygdala, nucleus medialis), pro motivaci, vyšší kognitivní a emoční procesy (prefrontální orbitální kortex). Důležitý je rovněž úzký vztah čichu a paměti. Například vůní vyvolané vzpomínky jsou dány specifickou aktivací amygdaly [55,56]. I přes to se jedná o nejvíce podceňovaný smysl. Odborné vyšetření čichu je v neurochirurgických studiích spíše výjimkou [8]. Příčinou nedostatečného vyšetření pacientů jsou pravděpodobně špatné funkční výsledky resekcí OGM z hlediska zachování čichu [57]. I v případě anatomicky intaktního olfaktoriálního aparátu může dojít k funkční anosmii [13]. Ačkoli je porucha čichu nejčastějším symptomem a je přítomna u většiny diagnostikovaných OGM, vzácně je důvodem návštěvy lékaře. Hyposmie se vyvíjí obvykle postupně, někdy i několik let. Proto pacienti zaznamenají až těžkou poruchu. Z tohoto důvodu je přesné vyšetření čichu u pacientů s OGM esenciální. Nejčastěji využívanou zkouškou je Sniffin’ Sticks Test, který testuje čichovou detekci, diskriminaci i identifikaci. Zachování čichu není snadné, ale v některých případech je možné. Na obr. 1 jsou shrnuty předoperační a pooperační MR nálezy u pacientky, kde vyšetření čichu před operací a po ní prokázalo obdobné nálezy, tj. zachování čichu. Peroperační monitorování OEP by v budoucnosti mohlo zlepšit funkční výsledky resekcí OGM.
Obr. 1. Předoperační MR, T1 vážené obrazy s kontrastní látkou, axiální a koronární řez (A, B). Pooperační MR, T1 vážené obrazy s kontrastní látkou, axiální a koronární řez, stav po radikální resekci, pooperačně pacientka bez neurologického defi citu, čich zachován (C, D). Fig. 1. Preoperative MRI, T1-weighted images with contrast agent, axial and coronary plane (A, B). Postoperative MRI, T1-weighted images with contrast agent, axial and coronary plane, after radical resection, postoperatively patient without neurological defi cit, sense of smell is preserved (C, D). 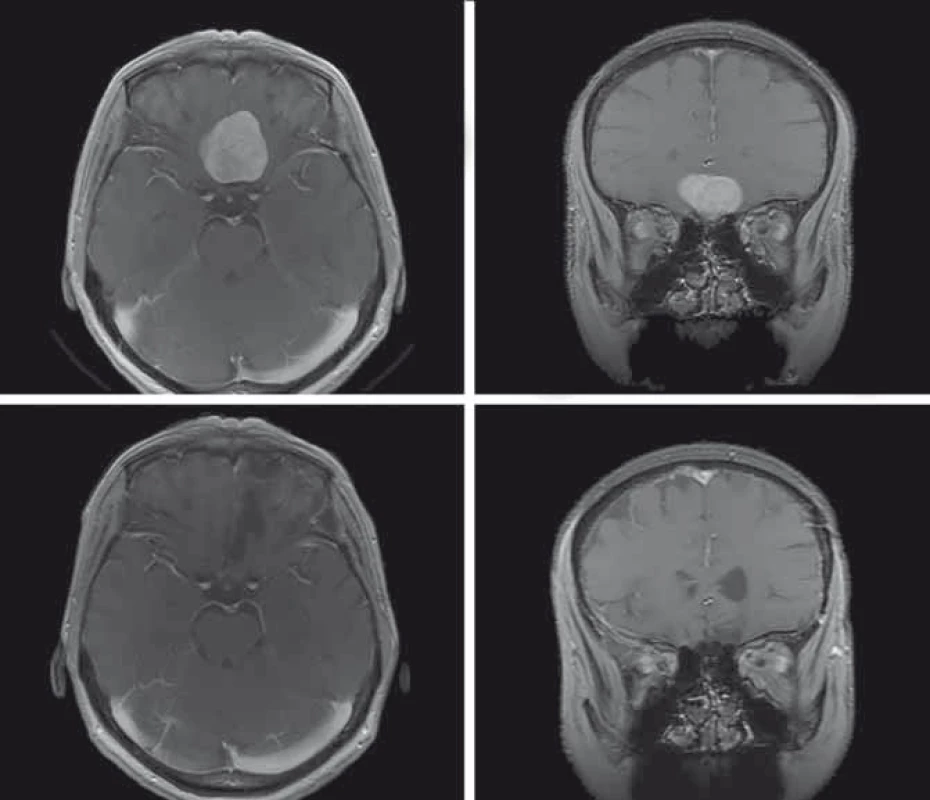
U většiny pacientů je cílem radikální resekce OGM. Mnohé studie totiž dokumentují, že rizikovým faktorem recidivy je vedle histologie také rozsah chirurgické resekce [58]. Limitacemi by neměly být ani hyperostóza a propagace meningiomu do dutiny nosní nebo paranazálních sinů [15]. Přítomnost rezidua meningiomu v oblasti cellulae ethmoidales velmi zvyšuje riziko recidiv [45,59]. Zabránit rekurenci je možné koagulací origa nádoru a přilehlé tvrdé pleny, odstraněním jeho infiltrativní části a kostní hyperostózy [45]. Parciální resekci volíme u vysoce rizikových nebo velmi starých pacientů. Další indikací parciální resekce je snaha zachovat olfaktoriální aparát u pacienta s intaktním čichem.
Při volbě vhodného operačního přístupu zohledňujeme především velikost nádoru, jeho propagaci do okolních struktur a čich pacienta. Bifrontální přístup je přístup invazivní s vyšší morbiditou i mortalitou. Na našem pracovišti jej v dnešní době používáme jen ojediněle u velkých nádorů, které dosahují konvexity. Pro většinu resekcí volíme přístupy unilaterální – pterionální nebo frontolaterální. Výhodou unilaterálních přístupů je dostatečná přehlednost operačního pole, minimální retrakce kontralaterálního frontálního laloku, celkově nižší morbidita i mortalita při vysokém procentu dosažených radikálních resekcí. Endoskopickou resekci lze zvážit u malých meningiomů při anosmii a propagaci meningiomu do dutiny nosní a paranazálních dutin.
Zachování čichu při resekci OGM zůstává nelehkým úkolem. Jang et al uvádí, že zachovaný čich i po operaci mělo 84,6 % pacientů bez prokázené poruchy čichu před operací (11/ 13), ale pouze 40,7 % pacientů, kteří měli poruchu čichu již před operací (11/ 27) [25]. V sérii Bassiouniho et al bylo 31,7 % pacientů s normosmií, 26,8 % s hyposmií a 41,4 % s anosmií před operací. Po operaci byla dokumentována normosmie u 12,2 %, hyposmie u 12,2 % a anosmie 70,7 % pacientů [13]. Ciurea et al ve své sérii udávají anosmii u 78 % pacientů před operací a 81,3 % po operaci [24]. Olfaktoriální aparát může být během operace poškozen přímo, prostřednictvím narušeného cévního zásobení nebo transekcí fila olfactoria. Jak prokázali Bassiouni et al, výsledné zachování čichu není závislé na použitém operační přístupu. I přes to autor preferuje přístupy unilaterální, které šetří druhostranný čichový aparát [13]. Jang et al ve své studii popisují statisticky významné faktory pro zachování čichu. Lepších výsledků bylo dosaženo u pacientů s normálním čichem a také u meningiomů menších než 4 cm. Zachování čichu se dařilo především při použití frontolaterálního přístupu v porovnání s přístupem bifrontálním [25]. Welge-Luessen et al uvádějí, že je zachování čichu na straně nádoru extrémně obtížné bez ohledu na velikost meningiomu i operační přístup [26]. Chirurgické komplikace způsobojící anosmii zpracovali v anatomické studii Cardali et al. Na deseti kadaverech měřili maximální možnou retrakci frontálních laloků, při které nebyl čichový aparát poškozen. Retrakce odpovídala 10–15 mm. Poškození čichu může být způsobeno přerušením fila olfactoria při retrakci frontálního laloku. Lepší funkční výsledky umožní otevření olfaktoriální cisterny na dorzální straně nervu a omezení manipulace olfaktoriálním bulbem. Další zranitelnou částí je proximální tractus olfactorius. Poslední možnou příčinou je komprese a poškození mikrovaskulatury dorzální strany čichového nervu [60].
Závěr
U většiny symptomatických OGM je indikována radikální resekce. Ani v dnešní době není shoda stran nejvhodnějšího přístupu. Morbidita těchto operací by měla být malá, až na případy gigantických OGM u starých pacientů, které patří mezi velmi riskantní operace. Hodnocení čichu je často opomíjeno. Zachování čichu není jednoduché, u velkých meningiomů mnohdy nemožné. Přesto by však vyšetření čichu mělo být součástí vyšetřovacího algoritmu před resekcí OGM a po ní. Stejně tak je vhodné i základní psychologické vyšetření u těchto pacientů.
Podpořeno granty 15-327 91A, MO 1012 a Q 25.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Přijato k recenzi: 6. 9. 2017
Přijato do tisku: 23. 11. 2017
doc. MUDr. David Netuka, Ph.D.
Neurochirurgická a neuroonkologická klinika 1. LF UK a ÚVN Praha
U vojenské nemocnice 1200
169 02 Praha 6
e-mail: david.netuka@uvn.cz
Zdroje
1. Abbassy M, Woodard TD, Sindwani R et al. An overview of anterior skull base meningiomas and the endoscopic endonasal approach. Otolaryngol Clin North Am 2016; 49(1): 141–152. doi: 10.1016/ j.otc.2015.08.002.
2. Bitter AD, Stavrinou LC, Ntoulias G et al. The role of the pterional approach in the surgical treatment of olfactory groove meningiomas: a 20-year experience. J Neurol Surg B Skull Base 2013; 74(2): 97–102. doi: 10.1055/ s-0033-1333618.
3. Romani R, Lehecka M, Gaal E et al. Lateral supraorbital approach applied to olfactory groove meningiomas: experience with 66 consecutive patients. Neurosurgery 2009; 65(1): 39–52. doi: 10.1227/ 01.NEU.0000346266.69493.88.
4. Durante F. Estirpazione di un tumore endocranico. Arch Atti Social Chir 1886; 2 : 252–255.
5. Cushing H, Eisenhardt TL. The olfactory groove meningiomas with primary anosmia. In: Cushing H, Eisenhardt TL (eds). Meningiomas. Springfield: Charles C. Thomas 1938. 250–282.
6. Sameš M, Vachata P, Zolal A et al. Chirurgie baze lební (uvnitř minimonografie video). Cesk Slov Neurol N 2013; 76/ 109(4): 402–424.
7. Netuka D, Masopust V, Belšan T et al. Endoskopické endonazální operace meningeomů baze lební. Cesk Slov Neurol N 2013; 76/ 109(4): 446–452.
8. Toller SV. Assessing the impact of anosmia: review of a questionnaire‘s findings. Chem Senses 1999; 24(6): 705–712.
9. Komotar RJ, Starke RM, Raper DM et al. Endoscopic endonasal versus open transcranial resection of anterior midline skull base meningiomas. World Neurosurg 2012; 77(5–6): 713–724. doi: 10.1016/ j.wneu.2011.08.025.
10. Hentschel SJ, DeMonte F. Olfactory groove meningiomas. Neurosurg Focus 2003; 14(6): e4.
11. Fox D, Khurana VG, Spetzler RF. Olfactory groove/ planum sphenoidale meningiomas. In: Lee JH (ed). Meningiomas: diagnosis, treatment, and outcome. London: Springer 2008.
12. Rosen CL, Ammerman JM, Sekhar LN et al. Outcome analysis of preoperative embolization in cranial base surgery. Acta Neurochir (Wien) 2002; 144(11): 1157–1164.
13. Bassiouni H, Asgari S, Stolke D. Olfactory groove meningiomas: functional outcome in a series treated microsurgically. Acta Neurochir (Wien) 2007; 149(2): 109–121.
14. Gazzeri R, Galarza M, Gazzeri G. Giant olfactory groove meningioma: ophthalmological and cognitive outcome after bifrontal microsurgical approach. Acta Neurochir (Wien) 2008; 150(11): 1117–1125. doi: 10.1007/ s00701-008-0142-z.
15. Spektor S, Valarezo J, Fliss DM et al. Olfactory groove meningiomas from neurosurgical and ear, nose, and throat perspectives: approaches, techniques, and outcomes. Neurosurgery 2005; 57 (4 Suppl): 268–280.
16. Nakamura M, Struck M, Roser F et al. Olfactory groove meningiomas: clinical outcome and recurrence rates after tumor removal through the frontolateral and bifrontal approach. Neurosurgery 2007; 60(5): 844–852.
17. Magerová H, Laczó J, Vyhnálek M et al. Vyšetření čichu a jeho význam pro diagnostiku neurodegenerativních onemocnění. Neurol Praxi 2008; 9(1): 30–32.
18. Doty RL. Office procedures for quantitative assessment of olfactory function. Am J Rhinol 2007; 21(4): 460–473.
19. Smith DV. Assessment of patients with taste and smell disorders. Acta Otolaryngol (Suppl) 1988; 458 : 129–133.
20. Schaller C, Rohde V, Hassler W. Microsurgical removal of olfactory groove meningiomas via the pterional approach. Skull Base Surg 1994; 4(4): 189–192.
21. Turazzi S, Cristofori L, Gambin R et al. The pterional approach for the microsurgical removal of olfactory groove meningiomas. Neurosurgery 1999; 45(4): 821–825.
22. Pallini R, Fernandez E, Lauretti L et al. Olfactory groove meningioma: report of 99 cases surgicallytreated at the Catholic University School of Medicine, Rome. World Neurosurg 2015; 83(2): 219–231. doi: 10.1016/ j.wneu.2014.11.001.
23. Guduk M, Yener U, Sun HI et al. Pterional and unifrontal approach for the microsurgical resection of olfactory groove meningiomas: experience with a series of 61 consecutive patients. Turk Neurosurg 2017; 27(5): 707–715. doi: 10.5137/ 1019-5149.JTN.17154-16.1.
24. Ciurea AV, Iencean SM, Rizea RE et al. Olfactory groove meningiomas: a retrospective study on 59 surgical cases. Neurosurg Rev 2012; 35(2): 195–202. doi: 10.1007/ s10143-011-0353-2.
25. Jang WY, Jung S, Jung TY et al. Preservation of olfaction in surgery of olfactory groove meningiomas. Clin Neurol Neurosurg 2013; 115(8): 1288–1292. doi: 10.1016/ j.clineuro.2012.12.004.
26. Welge-Luessen A, Temmel A, Quint C et al. Olfactory function in patients with olfactory groove meningioma. J Neurol Neurosurg Psychiatry 2001; 70(2): 218–221.
27. Allison T, Goff WR. Human cerebral evoked responses to odorous stimuli. Electroencephalogr Clin Neurophysiol 1967; 23(6): 558–560.
28. Kobal G, Hummel C. Cerebral chemosensory evoked potentials elicited by chemical stimulation of the human olfactory and respiratory nasal mucosa. Electroencephalogr Clin Neurophysiol 1988; 71(4): 241–250.
29. Sato M, Kodama N, Sasaki T et al. Olfactory evoked potentials: experimental and clinical studies. J Neurosurg 1996; 85(6): 1122–1126.
30. Thirumala PD, Habeych ME, Crammond DJ et al. Neurophysiologic intraoperative monitoring of olfactory and optic nerves. J Clin Neurophysiol 2011; 28(6): 538–542. doi: 10.1097/ WNP.0b013e31823e954e.
31. Lapid H, Hummel T. Recording odor-evoked response potentials at the human olfactory epithelium. Chem Senses 2013; 38(1): 3–17. doi: 10.1093/ chemse/ bjs073.
32. Fournel A, Ferdenzi C, Sezille C et al. Multidimensional representation of odors in the human olfactory cortex. Hum Brain Mapp 2016; 37(6): 2161–2172. doi: 10.1002/ hbm.23164.
33. Berlin HA, Stern ER, Ng J et al. Altered olfactory processing and increased insula activity in patients with obsessive-compulsive disorder: an fMRI study. Psychiatry Res 2017; 262 : 15–24. doi: 10.1016/ j.pscychresns.2017.01.012.
34. Yasargil MG. Microneurosurgery I. Stuttgart: Georg Thieme Verlag 1984.
35. Olivecrona H, Urban H. Über Meningeome der Siebbeinplatte. Brun‘s Beitr Klin Chir 1935; 161 : 224–253.
36. Dandy WE. Hirnchirurgie. Leipzig: Johann Ambrosius Barth 1938.
37. Tonnis W. Zur Operation der Meningeome der Siebbeinplatte. Zentralbl Neurochir 1938; 1 : 1–7.
38. Morley TP. Tumors of the cranial meninges. In: Youmans JR (ed). Neurological surgery: a comprehensive reference guide to the diagnosis and management of neurosurgical problems. Philadelphia: Saunders 1973.
39. MacCarty CS, Piepgras DG, Ebersold MJ. Meningeal tumors of the brain. In: Youmans JR (ed). Neurological surgery: a comprehensive reference guide to the diagnosis and management of neurosurgical problems. Philadelphia: Saunders 1982.
40. Ojemann RG. Meningiomas: clinical features and surgical management. In: Wilkins RH, Rengachary SS (eds). Neurosurgery. New York: McGraw-Hil 1985.
41. Adappa ND , Lee JY, Chiu AG et al. Olfactory groove meningioma. Otolaryngol Clin North Am 2011; 44(4): 965–980.
42. Liu JK, Christiano LD, Patel SK et al. Surgical nuances for removal of olfactory groove meningiomas using the endoscopic endonasal transcribriform approach. Neurosurg Focus 2011; 30(5): E3. doi: 10.3171/ 2011.2.FOCUS 116.
43. Tsikoudas A, Martin-Hirsch DP. Olfactory groove meningiomas. Clin Otolaryngol Allied Sci 1999; 24(6): 507–509.
44. Mielke D, Mayfrank L, Psychogios MN et al. The anterior interhemispheric approach: a safe and effective approach to anterior skull base lesions. Acta Neurochir (Wien) 2014; 156(4): 689–696. doi: 10.1007/ s00701-013-1972-x.
45. Obeid F, Al-Mefty O. Recurrence of olfactory groove meningiomas. Neurosurgery 2003; 53(3): 534–542.
46. Knopp U, Sepehrnia A. Preservation of olfaction in bifrontal craniotomies for lesions of the anterior and middle cranial fossa. Laryngorhinootologie 2005; 84(5): 319–322.
47. Schroeder HW. Indications and limitations of the endoscopic endonasal approach for anterior cranial base meningiomas. World Neurosurg 2014; 82 (6 Suppl): S81–S85. doi: 10.1016/ j.wneu.2014.07.030.
48. Liu JK, Hattar E, Eloy JA. Endoscopic endonasal approach for olfactory groove meningiomas: operative technique and nuances. Neurosurg Clin N Am 2015; 26(3): 377–388. doi: 10.1016/ j.nec.2015.03.009.
49. de Almeida JR, Snyderman CH, Gardner PA et al. Nasal morbidity following endoscopic skull base surgery: a prospective cohort study. Head Neck 2011; 33(4): 547–551. doi: 10.1002/ hed.21483.
50. Koutourousiou M, Fernandez-Miranda JC, Wang EWet al. Endoscopic endonasal surgery for olfactory groove meningiomas: outcomes and limitations in 50 patients. Neurosurg Focus 2014; 37(4): E8.
51. Shin M, Kondo K, Saito N. Current status of endoscopic endonasal surgery for skull base meningiomas: review of the literature. Neurol Med Chir (Tokyo) 2015; 55(9): 735–743.
52. Flickinger JC, Kondziolka D, Maitz AH et al. Gamma knife radiosurgery of imaging-diagnosed intracranial meningioma. Int J Radiat Oncol Biol Phys 2003; 56(3): 801–806.
53. Lomax NJ, Scheib SG. Quantifying the degree of conformity in radiosurgery treatment planning. Int J Radiat Oncol Biol Phys 2003; 55(5): 1409–1419.
54. Youssef AS, Sampath R, Freeman JL et al. Unilateral endonasal transcribriform approach with septal transposition for olfactory groove meningioma: can olfaction be preserved? Acta Neurochir (Wien) 2016; 158(10): 1965–1972. doi: 10.1007/ s00701-016-2922-1.
55. Herz RS, Eliassen J, Beland S et al. Neuroimaging evidence for the emotional potency of odor-evoked memory. Neuropsychologia 2004; 42(3): 371–378.
55. Moberg PJ, Agrin R, Gur RE et al. Olfactory dysfunction in schizophrenia: a qualitative and quantitative review. Neuropsychopharmacology 1999; 21(3): 325–340.
57. Passagia JG, Chirossel JP, Favre JJ et al. Surgical approaches to the anterior fossa, and preservation of olfaction. Adv Tech Stand Neurosurg 1999; 25 : 195–241.
58. Mirimanoff RO, Dosoretz DE, Linggood RM et al. Meningioma: analysis of recurrence and progression following neurosurgical resection. J Neurosurg 1985; 62(1): 18–24.
59. Maiuri F, Salzano FA, Motta S et al. Olfactory groove meningioma with paranasal sinus and nasal cavity extension: removal by combined subfrontal and nasal approach. J Craniomaxillofac Surg 1998; 26(5): 314–317.
60. Cardali S, Romano A, Angileri FF et al. Microsurgical anatomic features of the olfactory nerve: relevance to olfaction preservation in the pterional approach. Neurosurgery 2005; 57 (1 Suppl): 17–21.
Štítky
Detská neurológia Neurochirurgia Neurológia
Článek EditorialČlánek Neuropatologické okénkoČlánek Poděkování recenzentůmČlánek Dopis redakciČlánek Leiomyom dlaně
Článok vyšiel v časopiseČeská a slovenská neurologie a neurochirurgie
Najčítanejšie tento týždeň
2018 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Neuromultivit v terapii neuropatií, neuritid a neuralgií u dospělých pacientů
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Komentár ku kontroverziám Traumy ako príčina extrapyramídových syndrómov
- Trombóza kavernózního splavu – stále aktuální komplikace rinosinusitidy
- Radikulopatie Th1 na podkladě masivního výhřezu disku Th1/ 2
- Dlouhodobé sledování pacienta s primárním meningeálním melanocytomem krční míchy
- Neuropatologické okénko
- Neuropatologické post mortem vyšetření mozku a míchy v deseti bodech – co může neurolog od neuropatologa očekávat při verifikaci klinické diagnózy neurodegenerativního onemocnění?
- Olfaktoriální meningiomy – chirurgická léčba, její rizika a možnosti zachování čichu
- Poděkování recenzentům
- Analýza dat v neurologii LXVII. - Statistická analýza studií s jedním zařazeným pacientem („N of 1 trials“)
- Dopis redakci
- Zemřel prim. MU Dr. Jan Országh, CSc.
- Neuropaliativní a rehabilitační péče u pacientů v pokročilé fázi progresivních neurologických onemocnění
- Ochranné faktory kognitivního deficitu u roztroušené sklerózy
- Měření kognitivních funkcí pomocí krátkých opakovatelných neuropsychologických baterií
- Editorial
- Test gest (TEGEST) k rychlému vyšetření epizodické paměti u mírné kognitivní poruchy
- Význam morfologických a klinických klasifikací stenózy bederní páteře v předoperační rozvaze
- Parosmie a fantosmie u pacientů s poruchou čichu
- Syndróm Dravetovej s mutáciou v SCN1A géne, genetické aspekty a klinické skúsenosti
- Porozumenie viet u slovensky hovoriacich pacientov s Parkinsonovou chorobou
- Neurochirurgické předatestační vzdělávání v ČR
- Alternativní formy pro české verze Paměťového testu učení, Reyovy-Osterriethovy komplexní figury a testu Verbální fluence
- Traumata jako příčina extrapyramidových syndromů
- Pilotní studie efektu ambulantní funkční peroneální stimulace
- Spondylodiscitida z pohledu neurologa
- Traumy ako príčina extrapyramídových syndrómov
- Leiomyom dlaně
- Gigantický kavernózní hemangiom zadní jámy nasedající na duru napodobující hemangiopericytom
- Statiny a jejich vliv na periferní nervový systém
- Česká a slovenská neurologie a neurochirurgie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Spondylodiscitida z pohledu neurologa
- Parosmie a fantosmie u pacientů s poruchou čichu
- Měření kognitivních funkcí pomocí krátkých opakovatelných neuropsychologických baterií
- Trombóza kavernózního splavu – stále aktuální komplikace rinosinusitidy
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




