-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Krvácivé komplikace antikoagulační léčby u geriatrických pacientů
Haemorrhaging complications of anticoagulation therapy in geriatric patients.
Anticoagulants became an indispensable drug class in treatment and prevention of thromboembolic events, of both arterial and venous origin in geriatric patients. The paper reviews potential risks of anticoagulants treatment in seniors, particularly haemorrhaging complications. Special concern is given to novel anticoagulants (NOAC) in comparison to warfarin.
We present a case study and a pilot patients´ sample who suffered clinically significant bleeding complications while on anticoagulation therapy. Our data support the fact that patients of advanced age are at higher risk of bleeding. Therefore the decision to start the treatment with anticoagulants including the novel NOAC must be strictly individualized, based of risk/benefit assessment.KEYWORDS:
anticoagulants – NOAC - warfarin – bleeding complications – risk-scoring tools – benefit/risk assessment
Autoři: M. Nováková; L. Graur
Vyšlo v časopise: Geriatrie a Gerontologie 2016, 5, č. 1: 11-14
Kategorie: Kazuistiky
Souhrn
Antikoagulační léčba získala v geriatrii své nezastupitelné místo v léčbě a prevenci tromboembolických příhod tepenné i žilní etiologie. Článek se zabývá potenciálními riziky antikoagulační léčby u seniorů, zejména krvácivými komplikacemi. Pozornost je věnována novým antikoagulanciím (NOAC) ve srovnání s warfarinem.
Uvedená kazuistika i soubor dat pacientů, kteří prodělali krvácivou komplikaci v průběhu antikoagulační terapie, svědčí pro značnou rizikovost seniorské populace a vybízí k přísně individuálnímu hodnocení každého pacienta před nasazením antikoagulace včetně NOAC na základě zvážení poměru benefit/riziko.KLÍČOVÁ SLOVA:
antikoagulační léčba – NOAC – warfarin – krvácivé komplikace – skórovací schémata – poměr benefit/rizikoÚvod
Antikoagulační léčba získala v geriatrii v posledním desetiletí své nezastupitelné místo v léčbě a prevenci tromboembolických příhod tepenné i žilní etiologie. Jsou to právě geriatričtí pacienti, kteří jsou významně ohroženi tromboembolickými komplikacemi při fibrilaci síní, ale i hlubokou žilní trombózou a plicní embolií, zejména pokud jde o pacienty se sníženou mobilitou, pacienty po traumatech a operacích či pacienty s nádorovým onemocněním.
V minulosti převažovaly spíše obavy z komplikací antikoagulační léčby u polymorbidních a křehkých seniorů, především závažných krvácení. Proto v mnoha případech s ohledem na věk nebyla antikoagulační terapie použita vůbec nebo byla suplována terapií antiagregační, u které byl sice nižší výskyt krvácivých komplikací, ale také signifikantně vyšší počet významných komplikací tromboembolických, především v podobě kardioembolizačních cévních mozkových příhod.
Vzhledem k narůstajícímu počtu pacientů s fibrilací síní, která je často nazývána „epidemií 21. století“, narůstá i počet kardioembolizačních iktů, a to zejména ve skupině pacientů nad 65 let věku. Bylo prokázáno, že fibrilace síní zvyšuje pravděpodobnost iktu až pětkrát bez ohledu na to, zda je symptomatická či asymptomatická. Dopad cévní mozkové příhody na kvalitu života geriatrického pacienta je pochopitelně velice závažný, zvláště pokud jsou přítomny již premorbidně funkční deficity. Pokud bychom použili neurologické hodnocení tzv. Rankinovým skóre, až 40 % pacientů po iktu dosáhuje skóre 5, což znamená ležícího, inkontinentního, zcela nesoběstačného pacienta plně závislého na pečovateli(1).
Výskyt fibrilace síní a tromboembolických komplikací zejména v podobě CMP exponenciálně stoupá s věkem, a to v souvislosti se změnami ve stáří – chronickým srdečním selháním, renální insuficiencí, změnami v produkcikoagulačních faktorů – především vzestupem fibrinogenu, zvýšenou aktivitou trombocytů, zvýšením výskytu závažných kardiovaskulárních, onkologických, degenerativních a zánětlivých onemocnění. Incidence fibrilace síní se zdvojnásobuje s každou věkovou dekádou, ve věku 80–89 let je tedy incidence 8–10 %, přibližně 70 % nemocných s touto arytmií je ve věku mezi 65–85 lety(1,2). Správně vedenou antikoagulační léčbou lze snížit riziko kardioembolizačních iktů u pacientů s fibrilací síní až o dvě třetiny(2).
Stejně tak i žilní tromboembolickou nemocí jsou ohroženi senioři více než středněvěká populace. V patogenezi se zde více uplatňují získané rizikové faktory než hereditární. Ve vyšším věku také narůstá počet asymptomatických žilních trombóz, které nezřídka končí náhlou smrtí v důsledku masivní plicní embolizace(3).
Na základě výše uvedených faktů je jasné, že i populace geriatrických pacientů významně profituje z antikoagulační léčby. Je však potřeba si uvědomit i rizika, která s sebou podávání antikoagulační léčby nese.
Warfarin versus NOAC
Pilířem antikoagulační terapie byly po dlouhá léta antagonisté vitaminu K, respektive nejznámější a nejčastěji podávaný warfarin. Léčba warfarinem však s sebou nese mnohá úskalí, týkající se hlavně compliance pacienta – dodržování diety, pravidelné kontroly INR. K této compliance je samozřejmě zapotřebí dobrý kognitivní stav nemocného, případně zajištění spolehlivým pečovatelem. Z tohoto důvodu i geriatrická medicína s povděkem přivítala tzv. nová antikoagulancia (NOAC), zvláště když randomizované studie prokázaly jejich výtečnou účinnost s relativně nízkým výskytem krvácivých komplikací. Například v randomizované kontrolované studii RE-LY měl dabigatran v dávce 150 mg 2x denně oproti warfarinu nižší výskyt kardioembolizačních iktů a systémových embolizací (1,1 % vs. 1,7 % ročně) při srovnatelném výskytu závažných krvácivých komplikací (3,3 % vs. 3,6 % ročně). V Evropě byla schválena jako účinná i redukovaná dávka dabigatranu 110 mg 2x denně. Pozdější analýzy dat studie RE-LY prokázaly, že výskyt fatálních krvácení po dabigatranu v dávce 2x 110 mg je signifikantně nižší než u warfarinu (o 42 %) a nevýznamně nižší než u plné dávky dabigatranu (2x 150 mg), asi o 30 %(4).
NOAC se jeví jako bezpečná a účinná perorální antikoagulancia. Existují mezi nimi však rozdíly ve farmakokinetice, v mechanismu účinku, ale především v bezpečnosti léčby. Je tedy nutné přísně dodržovat pravidla jejich podávání a podávat správné léky správným pacientům (respektovat kontraindikace, zvážit rizikové faktory, jako jsou vyšší věk, ženské pohlaví, nižší hmotnost, mírná až střední renální insuficience). Jedině tak převáží benefity léčby nad možnými riziky(5, 6).
Monitorování terapie NOAC
Rutinní sledování účinku NOAC není nutné. V určitých situacích je ale vhodné, například při podezření na předávkování nebo při výskytu krvácivé komplikace. Velmi aktuální je také při léčbě fragilních nemocných, mezi něž patří i křehcí geriatričtí pacienti, většinou s nízkou hmotností a alterací funkce ledvin a jater.
Při terapii dabigatranem je možno k rychlé orientaci použít stanovení aktivovaného parciálního tromboplastinového času (aPTT). Podrobnějším vyšetřením je stanovení tzv. dilutovaného trombinového času komerčním testem Hemoclot. Ve skupině xabanů k rychlé orientaci stačí stanovení protrombinového či dilutovaného protrombinového času. Přesnější je ale kalibrovaná kvantitativní analýza aktivity antiXa(4).
Stanovení rizika antikoagulační léčby
Antikoagulační léčba u seniorů patří k potenciálně rizikovým terapeutickým postupům. Před zahájením léčby je vhodné provést stratifikaci výše rizika, která slouží jako důležitá pomůcka při výběru vhodné terapie a zhodnocení rizika nežádoucích účinků léčby.
Jako velmi důležitá pomůcka ke zvážení poměru benefit/riziko antikoagulační léčby byla vytvořena stratifikační schémata. Nejznámější pro riziko tromboembolie je CHADS2 vypracované v roce 2001, upravené v roce 2003 a v roce 2010 modifikované na přesnější schéma CHA2DS2-VASc. Tato schémata umožňují rozdělit nemocné s fibrilací síní do tří skupin podle stupně rizika tromboembolie a vzniku cévní mozkové příhody na nízké, střední a vysoké riziko. Pokud se nevyskytnou kontraindikace, doporučuje se u pacientů se skóre CHA2DS2-VASc ≥ 2 zahájení dlouhodobé antikoagulační léčby. Ke stanovení rizika krvácení byl vypracován skórovací systém HAS-BLED(4).
Při porovnání obou skórovacích schémat (tab. 1) je jasné, že některé rizikové faktory v obou schématech jsou prakticky shodné, např. věk, hypertenze nebo CMP v anamnéze, z čehož vyplývá, že pacienti s vysokým rizikem tromboembolie mají i vysoké riziko krvácení.
Tab. 1. Skórovací schémata pro hodnocení rizika tromboembolie a krvácivých komplikací před zahájením antikoagulační léčby 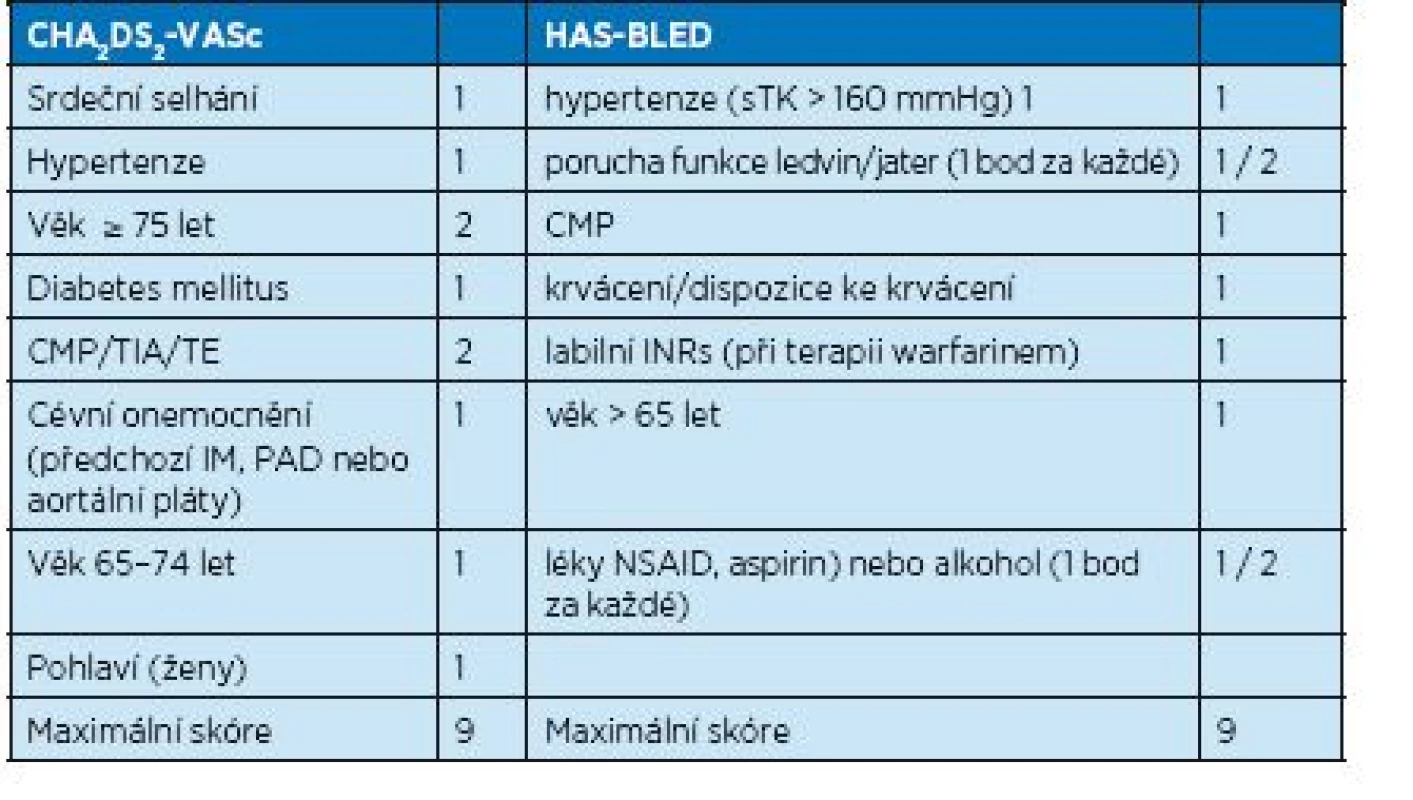
V tuto chvíli selhává pomocná role skórovacích schémat v rozhodování o způsobu terapie a musíme každého pacienta hodnotit přísně individuálně(1).
Kazuistika
Pacientka, nar. 1942
Anamnéza: Běžné dětské choroby, několik let léčena pro hypertenzi, depresivní syndrom a osteoporózu skeletu. Kardiálně nestonala, plicní choroby 0, diabetes 0, tromboembolie 0. Operace: Stav po TEP kyčelního kloubu vpravo v r. 2005, v r. 2007 komplikováno rozvojem hematomu v oblasti TEP pravé kyčle, řešeno punkcí hematomu pod CT kontrolou – úrazový mechanismus vzniku hematomu nebyl znám, antikoagulancia ani antiagregační léčbu neužívala.
Abúzus: nekuřačka, alkohol příležitostně, minimálně
AA: negativní
FA: Cipralex 10 mg 1–0–0 tbl., Micardis 80 mg 1–0–0 tbl., Fosamax 70 mg tbl. 1x týdně
NO: Přijata akutně na neurologickou kliniku pro asi 2 dny trvající slabost pravostranných končetin a zhoršení řeči. Deset dnů před vznikem této symptomatologie vertigo s pádem, trauma neutrpěla. Podle provedené MRI mozku zjištěno ložisko ischemie v zadním raménku capsulla interna vlevo. Na vstupním EKG sinusový rytmus, při Holterově monitoraci ale zjištěny paroxysmy fibrilace síní. Echokardiograficky normální funkce levé komory, TEE neprokázalo zdroj embolizace. Pacientka léčena terapeutickou dávkou LMWH (Clexane 2x 0,6 ml s. c.). Vzhledem k paroxysmální FiS zahájena antiarytmická terapie kombinací Propanorm 3x 150 mg + Betaloc ZOK 1x 50 mg, nasazen atorvastatin 80 mg denně, hypertenze i nadále korigována sartanem (Micardis 80 mg denně). Následně pacientka převedena na p. o. antikoagulační terapii dabigatranem (2x 150 mg denně).
V průběhu hospitalizace došlo k rozvoji neurologického nálezu ve smyslu zhoršení pravostranné hemiparézy z lehké na střední, při ukončení hospitalizace na neurologii pacientka schopna sedu s dopomocí, Rankin skóre 4. Pacientka normotenzní, na EKG opakovaně sinusový rytmus s komorovou odpovědí kolem 70/min, laboratorní parametry: biochemie a krevní obraz bez odchylek, kreatinin 63 µmol/l, urea 3,9 mmol/l, koagulace při propuštění: APTT 43,80, (APTT normal 30,50), INR 1,21, TT 160,80 s (TT normal 13,80 s), Hemoclot 80 ng/ml.
Po 18 dnech pacientka přeložena k další rehabilitaci na Kliniku rehabilitace a tělovýchovného lékařství, kde hospitalizována 25 dní, odtud přeložena k pokračování rehabilitace na naše oddělení (Centrum následné péče).
Průběh hospitalizace v Centru následné péče: Stav při přijetí – pacientka kardiopulmonálně kompenzovaná, přetrvává středně těžká pravostranná hemiparéza, více vyjádřená na PHK, schopna perorálního příjmu, bez fatické poruchy, schopna sedu s dopomocí a postavení do vysokého chodítka s dopomocí. Na EKG vstupně sinusový rytmus, normotenzní.
Zavedená medikace: Propanorm 150 mg 1–1–1 tbl., Betaloc ZOK 100 mg 1–0–0 tbl., Pradaxa 150 mg 1–0–1 tbl., Apo-atorvastatin 40 mg 0–0–2 tbl., Tolura 40 mg 1–0–0 tbl., Escirdec 20 mg 1–0–0 tbl., Trittico 75 mg 2/3 tbl. na noc
Průběh hospitalizace: Pacientka po dobu téměř 2 měsíců ve stabilizovaném stavu, kardiopulmonálně kompenzována, rehabilitovala stabilitu sedu a chůzi ve vysokém chodítku s dopomocí, prováděna taktéž ergoterapie zaměřená na rozcvičení paretické pravé horní končetiny. Chronická medikace nebyla měněna, pacientka neprodělala žádný infekt ani jinou chorobu komplikující stav. V průběhu hospitalizace 2x kontrolována laboratoř – bez závažné patologie – APTT 55,60 (norma 30,50) při terapii Pradaxou, pacientka bez známek krvácení. Během rehabilitace nedošlo k žádnému pádu či jinému traumatu. 59. den hospitalizace došlo ke zhoršení celkového stavu – malátnost, apatie, hypotenze 95/60 mmHg , zhoršení neurologické symptomatiky. Kontrolní CT mozku bez vývoje, nesvědčilo pro recidivu CMP. V akutně nabrané laboratoři však zjištěn významný pokles v hodnotě hemoglobinu ze 127 g/l na 78 g/l, souběžně leukocytóza 14,7 x 109/l. Odebrány též koagulační parametry vzhledem k chronické medikaci dabigatranem , kde zjištěno významné prodloužení TT nad 2 minuty, APTT 60,6 s, Hemoclot 257,4 ng/ml.
Pacientka urgentně přeložena na JIP chirurgické kliniky, kde pátráno po zdroji krvácení. Provedena endoskopie horní části trávicího traktu s negativním nálezem, USG břicha též bez alarmující patologie. Na CT břicha a malé pánve zjištěn rozsáhlý hematom retroperitoneálně: 130 x 130 x 100 mm.
Pacientce podány 3x TU erymasy, vysazena Pradaxa a nasazena redukovaná dávka LMWH – Clexane 0,4 ml s. c. 1x denně. Vzhledem ke stabilizaci stavu bylo i nadále postupováno konzervativně. Na kontrolním CT pánve po 11 dnech patrná regrese hematomu na 26 x 45 mm. Po 14 dnech pacientka navrácena na lůžko následné péče, kde obnovila přerušenou rehabilitaci. Dávka Clexanu upravena na 0,6 ml s. c. 1x denně (při hmotnosti pacientky 65 kg) za kontrol anti-Xa, které udržováno v terapeutickém rozmezí (hodnoty 0,53–0,77 U/ml).
V dalším průběhu již pacientka bez známek krvácení, bez komplikací, stran rehabilitace bylo dosaženo schopnosti chůze ve vysokém chodítku s asistencí a částečné kontinence, pacientka sebeobslužná v rámci lůžka, mimo lůžko nutná dopomoc druhé osoby.
Po 2 měsících hospitalizace propuštěna do domácí péče za pomoci homecare – má pečujícího manžela, který je povoláním lékař a který zajišťuje aplikaci LMWH.
Diskuse
Prezentovaná pacientka zcela jistě splňovala indikaci k zahájení antikoagulační léčby po proběhlé cévní mozkové příhodě kardioembolizační etiologie při nově zjištěné paroxysmální fibrilaci síní. Poměr rizik podle skórovacích systémů CHA2DS2-VASc/HAS-BLED byl 5 : 4, tedy riziko tromboembolie bylo vyšší než riziko krvácení. S ohledem na věk, dobrý fyzický i kognitivní stav a dobrou prognózu pacientky byla zvolena terapie dabigatranem. Redukce dávky dabigatranu nebyla nutná; pacientka měla normální ledvinné i jaterní funkce. Ostatní medikace pacientky byla zcela racionální, indikovaná a nezvyšovala riziko krvácení ani nepředstavovala rizikovou interakci s dabigatranem. Pacientka veškerou medikaci včetně dabigatranu užívala po dobu hospitalizace, byla jí tedy podávána zdravotnickým personálem, tudíž byla vyloučena non-compliance ze strany pacientky. Po celou dobu hospitalizace neprodělala pacientka žádné komplikující onemocnění (např. infekt, trauma apod.). Přesto došlo k závažné krvácivé komplikaci v podobě zakrvácení do retroperitonea, které vyžadovalo hospitalizaci a podání krevních derivátů.
Za jediný rizikový faktor může být považován anamnestický údaj o hematomu v oblasti TEP pravé kyčle v roce 2007, který byl punktován pod CT kontrolou. Antikoagulační léčba však byla nasazena až 8 let po této příhodě, tudíž se nepředpokládala recidiva krvácení v této oblasti.
Uvedená kazuistika ukazuje, že ani při pečlivém zvážení všech rizik se často nevyhneme komplikaci antikoagulační terapie v podobě závažného krvácení, a to i při užití preparátu ze skupiny nových antikoagulancií, která by podle provedených studií měla být bezpečnější než warfarin.
Naše zkušenosti s krvácivými komplikacemi antikoagulační léčby
V období od března 2014 do září 2015, tedy po dobu 18 měsíců, jsme zaznamenávali pacienty, kteří byli přijati do Centra následné péče FNM z akutních oddělení, kde byli hospitalizováni pro krvácení při antikoagulační léčbě. Celkem jsme zachytili 46 pacientů, z toho ve 2 případech došlo ke krvácivé komplikaci až v průběhu hospitalizace na našem oddělení. Centrum následné péče FNM disponuje 381 lůžky následné péče a obrat činí kolem 1300 přijatých pacientů ročně.
U pacientů jsme retrospektivně hodnotili věk a pohlaví pacientů a jejich rizikovost podle skóre CHA2DS2-VASc a HAS-BLED, indikaci k antikoagulační léčbě, zvolený léčivý přípravek, typ krvácení, nutnost chirurgické nebo endoskopické intervence.
Výsledky: Celkem jsme zachytili 46 pacientů, z toho 18 mužů a 28 žen. Průměrný věk pacientů činil 83,1 roku. Nejčastější indikací k užívání antikoagulační léčby byla fibrilace síní, a to u 37 pacientů (tab. 2). Nejčastěji pacienti krváceli při užívání warfarinu – ve 25 případech, 13 pacientů mělo krvácivou komplikaci při užívání NOAC , 8 pacientů krvácelo při léčbě LMWH (Fraxiparin a Clexane) (tab. 3). Nutnost chirurgické nebo endoskopické intervence k zastavení krvácení vyvstala u 11 pacientů, ostatní byli řešeni konzervativně. Ve skupině pacientů užívajících NOAC mělo krvácivou komplikaci nejvíce pacientů na terapii dabigatranem, a to jak v dávce plné, tak redukované.
Tab. 2. Indikace antikoagulační léčby u souboru nemocných s krvácivými komplikacemi (n = 46) 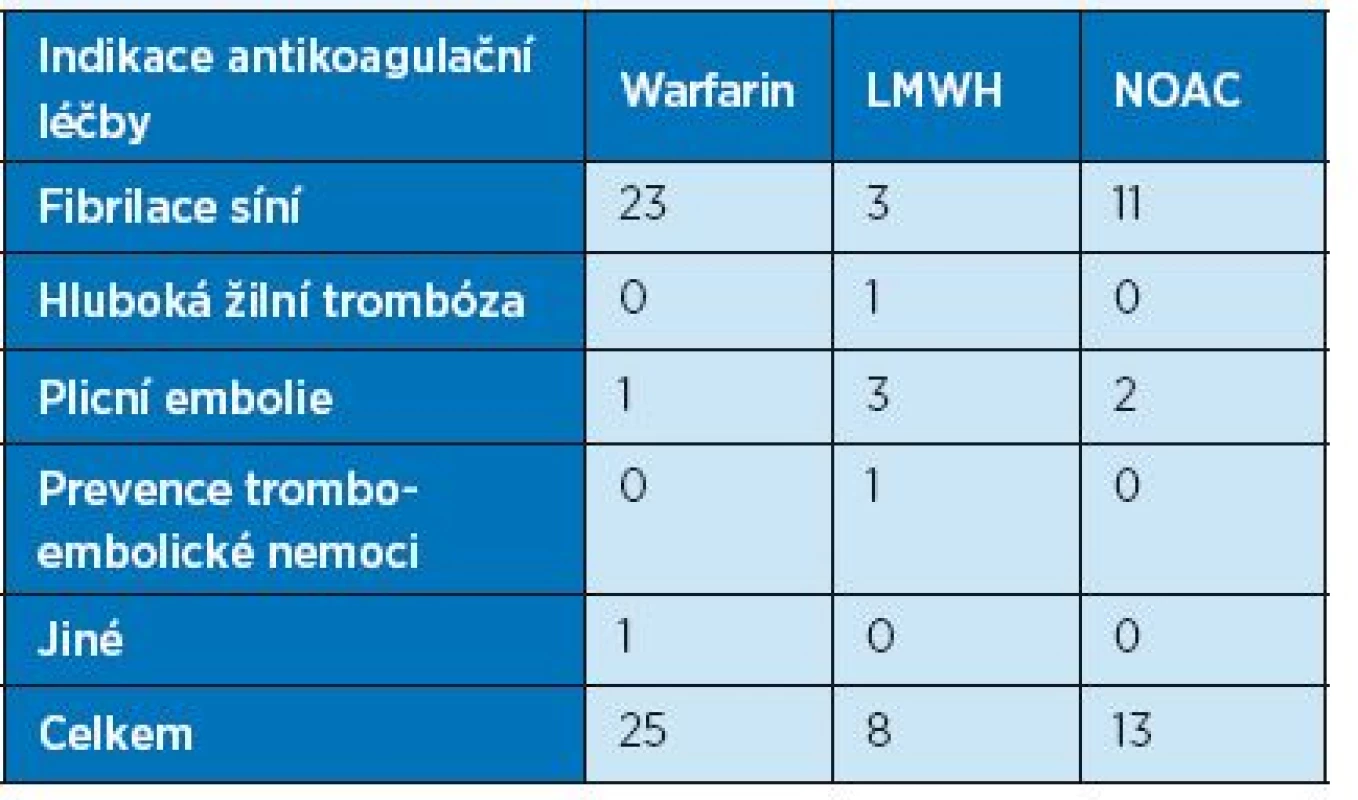
Tab. 3. Lokalizace krvácení a nutnost intervence u krvácivých komplikací při antikoagulační léčbě 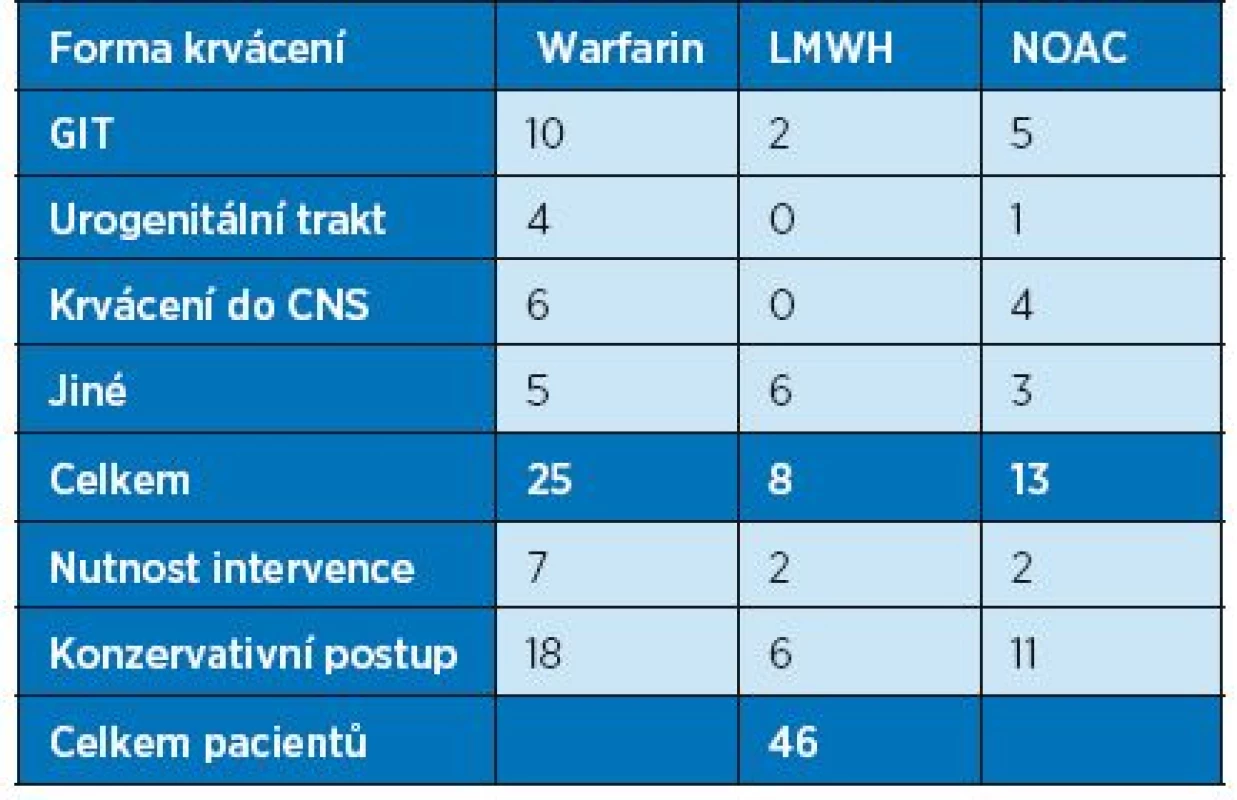
Tab. 4. Dávkování NOAC u souboru pacientů s krvácivou komplikací 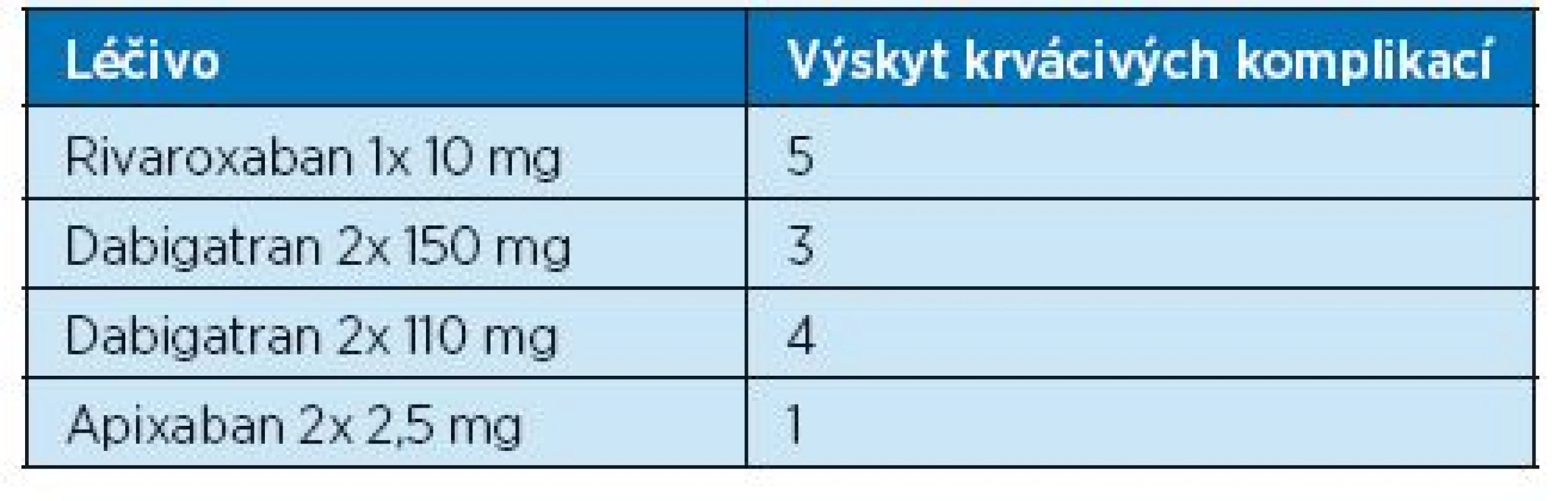
Retrospektivně jsme u všech pacientů provedli stanovení rizika tromboembolie a krvácení podle skórovacích systémů CHA2DS2-VASc a HAS-BLED. Z výsledků vyplynulo, že všichni pacienti měli současně vysoké riziko tromboembolie i krvácení (tab. 5). Jednoznačně však převažovali pacienti, u nichž riziko tromboembolie bylo vyšší než riziko krvácení, což svědčí o správné indikaci antikoagulační léčby (tab. 6). Pouze u 1 pacienta přesáhlo riziko krvácení riziko tromboembolie, u 4 pacientů byla rizika stejná.
Tab. 5. Rizikovost krvácivých a tromboembolických komplikací u souboru nemocných 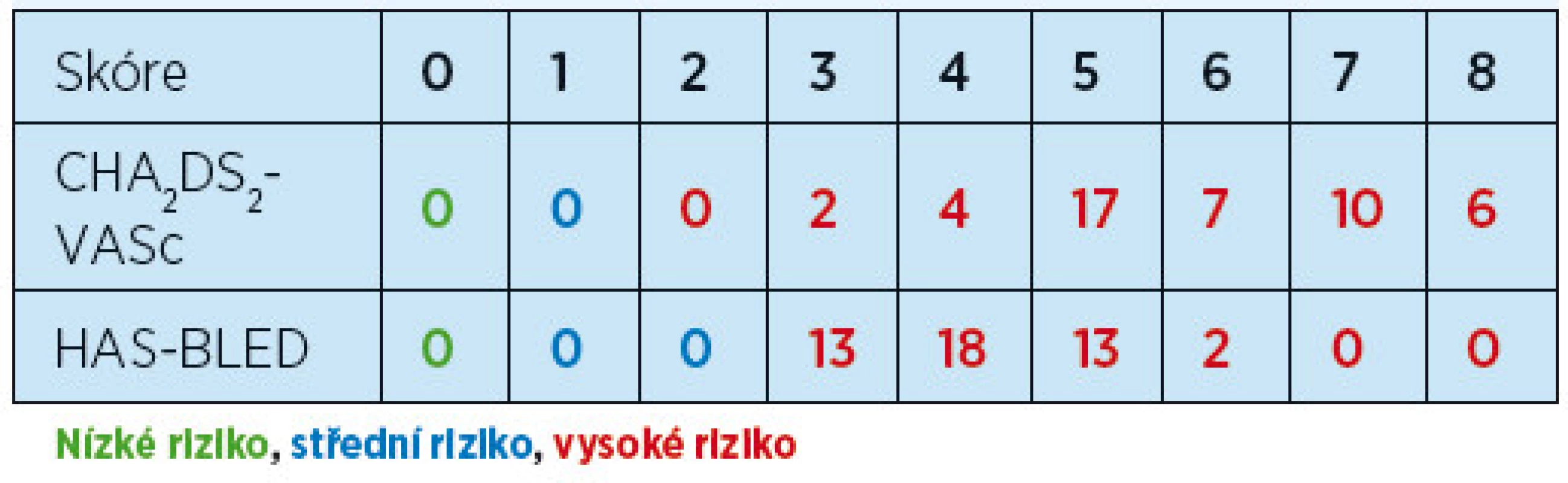
Tab. 6. Soubor nemocných podle převažujícího rizika 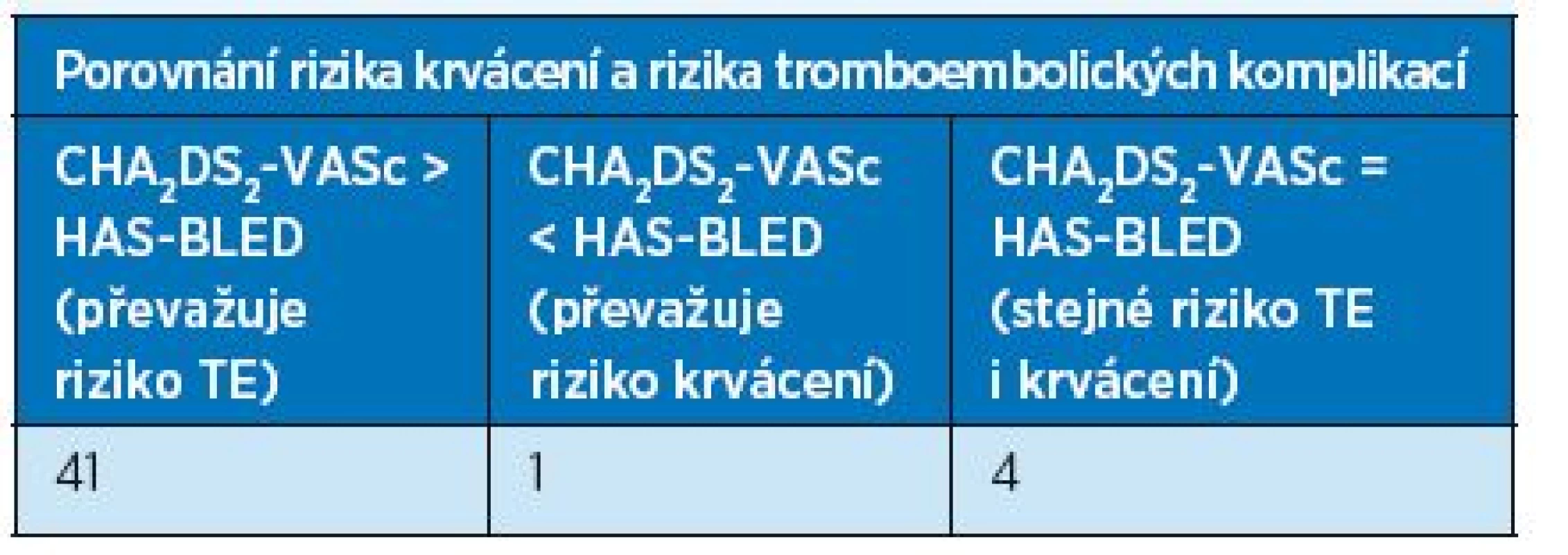
Závěr
Antikoagulační léčba u geriatrických pacientů i přes stále větší využití relativně bezpečnějších nových antikoagulancií představuje i nadále vysoce rizikovou oblast, kde je nutno počítat s výskytem nežádoucích komplikací, zejména v podobě krvácení. V uvedeném souboru pacientů jsme prokázali, že krvácivé komplikace se vyskytly i při podávání redukované dávky NOAC.
Nejvíce pacientů mělo krvácivou komplikaci při užívání warfarinu, toto číslo však svědčí spíše pro fakt, že většina geriatrických pacientů je léčena právě warfarinem.
Skórovací schémata CHA2DS2-VASc a HAS-BLED lze využít pouze hrubě orientačně a poměr benefit/riziko antikoagulační léčby je nutno stanovovat u každého pacienta přísně individuálně. U geriatrických pacientů, více než u ostatních, je třeba též pečlivě zkoumat anamnestická data, a to hluboko do minulosti, o čemž svědčí i uvedená kazuistika, kdy pacientka prodělala krvácení do oblasti kyčelního kloubu z neznámých příčin 2 roky po implantaci TEP a o 8 let později po nasazení antikoagulační léčby dabigatranem zakrvácela do retroperitonea. Je však nepochybné, že právě geriatričtí pacienti významně profitují z antikoagulační léčby. Je jen potřeba pečlivě a individuálně zhodnotit rizika a zvolit vhodné antikoagulans v optimální dávce.
Autoři prohlašují, že v souvislosti s publikací článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny farmaceutickou firmou.
MUDr. Martina Nováková,
MUDr. Ludmila Graur
Centrum následné péče 2. LF UK a FN Motol
MUDr. Martina Nováková
e-mail: Martina.Novakova@fnmotol.cz
Od roku 2012 pracuje jako primářka Centra následné péče FN Motol. Atestaci I. stupně z interního lékařství složila v roce 1995, atestaci II. stupně v témže oboru v roce 2000, atestaci z geriatrie v roce 2011. V období 1992 až 2012 pracovala na Interní klinice FN Motol. Je garantem výuky geriatrie na 2. lékařské fakultě UK.
Zdroje
1. Lefflerová K. Úskalí antikoagulační léčby fibrilace síní. Medical Tribune 14/2010.
2. Karetová D,Bultas J. Farmakoterapie tromboembolických stavů. Praha: Maxdorf 2015.
3. Musil D. Žilní tromboembolická nemoc a antikoagulační léčba u seniorů. Medicína pro praxi 10/2013.
4. Václavík J. Jak časté jsou krvácivé komplikace warfarinu a dabigatranu v praxi? Medical Tribune 8/2013.
5. Kopřiva K, Neužil P. Nová orální antikoagulancia v léčbě akutního koronárního syndromu. Intervenční a akutní kardiologie 2015 : 14(1).
6. Musil D. Žilní tromboembolická nemoc a antikoagulační léčba u seniorů. Medicína pro praxi 10/2013.
Štítky
Geriatria a gerontológia Praktické lekárstvo pre dospelých Protetika
Článek Editorial
Článok vyšiel v časopiseGeriatrie a Gerontologie
Najčítanejšie tento týždeň
2016 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
-
Všetky články tohto čísla
- Krvácivé komplikace antikoagulační léčby u geriatrických pacientů
- Vliv reminiscenční terapie na depresivitu a kognitivní funkce u seniorů v dlouhodobé péči
- Hluboká žilní trombóza a její léčba v otázkách a odpovědích
- Onemocnění štítné žlázy se zaměřením na seniorský věk
- Editorial
- Role nutrice v prevenci kognitivních poruch ve vyšším věku
- Transmisivní spongiformní encefalopatie jako příčina demence způsobená priony
- Ageismus – hrozba sociální izolace ve stáří
- 21. gerontologický kongres v Hradci Králové
- Specializace v geriatrii a kompetence geriatra
- Role výživy u seniorů podstupujících rehabilitaci
- Stručně o lidských potřebách ve stáří
- Geriatrie a Gerontologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Hluboká žilní trombóza a její léčba v otázkách a odpovědích
- Onemocnění štítné žlázy se zaměřením na seniorský věk
- Transmisivní spongiformní encefalopatie jako příčina demence způsobená priony
- Specializace v geriatrii a kompetence geriatra
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



