-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Onemocnění štítné žlázy se zaměřením na seniorský věk
Diseases of the thyroid gland with a focus on senior age.
Incidence of thyroid gland functional disorders is higher in women than in men (min. 8 : 1), whereas hyperfunction is usually connected with bothersome symptoms, reduced function often remains unnoticed. According to recent epidemiological studies the undiagnosed dysfunctions have a prevalence that reaches 6–7 %. Goitre used to be mainly a consequence of iodine deficiency. In the Czech Republic the iodine deficiency was solved in the 1950’s, so we only find goitre in the older population. Thyroid hyperfunction in senior population is usually a result of nodular goitre or toxic independent adenoma rather than from Grave´s disease. Treatment of such conditions is necessary, negative impacts on heart and bones are known, good experiences with radioiodine treatment predestine this method for application mainly in older population. Patients with hypothyroidisms must be treated and the method is the same as for young people, but it is important to start with minimal dose of levothyroxine and increase slowly. For very old seniors collaboration with the family necessary is sometimes necessary, mainly to control the exact dosing and application of the medication as well. The incidence of thyroid carcinoma is rising, surgeries are possible also for seniors, but always by specialized team of surgeons.
KEYWORDS:
goiter – hypothyroidism – hyperthyroidism – age – senior
Autoři: Z. Límanová
Vyšlo v časopise: Geriatrie a Gerontologie 2016, 5, č. 1: 28-33
Kategorie: Přehledové články
Souhrn
Výskyt poruch funkce štítné žlázy je častější u žen než u mužů (nejméně 8 : 1), zatímco hyperfunkce je obvykle provázena obtěžujícími příznaky, snížená funkce probíhá mnohdy nepozorovaně, zvláště u starších osob. Podle recentních epidemiologických studií dosahuje prevalence nediagnostikovaných dysfunkcí 6–7 %. Struma bývala dříve především důsledkem nedostatku jodu. V ČR byl deficit jodu eradikován po roce 1950, takže strumu nacházíme již jen u starší populace. Hyperfunkce štítné žlázy u seniorů bývá spíše důsledkem nodózní přestavby ve štítné žlázy nebo toxického adenomu než GB toxikózy. Léčba těchto stavů je nutná, negativní dopady na srdce a skelet jsou známé, dobré zkušenosti s léčbou radiojodem tuto metodu předurčují k využití zvláště u starší populace. Osoby s hypotyreózou musí být léčeny a postup se neliší od osob mladých, je však nutné zahájit minimální dávkou levothyroxinu a zvyšovat zvolna, u velmi starých seniorů je mnohdy při kontrole přesného dávkování i aplikace léku nutná spolupráce s rodinou. Výskyt karcinomu štítné žlázy stoupá, operace je možná i u seniorů, vždy však na specializovaném chirurgickém pracovišti
KLÍČOVÁ SLOVA:
struma – hypotyreóza – hypertyreóza – věk – seniorÚvod
Tyreopatie patří mezi nemoci masového výskytu a neléčené mají významné zdravotní dopady(1, 2). Nesprávně indikovaná či nesprávně vedená léčba nebo časté odkládání řešení choroby má pro pacienty jednoznačně negativní důsledky. Ty se mohou projevit i za několik let, tedy ve stáří, mnohdy už u polymorbidního pacienta. Proto je určení etiologie choroby, přesná diagnostika a včasný léčebný postup pro terapeutický úspěch zcela zásadní(3). U některých stavů je indikována tzv. expektace nebo terapeutický pokus – ale vždy s vědomím odpovědnosti lékaře za odklad případného radikálního řešení, např. u Gravesovy-Basedowovy choroby (GB) a nodózní strumy (NS). Vznik a rozvoj tyreoidálních onemocnění je ovlivněn vlivy zevního prostředí, vlivy imunologickými a neméně i genetikou. Prevalence chorob je do určité míry závislá na geografických podmínkách, tj. především na dostupnosti jodu (i selenu), dále na pohlaví a na věku. Prevalence hypotyreózy se v ČR udává 3–5 %, hypertyreózy 0,2–1 % a tyreoidálních uzlů až 30–40 % i více u žen nad 50 let. Prosté zvětšení štítné žlázy (struma) v České republice nacházíme spíše u osob narozených před zahájením jodace jedlé soli, což bylo v roce 1950. Výskyt tyreopatií je častější u žen než u mužů (6–8 : 1) a stoupá s věkem, např. u žen nad 70 let dosahuje až 10–15 %. Porucha funkce štítné žlázy (ŠŽ) je plně rozvinutá, je-li laboratorní odezva jak v tyreoidálním stimulačním hormonu (TSH), tak v periferním hormonu – tyroxinu (T4), a subklinická (latentní, event. chemická), je-li změna jen v TSH a T4 je v normě. V současné době je v našich geografických podmínkách nejčastější příčinou tyreoidální poruchy autoimunita. Na základě epidemiologických studií se odhaduje, že asi 11 % Evropanů má funkční poruchu ŠŽ, ale jen asi 50 % o této skutečnosti ví(4). Na základě meta-analýzy různých epidemiologických studií z Evropy autoři určili prevalenci nediagnostikovaných dysfunkcí ŠŽ 6,7 % (hypotyreóza 4,94 % a hyperfunkce 72 %), prevalenci již diagnostikovaných dysfunkcí 3,82 % (hypotyreóza) a 0,75 % (hyperfunkce). Roční incidence dysfunkcí je v průměru 259/100 000, tj. hypotyreózy 226/100 000 a hyperfunkce 51/100 000.
Pravděpodobnost tyreoidálního postižení je zvýšená u osob s výskytem tyreopatií a autoimunitních chorob v rodinné a osobní anamnéze, proto anamnéze věnujeme zvýšenou pozornost. Typ tyreopatie v rodině nebývá totožný, u někoho se vyskytne tyreotoxikóza GB typu, u dalšího hypotyreóza. Onemocnění štítné žlázy (ŠŽ) nemusí být provázeno jejím zvětšením, zvláště u starších osob s hypotyreózou není ŠŽ hmatná a na ultrazvuku (UZ) je mnohdy patrné zmenšení až atrofie. Důležitá je informace o podávání vybraných léků: nadbytek jodu nebo jeho dlouhodobý deficit nacházíme především u veganů, vliv mají dále amiodaron (Cordarone), cytokiny, lithium, prodělané ozáření krku či okolí. S prostou strumou se setkáme spíše u osob narozených před rokem 1950, tedy v době nedostatečného jodového zásobení.
Laboratorní diagnostika
Ukazatelem funkce ŠŽ je TSH, který citlivě zpětnovazebně reaguje na změny periferních hormonů. ŠŽ produkuje tyroxin (T4) a v malém množství trijodtyronin (T3). Je-li původcem onemocnění ŠŽ autoimunita, nacházíme přibližně u 90 % osob pozitivní protilátky proti tyreoidální peroxidáze (TPOab) či tyreoglobulinu (Tgab), Tgab jsou však ovlivněny i dalšími faktory. Protilátky proti TSH receptoru (rTSH neboli TRAK) využíváme v diferenciální diagnóze tyreotoxikózy, endokrinní oftalmopatie a některých imunogenních hypotyreóz. TSH v séru je tedy základním laboratorním testem. Periferní zásobení dokládá hladina T4, v krvi je vázán na bílkovinné nosiče, a jeho hladina je ovlivněna některými faktory (estrogeny, léky, chorobami), proto raději volíme jeho volnou frakci, tj. free T4 (FT4). T4 je prohormonem, především jeho dejodací vzniká T3. Při hypotyreóze, tj. nedostatečné produkci T4, se uplatňují dejodázy, které zvyšují hladinu T3 a tak zajišťují „nouzové“ fungování organismu. Naopak při energetické karenci, při stresu nebo vlivu určitých látek je hladina T3 vlivem dejodáz snížená, stav je označován jako syndrom nízkého T3 (low T3 syndrom, nonthyroidal illness syndrome – NTI) a není důsledkem tyreoidálního onemocnění.
Zobrazovací metody
Do zobrazovacích metod řadíme ultrazvuk (UZ) ŠŽ, který je dnes metodou první volby a v rukou zkušeného odborníka poskytne maximum informací o uložení, velikosti, ohraničení ŠŽ i uzlů, echogenitě, struktuře a charakteru případných změn, prokrvení o přítomnosti uzlin a jejich charakteru. Scintigrafie technecistanem je dnes indikována jen při odlišení autonomního adenomu od hyperfunkční polynodózní přestavby/strumy, zcela výjimečnou indikací je subakutní tyreoiditida, pokud UZ, klinický průběh a laboratorní výsledky nejsou dostatečné. Speciální indikací v onkologii štítné žlázy je scintigrafie s využitím značeného jodu při zjišťování pooperačních zbytků a metastáz. Tenkojehlová aspirační biopsie (fine needle aspiration biopsy, FNAB) k cytologickému hodnocení je indikována u nejasných uzlů ve ŠŽ, při růstu laloků, k upřesnění diagnózy při chronické lymfocytární tyreoiditidě (CLT). Kontraindikace FNAB jsou minimální, antikoagulační léčbu je však vhodné krátkodobě přerušit. Vyšetření CT je indikováno při retrosternálním zasahování strumy, ale podle možností bez rtg kontrastu. Při vyšetření PET z jiné indikace se často (náhodně) zobrazí aktivní ŠŽ, vychytávání je zvýšené u chronického zánětu, u některých adenomů a karcinomů a samozřejmě u metastáz do ŠŽ. Do základní výbavy vyšetření ŠŽ PET však nepatří.
Další diagnostická rozvaha
Volba laboratorních parametrů závisí na otázce, kterou si klademe, a na některých okolnostech:
- Pokud vyšetřujeme v rámci screeningu (vyjma ženy těhotné či plánující graviditu) a klinická symptomatologie chybí, postačí vyšetření TSH. Je-li výsledek normální, je aktuální funkce ŠŽ v normě, další vyšetření není potřeba. U hospitalizovaných pacientů, zvláště krátce po přijetí, je odchylka TSH netyreoidálního původu častá – především suprese TSH – až u 30 % vyšetřených. Suprese TSH může vyvolat diferenciálnědiagnostické rozpaky při syndromu nízkého T3 (low T3, NTI – nonthyroidal illness). Jde o komplexní situaci, obvykle vyvolanou energetickou karencí organismu, operací či jinou zátěží, sepsí, při těchto stavech se preferenčně dejoduje T4 na metabolicky neúčinný reverzní T3 (rT3), a tím je pacient chráněn před metabolickými účinky T4 a T3. Součástí syndromu nízkého T3 jsou vlivy řady cytokinů, např. TNF, které působí centrálně na hypotalamus a hypofýzu. Po odeznění choroby se laboratorní nálezy normalizují. Období rekonvalescence může být provázeno mírnou elevací TSH netyreoidálního původu. Optimálním postupem při chybění symptomatologie je jak u nejasné suprese TSH, tak mírné TSH elevace opakování odběru za 2–6 týdnů v době stabilizace zdravotního stavu, po uplynutí té doby jsou kontrolní vyšetření až u 25 % případů zcela normální. Vzhledem k tomu, že diagnóza tyreoidální funkční poruchy bývá celoživotní, je nezbytné se vždy opřít i u seniorů o jasný a jednoznačný laboratorní nález. Řešení hraničních odchylek TSH nebývá urgentní a u hospitalizovaných pacientů je většinou možné delegovat rozhodnutí na ambulantního lékaře, který nález ověří v odstupu času.
- Pokud je u vyšetřovaného patrná symptomatologie, je vhodné současně s TSH vyšetřit hladinu FT4 i TPOab a Tgab.
- Diagnóza hypotyreózy se opírá o zvýšenou hodnotu TSH nad 10–11 mIU/l a snížení FT4. Pro diagnózu subklinické hypotyreózy svědčí TSH zvýšený méně než 10–11 mIU/l, hladina T4 je v normě nebo na dolní hranici normy. Pozitivita TPOAb/Tgab svědčí pro imunogenní původ.
- Výjimkou diagnostického postupu je gravidita, kromě TSH je nutné vyšetřit ihned i TPOab a eventuálně FT4.
- Diagnóza hyperfunkce se opírá o TSH snížený a FT4 zvýšený. S normálním FT4 a sníženým TSH se můžeme setkat u subklinické hyperfunkce, obvykle na podkladě uzlové přestavby ŠŽ, dále u léčené tyreotoxikozy již při dosažení eufunkce (suprese TSH přetrvává déle) nebo při nadbytečné léčbě tyreoidálními hormony.
Choroby štítné žlázy
Struma
U starší populace se ještě setkáme se zvětšenou ŠŽ, zasahující někdy retrosternálně. V diferenciální diagnostice strumy je důležitá informace o trvání zvětšené ŠŽ. Jde-li o záležitost dávnou, často od mládí, půjde patrně o strumu tzv. prostou, s koloidními a cystickými přestavbami. Při palpaci nacházíme jeden nebo oba laloky zvětšené, tužší, hladké, mohou být zčásti retrosternálně zanořené a vysunují se při polykání, uzliny nejsou zvětšené. Vyšetření UZ potvrdí zvětšení, obvykle přiměřenou echogenitu s anechogenními okrsky, ty odpovídají cystickým změnám, uzliny nejsou zvětšené. Dříve se měřil objem krku a posuzoval se případný růst, dnes je moderní hodnotit nález podle UZ, nicméně u starých osob je i opakované měření obvodu krku využitelným ukazatelem. Při růstu ŠŽ nebo uzlu může pacient vnímat tlak či bolest, obtíže mohou být důsledkem krvácení do uzlu nebo zvětšení některé cysty, pro karcinom ŠŽ nebo transformaci adenomu v karcinom svědčí růst, přítomnost zvětšených uzlin a změny na UZ. Pokud pacient prodělal léčbu malignity (karcinom prsu, plic, ledvin), je nutné uvažovat i o metastázách do ŠŽ.
Struma na podkladě autoimunitního zánětu (chronická lymfocytární tyreoiditida, chronická autoimunitní tyreoiditida, CLT) je nejčastějším tyreoidálním onemocněním, je obvykle provázena již sníženou činností a pozitivním titrem protilátek. Je známá pod názvem Hashimotovo onemocnění (tyreoiditida – HT). Chronický zánět ŠŽ s infiltrací buněk lymfocytární řady a produkcí různých cytokinů vyvolá růst ŠŽ a vznik strumy. Pokud není klinická diagnóza jasná, lze doplnit FNAB. Vzácně se ve ŠŽ vyskytuje lymfom, obvykle v terénu CLT, ten se projeví rychlým růstem ŠŽ. Retrosternální struma se může manifestovat útlakem dechových cest až stridorem, dnes již nálezem výjimečným. Náhodným asymptomatickým nálezem bývá retrosternální struma na rtg S + P, nicméně dořešení nálezu je nutné. Vyšetření CT, raději bez rtg kontrastu, pomáhá při indikaci a určení rozsahu operačního řešení.
Léčba strumy se odvíjí od příčiny: dostatečný příjem jodu je pro funkci ŠŽ zásadní, přijímáme ho především z jodizované soli a z mořských produktů. Vzhledem k doporučenému omezení příjmu soli z nynějších asi 15 g na 5 g die a na druhé straně v České republice malé oblibě a spotřebě mořských produktů je vhodné i u starší populace o příjem jodu cíleně pečovat, nezapomeňme na oblíbené sardinky a pomazánky z nich. Struma vzniklá jako důsledek hypotyreózy je výborně léčitelná substitucí. Struma při HT je jednoznačnou indikací ke konzervativní léčbě – podávání T4 s cílem normalizovat TSH a upravit obtíže, provázející hypotyreózu (viz hypotyreóza). Je-li diagnóza a léčba správná, struma rychle reaguje, v průběhu měsíců se zmenšuje a po řadě let většinou ŠŽ atrofuje. Operaci HT se strumou indikujeme jen při nedostatečné reakci na léčbu, při nejasném nálezu palpačním, na UZ či při FNAB. Je zapotřebí si uvědomit, že papilární karcinom i lymfom vznikají právě v terénu HT, a to spíše nedostatečně léčeném.
V mladším věku, pokud má struma benigní charakter, je možné podávat tzv. supresivní léčbu, tj. podáváním tyroxinu snížit hladinu TSH. Tato léčba má být aplikována jen omezenou dobu a dnes ustupuje i u mladších osob do pozadí. U starší populace je vysloveně nevhodná pro možné negativní dopady na skelet a srdce. Velká struma, nejasný nález či obavy z malignizace jsou vždy indikací k operačnímu řešení, jde-li o benigní etiologii, zvláště u seniorů je možná zmenšovací léčba radiojodem.
Hypertyreóza
Zvýšená funkce ŠŽ se vyskytuje u 1 % populace. Příčina bývá autoimunitní (GB choroba) nebo autonomie buněk ŠŽ při nodózní strumě nebo autonomním (toxickém) adenomu. Vzácně hyperfunkci může vyvolat úvodní fáze de Quervainovy tyreoiditidy, úvodní fáze HT, u starších osob se při substituční léčbě setkáváme s předávkováním hormony – tzv. thyrotoxicosis factitia. GB choroba je u starší populace méně častá, spíše se setkáme s relapsem choroby. Případná průvodní endokrinní oftalmopatie může velmi komplikovat léčbu zvláště u polymorbidních osob. Nezbytné podávání kortikoidů u těchto nemocných, často již s poruchou glukózové tolerance bývá svízelné. GB choroba je zpravidla provázena pozitivitou TRAK (rTSH), nacházíme zvýšenou perfuzi na UZ ŠŽ, obvykle i sníženou echogenitu. Pro starší věk je však typická hyperfunkce v důsledku autonomie tyreoidálních uzlů nebo toxický adenom (negativní TRAK, nález uzlů na ultrazvuku, nález zvýšené akumulace v některých uzlech na scintigrafii ŠŽ). Příčina vzniku či relapsu GB choroby nebo rozvoje hyperfunkce u NS ve starší populaci může být iatrogenní – podání cytokinu (onkologická léčba, zvláště léčba melanomu, léčba RS), velká nálož jodu v rtg kontrastu, u kardiaků podání Cordaronu.
Léčebný postup u hyperfunkce ŠŽ je vždy dvoufázový: zklidnění podáním tyreostatik a rozhodnutí o dalším postupu. V úvahu přichází operace, radiojod nebo spíše ojediněle ponechání dlouhodobé minimální léčby tyreostatiky. Operace – totální tyreoidektomie má na specializovaných pracovištích minimální rizika (porucha zvratného nervu, hypoparatyreóza, krvácení). Definitivní řešení je prevencí relapsů, negativních dopadů nedoléčených stavů (srdce, skelet) i vzniku karcinomu při dlouhodobém podávání tyreostatik. Odklad rozhodnutí do seniorského věku, často u polymorbidních osob, není racionální. Omluvou může být skutečnost, že u části pacientů s GB chorobou může hyperfunkce spontánně přejít do hypotyreózy. U starších a často polymorbidních jedinců je ideálním řešením radiojod, léčba je bez rizika, efekt nastupuje za 3–6 měsíců. Jak po léčbě radiojodem, tak po operaci je nutné počítat se substituční léčbou a dlouhodobým sledováním.
Kazuistika 1
Pacientka, 55letá lékařka (narozená 1943), vnímala dysrytmie, současně v té době měla retrobulbární tlak, slzení očí, byla vyšetřena a stanovena diagnóza tyreotoxikózy GB typu, ověřena zvýšenou hladinou FT4 a supresí TSH, vyššími hodnotami TRAK. Léčba tyreostatiky pod kontrolou endokrinologa měla dobrý efekt, stav se i po kardiální stránce zklidnil a po 2 letech bylo možné léčbu ukončit. Pacientka přestala na endokrinologii docházet, kontroly TSH prováděla sama, byla bez obtíží, další relaps tyreotoxikózy se objevil v jejích 68 letech, ten léčila sama, ponechala si minimální dávku Thyrozolu 2,5 mg denně a pro dobrý stav sama léčbu ukončila v 70 letech. Po ukončení léčby za 3 měsíce se objevily dysrytmie a dušnost, pro fibrilaci síní byla akutně přijata na interní oddělení, kde jí byl ihned podán Cordarone. Odběr krve potvrdil relaps tyreotoxikózy (TSH pod 0,01 mIU/l a FT4 33 pmol/l). K endokrinologovi se dostavila až za další 3 týdny, k léčbě imunogenní hyperfunkce (TRAK 14,2IiU/l, n do 1,5). K Thyrozolu jsme přidali Prednison, neboť se jednalo o tyreotoxikózu akcentovanou Cordaronem, šlo o tzv. 2. typ cordaronové tyreotoxikózy. Léčba Cordaronem byla s ohledem na zlepšení a přání kardiologů zatím ponechána.
Poselství: Kontrola endokrinologem u osob léčených tyreostatiky je nezbytná, případné ukončení léčby musí být konzultováno s endokrinologem, relapsy jsou časté, pacient má být dlouhodobě po ukončení léčby sledován. Při kardiálních obtížích u osob s anamnézou tyreotoxikózy musí být nejdříve vyloučen (a zaléčen) relaps. Cordarone je u tyreotoxikózy kontraindikován. U pacientky měla být zavčas indikována definitivní léčba tyreotoxikózy, ve starším věku nejspíše radiojod.
Hypotyreóza
Hypotyreóza je onemocněním celoživotním a v dnešní době relativně častým – při cíleném vyšetření starších žen ji lze odhalit u 8–14 %, pokud počítáme i subklinické formy. U další části populace s přítomností CLT se hypotyreóza může v průběhu let rozvinout. Nejčastější příčinou hypotyreózy je CLT, v 80–90 % případů je doprovázena pozitivitou TPOAb a/nebo ultrazvukem štítné žlázy. Velmi často je pozitivní rodinná anamnéza. CLT je řazena mezi orgánově specifické autoimunity a bývá zpravidla i součástí jiných autoimunitních onemocnění a syndromů(5, 6). Osoby se zvýšeným rizikem rozvoje poruchy funkce ŠŽ jsou uvedeny v tabulce 1. Akceleraci poruchy funkce vyvolávají některé léky(7, 8) (tab. 2).Další příčiny jsou rovněž iatrogenní – operace, podání radiojodu, následky po zevním ozáření okolí ŠŽ (léčba m. Hodgkin, záření pro karcinom mammy). Mimo předávkování při podávání tyreostatik může vzniknout hypotyreóza při vysokém příjmu určité stravy (zelí, sója), při výrazném nedostatku jodu, v graviditě u žen s CLT, do té doby eufunkčních.
Tab. 1. Osoby se zvýšeným rizikem rozvoje poruchy funkce štítné žlázy 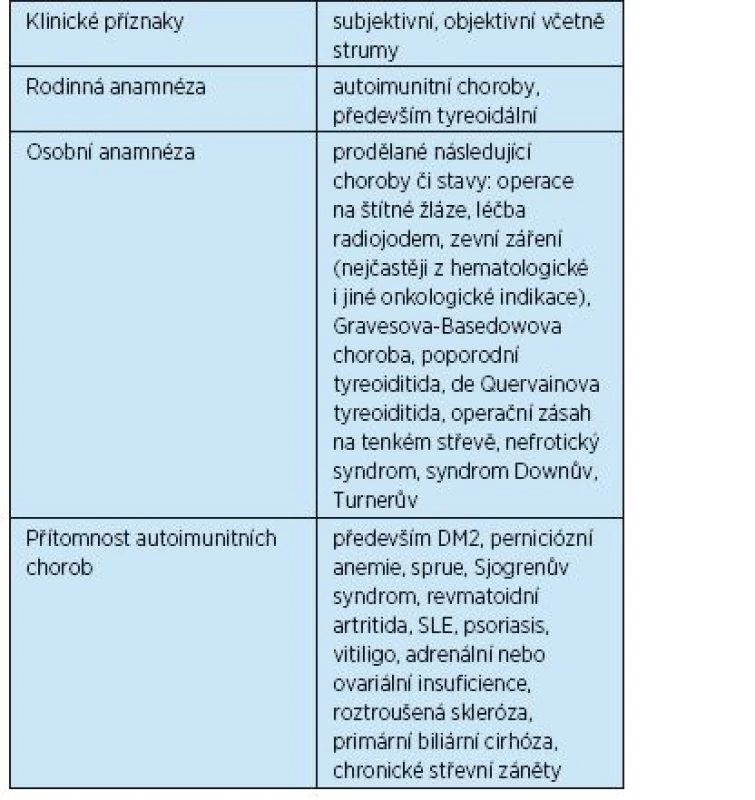
Tab. 2. Některé léky, které mohou způsobovat tyreoidální poruchu 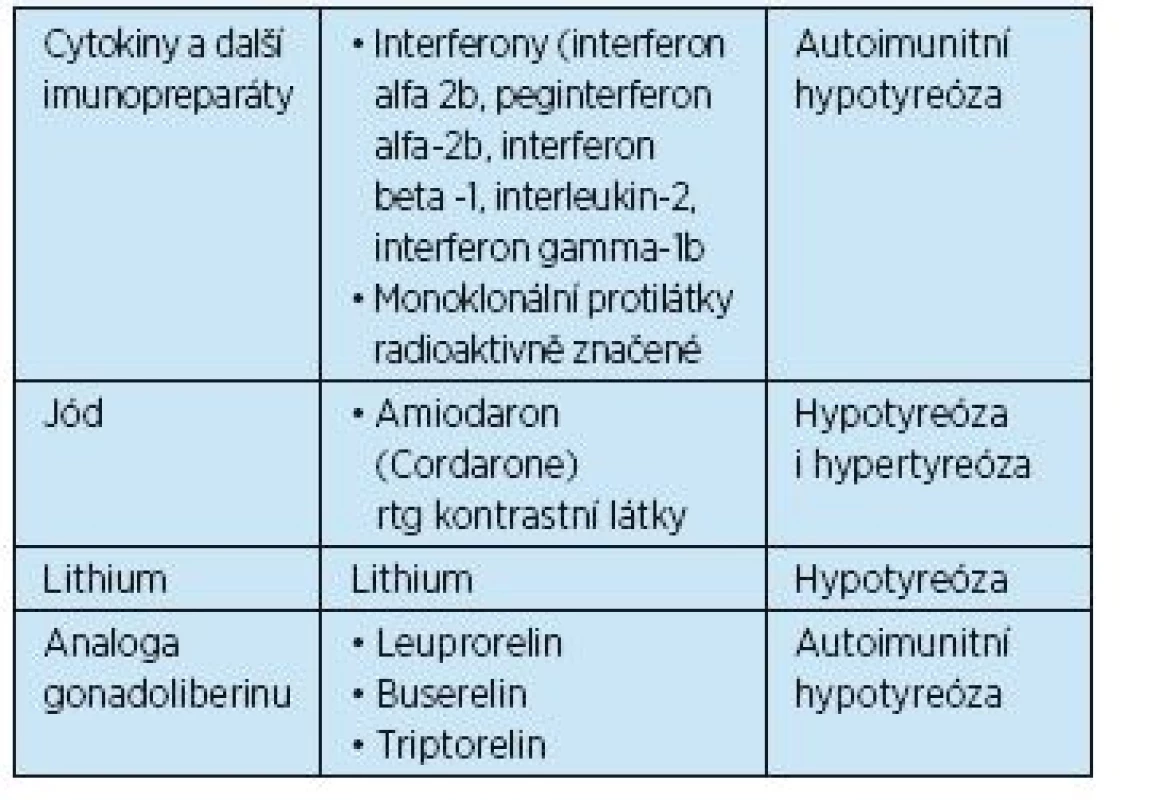
Výskyt CLT se v jednotlivých oblastech světa liší tak, jak se liší podíl rizikových faktorů. Onemocnění se vyskytuje u žen podstatně častěji než u mužů, může probíhat benigně a po léta může být ŠŽ plně funkční. Výskyt subklinické formy je obvykle náhodným nálezem při celkovém vyšetření nebo při screeningu, přechod do plné hypotyreózy je uváděn asi u 10 % ročně, někdy pozvolna, jindy během několika měsíců. Se spontánním přechodem SH do plné hypotyreózy však musíme u pacienta s CLT vždy počítat, proto je nutné osoby se SH pravidelně sledovat a kontrolovat TSH alespoň 1x ročně. Záludnost hypotyreózy je u starší populace v její „asymptomatičnosti“, tj. v pozvolném vývoji a záměně některých příznaků za důsledky stárnutí, i skutečnost, že dnes není hypotyreóza většinou provázena strumou. Příznaky jsou převážně nespecifické: únava, sklon k depresím, zapomnětlivost, prosáknutí obličeje nebo jen víček, hypomimie, hrubší hlas, parestezie v prekordiu, bolesti svalů či kloubů, neobratnost rukou či parestezie prstů, syndrom karpálního tunelu, vypadávání ochlupení, zhoršení kvality vlasů. Další symptomy jsou typické i pro stárnutí, např. hypoakuzie, zimomřivost, obstipace či celkové zpomalení. Překvapivě část osob výraznější obtíže nemá ani při cíleném dotazu. Dopady na laboratorní testy u déletrvající hypotyreózy jsou následující: hypertenze a větší systolicko-diastolický rozdíl, změny lipidového spektra, anemie, vyšší CK, mírná elevace jaterních enzymů, bradykardie, nízká voltáž na EKG, perikardiální výpotek. V současné době bývají nezřídka překryty medikací – proto před léčbou dyslipidemie či při hledání příčin patologických laboratorních testů (anemie, mírná elevace jaterních enzymů) je přínosné vyšetřit TSH.
Kazuistika 2
Pětašedesátiletá pacientka se dostavila k vyšetření pro zvýšenou únavu, sklon k depresím. Pro vyšší hladinu cholesterolu byla před několika měsíci zahájena léčba hypolipidemikem. ŠŽ nebyla zvětšená, hladina TSH byla 30,5 mIU/l, FT4 7,3 pmol/l, TPOab byly pozitivní. V anamnéze uvedla léčbu GB toxikózy po porodu ve 25 letech, léčba byla po 2 letech léčby ukončena, na kontroly dále nedocházela, cítila se zdráva.
Poselství: GB toxikóza spontánně v průběhu let přešla do hypotyreózy. Onemocnění ŠŽ je celoživotní, jedinci, kteří prodělali léčbu hyperfunkce, mají být pravidelně dispenzarizováni a kontrola TSH podle stavu po 6–12 měsících. Před nasazením hypolipidemik má být vyloučena sekundární příčina, v našem případě hypotyreóza.
Léčba hypotyreózy i u starší populace je snadná a radostná, pokud má lékař trpělivost a jemnou ruku(9, 10). U starší polymorbidní osoby s rozvinutou hypotyreózou a přítomností ICHS se léčby nemusíme obávat, je však nutné postupovat zvolna a citlivě. Podáváme tyroxin zpočátku v minimální dávce 25–50 µg denně a zvyšujeme po 4–6 týdnech, sledujeme klinický nález a TSH. Dodržení zásady požít tyroxin nalačno, zapít čistou vodou, 20–30 minut nic dalšího do žaludku (tedy rozhodně neužívat současně jiné léky!) je imperativem, který se však někdy u seniorů nedodržuje a nedodržuje se pro neinformovanost personálu ani v nemocnicích. Problémem je např. podávání blokátorů protonové pumpy, které rovněž mají být nalačno. Zhoršené vstřebávání levothyroxinu je běžné u pacientů s atrofickou gastritidou, u neléčené celiakie a při podávání určitých léků(7, 8, 11–13). U těchto nemocných se laboratorní hodnoty nezlepšují nebo kolísají. Obvyklá plná substituční dávka levothyroxinu je 1,5–1,7 µg/kg váhy, v seniorském věku spíše méně, ale jsou velké individuální rozdíly. Dávka se poněkud mění i při výraznější změně hmotnosti. Po dosažení normalizace TSH a při dobré spolupráci pacienta, případně rodiny u senilních osob, bývá dávka stabilní a kontroly postačí za 6–12 měsíců. Kontroly TSH také upozorní na případné předávkování.
Subklinické stavy
Tyto stavy vyžadují zvláštní přístup(14–22). Pokud je nálezem opakovaná suprese TSH a periferní hormon (FT4, event. FT3) je v normě a lze-li vyloučit vliv léků (dopamin, vysoké dávky kortikoidů), jde pravděpodobně o subklinickou hyperfunkci. S ohledem na negativní dopad na skelet (osteoporóza) a srdce (dysrytmie) je všeobecně akceptována nutnost léčby hyperfunkce. Obvykle je chorobu nutné zklidnit tyreostatiky, u starší populace je ideálním řešením podání radiojodu, s následnou hypotyreózou je nutné počítat. Ta je však lépe léčitelná než hyperfunkce.
Při laboratorním nálezu TSH do 10 mIU/l (podle některých až 15–20 mIU/l) a FT4 v normálním pásmu není substituční léčba u starších osob imperativem(14). Je však nutné zvážit řadu okolností: subjektivní obtíže, objektivní nález, přítomnost strumy, nález ŠŽ na UZ (přítomnost uzlů!), EKG, UZ nález srdce, laboratorní odchylky. Podle výsledků zvažujeme léčbu nebo expektaci. Uvádí se, že u osob nad 85 let spíše substituci nezahajujeme. S ohledem na podobnost některých obtíží při hypotyreóze, stárnutí a svalovém úbytku byly uskutečněny studie hledající vztah sarkopenie a tyreoidálního stavu u osob starších 65 let. Úvaha o možné souvislosti tzv. frailty syndrome se subklinickými tyreopatiemi se ale neprokázala(23).
Karcinom štítné žlázy
Karcinom je sice vzácný, v ČR se diagnostikuje asi 1000 případů ročně, avšak jeho záchyt stoupá, zatímco mortalita se nezvyšuje. O rozvoji karcinomu ŠŽ v terénu CLT se léta diskutuje, recentní výzkumy se ke vztahu obou onemocnění přiklánějí(24, 25). Stoupá i záchyt mikrokarcinomů. Přístup k léčbě karcinomu ŠŽ v českých podmínkách byl přehledně zpracován v roce 2015(26, 27). Karcinom ŠŽ je většinou pomalu rostoucím tumorem, vyskytuje se však ve všech věkových skupinách. Je-li nález indikací k operaci, není věk kontraindikací k operaci na specializovaném pracovišti. Následná léčba radiojodem je dobře tolerována a supresní léčba je překvapivě dobře snášena i u starších nemocných. Nutnost vyšších – suprafyziologických – dávek tyroxinu je zapotřebí podávat alespoň první rok, případně podle nálezu i déle. Narůstá počet osob léčených pro karcinom ŠŽ a tyto osoby jsou ohroženy druhou malignitou – u žen především karcinom prsu (kumulativní riziko 26 % za 25 let). Recentní studie dokazují, že riziko vzniku karcinomu prsu je vyšší u žen, u kterých byla diagnostikována rakovina ŠŽ(28, 29). Souvislost s léčbou radiojodem v souboru více než 17 000 žen s karcinomem ŠŽ prokázána nebyla. Je však vhodné připomenout studie zabývající se vztahem ŠŽ a prsu dokazující, že ženy s karcinomem prsu mají častěji (subklinickou) hypotyreózu imunogenního původu(30). Potvrzení vztahů ŠŽ a karcinomu prsu bude však vyžadovat další studie. Společným jmenovatelem je patrně jod a natrium-jodidový symporter.
Závěr
Onemocnění štítné žlázy je v populaci časté, ve stáří převažuje hypotyreóza. S ohledem na nespecifické příznaky, často běžné u seniorů (únava, zimomřivost, zapomínání, celková zpomalenost, parestezie prstů, syndrom karpálního tunelu, prosáknutí rukou a v obličeji), je vhodné vyšetřovat TSH nejen u osob s pozitivní rodinnou či osobní anamnézou, ale raději i v rámci preventivních prohlídek. Nález mírné elevace nebo suprese TSH máme ověřit po 6–8 týdnech. Rozhodnutí o léčbě subklinických stavů vyžaduje komplexní posouzení včetně posouzení přínosu a negativ. Léčba nemusí být vždy zahájena, ale pacient musí být sledován, protože progrese do plné funkční poruchy je ročně asi u 10 %. Je-li u seniora indikace k operaci ŠŽ, má být odeslán na specializované pracoviště, pacienti operovaní po 80. roce věku nejsou dnes výjimkou. U osob substituovaných je nezbytné opakovaně připomínat způsob aplikace tablet s levothyroxinem (nalačno, odděleně od ostatní léčby, zapít čistou vodou, 20–30 minut nic nejíst), u velmi starých seniorů je nutné informovat rodinu a léčbu častěji kontrolovat.
Autorka prohlašuje, že v souvislosti s publikací článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny farmaceutickou firmou.
doc. MUDr. Zdeňka Límanová, CSc.
III. interní klinika 1. LF UK a VFN Praha
doc. MUDr. Zdeňka Límanová, CSc.
e-mail: liman@vfn.cz
Po praxi na interním oddělení v Sušici a Kladně nastoupila na III. interní kliniku v Praze, vedenou profesorem Charvátem. Zaměřila se v rámci endokrinologie na tyreoidologii. Zaváděla nové diagnostické laboratorní metody, uváděla cytologii štítné žlázy do praxe, v posledních letech se soustředila na zpřesnění screeningových metod k časnému odhalení onemocnění štítné žlázy v těhotenství. Podporuje širokou mezioborovou zdravotnickou spolupráci, která optimalizuje kvalitní péči o nemocné s tyreopatiemi.
Zdroje
1. Klener P, a kol. Vnitřní lékařství, 2011. Praha: Galén. 939–953.
2. Zamrazil V. Kontroverzní otázky diagnostiky a léčby tyreopatií. Lékařské listy 2005; 49(9): 12 : 7–9.
3. Jiskra J. Management of hypothyroidism and hyperthyroidism. Vnitr Lek 2015; 61(10): 868–871.
4. Garmendia MA, Santos-Palacios S, et al. The incidence and prevalence of thyroid dysfunction in Europe: a metaanalysis. J Clin Endocrinol Metab 2014; 99(3): 923–931.
5. Límanová Z. Šedá eminence v medicině – štítná žláza. Čas Lek Čes 2009; 148 : 124–128.
6. Vondra K, Zamrazil V. Autoimmune polyendocrine syndrome. Vnitr Lek 2010; 56(11): 1111–1113.
7. Barbesino G. Drugs affecting thyroid function. Thyroid 2010; 20 : 763–770
8. Tajtáková M: Lieky a štitna žlaza. Vnitř Lék 2012; 58(2): 140–141.
9. Roberts CGP, Ladenson PW. Hypothyroidism. Lancet 2004; 6 : 793–803.
10. Chakera AJ, Pearce HS, Vaidya B. Treatment for primary hypo-tyroidism: current approach. Drug Des Devel Ther 2012; 6 : 1–11.
11. Burman KD. Factors affecting thyroid hormone gastrointestinal absorption. Thyroid International 2000; 5 : 3–11.
12. Jiskra J, Límanová Z, Vaníčková Z, et al. IgA and IgC antigliadin, IgA anti-tissue trans glutaminase and antiendomysial antibodies in patients with autoimmune thyroid disease and their relationship to thyroidal replacement therapy. Physiol Res 2003; 52(1): 79–88.
13. Centanni M, Gargano L, Cannetieri G, et al. Thyroxine in goiter, Helicobacter pylori infection and chronic gastritis. N Engl J Med 2006; 354 : 1787–1793.
14. Cappola A, Fried LP, Arnold LP, et al: Thyroid status, cardiovascular risk, and mortality in older adults. JAMA 2006; 289 : 1033–1041.
15. Cooper DS. Approach to the patient with subclinical hyperthyroidism. J Clin Endocrinol Metab 2007; 92 : 3–9.
16. Ochs N, Auer R, Bauer DC, et al. Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality. Ann Intern Med 2008; 148 : 832–845.
17. Razvi S, Shakoor A, Vanderpump M, et al. The influence of age on the relationship between subclinical hypothyroidism and hypothyroidism and ischemic heart disease: a metaanalysis. J Clin Endocrinol Metab 2008; 93 : 2998–3007.
18. Iacoviello M, Guida P, Guastamacchia E, et al. Prognostic role of sub-clinical hypothyroidism in chronic heart failure outpatients. Curr Pharm Des 2008; 14 : 2686–2692.
19. Goichot B, Sapin R, Schlienger JL. Subclinical hyperthyroidism: considerations in defining the lower limit of the thyrotropin reference interval. Clin Chem 2009; 55 : 420–424.
20.Vanderpump MP. How should we manage patients with mildly increased serum thyrotrophin concentrations? Clin Endocrinol (Oxf) 2009; Sep 24 [Epub ahead of print].
21. Virgini V, Collet TH, Christ E, et al. Should we treat subclinical hypothyroidism? Rev Med Suisse 2012; 8(331): 501–502, 504–565.
22. Biondi B. Heart failure and thyroid dysfunction. European J Endocrinol 2012; 167 : 609–618
23. Orgiazzi J, Virgini VS, Rodondi N, et al. Does subclinical thyroid dysfunction contribute to the frailty syndrome in men over 65 years of age? Clin Thyroidol 2015; 27 : 336–333.
24. Lee Ju-Han, Younghye Kim, Jung Woo Choi, et al. The association between papillary thyroid carcinoma and histologically proven Hashimoto‘s thyroiditis: a meta-analysis. Europ J of Endocrinol 2013; 168 : 343–349.
25. Jankovic B, Le KT, Hershman JM. Clinical review: Hashimoto‘s thyroiditis and papillary carcinoma: is there a correlation? J Clin Endocrinol metab 2013; 98(2): 474–482.
26. Machová M, Vlček P. Current trends to treatment and follow up of patients with differentiated thyroid carcinoma. Vnitř Lék 2013; 2 : 106–112.
27 Vlček P, Nováková D, Vejvalka J, et al. Draft of the best medical treatment in patiens with low risk thyroid cancer. Vnitř Lék 2015; 6(19): 769–777.
28. Din Cy, Lin CL, Huang WS, Kao CH. Risk of breast Cancer in patients with thyroid cancer receiving or not receiving I 131 treatment: a nationwide population based cohortt study. J Nucl med 2015. pil: jnumed 115.164830 (Epub ahead of print)
29. Pearce EN, Kuo JH, Chabot JA, et al. Thyroid cancer survivors are atincreased risk for breast cancer. Clin Thyroidol 2015; 27 : 329–331.
30. Limanová Z. Frequent incidence of thyropaties in women with breast cancer. Vnitr Lek 1998; 44(2): 76–82.
Štítky
Geriatria a gerontológia Praktické lekárstvo pre dospelých Protetika
Článek Editorial
Článok vyšiel v časopiseGeriatrie a Gerontologie
Najčítanejšie tento týždeň
2016 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
- Vareniklin jako pomocník v léčbě nikotinismu i u psychiatrických pacientů
-
Všetky články tohto čísla
- Krvácivé komplikace antikoagulační léčby u geriatrických pacientů
- Vliv reminiscenční terapie na depresivitu a kognitivní funkce u seniorů v dlouhodobé péči
- Hluboká žilní trombóza a její léčba v otázkách a odpovědích
- Onemocnění štítné žlázy se zaměřením na seniorský věk
- Editorial
- Role nutrice v prevenci kognitivních poruch ve vyšším věku
- Transmisivní spongiformní encefalopatie jako příčina demence způsobená priony
- Ageismus – hrozba sociální izolace ve stáří
- 21. gerontologický kongres v Hradci Králové
- Specializace v geriatrii a kompetence geriatra
- Role výživy u seniorů podstupujících rehabilitaci
- Stručně o lidských potřebách ve stáří
- Geriatrie a Gerontologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Hluboká žilní trombóza a její léčba v otázkách a odpovědích
- Onemocnění štítné žlázy se zaměřením na seniorský věk
- Transmisivní spongiformní encefalopatie jako příčina demence způsobená priony
- Specializace v geriatrii a kompetence geriatra
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



