-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Předoperační lokalizace nehmatných mamárních lézí
Pre-operative Localisation of Non-palpable Mammary Lesions
Summary:
Pre-operative Localisation of Non-palpable Mammary Lesions. Wide expansion of mammography, especially the introduction of screening mammography, has markedly increased the number of mammographically detected mammary gland lesions, the majority of them are not palpable. Only a small percentage of lesions can be identified as being unambiguously benign (pathognomic lesions) and therefore the majority of lesions require the use of other investigative modalities, including cytological and/or histological verification. An efficient technique in the group of these lesions is biopsy under mammographic/sonographic control. Pre-operative localisation techniques under MG/US control are necessary in non-palpable lesions, in mammography including the localisation of microcalcification clusters [1,2,4]. Specimen radiography is an integral part of localisation of non-palpable lesions and is a necessary part of the quality control of the entire diagnostic procedure [3,5,8,13].
We present the results of the analysis of 27 406 mammographic examinations performed in the period of September 2002 to September 6, 2005. Out of this total number, 57,29 % (15 701) screening mammographies were performed. In total, 414 mammary gland carcinomas were mammographically detected and subsequently histologically verified. 243 mammary gland carcinomas (58,7 %) in the screening group, 72 carcinomas (17,4 %) in the group under 45 years of age and 99 mammary gland carcinomas (23,9 %) in the group over 70 years of age were identified. Stereotactic mammographic localisation was performed in 57,5 % from the total number of malign mammographic findings.Keywords:
mammography – sonography - percutaneous diagnostic techniques - mammary gland carcinoma – biopsy – screening examination
Autoři: Z. Pačovský 1; K. Dvořák 2; E. Jandáková 3
Působiště autorů: chirurgické oddělení gynekologicko porodnické kliniky LF MU a FN Brno 1; mammodiagnostické oddělení gynekologicko porodnické kliniky LF MU a FN Brno 2; oddělení patologie gynekologicko porodnické kliniky LF MU a FN Brno 3
Vyšlo v časopise: Prakt Gyn 2005; 9(5): 24-28
Souhrn
Plošné rozšíření mamografie, zvláště zavedení screeningové mamografie, výrazně zvýšilo počet mamograficky detekovaných lézí mléčné žlázy, z nichž většina není hmatných. Pouze malé procento lézí může být označeno jako jednoznačně benigní (patognomické léze), a proto většina lézí tak vyžaduje užití dalších vyšetřovacích modalit, včetně cytologické a/nebo histologické verifikace. Výtěžnou technikou ve skupině těchto lézí je biopsie pod mamografickou/sonografickou kontrolou. Předoperační lokalizační techniky pod MG/UZ kontrolou jsou nezbytné u nehmatných lézí, u mamografie včetně lokalizace výsevu mikrokalcifikací [1,2,4]. Specimen radiografie je integrální součástí lokalizace nehmatných lézí a je nezbytnou součástí kontroly kvality celého diagnostického postupu [3,5,8,13].
Předkládáme výsledky analýzy 27 406 provedených mamografických vyšetření z období září 2002–září 2005. Z tohoto celkového počtu bylo provedeno 57,29 % (15 701) screeningových mamografií. Celkem bylo mamograficky detekováno a následně histologicky verifikováno 414 karcinomů mléčné žlázy. Ve screeningové skupině bylo prokázáno 243 karcinomů mléčné žlázy (58,7 %), ve skupině pod 45 let věku 72 karcinomů (17,4 %) a ve skupině nad 70 let věku ženy 99 karcinomů mléčné žlázy (23,9 %). Stereotaktická mamografická lokalizace byla provedena u 57,5 % z celkového počtu maligních mamografických nálezů.Klíčová slova:
mamografie – sonografie – perkutánní diagnostické techniky - karcinom mléčné žlázy – biopsie – screeningové vyšetřeníDiagnostická strategie a její cíle
A. Mamografie
Problematiku užití mamografie je možné rozdělit do základních 3 skupin:
- Pacientky 40leté - nižší incidence karcinomu mléčné žlázy, omezená senzitivita mamografie (vyšší denzita mléčné žlázy – nižší senzitivita i specificita mamografie, nutnost užití dalších zobrazovacích modalit), vyšší radiosenzitivita mléčné žlázy.
- Pacientky 40-50leté - screeningové vyšetření je stále předmětem diskusí, screeningová vyšetření však výrazně snižují mortalitu v této věkové skupině, vzhledem ke známému rychlejšímu růstu karcinomů v této skupině je doporučována roční screeningová kontrola.
- Pacientky 50leté: screeningová mamografie v této skupině je cenná (vysoká senzitivita i specificita mamografie), průkaz mikrokalcifikací i v terénu vysoce denzní mléčné žlázy, karcinomy bez obsahu mikrokalcifikací se často projeví distorzí/reakcí okolní tkáně, vhodná pravidelná klinická vyšetření.
B. Sonografie
Je cenná vyšetřovací modalita schopná detekce i drobných ložisek v terénu denzních mam (doplňovaná asi ve 15-20 %). Existuje však nižší specificita sonografie v terénu denzních mam, podobně jako u mamografie, zvláště u ložisek 5 mm.
C. Perkutánní diagnostické techniky
Je možno rozdělit do základních 5 skupin:
- diagnostická punkce cyst
- fine-needle (tenkojehlová) aspirační cytologie (FNA)
- core bioptické techniky
- preoperační lokalizační techniky
- vakuová biopsie.
I. Fine-needle aspirační cytologie (FNA) je často 1. krokem hodnocení mamograficky/sonograficky detekované suspektní léze. Znalost a zkušenost s FNA přináší validní diagnostické výsledky. Nejedná se přitom o samotnou aspiraci, ale o nátěr aspirátu na sklíčka a kvalitní cytologické vyšetření. Hodnocení aspirátu nezkušeným patologem výrazně zvyšuje počet nediagnostických nálezů o 30 % (Dronkers 2002). FNA je technikou zvyšující detekční potenciál mamografických nebo sonografických vyšetření v časném průkazu karcinomu mléčné žlázy. FNA s validním výsledkem (lege artis provedená) snižuje počet chirurgických intervencí. Falešná negativita FNA je nevyhnutelným faktem, se kterým je nutno počítat, a proto i negativní výsledek FNA zcela nevylučuje malignitu. Pacientkami je FNA snášena dobře, neexistují kontraindikace FNA. Nevýhodou FNA je, že nepřináší informace o možné invazivitě, stupni diferenciace a receptorovém statusu karcinomu. FNA je tedy bezpečnou, finančně i časově nenáročnou technikou dovolující i flowcytometrické vyšetření.
V případě průkazu solidní léze (non-cystické) je doporučován uvedený další postup:
- nehodnotitelný materiál – opakování FNA
- benigní nález – kontrola UZ/MG do 6 měsíců
- nejistý, atypický nález – core biopsie/excize
- maligní nález – core biopsie/excize.
Příčiny falešně negativního výsledku FNA mohou být:
- nezkušenost vyšetřujícího
- velikost a lokalizace ložiska malé, velké nebo hluboko uložené
- nekróza, hemoragie, cystické změny
- extenzivní dezmoplastická reakce
- specifické typy karcinomů sdružených s vyšším počtem falešně negativního výsledku FNA: lobulární, tubulární, dobře diferencovaný, intraduktální, papilární a mucinózní karcinom.
Léze spojené s falešně pozitivním/suspektním výsledkem FNA jsou:
- fibrózně cystická dysplazie: proliferativní/s atypiemi
- fibroadenomy
- tuková nekróza
- laktační změny mléčné žlázy
- papilomy
- radiální změny
- organizující se hematom
- gynekomastie.
II. Core bioptické techniky se dynamicky rozvíjejí v posledních desetiletích. Biopsií získaný cylindrický vzorek nepoškozené tkáně je vyšetřen histologicky. V současnosti jsou nejčastěji užívané automatické odběrové bioptické „pistole“ (vysokorychlostní) Bard, Manan, Biopty a ASAP. Při odběru je možná volba délky získaného vzorku od 22-23 mm, tuto délku je možno snížit na polovinu. Průměr 14-18 G je vyhovující. Je-li léze hmatná, užívá se free-hand technika. V případě verifikace nehmatné léze je nutný odběr pod sonografickou nebo stereotaktickou/mamografickou kontrolou.
Core biopsie dovoluje stanovení přesného histologického nálezu (počet odběrů, typ odběrové jehly) a na rozdíl od FNA potřebné informace o možné invazivitě, diferenciaci a receptorovém steroidním statusu. Většina takto verifikovaných lézí (benigních) tak nevyžaduje chirurgickou intervenci. V případě mamograficky a sonograficky nebo pouze sonograficky prokázané nehmatné léze je metodou volby cílený odběr pod sonografickou kontrolou.
Mezi výhody core biopsie pod sonografickou kontrolou patří:
- rychlost a jednoduchost
- real-time kontrola při umístění hrotu odběrové jehly a sledování průběhu odběru (při odběru lege artis je dobře patrný odběrový kanál)
- umožňuje různou polohu pacienta při odběru
- je využitelná a je metodou volby, je-li mamografický nález vágní
- má přednost před stereotaktickým odběrem při verifikaci velmi drobných lézí
- bezpečným průkazem kvalitního odběru je tzv. feet air (patrný odběrový kanál)
- nevýhodou je nemožnost spolehlivého odběru v případě verifikace výsevu mikrokalcifikací.
III. Stereotaktický odběr je možno provést na speciálním nebo mamografickém přístroji s možností stereotaxe (obr. 1). Moderní přístroje zaručují přesnost lokalizace, a tím odběru v toleranci ± 1 mm. Digitální stereotaktické jednotky výrazně snižují časovou náročnost výkonu.
Obr. 1. Schéma stereotaktického snímače. 1 rentgenka, 2 držák jehly, 3 kompresní plát, 4 mamma, 5 referenční bod, 6 jehla, 7 mammární léze, 8 film-foliový systém, I pozice rentgenky při první expozici, II pozice rentgenky při druhé expozici. 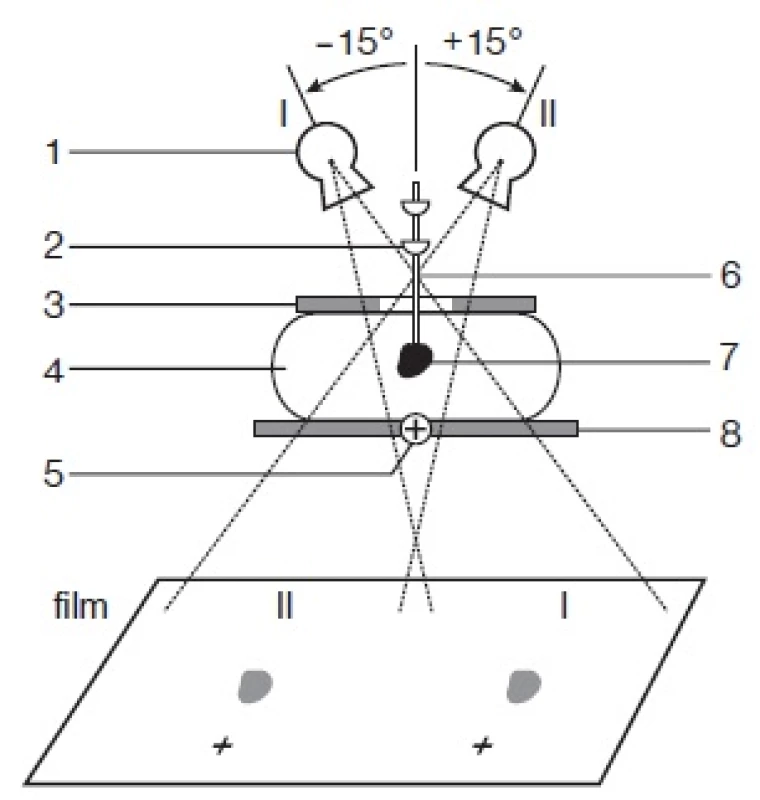
Komplikace core biopsie, které jsou uvedeny v přehledu, nebyly v souboru pacientek pozorovány:
- Krvácení a infekce, pneumotorax - opakované odběry jehlou 14G jsou samozřejmě více traumatizující než odběr jehlou16/18G, užití většího kalibru jehel je kontraindikováno u pacientek s hemoragickou diatézou nebo při podávání antikoagulačních preparátů.
- Implantace maligních buněk v odběrovém kanále byla průkazná při bioptické verifikaci mucinózního karcinomu při užití jehly 14G do několika dnů po odběru 12 a tato skutečnost by tedy měla být zvážena. Koaxiální technika s užitím jehly 16-18G by měla tuto možnost omezovat.
- Vazovagální reakce - odběr by se měl provádět v supinační poloze. U bojácných pacientek se doporučuje provést odběr v supinační poloze (nutný speciální odběrový stůl).
- Zlomení drátu, změna polohy drátu.
VI. Předoperační lokalizace je nezbytná u suspektních nehmatných/de novo vzniklých lézí detekovaných mamograficky/sonograficky. Průběh předoperační lokalizaci lze rozdělit do 3 fází:
1. Fáze: mamografická/sonografická lokalizace:
- a) znovu zhodnocení dostupných klinických, diagnostických dat pacientky (mamární komise)
- b) příprava pacientky (psychologický přístup je v 90 % naprosto dostačující)
- c) zavedení lokalizačního drátu (erudovaný radiolog)
- d) komunikace členů mamárního týmu (radiolog, chirurg a patolog především).
2. Fáze: chirurgický výkon
- a) odběr vzorku tkáně, orientace exstirpátu chirurgem - označení
- b) provedení specimen radiografie - informace od radiologa operatérovi o úspěšnosti výkonu
- c) spolupráce radiologa s patologem.
3. Fáze: stanovení histologické diagnózy
- a) zpracování vzorku
- b) histologický závěr.
Cílem předoperační lokalizace je: jistota exscize suspektní léze, frozen section, následně disekce axily a omezení rozsahu excize, a tím poškození okolních tkání, výsledné možné mutilace.
Indikace předoperační lokalizace nehmatných lézí:
- kalcifikace bez průkazu jádrového stínu
- suspektní kalcifikace
- shluk mikro/kalcifikací; popis distribuce mikrokalcifikací v práci je v souladu s doporučením současných autorů citovaných níže
- shluky kalcifikací: zaujímající < 2 cm3 objemu prsu
- segmentální rozložení: zaujímající > 2 cm3, ale < než regionální rozložení
- regionální rozložení: zaujímající značný objem prsu, ne v případě duktální distribuce a ne v celém prsu
- difuzní nebo roztroušené rozložení: prokazatelné kdekoliv v prsu jakéhokoliv tvaru
- lineární rozložení: zaujímající duktální systém (komedonový typ, casting type)
- lobulární rozložení: zaujímající mnohočetné tečkovité kalcifikace na velmi malé rozloze (2-3 mm), vytvářející tvar morušovitý nebo rosetovitý [5,9].
Mamografie prokáže:
- rozdílnou denzitu mikrokalcifikací
- rozdílnou velikost (délku) mikrokalcifikací
- neostrost ohraničení mikrokalcifikací. Tvar, velikost a denzita mají vyšší diagnosticko-prognostickou validitu než pouhé stanovení počtu mikrokalcifikací [6,7,11,12,13]. Přímo zvětšená mamografická vyšetření odhalují vyšší počet mikrokalcifikací než konvenční mamografické techniky. Granulární typ mikrokalcifikací byl v souboru prokázán v 51,26 %, odlitkový typ mikrokalcifikací (casting) byl prokázán v 33,85 % a výskyt granulárních a lineárních mikrokalcifikací byl průkazný v 14,89 %. Získané výsledky jsou v souladu s prací. Ve skupině s mamograficky prokazatelnými mikrokalcifikacemi byl současně zaznamenán vyšší výskyt orgánových metastáz, tento rozdíl je v práci hodnocen jako statisticky významný [13]. Uvedené výsledky pozorování jednoznačně vylučují využití mamografie k typingu karcinomů.
- cípatá ložiska s/bez obsahu kalcifikací
- ložiska kulovitá nebo se zvlněnými konturami
- špatně ohraničená nebo naznačeně jemně cípatá ložiska
- solidní ložiska detekovaná sonograficky > 10 mm2
- zvětšující se solidní ložiska
- distorze parenchymu
- nově vzniklá denzita
- fokální asymetrická denzita (ne asymetrie parenchymu)
- dilatace duktu, je-li ve spojení se sekrecí, vhodné je doplnění duktografie (samozřejmě po předchozím cytologickém vyšetření sekretu – obtisková cytologie).
V současnosti se preferuje lokalizace pod sonografickou kontrolou před mamografickou lokalizací (lokalizační fenestrovaná deska) nebo stereotaktickou lokalizací (výhodnější, rychlejší a přesnější než mamografická). Sonografickou lokalizaci lze provést i přímo na operačním sále.
Na našem pracovišti však převažuje mamografická stereotaktická lokalizace díky své vysoké přesnosti a spolehlivosti a navíc jsou výkony prováděny bez uvedených komplikací. K lokalizaci nehmatných lézí se užívá řada lokalizačních drátů (needle wire). Tyto je možno rozdělit do 2 základních typů: odstranitelné (možnost korekce lokalizace) a neodstranitelné. Schematicky jsou lokalizační dráty uvedeny na obr. 2.
Obr. 2. Typy lokalizačních drátů. a – Frankův typ, b – Homerův typ, c – Hawkinsův typ, e – Kopansův typ, f – X-Reidy typ. 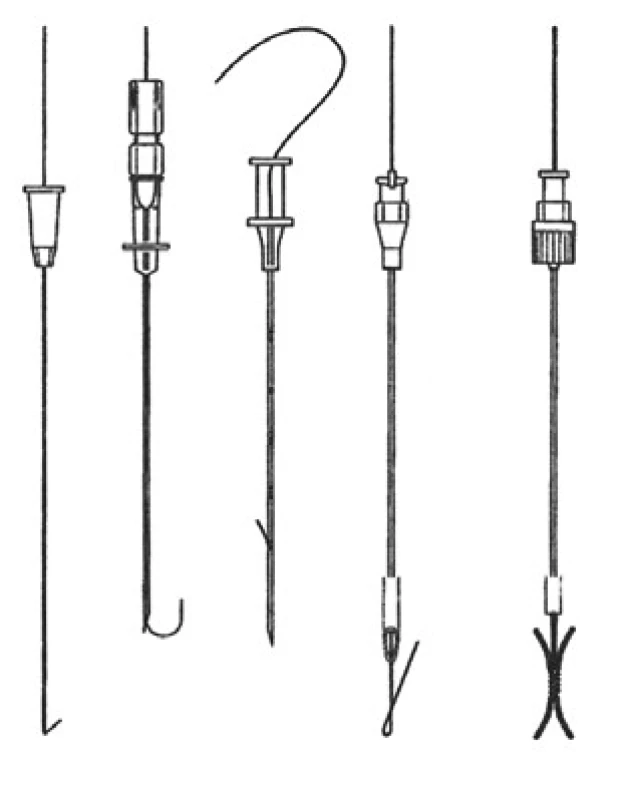
Mamografická lokalizace je vyhrazena pouze pro nehmatné léze, které nejsou detekovatelné sonograficky nebo kdy je lokalizace pod sonografickou kontrolou riskantní/obtížná a dále při lokalizaci mikrokalcifikací.
Značení metylenovou modří (jiná barviva), kontrastními látkami, uhlíkovými částicemi se v současnosti využívá již méně často.
Obr. 3. <em>Stereolokalizace</em> výsevu mikrokalcifikací pravé mammy v zevním horním kvadrantu u 41 leté ženy – převaha involuce, vazoskleroza, výsev mikrokalcifikací na rozloze 4 mm, typ mikrokalcifikací maligní – tečkovité + jemně granulární. 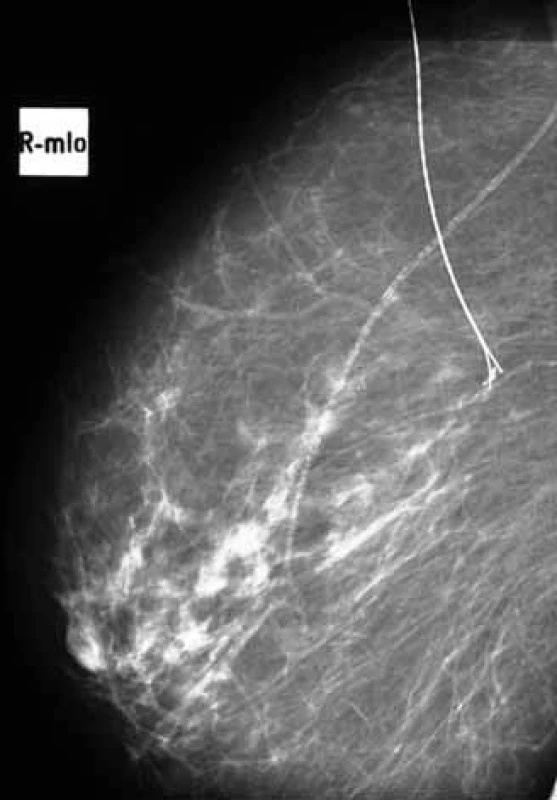
Obr. 4. <em>Specimen radiography</em>, převážně tukový exstirpát, shluk mikrokalcifikací na rozloze 3,5 mm. Nápadná vazoskleróza. Histologicky prokázán kribriformní + komedo in situ karcinom, Grade 3, vysoce pozitivní hodnota obou steroidních receptorů. 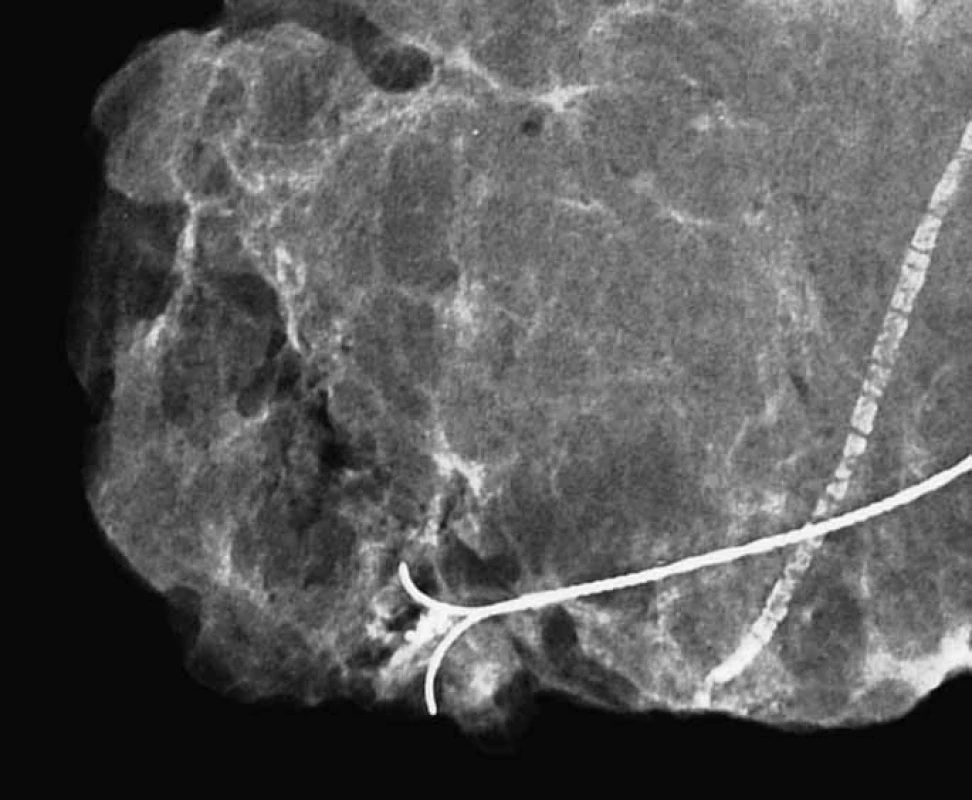
Obr. 5. <em>Specimen radiography</em> – lokalizace cípaté léze maligního vzhledu velikosti 4 mm, 52letá žena. Histologicky prokázán smíšený duktální a lobulární invazivní karcinom Grade 3, estrogenové receptory slabě pozitivní, progesteronový receptor negativní67, ki67 17%, Her2 +. 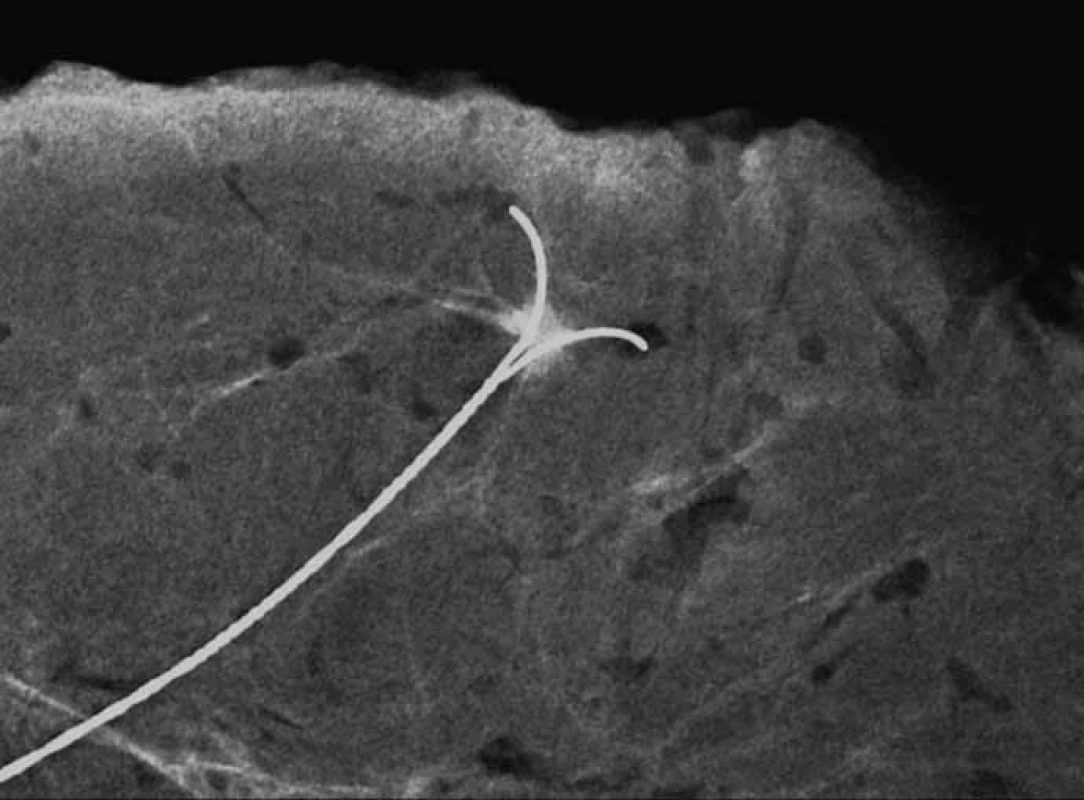
Obr. 6. <em>Specimen radiography</em> – lokalizace výsevu mikrokalcifikací a nepravidelné pruhovitá adenomatoidní léze v těsném okolí u které stanovený cévně rezistenční index vykazoval maligní hodnoty. Histologicky: Z oblasti výsevu mikrokalcifikací verifikován in situ karcinom komedo + papilárního typu Grade 3, z pruhovité arey (na obr. centrálně) invazivní lobulární a komedonový karcinom mléčné žlázy. Hodnota steroidních receptorů negativní, ki 67 15%, Her2 +++, Fish pozitivní. 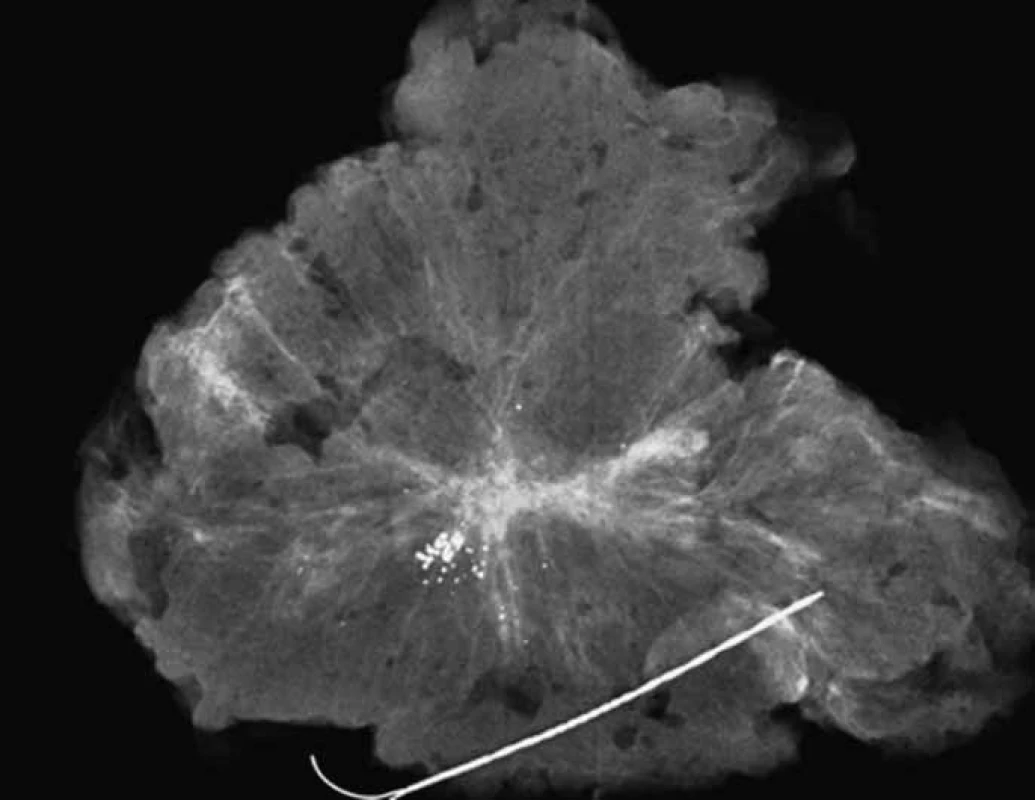
Komplikace lokalizačního výkonu jsou shodné s příčinami uvedenými u problematiky core biopsy. Některé z příčin nedokonalé lokalizace jsou vyjmenovány v tabulce.
Tab. 1. Některé z příčin nedokonalé lokalizace. 
Závěr
Nehmatné karcinomy mléčné žlázy představovaly z celkového počtu prokázaných 414 karcinomů 42,5 % (176 karcinomů). V roce 2002 (září–prosinec) se nehmatné karcinomy vyskytovaly ve 26,1 %, v roce 2003 ve 36,9 %, 2004 ve 43,7 % a v roce 2005 ve 46,1 %.
Z počtu 176 karcinomů mléčné žlázy bylo prokázáno 49 karcinomů in situ (27,9 %), ve stadiu pT1a pNo M0 22 karcinomů (12,5 %), ve stádiu pT1b pN0 M0 28 karcinomů (15,9 %), ve stadiu pT1b pN1 M0 9 karcinomů (5,1 %), ve stadiu pT1c pN0 M0 47 karcinomů (26,7 %) a ve stadiu pT1c pN1 M0 21 karcinomů (11,9 %). Ve skupině in situ karcinomů (49) byl stanoven grade 1 u 22,4 %, grade 2 u 28,6 % a grade 3 ve 49 %.
doc. MUDr. Zdeněk Pačovský, CSc.1,
MUDr. Karel Dvořák2,
CSc., prim. MUDr. Eva Jandáková 3
1chirurgické oddělení gynekologicko porodnické kliniky LF MU a FN Brno,
2mammodiagnostické oddělení gynekologicko porodnické kliniky LF MU a FN Brno,
3oddělení patologie gynekologicko porodnické kliniky LF MU a FN Brno
Zdroje
1. Kindermann G, Rummel W, Bischoff J et al. Early detection of of ductal breast cancer: the diagnostic procedure for pathological discharge of the nipple. Tumori 1979; 65(5): 555-62.
2. Balzer J et al. Early breast cancer. Berlin: Springer 1985 : 136-139.
3. Hall FM et al. Mammography in the diagnosis of in situ breast carcinoma. Radiology 1988; 168 : 279.
4. Troupin RH. Mammographic-pathologic correlation. Breast imaging 1988; 79.
5. Lanyi M. Diagnostik und Differential Diagnostik der Mammaverkalkungen. Berlin: Springer 1989.
6. Stomper PC, Connoly JL, Meyer JE et al. Clinically occult carcinoma in situ detected with mammography: analysis of 100 cases with radiologic-pathologic correlation. Radiology 1989; 172(1): 235-41.
7. Hilleren DJ, Anderson IT, Lindholm K et al. Invasive lobular carcinoma: mammographic findings in a 10-year experience. Radiology 1991; 178(1): 149-54.
8. Shaw DE, Parades E, Langer TG. Subtle signe of carcinoma. Applied Radiology 1992; 15.
9. Stomper PC, Connoly JL. Ductal carcinoma in situ of the breast: correlation between mammographic calcifications and tumour subtype. AJR1992; 159(3): 483-5.
10. Helvie MA, Paramagul C, Oberman HA, Adler DD. Invasive lobular carcinoma: imaging features and clinical detection. Invest.Radiol 1993; 28(3): 202-7.
11. Tabár L, Dean PB. Teaching Atlas of Mammography. New York: Thieme Verlag 2001.
12. Dronkers DJ, Hendriks JHCL, Holland R, Rosenbusch G. The Practise of Mammography. New York: Thieme Verlag 2002.
13. Dvořák K, Horák J. Diagnostické nejistoty spojené s jednotlivými zobrazovacími technikami. In Jitka Abrahámová, Ladislav Dušek et al Možnosti včasného záchytu rakoviny prsu. Praha: Grada Publishing 2003.
Štítky
Detská gynekológia Gynekológia a pôrodníctvo Reprodukčná medicína
Článek Perinatální infekce GBSČlánek Slovo úvodem
Článok vyšiel v časopisePraktická gynekologie
Najčítanejšie tento týždeň
2005 Číslo 5- Ne každé mimoděložní těhotenství musí končit salpingektomií
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Gynekologické potíže pomáhá účinně zvládat benzydamin
- Mýty a fakta ohledně doporučení v těhotenství
-
Všetky články tohto čísla
- Přednosti neinvazivní diagnostiky fetální anémie – kazuistika
- Perinatální infekce GBS
- Doporučený postup při diagnostice a léčbě streptokoků skupiny B v těhotenství a za porodu
- Zásady dispenzární prenatální péče ve fyziologickém těhotenství
- Doporučení k provádění screeningu poruch glukózové tolerance v graviditě
- Současný pohled na vztah hormonální substituční terapie a očních nemocí
- Předoperační lokalizace nehmatných mamárních lézí
- Paraaortální a pelvická lymfadenektomie - několik poznámek k operačním a pooperačním opatřením, komplikacím
- Slovo úvodem
- Radioterapie v léčbě zhoubných nádorů vulvy
- Podpůrná hormonální léčba v programu asistované reprodukce
- Praktická gynekologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Paraaortální a pelvická lymfadenektomie - několik poznámek k operačním a pooperačním opatřením, komplikacím
- Přednosti neinvazivní diagnostiky fetální anémie – kazuistika
- Perinatální infekce GBS
- Předoperační lokalizace nehmatných mamárních lézí
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



