-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Chronická pankreatitida – klasifikace, diagnostika a terapie
Autori: Petr Dítě 1
; I. Novotný 2; H. Nechutová 3; J. Trna 4
Pôsobisko autorov: Interní klinika Fakultní nemocnice, Ostrava 1; Endoskopické oddělení, Masarykův onkologický ústav, Brno 2; II. interní klinika FN u sv. Anny, Brno 3; Interní gastroenterologická klinika FNMU Brno 4
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 12, s. 684-691.
Kategória: Postgraduální vzdělávání
ÚVOD
Slinivka břišní patří mezi orgány s největší metabolickou aktivitou. Denně žláza produkuje 1000–1500 ml pankreatické šťávy s vysokým obsahem bílkovin 5–10 g/L. Zatímco pankreatické duktální buňky produkují především bikarbonáty a karboanhydrázu II, pankreatické trávicí enzymy jsou produkovány buňkami acinózními.
Hlavními zástupci pankreatických enzymů vyloučených do duodena jsou lipáza, amyláza a proteázy. Tyto enzymy jsou v acinárních buňkách secernovány ve formě proenzymů, intrapankreaticky enzymaticky neaktivních látek, které jsou až intraluminálně přeměněny na aktivní formu [1]. Je třeba zdůraznit, že trávení škrobů již začíná v dutině ústní a v duodenu je proces dokončen působením pankreatické amylázy, podobně jako počátek trávení tuků začíná již působením žaludeční lipázy, která tvoří asi 25 % celkové lipázy. Tím lze vysvětlit, proč aktivita lipázy je zaznamenávána i u osob s pankreatickou resekcí, avšak žaludeční lipáza nemůže nahradit efekt lipázy pankreatické. Lipáza v duodenu štěpí tuky a v součinnosti s přítomnosti žluče v duodenu umožní jejich vstřebávání [2]. Přitom kapacita pankreatu, pokud jde o produkci lipázy, je až 20krát vyšší, než je fyziologická potřeba pro trávení tuků, tj. přibližně 100 ml pankreatické šťávy u zdravých osob postačí pro trávení tuků přítomných v duodenu. Maximální sekreční vrchol v duodenu přítomných pankreatických enzymů je zaznamenán asi 30 min. po potravinovém podnětu.
Definice chronické pankreatitidy
Chronická pankreatitida je trvale progredující zánětlivý proces, při kterém je postupně nahrazen funkční parenchym žlázy tkání vazivovou. Fibrotizace je tak základním procesem, charakterizujícím chronickou pankreatitidu. Výsledkem těchto změn je nejprve objevení se exokrinní pankreatické nedostatečnosti, terminálním stadiem je vznik i endokrinní nedostatečnosti, tzv. pankreatogenního diabetu, pro vazivovou devastaci Langerhansových ostrůvků.
Nově nedávno identifikované formy chronické pankreatitidy však tuto definici již zcela nenaplňují, např. se toto týká formy pankreatitidy autoimunitní.
Klasifikace chronické pankreatitidy
Klasifikace chronické pankreatitidy se vyvíjela v závislosti na úrovni diagnostiky onemocnění.
Prvé klasifikace využívaly především možnosti stanovit zevně sekretorickou kapacitu žlázy tzv. funkčním testem s použitím enterohormonální stimulace pankreatu sekretinem a cholecystokininem, zavedeným do klinické praxe v 60.–70. letech minulého století. Jedním z diagnostických mezníků bylo zavedení zobrazovacích metod do diagnostiky pankreatopatií a dalším mezníkem byly poznatky z oblasti molekulární biologie a genetiky ve vztahu k chronické pankreatitidě.
V roce 2002 publikovaná klasifikace TIGARO odráží naše současné znalosti o rizikových a obecně etiologických faktorech, které jsou spojeny se vznikem chronické pankreatitidy [3].
Klasifikace chronické pankreatitidy dle etiologických faktorů
(T I G A R 0 klasifikace)
- T – toxicko-metabolická forma (alkohol, nikotin, hyperlipidemie, urémie, léky, toxiny)
- I – idiopatická forma
- idiopatická forma s časným začátkem nemoci
- idiopatická forma s pozdním začátkem nemoci
- tropická forma
- G – genetická forma
- hereditární chronická pankreatitida s průkazem geneticky indukované autoaktivace intrapankreatického kationického trypsinogenu na kodómu 29, 122 na trypsin ( SPINK 1, PRSST mutace)
- autosomálně recesivní forma (CFTR mutace)
- deficit alfa 1 antitrypsinu
- A – autoimunní forma
- R – rekurentní akutní pankreatitida spojená s morfologickými změnami u chronické pankreatitidy
- ischemická pankreatitida (cévní změny)
- postiradiační
- postnekrotická (reziduum po těžké akutní pankreatitidě)
- pancreas divisum
- O – obstruktivní forma – obstrukce vývodu (kámen, nádor)
- stenóza Vaterovy papily
- cystoid utlačující p. vývod
- vývojová anomálie
- jizva po traumatickém postižení žlázy
Uvedená klasifikace je odrazem našich současných znalostí o rizikových ? etiologických faktorech, které indukují vznik chronické pankreatitidy. V naprosté většině pro uvedené faktory platí (výjimkou je forma hereditární, obstruktivní a zřejmě i autoimunitní ), že zmíněné etiologické faktory samostatně nevedou ke vzniku chronické pankreatitidy, jsou tedy pouze r i z i k o v ý m i faktory, které se uplatní až za přítomnosti některého z dalších faktorů. Tím lze i vysvětlit, proč někteří alkoholici mají „jen“ jaterní cirhózu a ne chronickou pankreatitidu a naopak.
Snaha o vytvoření klasifikace, která by spojila pohled etiologický s klinickým a uvedení gradingu nemoci, dala vznik podrobné, ale z pohledu praktické medicíny až příliš komplikované klasifikace M-ANNHEIM [4].
Rizikové faktory dle M-ANNHEIM klasifikace:
Alkohol, kouření, nutriční faktory, hereditární onemocnění, imunologické a metabolické faktory. Poprvé je uveden jako nezávislý faktor nikotin.
Charakteristika jednotlivých rizikových faktorů:
- A – Alkohol – silný piják denní příjem více než 80 g alkoholu/den, střední příjem 20 g alkoholu/den a vyšší příjem alkoholu je právě v rozmezí 20–80 g alkoholu denně.
- N – Nikotin (počet cigaret denně)
- N – Nutrice, vysoký denní příjem tuků a proteinů, dyslipidemie
- H – Heredita
- E – Efferentní faktory pankreatického vývodu (pancreas divisum, obstrukce p. vývodu, M. Oddi dysfunkce)
- I – Imunologické faktory (autoimunitní forma pankreatitidy)
- M – Metabolické faktory (hyperkalcemie, chronická uremie, některé léky, toxiny)
Klinická stadia nemoci jsou dělena na 1. stadium (asymptomatické), 2. stadium symptomatické.
Stupně symptomatického stadia:
- a) chronická pankreatitida (CHP) bez pankreatické insuficience
- b) CHP s tzv. parciální pankreatickou nedostatečností
- c) CHP – algická forma s plnou pankreatickou nedostatečností
- d) CHP – nebolestivá forma s exokrinní i endokrinní nedostatečností
Diagnostická kritéria chronické pankreatitidy:
Dle naplnění kritérií je diagnóza nemoci označena jako jistá – pravděpodobná – hraniční – pankreatitida asociovaná s alkoholem.
Znaky jisté diagnózy chronické pankreatitidy
- pankreatické kalcifikace
- středně a významně manifestní změny pankreatického vývodu
- pankreatická steatorea reagující na podávání enzymů
- histologická kritéria
Pravděpodobná diagnóza chronické pankreatitidy:
- lehké změny pankreatického vývodu dle Cambridge kritérií,
- rekurentní nebo perzistující cystomy,
- patologický test exokrinní pankreatické sekrece,
- endokrinní pankreatická nedostatečnost.
Hraniční diagnóza chronické pankreatitidy:
- pouze typická symptomatologie CHP bez dalších kritérií dg CHP asociovaná s alkoholem,
- naplněna diagnostická kritéria a jednoznačný průkaz abusu alkoholu.
Diagnostická kritéria při použití zobrazovacích metod:
Původně hodnocení změny pouze dle ERCP, nyní jsou mandatorní kritéria při vyšetření počítačovou tomografií, magnetickou rezonancí (MRI a MRCP), endosonografií, která je metodou zobrazující již iniciální stadia změny pankreatického parenchymu (tzv. pankreatické textury).
Cambridgská kritéria posuzují změny jak pankreatického vývodu, tak sekundárních větví, konkrementy ve vývodném systému pankreatu i v parenchymu, přítomnost cystoidů, ohraničení žlázy, homogennost parenchymu.
Dle počtu jednotlivých patologických markerů lze rozlišit chronickou pankreatitidu na lehkou, středně těžkou a těžkou (bodovací systém).
M-ANNHEIM skórovací systém:
Pacientem udávaná bolest
- bez bolesti 0
- bolestivá recidivující pankreatitida 1
- nebolestivý průběh při analgetikách 2
- intermitentní bolest 3
- trvalá bolest 4
Kontrola bolesti
- bez léků 0
- neopioidní léky 1
- opioidy 2
Chirurgická intervence 4
Exokrinní insuficience
- nepřítomna 0
- mírná insuficience 1
- významná insuficience-steatorea 4
Endokrinní insuficience
- bez diabetu 0
- s diabetem 4
Zobrazovací metody
- normální nález 0
- neurčitý nález 1
- lehké změny 2
- středně těžké změny 3
- těžké změny 4
Hodnocení závažnosti nemoci (škála A–E):
- A – mírně závažná 0 – 5 (bodů)
- B – zvýšená závažnost 6–10
- C – pokročilá závažnost 11–15
- D – výrazná závažnost 16–20
- E – zvláště významná závažnost více než 20
Klasifikace je velmi dobře zpracovaná, podrobná, ale pro klinickou praxi příliš komplikovaná.
Epidemiologie
Incidence chronické pankreatitidy je rozdílná, např. ve Švýcarsku je udáván počet nových pacientů na 100 000 obyvatel 2 za rok, v Polsku 4 za rok a ve Skandinávii 8–10 pacientů za rok. Zcela výjimečný údaj je z Finska – 23 osoby na 100 000 za 1 rok [5]. V České republice je incidence chronické pankreatitidy 7,9 [6]. Rozdíly v incidenci nemoci jsou dány řadou faktorů, jako jsou: způsob stravování, denní příjem alkoholu, ale i genetické faktory. Kromě toho i metodiky získávání epidemiologických dat byly rozdílné, přesto lze konstatovat, že ve střední Evropě je incidence chronické pankreatitidy v rozmezí 6,00–8,00.
Chronická pankreatitida – diagnostické přístupy
Diagnostika chronické pankreatitidy je založena, kromě klasického vyšetření s odběrem anamnestických dat a málo přínosného vyšetření klinického, především na vyšetření zobrazovacími metodami CT, NMR, ERCP, ENDOSONOGRAFIE.
Pro bližší určení typu chronické pankreatitidy je ale třeba využít komplex dalších diagnostických metod:
- histomorfologické metody,
- molekulárně-biologické vyšetření,
- genetické vyšetření,
- vybraná vyšetření biochemická, imunologická.
Iniciální je znalost klinického obrazu onemocnění [7].
Anamnestické údaje jsou velmi důležité ke zhodnocení údajů z předchorobí. Významné je získání údajů o dietních návycích, o dlouhodobém pití alkoholu, o prodělaných infekčních chorobách, o autoimunitních chorobách, s kterými je/byl pacient léčen, o rodinné anamnéze pankreatitidy nebo o rodinném výskytu malignit atd.
Symptomy chronické pankreatitidy
Nejčastějším příznakem chronické pankreatitidy je bolest, kterou udává 85–90 % osob. Pouze malá část nemocných má bezbolestnou formu chronické pankreatitidy. Pankreatická bolest je stálá, doba trvání je od několika hodin po několik dnů. Klasická lokalizace bolesti je v okolí pupku, odkud se šíří pod oba oblouky žeberní. Bolest se dostavuje záhy po jídle a bývá tak intenzivní, že nemocní se z obavy jejího vyvolání bojí jíst. Bezbolestná forma nemoci je charakteristická pro tzv. late-onset idiopatické formy chronické pankreatitidy, kdy nemoc je diagnostikována ve věku kolem 50 let a žláza bez významnějších předchozích prodromů je nalezena již významně morfologicky změněná.
Poměrně konstantním symptomem je hubnutí. U některých osob je hubnutí tak progresivní, že nemocní nejsou schopni sami pouze perorálním příjmem potravy hmotnostní úbytek zastavit a dochází k příznakům malabsorbce. V takovém případě je nezbytná nutriční podpora (podávání MCT olejů, sippping, enterální výživa).
Dalším příznakem chronické pankreatitidy může být ikterus, mající obstrukční charakter. Je vyvolán poruchou odtoku žluči díky obstrukci intrapankreatické části žlučovodu, nejčastěji fibrózními změnami parenchymu. Ikterus je někdy i prvým příznakem autoimunitní formy nemoci, kdy masivní buněčná infiltrace pankreatického parenchymu doslova utlačuje intrapankreatickou část d. choledochus. Bezbolestný ikterus provází rovněž karcinom pankreatu a v takovém případě je dif. dg nutná.
Stolice u těžké exokrinní insuficience bývá frekventní, objemná, mastná, s nestrávenými zbytky potravy (jílovitého charakteru), ale i formovaná stolice jílovitého vzhledu se zbytky potravy patří do obrazu nemoci.
Pokročilé formy chronické pankreatitidy jsou provázeny většinou velmi labilním diabetem.
Asi u 2–3 % osob s chronickou pankreatitidou může být přítomen pankreatický ascites. V ascitu nacházíme vysoké hodnoty amylázy, lipázy a bílkovin.
Kromě ascitu asi u 10 % osob lze současně nalézt i hydrothorax, většinou levostranný, s vysokým obsahem amylázy, event. lipázy.
Odlišný klinický průběh má autoimunitní forma pankreatitidy, kdy průběh je klinicky charakterizovatelný spíše jako břišní dyskomfort než typická pankreatická bolest a úvodním příznakem může být pouze obstrukční ikterus (nejedná se ale o malignitu).
Vyšetření enzymatické aktivity je vyšetřením orientačním. Amylázemie a lipázemie nejsou dostatečně přesnými markery pro stanovení diagnózy chronické pankreatitidy, jejich specificita mírně stoupá, jestliže je doplníme o stanovení pankreatického isoenzymu-P-isoenzym v séru. Přesnějším vyšetřením je stanovení elastázy ve stolici. Ale abnormální hodnoty elastázy 1 ve stolici nacházíme až u morfologicky pokročilejších stadií [13].
Citlivějším vyšetřením je hodnocení exokrinní kapacity pankreatu po stimulaci slinivky břišní, např. enterohormony. Tyto látky se podávají intravenózně a nemocnému je dvoucestnou sondou odčerpán duodenální a žaludeční obsah. Tento test je poměrně přesný, avšak ekonomicky velmi náročný, a navíc zjištění, že se jedná skutečně o exokrinní pankreatickou nedostatečnost, ještě nic nevypovídá o etiologii. Dnes jsou tyto testy vyhrazeny především výzkumným studiím. Avšak již výše uvedená klasifikace M - ANNHEIM má jako jedno z kritérií posouzení exokrinní kapacity slinivky břišní. Mezi novější testy, posuzující pankreatickou funkci, patří testy dechové. Dechové testy jsou neinvazivní, neumožňují stanovit časná stadia onemocnění slinivky břišní, hodí se k monitoringu terapie exokrinní nedostatečnosti slinivky břišní [8].
Zásadní význam v diagnostice onemocnění slinivky břišní má vyšetření sledující změny morfologie žlázy [9]. UZ vyšetření je vždy prvotním vyšetřením a informuje o velikosti žlázy, její nehomogenitě, významným nálezem je rozšíření pankreatického vývodu nad 3 mm, velikost žlázy, její ohraničení a homogenita parenchymu (Obr. 1).
Obr. 1. Ultrazvukový obraz pankreatu s dilatovaným pankreatickým vývodem (šíře označena značkami) – patrny jsou i rozšířené sekundární pankreatické větve 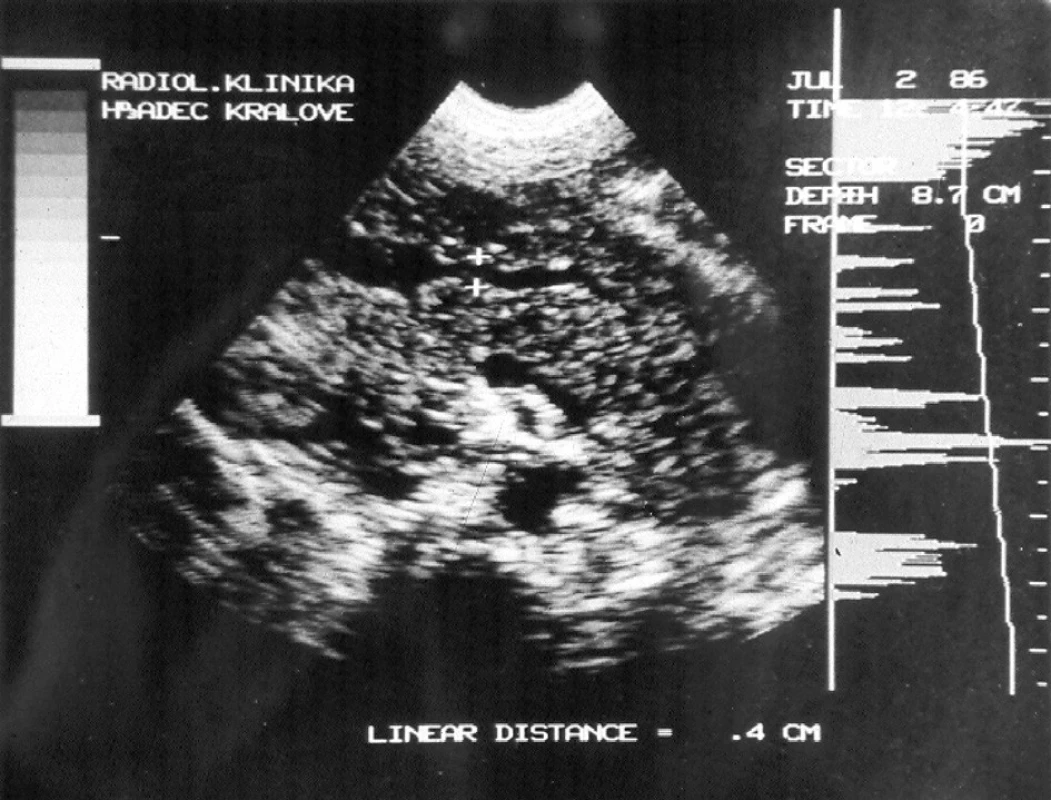
Počítačová tomografie umožňuje výbornou prostorovou orientaci, se spolehlivou diagnostikou kalcifikací, dobrým zobrazením pankreatického vývodu včetně jeho patologického obsahu. Metoda je efektivní v diagnostice cystoidů a ložiskových procesů od velikosti 1,0 cm. Metoda podává cenné informace i o vztahu žlázy k velkým cévám [10] (Obr. 2).
Obr. 2. CT obraz neostře ohraničeného pankreatu se širokým pankreatickým vývodem v celém průběhu žlázy – obraz mucinózní intrapankreatické neoplazie 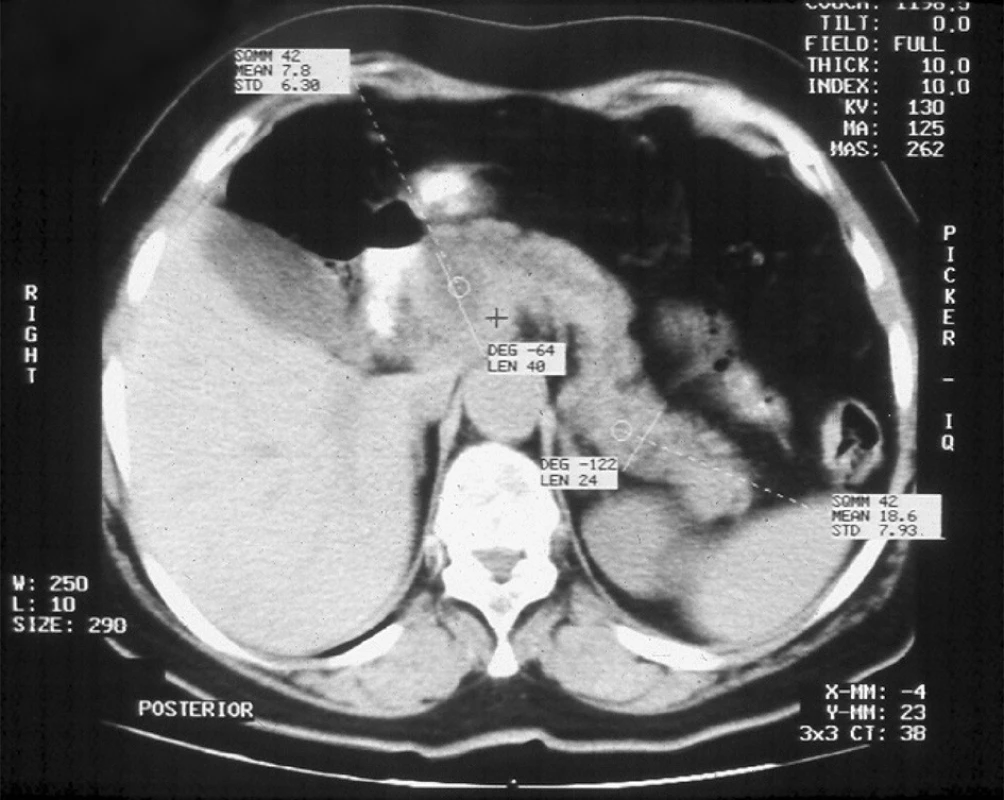
Zlatým diagnostickým standardem byla dlouhodobě endoskopická retrográdní cholangiopankreatografie (ERCP), při níž zobrazujeme pankreatický vývod, event. žlučové cesty retrográdně přes Vaterovu papilu, při zavedeném duodenoskopu do sestupného raménka duodena. Metoda je ale metodou invazivní s možnými, i velmi závažnými, komplikacemi a dnes je především metodou endoskopického terapeutického armentaria [9] (Obr. 3).
Obr. 3. Postmortem zobrazený pankreatický vývod s větvením sekundárních i terciárních větví 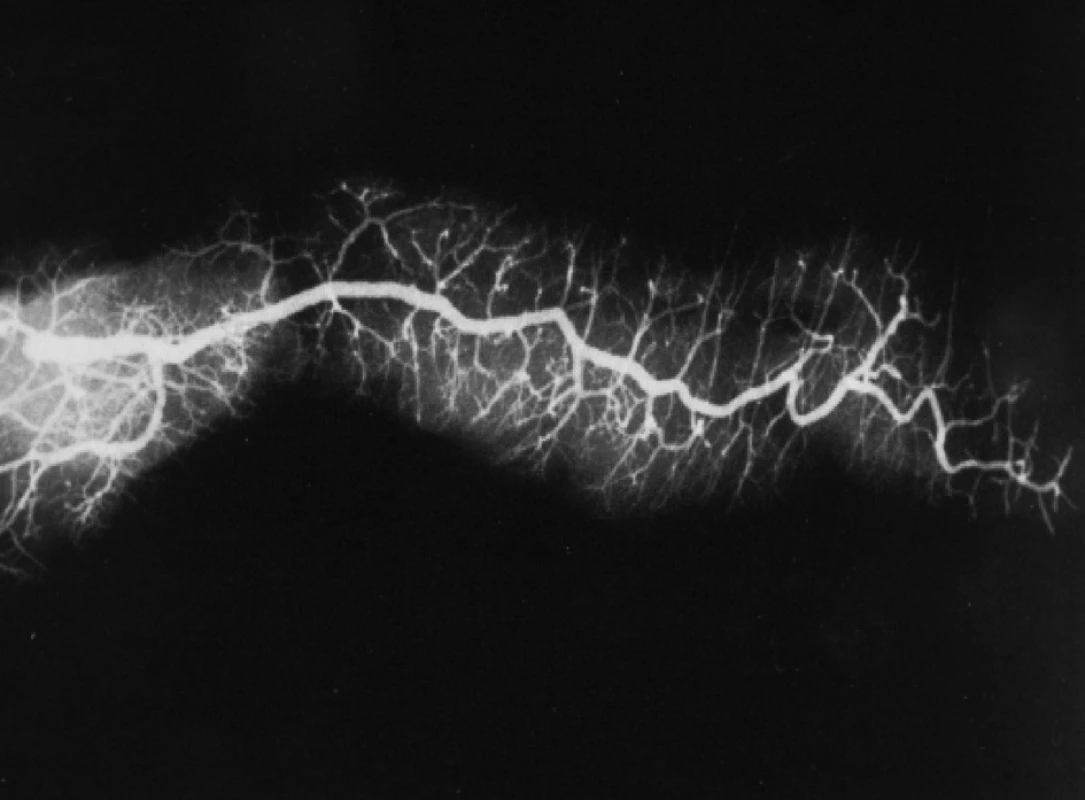
Vyšetřením, která přispívá k včasné diagnostice chronické pankreatitidy, identifikaci ložiskových lézí a zvláště diagnostice neuroendokrinních nádorů, je endoskopická ultrasonografie, která může být doplněna o vyšetření elastografické. Výhodou metody je možnost cílené a bezpečné pankreatické biopsie, jako jediná z diagnostických metod umožní zobrazit texturu parenchymu, tj. nejen vývodné systémy [11, 12]. Nevýhodou je určitá invazivita vyšetření, přesnost diagnózy je významně závislá od zkušeností vyšetřujícího (Obr. 4, Obr. 5).
Obr. 4. Endosonografický obraz typické lalůčkovité struktury parenchymu slinivky břišní 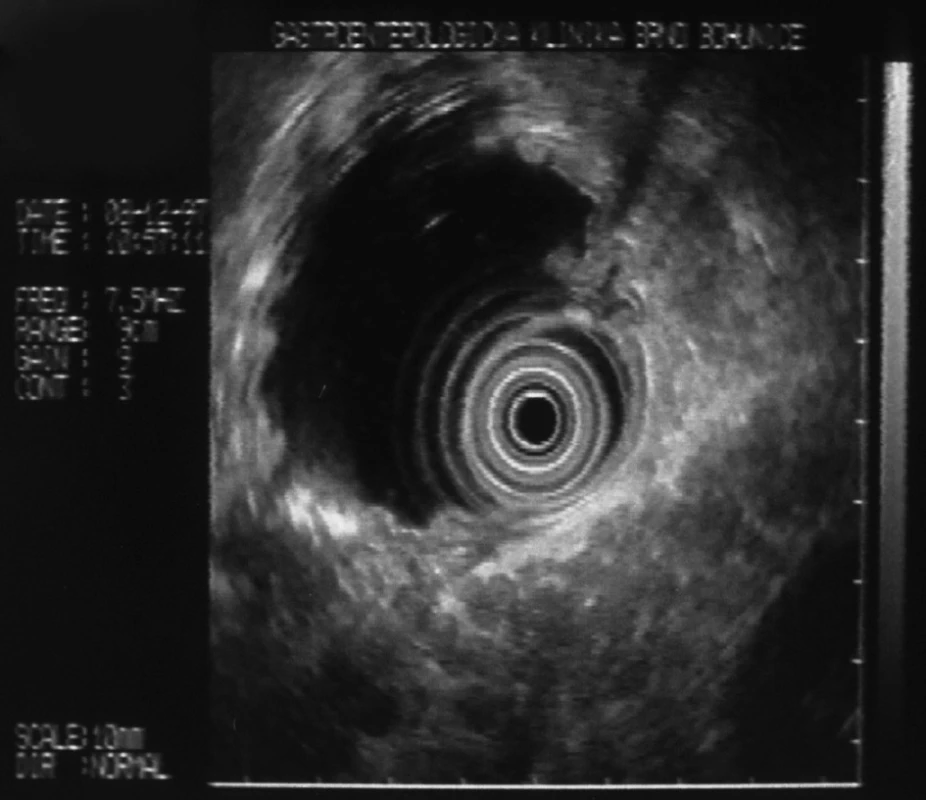
Obr. 5. Endosonografické zobrazení konkrementů v pankreatickém vývodu 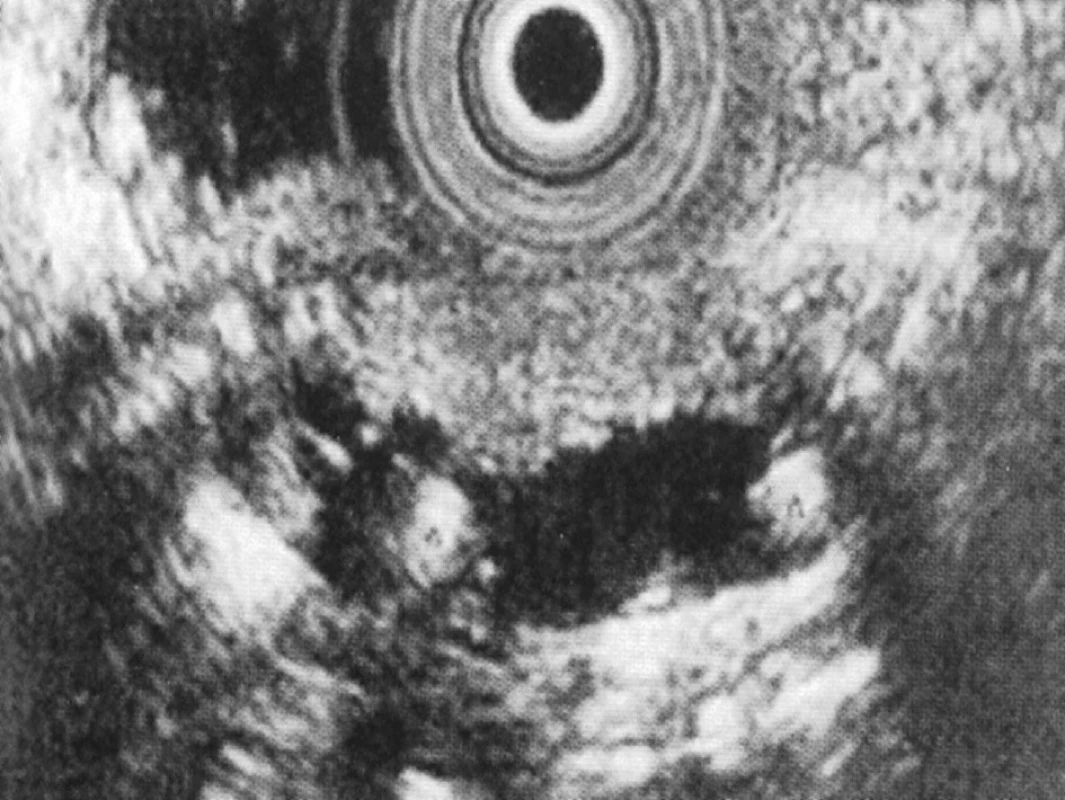
V současnosti lze za prvou metodu volby označit nukleárně magnetickou rezonanci – MRI nebo cholangiopankreatografie (MR-CP [13]). Neinvazivní cestou lze poměrně dobře zobrazit žlučové cesty a pankreatický vývod, pro zvýšení citlivosti s použitím sekretinu i. v. (Obr. 6). Oproti ERCP není metoda zatížena žádnými komplikacemi, pramenícími z alergické reakce na podání jodového kontrastu. Po podání sekretinu jsou vypracována i kritéria k orientačnímu hodnocení exokrinní kapacity pankreatu [14]. MRI zobrazí pankreatickou tkáň, ale toto vyšetření není lepší než CT.
Obr. 6. Magnetická rezonanční pankreatografie se zobrazením normální morfologie pankreatického vývodu v oblasti hlavy pankreatu, chybějící náplň v oblasti těla žlázy a dilatace v oblasti kaudy pankreatu za vývod stenozující maligní lézí slinivky břišní 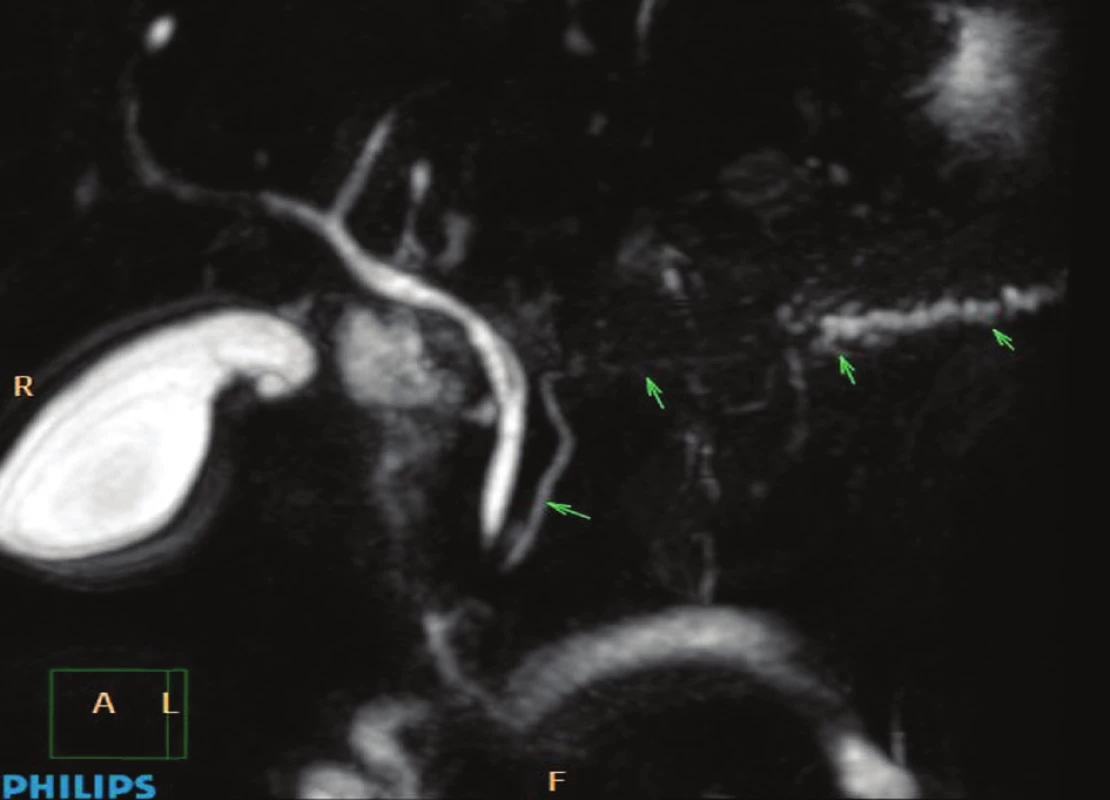
Stanovení mutací CFTR, SPINK-1 a PRSST genu patří mezi standardní vyšetření všude tam, kde pomýšlíme na genetickou formu chronické pankreatitidy [15, 16, 17, 18].
U osob s podezřením na autoimunní formu nemoci (AIP) jsou stanovovány některé protilátky v krevním séru, jako např. antilaktoferrin, antikarboanhydráza II, protilátky proti pankreatickým vývodům , revmatoidní faktor, antinukleární antigen (ANA), protilátky proti hladkým svalům (ASMA) [19], sérové globuliny a imunoglobuliny včetně frakce IgG4, jejíž pozitivita je jedním z nejspolehlivějších ukazatelů, že se jedná o AIP. V dg. AIP je někdy nutná biopsie pankreatické tkáně. U relativně vzácného tzv. 2. typu autoimunní formy pankreatitidy je biopsie vyžadována vždy, protože u těchto nemocných je hodnota IgG4 normální (méně než 135 mg/dL) [20].
Formy CHP – charakteristika
Při využití TIGARO klasifikace chronické pankreatitidy lze charakterizovat některé typické znaky jednotlivých forem pankreatitidy chronické.
Obstruktivní forma vzniká na základě indukce obstrukce hlavního pankreatického vývodu. Tím může být stenóza Vaterovy papily, striktury pankreatického vývodu po odhojení např. akutní pankreatitidy, obstrukce vývodu konkrementem, tlak na pankreatický vývod cystomem anebo jako důsledek tupého poranění dutiny břišní. Podstatou je porucha odtoku pankreatického sekretu do duodena, vznik přetlaku v pankreatickém vývodu, který se přenáší na vývody sekundární a terciární. Tato skutečnost vede ke vzniku pankreatické ischemie, tím k aktivaci stelátových buněk a indukce fibrogeneze.
Včasná diagnostika a odstranění obstrukce endoskopicky nebo chirurgicky je zásadní léčbou.
Toxonutritivní forma je v našich zemích nejčastější. Znovu je však třeba zdůraznit, že alkohol je významným rizikovým faktorem, který však vyžaduje k vyvolání chronické pankreatitidy přítomnost některého dalšího faktoru, nejčastěji u pijáků je to kouření. Platí, že obvykle více než 5letý pravidelný příjem alkoholu u mužů v množství 60–70 g/den a u žen 40 g/den je toxický. Přesto jsou tzv. alkohol „senzitivní“ jedinci, kde alkoholická forma vzniká již po mnohem menším denním příjmu alkoholu a nepochybně zde hraje významnou roli genetická výbava jedince. Kouření je dnes jednoznačně považováno za samostatný rizikový faktor, protože vyvoláním tkáňové ischemie je indukována fibrogeneze pankreatické tkáně. Z pohledu diagnostiky jsou iniciální stadia poškození pankreatu v naprosté většině případů klinicky asymptomatická, a tak v době, kdy přichází nemocný k lékaři se svými potížemi, nacházíme již pokročilý fibrózní proces, který je ireverzibilní. V rámci objektivity je ale třeba říci, že naše vyšetřovací metody jsou stále málo citlivé v identifikaci skutečně iniciálních, tzv. minimálních změn žlázy.
Genetická forma pankreatitidy je dnes neobyčejně sledovanou oblastí a s nadsázkou lze konstatovat, že genetika má jistý podíl na rozvoji všech forem chronické pankreatitidy. Je ale třeba rozlišit geneticky indukované pankreatitidy a pankreatitidu hereditární. Zatímco hereditární forma, kde zásadní roli hraje mutace PRSS1 pro kationický trypsinogen, je přísně hereditární a nepotřebuje pro vznik nemoci žádný další rizikový faktor, u geneticky indukované formy, kde roli hraje mutace CFTR a SPINK 1, jsou tyto mutace pouze jedněmi z významných rizikových faktorů. Např. CFTR mutace byla až ve 25 % prokázána u osob alkoholem indukované formy nemoci [18].
Hereditární forma nemoci je prekancerózním stavem, kdy výskyt pankreatického karcinomu u těchto osob je až 80x vyšší než u ostatní populace [21].
Autoimunitní pankreatitida byla poprvé popsána v r. 1991 a dnes je součástí komplexu chorob, označeného jako „IgG4 asociovaná onemocnění“, kam patří např. IgG4 cholangitida, IgG4 retroperitoneální fibroza nebo Mikuliczův syndrom. U této formy nemoci má zásadní význam včasná a správná diagnóza [20]. Nasazení steroidů v naprosté většině případů stav upraví a není třeba chirurgická terapie, což se omylem nezřídka stává, ale navíc v rámci diferenciální diagnostiky je třeba spolehlivě rozlišit mezi fokální formou autoimunitní formy pankreatitidy a pankreatickou malignitou. Zde musíme spoléhat kromě kliniky na výsledek biopsie pod EUS kontrolou [19].
Terapie chronické pankreatitidy
Léčení chronické pankreatitidy je i v r. 2011 dělitelná do 3 skupin:
- konzervativní (medikamentózní) léčba;
- endoskopická léčba;
- chirurgická léčba.
Konzervativní léčba obsahuje vždy dietetická opatření. Absolutní zákaz alkoholu je samozřejmou podmínku pro to, abychom mohli uvažovat o efektivní terapii nemocného s chronickou pankreatitidou. Z diety vylučujeme živočišné tuky a nahrazujeme je rostlinnými, množství tuků nemá přesáhnout 80 g denně. Tam, kde je nutné množství tuků snížit, je doporučeno podání MCT olejů v množství 80–120 g. Množství cukru je odvislé od toho, zda nemocný má nebo nemá diabetes, a činí asi 300 g denně. Bílkoviny podáváme zhruba v dávce 80–100 g/den. Pacienti s velice těžkým stavem výživy jsou léčeni enterální formou výživy [22, 23].
Léky, které používáme v terapii chronické pankreatitidy, mají za cíl korigovat hlavní příznaky nemoci. V žádném případě nelze říci, že používáme kauzální léčbu. Je to léčba pouze suplementační, nebo léčba symptomová.
Nejčastěji používanými preparáty u osob s chronickou pankreatitidou jsou léky obsahující pankreatické enzymy [24, 25]. Jednoznačně jsou preferovány kapsle, které se skládají z mikropelet, jejichž velikost je optimálně 1,0–2,0 mm. Tyto pelety jsou na svém povrchu chráněny acidorezistentním obalem, aby enzymy v nich nebyly kyselinou solnou inaktivovány (Obr. 7).
Obr. 7. Grafické zobrazení podání léku s obsahem pankreatické lipázy v průběhu 24 hodin při jednotlivých jídlech 
Pankreatické enzymy, které jsou obsaženy v kapslích, jsou amyláza, lipáza a proteázy. Tam, kde potřebujeme korigovat především známky steatorey a malabsorpce, použijeme léky s vysokým obsahem lipázy – denně 40 000 j. ke každému hlavnímu jídlu [26, 27]. Chceme-li ovlivnit i pankreatickou bolest, je doporučeno preferovat léky, které mají vysoký obsah proteáz. Tento pokus je však stále předmětem diskuzí. Obvyklá klasická dávka pankreatických enzymů bývá udávána 3x25 000 j. (3x1 kapsle). V současné době je zdůrazněna potřeba podávat kapsli s pankreatinem ke každému jídlu, u významné steatorhey podat během hlavních jídel 40 000–50 000 j. lipázy (Obr. 8). Pro úspěšnost léčby pankreatickou substitucí je podstatné, aby byla zachována synchronizace, kdy do horní části vstoupí žaludeční chymus, a ve stejnou dobu jsou uvolněny pankreatické enzymy. Jen tak je zachováno fyziologické trávení, a jestliže je v duodenu přítomna žluč, pak je zachována i resorbce v tucích rozpustných látek.
Obr. 8. Grafické zobrazení procesu uvolnění granulí s ochranným obalem proti inaktivaci enzymů žaludeční kyselinou chlorovodíkovou v žaludku a jejich synchronní proniknutí do horní části duodena se žaludečním chymem (Z granulí jsou v duodenu, v souvislosti s hodnotou duodenálního pH, uvolněny pankreatické enzymy.) 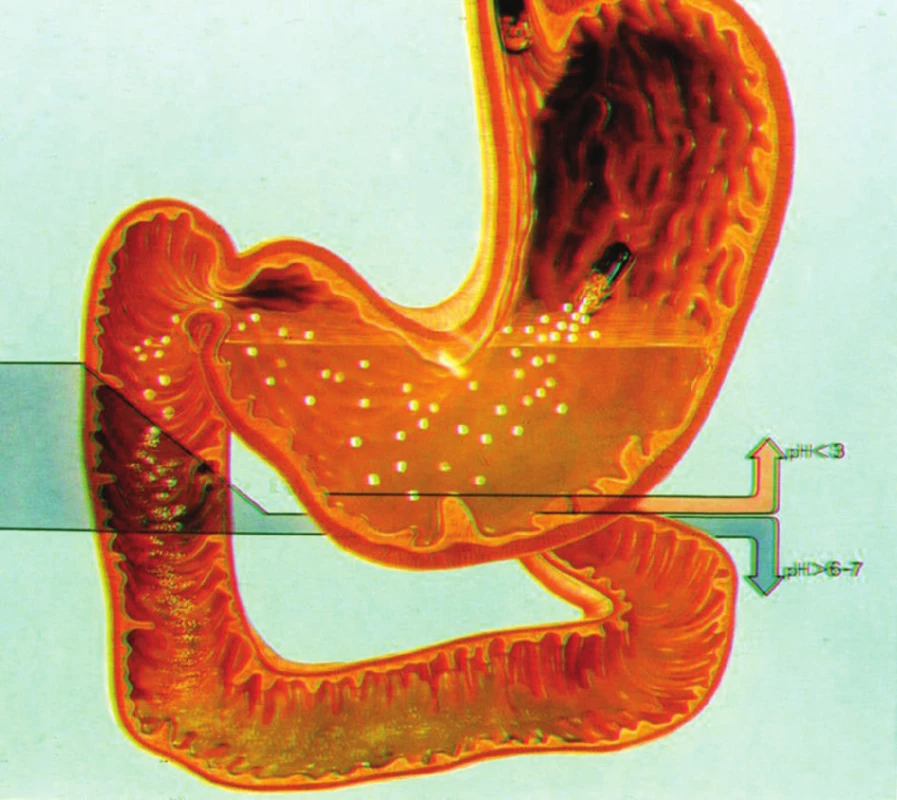
Vedlejší a možné nežádoucí příznaky léčby
Vysoké dávky enzymů – více než 100 000 j. jednorázově – mohou být provázeny pocitem na zvracení, bolestmi břicha, říháním, hypersenzitivitou. Tyto příznaky byly popsány především u dětí léčených vysokými dávkami pro diagnózu mukoviscidózy. Není jasná fenomen fibrotizující kolonopatie, zdá se, že se jedná o lokální efekt pryskyřice, která je obalem kapslí, a nikoliv o efekt vlastních enzymů.
Možnosti nových preparátů s obsahem lipázy:
V současnosti jsou používány enzymy připravené z hovězího substrátu, a to v případech, že z jakéhokoliv důvodu nelze použít standardní preparáty, připravené z vepřového substrátu. Obecně platí, že bovinní preparáty obsahují až o 75 % méně lipázové aktivity než standardní.
Nadějí se zdála být suplementace bakteriální lipázou, která je pH stabilní. Nevýhodou je, že neexistují bakteriální amyláza a proteázy.
Jestli v budoucnu uspěje tzv. znovuobnovení vlastní lidské lipázy metodami z oblasti bioinženýrských technologií, je stále velkou futurologií, ale in vitro takové studie probíhají, ale na zavedení genové terapie v této indikaci stále čekáme.
Exokrinní pankreatická nedostatečnost je vždy závažným stavem, který je spojen etiologicky především s chronickou pankreatitidou, pankreatickým karcinomem, stavy po resekčních výkonech na pankreatu a u osob s mukoviscidózou. Ztráta přítomnosti pankreatických enzymů v duodenu vede k nedostatečné absorpci tuků, proteinů a karbohydráz, které se projeví steatoreou, kreatorheou, břišním dyskomfortem, ztrátou tělesné hmotnosti a deficiencí řady pro organismus základních nutrientů. Suplementační terapie léky s obsahem pankreatických enzymů má být proto zahájena ihned po průkazu exokrinní pankreatické nedostatečnosti. Řada studií prokázala, že dostatečná dávka a správně zvolená galenická forma použité pankreatické suplementace zásadně pozitivně ovlivní tzv. koeficient tukové absorpce (CFA), aniž by vždy vymizela steatorea.
Kromě pankreatické substituce je často nutné pacientovi s chronickou pankreatitidou podávat analgetika. U některých osob vystačíme s podáváním léků se spazmolytickým účinkem, u jiných je třeba podávat tzv. synaptická analgetika, např. tramadol. Dle standardu německé gastroenterologické společnosti je prvým lékem volby paracetamol v analgetické dávce. Protože chronická pankreatitida bývá spojena i se změnami motility tenkého střeva (dysmotilita), řada pacientů udává zlepšení potíží po prokineticích.
U osob s autoimunní formou nemoci jsou zásadní léčbou kortikoidy podávané perorální formou, iniciální dávka je 40 mg po dobu 4 týdnů, dále dávku snižujeme v intervalu 7 dnů o 5 mg. Dlouhodobá terapie 10 mg prednisonu trvá 6 měsíců [18] (Obr. 9).
Obr. 9. Racionální aplikace analgetik u osob s chronickou algickou pankreatitidou 
Endoskopická léčba chronické pankreatitidy je indikována u obstruktivní algické formy nemoci [29]. Její podstatou je protětí sfinkterů Vaterovy papily a uvolnění toku pankreatického sekretu do duodena, nebo odstranění konkrementu z pankreatického vývodu pomocí košíčku či balonku. Dále je možné přemostění pankreatické stenózy zavedením plastikového stentu. V současné době se objevují i prvé zprávy o možnosti využit tzv. self-expanding odstranitelný drén. Endoskopická léčba je rovněž efektivní v terapii pankreatických cystoidů, které buď komunikují s pankreatickým vývodem, nebo přímo naléhají na žaludeční stěnu [30]. Intraduktální pankreatické kameny jsou drceny pomocí rázové vlny (ESWL) a potom odstraněny [30, 31].
Endoskopická léčba nabízí proti léčbě chirurgické pouze drenážní výkony, v dlouhodobých výsledcích může být proto méně výhodná [32, 33].
Stále v klinické praxi platí, že s výjimkou autoimunitní formy nemoci můžeme chronickou pankreatitidu léčit, ale neumíme naše nemocné vyléčit.
Prof. MUDr. Petr Dítě, DrSc.
Atriová 11
62 100 Brno
e-mail: pdite.epc.@gmail.com
Zdroje
1. Keller J, Layer P. Human pancreatic exocrine response in nutrients in healthy and disease. Gut 2005;54(Suppl. 6):21–28.
2. Carriere F, Barrowman JA, Verger R et al. Secretion and contribution to lipolysis of gastric and pancreatic lipases during a text meal in human. Gastroenterology 1993;105(3):876–878.
3. Etemad B, Whitcomb DC. Chronic pancreatitis: diagnosis, classification, and new genetic developments. Gastroenterology 2001;120 : 682–707.
4. Ammann RW, Hertz PU, Kloppel G. Course of alcoholic chronic pancreatitis: a prospective clinicomorphological long-term study. Gastroenterology 1996;111 : 224–231.
5. Spanier BWM, Dijkgraaf MGW, Bruno MJ. Epidemiology, etiology and outcome of acute and chronic pancreatitis: An update. Best Praktice and Research Clinical Gastroenterology 2008;22(1): 45–68.
6. Dite P, Stary K, Novotny I et al. Incidence of chronic pancreatitis in the Czech republic. Eur J Gastroenterol Hepatol 2001;13 : 749–750.
7. Dite P a kol. Chronická pankreatitida, Praha, Galén 2003.
8. Braden B. C breath tests for the assessment of exocrine pancreatic function. Pancreas 2010;39(7):955–959.
9. Graziani R, Tapparelli M, Malago R et al. The various imaging aspects of chronic pancreatitis. JOP 2005;6 : 73–88.
10. Shams J, Stein A, Cooperman AM. Computed tomography for pancreatic diseases. Surg Clin North Am 2001;81 : 283–36.
11. Wallace MB, Hles RH. Endoscopic ultrasound in the evaluation and treatment of chronic pancreatitis. Pancreas 2001;23 : 26–35.
12. Catalano MF. Diagnosing early-stage chronic pancreatitis: is endoscopic ultrasound a reliable modality? J Gastroenterol 2007;42 Suppl 17 : 78–84.
13. Sugiyama M, Haradome H, Atomi Y. Magnetic resonance imaging for diagnosing chronic pancreatitis. J Gastroenterol 2007;42 Supp 17 : 108–112.
14. Czako L. Diagnosis of early-stage chronic pancreatitis by J Gastroenterol 2007;42 Suppl 17 : 113–117.
15. Witt H, Apte MV, Keim V et al. Chronic pancreatitis: challenges and advances in pathogenesis, genetics, diagnosis, and therapy. Gastroenterology 2007;132 : 1557–1573.
16. Sharer N, Schwarz M, Malone G et al. Mutation of the cystic fibrosis gene in patiens with chronic pancreatitis. N Eng J Med 1998;339 : 645–652.
17. Cohn JA, Friedman KJ, Noone PG, et al. Relation between mutations of the cystic fibrosis gene and idiopathic pancreatitis. N Engl J Med 1998;339 : 653–658.
18. Witt H, Luck W, Hennies HC et al. Mutations in the gene encoding the serine protease inhibitor, Kazal type 1 are associated with chronic pancreatitis. Nat Genet 2000;25 : 213–216.
19. Kamisawa T, Anjiki H, Takuma K et al. The natural course of autoimmune pancreatitis. Hepatogastroenterology 2009;56 : 866–870.
20. Buscarini E, Frulloni L, De Lisi S et al. Autoimmune pancreatitis: a challenging diagnostic puzzle for clinicians. Dig Liver Dis 2010;42 : 92–98.
21. Lowenfels AB, Maisonneuve P, Cavallini G et al. Pancreatitis and the risk of pancreatic cancer. International Pancreatitis Study Group. N Engl J Med 1993;328 : 1433–1437.
22. Meier R, Ockenga J, Pertkiewicz M et al. ESPEN Guidelines on Enteral Nutrition: Pancreas. Clin Nutr 2006;25 : 275–284.
23. Caliari S, Benini L, Sembenini C et al. Medium-chain triglyceride absorption in patiens with pancreatic insufficiency. Scand J Gastroenterol 1996;31 : 90–94.
24. Layer P, Keller J, Lankisch PG. Pancreatic enzyme replacement therapy. Curr Gastroenterol Rep 2001;3 : 101–108.
25. Dominguez-Munoz JE. Pancreatic enzyme therapy for pancreatic exocrine insufficiency. Curr Gastroenterol Rep 2007;9 : 116–122.
26. Silkens ECM, Cahen DL, Kuipers EJ, Bruno M. Pancreatic enzyme replacement therapy in chronic pancreatitis. Best Practice Prs Clin Gastroenterol 2010;24 : 337–347.
27. Ferrone M. Raimondo M et al. Pancreatic enzyme pharmacotherapy. Pharmacotherapy 2007;27(6): 910–920.
28. Delhaye M, Arvanitakis M, Verset G et al. Long-term clinical outcome after endoscopic pancreatic ductal drainage for patiens with painful chronic pancreatitis. Clin Gastroenterol Hepatol 2004;2 : 1096–1106.
29. Delhaye M, Arvanitakis M, Bali M et al. Endoscopic therapy for chronic pancreatitis. Scand J Surg 2005;94 : 143–153.
30. Tringali A, Boskoski I, Costamagna G. The role of endoscopy in the therapy of chronic pancreatitis. Best Pract Res Clin Gastroenterol 2008;22 : 145–165.
31. Deviere J, Bell RH, Jr., Beger HG, Traverso LW. Treatment of chronic pancreatitis with endotherapy or surgery: critical review of randomized control trials. J Gastrointest Surg 2008;12 : 640–644.
32. Cahen DL, Gouma DJ, Nio Y et al. Endoscopic versus surgical drainage of the pancreatic duct in chronic pancreatitis. N Engl J Med 2007;356 : 676–684.
33. Dite P, Ruzicka M, Zboril V et al. A prospective, randomized trial comparing endoscopic and surgical therapy for chronic pancreatitis. Endoscopy 2003;35 : 553–558.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článek Upside down stomachČlánek Pankreatitida
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2012 Číslo 12- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Impakt radikální resekce v komplexní léčbě nemocných se solidním maligním nádorem
- STARR operace v léčbě rektokély a intususcepce rekta
- Metody odběru vzorku na kultivační vyšetření v chirurgické praxi, otiskové metody
- Centrální kanylace s využitím sonografie a skiaskopie – 2leté zkušenosti
- Klasifikace chirurgických komplikací: analýza vlastní skupiny nemocných
- Upside down stomach
- Pľúcna pneumatokéla u dospelého pacienta – kazuistika
- Pankreatitida
- Chronická pankreatitida – klasifikace, diagnostika a terapie
- Akutní pankreatitida – komplexní problematika
- Chirurgická terapie chronické pankreatitidy
- Chirurgická léčba karcinomu pankreatu
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Upside down stomach
- STARR operace v léčbě rektokély a intususcepce rekta
- Klasifikace chirurgických komplikací: analýza vlastní skupiny nemocných
- Chirurgická terapie chronické pankreatitidy
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



