-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Nové možnosti léčby chronické tromboembolické plicní hypertenze v České republice
New possibilities in the treatment of chronic thromboembolic pulmonary hypertension
Pulmonary arterial hypertension (PAH) has a multifactorial pathobiology. Vasoconstriction, remodeling of the pulmonary vessel wall, and thrombosis contribute to increased pulmonary vascular resistance in PAH. Prostanoids have played a prominent role in the treatment of PAH. They improves exercise capacity, hemodynamics, and survival in patients with idiopathic pulmonary arterial hypertension (IPAH). Several interventional and surgical approaches are available for treatment of PAH - atrial septostomy, lung or heart-lung transplantation. Pulmonary endarterectomy is the accepted method of treatment for patients with chronic thromboembolic pulmonary hypertension (CTEPH). Establishing the diagnosis and the classification of the type of lesions by pulmonary angiography is crucial for optimal patients selection. Fewer then 3,000 PEA operations have been performed worldwide, although it is potentially curative treatment option patients with CTEPH. Pulmonary endarterectomy have been performed successfully in the Czech Republic in the Clinic of Cardiovascular Surgery at the General Teaching Hospital in Prague in September 2004.
Key words:
chronic tromboembolic pulmonary hypertension - pulmonary endarterectomy
Autoři: M. Škvařilová 1; P. Jansa 1; J. Lindner 2; J. Kunstýř 3; E. Mayer 4; S. Heller 1; T. Paleček 1; M. Aschermann 1; J. Tošovský 2
Působiště autorů: II. interní klinika kardiologie a angiologie 1. lékařské fakulty UK a VFN Praha, přednosta prof. MUDr. Michal Aschermann, DrSc., FESC 1; II. chirurgická klinika kardiovaskulární chirurgie 1. lékařské fakulty UK a VFN, Praha, přednosta doc. MUDr. Jan Tošovský, CSc. 2; Klinika anesteziologie a resuscitace 1. lékařské fakulty UK a VFN, Praha, přednosta MUDr. Martin Stříteský, CSc. 3; Klinik für Herz-, Torax- und Gefäßchirurgie, Johanes Gutenberg Universität Mainz, Německo, direktor prof. Dr. Med. Christian-F. Vahl 4
Vyšlo v časopise: Vnitř Lék 2005; 51(11): 1289-1296
Kategorie: Přehledný referát
Souhrn
Plicní arteriální hypertenze (PAH) má multifaktoriální příčiny. Patogenetickými mechanizmy, které se podílejí na jejím rozvoji, jsou vazokonstrikce, cévní remodelace a trombózy in situ. Určení správné diagnózy a etiologie PAH je zásadní pro správné vedení léčby. Zavedením prostacyklinu do léčby idiopatické plicní hypertenze (IPAH) v posledních letech došlo k výraznému zlepšení prognózy nemocných tzv. primární plicní hypertenzí. Tato léčba zlepšuje toleranci fyzické zátěže. hemodynamiku i přežívání. Vedle farmakologické léčby se v posledních dvaceti lety pro nemocné s PAH rozvíjejí také intervenční a chirurgické postupy - perkutánní balónková atriální septostomie, transplantace plic, případně transplantace srdce - plíce. Plicní endarterektomie se stala akceptovaným výkonem u nemocných s chronickou tromboembolickou plicní hypertenzí (CTEPH). Klíčovou roli pro správný výběr nemocných k této operaci hraje stanovení diagnózy a klasifikace typu postižení plicních tepen pomocí plicní angiografie. Zatím bylo na světě provedeno necelých 3 000 těchto výkonů. Od září roku 2004 prodělalo tuto operaci (vůbec poprvé provedenou v České republice) na Klinice kardiovaskulární chirurgie VFN Praha úspěšně už celkem 6 nemocných. Kazuistiky dvou prvních nemocných budou v nejbližší době zveřejněny v časopise Cor et Vasa.
Klíčová slova:
chronická tromboembolická plicní hypertenze - plicní endarterektomieChronická tromboembolická plicní hypertenze (CTEPH) je často podhodnocené onemocnění, jehož skutečná incidence je vyšší než se obvykle uvádí. Odhaduje se, že až u 70 % nemocných, kteří prodělali akutní embolizaci do plic, není tato klinická diagnóza stanovena [1]. To je dáno tím, že řada těchto nemocných uvádí jako hlavní příznak pouze nespecifickou dušnost a případně únavu. V diferenciální diagnostice je nutné ji odlišit od jiných příčin plicní arteriální hypertenze (viz tab. 1). CTEPH je charakterizována intraluminárně organizovanými tromby, fibrózními stenózami a úplnými uzávěry jednotlivých větví plicnice. Ty jsou příčinou narůstajících tlaků v plicnici a zvýšení plicní cévní resistence, což postupně vede k progresivnímu pravostrannému selhání. K rozvoji CTEPH dochází pouze u 0,1 - 0,5 % pacientů, kteří přežili plicní embolii [2]. Jedna z teorií vysvětluje vznik tohoto postižení nedostatečnou spontánní fibrinolýzou plicních embolů. Hyperkoagulační stav lze identifikovat pouze u malého počtu případů [3,4].
Tab. 1. Dělení plicních hypertenzí. 
Klinický obraz
Základními příznaky jsou zejména narůstající dušnost a pokles funkční zdatnosti. Nepříliš často se objevuje anginózní bolest, příčinou je ischemie hypertrofické pravé komory a dilatace plicnice. Poměrně zřídka se objevuje hemoptýza. Při rozvoji pravostranné dekompenzace je možné vidět i hmatat pulzaci v prekordiu pod mečíkem a slyšíme akcentaci II. ozvy nad plicnicí, případně rozštěp II. ozvy nad plicnicí. Pokud dojde k dilataci kmene plicnice a regurgitaci krevního proudu do pravé komory, projeví se to diastolickým šelestem (šelest Grahama Steela). Při selhávání pravé komory se objevují otoky dolních končetin, zvětšená městnavá játra, je zvýšená žilní náplň krčních žil a objevuje se hepatojugulární reflux.
Diagnostika CTEPH
Anamnéza a fyzikální vyšetření může upozornit na zátěž nebo selhávání pravé komory. Většina nemocných přichází pro postupně narůstající dušnost, únavnost a nevýkonnost. Někteří z nich již udávají v anamnéze prodělanou trombózu žil dolních končetin s následnou embolizací do plic. Pokud embolizace do plic proběhla skrytě, je na sukcesivní embolizaci s následnou plicní hypertenzí pomýšleno málokdy. Rentgenové vyšetření pomáhá při diferenciální diagnóze PAH a usnadňuje interpretaci dalších vyšetření (např. scintigrafie plic). U plicní hypertenze dochází k rozšíření centrálních kmenů plicnice. Jeho šířka více než 17 mm u mužů a více než 15 mm u žen přispívá k diagnóze plicní hypertenze. Důležitější než jednorázové měření šířky trunku je jeho sledování. Pokud dojde k rozšíření o 3 mm a více, je pravděpodobné, že střední tlak v a. pulmonalis je vyšší než 30 mm Hg [5,6]. EKG známky významné plicní hypertenze stojí na kritériích hypertrofie a případně i zátěže pravé komory. Nejčastější EKG kritéria znaků hypertrofie PK uvádí tab. 2. Hypertrofie PK a deviace osy doprava je nalézáno až u 89 % těchto nemocných a může být prvním signálem, že se u nemocného jedná o PAH [7]. Vývoj EKG změn před a po prodělané PE u našich dvou nemocných, ukazují obr. 1 - 4.
Tab. 2. EKG známky hypertrofie a zátěže pravé komory 
Obr. 1, 2. EKG nemocných před provedením plicní endarterektomie. Jsou patrny všechny známky hypertrofie a zátěže pravé komory. 
Obr. 3, 4. EKG nemocných měsíc po provedení PEA. Ústup známek zátěže i hypertrofie pravé komory. 
Základní metody v diagnostickém algoritmu představují echokardiografie, plicní scintigrafie a pravostranná katetrizace.
Echokardiografie je u nemocných s obecně chronickou plicní hypertenzí klíčovým neinvazivním vyšetřením, proto je její metodika rozvedena podrobněji. Echokardiografie iniciálně umožňuje odlišit jedince, u kterých je s vysokou pravděpodobností přítomna plicní venózní hypertenze, dříve nazývaná postkapilární (těžká dysfunkce levé komory, pokročilá stadia chlopenních vad levého srdce) či plicní hypertenze v důsledku vrozené zkratové vady. Následný diagnostický postup se pak liší od pacientů s prekapilární plicní hypertenzí nejrůznější etiologie. Echokardiografické hodnocení pravého srdce přináší informace o velikosti a funkci pravostranných oddílů, především PK, o významnosti pulmonální a trikuspidální regurgitace a umožňuje se s poměrně vysokou přesností vyjádřit k tlakovým poměrům v plicnici a v pravé síni [8,9,10]. Chronická plicní hypertenze vede k dilataci pravostranných oddílů, hypertrofii PK, snížení systolické funkce PK a poruše jejího plnění. Za dilataci PK je považován její konečný diastolický rozměr v parasternální projekci větší než 30 mm, resp. zaujímá více než polovinu diastolického rozměru levé komory. V apikální projekci svědčí pro zvětšení pravostranných oddílů poměr jejich konečných diastolických rozměrů vůči levostranným nad 0,6. Tloušťku stěny PK hodnotíme v subkostální projekci, hypertrofie PK je definována hodnotou více než 5 mm. K posouzení systolické funkce PK jsou v klinické praxi pro jednoduchost nejčastěji používány dva přístupy. V apikální projekci lze pomocí jednorozměrné echokardiografie měřit exkurzi roviny trikuspidálního anulu během systoly (TAPSE - tricuspid annular plane systolic excursion), s normálními hodnotami nad 20 mm, těžká systolická dysfunkce PK je přítomna při hodnotách pod 15 mm [11]. Druhou možností je posouzení procentuální změny plochy PK v průběhu srdečního cyklu. Jedná se vlastně o planimetrickou obdobu měření ejekční frakce. Pro snížení systolické funkce PK svědčí hodnoty menší než 40 - 45 % [10]. Chronické tlakové přetížení PK vede k oploštění mezikomorové přepážky, které je při čistě tlakovém přetížení charakteristicky přítomno jak v systole, tak i v diastole. Tuto distorzi mezikomorového septa, která vede k typickému obrazu levé komory do varu písmene D (tzv. D-shape) lze hodnotit pomocí indexu excentricity v parasternální projekci na krátkou osu (obr. 5). Jedná se o poměr dvou příčných rozměrů levé komory. Za normálních podmínek má levá komora kruhovitý průřez a hodnota indexu je 1,0. U přetížení PK dochází v důsledku oploštění pohybu mezikomorového septa k jeho změně [10]. Alterace geometrie levé komory vede pravidelně k poruše její diastolické funkce, kterou posuzujeme pomocí dopplerovské echokardiografie s hodnocením transmitrálního průtoku a toku v plicních žilách. Obdobně posuzujeme i diastolickou funkci PK s měřením parametrů transtrikuspidálního průtoku a proudění jaterních žil. Pro značnou respirační variabilitu měřených veličin je však hodnocení diastolického plnění PK obtížné. K posouzení významnosti trikuspidální regurgitace je využíváno barevné dopplerovské mapování regurgitační trysky v apikální projekci. Hodnocena je nejčastěji plocha trysky, poměr její velikosti k ploše pravé síně, šíře regurgitačního proudění pod chlopní, tzv. vena contracta [12]. Za významnou trikuspidální regurgitaci je považována plocha regurgitační trysky nad 8 - 9 cm2, resp. poměr plochy regurgitace k ploše pravé síně nad 35 - 40 % a vena contracta nad 7 - 8 mm. Pulmonální regurgitaci hodnotíme také pomocí barevné dopplerovské echokardiografie, v parasternální projekci na krátkou osu.
Obr. 1. Oploštění mezikomorové přepážky (šipky) v důsledku chronického tlakového přetížení pravé komory (PK) vedoucí k typickému tvaru levé komory (LK) do podoby písmene D. 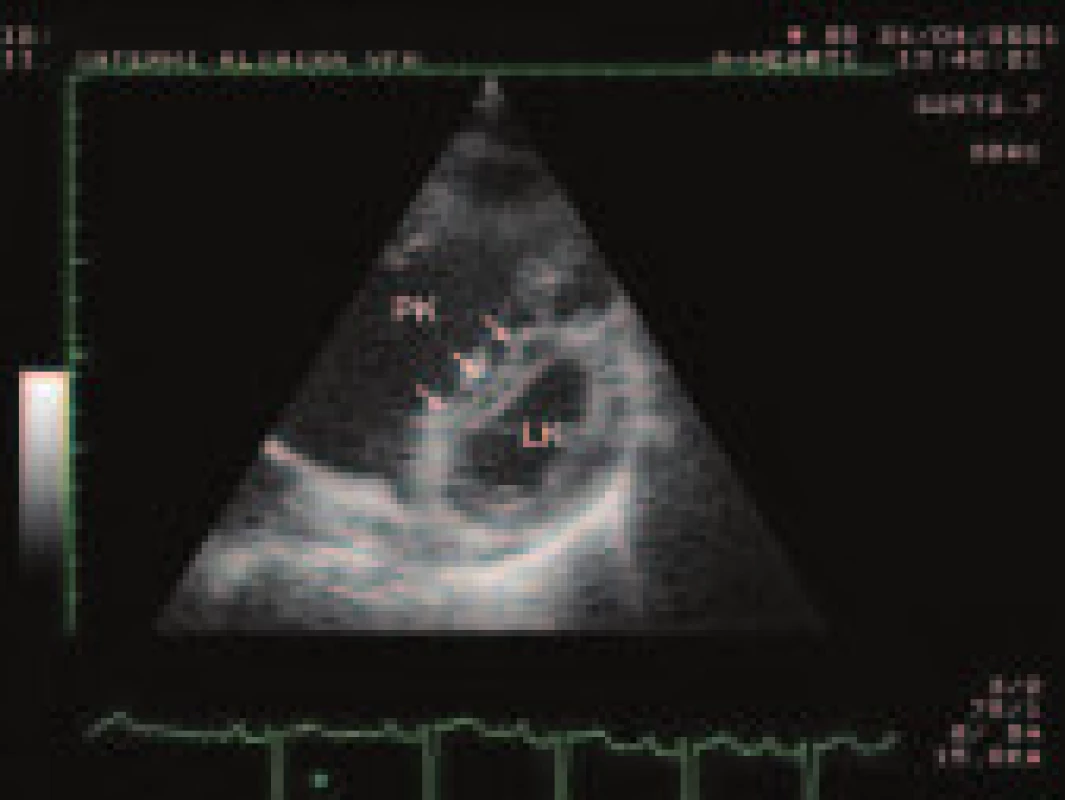
Dopplerovské vyšetření je klíčovým k posouzení přítomnosti zvýšené tenze v plicnici a v pravé síni. Nepřímou známkou hypertenze v plicnici je zkrácení akceleračního času proudění ve výtokovém traktu PK, tj. doby od jeho počátku k vrcholu, pod 100 ms. Přesněji se lze k tlakovým poměrům v plicnici vyjádřit na základě kontinuálního dopplerovského hodnocení vrcholového a telediastolického gradientu pulmonální regurgitace a především vrcholového gradientu regurgitace trikuspidální. Vrcholový gradient pulmonální regurgitace koreluje s středním tlakem v plicnici, telediastolický pak s tlakem telediastolickým [13] (obr. 6). Při odhadu obou tlaků je nutno ještě k naměřeným hodnotám gradientů přičíst odhadovaný tlak v pravé síni. Nejpřesnější dopplerovskou metodou k hodnocení tenze v plicnici je odhad systolického tlaku pomocí měření vrcholového gradientu trikuspidálního regurgitačního proudění [14] (obr. 7). Opět je nutno k naměřenému gradientu přičíst odhadnutý tlak v pravé síni. Tenzi v pravé síni odhadujeme pomocí měření rozměru dolní duté žíly a jeho respirační variace [15]. Rozměr duté žíly pod 20 mm s respirační variací nad 50 % svědčí pro normální hodnoty tlaku v pravé síni, naopak dilatace a absence respirační variability rozměru duté žíly ukazuje na přítomnost výrazné elevace tenze v pravé síni.
Obr. 2. Kontinuálně dopplerovský záznam pulmonální regurgitace s vyznačením vrcholového a telediastolického gradientu (šipky) 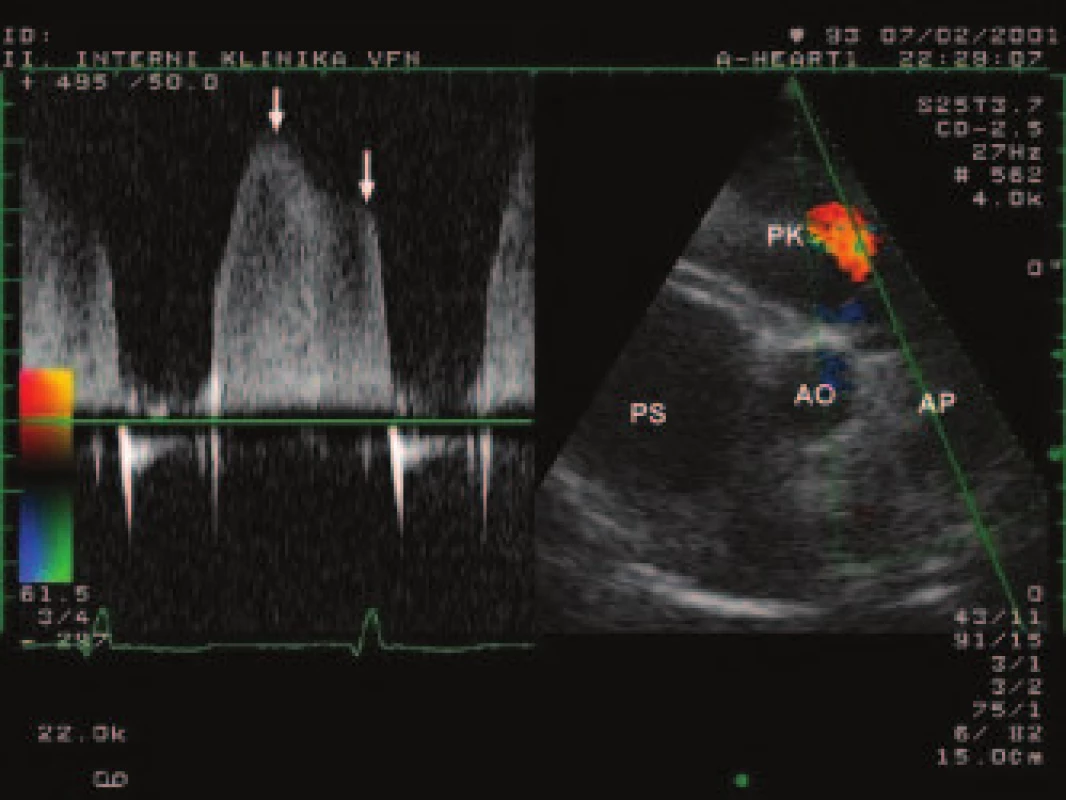
(AP – arteria pulmonalis, PK – pravá komora, PS – pravá síň, Ao – aorta). Obr. 3. Kontinuálně dopplerovský záznam trikuspidální regurgitace, vrcholový gradient (85 mm Hg) svědčí pro těžkou hypertenzi v plicnici 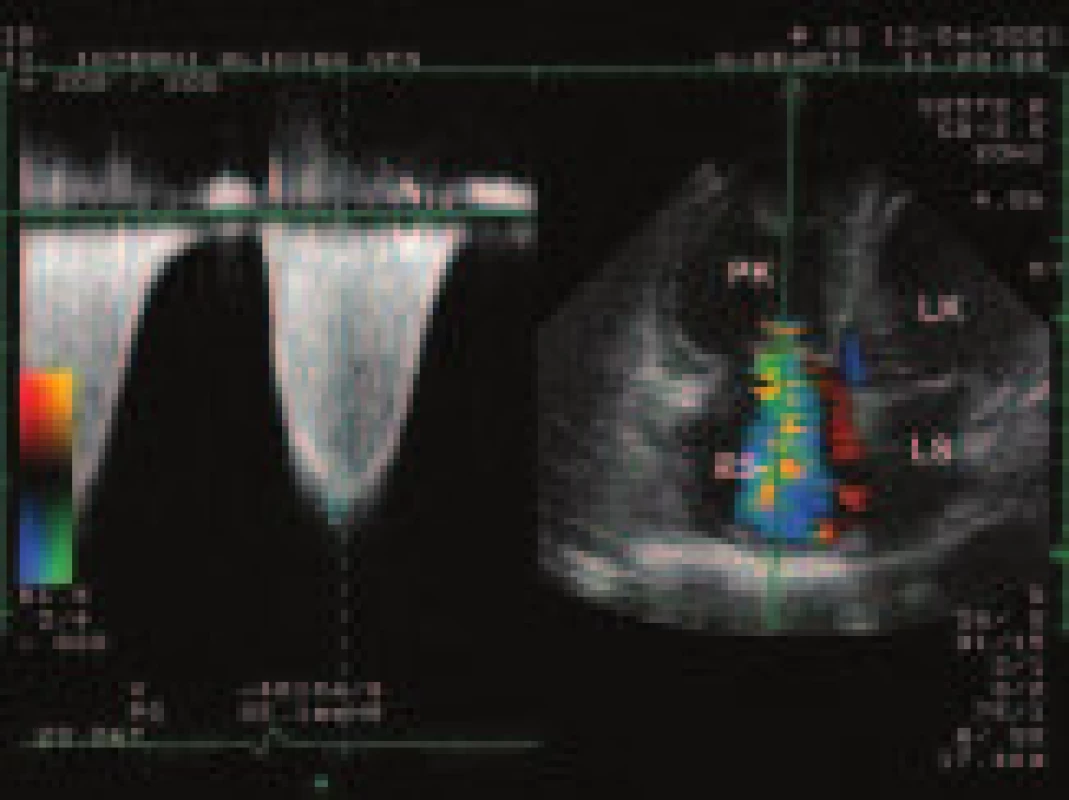
(PK – pravá komora, PS – pravá síň, LK – levá komora, LS – levá síň). Echokardiografie neumožňuje odlišit CTEPH od plicní arteriální hypertenze familiární či jiné etiologie. Práce japonských autorů naznačila možnost diferenciace těchto dvou patologií na základě tzv. indexu pulzatility, který je spočten jako podíl pulzního tlaku vůči systolickému tlaku v plicnici, kdy pro CTEPH by svědčily vyšší hodnoty tohoto indexu jakožto obraz nižších diastolických tlaků [16]. Prospektivní studie Ghia et al však neprokázala přínos echokardiografického hodnocení indexu pulzatility pro odlišení různých etiologií chronické plicní hypertenze [17]. Ojediněle lze u nemocných s CTEPH pomocí jícnové echokardiografie prokázat organizovaný trombus v kmeni plicnice a jeho hlavních větvích (obr. 8), jedná se však o nález nespecifický, neboť podobný obraz může být přítomen i u jedinců s plicní arteriální hypertenzí v důsledku poruchy funkce a struktury stěny plicnice.
Obr. 4. Organizovaný nástěnný trombus v pravé větvi plicnice, zobrazený pomocí jícnové echokardiografie 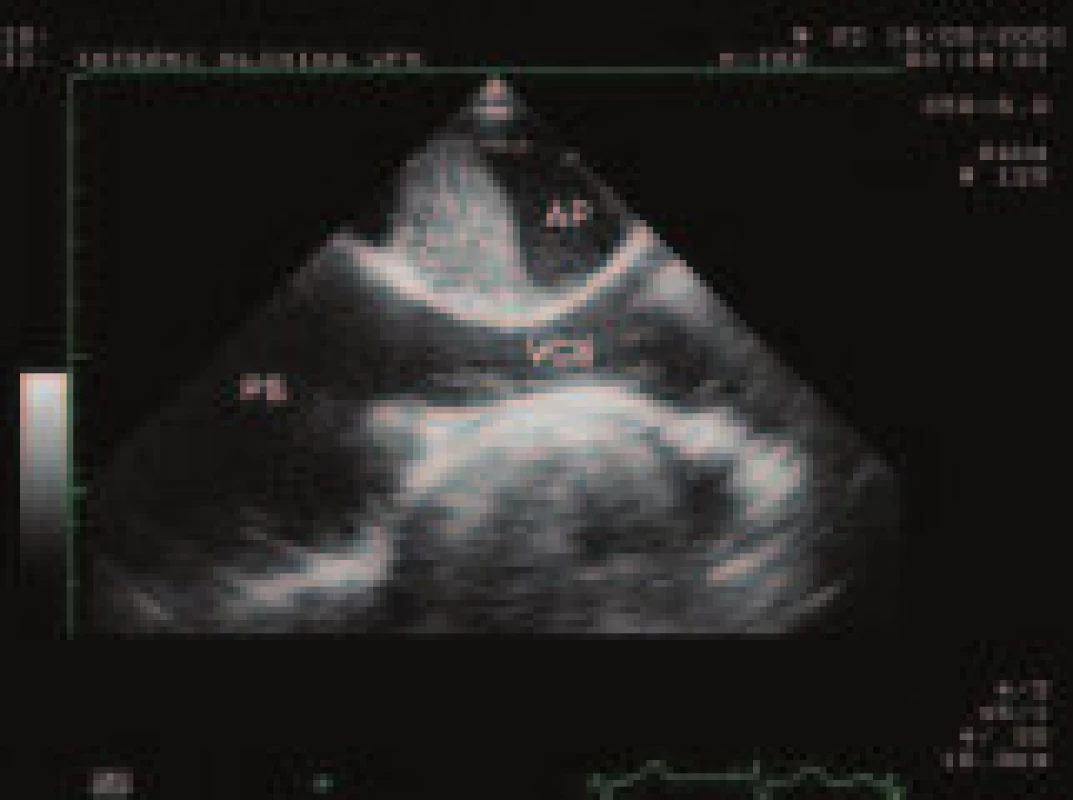
(AP – arteria pulmonalis, VCS – vena cava superior, PK – pravá komora). K určení lokalizace postižení jednotlivých větví plicnice slouží vysoce senzitivní počítačová tomografie (HRCT) a magnetická rezonance s podáním kontrastní látky. V Berginově studii [18] byla diagnóza chronické tromboembolické choroby diagnostikována pomocí CT s přesností 0,79 ve srovnání s plicní angiografií. S větší přesností než angiografie však stanoví jinou diagnózu vedoucí k PAH např. plicní arteriální sarkom nebo fibrózní mediastinitidu nebo intersticiální plicní proces. Pokud uvažujeme o operačním řešení, tedy o plicní endarterectomii, klíčovým vyšetřením se stává plicní angiografie [19], která jako jediná dokáže určit, zda je plicní obstrukce lokalizována v centrálních větvích plicnice nebo v jejich periferii.
Pravostranná katetrizace umožňuje změřit tlaky v pravé síni, v pravé komoře, v plicnici a tlak v zaklínění a vypočítat plicní vaskulární resistenci (PVR). Je tak možné odlišit prekapilární, postkapilární a hyperkinetickou plicní hypertenzi [20]. Pravostranná katetrizace je většinou u těchto nemocných doplněna vyšetřením kolaterálního bronchopulmonálního řečiště. Rozsáhlé bronchopulmonální kolaterály bývají vyvinuty u CTEPH, ale ne u idiopatické PAH. Toto vyšetření je proto jedno z mála, která dokážou tyto dvě odlišné formy PAH od sebe odlišit. Typické rozsáhlé bronchopulmonální kolaterály jsou ukázány na obr. 9. Normální hodnoty při pravostranné katetrizaci a hodnoty u dvou žen, které jako první prodělaly operaci, uvádí tab. 3.
Obr. 5. Bronchopulmonální kolaterály u nemocného s těžkou tromboembolickou chorobou. 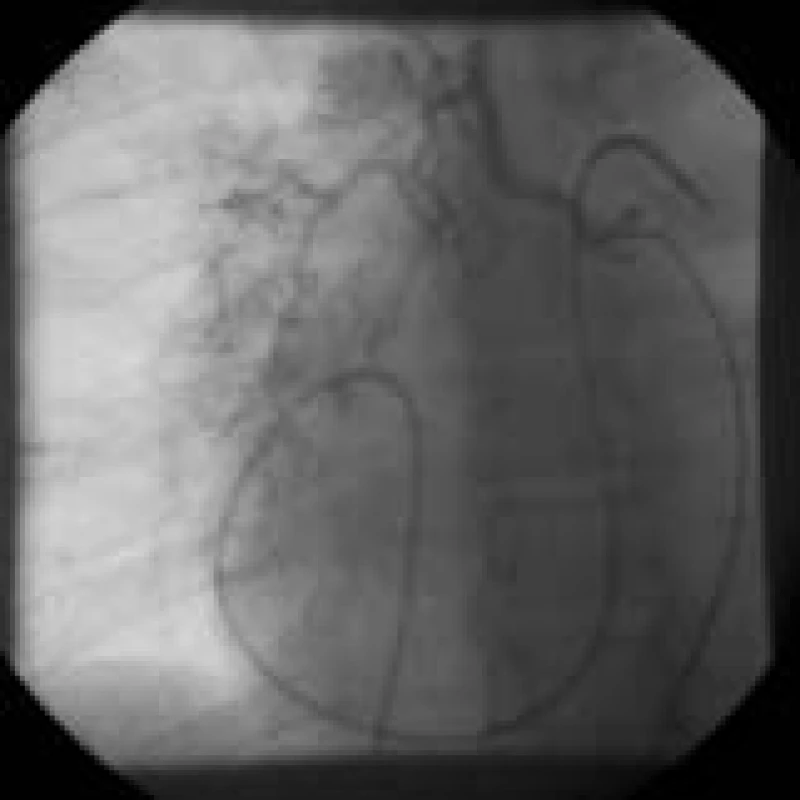
Tab. 3. Normální pravostranné tlaky a tlaky prvních nemocných s CTEPH před provedenou endarterectomií. 
Ventilačně-perfuzní scintigrafie plic. U nemocných vhodných k chirurgické léčbě je typickým nálezem nejméně jeden segmentální nebo i větší perfuzní defekt. Normální nález zpochybňuje diagnózu CTEPH [21].
Laboratorní vyšetření. Pomáhá vyloučit jiné příčiny PAH jako jsou vaskulitidy, infekci HIV, portální hypertenzi, systémová onemocnění. Stanovení Astrupa je důležitou informací oxygenace organizmu a kompenzace hypoxemie [22].
Farmakologická léčba CTEPH
Všem nemocným se doporučuje trvalá antikoagulační léčba, která vede ke zlepšení prognózy. Snižuje riziko dalších embolizací a také zabraňuje vzniku mikrotrombóz in situ v drobných plicních cévách. Pomáhá tak pozitivně ovlivnit probíhající remodelaci plicních cév, charakterizovanou poškozením endotelu, poruchami vazodilatačních, vazokonstrikčních a růstových faktorů a vytvářením novětvořených cévních útvarů, tzv. plexiformních lézí v plicní periferii a k trombózám in situ [23].
Dlouhodobá oxygenoterapie se používá u nemocných s plicní hypertenzí s hypoxemií, kteří mají v klidu PaO2 < 8 kPa. K indikaci je nutné provést kyslíkový test [24].
Diuretika zejména kličková, významným způsobem zlepšují symptomy v souvislosti s městnáním při srdečním selhání. Ke zlepšení prognózy však velmi pravděpodobně nevedou, protože nijak nezasahují do patogenetických mechanizmů. Při jejich dávkování je nezbytná opatrnost, snižují totiž předtížení pravé komory jako zásadní parametr určující minutový srdeční výdej. Zvyšují také viskozitu krve a tak potencují riziko tromboembolických komplikací.
Pozitivně inotropní látky. V současné době nemáme k dispozici přesvědčivá klinická data opravňující paušální podávání digoxinu u těchto nemocných. S výhodou jej používáme ke kontrole frekvence komor při fibrilaci síní při velmi pečlivé monitoraci hladin kalia. Dopamin a dobutamin může akutně zlepšit symptomy pravostranného selhávání, vliv na prognózu však znám není.
Analoga prostacyklinu (epoprostenol, treprostinil, illomedin a beraprost), která začala být podávána s velmi dobrým efektem u idiopatické primární plicní hypertenze, se u CTEPH teprve zkoušejí [25]. U nás však zatím v této indikaci nejsou pojišťovnami hrazeny stejně jako bosentan.
ACE-inhibitory. Předpokládá se, že malé dávky ACE-inhibitorů, které nevedou k systémové hypotenzi, mohou bránit proliferaci hladkých svalů a tak zpomalit progresi remodelace plicních cév. Prostřednictvím bradykininu zvyšují uvolňování prostacyklinu a NO. Jejich podávání je v současnosti ve fázi klinického zkoušení.
Intervenční a chirurgické a možnosti léčby
Perkutánní balónková atriální septostomie
Jedná se o invazivní terapeutickou metodu, při níž se katetrizačně vytvoří arteficiální pravolevý zkrat na úrovni mezisíňového septa. Hemodynamickým efektem je bezprostřední zvýšení minutového srdečního výdeje a redukce žilní kongesce spojená se zlepšením symptomatologie a snad i několikaměsíčním zlepšením prognózy, neovlivňuje však žádný z patogenetických mechanizmů vzniku plicní hypertenze. Výkon je navíc zatížen vysokou mortalitou. Je pouze mostem k transplantaci plic nebo k plicní endarterectomii a má svá přísná indikační kritéria [26,27,28]. Z této indikace byla atriální septostomie provedena poprvé v ČR na II. interní klinice VFN v Praze na podzim roku 2003.
Transplantace plic, transplantace srdce a plic
První transplantaci plic provedl J. Hardy v roce 1963 [29]. Po roce 1980 se stala základní efektivní léčbou u nemocných v terminálním stadiu plicní hypertenze po vyčerpání všech ostatních dostupných léčebných možností. V letech 1981 - 1998 bylo na celém světě provedeno více než 1 000 transplantací jedné nebo obou plic nebo srdce a plic. Od společné transplantace srdce a plic se ale ustupuje, protože se u nemocných s CTEPH prokázalo, že změny na pravém srdci jsou po poklesu tlaku v plicnici do 3 - 6 měsíců plně reverzibilní [30,31]. Nedostatek dárců rovněž přispívá k tomu, že se v současné době upřednostňuje transplantace pouze jedné nebo obou plic. Tento výkon je však provázen poměrně vysokou mortalitou, 16 - 29 %, která je dána závažností onemocnění. Jeden rok přežívá 65 - 75 % operovaných, pět let necelá polovina. Indikace a kontraindikace k provedení transplantace jsou shrnuty v tab. 4.
Tab. 4. Indikace a kontraindikace k transplantaci plic. 
Plicní endarterektomie (PEA)
Prognóza neléčených nemocných s CTEPH je závažná a závisí zejména na tíži plicní hypertenze. Pacienti se středním tlakem v plicnici vyšším jak 40 mm Hg přežívají 5 roků ve 30 %, pokud je střední tlak v plicnici vyšší než 50 mm Hg, je pětileté přežívání pouze 10 % [32].
Plicní endarterektomie (PEA) představuje potenciálně kurativní metodu pro pacienty s CTEPH, především při postižení centrálních větví plicnice. Principem operace není embolektomie, ale endarterektomie, tedy odstranění organizovaného fibrotizovaného trombu s částí cévní stěny plicnice (obr. 10). Výkon se provádění ze sternotomie v mimotělním oběhu a v hluboké hypotermii. Pro úspěch operace je nezbytná vizualizace distálních větví plicnice. U této operace tedy nestačí napojení nemocného na mimotělní oběh, protože kolaterálním řečištěm z bronchiálních tepen dochází k příliš velkému přívodu krve do plicních tepen znemožňující přehlednost v plicních tepnách. Proto se vlastní endarterektomie, která trvá 20 - 30 minut vpravo a 20 - 30 minut vlevo, provádí v kompletní cirkulační zástavě. Jako ochrana mozku slouží především hypotermie na 18 ºC [33]. Proto tato operace vyžaduje dokonalou spolupráci kardiologa, anesteziologa a operačního týmu.
Obr. 6. Endarterektomie – odstranění organizovaného fibrotizovaného trombu s částí cévní stěny plicnice. 
První úspěšnou PEA provedl v roce 1958 Synder et al [34]. Do roku 1976 bylo referováno pouze 18 operací s mortalitou 22 %. K většímu rozvoji došlo až v letech 1976 - 1984, kdy bylo provedeno 80 - 90 operací, mortalita ale zůstala stejně vysoká. Teprve v posledních dvaceti letech dochází celosvětově k výraznému nárůstu počtu operací, v současné době bylo odoperováno téměř 3000 těchto nemocných a s přibývajícími zkušenostmi došlo k poklesu mortality na 5 - 7 %. Největší počet výkonů s nejnižší mortalitou připadá na pracoviště v San Diegu [35,36] a v německém Mainzu [37]. Na obou těchto pracovištích byly odoperovány již stovky nemocných s CTEPH.
Klíčová kritéria pro výběr pacientů k operaci představuje funkční zdatnost, závažnost plicní hypertenze a chirurgická dostupnost trombotické obstrukce. Indikováni jsou nemocní ve funkční stadiu NYHA III a IV, kteří mají plicní vaskulární rezistenci vyšší jak 800 dyn.s.cm-5 (10 WU) [38,39]. Chirurgická dostupnost obstrukce závisí do jisté míry i na zkušenosti operačního týmu, technicky lze dosáhnout až úrovně subsegmentárních větví plicnice. Před operací je nezbytná nejméně tříměsíční účinná antikoagulační léčba.
K nejzávažnějším pooperačním komplikacím patří perzistující plicní hypertenze (při neadekvátní endarterektomii nebo nediagnostikovaném významném periferním postižení) a reperfuzní edém v endarterektomovaných oblastech plic. Antikoagulaci heparinem jako prevenci reokluze je nutno zahájit 4 - 8 hodin po výkonu, od 8. - 14. dne se pokračuje v perorální antikoagulaci warfarinem. Dlouhodobá antikoagulační léčba po operaci je všeobecně akceptovaným standardem, některá pracoviště rovněž implantují kavální filtr [40].
Mortalita PEA se pohybuje v rozmezí 5 - 24 % a výrazně závisí na zkušenostech pracoviště. Úspěšná operace vede v důsledku signifikantního poklesu PVR ke zlepšení funkční zdatnosti, zvýšení srdečního výdeje, zlepšení funkce pravé komory a ke zmenšení nebo i vymizení sekundární trikuspidální regurgitace. Pětileté přežívání po PEA se pohybuje mezi 75 - 80 %. Výsledky jsou podstatně povzbudivější než u farmakoterapie nebo u transplantace plic [41].
U pacientů s CTEPH, kteří nejsou kandidáty chirurgické léčby, může alternativu představovat farmakoterapie (prostacyklin, bosentan, sildenafil), perkutánní balónková atriální septostomie, která již byla provedena i v ČR [42] nebo transplantace plic. Rozsáhlejší zkušenosti však scházejí [43].
Závěr
CTEPH je relativně vzácné onemocnění. Představuje jeden z mála typů chronické plicní hypertenze, který lze úspěšně vyléčit chirurgicky. Klíčovým problémem je správná diagnostika, jejímž cílem je určit typ plicní hypertenze a v případě průkazu CTEPH stanovit lokalizaci postižení. Samozřejmostí je interdisciplinární spolupráce kardiochirurga, intenzivisty, kardiologa a radiologa, optimálně ve specializovaném centru s komplexními zkušenostmi s problematikou plicní hypertenze. To je většinou možné jen při soustředění péče o tyto nemocné do specializovaného centra, které má dostatek zkušeností se srdečními katetrizacemi, testováním plicní vazoaktivity a s vedením terapie jak konvenčními přípravky tak léky, které se teprve objevují na našem trhu. Projekt PEA v České republice vznikl a je rozvíjen v rámci Kardiocentra VFN II. chirurgickou klinikou kardiovaskulární chirurgie VFN ve spolupráci s prof. dr. Mayerem z Mainzu a s Centrem pro plicní hypertenzi na II. interní klinice VFN. V České republice lze očekávat přibližně 5 - 10 vhodných kandidátů pro PEA ročně, zatím bylo úspěšně odoperováno prvních 6 pacientů. Komplikovaní nemocní mohou být operováni na spolupracujícím německém pracovišti v Mainzu.
MUDr. Marcela Škvařilová, Ph.D.
www.vfn.cz
e-mail: marcela.skvarilova@centrum.cz
Doručeno do redakce: 14. 12. 2004
Přijato po recenzi: 12. 4. 2005
Zdroje
1. Pineda LA, Hathwar VS, Grant BJ. Clinical suspection of fatal pulmonary embolism. Chest 2001; 120 : 791-795.
2. Rich S, Levitsky S, Brundage BH. Pulmonary hypertension from chronic thromboembolism. Ann Intern Med 1988; 108 : 425-434.
3. Jansa P, Aschermann M, Linhart A. Primární plicní hypertenze. Nakladatelství Target MD 2003.
4. Martinuzzo ME, Pombo G, Azarian R et al. Lupus anticoagulant, high level of anticardiolipin, and anti-β2-glykoprotein I antibodies are associated with chronic thromboembolic pulmonary hypertension. J Rheumatol 1998; 25 : 1313-1319.
5. Lupi E, Dumont C, Tejada VM et al. A radiologic index of pulmonary arterial hypertension. Chest 1975; 68 : 28-31.
6. Rich S, Dantzker DR, Ayres SM et al. Primary pulmonary hypertension: a national prospective study. Ann Intern Med 1987; 107 : 216-223.
7. Bossone E, Paciocco G, Iarussi D et al. The prognostic role of the ECG in primary pulmonary hypertension. Chest 2002; 121 : 513-518.
8. Linhart A, Paleček T, Aschermann M. Echokardiografie pro praxi. Praha: Audioscan 2002.
9. Sahn DJ, DeMaria A, Kisslo J et al. Recommendations regarding quantitation in M-mode echocardiography: results of a survey of echocardiographic measurements. Circulation 1978; 58 : 1072-1083.
10. Daniels LB, Krummen DE, Blanchard DG. Echocardiography in pulmonary vascular disease. Cardiol Clin 2004; 22 : 383-399.
11. Kaul S, Tei C, Hopkins JM et al. Assessment of right ventricular function using two-dimensional echocardiography. Am Heart J 1984; 107 : 526-531.
12. Shapira Y, Porter A, Wurzel M et al. Evaluation of tricuspid regurgitation severity: echocardiographic and clinical correlation. J Am Soc Echocardiogr 1998; 11 : 652-659.
13. Masuyama T, Kodama K, Kitabatake A et al. Continuous-wave Doppler echocardiographic detection of pulmonary regurgitation and its application to noninvasive estimation of pulmonary artery pressure. Circulation 1986; 74 : 484-492.
14. Yock PG, Popp RL. Noninvasive estimation of right ventricular systolic pressure by Doppler ultrasound in patients with tricuspid regurgitation. Circulation 1984; 70 : 657-662.
15. Kircher BJ, Himelman RB, Schiller NB. Noninvasive estimation of right atrial pressure from the inspiratory collapse of the inferior vena cava. Am J Cardiol 1990; 66 : 493-496.
16. Nakayama Y, Sugimachi M, Nakanishi N et al. Noninvasive differential diagnosis between chronic pulmonary thromboembolism and primary pulmonary hypertension by means of Doppler ultrasound measurement. J Am Coll Cardiol 1998; 31 : 1367-1371.
17. Ghio S, Raineri C, Scelsi L et al. Usefulness and limits of transthoracic echocardiography in the evaluation of patients with primary and chronic thromboembolic pulmonary hypertension. J Am Soc Echocardiogr 2002; 15 : 1374-1380.
18. Bergin CJ, Haudchildt J, Rios G et al. Accuracy of MR angiography compared with radionuclide scanning in identifying the cause of pulmonary arterial hypertension. Am J Roentgenol 1997; 168 : 1549-1555.
19. Hull RD, Hirsch J, Carter CJ et al. Pulmonary angiography, ventilation lung scanning, and venography for clinically suspected pulmonary embolism with abnormal perfusion lung scan. Ann Intern Med 1983; 98 : 891-899.
20. Rich S, D´Alonzo GE, Dantzker et al. Magnitude and implications of spontaneous hemodynamic variability in primary pulmonary hypertension. Am J Cardiol 1985; 55 : 159-163.
21. D´Alonzo GE, Bower JS, Dantzker DR. Differentiation of patients with primary and trombembolic pulmonary hypertension. Chest 1984; 85 : 457-461.
22. Nagaya N, Nishikimi T, Okano Y et al. Plasma brain natriuretic peptide levels increase in portion to the extent of right ventricular dysfunction in pulmonary hypertension. J Am Cardiol 1998; 31 : 202-208.
23. Ogata M, Ohe M, Shirato K et al. Effects off a combination therapy of anticoagulant and vasodilator on the long-term prognosis of primary pulmonary hypertension. Jpc Circ J 1993; 57 : 63-69.
24. Weitzenblum E, Sautegeau A, Ehrhart M et al. Long-term oxygen therapy can reverse the progression of pulmonary hypertension in patients with chronic obstructive pulmonary disease. Am Rev Resp Dis 1985; 131 : 493-498.
25. Barst RJ, Rubin LJ, Long WA et al. A comparison of continuous intravenous epoprostenol (prostacyklin) with convential therapy for primary pulmonary hypertension. N Enng J Med 1996; 334 : 296-301.
26. Sandaloval J, Gaspar J, Pulido T et al. Graded balloon dilatation atrial septostomy in severe primary pulmonary hypertension: a therapeutic alternative for patients nonresposive to vasodilatator treatment. J Am Coll Cardiol 1998; 32 : 297-304.
27. Nehill MR, O´Laughlin MP, Mullins CE. Effects of atrial septostomy in patients with terminal cor pulmonale due to pulmonary vascular disease. Cathet Cardiovasc Diagn 1991; 24 : 166-172.
28. Kothari SS, Yusuf A, Juneja R et al. Graded balloon dilatation atrial septostomy in severe primary pulmonary hypertension. Indian Heart J 2002; 54 : 164-169.
29. Lischke R, Šimonek J, Stolz A et al. Transplantac plic u primární plicní hypertenze. Vnitř Lék 2004; 50 : 695-697.
30. Doyle RL, McCrory D, Channick RN et al. Surgical treatments/interventions for pulmonary arterial hypertension. Chest 2004; 126 : 63S-71S.
31. ASTP, ATS, ERS, ISHLT Joint statement international guidelines for the selection of lung transplant patients. Am J Respir Crit Care Med 1998; 158 : 335-339.
32. Archibald CJ, Auger WR, Fedullo PF et al. Long-term outcome after pulmonary thromboendarterectomy. Am J Respir Critic Care 1999; 160 : 523-528.
33. Ando M, Okita Y, Tagusari O et al. Surgical treatment for chronic thromboembolic pulmonary hypertension under profound hypotermia and circulatory arest in 24 patients. J Card Surg 1996; 14 : 377-385.
34. Synder WH, Kent DC, Baesch BF et al. Successful endarterectomy of chronically occluded pulmonary artery; clinical report and physiologic. J Thorac Surg 1964; 45 : 482.
35. Jamieson SW, Kapelanski DP, Sakakibara N et al. Pulmonary thromboendarterectomy. Experience and results in 1,500 cases. Ann Thorac Surg 2003; 76 : 1457-1464.
36. Jamieson SW, Auger WR, Cedulko PF et al. Experience and results with 150 pulmonary thromboendarterectomy operations over a 29-month period. J Thorac Cardiovasc Surg 1993; 106 : 116-127.
37. Mayer E, Dahm M, Hake U et al. Mid-term results of pulmonary thromboendarterectomy for chronic thromboembolic pulmonary hypertension. Ann Thorac Surg 1996; 62 : 1788-1792.
38. Lewcuzuk J, Piszko P, Jagas J et al. Prognostic factors in medically treated patients with chronic pulmonary embolism. Chest 2001; 119 : 818-823.
39. Thistlethwaite PA, Mo A, Madami MM et al. Operative classification of thromboembolic disease determines outcome after pulmonary endarterectomy. J Thorac Cardiovasc Surg 2002; 124 : 1203-1211.
40. Kim NHS, Fesler P, Channick RN et al. Preoperative partitioning of pulmonary vascular resistence correlates with early outcome after thromboendarterectomy for chronic thromboembolic pulmonary hypertension. Circulation 2004; 109 : 18-22.
41. Klepetko W, Mayer E, Sandoval J et al. Interventional and surgical modalities of treatment for pulmonary arterial hypertension. J Am Coll Cardiol 2004; 43 : 73S-80S.
42. Jansa P, Aschermann M, Riedel M. Doporučení pro diagnostiku a léčbu plicní arteriální hypertenze v ČR. Vnitř Lék 2004; 50 : 698-708.
43. McLaughlin VV, Presberg KW, Doyle RL et al. Prognosis of pulmonary arterial hypertension, ACCP Evidence-based Clinical Practice Guidelines. Chest 2004; 126 : 78S-92S
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2005 Číslo 11- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Stanovení monoklonálních imunoglobulinů a jejich fragmentů u monoklonálních gamapatií - editorial
- Prolaktin - významný činitel vztahu mezi neuroendokrinním a imunitním systémem člověka - editorial
- Diabetes mellitus 1. typu a autoimunita - editorial
-
Incizionální a neincizionální síňové makroreentry tachykardie u dospělých pacientů
Příčiny, principy mapování a dlouhodobé výsledky katétrové ablace - Význam sérových hladin volných lehkých řetězců imunoglobulinu v diagnostice a hodnocení aktivity mnohočetného myelomu a vybraných monoklonálních gamapatií
- Vzťah medzi hodnotami prolaktínu a mierou funkčnej neschopnosti hodnotenej dotazníkom HAQ u pacientov s reumatoidnou artritídou
- Rizikové faktory ovlivňující přežívání pacientů s implantabilními kardiovertery-defibriátory
- Vplyv skrátenia pasívnej fázy na diagnostickú výťažnosť nitroglycerínom stimulovaného head-up tilt testu
- Regresné rovnice pre interval QT a QTc elektrokardiogramu
- Nové možnosti léčby chronické tromboembolické plicní hypertenze v České republice
- Diabetes mellitus 1. typu a autoimunita
- Neobvyklá komplikace po aortokoronárním bypassu: akutní cholestatická hepatitida a agranulocytóza indukovaná tiklopidinem a simvastatinem u pacienta s alergií na salicyláty
-
Diagnostika a léčba chronické hepatitidy C
Doporučený postup České hepatologické společnosti a Společnosti infekčního lékařství České lékařské společnosti J. E. Purkyně - První zkušenosti s léčbou chronické hepatitidy C PegIntronem a Rebetolem v České republice
- Doc. MUDr. Ilja Topinka, CSc. osmdesátiletý
- Zamyšlení nad půlstoletím interní medicíny v Baťově nemocnici
- Východoslovenské lekárske dni v Novom Smokovci vo Vysokých Tatrách v rokoch 1991–2003
- Kongres EFIM 2005 očima mladého internisty
- Z odborné literatury
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Regresné rovnice pre interval QT a QTc elektrokardiogramu
- Neobvyklá komplikace po aortokoronárním bypassu: akutní cholestatická hepatitida a agranulocytóza indukovaná tiklopidinem a simvastatinem u pacienta s alergií na salicyláty
- Diabetes mellitus 1. typu a autoimunita
- Doc. MUDr. Ilja Topinka, CSc. osmdesátiletý
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy





