-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Lokální cévní komplikace u pacientů s akutním infarktem myokardu řešeným direktní perkutánní koronární intervencí
Vascular complications after direct percutaneous coronary interventions
Objectives:
We assessed the rate and identified risk factors for postprocedure vascular complications following direct percutaneous intervention (dPCI).Methods:
Data were collected on 881 consecutive patients who underwent dPCI in our cath-lab from January 2002 to December 2003. Multivariate regression was used to identify characteristics associated with vascular complications.Results:
Out of 881 patients, hematoma was found in 148 (16,8 %) cases. Pseudoaneurysm was detected by ultrasound in 40 (4,5 %) patients, 5 (0,6 %) patients underwent surgery. Variables associated with increased risk included age, female sex, low body mass index (BMI) and body surface area (BSA) and presence of diabetes mellitus.Conclusions:
Predicting the risk of post-PCI vascular complications is feasible. This information may be useful for clinical decision-making and institutional efforts at quality improvement.Key words:
pseudoaneurysm - direct percutaneous coronary intervention - myocardial infarction
Autoři: M. Orban 1; O. Hlinomaz 1; F. Lehar 1; M. Rezek 1; M. Eisenberger 1; Z. Konečný 2; L. Groch 1
Působiště autorů: I. interní kardio-angiologická klinika Lékařské fakulty MU a FN u sv. Anny, Brno, přednosta prof. MUDr. Jiří Vítovec, CSc., FESC 1; II. chirurgická klinika Lékařské fakulty MU a FN u sv. Anny, Brno, přednosta doc. MUDr. Jindřich Leypold, CSc. 2
Vyšlo v časopise: Vnitř Lék 2006; 52(1): 51-56
Kategorie: Původní práce
Souhrn
Cíl:
Hodnotili jsme výskyt lokálních cévních komplikací u pacientů s akutním infarktem myokardu řešeným direktní perkutánní intervencí (dPCI) s následnou manuální kompresí při vytažení cévky a závislost na definovaných charakteristikách pacientů (věk, pohlaví, body mass index - BMI, plocha povrchu těla - BSA, diabetes mellitus - DM, použité instrumentarium).Soubor pacientů a metodika:
Retrospektivně jsme zhodnotili celkem 881 konsekutivních pacientů (683 mužů) hospitalizovaných našem pracovišti od 1. 1. 2002 do 31. 12. 2003. Cévka byla po úspěšné dPCI vytažena s následnou manuální kompresí. Hodnotili jsme četnost výskytu cévních komplikací a provedli korelace mezi výskytem významnějších komplikací a definovanými charakteristikami pacientů.Výsledky:
Z celkového počtu 881 pacientů byl plošný hematom zjištěn u 148 (16,8 %), UZ třísla pro zjištěnou hmatnou rezistenci nebo šelest byl proveden v 98 (11,1 %) případech, pseudoaneuryzma bylo detekováno u 40 (4,5 %), chirurgické konzilium bylo indikováno u 17 (1,9 %) pacientů, u 5 (0,6 %) bylo potřeba provést chirurgický výkon. S četností komplikací statisticky významně korelovaly věk, ženské pohlaví, přítomnost DM a nízká hodnota BSA i BMI.Závěr:
Četnost cévních komplikací po dPCI s manuální kompresí odpovídá údajům z jiných odborných zdrojů. Cílem je snížení jejich výskytu přes narůstající počet rizikových pacientů. Novější přístupy mechanické komprese nebo lokálního ošetření cévní stěny slibují další snížení počtu lokálních komplikací. Nadějnou alternativou k operačnímu řešení je v některých případech uzávěr dutin pseudoaneuryzmat použitím tkáňových lepidel.Klíčová slova:
pseudoaneuryzma - direktní perkutánní koronární intervence - infarkt myokarduÚvod
Metodou volby v léčbě akutního infarktu myokardu (AIM) je v nemocniční fázi terapie urgentní koronarografií s následnou primární (direktní) perkutánní koronární intervencí (dPCI). Ve většině případů je v průběhu dPCI do ošetřeného místa koronární tepny implantovaný stent. Výkon se provádí punkční technikou dle Seldingera. Místem přístupu bývá většinou arteria femoralis, vzácněji arteria radialis, zcela výjimečně arteria axillaris nebo brachialis. Velikost použitého instrumentaria se udává v jednotkách french (F) a číselná hodnota představuje délku obvodu katétru v milimetrech. Kupříkladu katétr velikosti 6 F má obvod 6 mm a průměr je 1,91 mm. K dPCI se většinou používá instrumentarium velikosti 6 nebo 7 F, v případě zavedení mechanické podpory oběhu pomoci intraarteriální balonkové kontrapulzace (IABC) je použito až 9 F instrumentarium. Vzhledem k účinné antikoagulační a antiagregační léčbě podávané v průběhu přednemocniční fáze léčby a v průběhu výkonu, které slouží k prevenci akutní trombózy stentu a záchování integrity mikrocirkulace, se cévka po zákroku většinou nechává několik hodin v místě intervence. Poté následuje její vytažení s následnou kompresí. Komplikacemi, které mohou vzniknout v místě punkce, jsou hematom, někdy i s větší ztrátou krve, pseudoaneuryzma, arteriovenózní píštěl. Jejich vznik se uvádí u 1 % - 14 % pacientů [1].
V naší práci jsme hodnotili výskyt cévních komplikací u pacientů s akutním infarktem myokardu řešeným direktní PCI s následnou manuální kompresí po vytažení cévky a zjišťovali závislost mezi četností lokálních komplikací v místě intervence a rizikovými faktory: věk, pohlaví, plocha povrchu těla (BSA), body mass index (BMI), diabetes mellitus (DM), velikost použitého instrumentaria, intenzifikovaná antiagregační léčba (IIb-IIIa blokátory). Tyto komplikace zatěžují pacienta (opětovná komprese třísla, krevní transfuze, chirurgické řešení) a prodlužují dobu hospitalizace, proto je potřeba hledat nové přístupy vedoucí k omezení jejich výskytu na minimum. Jednou z možností je i selekce rizikových pacientů, u kterých lze použít moderní způsoby uzávěru tepny v místě koronární intervence.
Soubor pacientů a metody
Retrospektivně jsme zhodnotili skupinu 881 konsekutivních pacientů hospitalizovaných na koronární jednotce od 1. ledna 2002 do 31. prosince 2003 s diagnózou akutního infarktu myokardu (IM), který byl řešen pomocí dPCI provedené cestou arteria femoralis. Všichni pacienti byli léčeni intenzivní antiagregační a antikoagulační terapií dle algoritmu, který na našem pracovišti zahrnuje kyselinu acetylsalicylovou 100 mg denně, klopidogrel 75 mg denně po nasycovací dávce 300 mg při přijetí, 5000 - 10000 UI heparinu i.v. před intervencí s eventuelní další periprocedurální úpravou dávky dle hodnoty ACT (terapeutické rozmezí 250 - 300 s). U všech pacientů po dPCI byl první 2 dny hospitalizace podkožně podáván nízkomolekulární heparin (enoxaparin) dle hmotnosti pacienta v dávce 1 mg/kg po 12 hodinách. V případech podezření na přítomnost trombů v infarktové tepně nebo při podezření na periferní embolizaci trombotických hmot při intervenci byla medikace doplněna blokátorem IIb-IIIa receptorů trombocytů (abciximab nebo eptifibatid) podávaných infuzní formou. Pacienti, u kterých nebylo z jakéhokoliv důvodu možné dodržet tento terapeutický postup, nebyli zařazení do hodnocení. Cévka byla ze stehenní tepny vytažena 3 hodiny po výkonu s následnou manuální kompresí po dobu nejméně 15 minut. Poté byl naložen tlakový obvaz na dobu minimálně 12 hodin. Výjimkou byli pacienti v kardiogenním šoku s nutností podpory oběhu pomocí IABC, u kterých byla cévka vytažena společně s kontrapulzačním katétrem po stabilizaci stavu. V průběhu hospitalizace bylo tříslo u všech pacientů po dPCI a kompresi místa intervence průběžně kontrolováno a opakovaně pečlivě fyzikálně vyšetřeno palpaci a auskultací. Při podezření na vznik pseudoaneuryzmatu (pulzující rezistence v místě vpichu nebo přítomnost šelestu) bylo provedeno ultrazvukové duplexní vyšetření. V případě průkazu pseudoaneuryzmatu se označené místo opět komprimovalo a při trvání nálezu následovalo chirurgické konzilium, při kterém bylo zváženo operační řešení. U 24 pacientů vyžadoval jejich klinický stav zavedení intraaortální balonkové kontrapulzace (IABK), u které je potřeba zavedení silnějšího instrumentaria (9 Fr).
Data byla získána z propouštěcích zpráv, nemocničního informačního systému a sesterské dokumentace. Vznik komplikací jsme sledovali v průběhu celé hospitalizace - po čas pobytu na koronární jednotce (KJ) i na standardním oddělení. Hodnotili jsme četnost výskytu těchto lokálních cévních komplikací: plošného hematomu v místě punkce, pseudoaneuryzmatu ověřeného ultrazvukovým (UZ) vyšetřením, řešeného konzervativně nebo chirurgicky. Byly provedeny korelace mezi výskytem pseudoaneuryzmat a těmito definovanými charakteristikami pacientů: věkem, pohlavím, plochou povrchu těla (BSA), body mass indexem (BMI), přítomností diabetes mellitus (DM), velikostí použitého instrumentaria, použitím intenzifikované antiagregační léčby (IIb-IIIa blokátory). Ke stanovení BSA a BMI byly použity tyto vzorce: BSA = 0,20247 x výška (m)0,725 x váha (kg)0,425, BMI = váha pacienta (kg)/výška pacienta (m)2. Ke statickému vyhodnocení byly použity metody χ2 a Mannův-Whitneyův test.
Výsledky
Základní charakteristika souboru pacientů je uvedena v tab. 1. Průměrný věk nemocných byl 65,7 let, z 881 pacientů bylo 638 (72 %) mužů. Po revaskularizaci pomocí dPCI byla průměrná délka hospitalizace na KJ 50 hodin. Infarktovou tepnou byla ACD u 340 (39 %) pacientů, RIA u 389 (44 %) a RC u 145 (16 %) nemocných. V 7 případech bylo příčinou akutního IM postižení kmene levé věnčité tepny (ACS). Úspěšné obnovení průtoku postiženou tepnou hodnocené pomocí toku infarktovou tepnou po dPCI (TIMI flow III) bylo provedeno v 817 (92,7 %) případech. Celkem 223 (25 %) nemocných mělo při propuštění stanovenou diagnózu diabetes mellitus.
Zjistili jsme, že z celkového počtu 881 pacientů bylo bez lokální komplikace v místě intervence 733 (83,2 %) pacientů, u 148 pacientů (16,8 %) byl zjištěn plošný hematom. Ultrazvukové vyšetření třísla pro hmatnou rezistenci nebo šelest bylo provedeno v 98 (11,1 %) případech, pseudoaneuryzma bylo detekováno ve 40 (4,5 %) případech, chirurgické konzilium následovalo u 17 (1,9 %) pacientů, u 5 (0,57 %) z nich byl indikován chirurgický výkon (graf 1). U 5 pacientů došlo k výraznému poklesu v krevním obrazu, který vyžadoval krevní transfuzi. S četností výskytu pseudoaneuryzmat statisticky významně korelovaly vzrůstající věk (p < 0,02, graf 2), ženské pohlaví (p < 0,0001) a přítomnost DM (p < 0,007). U pacientů s výrazně sníženým BMI (pod 20) byl zjištěn statisticky významný nárůst četnosti pseudoaneuryzmat (p < 0,007), s narůstajícím BMI (nad 30) bylo spojeno zvýšení výskytu komplikace, které ovšem nedosáhlo statistické významnosti (graf 3). Jak je patrné z grafu 4, podobných výsledků bylo dosaženo hodnocením plochy povrchu těla, pacienti s BSA < 1,6 měli významně vyšší četnost výskytu pseudoaneuryzmat (p < 0,15). Velikost použitého instrumentaria (6 F, 7 F a 9 F) ani intenzivnější režim antiagregační léčby (abciximab, eptifibatid) nebyly statisticky významně spojeny s výskytem komplikací (tab. 2).
Diskuse
Četnost cévních komplikací po PCI, jak byla hodnocena v různých studiích, záleží na přesné definici. Některé studie zahrnuly všechny lokální komplikace (hematomy, pseudoaneuryzmata, arteriovenózní píštěle), jiné jenom ty, které vyžadovaly léčebný zásah [2,3,4]. Většina studií hodnotí výskyt lokálních komplikací po provedení převážně elektivních PCI a jejich četnost uvádí v rozmezí 2,6 % - 6,6 % [1,5,6]. Vzhledem k faktu, že v našem souboru jsou zahrnuti výhradně pacienti s akutním infarktem myokardu řešeným dPCI a s následnou intenzivní antiagregační a antikoagulační léčbou, která zvyšuje riziko krvácivých komplikací, považujeme naše výsledky (4,5 %) za velmi uspokojivé [7]. Rovněž jsme potvrdili, že většina pseudoaneuryzmat trombotizuje při následné cílené kompresi pod UZ kontrolou, proto jen malý počet pacientů se musel podrobit chirurgickému řešení (0,6 %).
V souladu s výsledky několika podobných prací jsme i my prokázali, že vyšší věk, ženské pohlaví a nižší BMI byly spojeny s vyšším rizikem cévních komplikací [1,3,4,6]. V případě hodnocení významu souvislosti nižšího BMI s četností pseudoaneuryzmatu je jistým omezením nízký počet pacientů v této skupině, proto jsme soubor pacientů rozdělili i podle hodnoty BSA a potvrdili vyšší četnost pseudoaneurysmat u pacientů s nízkou hodnotou BSA. Na rozdíl od výsledků některých jiných publikací, byla přítomnost DM u pacientů zahrnutých do naší studie hodnocena jako rizikový faktor, co se jeví celkem logické vzhledem k postižení cévní stěny a zhoršenému procesu hojení tkání u diabetiků. Vztah mezi použitím inhibitorů receptorů IIb/IIIa a četností lokálních komplikací, včetně krvácení z místa intervence, hodnotilo několik studií s rozdílnými výsledky [8,9,10]. V naší práci jsme podobně jak novější publikace neprokázali souvislost mezi aplikací těchto preparátu a vznikem pseudoaneuryzmatu [11].
Výsledky naší práce jsou limitovány faktem, že data byla hodnocena retrospektivně. Duplexní UZ vyšetření bylo provedeno rutinně jedním vyšetřujícím a hodnocení velikosti pseudoaneuryzmatu bylo zatíženo subjektivní chybou. Cílem práce nebylo posuzovat samotnou velikost útvaru, ale četnost a okolnosti vzniku. Výhodou práce je naopak veliký soubor selektovaných nemocných a akutním infarktem myokardu řešeným pomocí dPCI s následnou hospitalizací a jednotnou léčebnou strategií na jednom oddělení intenzivní péče.
Vzhledem k tomu, že lokální komplikace zatěžují pacienta (opětovná komprese třísla, krevní transfuze, chirurgické řešení) a prodlužují dobu hospitalizace, je jasným cílem snížení jejich výskytu i přes narůstající počet rizikových pacientů. Tím, že se již dříve přešlo od agresivní antikoagulační medikace k šetrnější antiagregační terapii v kombinací s nízkomolekulárním heparinem dávkovaným dle hmotnosti pacienta, počet těžkých krvácení a pseudoaneuryzmat výrazně klesl. Vyšší věk, ženské pohlaví, nízkou hodnotu BMI ani přítomnost diabetes mellitus, u kterých jsme zjistili, že zvyšují riziko tvorby pseudoaneuryzmat v místě intervence, nemůžeme významně ovlivnit. Proto další snížení komplikací spočívá v zavedení novějších přístupů mechanické komprese nebo lokálního ošetření cévní stěny. Alternativou k tradiční manuální kompresi je zařízení Femo-Stop, zajišťující dokonalejší mechanickou kompresi [12]. Novějšími způsoby uzavření cévy jsou systémy jako AngioSeal®, Perclose® anebo Starclose®, které patří do skupiny perkutánních tepenných uzavíracích zařízení (percutaneous closure device). Pomocí AngioSeal® se uzavře arterotomie kolagenní zátkou fixovanou pomocí intravaskulární kotvičky. Nevýhodou systému je určité riziko periferní embolizace kolagenního materiálu. Systémem Perclose® je místo arterotomie v cévní stěně uzavřeno pomocí 2 nevstřebatelných sutur. Její výhodou, kromě prokázaného snížení komplikací, je možnost opětovné katetrizace ze stejné tepny a rovněž použití systému při přístupu přes arteria brachialis [13]. Zvláštností zařízení Starclose® je způsob uzavření otvoru v tepenné stěně, kdy je pružná kovová struktura fixována na zevní straně tepny a nezasahuje do lumina. Obecně platí, že bezpečnost a účinnost těchto systémů musí být prokázány většími studiemi, protože dosavadní výsledky jsou zatím rozporuplné [14]. Většímu rozšíření těchto systémů stále brání i omezené finanční možnosti, proto byla na našem pracovišti v roce 2004 u více než 95 % pacientů po PCI použita manuální komprese.
Cílem našeho a jemu podobných hodnocení je určitá stratifikace pacientů a určení rizika vzniku lokálních komplikací a výsledně zvážení použití novějších, účinnějších, ale zároveň dražších metod lokální hemostázy u vybrané skupiny rizikových pacientů.
Zcela novou a nadějnou cestou řešení většiny z těch lokálních cévních komplikací, které se nepodaří zvládnout konzervativně, je uzávěr dutiny pseudoaneuryzmatu pomocí tkáňového lepidla na bázi humánního trombinu, instilovaného přímo do výdutě (obr. 1 a 2) [15]. Ověření správné pozice hrotu jehly a celý výkon probíhá pod ultrazvukovou kontrolou [16]. Obzvláště u pacientů krátce po akutním IM je rychlý výkon v lokální anestezií bezpečnější než operace s následnou imobilizací.
Obr. 1. Duplexní ultrazvukové (UZ) vyšetření: dutina pseudoaneuryzmatu plněná arteriální krví. 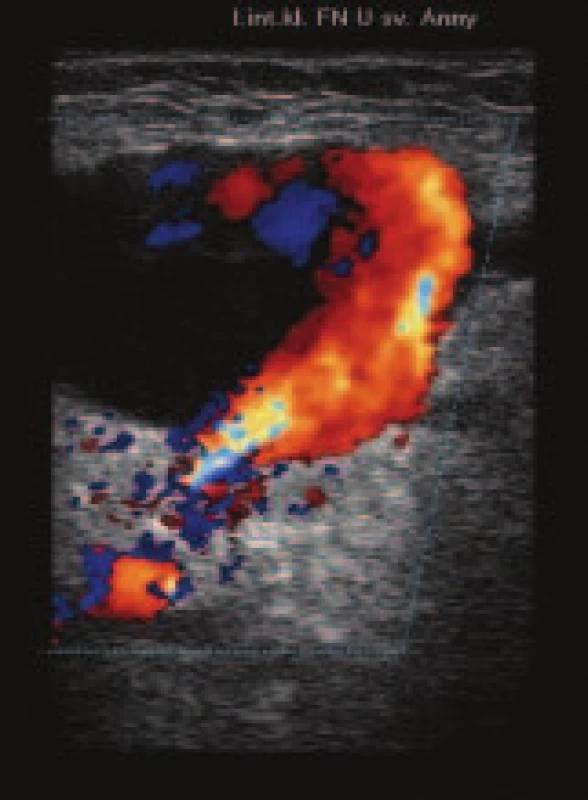
Obr. 2. Duplexní UZ vyšetření po aplikaci trombinu do pseudoaneuryzmatu: echogenní struktura vyplňuje původní dutinu, bez známek krevního toku. 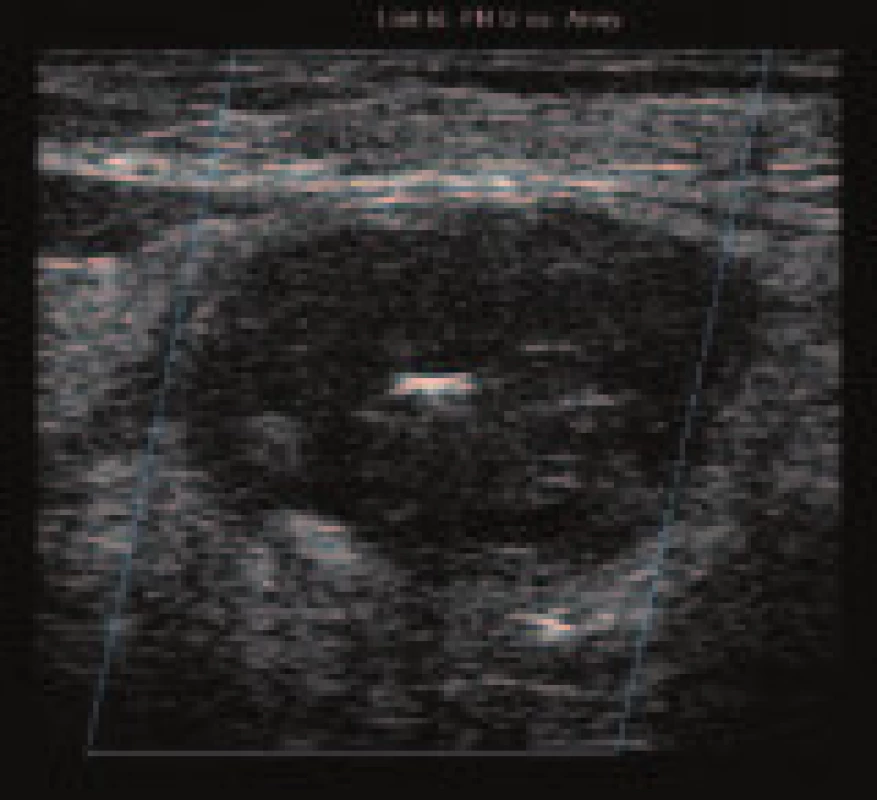
Prokázali jsme souvislost výskytu cévních komplikací u pacientů s akutním IM řešeným direktní PCI s vyšším věkem pacientů, ženským pohlavím, snížením BSA a BMI a přítomností DM. U těchto nemocných lze v současnosti s výhodou využít perkutánních uzavíracích systémů. K uzávěru pseudoaneuryzmat s úspěchem používáme trombin, který aplikujeme přímo do výdutě, a tím předcházíme operační revizi.
MUDr. Marek Orban
www.fnusa.cz
e-mail: maor@post.cz
Doručeno do redakce: 4. 4. 2005
Přijato po recenzi: 8. 11. 2005
Zdroje
1. Winthrop D, Piper, David J et al. Predicting vascular complications in percutaneous coronary interventions. American Heart J 2003; 145 : 1022-1029.
2. Ricci MA, Trevisani GT, Pilcher DB. Vascular complications of cardiac catheterization. Am J Surg 1994; 167 : 375-378.
3. Popma JJ, Satler LF, Pichard AD et al. Vascular complications after balloon and new device angioplasty. Circulation 1993; 88 : 1569-1578.
4. Muller DW, Shamir KJ, Ellis SG et al. Peripheral vascular complications after conventional and complex percutaneous coronary interventional procedures. Am J Cardiol 1992; 69 : 63-68.
5. Waksman R, King SB III, Douglas JS et al. Predictors of groin complications after balloon and new-device coronary intervention. Am J Cardiol 1995; 75 : 886-889.
6. Blankenship JC, Hellkamp AS, Aguirre FV et al. Vascular access site complications after percutaneous coronary intervention with abciximab in the evaluation of c7E3 for the Prevention of Ischemic Complications (EPIC) trial. Am J Cardiol 1998; 81 : 36-40.
7. Topol EJ. Toward a new frontier in myocardial reperfusion therapy: emerging platelet preeminence. Circulation 1998; 97 : 211-218.
8. Platelet glycoprotein IIb/IIIa receptor blockade and low-dose heparin during percutaneous coronary revascularization. The EPILOG Investigators. N Engl J Med 1997; 336 : 1689-1696.
9. The RESTORE Investigators. Effects of platelet glycoprotein IIb/IIIa blockade with tirofiban on adverse cardiac events in patients with unstable angina or acute myocardial infarction undergoing coronary angioplasty: Randomized Efficacy Study of Tirofiban for Outcomes and REstenosis. Circulation 1997; 96 : 1445-1453.
10. The PURSUIT Trial Investigators. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes: platelet glycoprotein IIb/IIIa in unstable angina: receptor suppression using integrilin therapy. N Engl J Med 1998; 339 : 436-443.
11. Ellis K, Boccalandro F, Burjonroppa S et al. Risk of Bleeding Complications Is Not Increased in Patients Undergoing Rescue versus Primary Percutaneous Coronary Intervention for Acute Myocardial Infarction. J Interv Cardiol 2005;18 : 361-365.
12. Jaspers L, Benit E Immediate sheath removal after PCI using a Femostop is feasible and safe. Results of a registry. Acta Cardiol 2003; 58 : 535-537.
13. Rinder MR, Tamirisa PK, Taniuchi M et al. Safety and efficacy of suture-mediated closure after percutaneous coronary interventions. Catheter Cardiovasc Interv 2001; 54 : 146-151.
14. Nikolsky E, Mehran R, Halkin A et al. Vascular complications associated with arteriotomy closure devices in patients undergoing percutaneous coronary procedures: a meta-analysis.J Am Coll Cardiol 2004; 44 : 1200-1209.
15. Tuna M, Raupach J, Chovanec V et al. Postkatetrizační pseudoaneurysmata. Interv Akut Kardiol 2004; 3 : 128-130.
16. Morgan R, Belli AM. Current treatment methods for postcatheterization pseudoaneurysms. J Vasc Interv Radiol 2003; 14 : 697-710.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2006 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Statinová intolerance
- Genetický podklad a screening familiární hypercholesterolémie
- Metabolit živočišné stravy produkovaný střevní mikroflórou zvyšuje riziko závažných kardiovaskulárních příhod
-
Všetky články tohto čísla
- Polymorfizmus genu pro endotelin u pacientů se srdečním selháním
- Diastolická dysfunkce levé komory u populace vyššího věku
- Volumy štítné žlázy u dospělé populace
- Antikoagulační léčba u antifosfolipidového syndromu
- Vliv cílené intervence na výskyt rizikových faktorů kardiovaskulárních onemocnění u zdravotnických zaměstnanců
- Klidový energetický výdej při hemodialýze
- Má polymorfizmus G8002A v genu pro endotelin význam pro další rizika u pacientů se srdečním selháním?
- Je zvýšený enddiastolický tlak v levé komoře u populace staršího věku patologický?
- Intervalový a kontinuální trénink v kardiovaskulární rehabilitaci
- Úvodník
- Lokální cévní komplikace u pacientů s akutním infarktem myokardu řešeným direktní perkutánní koronární intervencí
- Volumy štítné žlázy u dospělé populace ve věku 18 - 65 let v České republice - stanovení norem
- AIP - Aterogenní index plazmy jako významný prediktor kardiovaskulárního rizika: od výzkumu do praxe
- Vliv cílené intervence na výskyt rizikových faktorů KV onemocnění – editorial
- Nefluoroskopické mapovacie techniky v súčasnej katétrovej ablačnej liečbe dysrytmií
- Studie FIELD přednesena a uveřejněna. Nepřesvědčivé výsledky fenofibrátu u diabetiků.
-
Diagnostika a léčba jaterní encefalopatie
Doporučený postup vypracovaný skupinou pro portální hypertenzi při České hepatologické společnosti České lékařské společnosti J. E. Purkyně a schválený výborem České hepatologické společnosti České lékařské společnosti J. E. Purkyně - „Nejasná“ příčina vzniku a recidivy venózního tromboembolizmu
- Antifosfolipidový syndrom - popisy dvou případů
- Prof. MUDr. Josef Marek, DrSc. sedmdesátníkem
- Špička I et al. Mnohočetný myelom a další monoklonální gamapatie. Praha: Galén 2005. 128 stran. ISBN 80-7262-330-3
- Samuel Vokurka et al. Ošetřovatelské problémy a základy hemoterapie. Praha: Galén 2005. 140 stran. ISBN 80-7262-299-4.
- Stárka L, Zamrazil V et al. Základy klinické endokrinologie. 2. rozšířené vydání. Praha: Maxdorf 2005. 378 stran. ISBN 80-7345-066-6.
- Václav Špičák, Petr Panzner et al. Alergologie. Praha, Galén a Karolinum 2004. 348 stran. ISBN 80-7262-265-X (Galén), 80-246-0846-4 (Karolinum).
- Marek J et al. Farmakoterapie vnitřních nemocí. 3.(zcela přepracované a doplněné) vydání. Praha: Grada 2005. 773 stran. ISBN 80-247-0839-6.
- Widimský Jiří, Malý Jaroslav et al. Akutní plicní embolie a žilní trombóza. 2. rozšířené a přepracované vydání. Praha: TRITON 2005. Počet stran 381. ISBN 80-7254-639-2.
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- AIP - Aterogenní index plazmy jako významný prediktor kardiovaskulárního rizika: od výzkumu do praxe
- Volumy štítné žlázy u dospělé populace ve věku 18 - 65 let v České republice - stanovení norem
-
Diagnostika a léčba jaterní encefalopatie
Doporučený postup vypracovaný skupinou pro portální hypertenzi při České hepatologické společnosti České lékařské společnosti J. E. Purkyně a schválený výborem České hepatologické společnosti České lékařské společnosti J. E. Purkyně - Diastolická dysfunkce levé komory u populace vyššího věku
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy