-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vliv sekundárního zavedení ePTFE potahovaného stentu na udržení průchodnosti TIPS
The impact of secondary insertion of ePTFE-coated stent on sustainable TIPS patency
Objective:
Retrospective evaluation of the effect of secondary insertion of ePTFE-coated stent in the treatment of TIPS dysfunction versus other current options (simple angioplasty, insertion of additional non-coated stent).Patient set and methodology:
From the beginning of 2000 to the end of 2004, there were 121 interventions for TIPS dysfunction performed in our centre in which a non-coated stent was used to make up the shunt at the time of intervention. Depending on the type of intervention, the patient set was divided in 4 groups: simple angioplasty (52 cases, 43 %), insertion of non-coated stent (35 cases, 28.9 %), insertion of non-dedicated ePTFE-coated stent (15 cases, 12.4%), and insertion of dedicated ePTFE-coated stent (19 cases, 15.7%). All patients were monitored on a regular basis after the intervention for shunt patency with the use of clinical examination and Doppler ultrasonography, or also portal venography. Primary shunt patency after the intervention was evaluated in all four groups by Kaplan-Meier analysis. The primary shunt patency results after the intervention were compared with the use Cox F text and logrank test.Results:
The intervention was successful in 120 cases (the overall technical success rate of all interventions was 99.2%). The primary shunt patency was 49.7 % after 12 months and 25.3 % after 24 months following sole angioplasty intervention; 74.9 % after 12 and 64.9 % after 24 months following intervention involving the insertion of non-coated stent; 75.2 % after 12 months and 64.5 % after 24 months following intervention involving the insertion of non-dedicated ePTFE-coated stent, and 88.1 % after 12 months and 80.8 % after 24 months following intervention involving the insertion of a dedicated ePTFE-coated stent. A statistically significant improvement in shunt patency was obtained in the group of interventions involving the insertion of dedicated ePTFE-coated stent and in the group of interventions involving the insertion of non-coated stent as compared with the group of interventions involving sole angioplasty (p < 0.01). Conclusion: From among all the currently used methods of therapeutic intervention for TIPS dysfunction, the best, the best subsequent TIPS patency was obtained after intervention involving insertion of dedicated ePTFE-coated stent.Key words:
TIPS – portal hypertension therapy – stentgraft
Autoři: V. Jirkovský 1; T. Fejfar 1; V. Šafka 1; P. Hůlek 1; V. Chovanec 2; A. Krajina 2; J. Raupach 2; Miroslav Lojík 2
Působiště autorů: II. interní klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc. 1; Radiologická klinika Lékařské fakulty UK a FN, Hradec Králové, přednosta prof. MUDr. Pavel Eliáš, CSc. 2
Vyšlo v časopise: Vnitř Lék 2007; 53(2): 123-128
Kategorie: Původní práce
Souhrn
Cíl:
Retrospektivně zhodnotit efekt sekundárního zavedení ePTFE potahovaného stentu v léčbě dysfunkce TIPS ve srovnání s dalšími běžnými možnostmi (prostá angioplastika, zavedení dalšího nepotahovaného stentu).Soubor nemocných a metodika:
Od začátku roku 2000 do konce roku 2004 byla na našem pracovišti provedena intervence pro dysfunkci TIPS ve 121 případech, kdy byl v době intervence zkrat tvořen pouze nepotahovaným stentem. Dle způsobu intervence byl soubor rozdělen do 4 skupin, a to na intervence s prostou angioplastikou (52 případů, 43,0 %), intervence se zavedením nepotahovaného stentu (35 případů, 28,9 %), intervence se zavedením nededikovaného ePTFE potahovaného stentu (15 případů, 12,4 %) a na intervence se zavedením dedikovaného ePTFE potahovaného stentu (19 případů, 15,7 %). U všech pacientů byla po dané intervenci v pravidelných intervalech sledována další průchodnost zkratu pomocí klinického vyšetření a dopplerovské ultrasonografie, případně i portální venografie. Ve všech 4 skupinách byla zhodnocena primární průchodnost zkratu po dané intervenci pomocí Kaplanovy-Meierovy analýzy. Tyto výsledky primární průchodnosti zkratu po dané intervenci byly vzájemně porovnány pomocí Coxova F-testu a log-rank testu.Výsledky:
Intervence byla úspěšná ve 120 případech (celková technická úspěšnost všech intervencí byla 99,2 %). Primární průchodnost zkratu po intervenci samotnou angioplastikou byla 49,7 % po 12 měsících a 25,3 % po 24 měsících, po intervenci se zavedením nepotahovaného stentu byla 74,9 % po 12 a 64,9 % po 24 měsících, po intervenci se zavedením nededikovaného ePTFE potahovaného stentu byla 75,2 % po 12 a 64,5 % po 24 měsících a po intervenci se zavedením dedikovaného ePTFE potahovaného stentu byla 88,1 % po 12 a 80,8 % po24 měsících. Statisticky významně lepší průchodnosti zkratu bylo dosaženo ve skupině intervencí se zavedením dedikovaného ePTFE potahovaného stentu a ve skupině se zavedením nepotahovaného stentu oproti skupině intervencí s prostou angioplastikou (p < 0,01). Závěr: Ze všech běžně používaných metod léčebné intervence pro dysfunkci TIPS bylo dosaženo nejlepší následné průchodnosti TIPS po intervenci se zavedením dedikovaného ePTFE potahovaného stentu.Klíčová slova:
TIPS - terapie portální hypertenze - stentgraftÚvod
Metoda TIPS je u nás v současnosti jednou z hlavních dostupných možností řešení závažných komplikací portální hypertenze [1]. Největším problémem metody stále zůstává limitovaná a dopředu neodhadnutelná průchodnost zkratu. Při použití konvenčního nepotahovaného stentu je pravděpodobnost výskytu dysfunkce zkratu okolo 25 % během 6 měsíců a 50 % během 1 roku po vytvoření TIPS [2-4]. Vytvořením TIPS pomocí ePTFE potahovaného stentu se pravděpodobnost výskytu dysfunkce zkratu sníží asi na 13 % během prvních 6 měsíců a na 15-20 % během 1. roku po zavedení TIPS [5-8]. Proto je použití ePTFE potahovaného stentu v současnosti nejlepší primární prevencí dysfunkce TIPS. Taktéž v sekundární prevenci dysfunkce TIPS má ePTFE stentgraft významné místo a dokáže zlepšit dlouhodobou průchodnost [9-16], ale výsledky rozsáhlejších studií stále chybí. V současnosti je na trhu jediný přímo pro TIPS určený (dedikovaný) ePTFE potahovaný stent, a to stentgraft Viatorr společnosti W. L. Gore & Associates, který je dostatečně dlouhý a flexibilní a je schopen překrýt celý intraparenchymový úsek zkratu včetně jaterní žíly až do jejího ústí v dolní duté žíle. Nicméně vzhledem k jeho ceně jsou stále alternativně používány nededikované ePTFE potahované stenty (např. Ella stentgraft od firmy ELLA, či Jostent od firmy Abbott).
Cíl
Retrospektivně zhodnotit efekt terapie dysfunkce TIPS sekundárním zavedením ePTFE potahovaného stentu ve srovnání s dalšími běžnými možnostmi řešení dysfunkce TIPS a to prostou angioplastikou nebo angioplastikou v kombinaci se zavedením nepotahovaného stentu.
Soubor nemocných a metodika
Od ledna roku 2000 do prosince roku 2004 bylo provedeno na našem pracovišti celkem 179 intervencí TIPS. V 5 případech se jednalo o redukci zkratu pro závažnou jaterní encefalopatii. V 49 případech byl již v době intervence ve zkratu přítomen potahovaný stent, a to buď jako primoimplantát či sekundárně zavedený při předchozí intervenci. Tito pacienti nemohli být do sledovaného souboru zařazeni. Ze zbylých 125 intervencí bylo nutno ještě vyřadit 4 případy, kdy byl sekundárně vytvořen nový TIPS, protože původní zkrat se již nepodařilo zprůchodnit. Vlastní soubor tvořilo celkem 121 intervencí provedených v daném časovém období pro dysfunkci TIPS ve zkratu tvořeném pouze pomocí nepotahovaného stentu v době sledované intervence. Podle způsobu intervence byl soubor rozdělen do 4 skupin, a to na intervence s prostou angioplastikou, intervence se zavedením nepotahovaného stentu, na intervence se zavedením nededikovaného ePTFE potahovaného stentu (Jostent, Ella stentgraft) a na intervence se zavedením dedikovaného ePTFE potahovaného stentu (Viatorr).
První skupinu intervencí s prostou angioplastikou tvořilo 52 případů (43 %). Jednalo se o 43 mužů a 9 žen ve věku od 24 do 71 let (průměr 50,4 ± 9,7). Indikací k zavedení TIPS bylo u 32 pacientů (61,5 %) aktivní krvácení či prevence opakovaného krvácení z varixů a u 20 pacientů (38,5 %) refrakterní ascites či hydrotorax. Příčinou jaterního onemocnění byl 36krát abúzus alkoholu (69,2 %), 7krát Buddův-Chiariho syndrom (13,5 %), 7krát virová hepatitida (13,5 %), 2krát neznámá příčina (3,8 %). Časový odstup angioplastiky od vytvoření TIPS byl v rozmezí od 0,2 do 128 měsíců (medián 23,5). Jednalo se o 1. až 6. intervenci po zavedení TIPS (průměr 1,9, medián 1). Při portografii byla 26krát zjištěna výtoková stenóza (50,0 %), 23krát instent stenóza (44,2 %), 2krát okluze zkratu (3,8 %) a 2krát nebyla zjištěna morfologická příčina a důvodem intervence byl vysoký PSG (3,8 %). V jednom případě šlo o kombinaci instent a výtokové stenózy. U 38 pacientů (73,1 %) se jednalo o asymptomatickou dysfunkci, u 10 pacientů (19,2 %) byla přítomna recidiva ascitu a u 5 pacientů (9,6 %) šlo o recidivu krvácení. U jednoho pacienta byla recidiva krvácení i ascitu.
Druhou skupinu intervencí se zavedením nepotahovaného stentu tvořilo 35 případů (28,9 %). Jednalo se o 30 mužů a 5 žen ve věku od 12 do 75 let (průměr 53,7 ± 11,9). Indikací k zavedení TIPS bylo u 25 pacientů (71,4 %) aktivní krvácení či prevence opakovaného krvácení z varixů a u 10 pacientů (28,6 %) refrakterní ascites. Příčinou jaterního onemocnění byl abúzus alkoholu 23krát (65,7 %), virová hepatitida 6krát (17,1 %), autoimunitní hepatitida 2krát (5,7 %), Buddův-Chiariho syndrom 1krát (2,9 %), jiná či neznámá příčina 3krát (8,6 %). Časový odstup sledované intervence od zavedení TIPS byl v rozmezí od 3 do 89 měsíců (medián 17,5). Jednalo se o 1. až 6. intervenci po zavedení TIPS (průměr 1,5, medián 1). Při portografii byla zjištěna výtoková stenóza 22krát (62,8 %), okluze zkratu 8krát (22,9 %), vtoková stenóza 3krát (8,6 %), instent stenóza 2krát (5,7 %) a 1krát (2,9 %) nebyla zjištěna morfologická příčina a důvodem intervence byl vysoký PSG. V jednom případě byla koincidence vtokové a výtokové stenózy. U 21 pacientů (60,0 %) se jednalo o asymptomatickou dysfunkci, u 10 pacientů (28,6 %) byla přítomna recidiva ascitu a u 4 pacientů (11,4 %) šlo o recidivu krvácení.
Třetí skupinu intervencí se zavedením nededikovaného ePTFE potahovaného stentu (Jostent či Ella stentgraft) tvořilo 15 případů (12,4 %). Jednalo se o 11 mužů a 4 ženy ve věku od 22 do 75 let (průměr 52,3 ± 13,1). Indikací k zavedení TIPS bylo u 11 pacientů (73,3 %) aktivní krvácení či prevence opakovaného krvácení z varixů a u 4 pacientů (26,7 %) refrakterní ascites či hydrotorax. Příčinou jaterního onemocnění byl 10krát abúzus alkoholu (66,7 %), 3krát virová hepatitida (20,0 %) a 2krát Buddův-Chiariho syndrom (13,3 %). Časový odstup sledované intervence od zavedení TIPS byl v rozmezí od 0 do 46 měsíců (medián 14,5). Jednalo se o 1. až 5. intervenci (průměr 2,1, medián 2). Při portografii byla zjištěna 8krát instent stenóza (53,4 %), 3krát výtoková stenóza (20,0 %), 2krát vtoková stenóza (13,3 %) a 2krát okluze zkratu (13,3 %). U 8 pacientů (53,4 %) šlo o asymptomatickou dysfunkci TIPS, u 5 pacientů (33,3 %) se jednalo o recidivu krvácení a u 2 pacientů (13,3 %) o recidivu ascitu.
Čtvrtou skupinu intervencí se zavedením dedikovaného ePTFE potahovaného stentu (Viatorr) tvořilo 19 případů (15,7 %). Jednalo se o 16 mužů a 3 ženy ve věku od 25 do 69 let (průměr 51,7 ± 11,7). Indikací k vytvoření TIPS bylo u 15 pacientů (78,9 %) aktivní krvácení či prevence opakovaného krvácení z varixů a u 4 pacientů (21,1 %) refrakterní ascites. Příčinou jaterního onemocnění byl 13krát abúzus alkoholu (68,4 %), 3krát Buddův-Chiariho syndrom (15,8 %), 2krát virová hepatitida (10,5 %) a 1krát byla příčina nejasná (5,3 %). Časový odstup sledované intervence od zavedení TIPS byl v rozmezí od 0 do 131 měsíců (medián 20). Jednalo se o 1. až 6. intervenci (průměr 2,4, medián 2). Při portografii byla zjištěna 9krát okluze zkratu (47,4 %), 8krát výtoková stenóza (42,1 %) a 2krát instent stenóza (10,5 %). U 11 pacientů (57,9 %) se jednalo o asymptomatickou dysfunkci TIPS, u 6 pacientů (31,6 %) šlo o recidivu ascitu a u 2 pacientů (10,5 %) o recidivu krvácení.
Po dané intervenci byla ve všech 4 skupinách hodnocena další průchodnost TIPS na základě klinického vyšetření a dopplerovské ultrasonografie v odstupu 1 a 3 měsíců a dále dle potřeby každé 3 až 6 měsíců. Portální venografie s měřením PSG byla provedena vždy v případě klinického či ultrazvukového podezření na dysfunkci TIPS. Dysfunkce TIPS byla definována jako zúžení zkratu při portální venografii o 50 a více % a/nebo vzestup PSG na více než 12 mm Hg.
Ve všech 4 skupinách byla zhodnocena primární průchodnost zkratu po dané intervenci (doba od dané intervence do následující reintervence) pomocí Kaplanovy-Meierovy analýzy. Výsledky primární průchodnosti zkratu po dané intervenci byly v jednotlivých skupinách vzájemně statisticky porovnány pomocí Coxova F-testu a log-rank testu. K vzájemnému porovnání klinické symptomatiky u jednotlivých morfologických typů dysfunkce TIPS byl použit χ2-test. Veškeré statistické zpracování dat bylo provedeno pomocí počítačového programu Statistica 5.0 (StatSoft, Inc., USA).
Výsledky
Ze všech 121 intervencí byla pouze 1 neúspěšná, a to v 1. skupině, kdy došlo při angioplastice výtokové stenózy k deformaci Palmazova stentu a okluzi zkratu, kterou se již nepodařilo rekanalizovat a následně byla řešena vytvořením nového TIPS. Ve všech ostatních 120 případech výkon proběhl bez závažnějších periprocedurálních komplikací. Celková technická úspěšnost všech intervencí tedy byla 99,2 %.
Po intervenci došlo v průměru k poklesu PSG v 1. sledované skupině z 16,7 ± 5,1 mm Hg na 7,2 ± 3,0 mm Hg, ve 2. sledované skupině z 19,1 ± 6,3 mm Hg na 7,8 ± 3,4 mm Hg, ve 3. skupině z 16,7 ± 5,5 mm Hg na 7,1 ± 3,5 mm Hg a ve 4. skupině z 23,1 ± 5,0 mm Hg na 8,1 ± 3,9 mm Hg.
V 1. skupině 52 intervencí s prostou angioplastikou byla průměrná doba sledování 33,1 ± 21,2 měsíců (rozmezí 0 až 65, medián 33). Během této doby byla opětovná dysfunkce TIPS diagnostikována v 33 případech. 32 pacientů (61,6 %) z této skupiny je dále sledováno, 18 pacientů zemřelo (34,6 %), 1 pacient (1,9 %) podstoupil transplantaci jater a 1 pacient (1,9 %) byl ztracen z dispenzarizace.
Ve 2. skupině 35 intervencí se zavedením nepotahovaného stentu byla průměrná doba sledování 24,6 ± 21,9 měsíců (rozmezí 0,2 až 67, medián 19). Během této doby byla recidiva dysfunkce TIPS zjištěna v 10 případech. 24 pacientů (68,5 %) z této skupiny zemřelo, 9 pacientů (25,7 %) je dále sledováno, 1 pacient (2,9 %) podstoupil transplantaci jater a 1 pacient (2,9 %) byl ztracen z dispenzarizace.
Ve 3. skupině 15 intervencí se zavedením nededikovaného ePTFE potahovaného stentu byla průměrná doba sledování 26,1 ± 22,8 měsíců (rozmezí od 0,4 až 66, medián 20). Během této doby byla opětovná dysfunkce TIPS zjištěna v 6 případech. 7 pacientů (46,6 %) v této skupině zemřelo, 6 pacientů (40,0 %) je dále sledováno, 1 pacient (6,7 %) podstoupil transplantaci jater a 1 pacient (6,7 %) byl ztracen z dispenzarizace.
Ve 4. skupině 19 intervencí se zavedením dedikovaného ePTFE potahovaného stentu byla průměrná doba sledování 24,9 ± 15,5 měsíců (rozmezí 1 až 48, medián 27). Během této doby byla recidiva dysfunkce TIPS diagnostikována ve 3 případech. 14 pacientů (73,7 %) z této skupiny je dále sledováno, 4 pacienti (21,0 %) zemřeli a 1 pacient (5,3 %) byl ztracen z dispenzarizace.
Primární průchodnost zkratu po intervenci prostou angioplastikou byla 49,7 % po 12 měsících a 25,3 % po 24 měsících. Primární průchodnost zkratu po intervenci se zavedením nepotahovaného stentu byla 74,9 % po 12 měsících a 64,9 % po 24 měsících. Primární průchodnost zkratu po intervenci se zavedením nededikovaného ePTFE potahovaného stentu byla 75,2 % po 12 měsících a 64,5 % po 24 měsících. Primární průchodnost zkratu po intervenci se zavedením dedikovaného ePTFE potahovaného stentu byla 88,1 % po 12 měsících a 80,8 % po 24 měsících (graf 1, tab. 1).
Tab. 1. Primární průchodnost zkratu po dané intervenci. 
Graf 1. Primární průchodnost zkratu po dané intervenci. 
Výsledky statistického porovnání primární průchodnosti zkratu po dané intervenci v jednotlivých skupinách jsou znázorněny v tab. 2.
Tab. 2. Vzájemné statistické porovnání primární průchodnosti TIPS po dané intervenci. 
Primární průchodnost zkratu po intervenci se zavedením dedikovaného ePTFE potahovaného stentu či se zavedením nepotahovaného stentu je statisticky významně lepší než po intervenci s pouhou angioplastikou (Coxův F-test p = 0,01 resp. p = 0,006; log-rank test p = 0,0001 resp. p = 0,005).
Statisticky významnému zlepšení se blíží primární průchodnost zkratu po intervenci se zavedením nededikovaného ePTFE potahovaného stentu ve srovnání s intervencí se samotnou angioplastikou (Coxův F-test p = 0,09; log-rank test 0,09) a také primární průchodnost po intervenci se zavedením dedikovaného ePTFE potahovaného stentu ve srovnání s intervencí se zavedením nededikovaného ePTFE potahovaného stentu (Coxův F-test p = 0,1; log-rank test p = 0,09).
Během všech 121 intervencí bylo při portografii zjištěno 59 výtokových stenóz (15 symptomatických), 35 instent stenóz (14 symptomatických), 21 okluzí zkratu (10 symptomatických) a 5 vtokových stenóz (4 symptomatické). Ve 3 případech nebyla zjištěna stenóza ani okluze a příčinou dysfunkce TIPS byl vysoký PSG, v jednom případě s klinickou symptomatologií (tab. 3). Z výsledků je patrno, že nejčastěji se klinické symptomy portální hypertenze vyskytují u vtokových stenóz (80 %), dále u okluzí zkratu (47,6 %), instent stenóz (40 %) a nejméně často jsou klinické symptomy přítomny u výtokových stenóz (25,4 %). Statisticky významného rozdílu však bylo v našem souboru dosaženo pouze při porovnání vtokových a výtokových stenóz (χ2-test p = 0,01).
Tab. 3. Četnost jednotlivých morfologických typů dysfunkce TIPS a jejich symptomatologie. 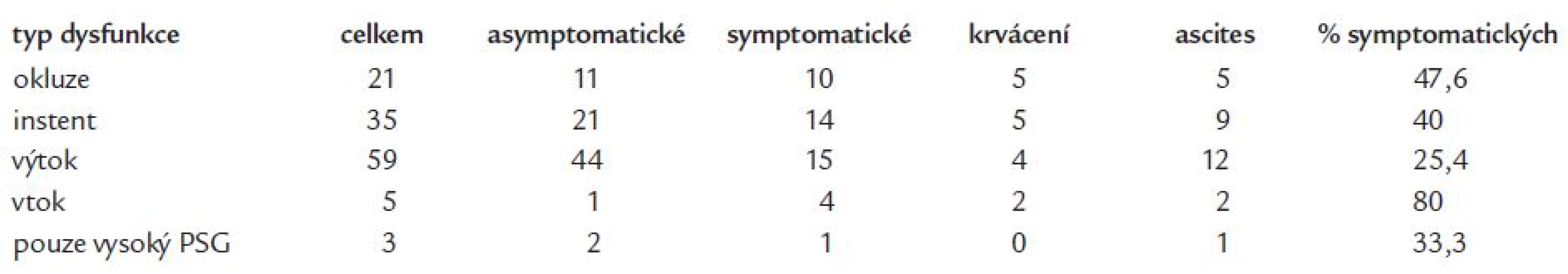
Diskuse
Hlavním problémem TIPS je jeho limitovaná a dopředu neodhadnutelná průchodnost. Dysfunkci TIPS nejčastěji způsobují 3 různé příčiny: akutní trombóza zkratu, pseudointimální hyperplazie v intraparenchymální části zkratu a intimální hyperplazie v oblasti jaterní žíly [10,12,17]. V literatuře se popisuje, že stenózy v intraparenchymální části zkratu jsou častěji spojeny s klinickou symptomatologií portální hypertenze (recidiva krvácení či ascites) než výtokové stenózy v oblasti jaterní žíly [20]. V souladu s tím i naše výsledky prokazují fakt, že čím více je morfologická příčina dysfunkce TIPS lokalizována kaudálně, tím častější jsou klinické příznaky portální hypertenze, jako je krvácení či ascites. Naopak, čím více je morfologická příčina lokalizována kraniálně, tím méně často jsou tyto klinické známky portální hypertenze přítomny. Statisticky významného rozdílu však bylo dosaženo pouze mezi kaudálně uloženými (vtokovými) a kraniálně uloženými (výtokovými) stenózami.
Pravděpodobnost výskytu dysfunkce TIPS vytvořeného pomocí nepotahovaného stentu je okolo 25 % během 6 měsíců a 50 % během 1 roku po vytvoření TIPS [2-4]. Proto je nutné k udržení průchodnosti TIPS pravidelné sledování zkratu pomocí dopplerovského ultrazvuku a ev. přímé či nepřímé portografie a časté sekundární intervence. Tato strategie je úspěšná, ale ekonomicky náročná a invazivní a nechrání pacienta před další potenciální dysfunkcí zkratu s případnou manifestací některých závažných projevů portální hypertenze.
Jako nejlepší řešení problému dysfunkce TIPS se v současnosti jeví použití ePTFE potahovaného stentu, který díky izolaci krve a jaterního parenchymu přeruší spouštěcí mechanizmy hyperplazie či trombózy. V prvních klinických studiích, ve kterých byl použit k vytvoření TIPS nededikovaný ePTFE potahovaný stent, došlo k poklesu výskytu instent stenóz a okluzí zkratu, ale nebyl zaznamenán vliv na výskyt výtokových stenóz [18,19]. Další klinické studie s primárním použitím dedikovaných ePTFE potahovaných stentů jasně prokázaly výrazné zlepšení průchodnosti TIPS ve srovnání s použitím nepotahovaných stentů [5-8]. ePTFE potahované stenty mohou být použity i sekundárně při revizi stenózovaného či rekanalizaci uzavřeného TIPS, ale v literatuře není příliš mnoho informací o klinickém použití ePTFE potahovaných stentů při vlastní léčbě dysfunkce TIPS. Doposud bylo publikováno několik spíše kazuistických případů použití nededikovaného ePTFE potahovaného stentu při léčbě dysfunkce TIPS s následným výrazným zlepšením průchodnosti zkratu [9-14]. Sekundárním zavedením dedikovaného ePTFE potahovaného stentu v léčbě stenóz či okluzí TIPS se zabývají pouze 2 práce, a to Cejnova [15] a Echenagusiaova [16]. Cejna et al [15] v roce 2002 publikovali použití stentgraftu Viatorr při intervenci pro dysfunkci TIPS u 9 pacientů. Primární průchodnost zkratu po této intervenci byla 100% při průměrné době sledování 201 dní. Echenagusia et al [16] publikovali v roce 2005 studii se sekundárním zavedením stentgraftu Viatorr u 12 pacientů. Následná dysfunkce TIPS byla pozorována u 2 pacientů při průměrné době sledování 21,9 měsíců. Primární průchodnost zkratu po intervenci se zavedením stentgraftu Viatorr byla 100 % po 12 měsících a 88,8 % po 24 měsících.
Naše práce oproti výše citovaným [15,16] má ve skupině intervencí s dedikovaným ePTFE potahovaným stentem více pacientů (19 pacientů) a delší průměrnou dobu sledování (24,9 měsíců) a navíc porovnává výsledky i s dalšími běžnými možnostmi léčby dysfunkce TIPS z jednoho pracoviště. Primární průchodnost po intervenci se zavedením dedikovaného ePTFE potahovaného stentu v našem souboru (88,1 % po 12 měsících a 80,8 % po 24 měsících) je jen o málo horší než ve výše citovaných pracích [15,16], ale srovnatelná s primární průchodností TIPS vytvořeného primárně pomocí dedikovaného ePTFE potahovaného stentu [5-8]. Z našich výsledků je patrné, že lepší průchodnosti TIPS dosáhneme po intervenci se zavedením dalšího stentu než po intervenci s prostou angioplastikou. Toto může být dáno lepším udržením šířky zkratu díky vyztužení a radiální síle dalšího stentu, a navíc u ePTFE potahovaných stentů izolací dilatací porušené endoteliální výstelky pseudointimy či neointimy. Statisticky významného rozdílu bylo dosaženo ve skupině intervencí s dedikovaným ePTFE potahovaným stentem a ve skupině intervencí s nepotahovaným stentem ve srovnání se skupinou intervencí s angioplastikou. Primární průchodnost TIPS po intervenci s nededikovaným ePTFE potahovaným stentem a po intervenci s nepotahovaným stentem je v našem souboru srovnatelná. Důvodem horší průchodnosti TIPS po intervenci s nededikovaným ve srovnání s dedikovaným ePTFE potahovaným stentem je pravděpodobně nedostatečná délka nededikovaných ePTFE potahovaných stentů, které nejsou schopny překrýt celou délku zkratu až do výtoku jaterní žíly v dolní duté žíle.
Vzhledem k lepší primární průchodnosti je snaha stále častěji používat dedikované ePTFE potahované stenty již při vytvoření TIPS, hlavně u pacientů s vyšším rizikem dysfunkce zkratu, což jsou například pacienti s poraněním žlučových cest během výkonu, pacienti s trombofilním stavem nebo mladší pacienti. Cena dedikovaného ePTFE potahovaného stentu je asi 2,6krát vyšší než nepotahovaného stentu, proto tyto stentgrafty zatím zcela nenahradí běžné stenty. Nicméně díky nutnosti menšího počtu reintervencí u pacientů s dedikovaným ePTFE potahovaným stentem může být výsledná celková cena léčby komplikací portální hypertenze pomocí TIPS nižší než při použití nepotahovaných stentů. Nyní však neexistuje žádná medicínsko-ekonomická studie, která by se danou problematikou zaobírala.
Závěr
V současnosti je nejvíce úspěšnou metodou v léčbě dysfunkce TIPS sekundární zavedení dedikovaného ePTFE potahovaného stentu. Cena tohoto stentgraftu je stále velmi vysoká oproti běžným stentům. Proto je nutné do budoucna vytvořit medicínsko-ekonomické studie a dle jejich výsledků eventuálně rozšířit tuto léčbu.
Použité zkratky
ePTFE - expandovaný polytetrafloretylén,
TIPS - transjugulární intrahepatální portosystémová spojka,
PSG - portosystémový gradient
Práce byla podpořena Výzkumným záměrem MZO 00179906 a IGA MZČR NR 8419-4.
MUDr. Václav Jirkovský
www.fnhk.cz
e-mail: vrtula@post.cz
Doručeno do redakce: 28. 8. 2006
Přijato po recenzi: 10. 11. 2006
Zdroje
1. Hůlek P, Vaňásek T, Lata J et al. Vývoj v léčbě portální hypertenze. Folia Gastroenterol Hepatol 2005; 3(Suppl 1): S32-S39.
2. Haskal ZJ, Pentecost MJ, Soulen MC et al. Transjugular Intrahepatic Portosystemic Shunt Stenosis and Revision: Early and Midterm Results. AJR 1994; 163 : 439-444.
3.Narazian GK, Ferral H, Castaneda-Zunica WR et al. Development of Stenoses in Transjugular Intrahepatic Portosystemic Shunts. Radiology 1994; 192 : 231-234.
4. Sterling KM, Darcy MD. Stenosis of Transjugular Intrahepatic Portosystemic Shunts: Presentation and Management. ARJ 1997; 168 : 239-244.
5. Hausegger KA, Karnel F, Georgieva B et al. Transjugular Intrahepatic Portosystemic Shunt Creation with the Viatorr Expanded Polytetrafluoroethylene-Covered Stent-Graft. J Vasc Interv Radiol 2004; 15 : 239-248.
6. Bureau C, Garcia-Pagan JC, Otal P et al. Improved Clinical Outcome Using Polytetrafluoroethylene-Coated Stents for TIPS: Results of a Randomized Study. Gastroenterology 2004; 126 : 469-475.
7. Charon JPM, Alaeddin FH, Pimpalwar SA et al. Results of a Retrospective Multicenter Trial of the Viatorr Expanded Polytetrafluoroethylene-Covered Stent-Grafts for Transjugular Intrahepatic Portosystemic Shunt Creation. J Vasc Interv Radiol 2004; 15 : 1219-1230.
8. Rossi P, Salvatori FM, Fanelli F et al. Polytetrafluoroethylene-Covered Nitinol Stent-Graft for Transjugular Intrahepatic Portosystemic Shunt Creation: 3-year Experience. Radiology 2004; 231 : 820-830.
9. Cohen GS, Young HY, Ball DS. Stent-graft as Treatment for TIPS-biliary Fistula. J Vasc Interv Radiol 1996; 7 : 665-668.
10. Saxon RR, Timmermans HA, Uchida BT et al. Stent-grafts for Revision of TIPS Stenoses and Occlusions: A Clinical Pilot Study. J Vasc Interv Radiol 1997; 8 : 539-548.
11. DiSalle RS, Dolmach BL. Treatment of TIPS stenosis with ePTFE Graft-covered Stents. Cardiovasc Intervent Radiol 1998; 21 : 172-175.
12. Sze DY, Vestring T, Liddell RP et al. Recurrent TIPS Failure Associated with Biliary Fistulae: Treatment with PTFE-covered Stenos. Cardiovasc Intervent Radiol 1999; 22 : 298-304.
13. Haskal ZJ. Improved Patenty of Transjugular Intrahepatic Portosystemic Shunts in Humans: Creation and Revision with PTFE Stentgrafts. Radiology 1999; 213 : 759-766.
14. Haskal ZJ, Weintraub JL, Susman, J. Recurrent. TIPS Thrombosis After Polyethylene Stent-grafts Use and Salvage with Polytetrafluoroethylene Stent-grafts. J Vasc Interv Radiol 2002; 13 : 1255-1259.
15. Cejna M, Peck-Radosavljevic M, Thurnher S et al. ePTFE-Covered Stent-Grafts for Revision of Obstructed Transjugular Intrahepatic Portosystemic Shunt. Cardiovasc Intervent Radiol 2002; 25 : 365-372.
16. Echenagusia M, Rodriguez-Rosales G, Simo G et al. Expanded PTFE-Covered Stent-Grafts in the Treatment of Transjugular Intrahepatic Portosystemic Shunt (TIPS) Stenoses and Occlusions. Abdom Imaging 2005; 30 : 750-754.
17. Ducoin H, El-Khoury J, Rousseau H et al. Histopathologic Analysis of Transjugular Intrahepatic Portosystemic Shunts. Hepatology 1997; 25 : 1064-1069.
18. Krajina A, Hulek P, Lojik M et al. Creation of TIPS with The Use of ePTFE Stent-graft (Abstract). Cardiovasc Intervent Radiol 1999; 22(Suppl 2): S122.
19. Andrews RT, Saxon RR, Bloch RD. Stent-grafts for De Novo TIPS: Technique and Early Results. J Vasc Interv Radiol 1999; 10 : 1371-1378.
20. Saxon RR, Ross PL, Mendel-Hartving J et al. Transjugular Intrahepatic Portosystemic Shunt Patenty and The Importace of Stenosis Location in The Development of Recurrent Symptoms. Radiology 1998; 207 : 683-693.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Indrák K et al. Hematologie.Článek Pankreatikopleurální píštěle
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2007 Číslo 2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Pankreatikopleurální píštěle - editorial
- Chirurgická ablace fibrilace síní: budoucnost kardiochirurgie? - editorial
- Reziduální echokardiografické nálezy a NT-proBNP u asymptomatických dospělých pacientů po radikální korekci Fallotovy tetralogie
- Vliv sekundárního zavedení ePTFE potahovaného stentu na udržení průchodnosti TIPS
- Nízkodávkovaný talidomid u refrakterního a relabujícího mnohočetného myelomu
- Pankreatikopleurální píštěle
- Paradoxní embolizace při foramen ovale patens u potápěčů: možnosti screeningu
- Klinicky manifestní gastrointestinální krvácení u koronarografovaných nemocných
- Dlouhodobá účinnost chirurgické kryoablace chronické fibrilace síní provedené při operaci pro závažnou mitrální regurgitaci
- Dysfunkce transjugulární intrahepatální portosystémové spojky (TIPS) a její řešení
- Enkapsulující peritoneální skleróza
- Teplota nejasné etiologie: příčiny a diagnostický postup
- Doporučení pro diagnostiku a léčbu dyslipidemií v dospělosti, vypracované výborem České společnosti pro aterosklerózu
- Dialog hematologa a internisty: problém specializace a informací v medicíně
- Kalita Z et al. Akutní cévní mozkové příhody. Diagnostika, patofyziologie, management.
- Safar ME, O’Rourke MF (eds). Arterial stiffness in hypertension.
- Veselka J et al. Hypertrofická kardiomyopatie a příbuzná témata.
- Válek V, Kala Z, Kiss I et al. Maligní ložiskové procesy jater. Diagnostika a léčba včetně minimálně invazivních metod.
- Krajsová I. Melanom. Klasifikace, diagnostika, terapie, prevence.
- Tesař V, Schück O et al. Klinická nefrologie.
- Klener P et al. Propedeutika ve vnitřním lékařství.
- Goldberg E. Paradox moudrosti. Jak být duševně výkonnější, přestože mozek stárne.
- Štejfa M et al. Kardiologie. 3. přepracování a doplněné vydání.
- Indrák K et al. Hematologie.
- Šafránková A, Nejedlá M. Interní ošetřovatelství I a II.
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Teplota nejasné etiologie: příčiny a diagnostický postup
- Doporučení pro diagnostiku a léčbu dyslipidemií v dospělosti, vypracované výborem České společnosti pro aterosklerózu
- Enkapsulující peritoneální skleróza
- Dlouhodobá účinnost chirurgické kryoablace chronické fibrilace síní provedené při operaci pro závažnou mitrální regurgitaci
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



