-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Kolorektální karcinom (část 1)
Vyšlo v časopise: Čas. Lék. čes. 2014; 152: 100-111
Kategorie: Abstrakta
6.–7. prosince 2013, Praha
Vážené kolegyně, vážení kolegové,
koncem minulého roku (6.–7. prosince 2013) se v Praze konal druhý ročník Národního kongresu o kolorektálním karcinomu, jehož součástí byl i 4. postgraduální kurz Společnosti pro gastrointestinální onkologii ČLS JEP. Tato odborná akce vznikla jako společná iniciativa pěti odborných společností České lékařské společnosti JEP (Společnost pro gastrointestinální onkologii, Česká gastroenterologická společnost, Česká chirurgická společnost, Česká onkologická společnost a Česká radiologická společnost), ale přesahuje i do dalších specializací (praktické lékařství, molekulární genetika, klinická biochemie a další). Kongres byl koncipován do 14 sekcí rozdělených do dvou paralelních programů (postgraduální kurz a sympozia).
Texty k přednáškám, doporučené literatura a powerpointové prezentace byly shrnuty v syllabu kongresu. S cílem poskytnout tyto informace širší odborné veřejnosti budou v letošním roce v Časopisu lékařů českých publikována abstrakta jednotných přednášek. Vzhledem k jejich vysokému počtu budou rozdělena do několika částí dle podobné tematiky. První část je zaměřena na epidemiologii, rizikové faktory a screening.
Texty doc. L. Duška a dr. O. Májka potvrzují nepříliš příznivá epidemiologická data. V České republice je ročně diagnostikováno 7800–8200 pacientů s KRK, z toho více jak 50 % v pokročilém stadiu. Dle modelu predikce bude prevalence KRK narůstat o 13–30 % (srovnání let 2008–2015). Dr. Š. Suchánek a doc. L. Dušek shrnují základní informace o Národním programu screeningu KRK v ČR, včetně pokrytí cílové populace, které v roce 2011 činilo 25 %. Pro zvýšení efektivity programu bylo počátkem letošního roku zahájeno cílené adresné zvaní organizované Ministerstvem zdravotnictví ČR a realizované zdravotními pojišťovnami. Screeningu byla dále věnována jedna sekce. Příspěvek doc. B. Seiferta potvrzuje ústup od guajakových testů na okultní krvácení (TOKS) ve prospěch imunochemických TOKS a zároveň stoupající míru pozitivity TOKS, která dosáhla 6,7 %. Dr. P. Kocna prezentuje přehled evropských programů či studií s využitím FIT, včetně české studie s cut-off hladinou 75 ng/ml. Prim. P. Vítek a dr. O. Májek ve svém sdělení uvádejí souhrnný přehled doporučených indikátorů kvality z pohledu endoskopisty a biostatistika. Dr. M. Minárik předkládá základní informace o molekulární onkologii KRK, zejména využití molekulární markerů. Prim. M. Šachlová se zaměřuje na metabolické rizikové faktory KRK s konstatováním, že diabetici 2. typu a osoby s metabolickým syndromem a obezitou pravděpodobně představují rizikovou skupinu pro vznik KRK. Samostatná sekce byla vyhrazena vztahu nespecifických střevních zánětů a KRK. Dr. T. Douda uvádí správné indikace kolonoskopického vyšetřování a dispenzarizace, prof. P. Frič roli gastrointestinálního ekosystému a terapii probiotiky a prof. J. Bureš objasňuje problematiku butyrátového paradoxon. Toto téma shrnuje prof. Frič ve state of the art přednášce.
prof. MUDr. Miroslav Zavoral, Ph.D.
předseda organizačního výboru kongresu
předseda Společnosti pro gastrointestinální onkologii ČLS JEP
EPIDEMIOLOGIE A RIZIKOVÉ FAKTORY, SCREENING
Nové trendy v epidemiologii kolorektálního karcinomu v ČR
Dušek L., Mužík J., Májek O.
Institut biostatistiky a analýz MU, Brno
V ČR je ročně nově diagnostikováno 7800–8200 pacientů se zhoubným novotvarem tlustého střeva nebo konečníku. Ve stejné době na tento nádor 3800–4200 pacientů zemře. Prevalence, tedy počet žijících osob, které mají nebo měly diagnostikovaný tento typ nádoru, dosáhla v roce 2010 hodnoty 49 470 osob a ve srovnání s rokem 2000 tak vzrostla o 64,1 %. V ČR je nadto více než 50 % nových pacientů s kolorektálním karcinomem diagnostikováno v pokročilém stadiu onemocnění (stadium 3. nebo vyšší), což významně zhoršuje prognózu pacientů a dosažitelné výsledky léčby.
Dostupnost a kvalita populačních dat o kolorektálním karcinomu: Základním zdrojem údajů pro populační hodnocení epidemiologie kolorektálního karcinomu je Národní onkologický registr České republiky (NOR). Jde o unikátní databázi v evropském i celosvětovém měřítku, ve které jsou od roku 1977 zaznamenávány všechny novotvary zjištěné v české populaci. Za období 1977–2010 je v databázi více než 1,8 mil. záznamů všech novotvarů, z nichž téměř 12 % představují hlášení o kolorektálním karcinomu. V tabulce 1 je popsána struktura záznamů NOR s ohledem na jejich úplnost a využitelnost pro další hodnocení.
Tab. 1. Struktura a kvalita záznamů NOR o kolorektálním karcinomu (C18–C20; období 2006–2010; 40 030 záznamů) 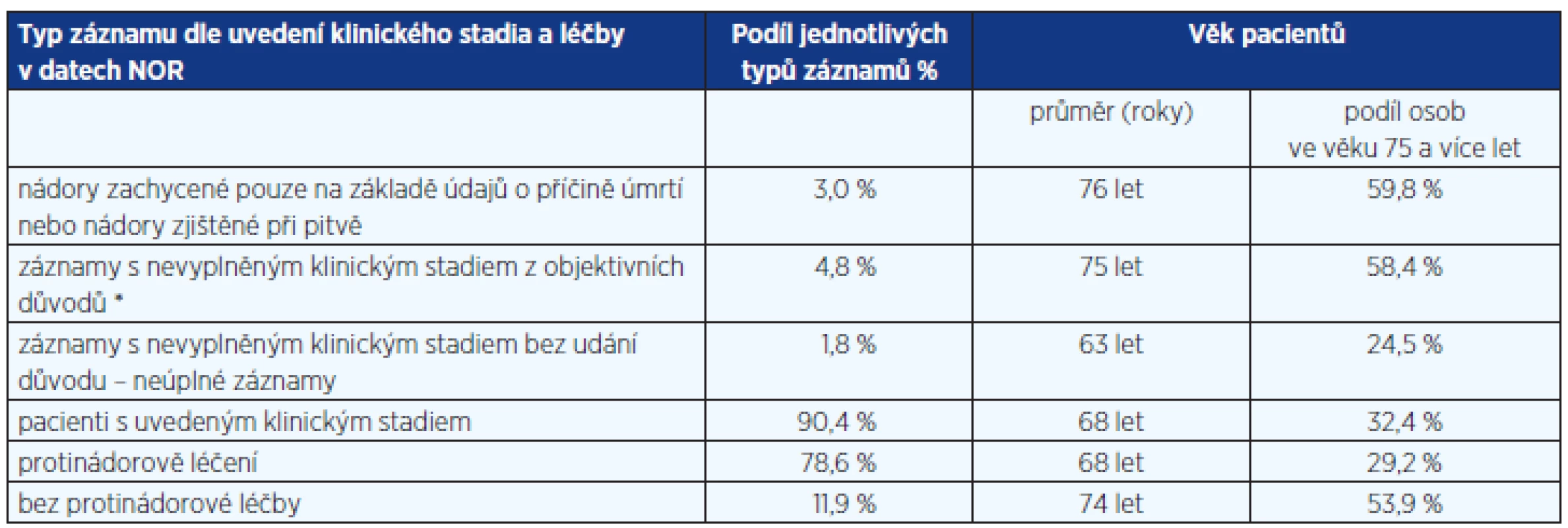
* Časná úmrtí, pacienti bez dokončené diagnostiky a určení klinického stadia, pacienti bez zahájení terapie z důvodu kontraindikace léčby, pacienti odmítající léčbu. Epidemiologie kolorektálního karcinomu v ČR: Česká republika obsazuje přední místa v mezinárodních statistikách incidence kolorektálního karcinomu. Dle studie Globocan 2008 je ČR v incidenci C18–C21 na 3. místě v Evropě u mužů, na 9. místě u žen, celkově na 3. místě. Populační zátěž je skutečně vysoká, ročně je v ČR nově diagnostikováno 7800–8200 pacientů s tímto karcinomem a 3800–4200 pacientů na něj zemře. Rovněž mortalita je na předních světových pozicích, dle studie Globocan 2008 je ČR v mortalitě C18-C21 na 3. místě u mužů, na 9. místě u žen a celkově na 3. místě v Evropě. Incidence přitom stále roste, v roce 2010 byla o 8 % vyšší než v roce 2000. I při rostoucí incidenci se v ČR podařilo stabilizovat mortalitu na toto onemocnění, což ovšem vede k nárůstu prevalence, tedy počtu žijících osob, které mají nebo měly diagnostikovaný kolorektální karcinom. Prevalence dosáhla v roce 2010 hodnoty 49 470 osob a ve srovnání s rokem 2000 tak vrostla o 64,1 %. Souhrnný přehled českých epidemiologických dat je uveden v tabulce 2.
Tab. 2. Základní epidemiologické charakteristiky nádorů kolorekta v ČR 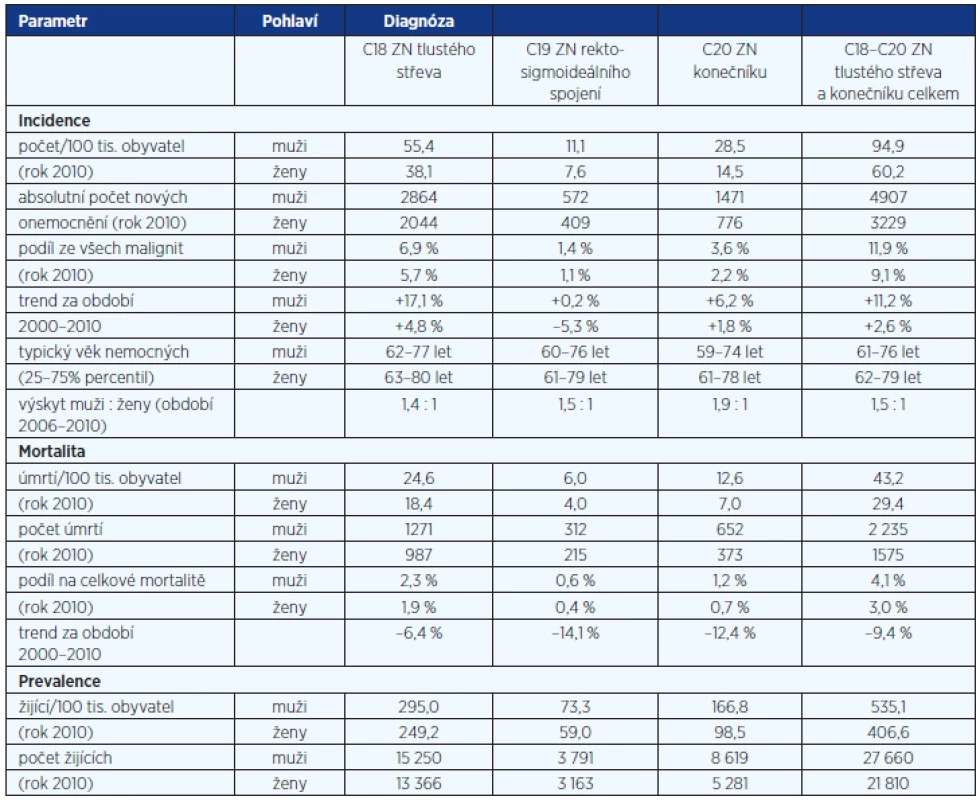
Společenské důsledky tohoto stavu jsou zřejmé. Jsou o to závažnější, že nemoc v podstatné míře postihuje pacienty v produktivním věku. Typický věk českého pacienta s kolorektálním karcinomem sice leží v intervalu 61–77 let, ale 20,5 % všech nemocných je mladších 60 let. Prudký nárůst incidence tohoto onemocnění pak začíná již po 45. roku života.
Tabulka 3 dokumentuje, že kolorektální karcinom se v ČR velmi významně podílí i na celkovém sumárním riziku onemocnění zhoubnými nádory. Hodnoty v tabulce jsou uvedeny s ohledem na tzv. naději dožití (střední délka života) v české populaci, která je 74,4 let u mužů a 80,6 let u žen (Veřejná databáze ČSÚ).
Tab. 3. Kumulativní riziko vzniku nádorového onemocnění v české populaci v období 2006–2010 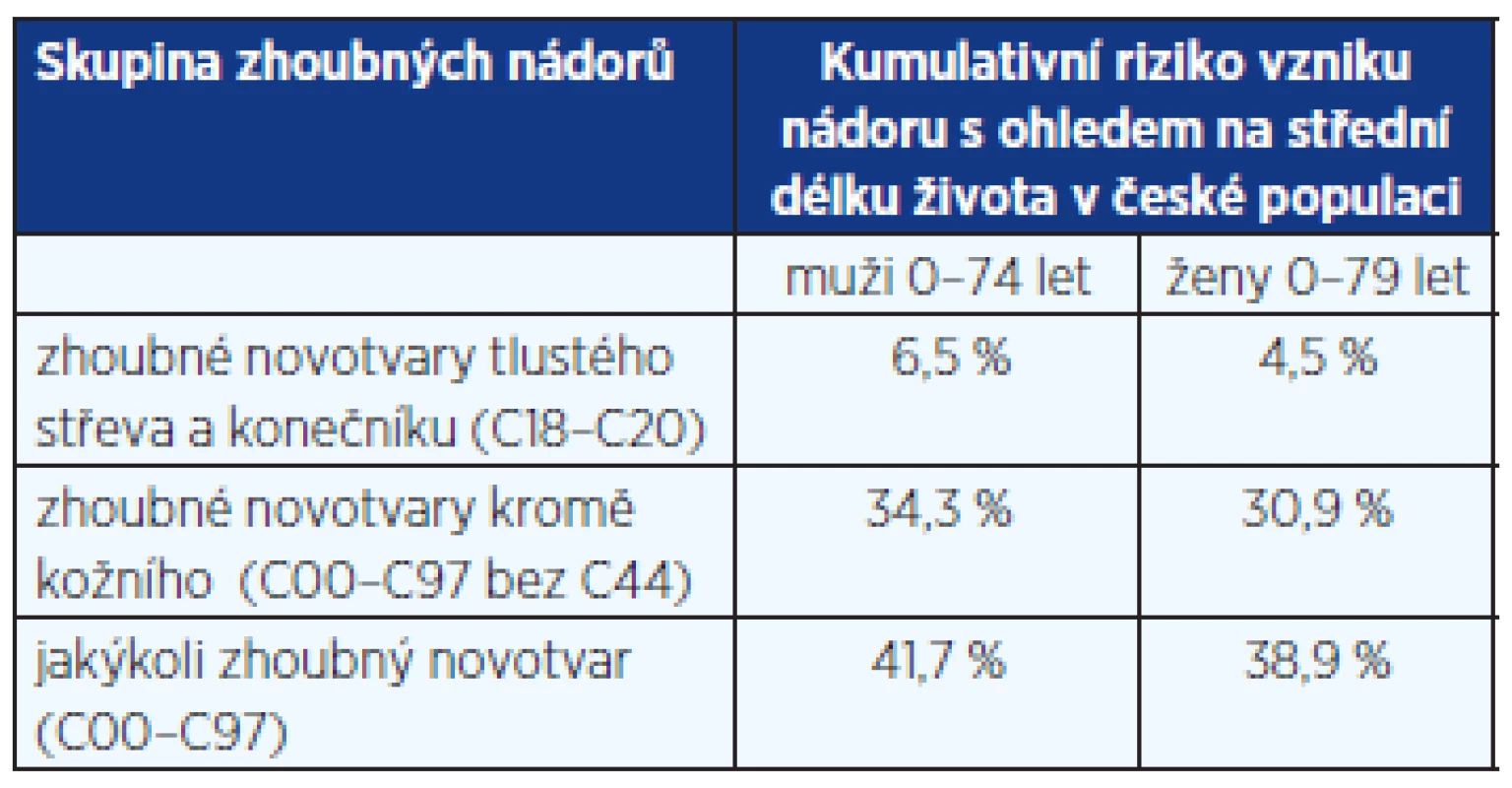
Důležitým zjištěním také je, že nádory kolorekta jsou stále častěji zjišťovány jako další primární novotvar u pacientů, kteří již dříve měli diagnostikováno jiné nádorové onemocnění (tab. 4). Zatímco v období do roku 1990 šlo o cca 6 % z celkového počtu diagnostikovaných nádorů kolorekta, v období po roce 2001 již tento podíl překročil 12–13 % a dostupná data z roku 2010 odhalují 18 % těchto onemocnění.
Tab. 4. Kolorektální karcinom jako další primární nádor u téhož pacienta dle dat NOR 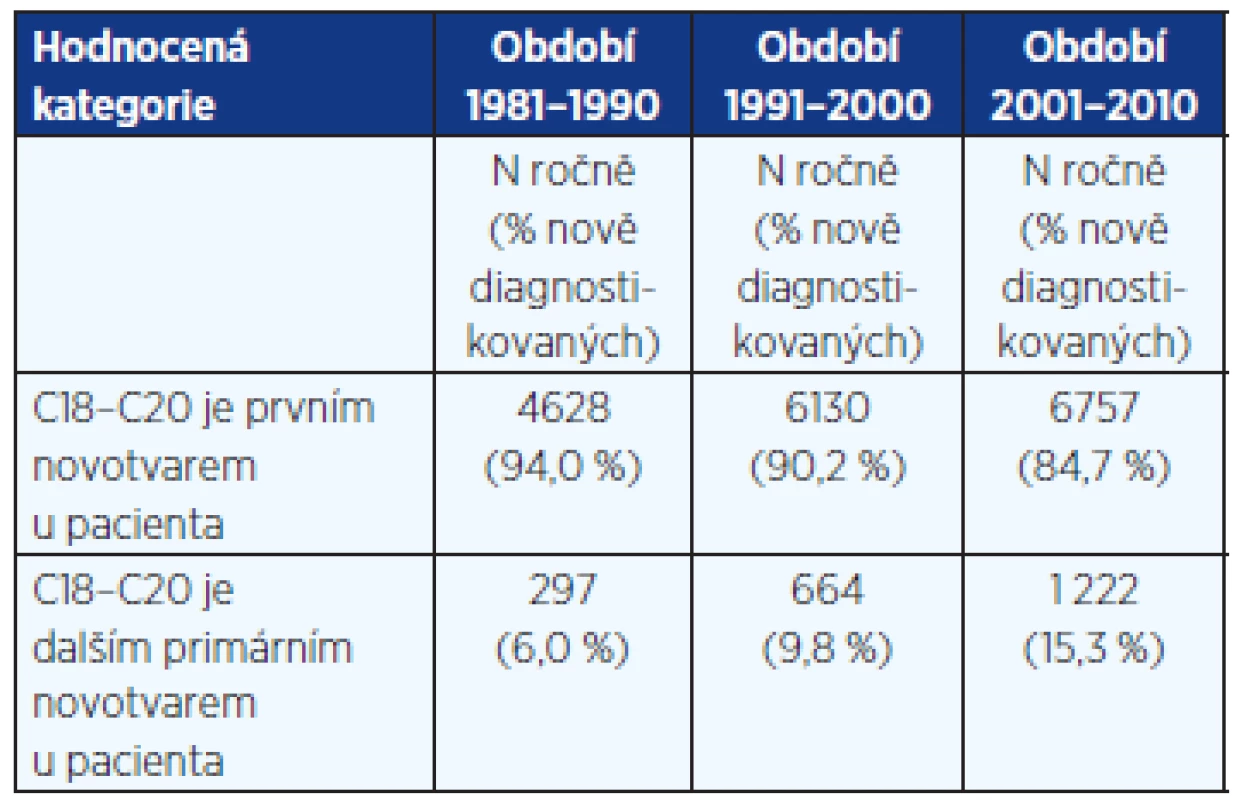
Včasná diagnostika kolorektálního karcinomu v ČR: Velmi závažnou skutečností v epidemiologii nádorů kolorekta v České republice je dlouhodobě nepříznivý poměr stadií onemocnění u nově diagnostikovaných pacientů. V ČR je téměř 50 % pacientů s kolorektálním karcinomem diagnostikováno v klinickém stadiu 3 nebo vyšším. Rovněž u nádorů kolorekta, které jsou dalším nádorem u již léčeného onkologického pacienta, pozorujeme v ČR vysoký podíl pozdě zachycených onemocnění v klinickém stadiu III nebo IV. Tento fakt významně zhoršuje celkovou prognózu pacientů a dosažitelné výsledky léčby. Nepříznivá situace se navíc v čase nijak nelepší a ani poslední dostupná data z roku 2010 nenaznačují pozitivní trend.
Český program screeningu KRK a jeho možnépopulační dopady
Suchánek Š.1, Májek O.2, Seifert B.3, Dušek L.2, Frič P.1, Zavoral M.2
1Interní klinika 1. LF UK a ÚVN, Praha
2Institut biostatistiky a analýz MU, Brno
3Ústav všeobecného lékařství 1. LF UK, Praha
Kolorektální karcinom je druhým nejčastějším maligním onemocněním ve vyspělých zemích. Vzhledem k tomu, že proces kancerogeneze sporadického karcinomu probíhá relativně pomalu, je možné tomuto onemocnění úspěšně předcházet. Národní screening kolorektálního karcinomu byl v České republice zahájen v roce 2000 a od této doby prochází kontinuálním vývojem s cílem zvýšení efektivního pokrytí cílové populace.
V současné době je asymptomatickým klientům od 50 do 54 let nabízen imunochemický test (FIT) na okultní krvácení ve stolici v jednoročním intervalu a při pozitivním výsledku je nabídnuta screeningová kolonoskopie. Od 55 let se nabízí výběr mezi pokračováním v pravidelném provádění testu na okultní krvácení, ale již ve dvouletých intervalech, nebo provedení tzv. primární screeningové kolonoskopie, která se v případě negativního nálezu opakuje za 10 let.
Z dosavadních výsledků lze konstatovat, že screeningový program kolorektálního karcinomu v ČR je plně funkční. Z posledních epidemiologických údajů je patrné, že dochází k mírnému poklesu mortality na toto onemocnění a jsou stále častěji diagnostikovány časnější formy kolorektálního karcinomu. Celkové pokrytí cílové populace screeningovými metodami (FIT, kolonoskopie) postupně narůstá, v roce 2011 činilo celkové pokrytí cílové populace 25,0 %, což je nárůst oproti roku 2010 o 2,3 %. Počet kolonoskopických vyšetření se každoročně zvyšuje. Od roku 2006 bylo provedeno celkem 108 706 screeningových kolonoskopií, adenomy byly endoskopicky odstraněny u 34 453 jedinců (32,6 %) a karcinom byl diagnostikován u 4304 pacientů (4,0 %). Na tomto trendu má zásadní podíl národní screeningový program a jeho postupné zdokonalování.
I přes velký pokrok ve vývoji screeningového programu je zde stále velký prostor ke zdokonalování, neboť programu se účastní pouze čtvrtina osob z cílové populace. Dle evropských doporučení by mělo celkové pokrytí cílové populace činit minimálně 45%. Dle posledních analýz je patrné, že počet provedených TOKS intenzivně narůstal od roku 2009, kdy došlo k zapojení gynekologů do screeningového programu a zahájení imunochemických testů na okultní krvácení. V roce 2010 došlo ke stagnaci počtu TOKS a kolonoskopií včetně diagnostikovaných karcinomů. Určitou možností zvýšení efektivity screeningového programu se zdá populační program založený na adresném zvaní cílové populace a zvyšování informovanosti a motivace jak laické, tak odborné veřejnosti.
V ČR je vybudována celostátní síť endoskopických pracovišť (Centra pro screeningové kolonoskopie), která splňují přísná pravidla kvality pro provádění preventivních kolonoskopií tak, jak je uvedeno ve Věstníku MZ ČR 01/2009. Mezi hlavní kritéria kvality patří adekvátní personální i materiální vybavení, dostatečný počet prováděných diagnostických a terapeutických kolonoskopií (minimálně 50 za rok), zkušenosti se screeningovým programem kolorektálního karcinomu. Takových center je v současné době 160 a jejich geografická distribuce pokrývá všechny kraje ČR. Akreditace center je průběžně hodnocena na základě auditů prováděných MZ ČR. Kolonoskopie patří mezi základní metody využívané ve screeningu kolorektálního karcinomu. V současnosti se dají využívat i jiné alternativní vyšetření (CT kolonografie a kapslová kolonoskopie), nicméně optická kolonoskopie zůstává zlatým standardem. Dle recentně publikovaných dat (guidelines ASGE 2012, ESGE 2012 a European Guidelines 2010) je zcela zásadní kontrola kvality kolonoskopického vyšetření na základě jasně definovaných indikátorů kvality. V současné době jsou využívány tři základní indikátory kvality: počet provedených preventivní kolonoskopií (minimálně 50 za rok), procento zachycených adenomů (adenoma detection rate, ADR, 34,9 % v roce 2012) a podíl totálních kolonoskopií (cecal intubation rate, CIR, 96,2 % v roce 2012). Většina měřitelných indikátorů kvality je v ČR monitorována a plněna.
Efektivita Českého screeningového programu je určována pomocí dlouhodobých a krátkodobých ukazatelů kvality. Zatímco krátkodobé ukazatele kvality (počet provedených TOKS a screeningových kolonoskopií, ADR a CIR) se daří dobře plnit, v dlouhodobých ukazatelích je Český program podle evropských doporučení jen částečně úspěšný. Mezi dlouhodobé ukazatele kvality, které se daří plnit, patří snížení mortality kolorektálního karcinomu a zvýšení záchytu karcinomů v časném stadiu. Mezi nedostatečně sledované parametry kvality patří sledování výskytu tzv. intervalových karcinomů (karcinom vzniklý v průběhu screeningového intervalu po screeningovém vyšetření s negativním výsledkem), problémem je dále nedostatečné celkové pokrytí cílové populace, která není ke screeningovému vyšetření adresně zvána. Z toho důvodu nelze současný program hodnotit jako populační. V ČR není možné vzhledem k legislativním podmínkám získávat individuální data (vázaná na rodné číslo jedince), a tak nelze propojit jednotlivé informační databáze (screeningová databáze, Národní onkologický registr a Národní referenční centrum). Možností jak docílit doporučovaných hodnot celkového pokrytí populace je identifikace a adresné zvaní cílové populace. Takto organizovaný program lze podle mezinárodních doporučení nazývat populační.
Velkým očekáváním je v současnosti zavedení centrálně organizovaného adresného zvaní cílové populace. Jedná se o celostátní projekt MZ ČR podporovaný z finančních zdrojů Evropské unie (EU), který bude podpořen masivní mediální kampaní. Jeho realizace je plánována na druhou polovinu roku 2013. Dalším krokem je snaha o zavedení screeningové odbornosti pro výkony v rámci screeningu kolorektálního karcinomu, jak je tomu v případě screeningu mamárního a cervikálního. Zavedení této odbornosti by zcela jistě zpřehlednilo stávající situaci v platbě za screeningové výkony a zároveň ještě zvýšilo motivaci odborné veřejnosti. Budoucnost také ukáže, jak ideálně nastavit prahovou pozitivní hodnotu (tzv. „cut off“) imunochemických testů na okultní krvácení.
Predikce budoucího vývoje počtu pacientůs kolorektálním karcinomem v ČR
Májek O., Pavlík T., Mužík J., Dušek L.
Masarykova univerzita, Brno
Navržený model využívá výhradně údajů populačního Národního onkologického registru ČR (NOR ČR). Vedle odhadu počtu nově diagnostikovaných pacientů s KRK model rovněž zahrnuje pacienty diagnostikované v minulosti, kteří nicméně ve sledovaném období prodělají terminální nebo neterminální návrat onemocnění. Navržená metoda poskytuje odhady s ohledem na rozsah onemocnění, protože právě stadium představuje klíčový stratifikační faktor s ohledem na prognózu pacienta, ale i předpokládané náklady spojené s protinádorovou léčbou.
Vzhledem k tomu, že změny v incidenci onkologických onemocnění velmi často odrážejí změny v zastoupení věkových kategorií ve sledované populaci, je v odhadu incidence zohledněna informace o vývoji věkové struktury české populace. Pro předpověď incidence je používán Poissonův regresní model ze třídy zobecněných lineárních modelů. Neméně důležitou skupinu potenciálně léčených pacientů v daném kalendářním roce tvoří pacienti diagnostikovaní v minulosti (počet těchto pacientů představuje prevalenci onemocnění), kteří budou v daném roce léčeni s relapsem nebo progresí onemocnění. Pro výpočet prevalence pacientů je používán odhad prostřednictvím analýzy přežití onkologických pacientů. Pro výpočet rizika neterminálního a terminálního návratu onemocnění byly analyzovány záznamy kontrolních hlášení NOR ČR a informace o úmrtích z příčiny KRK. Modelována byla rovněž pravděpodobnost, že pacient v určitém stadiu onemocnění podstoupí protinádorovou léčbu.
Aby byla znázorněna nejistota v budoucím vývoji sledovaných veličin, bylo zpracováno několik scénářů vývoje incidence, přežití a pravděpodobnosti protinádorové léčby. Ve srovnání s rokem 2008 model predikuje nárůst prevalence pacientů s KRK o 13–30 %. Model předpovídá, že v roce 2015 bude pro protinádorovou terapii indikováno 10 074–11 440 pacientů. Při zahrnutí všech pacientů s terminálním návratem onemocnění a všech pacientů primárně diagnostikovaných ve stadiu IV model předpovídá léčbu 3485–4469 pacientů s diseminovaným onemocněním, což představuje více než třetinu všech pacientů léčených v tomto roce s KRK.
Nabízí se otázka, jak může incidenci KRK v české populaci ovlivnit probíhající program screeningu KRK. Pro tento účel byl navržen model předpovídající přirozený vývoj onemocnění u pacientů, kterým byl v rámci organizovaného programu odstraněn při endoskopické polypektomii pokročilý adenomový polyp. Tento model předpověděl, že samotný screening může předejít v české populaci v roce 2015 přibližně 4–5 % onemocnění KRK. Důvodem spíše nižšího dopadu na populační incidenci je nízká účast a dlouhý přirozený vývoj KRK z adenomu, který způsobuje pomalejší nástup efektu organizovaného screeningu.
Metabolické rizikové faktory kolorektálního karcinomu
Šachlová M.
Gastroenterologické odd. MOÚ, Brno
Kolorektální karcinom představuje jeden z největších problémů současného zdravotnictví všech vyspělých zemí. Existují literární podklady pro tvrzení, že pacienti s DM 2. typu představují populaci se zvýšeným rizikem kolorektálního karcinomu (KRCA). Na vzniku se zřejmě podílí inzulinová rezistence. Inzulin mimo jiné stimuluje proliferaci, redukuje apoptózu buněčných linií karcinomu a podporuje růst kolorektálního karcinomu ve zvířecích modelech. Některé práce se zaměřují na hodnotu C-peptidu, kdy hladina koreluje s rizikem KRCA (Ma 2004), jiná práce korelaci s KRCA neprokázala (Wei 2005). Zdá se, že ještě důležitější roli v kancerogenezi má růstový faktor insulin-like growth factor protein IGFB-1 než hladina inzulinu (Renehan 2004). Jsou práce, které se zaměřují na hodnotu glykosylovaného hemoglobinu, další studií hladiny leptinu. Riziko narůstá i v rámci metabolického syndromu. Významný je zvláště abdominální typ obezity. Je nezbytné podporovat nejen screening kolorektálního karcinomu, ale je potřeba se zaměřit i na primární prevenci. Je potřeba vést pacienty ke změně životního stylu. Je vhodné spolupracovat s poradnami výživy a odvykání kouření, motivovat pacienty k pohybu.
Molekulární onkologie kolorektálních nádorů: Od screeningu po individualizovanou léčbu
Minárik M.
CEGES; Laboratoř molekulární genetiky a onkologie, Genomac výzkumný ústav, Praha
V posledních 10 letech došlo k významnému pokroku v oblasti poznání základních mechanismů vzniku a progrese u celé řady solidních nádorů. Současně byla identifikována řada nových molekulárních markerů a představeno jejich použití v klinické praxi. Vzhledem k vysoké incidenci bývají kolorektální karcinomy (CRC) v centru pozornosti těchto výzkumů.
Molekulární markery můžeme definovat jako alterace v genové sekvenci, změny hladin exprese nebo struktury proteinů vedoucí k nekontrolovatelnému buněčnému dělení a růstu. Zcela zásadní je, že tyto mohou být buď zárodečné (často se používá i ne zcela přesný termín vrozené), nebo somatické (též označovány jako získané). Zárodečné markery jsou v naprosté většině genové mutace, které se u vyšetřovaného pacienty nacházejí v každé buňce, tedy, pro jejich odhalení postačí libovolný vzorek z pacientova těla – většinou nesrážlivá krev. Hlavní význam zárodečných mutací je především v diagnostice hereditárních nádorových syndromů (FAP, HNPCC). Na rozdíl od zárodečných markerů jsou somatické markery vždy přítomny pouze v postižené tkáni. Pro jejich vyšetření je tedy třeba získání vzorku nádoru formou biopsie či resekátu. Na vyšetřování somatických molekulárních markerů je založena většina postupů v klinickém managementu CRC zahrnujícího screening a diagnostiku, sledování průběhu onemocnění, volbu terapie a odhad prognózy. Z hlediska využití tak můžeme markery rozdělit na 1. diagnostické, 2. identifikační, 3. prediktivní a 4. prognostické.
Diagnostické molekulární markery CRC: Význam screeningových programů pro časnou diagnostiku léčitelných stadií CRC není třeba zdůrazňovat. V posledních několika letech přibyla do spektra využitelných postupů možnost minimálně-invazivního vyšetřování molekulárního markeru SEPTIN9. Jedná se o zjištění přítomnosti metylace určitých míst v tomto genu. Kromě tohoto markeru se stále častěji hovoří i o nových generacích testů zaměřených na přítomnost molekulárních markerů ve stolici.
Identifikační molekulární markery CRC: Molekulární identifikace podtypů CRC je především založena na určení základních podtypů definujících jednak pravděpodobný mechanismus vzniku a dále i další chování. Nejčastější je tzv. mutátorový subtyp typicky se vyznačující jevem označovaným jako mikrosatelitová nestabilita (microsatellite instability, MSI), ke kterému dochází na základě poruch systému DNA oprav. V důsledku neschopnosti buňky zajistit opravu chyb při DNA transkripci dochází k celkové genetické nestabilitě, a proto se pro tento typ vžila také zkratka CIN (chromosomal instability). Většina sporadických kolorektálních tumorů vznikajících na podkladu adenomových polypů vykazuje CIN fenotyp.
Druhým molekulárním podtypem je tzv. metylátorový typ, který je charakterizován přítomností metylací specifických míst v DNA (tzv. CpG ostrůvků). Tento typ též často vykazuje přítomnost bodové mutace genu BRAF. Tento typ je označován jako CIMP (CpG island methylator phenotype) a je typický pro hyperplastické a pilovité tumory.
Prediktivní molekulární markery CRC: V roce 2008 byla odhalena zcela zásadní role aktivačních mutací genu KRAS pro účinnost (resp. neúčinnost) biologické terapie cílené na signální dráhu receptoru pro epidermální růstový faktor (EGFR). Bylo ukázáno, že nádory nesoucí některou z těchto mutací neodpovídají na terapii založenou na inhibici EGFR pomocí monoklonálních protilátek. Vyšetřování mutačního statusu genu KRAS se tak stalo prvním prediktivním testem u CRC. Nedávno byla indikační kritéria pacientů pro nasazení anti-EGFR terapie rozšířena o další dva obdobné prediktory – mutace v genech BRAF a NRAS.
Prognostické molekulární markery CRC: Mezi nejvýznamnější molekulární markery s prognostickým potenciálem (tzn. význam pro odhad přežívání pacientů, riziko relapsu či progrese onemocnění) se v současné době nejčastěji řadí cirkulující nádorové buňky (circulating tumor cells, CTC) a cirkulující volná nádorová DNA (cell-free tumor DNA, cftDNA). V obou případech se zdůrazňuje jedinečná možnost jejich vyšetřování s minimální invazivitou, neboť CTC i cftDNA se vyšetřují z periferní krve pacienta (CTC), respektive z plazmy (cftDNA). Často se v této souvislosti hovoří o tzv. tekuté biopsii (liquid biopsy), neboť získaná informace věrně odráží vlastní nádorovou tkáň.
Lze očekávat, že s pokračujícím rozvojem nových technologií pro genetickou analýzu zahrnující především další generace DNA sekvenátorů se bude okruh molekulárních nádorových markerů nadále rozšiřovat. Je však zřejmé, že pro jejich zavádění do klinické praxe a s tím související faktory (guidelines, logistika, kontrola kvality apod.) bude i nadále zcela zásadní interdisciplinární spolupráce (praktický lékař, gastroenterolog, patolog, onkolog).
SCREENING KOLOREKTÁLNÍHO KARCINOMU
Metodika adresného zvaní občanů do českého programu screeningu nádorů tlustého střeva a konečníku
Dušek L.1, Májek O.1, Ing. Blaha M.1, Suchánek Š.2, Seifert B.3,Zavoral M.2
1Institut biostatistiky a analýz MU, Brno
2Ústřední vojenská nemocnice, Praha
31. lékařská fakulta, Karlova univerzita, Praha
Význam populačního screeningu karcinomu tlustého střeva a konečníku: Karcinom tlustého střeva a konečníku (KRK) je jedním z nejčastějších nádorových onemocnění vyspělých zemí a jednou z hlavních příčin úmrtí na zhoubné nádory vůbec. Každoročně v Evropě umírá na toto onemocnění více než 200 000 osob. ČR vede společně se Slovenskem a Maďarskem evropské statistiky v incidenci i mortalitě KRK. Epidemiologickou situaci nadto podstatně zhoršuje fakt, že více než 50 % nově diagnostikovaných onemocnění je zachyceno v pokročilém klinickém stadiu III nebo IV, kdy je šance na vyléčení pacienta značně snížena. Společenské a ekonomické důsledky tohoto stavu jsou více než zřejmé a výše uvedená čísla jsou tak sama o sobě obhajobou preventivních programů zaměřených na KRK.
Nicméně zkušenosti z řady vyspělých států dokládají, že samotná existence screeningu této choroby nestačí. Ani sebelepší preventivní program nebude funkční, pokud se do něj nezapojí cílová skupina občanů. Tento problém pozorujeme i u české populace, kde sice pokrytí dosahované screeningem KRK postupně narůstá, nicméně aktuálně dosahuje pouze 25 %. To je poměrně nízká hodnota, která nemůže vést k významnému populačnímu poklesu mortality či incidence.
KRK naštěstí patří mezi preventabilní zhoubné nádory a dobře organizovaný screeningový program má velký potenciál snížit mortalitu a dokonce i incidenci tohoto onemocnění. Český program screeningu je postaven ve shodě s mezinárodními doporučeními a nabízí občanům buď dvouetapové vyšetření (od 50 let věku test na okultní krvácení do stolice a při pozitivním výsledku screeningovou kolonoskopii) anebo jednoetapové vyšetření tzv. primární screeningovou kolonoskopií (od 55 let věku). Český program je kapacitně dobře zajištěn a je garantován širokým spektrem lékařských odborností. Program má mezinárodně kompatibilní informační zázemí a veškeré informace, kontakty a výsledky jsou plně dostupné na portálu www.kolorektum.cz
Je zřejmé, že screening KRK vyžaduje zvláštní pozornost a společenskou podporu v podobě účinné propagace, zapojení společenských elit a politické reprezentace. To je ostatně v souladu se strategickými metodickými materiály a deklaracemi orgánů Evropské unie, která řadí boj s KRK mezi nejvíce prioritní oblasti zdravotnické politiky.
Screening je tedy nutné podporovat edukační a motivující kampaní tak, aby o něm cílová skupina osob věděla, rozuměla mu a neměla z něj nepodložené obavy. Jedním z klíčových opatření v této oblasti je institut státem organizovaného adresného zvaní, kdy jsou občané pravidelně zváni k účasti na screeningu a jejich odezva (participation rate) je vyhodnocována a využívána pro optimalizaci programu. Preventivní programy, které takto organizovaně zasahují celou cílovou populaci, nazýváme populační. Zavedení populačního screeningu KRK je v souladu s metodickým doporučením Rady EU i metodickými normami pro vysoce kvalitní a funkční preventivní program. Adresné zvaní je také jednoznačným vyjádřením zájmu státu a jeho politické reprezentace na daném preventivním programu.
Metodika adresného zvaní navržená pro český program screeningu KRK: V ČR neexistuje státní instituce, která shromažďuje osobní data všech účastníků zdravotního pojištění a která by tudíž mohla zajistit adresné zvaní do programu z jednoho místa. Z tohoto důvodu bylo schváleno, že adresné zvaní zajistí jednotlivé zdravotní pojišťovny, což je řešení, která má řadu výhod:
- Pojišťovny mohou přímo kontaktovat své pojištěnce, není tedy nutný žádný zdlouhavý legislativní proces při zajištění zvaní.
- Pojišťovny pracují se zdravotnickou dokumentací a jsou schopné odborně identifikovat pojištěnce, kteří mají být do programu screeningu pozváni, a vyloučit pacienty, pro které screening určen není (např. těžce nemocné osoby, jejichž účast ve screeningu není možná apod.).
- Pojišťovny mají organizační i odborné zkušenosti s realizací různých informačních kampaní a s jejich udržitelností.
- Pojišťovny jsou schopny přímo zjistit výsledný efekt zvaní, opět analýzou svých databází.
Adresné zvaní bude tedy realizováno na straně zdravotních pojišťoven, a to s využitím jejich stávajících databází a informačních systémů, u kterých se předpokládá dílčí rozšíření za účelem realizace agendy zvaní pojištěnců do screeningových programů. Nicméně většina potřebných údajů je již v databázích plátců běžně přítomna a bude možné je využít. Výběr zvaných pojištěnců a systém jejich zvaní bude řízen jednotnou metodikou, která definuje závazná minimální společná pravidla a zajistí stejnou dostupnost screeningových programů pro všechny občany ČR. Zejména jde o tato pravidla:
- Kdo má být pojišťovnami pozván do screeningového programu a kdo může být vyloučen ze zvaní.
- Systém vyhodnocení a kritéria pro vyhodnocení účinnosti zvaní.
- Časový rámec zvaní a opakovaného zvaní.
- Formát dat předávaných za účelem vyhodnocení úspěšnosti screeningu a pravidla pro jejich předání.
Přijatá metodika definuje především následující fáze procesu adresného zvaní:
- výběr pojištěnců vhodných pro zvaní do screeningu
- obsah zvacího dopisu
- zpětnou kontrolu účinku zvaní (zapojení pozvaného pojištěnce do screeningu, absolvovaná vyšetření, výsledek vyšetření – pozitivita TOKS, diagnostické nálezy),
- podmínky pro opakované zvaní klienta screeningu,
- hodnocení výsledků adresného zvaní na populační úrovni.
Základním předpokladem úspěchu zvaní je precizní specifikace způsobilosti pojištěnců k pozvání do screeningového programu a specifikace kritérií pro vyřazení pojištěnce z tohoto procesu. Souhrn těchto kritérií, který vychází z konsenzu expertního týmu připravujícího realizaci adresného zvaní, byl jasně specifikován a promítnut do algoritmů využívaných při prohledávání datových skladů jednotlivých pojišťoven. Všichni pojištěnci, kteří splní zařazovací kritéria daného screeningového programu a současně nebudou z procesu vyřazeni na základě dalších níže definovaných podmínek, budou obesláni konkrétní variantou zvacího dopisu.
Pojištěnec bude zařazen do procesu adresného zvaní do screeningu KRK, pokud:
- Je pojištěncem dané ZP alespoň 4 roky.
- Je ve věku od 50 let včetně do 70 let včetně.
Pojištěnec bude vyřazen z procesu adresného zvaní do screeningu KRK, pokud:
- Je cizinec.
- Je občan ČR dlouhodobě pobývají v cizině.
- Nemá úplnou adresu v databázi pojišťovny, např. PSČ 000 00, nebo má adresu na P.O. Box, případně je u něj evidována nedoručitelnost zásilek.
- Byl již pozván na konkrétní screeningový program před 11 a méně měsíci (zvažovat kalendářní měsíce, ne skutečný odstup).
- Má vykázané výkony/diagnózy dle klíče uvedeného v tab. 3.
- Má vykázané náklady na léčbu během posledních 365 dní nad 1 mil. Kč (náklady se rozumí suma všech vykázaných nákladů na ambulantních, hospitalizačních dokladech, na žádankách a receptech; 1 bod je jedna koruna).
Z výše uvedených kritérií je zřejmé, že adresné zvaní organizované zdravotními pojišťovnami se bude týkat občanů, kteří se screeningu KRK dosud neúčastnili nebo svou účast přerušili v posledních 3–5 letech. Vzhledem ke zpoždění, se kterým plátci zdravotní péče obvykle obdrží k-dávky od zdravotnických zařízení (až tři měsíce), není možné zejména kritéria pro vyřazení nikdy určit zcela přesně v souladu s realitou. Kritéria tedy budou v daném časovém okamžiku vyhodnocována ve vztahu k aktuálně dostupným datům. Určité chybovosti ve vyhodnocování kritérií se tedy nelze vyhnout a je očekávanou součástí procesu adresného zvaní. Případné rozpory budou ošetřeny v textu zvacích dopisů.
Aby byly kohorty pozvaných občanů nově vstupujících do programu kapacitně zvládnutelné, byl nastaven následující systém a časový rámec zvaní:
- Průběžně budou zváni občané dle měsíce jejich narození; tím dojde k rovnoměrnému rozložení zátěže v průběhu roku.
- Ověření, zda se pozvaný pojištěnec dostavil do screeningu, či nikoliv, provede pojišťovna dle svých záznamů vždy po roce od odeslání dopisu.
- Pokud se zvaný pojištěnec nedostavil do screeningu (tzn. nebyl u něj vykázán žádný z kódů označujících screeningové testy), bude pozván opakovaně.
Proces adresného zvaní, bude-li mít v populaci pozitivní odezvu, značně navýší zátěž zapojených klinických odborností, především specialistů v první linii poskytování péče, tedy praktických lékařů a gynekologů. Zvýšená kapacita musí být k dispozici také v akreditovaných kolonoskopických centrech (www.kolorektum.cz). Odezva populace, narůstající počty vyšetření a jejich výsledky budou průběžně hodnoceny pomocí již vybudovaného a implementovaného informačního zázemí pro screening KRK. Na hodnocení se budou podílet všechny subjekty zapojené do procesu zvaní a do realizace screeningu, včetně plátců péče prostřednictvím Národního referenčního centra (www.nrc.cz).
Závěrem je nutné zdůraznit, že sama administrace adresného zvaní je sice náročná, ale představuje jen malou část nákladů, které bude nutné při navýšení účasti občanů ve screeningu investovat. Zvána bude část populace, která se preventivních vyšetření dlouhodobě neúčastní, a tudíž lze očekávat zvýšený podíl pozitivních nálezů jak při vyšetření pomocí TOKS, tak u kolonoskopií. Po určitou přechodnou dobu může dokonce dojít k nárůstu incidence vlivem zvýšeného záchytu kolorektálních karcinomů (harvesting effect). Tyto investice jsou však nezbytným vkladem, který se dlouhodobě vrátí v podobě klesající incidence a mortality na kolorektální karcinom a v podobě rostoucího podílu včasně zachycených onemocnění, jejichž léčba je řádově méně finančně náročná než u pokročilých klinických stadií.
Vývoj a implementace metodiky adresného zvaní do screeningových programů ČR jsou podpořeny projektem „Zajištění informační podpory a hodnocení kvality programů screeningu zhoubných nádorů v České republice“ v rámci programu Národní akční plány a koncepce Ministerstva zdravotnictví, 2013.
Praktičtí lékaři a gynekologové v českém screeningu KRK – zamyšlení nad daty
Seifert B.1, Dušek L.2, Májek O.2, Král N.1
11. lékařská fakulta UK, Praha
2Institut biostatistiky a analýz, Brno
Východisko: Změna ve screeningu kolorektálního karcinomu (KRK) byla zavedena Věstníkem MZ ČR č. 01/2009 (s. 20–23): Standard při poskytování a vykazování výkonů screeningu nádorů kolorekta v ČR s cílem oživit stagnující program, ve kterém účast nepřesáhla 20 % a jehož efektivita nebyla uspokojivá. Nová metodika, kromě každoročního testování ve věkovém intervalu 50–55 let, uvedení imunochemických testů a screeningové kolonoskopie jako volby v 55 letech, zapojila do screeningu testem na okultní krvácení ve stolici (TOKS) vedle všeobecných praktických lékařů (VPL) také ambulantní gynekology (AG). Předmětem sdělení je analýza aktivit VPL a AG ve screeningu KRK.
Metodika: Aktivity VPL a AG ve screeningu lze sledovat a hodnotit na základě dat, poskytovaných pojišťovnám formou kódů výkonů „15120 – Stanovení okultního krvácení ve stolici speciálním testem v rámci screeningu KRK – nález negativní“ a „15121 – Stanovení okultního krvácení ve stolici speciálním testem v rámci screeningu KRK – nález pozitivní“. Pojišťovny předávají kódy Národnímu referenčnímu centru, které je agreguje a k centrálnímu vyhodnocení poskytuje Institutu biostatistiky a analýz Masarykovy univerzity (IBA MU). Analýzy umožňují sledovat následující indikátory:
- celkový počet provedených TOKS v ordinacích VPL a AG,
- počet provedených TOKS v ordinacích PL a AG podle věku a pohlaví,
- pokrytí cílové populace TOKS; celkové, podle věku a pohlaví,
- regionální odlišnosti v pokrytí TOKS; celkové, podle věku a pohlaví,
- pozitivita testu na okultní krvácení; celková, podle věku, pohlaví a region,
- výše uvedené indikátory v historických trendech.
Výsledky screeningu v datech 2010–2011: Počet vydaných a vyhodnocených TOKS narůstá, s akcelerací po zavedení nového standardu v roce 2009. V roce 2011 proplatily pojišťovny 527 470 TOKS. Nárůst lze zdůvodnit zvýšením frekvence TOKS mezi 50. a 55. rokem, používáním přijatelnějších imunochemických testů a zapojením gynekologů. Od roku 2010 je patrná stagnace, která naznačuje, že oportunní program 2,3 narazil na hranice svých možností, které nebudou překročeny bez zavedení adresného zvaní. Současné pokrytí je 25 % cílové populace nad 50 let, resp. 30 % v mezinárodně srovnatelné skupině 60–69 let. Ke zvýšení pokrytí došlo ve všech okresech ČR, nicméně variabilita přetrvává.
Celkový podíl gynekologů na provedených TOKS činil v roce 2009 3,6 %, v roce 2010 8,3 % a v roce 2011 7,9 %. Zatímco v roce 2009 dosáhl 6,2%, v roce 2010 to bylo 14,1 %. Podíl se dále nezvyšuje, v roce 2011 klesl na 13,3%. Ve věkové skupině 50–54 let provedou gynekologové 23 % všech TOKS u žen, zatímco s přibývajícím věkem podíl rovnoměrně klesá. Variabilita v krajích je výraznější v celkovém pokrytí, než v podílu gynekologů. Z podrobnější analýzy dat ale vyplývá, že zhruba v 25 % okresů se gynekologové do screeningu téměř vůbec nezapojili. Celkově zaznamenáváme vzestup pozitivity TOKS až k hodnotě 6,7% v roce 2011. Míra pozitivity TOKS u gynekologů z původních téměř 10 % spíše klesá, nicméně zůstává vyšší o zhruba 2 % než u VPL.
Diskuze: Všeobecní praktičtí lékaři hrají ve screeningu KRK v ČR klíčovou roli. Ambulantní gynekologie má z hlediska screeningových programů v ČR unikátní postavení, protože je přímo nebo nepřímo zapojena do všech tří aktuálně probíhajících. Zapojení gynekologů do screeningu KRK není výsadou ČR; v USA je součástí doporučení gynekologické společnosti. Někteří gynekologové v USA provádějí i sigmoideoskopii. Podobně je zapojení gynekologů (a urologů) zvažováno i v Německu.
Zapojení gynekologů přispělo k oživení screeningu a ke zvýšení účasti žen, zejména ve věkové skupině 50–54 let. Teoreticky mohou být prostřednictvím žen motivováni k vyšetření jejich manželé.
Vyšší míra pozitivity TOKS je dána přechodem na imunochemické testy, což od počátku charakterizuje testování u gynekologů. Do určité míry může hrát roli také menší zkušenost gynekologů s TOKS, případně zařazování symptomatických pacientek.
Zapojení gynekologů lze doporučit i mezinárodně v zemích s podobnou strukturou zdravotní péče. Podle mezinárodních zkušeností lze předpokládat, že po zavedení adresného zvaní agenda TOKS v ordinacích VPL a gynekologů poroste o 10–30%.
Evropské zkušenosti s FIT testy
Kocna P.
Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN, Praha
Souhrnné review je zaměřeno na screening CRC metodou FIT – imunochemické detekce okultního krvácení ve stolici. Analyzováno bylo 152 odborných publikací zveřejněných během posledních 5 let (2008–2013) a tato prezentace sumarizuje zkušenosti evropských zemí.
Španělská multicentrická, prospektivní studie na souboru 5595 osob (Int J Cancer. 2013) prokázala, že provedení dvou testů nezvýší diagnostickou přesnost, ale zvýší cenu, počet nutných koloskopií a také počet nalezených lézí. Optimální nalezená cut-off je 115 ng/ml.
Skotská studie s rozesláním 1 kazety OC-Sensor 66 225 osobám ve věku 50–74 (J Clin Pathol. 2013) prokázala vysokou návratnost testu – 60,6% a skutečnost, že koncentrace f-Hb je ve vztahu k závažnosti a stádiu CRC a současně je ve vztahu k velikosti lézí.
Irská studie s poštovním rozesláním 2 testů OC-Sensor 9704 osobám ve věku 50–74 let (Colorectal Dis. 2013) měla návratnost 52 % a prokázala, že při provedení jen jednoho testu je procento nezachycených karcinomů 17,6 % a neoplazií včetně pokročilých adenomů 30 %.
Německá studie (Eur J Cancer. 2013) porovnávala spolehlivost ELISA FIT testů s detekcí Hb nebo Hb/Hpt a automatizované analýzy s OC-Sensorem, u které prokázali nejvyšší záchyt neoplazií, 73,3 % pro CRC a 25,7 % pro pokročilé adenomy.
Slovinská studie (Eur J Cancer Prev. 2013) na souboru 9189 osob ve věku 65–69 let, kterým byly poštou zaslány dvě odběrové kazety pro MagStream HT, měla návratnost kitů 90,8 %, pozitivitu 7,4 %, adenoma detection rate 53,8 % a 73,3 % nalezených CRC bylo ve stadiu Dukes I or II.
Francouzská studie (Gastroenterology 2013) analyzovala soubor 19 797 osob ve věku 50−74 let, které provedly tři testy, ve třech stolicích – guajakový test, MagStream a OC Sensor, který prokázal nejvyšší spolehlivost a nejvyšší záchyt osob s CRC.
Holandská studie (Int J Cancer 2013) podrobně analyzuje vyšetřený soubor osob z hlediska rizikových faktorů pro falešnou negativitu FIT testu – 5,8 % nebo falešnou pozitivitu FIT testu – 5,9 %, je-li screening proveden jedním FIT testem OC-Sensor s cut-off hodnotou 50 ng/ml.
Belgická studie (Cancer Epidemiol 2012) porovnávala na souboru 19 542 rezidentů Flanders, ve věku 50–74 let, dvě strategie screeningu. Prokázala, že zasílání kazety OC-Sensor poštou má signifikantně vyšší návratnost 52,3 % s detekcí neoplazií a CRC 2,86 % než strategie zvaní osob k praktickým lékařům.
Italská studie (Clin Gastroenterol Hepatol 2012) analyzovala význam opakovaného FIT testu na souboru 9800 obyvatel, kterým byl FIT test nabízen ve čtyřech cyklech, v letech 2001, 2003, 2006 a 2008.
Česká pilotní studie byla provedena ve VFN a FTN na souboru 815 nemocných indikovaných ke kolonoskopii (Biomed Pap 2012) a doporučuje pro screening v ČR provedení jednoho FIT testu při cut-off hodnotě 75 ng/ml.
Kvantitativní imunochemická detekce okultního krvácení ve stolici se stává primárním screeningovým testem pro kolorektální karcinom. Kvantitativní analýza vyžaduje zajištění přesného a správného měření koncentrace hemoglobinu ve stolici. Systém externí kontroly kvality tuto spolehlivost ověřuje a v ČR je nabízen od ledna 2012.
Centrum pro screeningovou kolonoskopii – výhody a nevýhody
Vítek P., Mikoviny Kajzrlíková I., Chalupa J., Kuchař J.
Beskydské gastrocentrum, Interní oddělení, Nemocnice ve Frýdku-Místku
LF, Ostravská Univerzita v Ostravě
Od počátku 2009 došlo k úpravám parametrů screeningu kolorektálního karcinomu (KRK) v ČR, které zahrnovaly kromě screeningové kolonoskopie, prováděné při pozitivitě na okultní krvácení u asymptomatických jedinců ve věku 50–54 let, také primární screeningovou kolonoskopii od 55 let bez nutnosti předchozího vyšetření testu okultního krvácení. Uvedená změna vedla k významnému zvýšení počtu prováděných kolonoskopií. K realizaci praktického provádění endoskopického screeningu nyní slouží síť endoskopických pracovišť (Centra pro screeningovou kolonoskopii). Aktuální seznam center je možno nalézt na webu www.kolorektum.cz
Hlavním motivem pro vznik těchto center bylo zajištění standardní kvality screeningového kolonoskopického vyšetření pro vyšetřované pacienty. V roce 2010 byla publikována Evropská doporučení pro screening KRK, v roce 2012 pak podrobné stanovisko Evropské společnosti gastrointestinální endoskopie (ESGE) pro kvalitu screeningové kolonoskopie. Přehled parametrů těchto doporučení je možno nalézt v tabulce 1, český překlad kompletního doporučení je pak k dispozici na stránkách Endoskopické sekce České gastroenterologické společnosti www.endoskopiste.cz
Tab. 1 Kvalita ve screeningové kolonoskopii – přehled doporučených indikátorů ESGE (2012) 
Na základě praktických zkušeností můžeme hovořit o řadě výhod, které ustanovení Center pro screeningovou kolonoskopii endoskopickým pracovištím přineslo. Došlo k pozitivní propagaci endoskopických pracovišť v rámci jejich regionů, kvalitní technické i personální vybavení jednotlivých jednotek se stalo významným tématem pro managementy nemocnic i ambulantních zařízení. Pro vedoucí endoskopických pracovišť byla existence centra podnětem pro zavádění standardizovaných systémů sledování kvality, které lze využít i pro ostatní kolonoskopie a další endoskopické metody. Cílem těchto systémů kontroly kvality endoskopických vyšetření je dosažení standardního výstupu z kolonoskopického vyšetření pro pacienta. Hovoříme o systémech srovnávání (benchmarking) jednotlivých endoskopistů se snahou o minimalizaci interindividuální variability kvality screeningové kolonoskopie v rámci pracoviště. Realizace kontroly kvality kolonoskopie zahrnuje především sledování a dokumentaci ADR (adenoma detection rate), prohlížecího času, procenta dosažení céka a evidenci komplikací výkonu.
Kód primární screeningové kolonoskopie 15105 pak pro gastroenterology a ostatní lékaře přinesl možnost přímé indikace endoskopického vyšetření u asymptomatického pacienta ve věku nad 55 let bez nutnosti vymýšlení „symptomů“. Dostupnost kolonoskopie v centrech je v současnosti dobrá, na pracovišti autora tvoří screeningové výkony 18 % všech prováděných kolonoskopií.
Zajištění vysoké kvality endoskopického vyšetření v centru s sebou logicky přináší i nemalé finanční náklady. Financování endoskopické části screeningu ze strany zdravotních pojišťoven však za pokroky v endoskopické části screeningu KRK pokulhává. V současném systému úhrad jsou sice kódy screeningové kolonoskopie 15101 a 15105 vyjmuty z regulace objemu a degresivní hodnoty bodu, toto ovšem neplatí pro asociované výkony (biopsie, polypektomie, endoskopická mukózní resekce). Pro zdravotnická zařízení navíc spadají i tyto screeningové kolonoskopie do hodnoty celkového ambulantního paušálu. Část nalezených neoplastických lézí si také vyžaduje terapeutické řešení ve druhé době, které je ovšem vykazováno jako běžná kolonoskopie se všemi regulacemi, z toho vyplývajícími. Je tedy zřejmé, že tento způsob financování endoskopického screeningu KRK není dlouhodobě udržitelný. Významné zlepšení současné situace by mělo přinést přijetí nového Seznamu výkonů, který již obsahuje biopsii a polypektomii, asociované se screeningovou kolonoskopií.
V odborné části je organizačně velmi obtížná praktická realizace ESGE doporučené evidence pozdních komplikací, která by vyžadovala přímý kontakt s každým pacientem 30 dnů od výkonu. Běžné jsou také případy pacientů, u kterých jsou přes negativní výsledek primární screeningové kolonoskopie nadále prováděny testy na okultní krvácení do stolice a v případě pozitivity jsou pacienti opět odesíláni ke kolonoskopii. V těchto případech je zbytečně zatěžován zdravotní systém i pacient případnou komplikací výkonu. Není také zcela jasné, jaký je v současném screeningu podíl pacientů s vyšším rizikem (například příbuzní I. stupně nemocných s KRK), u kterých je indikace ke kolonoskopii časnější než v 55 letech. Přehled výhod a nevýhod současné praxe je uveden v tabulce 2.
Tab. 2 Výhody a nevýhody statutu Centra pro screeningovou kolonoskopii 
Klíčové indikátory kvality v programu screeningu kolorektálního karcinomu
Májek O., Dušek L.
Masarykova univerzita, Brno
V ČR je v souladu s doporučením Rady EU nabízen program screeningu kolorektálního karcinomu (KRK). Tento program je dle výsledků zahraničních klinických studií účinný při snižování mortality i incidence tohoto závažného nádorového onemocnění v cílové populaci. Příznivá bilance mezi přínosy a riziky doložená v rámci pečlivě organizované klinické studie ovšem sama o sobě nezaručuje obdobnou prospěšnost v cílové populaci v rámci screeningového programu určeného pro širokou veřejnost.
Pro zajištění vysoké kvality organizovaného screeningového programu sestavila v roce 2010 Evropská komise ve spolupráci s Mezinárodní agenturou pro výzkum rakoviny dokument European Guidelines, který se vedle doporučeného poskytování screeningového procesu zabývá i jeho monitoringem a vyhodnocením. Cílem tohoto sdělení je diskutovat proveditelnost hodnocení českého programu prostřednictvím indikátorů kvality definovaných ve zmíněném dokumentu.
Pro monitoring programu je k dispozici několik nezávislých datových zdrojů. Předpokladem hodnocení zátěže populace zhoubnými nádory je kvalitní onkologický registr. Národní onkologický registr ČR sbírá podrobné údaje o diagnostikovaných onemocněních již od roku 1977. Protože výkony související se screeningem KRK jsou v ČR hrazeny z veřejného zdravotního pojištění, jsou údaje vhodné k hodnocení screeningových testů dostupné v datových skladech plátců zdravotní péče, pro analýzu jsou pak agregovaná data poskytována Národním referenčním centrem. V neposlední řadě je pro monitoring programu k dispozici Registr screeningu KRK (vedený Institutem biostatistiky a analýz MU), do kterého podrobné údaje o provedených vyšetřeních vkládají všechna endoskopická pracoviště doporučená ke screeningu KRK.
Dokument European Guidelines rozeznává časné indikátory kvality a dlouhodobé indikátory dopadu programu. Časné indikátory jsou pak rozděleny do skupin týkajících se pokrytí cílové populace programem, výsledků screeningu prostřednictvím testu na okultní krvácení do stolice (TOKS) a prostřednictvím primární screeningové kolonoskopie. Pokrytí cílové populace a pozitivitu TOKS lze monitorovat prostřednictvím dat PZP o provedených screeningových testech. Vysoce kvalitní databáze preventivních kolonoskopií umožňuje monitorovat záchyt nádorů a prekanceróz (pozitivní prediktivní hodnota TOKS, detekční míra primární screeningové kolonoskopie), zastoupení totálních kolonoskopií, rozdělení klinických stadií diagnostikovaných nádorů a míru závažných komplikací při endoskopickém vyšetření. Tento systém navržený pro monitoring programu v ČR byl již publikován i v mezinárodním periodiku, tato publikace rovněž zahrnovala výsledky programu z let 2006–2011.
Vzhledem k tomu, že program v ČR prozatím není populační, osoby z cílové populace nejsou adresně zvány a chybí legislativní rámec pro evaluaci screeningového procesu prostřednictvím individuálního propojení různých datových zdrojů (populační, onkologický a screeningový registr). Z tohoto důvodu nelze prozatím hodnotit indikátory týkající se adresného zvaní, detekční míru screeningu TOKS, hodnocení intervalových karcinomů a provádět univerzální epidemiologické studie dlouhodobého dopadu programu na cílovou populaci.
Zavedení populačního screeningového programu zahrnujícího adresné zvaní je plánováno na závěr roku 2013. Nedílnou součástí zvacího procesu bude i monitoring míry účasti pozvaných osob. V souvislosti s rozšířením datových zdrojů pro monitoring je plánován i export plátců zdravotní péče, který by umožnil monitoring anonymizovaných individuálních dat a umožnil tak rozšířit aktuální možnosti systému informační podpory programu screeningu KRK.
KOLOREKTÁLNÍ KARCINOM A IBD
Rizika, prevence a screening kolorektálního karcinomu u idiopatických střevních zánětů
Douda T.
II. interní gastroenterologická klinika, FN Hradec Králové
Idiopatické střevní záněty – ulcerózní kolitida a Crohnova choroba patří do skupiny onemocnění spojené s vysokým rizikem vzniku kolorektálního karcinomu. Tato skutečnost je dlouhodobě známa již z poloviny 20. století. Časné studie z terciálních center udávaly vysoké riziko, recentní studie ukazují riziko nižší. V současné době je považováno relativní riziko vzniku kolorektálního karcinomu asociovaného s kolitidou za 2–3krát vyšší než u všeobecné populace. Proti sporadickému kolorektálnímu karcinomu vzniká o 10–20 let dříve (průměrný věk v době diagnózy 43 let). Mortalita na kolorektální karcinom u IBD pacientů se ale v posledním desetiletí se snížila a neliší se od všeobecné populace. V patogenezi vzniku karcinomu asociovaného s kolitidou se podílí velké množství pozitivních i negativních regulátorů odlišných od regulátorů při vzniku sporadického kolorektálního karcinomu, stejně tak projevují jiné molekulární cesty vedoucí k maligní transformaci tkáně epiteliálních buněk. Riziko vzniku karcinomu závisí nejen na době trvání onemocnění, ale zvyšuje ho také extenzivní postižení tračníku, mladý věk v době diagnózy, pozitivní rodinná anamnéza kolorektálního karcinomu, přítomnost aktivního zánětu a zánětlivých pseudopolypů. Riziko vzniku kolorektálního karcinomu můžeme snížit třemi možnostmi. Definitivním řešením je kolektomie (s ileostomií, ileorektoanastomózou nebo ileo-pouch-anální anastomózou). Chirurgický výkon má svá rizika a je pro pacienta částečně mutilující. Další možností je dlouhodobá aplikace chemopreventivně působících látek. Vlastní nádorová transformace probíhá pomalu a odhaduje se na 7–10 let. Nicméně výsledky chemoprevence kolorektálního karcinomu u idiopatických střevních zánětů jsou kontroverzní. Existují dostatečné důkazy pro doporučení medikace 5-aminosalicylátů v rámci chemoprevence v dávce větší než 1,2 g/denně. Efekt mesalazinu je nejen protizánětlivý, ale inteferuje s mnoha molekulárními cestami vzniku nádoru. Histologická intenzita zánětu je dalším nezávislým rizikovým faktorem vzniku karcinomu, a proto slizniční zhojení při medikaci imunomodulátory a biologiky může bránit vzniku karcinomu asociovaného s kolitidou. Nicméně pro použití thiopurinů v chemoprevenci nejsou dostatečné údaje. Poslední dvě studie z roku 2010 a 2011 ukazují na snížení incidence neoplazie. Kyselina ursodeoxycholová pravděpodobně u pacientů s asociovanou primární sklerózující cholangoitidou snižuje riziko vzniku karcinomu ve standardním dávkování, zejména ve vysokých dávkách je ale její podávání kontroverzní. Podávání kyseliny listové je ponecháno na uvážení lékaře. Třetím možným řešením je provádění dispenzárního programu, jehož základem jsou pravidelné koloskopické kontroly se snahou časné detekce dysplazie. Optimální strategie endoskopického sledování se různě liší dle doporučení jednotlivých gastroenterologických a endoskopických společností. V Evropě se většinou respektuje doporučení Britské gastroenterologické společnosti nebo doporučení ECCO (Evropské společnosti pro Crohna a kolitidu). V doporučeních jsou nemocní stratifikování dle individuální míry rizika a částečně reflektují změny praktického provádění dispenzarizace a strategie endoskopické léčby. Původní a stále uznávaná strategie necílených biopsií vznikla v období vláknové endoskopie, kdy se považovala plošná dysplazie za nedetekovatelnou. V současné době při užití vysokorozlišovacích videoendoskopů a při použití chromoendoskopie a zvětšovacích technik (zoom) je možné tyto dysplazie detekovat. Při použití těchto technik se umožní výrazně snížit počet biopsií a vhodné léze endoskopicky odstranit bez nutnosti indikace kolektomie. Endoskopické sledování má výrazný efekt v časné diagnostice kolorektálního karcinomu, zlepšení výsledků léčby a lepších výsledků přežívání pacientů.
Gastrointestinální ekosystém, zánět, kolorektální karcinom a probiotika
Frič P.
Interní klinika ÚVN – Vojenské fakultní nemocnice a 1. LF UK, Praha
Gastrointestinální ekosystém: Tento název označuje vysoce integrovaný komplex, který zahrnuje střevní mikrobiota (SM), slizniční imunitní systém (SIS) a střevní slizniční bariéru (SSB). GIE zajišťuje nositeli výživu, látkovou přeměnu a regulaci slizniční a systémové imunity. Jednotlivé složky se mohou vyvíjet samostatně jen zčásti. Jejich úplná morfologická a funkční vyzrálost vyžaduje četné interakce, mezi nimiž je křehká rovnováha. Systém SM je postnatálně získaný orgán, který využívá velký povrch střeva s množstvím nutričních substrátů. Metabolická aktivita SM je srovnatelná s metabolismem jater. Jeho vývoj v časném dětství je rozhodující pro vývoj a vyzrávání SIS. SM a SIS společně mají kritický význam pro vývoj SSB tvořené střevními epiteliemi a tzv. těsnými spojeními mezi nimi.
SM vykazují gradient kvantitativní a kvalitativní, jakož i proximodistální a radiální (lumen – střevo). V jejunu je 103–104 mikrobů/g střevního obsahu a koncentrace vyšší než 105 je označována jako dysbióza, tj. kvantitativní i kvalitativní odchylka. V ileu je však považována za fyziologickou hodnota 107 a v Bauhinské chlopni a těsně nad ní 109. Současně přibývá aborálně anerobních mikrobiotů, které převažují v tračníku a v rektu dosahují mikrobiota koncentrace 1012. SM významně ovlivňují prostřednictvím svých metabolitů funkce a vývoj střeva. Epitel je denně exponován komenzálním mikrobiotům, jejichž antigeny vyvolávají fyziologickou zánětlivou odpověď střevní sliznice. Tato odpověď není škodlivá. Indukuje sekreci imunoglobulinu A (IgA) a tzv. orální toleranci, tj. potlačení humorální odpovědi na určitý antigen po předchozím podání téhož antigenu. Tolerance je zprostředkována antigen-prezentujícími buňkami a T-lymfocyty. Mezibuněčná signalizace je kritická pro zachování morfologie a funkcí SSB. Poruchy těchto mechanismů vedou k prozánětlivé odpovědi, která je součástí patogeneze chorob zánětlivých, autoimunitních i karcinomu.
Zánět a karcinom: Chronický zánět je rizikový faktor karcinomu zejména ve tkáních, které trvale hostí mikroorganismy. Zánětlivá složka je však často přítomna i v nádorech, které nejsou v příčinném vztahu k zánětu. Zánětlivé mikroprostředí lze považovat za charakteristický znak karcinogeneze.
Vyvolávající příčiny zánětu jsou infekce, autoimunitní choroby, poškození tkáně, tkáňový stres a porucha funkce. Změny komplexního prostředí hostitele mohou vést k poruchám signalizace nespecifické imunity a vytvoření prozánětlivého prostředí. Podobně může působit geneticky determinovaná porucha funkce vrozené imunity.
Zánětlivý proces je charakterizován přítomností makrofágů, transkripčních faktorů, prozánětlivých cytokinů a chemokinů, kyslíkových a dusíkových radikálů, cyklooxygenázy (C0X2) a NO-syntázy (NOS). Klíčové postavení v regulaci nespecifické imunity má nukleární faktor kappaB (NF-κB), který indukuje expresi zánětlivých cytokinů, adhezních molekul, enzymů (COX2, NOS), angiogenních faktorů a antiapoptotických genů. Hlavní efektorovou molekulou aktivace NF-κB jsou multifunkční, pronádorové cytokiny IL-6, TNF-α IL-1β.
Významné prozánětlivé působení v nádorovém vazivu vykazují makrofágy, které spolu s myeloidními supresorovými buňkami působí významně imunosupresivně a způsobují neschopnost hostitele reagovat přiměřenou protinádorovou imunitní odpovědí. Na metabolických změnách nádoru se podílí také extracelulární matrix, které působí jako spojovací článek mezi nádorovými buňkami a makrofágy.
Kyslíkové a dusíkové radikály zprostředkují poškození nádorové DNA nebo jejich opravných mechanismů a změn fází buněčného cyklu. Nestabilní genom je základním projevem solidních nádorů. Projevem genetické nestability je mikrosatelitní a chromozomální instabilita.
Střevní mikrobiota a kolorektální karcinom: Střevní mikrobiota a chronický zánět ovlivňují celý průběh kolorektální karcinogeneze. Modelové studie prokázaly, že 1. manipulace mikrobioty mění vývoj KRK, 2. signální dráha MyD88 je nezbytná pro vývoj KRK indukovaného mikroby, 3. tíže střevního zánětu koreluje s vývojem KRK a 4. mikroby indukovaný zánět podporuje vývoj adenomu do invazivního KRK.
Tyto nálezy potvrzují studie u nemocných KRK a jejich srovnání s kontrolami. Vývoj KRK je spojen s dynamickými změnami střevních mikrobiotů v nádoru, nepostižené sliznici i lumen (tab. 1). Chronické zánětlivé mikroprostředí nádoru moduluje složení mikrobiotů a vývoj KRK. Slizniční mikroby ovlivňují riziko KRK přímou interakcí s hostitelem. Tyto poznatky vytvářejí prostor pro primární prevenci KRK ovlivněním střevních mikrobiotů prostřednictvím nutriční intervence.
Tab. 1 Změny střevních mikrobiotů při KRK v jednotlivých strukturách kolorekta 
Vysvětlivky: ↓snížení, ↑zvýšení *Firmicutes poskytují hostiteli další energetické substráty a účastní se metabolické výměny s hostitelem. Probiotika a kolorektální karcinom: Probiotika jsou živé mikroorganismy, které aplikovány v přiměřeném množství ovlivňují příznivě zdravotní stav příjemce. Hlavní představitelé probiotik jsou species rodu Bifidobacteria a Lactobacilli. Probiotika je možno kombinovat s prebiotiky, tj. specifickými substráty probiotik, neštěpitelné enzymy trávicí trubice, ale štěpitelné mikrobiálními enzymy. Jde zejména o některé oligo - a polysacharidy (např. oligofruktoza, rezistentní škrob, inulin) a polypeptidy. Preparáty obsahující probiotikum i prebiotikum se nazývají synbiotika a některá z nich poskytují nejen aditivní, ale i synergní účinek. Probiotika poskytují hostiteli významné metabolické substance (viz dále).
Probiotika jsou schopna dočasně upravit dysbiózu, tj. změny distribuce mikrobiálních komunit, jejich metabolických aktivit a udržet homeostázu střevního prostředí na úrovni fyziologického zánětu. Dysbióza se vyskytuje u řady chorob (choroby autoimunitní, alergické, metabolické, bakteriální) a také u KRK. V celé řadě modelových situací bylo prokázáno, že bezmikrobní zvířata mají méně výraznou neoplazii nebo kolitidu než zvířata monoasociovaná nebo konvenční. Probiotika ovlivňují střevní mikrobiota různými mechanismy (tab. 2).
Závěr: SM jsou složkou GIE a dysbióza je úvodním patogenetickým procesem, který pokračuje postižením zbývajících složek (SIS a SSB) u řady chorob. Patří k nim: choroby autoimunitní, alergické, metabolické (obezita, diabetes 2. typu, inzulinová rezistence), syndrom dráždivého střeva, idiopatické střevní záněty, alkoholická choroba jater, karcinom kolorekta a pravděpodobně i jiných lokalizací. Úprava dysbiózy a udržení nízkoaktivního zánětlivého prostředí (fyziologického zánětu) ve střevě prostřednictvím probiotik (vedle jiných protizánětlivých prostředků) se jeví přirozeným opatřením.
Skutečnost je však zcela odlišná. Experimentální práce prokazující možnosti probiotik velmi předčily počet a úroveň kontrolovaných, randomizovaných a dvojitě slepých klinických studií.
Vysvětlení je prosté. Probiotika jsou považována za součást zdravotního životního stylu. Trh je přeplněn probiotickými přípravky ve formě potravinových doplňků, z nichž jen nepatrná část splňuje požadavky na dosažení fyziologického či terapeutického účinku. Finanční efekt tohoto přístupu je však tak velký, že nenutí výrobce kvalitních probiotik, aby podporovali klinické studie odpovídajících parametrů a požadovali registraci svých výrobků jako léčiv. Průlomovou pro terapeutické použití probiotik mohou být publikace o významném snížení zonulinu při aplikaci probiotik nemocným operovaným pro KRK. Zonulin má klíčový význam v regulaci propustnosti střevní slizniční bariéry. Potvrzení tohoto nálezu by znamenalo vedle úpravy dysbiózy další terapeutický účinek probiotika v reverzibilní fázi selhání GIE před vznikem systémového onemocnění.
Butyrátové paradoxon
Bureš J.
II. interní gastroenterologická klinika LF UK a FN, Hradec Králové
Řada laboratorních, klinických, nutričních a epidemiologických studií prokázala příznivý protektivní účinek potravinové vlákniny proti kolorektálnímu karcinomu. Nejméně dvě rozsáhlé studie však tento příznivý účinek nezjistily (Nurses’ Health Study, Women’s Health Initiative Trial). Možné protektivní mechanismy vlákniny proti kolorektálnímu karcinomu nejsou beze zbytku objasněny. Vedle fermentovatelné dietní vlákniny (trávené v tenkém střevě) zřejmě důležitou roli hrají také polysacharidy, které jsou metabolizovány až v tlustém střevě (tzv. resistant starch). Jsou fermentovány na mastné kyseliny s krátkým řetězcem. Nejdůležitější z nich je butyrát. Studie zkoumající roli butyrátu proti/při vzniku kolorektálního karcinomu však přinesly rozporuplné výsledky, proto se v této souvislosti používá termínu „butyrátové paradoxon“.
Pro diskrepantní výsledky je možné najít několik možných vysvětlení. Jsou to rozdílné účinky butyrátu in vitro a in vivo (stabilní pufrované pH, abnormální krypty kolonické sliznice) nebo načasování podání butyrátu (inhibitor histon deacetylázy). Roli pravděpodobně sehrávají také rozdílné zdroje butyrátu (fermentovatelná vláknina fytosteroly), množství podaného butyrátu (nízké dávky stimulují, vysoké dávky tlumí proliferaci) a interakce s potravinovými tuky (omega-3 mastné kyseliny).
U idiopatických střevních zánětů, především u ulcerózní kolitidy, argumenty pro příznivý chemopreventivní účinek butyrátu převažují. Butyrát je základní energetický substrát pro kolonocyt (u aktivního zánětu je oxidace butyrátu narušena), snižuje intraluminální pH, suprimuje některé bakteriální enzymatické systémy (beta-glukuronidáza, 7-alfa-dehydroxyláza), tlumí slizniční zánětlivou reakci a stimuluje apoptózu (závislou na p53).
STATE OF THE ART LECTURE
Idiopatické střevní záněty a kolorektální karcinom
Frič P., Zavoral M.
Interní klinika ÚVN – Vojenské fakultní nemocnice a 1. LF UK, Praha
Zvýšené riziko kolorektálního karcinomu (KR-CA) u idiopatické proktokolitidy (IPK) je známo od poloviny 20. století, kdežto u Crohnovy nemoci (CN) bylo popsáno až o 40 let později. KR-CA při idiopatických střevních zánětech (ISZ) se manifestuje dříve než sporadický KR-CA (průměrný věk 50 vs. 62 roků). Při IPK je kumulativní riziko za 20 let trvání choroby 8,3 % a za 30 let 18,4 %. Celkové riziko KR-CA u CN je 2,5%, ale liší se výrazně podle lokalizace (terminální ileum 1,0, ileocékum 3,2, tračník 5,6 %). Při vzniku Crohnovy kolitidy do 30 let je riziko KR-CA mnohem vyšší než při pozdějším onemocnění (20,9 vs. 2,2). Vysoké riziko vzniku karcinomu provází Crohnovu enteritidu (ve třech populacích 66,7, 27,1 a 40,6 %). Třebaže KR-CA se vyskytuje jen asi u 1 % celkového počtu nemocných ISZ, odhaduje se jeho podíl na celkové mortalitě ISZ na 10–20 %.
Identifikace rizikových nemocných ISZ vyžaduje přiměřený dispenzární program k časné diagnostice nádorového procesu. Hlavní příčinou maligní transformace střevní sliznice je chronické prozánětlivé prostředí, které přetrvává i v klinické remisi ISZ. Jeho projevy jsou oxidační stres, zvýšená proliferace a nedokonalá diferenciace střevního epitelu, zvýšená propustnost slizniční střevní bariéry a zánětlivá odpověď imunitního systému. Genetické mutace při ISZ-asociovaném s KR-CA jsou podobné jako při sporadickém KR-CA, ale mají jiný časový sled a frekvenci. Nejvýznamnější marker souběžného nebo pozdějšího KR-CA při ISZ je dysplazie, tj. nádorová přeměna epitelu bez postižení slizniční proprie. Dysplazie je plochá (flat) nebo vyvýšená (raised). Plochá dysplazie je pouhým okem v běžném světle nerozeznatelná. Vyvýšená dysplazie (dysplasia associated lesion or mass, DALM) je unifokální nebo multifokální a má podobu povlaku, polypoidní léze (adenoma-like mass, ALM), novotvaru nebo striktury. Dysplazie se klasifikuje jako negativní, neurčitá (indefinite) a pozitivní: nízkého (low-grade, LGD) nebo vysokého (high-grade, HGD) stupně. Dysplazie předchází vznik KR-CA, ale tento může vzniknout také bez předchozí dysplazie (de novo). KR-CA při ISZ je často multifokální a více agresivní než sporadický KR-CA.
Dispenzarizace se doporučuje při IPK s postižením levé poloviny kolon nebo s pankolitidou a při CN s postižením alespoň jedné třetiny tračníku. U proktosigmoiditidy s postižením méně než 35 cm tračníku se považuje za dostatečné opatření aplikace stejného programu jako při populačním screeningu sporadického KR-CA. Zahájení dispenzarizace bylo dosud vázáno na dobu od stanovení diagnózy: 8–10 let u nemocných s postižením více než poloviny tračníku, 15 let u ostatních. U 22–35 % nemocných s IPK byl však nalezen KR-CA před zahájením dispenzarizace podle tohoto pravidla. Proto se doporučuje stanovit dobu zahájení dispenzarizace tímto počtem roků od objevení příznaků ISZ. Tento postup je také podporován nálezem 15 % KR-CA zjištěných u nemocných s ISZ po kolonoskopii provedené před 6–36 měsíci ve srovnání s nemocnými bez ISZ (5 %).
Základní metodou dispenzární kolonoskopie jsou etážové biopsie ze všech čtyř kvadrantů střevní sliznice celého tračníku v intervalu 10 cm. Doplňkové endoskopické zobrazovací metody, zejména chromoendoskopie (metylénová modř, indigokarmín), zobrazení úzkým svazkem, ale i další (zvětšovací endoskopie, konfokální endomikroskopie a autofluorescence) umožňuji cílené odběry ze změněných míst sliznice a častější nález dysplazie při nižším počtu biopsií. Při první negativní kolonoskopii se vyšetření opakuje v intervalu 1–2 let. Jestliže tato druhá kolonoskopie je rovněž negativní, je možno interval rozšířit až na 3 roky. Po 20 letech trvání choroby se interval opět zkracuje na 1–2 roky. Kolonoskopie se provádějí v klidové fázi bez aktivního zánětu a reaktivních změn, které mohou interferovat s histologickým hodnocením dysplazie.
Hodnocení dysplazie: Nález HGD nebo multifokální LGD se považuje za indikaci k profylaktické proktokolektomii. Při neurčité dysplazii se doporučuje druhé čtení nebo opakování kolonoskopie za 3–6 měsíců. Při nálezu jednoho plochého ložiska LGD je třeba pacientovi vysvětlit, že v těchto případech dochází k vývoji do HGD v širokém rozmezí 2–50 % a ponechat mu volbu: kolonoskopie v intervalu 3–6 měsíců nebo chirurgické řešení. Pokud pacient zvolí první alternativu, je třeba jej informovat, že při nálezu multifokální LGD, opakované LGD nebo HGD, bude doporučena proktokolektomie. Při nálezu ploché nebo vyvýšené léze bez ohraničení k okolí (DALM) se doporučuje proktokolektomie, neboť karcinom je přítomen až u poloviny nemocných s tímto nálezem. Při lézi podobné adenomu (ALM) se doporučuje kompletní resekce včetně báze a vícečetné biopsie okolní sliznice. Při negativní dysplazii, následují další kolonoskopie v intervalu 6 měsíců, při pozitivní dysplazii chirurgická terapie. Stenózy tračníku při IPK jsou indikovány k chirurgickému řešení pro častou malignitu. Při CN je významný endoskopický nález nad stenózou. Po 20 letech trvání choroby je malignita přítomná v 7 %. Pokud není možno zobrazit střevo nad stenózou, doporučuje se chirurgická terapie.
Histologické hodnocení nálezů dysplazie vykazuje individuální rozdíly zejména v termínech neurčitá dysplazie, LGD a unifokální LGD. Dispenzarizace nemocných ISZ dovoluje časnější diagnózu a lepší prognózu asociovaného KR-CA, snižuje jeho riziko a je přijatelná v pojmech náklady – účinek. Dispenzární program je časově náročný. I při zachování doporučeného postupu představují odebrané biopsie méně než 1% slizničního povrchu tračníku.
Cílem prevence dysplazie je udržení nízkého prozánětlivého prostředí v ileu a tračníku v remisi ISZ. Předpokladem je omezení přerůstání kmenů Gram-negativních mikrobiotů v prostředí oxidačního stresu. Prostředky k dosažení tohoto cíle jsou: zdravý životní styl, dostatek vlákniny v potravě, farmakoterapie, probiotika a preference terapeutické strategie top-down před step-up. Aminosalicyláty snižují aktivitu transkripčního faktoru c-myc, který ovlivňuje expresi asi 15 % všech genů. Kromě toho regulují aktivitu NF-κB, který moduluje interakce mezi střevním epitelem a slizničním imunitním systémem. Probiotika (bifidobakterie, laktobacily, E. coli Nissle) ovlivňují funkci NF-κB podobně jako aminosalicyláty a snižují aktivitu zonulinu, který řídí propustnost střevní slizniční bariéry. Kyselina ursodeoxycholová je pravidelnou součástí farmakoterapie při kombinaci IPK a sklerózující cholangitidy. Nejbližšími praktickými úkoly v prevenci dysplazie a KR-CA při ISZ je zavedení cílených biopsií při dispenzárních kolonoskopiích aplikací chromodiagnostických metod (metylénová modř, indigokarmín) nebo vyšetření použitím NBI a zavedení stanovení imunopozitivity p53 jako časného markeru malignizace. Základní cíl zůstává: snížení morbidity, mortality a lepší kvalita života.
pokračování v dalším čísle
Štítky
Adiktológia Alergológia a imunológia Angiológia Audiológia a foniatria Biochémia Dermatológia Detská gastroenterológia Detská chirurgia Detská kardiológia Detská neurológia Detská otorinolaryngológia Detská psychiatria Detská reumatológia Diabetológia Farmácia Chirurgia cievna Algeziológia Dentální hygienistka
Článok vyšiel v časopiseČasopis lékařů českých
Najčítanejšie tento týždeň
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Kolorektální karcinom (část 1)
- EPMA summit
- Diabetes mellitus – oční komplikace
- Již počtrnácté plný Lékařský dům na konferenci Tabák a zdraví
- Doc. MUDr. Ivo Přerovský, DrSc. 1924–2014
- Vzpomínka na prof. MUDr. Zdeňka Reiniše, DrSc.
- Erratum
- ROSALYN SUSSMAN YALOWOVÁ
- Potenciální interakce mezi léčivy a doplňky stravy rostlinného původu*
- Plánované akce složek ČLS JEP
- Cirkulující nádorové buňky a prognóza karcinomu prostaty
- Krevní destičky v patogenezia léčbě solidních nádorů
- Plánované akce složek ČLS JEP
- Imunologické vlastnosti ženských slin a jejich vliv na pohyblivost spermií
- CREATIVE DESTRUCTION OF MEDICINE
- Vztah rizikových faktorů mezi metabolickým syndromem a nealkoholickým ztučněním jater u dětí a dospívajících
- OMLUVA
- Porodnicko-gynekologicky orientované texty v díle Jana Černého
- Časopis lékařů českých
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Krevní destičky v patogenezia léčbě solidních nádorů
- Imunologické vlastnosti ženských slin a jejich vliv na pohyblivost spermií
- Potenciální interakce mezi léčivy a doplňky stravy rostlinného původu*
- Cirkulující nádorové buňky a prognóza karcinomu prostaty
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy





