-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Individualizovaná farmakoterapie ložiskové psoriázy perorálním metotrexátem: fikce nebo reálná možnost?
Individualized Pharmacotherapy of Plaque Psoriasis with Oral Methotrexate: Fiction or Reality?
Methotrexate (MTX) is an effective immunosuppressive drug for moderate-to-severe psoriasis. In an open prospective study patients with chronic plaque psoriasis (n = 25, aged 28–79 yr) were treated with oral methotrexate using an individualized dose guided by plasma concentrations and with folic acid in case the concentration of blood folates dropped below the lower limit of normal range. The aim was to study the relationship between changes in PASI (the Psoriasis Area and Severity Index) and concentrations of MTX polyglutamates (MTXPG) in erythrocytes and blood folates. After 26 weeks, PASI improved from the median of 13.5 (range 2.2–33) by 91% on the average and the frequency of PASI75 (improvement ≥ 75 %) was 76%. There was a correlation between PASI improvement and the ratio of concentrations MTXPG/folates (rs = 0. 51, P < 0.01). In patients experiencing PASI75, the ratio achieved 0.61 as compared to 0.26 in those with less improvement (P < 0.05). In conclusion, individual-tailored therapy with MTX and folic acid can improve the results in the remission-induction phase of psoriasis treatment. Its efficacy should be compared with other established drug regimens in controlled studies.
Key words:
psoriasis – PASI – methotrexate – folates
Autoři: J. Chládek 1; M. Šimková 2; J. Vaněčková 2; M. Hroch 1; J. Ettler 2; J. Vávrová 3; K. Ettler 2
Působiště autorů: Ústav farmakologie, Lékařská fakulta, Hradec Králové přednosta doc. MUDr. Stanislav Mičuda, Ph. D. 1; Klinika nemocí kožních a pohlavních, Fakultní nemocnice a Lékařská fakulta, Hradec Králové přednosta doc. MUDr. Karel Ettler, CSc. 2; Ústav klinické biochemie a diagnostiky, Fakultní nemocnice a Lékařská fakulta, Hradec Králové přednosta doc. MUDr. Pavel Živný, CSc. 3
Vyšlo v časopise: Čes-slov Derm, 87, 2012, No. 6, p. 221-228
Kategorie: Terapie, farmakologie a klinické studie
Souhrn
Metotrexát (MTX) je imunosupresivum používané v léčbě středně těžké a těžké psoriázy. V otevřené prospektivní studii byli nemocní s chronickou ložiskovou psoriázou (n = 25, věk 28–79 let) léčeni MTX per os v dávce individuálně nastavené podle plazmatických koncentrací léčiva a užívali kyselinu listovou, pokud se hladina folátů v krvi snížila pod spodní hranici referenčního rozmezí. Cílem bylo analyzovat vztah mezi změnami skóre PASI (The Psoriasis Area and Severity Index) a koncentracemi polyglutamátů MTX v erytrocytech (MTXPG) a folátů v krvi. Po 26 týdnech se PASI zlepšilo z hodnoty 13,5 (rozsah 2,2–33) v průměru o 91 % a četnost PASI75 (zlepšení o ≥ 75 %) byla 76%. Zlepšení PASI korelovalo s poměrem koncentrací MTXPG a folátů (rs = 0,51, p < 0,01), který u nemocných s PASI75 dosáhl 0,61 oproti 0,26 u nemocných s menším zlepšením (p < 0,05). Individualizace dávkování MTX a kyseliny listové může zlepšit výsledky úvodní fáze léčby psoriázy perorálním MTX, ale je nutné provést srovnání s jinými postupy léčby v kontrolovaných studiích.
Klíčová slova:
psoriáza – PASI – metotrexát – foláty
Psoriáza je chronické zánětlivé onemocnění kůže, které se rozvíjí na základě patologických imunitních reakcí organismu. V různých formách postihuje 1–3 % populace. Středně těžká a těžká psoriáza (30 % případů) je spojená s vysokou morbiditou a významně snižuje kvalitu života nemocného včetně možností jeho společenského uplatnění. Nemocní mají sníženou očekávanou délku života. Náklady spojené s léčbou a ostatní náklady představují značnou ekonomickou zátěž jak pro zdravotní a sociální systémy, tak pro nemocného [20]. Psoriáza je v současnosti nevyléčitelné onemocnění. Je nutná dlouhodobá léčba, která snižuje aktivitu zánětu a tím postižení kůže redukuje až zcela potlačuje. Těžší formy psoriázy vyžadují celkovou imunosupresivní léčbu, ve které má významné místo perorální metotrexát (MTX) [7].
MTX je 4-amino-10-methyl substituovaný analog kyseliny listové. Jedná se o antimetabolit ze skupiny antifolátů. MTX soutěží s kyselinou listovou o vazbu na stejné enzymy a membránové přenašeče. Podobně jako kyselina listová je i MTX v buňkách metabolizován na polyglutamáty (MTXPG), které jsou farmakologicky aktivní [30]. MTX a MTXPG ovlivňují celou řadu biochemických pochodů. Inhibují dihydrofolát reduktázu a tím dochází k úbytku redukovaných folátů, účastnících se biochemických reakcí přenosu jednouhlíkových skupin. Snížená metylace homocysteinu na methionin má za následek pokles tvorby polyaminů (spermidin a spermin) a nárůst koncentrace homocysteinu. Inhibice thymidylát syntetázy vede k redukci syntézy deoxythymidin monofosfátu a snížení replikace DNA. Účinkem MTXPG dochází také k zásahu do syntézy purinů a nárůstu koncentrací adenozinu, protože je inhibován enzym 5-aminoimidazol-4-karboxamid transformyláza. Není jednoznačně objasněno, který z výše uvedených molekulárních mechanismů má hlavní význam pro rozvoj imunosupresivního působení MTX. Některé studie zdůrazňují úlohu adenozinu a jeho imunosupresivního účinku zprostředkovaného vazbou na receptor, zahrnujícího zvýšenou syntézu protizánětlivých cytokinů (IL-10) a sníženou syntézu prozánětlivých transkripčních faktorů (NF-κB), cytokinů (TNFα) a adhezivních molekul [28].
Farmakoterapie perorálním MTX je ekonomicky velmi výhodná zejména při srovnání s biologickými léčivy. Poměrně často ale musí být zvolen jiný způsob léčby z důvodu nedostatečného terapeutického účinku nebo pro nežádoucí účinky. Retrospektivní studie udávají, že pro netoleranci (nevolnost, zvracení, průjem, bolest hlavy, únava) nebo orgánové nežádoucí účinky MTX (zejména hepatotoxicita a útlum krvetvorby) je léčba předčasně ukončována až u 30 % nemocných [21, 23].
Farmakokinetika MTX je interindividuálně velmi variabilní, což může být jednou z hlavních příčin selhání farmakoterapie. Vliv farmakokinetiky na výsledky léčby a možný přínos farmakokineticky řízeného dávkování MTX byl v minulosti prospektivně hodnocen ve studiích organizovaných Klinikou nemocí kožních a pohlavních Fakultní nemocnice a Ústavem farmakologie Lékařské fakulty v Hradci Králové. Výsledky byly publikovány v Česko-slovenské dermatologii v roce 2001 [8–10] a v zahraničním odborném tisku [12, 14–17]. Po perorálním podání stejné dávky se interindividuální variabilita v absorpci a eliminaci léčiva projevovala až pětinásobnými rozdíly v plazmatických koncentracích MTX a v odvozených charakteristikách maximální koncetrace (Cmax) a plocha pod křivkou koncentrací (AUC). Originálním zjištěním byla těsná korelace mezi AUC vyšetřenou v prvním týdnu a výsledky léčby. Vyšší hodnotě AUC odpovídal větší procentuální pokles skóre PASI po 3 měsících farmakoterapie. Dalším zajímavým poznatkem bylo, že MTXPG se postupně kumulují v erytrocytech a po 8–12 týdnech dosahují ustálených koncentrací, jejichž výše koreluje s AUC MTX v plazmě a s procentuální změnou PASI. Analýza vztahu mezi farmakokinetikou a farmakodynamikou umožnila definovat terapeutické rozmezí pro AUC, tj. hodnoty spojené s vysokou pravděpodobností dosažení PASI50 (50% a větší pokles PASI z počáteční hodnoty). Farmakokineticky řízená individualizace dávky spočívala v podání testovací dávky 10 mg p. o., vyšetření plazmatických koncentrací v časech 1 h, 4 h a 8 h, výpočtu AUC v intervalu 0–8 h po podání a v úpravě týdenní dávky MTX tak, aby byla hodnota AUC v terapeutickém rozmezí. Ve dvou prospektivních studiích byly výsledky individualizovaného dávkování velmi nadějné. Průměrné zlepšení PASI bylo 67% a 83% a PASI50 bylo dosaženo u více než 85 % nemocných se středně těžkou až těžkou ložiskovou psoriázou [12, 17].
Práce navazuje na poznatky předchozího výzkumu a nabízí hlubší pohled na vztahy mezi farmakokinetikou a účinkem MTX v průběhu iniciální fáze individualizované farmakoterapie ložiskové psoriázy. Pozornost je věnována zejména kinetice změn koncentrací MTXPG v erytrocytech a folátů v krvi a jejich vztahu k vývoji skóre PASI. Aby bylo možné širší posouzení možných výhod individualizované farmakoterapie MTX, je uveden také souhrn výsledků randomizovaných kontrolovaných studií s MTX publikovaných v literatuře a výsledky biologické léčby prováděné na Klinice nemocí kožních a pohlavních v Hradci Králové ve stejném období.
METODY
Studie individualizovaného dávkování MTX při léčbě středně těžké a těžké psoriázy, registrovaná pod kódem Eudra CT 2009-015403-95, byla organizována na Klinice nemocí kožních a pohlavních Fakultní nemocnice v Hradci Králové v období listopad 2009 až listopad 2011. Protokol studie schválila Etická komise Lékařské fakulty a Fakultní nemocnice v Hradci Králové a všichni nemocní podepsali informovaný souhlas s účastí. Kritéria přijetí do programu individualizované farmakoterapie MTX zahrnula věk 18 let nebo vyšší, diagnózu chronická ložisková psoriáza po dobu 2 roky nebo déle a postižení 10 % povrchu těla nebo větší plochy. Nemocný nebyl přijat do studie, pokud byl léčen MTX v minulosti, nebo pokud měl jiné onemocnění, nebo byly přítomny skutečnosti, které tvoří kontraindikace nebo omezení použití MTX podle dokumentu S3 Evropské akademie dermatovenereologie [22]. Psoriatická artritida nebyla důvodem k nepřijetí. Nemocní byli instruováni, aby neužívali alkoholické nápoje. Údaje o výsledcích biologické léčby byly shromážděny retrospektivně k 3. 3. 2011. Skóre PASI bylo vyhodnoceno na začátku a po 3 měsících terapie. Statisticky reprezentativní byly soubory nemocných léčených etanerceptem – Enbrel® (n = 74) a adalimumabem – Humira® (n = 26).
Individualizované dávkování MTX
Po vstupním vyšetření byla nemocným podána testovací dávka 10 mg MTX per os. V časech 1, 4 a 8 h po podání byla z kubitální žíly do heparinizované monovety odebrána krev na stanovení koncentrace MTX v plazmě. Plocha pod křivkou plazmatických koncentrací MTX v intevalu 0–8 h po podání (AUC0-8h) byla vypočítána lichoběžníkovým pravidlem. Hodnotám AUC0-8 h v rozmezích 2000–2400, 1600–2000, 1200 až 1600, 800–1200 a < 800 h.nmol/l odpovídaly individualizované týdenní dávky 7,5, 10, 12,5, 17,5 a 22,5 mg MTX (Metotrexat Lachema, Brno, Česká republika, tableta 2,5 mg MTX). Léčba individualizovanou dávkou byla zahájena v týdnu následujícím po podání testovací dávky a týdenní dávka byla rozdělena do 3 dávek (ráno-večer-ráno). Z důvodu bezpečnosti terapie ji předcházelo kontrolní hematologické a biochemické vyšetření krve. Další plánovaná vyšetření se uskutečnila za 4, 8, 16 a 26 týdnů. Byly provedeny laboratorní testy. Dva zkušení dermatologové vyhodnocovali skóre PASI a dotazovali se na přítomnost nežádoucích účinků nebo jakýchkoli změn zdravotního stavu v uplynulém období. Koncentrace MTX v plazmě a MTXPG v erytrocytech byly vyšetřeny technikou kapalinové chromatografie [13]. Biochemická a hematologická vyšetření krevních vzorků byla provedena v akreditovaných laboratořích Fakultní nemocnice v Hradci Králové. Týdenní dávka MTX mohla být snížena, pokud bylo dosaženo PASI75 nebo zvýšena při nedostatečném účinku (menší než 25% zlepšení oproti vstupní hodnotě). Pokud se koncentrace folátů snížila pod dolní hranici referenčního rozmezí (254 nmol/l), byla zahájena suplementace folátů kyselinou listovou (Acidum folicum, Zentiva a.s., Praha, 10 mg/týden, 24 h po poslední dávce MTX).
Statistické vyhodnocení
Výběr statistických metod se řídil rozložením vstupních dat. Farmakokinetické parametry MTX a koncentrace MTXPG měly rozložení sešikmené k vysokým hodnotám. Po logaritmické transformaci rozložení odpovídalo gausovskému. Jako popisné statistické charakteristiky byly proto zvoleny medián, 25. až 75. percentil a rozsah. Změny výsledků v průběhu studie byly hodnoceny analýzou rozptylu pro opakované pozorování po logaritmické transformaci hodnot. Pro výpočty byl použit program GraphPad Prism verze 5.00 pro Windows (GraphPad Software, San Diego California, USA). Závislost pravděpodobnosti dosažení PASI75 na poměru koncentrací MTXPG/foláty byla získána logistickou regresí provedenou v programu NCSS (NCSS, Kaysville, Utah, USA).
VÝSLEDKY
Demografické a klinické charakteristiky jsou uvedeny v tabulce 1. Věk nemocných léčených MTX byl vyšší (p < 0,05) než v ostatních dvou skupinách. Doba od stanovení diagnózy se nelišila. Počáteční skóre PASI bylo vyšší ve skupině léčené etanerceptem (MTX: p < 0,01, adalimumab: p < 0,05). Do skupiny léčené MTX bylo zařazeno i 6 nemocných s PASI < 10. U 5 z nich přesáhla plocha postižené kůže 10 %. Jeden nemocný s velmi nízkou hodnotou PASI (2,2) měl postižení i v inverzní lokalizaci, kde ho značně obtěžovalo. Zastoupení nemocných s psoriatickou artritidou bylo vyšší ve skupině léčené etanerceptem (p < 0,05) než v ostatních dvou skupinách. Systémová imunosupresivní léčba byla v minulosti častěji aplikována ve skupinách léčených biologickými léčivy než u nemocných léčených MTX (p < 0,001).
Tab. 1. Demografické a klinické údaje o nemocných 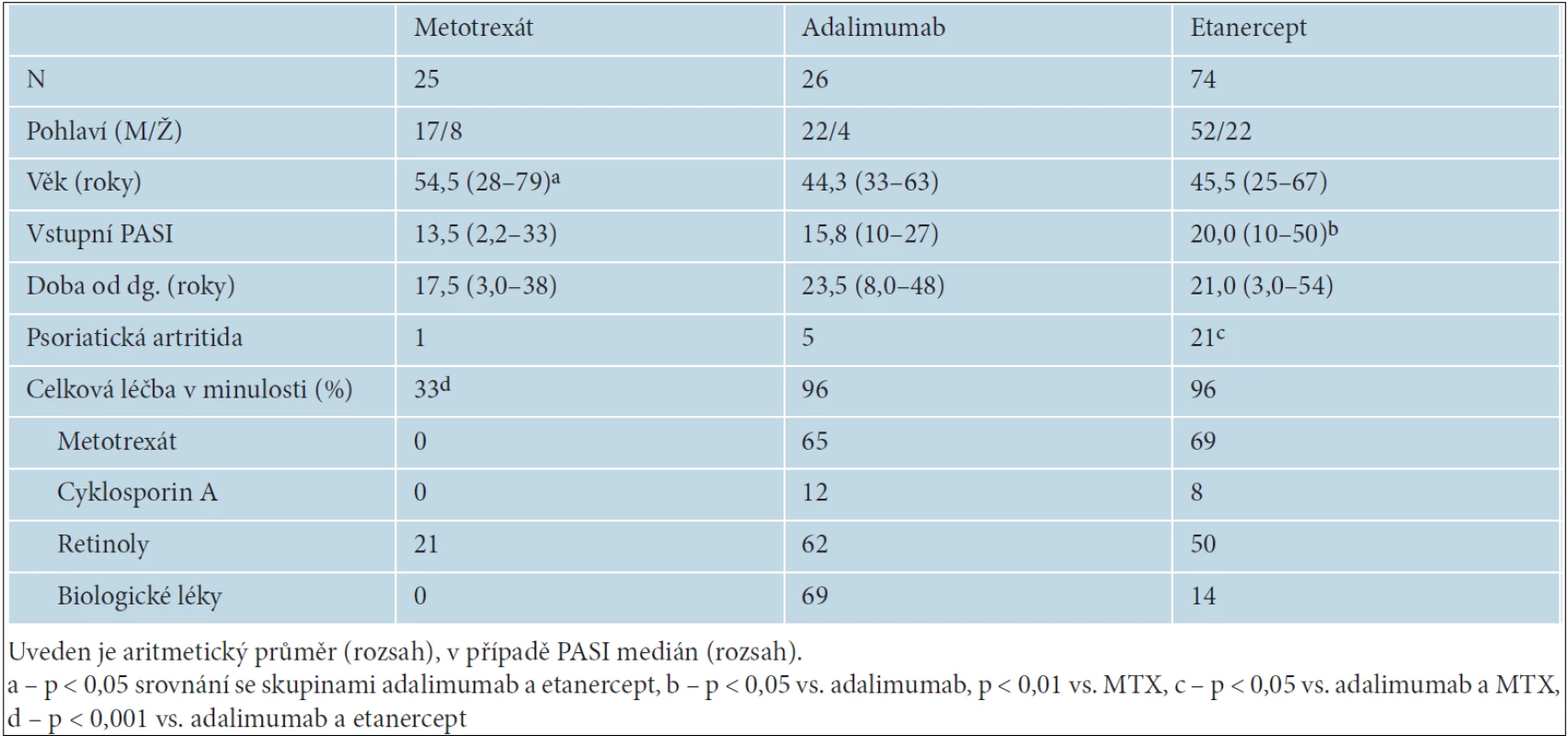
Farmakokinetika MTX v plazmě
Interindividuální odlišnosti plazmatických koncentrací MTX po perorálním podání testovací dávky 10 mg dokumentuje obrázek 1. Hodnota plochy pod křivkou plazmatických koncentrací v intervalu 0–8 h (AUC0-8h) byla v rozmezí 814 až 4730 h.nmol/l a geometrický průměr činil 1610 h.nmol/l. Průměrná týdenní dávka MTX individuálně navržená podle AUC0-8h byla 13,4 mg (rozsah: 7,5–22,5 mg).
Obr. 1. Individuální průběhy koncentrace MTX v plazmě po perorálním podání 10 mg MTX nemocným se středně těžkou a těžkou psoriázou (n = 25) 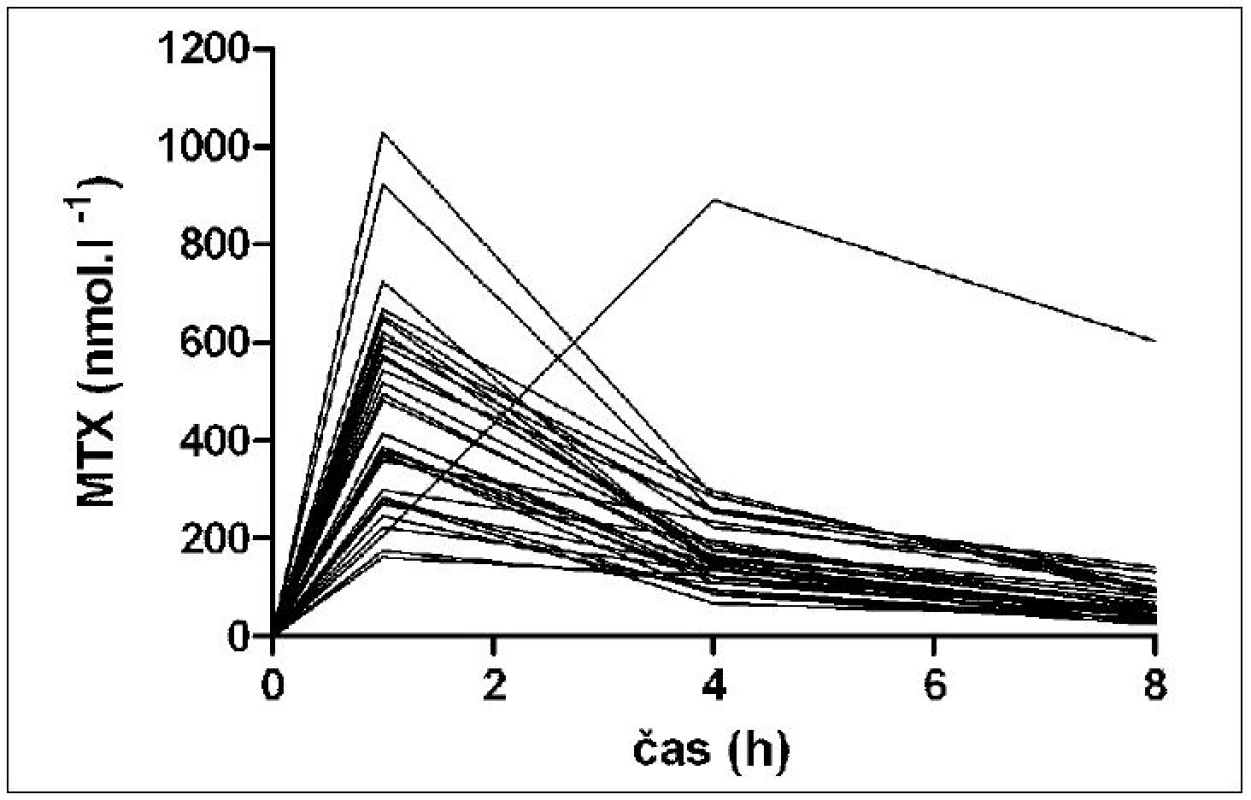
Koncentrace folátů a polyglutamátů MTX
Statistický souhrn výsledků vyšetření polyglutamátů MTX v erytrocytech (MTXPG), koncentrací folátů v krvi a jejich poměru uvádí tabulka 2. Byl zaznamenán statisticky významný postupný pokles koncentrace folátů v krvi, který v 26. týdnu dosáhl v průměru 34 % (p < 0,001). Snížení hladiny folátů pod spodní hranici referenčního rozmezí si vynutilo suplementaci kyselinou listovou, která byla u jednoho nemocného zahájena v 9. týdnu a u dvou v 16. týdnu. Koncentrace MTXPG v erytrocytech se v průběhu prvních 26 týdnů postupně zvyšovaly (p < 0,01, ANOVA pro opakovaná pozorování po logaritmické transformaci koncentrací vyšetřených ve 4. až 26. týdnu). Od 8. týdne od zahájení farmakoterapie již nárůst nebyl statisticky významný a došlo k postupnému ustálení koncentrace. Poměr koncentrací MTXPG v erytrocytech a folátů v krvi se zvyšoval pomaleji. Statisticky významný byl ještě rozdíl mezi jeho hodnotami v 8. a 16. týdnu, ale nikoli v 16. a 26. týdnu. Nárůst geometrického průměru koncentrace MTXPG a poměru MTXPG/foláty odpovídal kinetice prvního řádu s průměrnou hodnotou poločasu 4 a 7 týdnů (obr. 2).
Tab. 2. Popisná statistika výsledků vyšetření koncentrace polyglutamátů metotrexátu v erytrocytech (MTXPG), folátů v krvi a jejich vzájemného poměru. 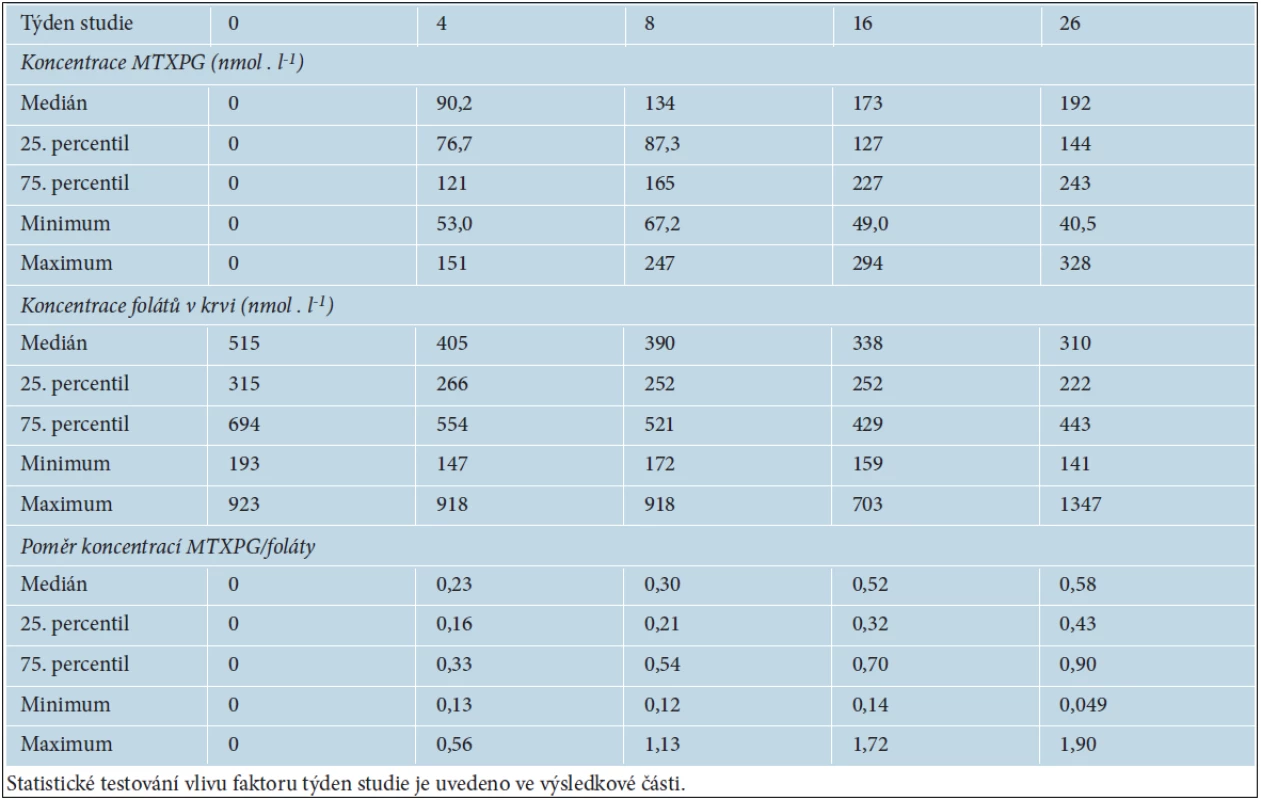
Obr. 2. Geometrické průměry koncentrace polyglutamátů metotrexátu v erytrocytech (MTXPG, nahoře) a jejího poměru ke koncentraci folátů v krvi (MTXPG/foláty, dole) Nárůst hodnot probíhal podle kinetiky prvního řádu s poločasem 4 (MTXPG) a 7 týdnů (MTXPG/foláty). SE – standardní chyba odhadu 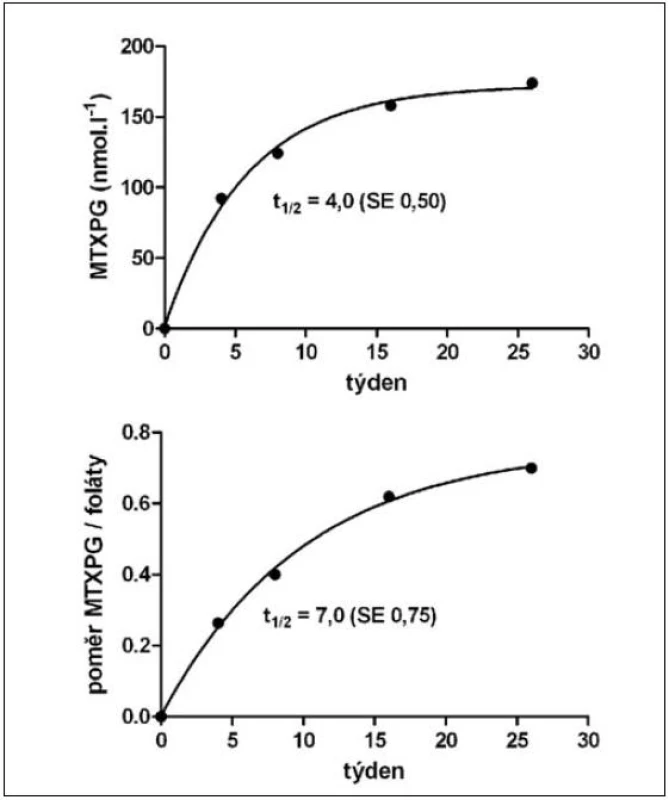
Skóre PASI
Výsledky vyšetření PASI u nemocných léčených MTX jsou znázorněny na obrázku 3. Mediány zlepšení PASI v týdnech 4, 8, 16 a 26 oproti počáteční hodnotě dosáhly 36, 68, 77 a 84 %. Pokles průměrného skóre probíhal podle kinetiky prvního řádu s poločasem 4 týdny. Změny PASI a procenta nemocných s PASI50 a PASI75 jsou pro nemocné léčené individualizovanou dávkou MTX a pro nemocné léčené etanerceptem a adalimumabem ve stejném období shrnuty v tabulce 3. Statisticky významně lepší byly výsledky po 26 týdnech užívání MTX ve srovnání s 14týdenní léčbou etanerceptem. Tabulka 4 nabízí přehled randomizovaných studií, které porovnávaly výsledky léčby MTX s jinými postupy celkové imunosupresivní léčby.
Obr. 3. A) Skóre PASI v průběhu prvních 26 týdnů individualizované léčby perorálním metotrexátem (mediány, 25.–75. percentil, rozsahy); byl pozorován statisticky významný pokles PASI (p < 0,001, Friedmanův test). b) Procenta nemocných, u kterých bylo dosaženo PASI50 a PASI75. 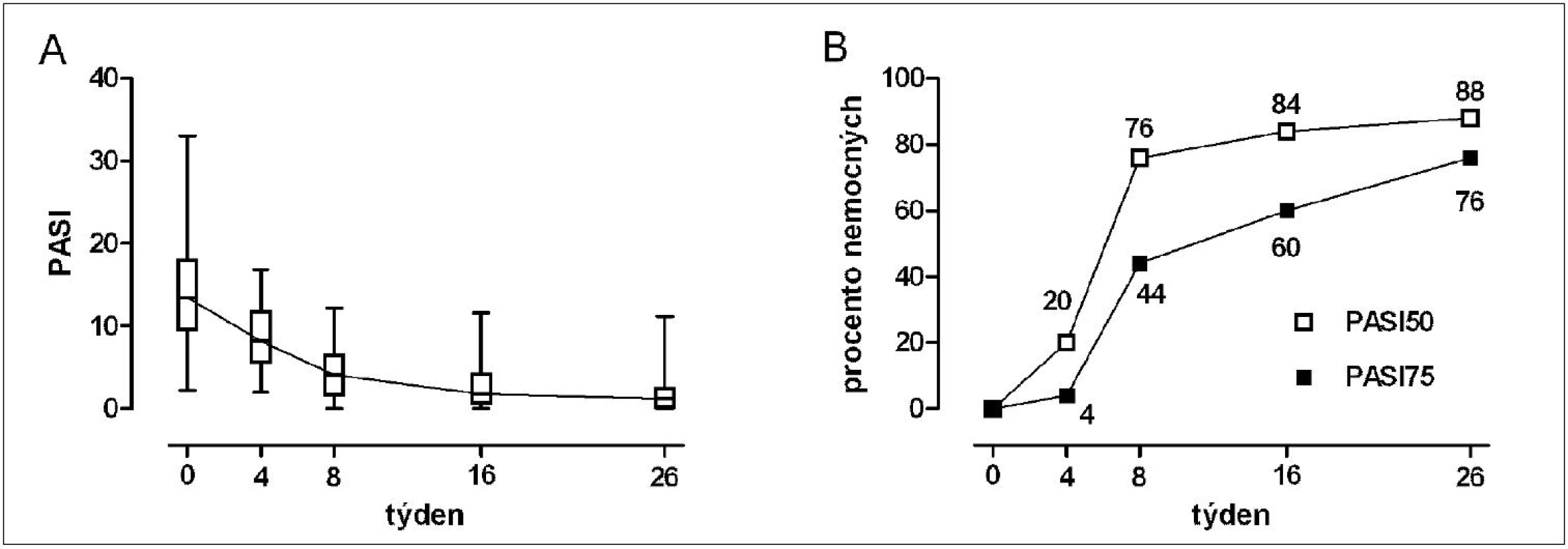
Tab. 3. změny skóre PASI (the Psoriasis Area and Severity Index) a procenta nemocných, u kterých se PASI snížilo o ≥ 50 % (PASI50) a 70 % (PASI70) 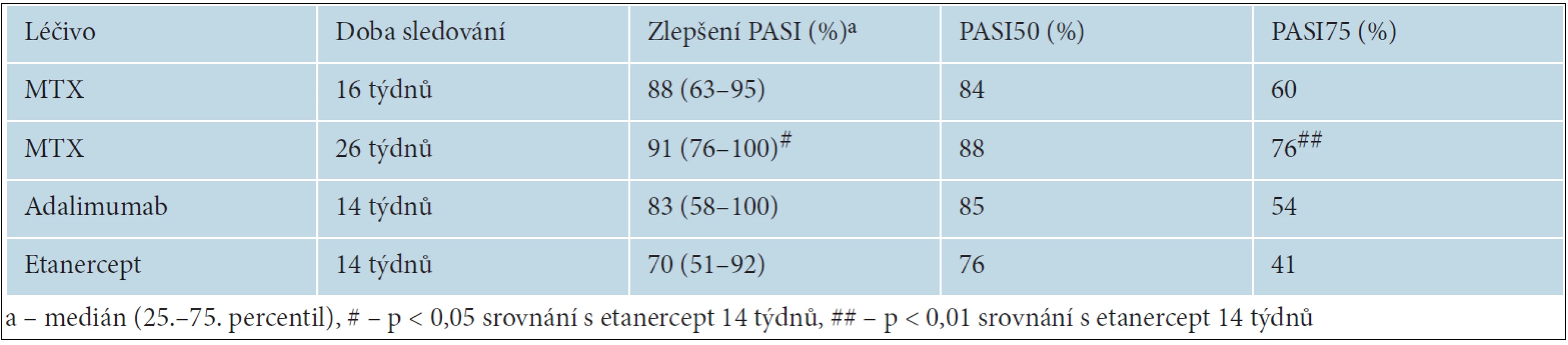
Vztah mezi poměrem koncentrací MTXPG/foláty a účinkem
Procentní zlepšení skóre PASI v týdnu 26 korelovalo s poměrem koncentrací MTXPG a folátů (obr. 4). U nemocných s PASI75 činil medián poměru MTXPG/foláty 0,61 oproti 0,26 u nemocných s menším zlepšením PASI (p < 0,05). Závislost mezi pravděpodobností úspěchu terapie podle kritéria PASI75 a hodnotou poměru MTXPG/foláty je na obrázku 5. Pravděpodobnosti 90% odpovídala hraniční hodnota poměru 0,52.
Obr. 4. závislost procentního zlepšení skóre PASI v 26. týdnu na hodnotě poměru koncentrací polyglutamátů MTX v erytrocytech a folátů v krvi (průměr hodnot poměru v 16. a 26. týdnu) 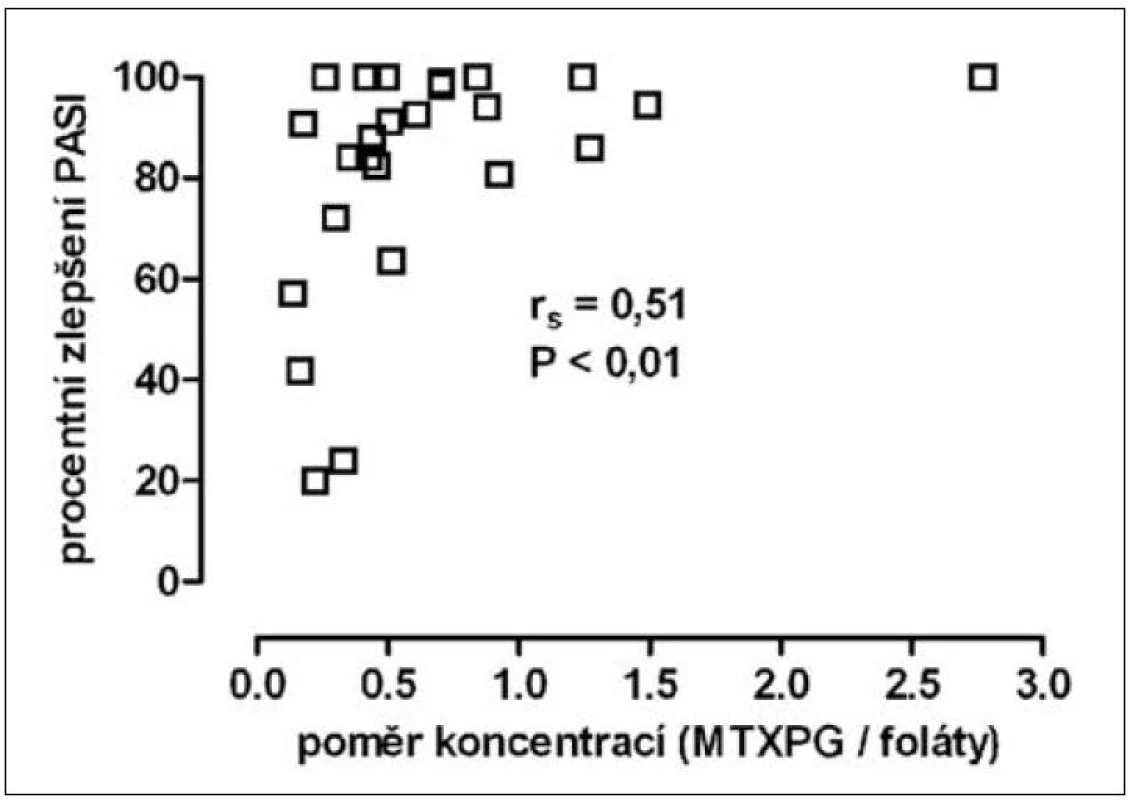
Obr. 5. Vztah mezi pravděpodobností dosažení PASI75 a hodnotou poměru koncentrací polyglutamátů MTX v erytrocytech a folátů v krvi (průměr hodnot poměru v 16. a 26. týdnu) šipky ukazují hraniční hodnotu poměru spojenou s 90% pravděpodobností PASI75. 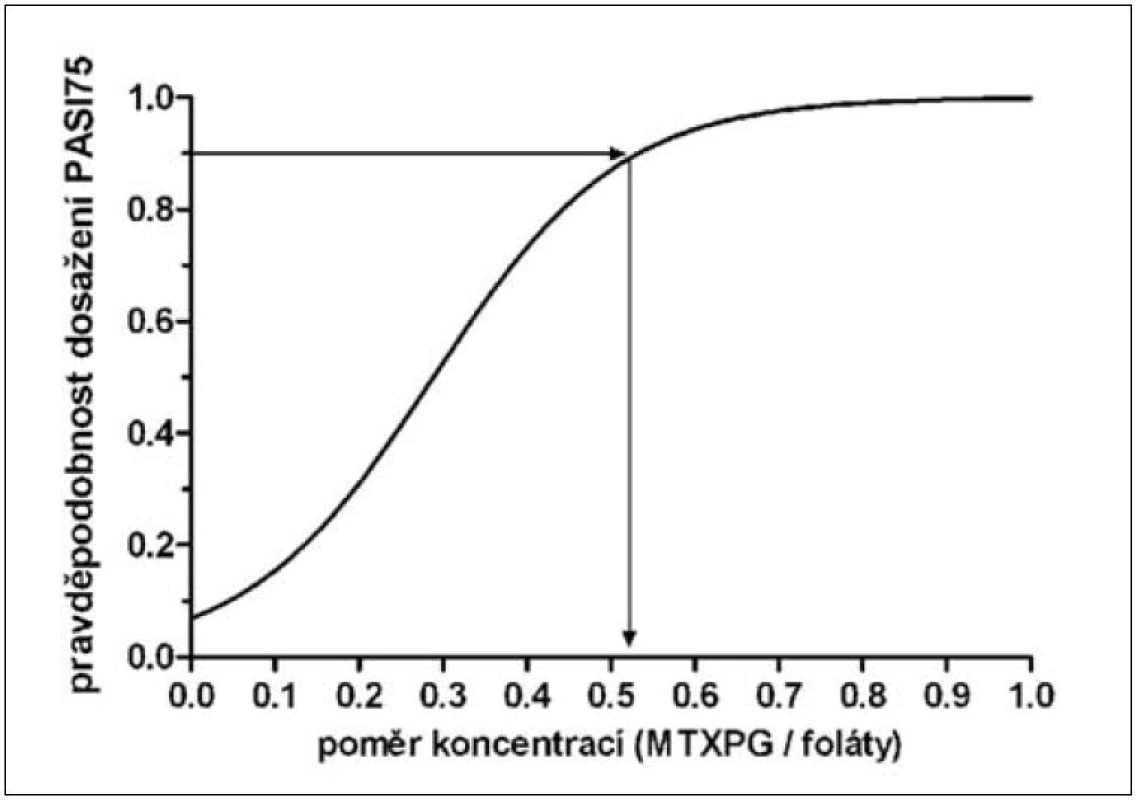
Bezpečnost individualizované léčby MTX
Dva nemocní ukončili účast po vyšetření v 16. týdnu pro nevolnost a bolest břicha. Místo chybějících výsledků vyšetření PASI v 26. týdnu byly u těchto nemocných použity výsledky získané v 16. týdnu. Původně zahájilo studii 27 nemocných. Dva nemocní ukončili účast již ve 4. týdnu a jejich výsledky nebyly zahrnuty do hodnocení. V jednom případě byla důvodem nevolnost a bolest hlavy. U druhého nemocného bylo podávání MTX ukončeno pro rychlý nárůst aktivit jaterních enzymů (ALT 15krát, AST 8krát, γ-GT 4krát). Výsledky se normalizovaly do 2 měsíců. Celkem byla léčba MTX z důvodu nežádoucích účinků před 26. týdnem vysazena u 4 z 27 nemocných (15 %).
DISKUSE
Výsledky studie ukazují, že individualizované dávkování perorálního MTX podle farmakokinetiky MTX v plazmě (AUC0-8h po testovací dávce 10 mg) spolu s racionálním postupem farmakologické suplementace folátů kyselinou listovou mohou pomoci zlepšit výsledky úvodní fáze léčby středně těžké a těžké ložiskové psoriázy. Střední hodnota relativního zlepšení PASI 91% a četnost PASI75 76% po 26 týdnech léčby jsou výsledky srovnatelné s úspěšností léčby biologickými léčivy v publikovaných kontrolovaných studiích. Impozantní je i medián zlepšení PASI o 68 % již v 8. týdnu. Současná metodická doporučení European Academy of Dermatovenereology navrhují iniciální dávku 5–10 mg MTX a její rychlé zvyšování na udržovací dávku v rozmezí 5–30 mg/týden [22]. Z přehledu kontrolovaných studií v tabulce 4 je patrné, že výsledky takto vedené léčby byly ve většině studií horší než naše zkušenosti s individualizovaným dávkováním. Retrospektivní vyhodnocení výsledků biologické léčby umožnilo alespoň nepřímé srovnání individualizované farmakoterapie MTX s jiným postupem léčby prováděným na Klinice nemocí kožních a pohlavních ve srovnatelném období. Nemocní léčení etanerceptem měli ale vyšší PASI před léčbou a také zastoupení nemocných s psoriatickou artritidou bylo v této skupině vyšší. Vzhledem k pravidlům nasazování biologické léčby bylo ve skupinách léčených biologickými léčivy vyšší procento nemocných, kteří absolvovali celkovou imunosupresivní léčbu (včetně MTX) v minulosti než ve skupině léčené MTX. Je nutné zdůraznit, že pouze randomizovaná kontrolovaná studie by umožnila validní porovnání výsledků individualizované léčby MTX a biologické léčby.
Tab. 4. Přehled randomizovaných kontrolovaných studií hodnoticích účinek metotrexátu (MTX) v léčbě středně těžké a těžké ložiskové psoriázy 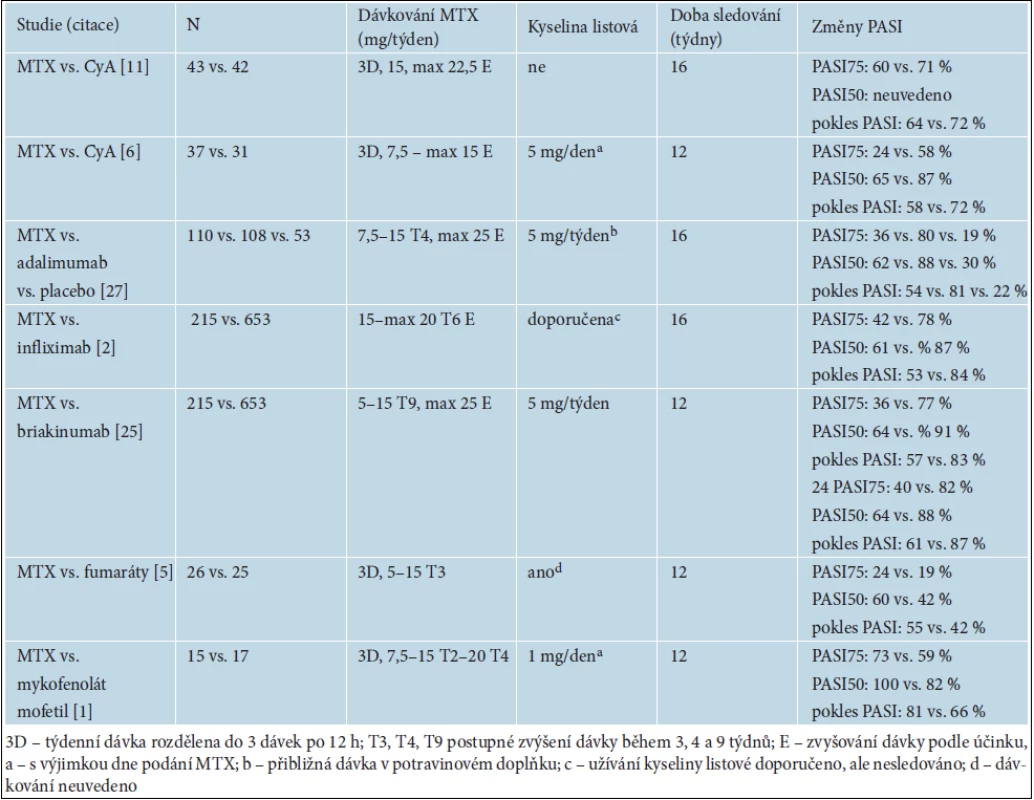
V dříve publikovaných studiích jsme opakovaně prokázali, že i když existuje vztah mezi dávkou MTX v rozmezí 7,5–22,5 mg/týden a intenzitou účinku, v důsledku vysoké interindividuální variability farmakokinetiky perorálně podávaného MTX nejsou u mnoha nemocných dosaženy terapeuticky účinné koncentrace MTX v plazmě a MTXPG v erytrocytech [15]. V randomizované studii s malým počtem nemocných jsme v rameni studie s individualizovaným dávkováním MTX prováděným bez suplementace kyselinou listovou pozorovali v průměru 83% zlepšení PASI, PASI75 bylo docíleno u 6 z 10 nemocných (60 %) a PASI50 u všech nemocných [17]. V jiné studii s individuálně nastavenou dávkou MTX byla častěji zahajována suplementace a střední zlepšení PASI dosáhlo 67 %. PASI75 bylo dosaženo u 47 % a PASI50 u 87 % z celkového počtu 16 nemocných [12]. V podmínkách individualizovaného dávkování MTX se snižuje interindividuální variabilita koncentrací MTXPG v erytrocytech a výsledek léčby je pravděpodobně více ovlivněn hladinou polyglutamátů folátů (foláty v krvi), která se při suplementaci zvyšuje. V souladu se závěrem dřívější studie, provedené na našich pracovištích stejnými metodami [17], jsme i v této studii zjistili, že v podmínkách individualizovaného dávkování existuje korelace mezi poměrem koncentrací MTXPG v erytrocytech a folátů v krvi a relativním zlepšením PASI. Nemocní s PASI75 měli v průměru 2,4násobně vyšší hodnotu tohoto poměru než nemocní s horším výsledkem léčby. Pomocí logistické regrese byla vypočítána hraniční hodnota poměru 0,52, která odpovídá 90% pravděpodobnosti dosažení PASI75.
Podle přehledů publikovaných studií kyselina listová snižuje výskyt změn v krevním obraze, nežádoucích účinků v gastrointestinálním traktu a hepatotoxicitu MTX, aniž by ovlivňovala terapeutický účinek u nemocných s revmatoidní artritidou nebo psoriázou [24, 29, 31]. Naprostá většina analyzovaných studií se ale týkala nemocných s revmatoidní artritidou a léčbou psoriázy se zabývala pouze jedna studie špatné metodologické kvality [4]. První randomizovaná dvojitě slepá placebem kontrolovaná studie naopak doložila, že u nemocných dlouhodobě užívajících MTX zahájení suplementace kyselinou listovou v dávce 5 mg/den vede ke zhoršení PASI [26]. Podle našich zkušeností, kyselina listová v dávce 20 mg/týden negativně ovlivňuje výsledky léčby také v iniciální fázi, která je rozhodující pro spokojenost a compliance nemocného a lékaře s terapií. V prospektivní randomizované zkřížené studii bylo pozorováno zlepšení PASI po 16 týdnech o 83 % v rameni studie s monoterapií MTX a 42 % v rameni studie při kombinované léčbě MTX a kyselinou listovou. Příčinná souvislost mezi podáváním kyseliny listové a nižším účinkem MTX byla potvrzena v druhé fázi studie, kdy se ukončení podávání kyseliny listové projevilo zlepšením PASI z hodnoty 42 % na hodnotu 60 % ve 32. týdnu studie. U nemocných, kteří začali užívat kyselinu listovou až od 17. týdne, dobrý účinek MTX přetrvával i ve 32. týdnu [17]. Změny PASI v kontrolovaných studiích uvedených v tabulce 4 ukazují, že pokud suplementace nebyla v iniciální fázi léčby použita [11] nebo dávka kyseliny listové byla nízká [1], byl účinek MTX lepší.
V dotazníkové studii britské asociace dermatologů publikované v roce 2000 kyselinu listovou předepisovalo spolu s MTX vždy 26 % lékařů a 74 % pouze při projevech nežádoucích účinků a laboratorních známkách toxicity [19]. V roce 2005 byly publikovány výsledky odpovědí 69 dermatologů ze 32 evropských zemí na dotazník zaměřený na postupy při léčbě psoriázy MTX. Ukázalo se, že u 86 % lékařů byl MTX nejčastěji předepisovaným klasickým imunosupresivem. Suplementaci kyselinou listovou používalo u všech nemocných 32 % lékařů, pouze v případě nežádoucích účinků a laboratorních známek toxicity 32 % a bez suplementace předepisovalo MTX 36 % lékařů. Variabilita dávkovacích schémat a týdenních dávek kyseliny listové byla vysoká [3]. European Academy of Dermatovenereology ve svém současném metodickém doporučení neuvádí přesná pravidla pro suplementaci folátů. Dávkování nespecifikuje a suplementaci zmiňuje jen jako možnost jak snížit výskyt nežádoucích účinků [22]. Doporučení komise expertů americké organizace National Psoriasis Foundation také zaujímá ambivalentí stanovisko k otázce, zda zahajovat suplementaci vždy nebo jen při výskytu nežádoucích účinků MTX [18]. Doporučená dávka kyseliny listové je 1 mg/den. Alternativně je možné podat leukovorin (kyselina formyltetrahydrolistová) v dávce 15 mg/týden rozděleně do 3 dávek (5 mg ráno-večer-ráno s odstupem 12 h od podání MTX). Komise expertů European Academy of Dermatovenereology uveřejnila výsledky systematického přehledu léčby psoriázy MTX a svoje konsenzuální stanoviska v roce 2011 [23]. Doporučila suplementaci u všech nemocných a navrhla podávat kyselinu listovou jednou denně v dávce 5 mg/den, jednu až tři dávky týdně s odstupem 48 h po MTX.
Zajímavým zjištěním je časová souvislost mezi kinetikou kumulace MTXPG v erytrocytech a dynamikou poklesu skóre PASI. Oba děje charakterizoval průměrný poločas 4 týdny. Zvyšování hodnot poměru koncentrací MTXPG/foláty probíhalo podstatně pomaleji (poločas 7 týdnů), a to z důvodu pokračujícího poklesu koncentrace folátů. V období mezi 4. a 6. měsícem od zahájení terapie je terapeutický účinek u většiny nemocných plně rozvinut a zdá se být vhodné zahájit suplementaci, pokud hladiny folátů v krvi dále klesají ke spodní hranici referenčního rozmezí. Pokud došlo k dostatečnému zlepšení PASI již před tímto obdobím, mělo by být zahájeno snižování dávky MTX a je možné také doporučit cílenou preskripci kyseliny listové podle koncentrací folátů. S ohledem na evidentní vliv koncentrací folátů na výsledek iniciální fáze léčby se nezdá být racionální zahajovat kombinací MTX a kyselina listová, pokud není koncentrace folátů nízká již před léčbou.
Otevřená prospektivní studie individualizovaného dávkování MTX a suplementace kyselinou listovou ukázala, že takové postupy mohou potenciálně zlepšit výsledky úvodní fáze léčby středně těžké a těžké ložiskové psoriázy perorálním MTX. Vzhledem k uspořádání studie a malé velikosti souboru nemocných je nutné její výsledky posuzovat jako hypotézy generující a vyžadující potvrzení formou přímého srovnání s jinými postupy léčby v randomizovaných kontrolovaných studiích.
Poděkování: Autoři děkují nemocným za účast ve studii a spolupracujícím sestrám Ivaně Polákové, Vlastě Benešové a Ivaně Novotné a laborantce Ivaně Tothové.
Práce byla finančně podpořena grantem Interní grantové agentury Ministerstva zdravotnictví č. NS10364-3/2009.
Do redakce došlo dne 13. 4. 2012.
Kontaktní adresa:
Doc. Ing. Jaroslav Chládek, PhD.
Ústav farmakologie,
Univerzita Karlova v Praze,
Lékařská fakulta v Hradci Králové
Šimkova 870, 500 38 Hradec Králové
e-mail: chladekj@lfhk.cuni.cz
Zdroje
1. AKHYANI, M., CHAMS-DAVATCHI, C., HEMAMI, MR., FATEH, S. Efficacy and safety of mycophenolate mofetil vs. methotrexate for the treatment of chronic plaque psoriasis. J. Eur. Acad. Dermatol. Venereol., 2010, 24, 12, p. 1447–1451.
2. BARKER, J., HOFFMANN, M., WOZEL, G., ORTONNE, J. P., ZHENG, H., VAN HOOGSTRATEN, H., REICH, K. Efficacy and safety of infliximab vs. methotrexate in patients with moderate-to-severe plaque psoriasis: results of an open-label, active--controlled, randomized trial (RESTORE1). Br. J. Dermatol., 2011, 165, 5, p. 1109–1117.
3. BOFFA, M. J. Methotrexate for psoriasis: current European practice. A postal survey. J. Eur. Acad. Dermatol. Venereol., 2005, 19, 2, p. 196–202.
4. DUHRA, P. Treatment of gastrointestinal symptoms associated with methotrexate therapy for psoriasis. J. Am. Acad. Dermatol, 1993, 28 (3), p. 466–469.
5. FALLAH ARANI, S., NEUMANN, H., HOP, W. C., THIO, H. B. Fumarates vs. methotrexate in moderate to severe chronic plaque psoriasis: a multicentre prospective randomized controlled clinical trial. Br. J. Dermatol., 2011, 164, 4, p. 855–861.
6. FLYTSTRÖM, I., STENBERG, B., SVENSSON, A., BERGBRANT, I. M. Methotrexate vs. ciclosporin in psoriasis: effectiveness, quality of life and safety. A randomized controlled trial. Br. J. Dermatol., 2008, 158, 1, p. 116–121.
7. GRIFFITHS, C. E., BARKER, J. N. Pathogenesis and clinical features of psoriasis. Lancet, 2007, 370, 9583, p. 263–271.
8. GRIM, J., CHLÁDEK, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., KOUDELKOVÁ, V., MARTÍNKOVÁ, J. Modelování farmakokinetiky a farmakodynamiky nízkodávkovaného metotrexátu v léčbě psoriázy pro individualizaci dávkování. Čes-slov Derm, 2002, 77, č. 4, s. 154–162.
9. GRIM, J., CHLÁDEK, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., KOUDELKOVÁ, V., MARTÍNKOVÁ, J., NOŽIČKOVÁ, M. Koncentrace metotrexátu v erytrocytech při nízkodávkovém způsobu podání a jejich vztah k úspěchu léčby psoriázy. Čes-slov Derm, 2001, 76, č. 5, s. 237–242.
10. GRIM, J., CHLÁDEK, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., KOUDELKOVÁ, V., MARTÍNKOVÁ, J. Účinek a farmakokinetika metotrexátu v léčbě psoriázy. Čes-slov derm, 2001, roč. 76, č. 4, s. 183–188.
11. HEYDENDAEL, V. M., SPULS, P. I., OPMEER, B. C. et al. Methotrexate versus cyclosporine in moderate-to-severe chronic plaque psoriasis Methotrexate versus cyclosporine in moderate-to-severe chronic plaque psoriasis. N. Engl. J. Med., 2003, 349, 7, p. 658–665.
12. HROCH, M., CHLADEK, J., SIMKOVA, M., VANECKOVA, J., GRIM, J., MARTINKOVA, J. A pilot study of pharmacokinetically guided dosing of oral methotrexate in the initial phase of psoriasis treatment. J. Eur. Acad. Dermatol. Venereol., 2008, 22, 1, p. 19–24.
13. HROCH, M., TUKOVÁ, J., DOLEZALOVÁ, P., CHLÁDEK, J. An improved high-performance liquid chromatography method for quantification of methotrexate polyglutamates in red blood cells of children with juvenile idiopathic arthritis. Biopharm. Drug Dispos., 2009, 30, 3, p. 138–148.
14. CHLÁDEK, J., GRIM, J., MARTÍNKOVÁ, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., KOUDELKOVÁ, V., NOŽIČKOVÁ, M. Pharmacokinetics and pharmacodynamics of low-dose methotrexate in the treatment of psoriasis. Br. J. Clin. Pharmacol., 2002, 54, 2, p. 147–156.
15. CHLÁDEK, J., GRIM, J., MARTÍNKOVÁ, J., ŠIMKOVA, M., VANĚČKOVÁ, J. Low-dose methotrexate pharmacokinetics and pharmacodynamics in the therapy of severe psoriasis. Basic Clin. Pharmacol. Toxicol., 2005, 96, 3, p. 247–248.
16. CHLÁDEK, J., MARTÍNKOVÁ, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., KOUDELKOVÁ, V., NOŽIČKOVÁ, M. Pharmacokinetics of low doses of methotrexate in patients with psoriasis over the early period of treatment. Eur. J. Clin. Pharmacol., 1998, 53, 6, p. 437–444.
17. CHLÁDEK, J., ŠIMKOVÁ, M., VANĚČKOVÁ, J., HROCH, M., CHLÁDKOVA, J., MARTÍNKOVÁ, J., VÁVROVÁ, J., BERÁNEK, M. The effect of folic acid supplementation on the pharmacokinetics and pharmacodynamics of oral methotrexate during the remission-induction period of treatment for moderate-to-severe plaque psoriasis. Eur. J. Clin. Pharmacol., 2008, 64, 4, p. 347–355.
18. KALB, R. E., STROBER, B., WEINSTEIN, G., LEBWOHL, M. Methotrexate and psoriasis: 2009 National Psoriasis Foundation Consensus Conference. J. Am. Acad. Dermatol., 2009, 60, 5, p. 824–837.
19. KIRBY, B., LYON, C. C., GRIFFITHS, C. E., CHALMERS, R. J. The use of folic acid supplementation in psoriasis patients receiving methotrexate: a survey in the United Kingdom. Clin. Exp. Dermatol., 2000, 25, 4, p. 265–268.
20. MATEŘANKOVÁ, A., SCHMIEDBERGEROVÁ, R., HERCOGOVÁ, J. Kvalita života a psoriáza – první výsledky dotazníkového šetření mezi českými psoriatiky. Čes-slov Dermatol., 2008, roč. 83, č. 6, s. 299–304.
21. MONTAUDIÉ, H., SBIDIAN, E., PAUL, C., MAZA, A., GALLINI, A., ARACTINGI, S., AUBIN, F., BACHELEZ, H., CRIBIER, B., JOLY, P., JULLIEN, D., LE MAÎTRE, M., MISERY, L., RICHARD, M. A., ORTONNE, J. P. Methotrexate in psoriasis: a systematic review of treatment modalities, incidence, risk factors and monitoring of liver toxicity. J. Eur. Acad. Dermatol. Venereol., 2011, 25 (Suppl 2), p. 12–18.
22. PATHIRANA, D., ORMEROD, AD., SAIAG, P., SMITH, C. et al. European S3-guidelines on the systemic treatment of psoriasis vulgaris. J. Eur. Acad. Dermatol. Venereol., 2009, 23 (Suppl 2), p. 1–70.
23. PAUL, C., GALLINI, A., MAZA, A., MONTAUDIÉ, H., SBIDIAN, E., ARACTINGI, S., AUBIN, F., BACHELEZ, H., CRIBIER, B., JOLY, P., JULLIEN, D., LE MAÎTRE, M., MISERY, L., RICHARD, M. A., ORTONNE, J. P. Evidence-based recommendations on conventional systemic treatments in psoriasis: systematic review and expert opinion of a panel of dermatologists. J. Eur. Acad. Dermatol. Venereol., 2011, 25 (Suppl 2), p. 2–11.
24. PREY, S., PAUL, C. Effect of folic or folinic acid supplementation on methotrexate-associated safety and efficacy in inflammatory disease: a systematic review. Br. J. Dermatol., 2009, 160, 3, p. 622–628.
25. REICH, K., LANGLEY, R. G., PAPP, K. A., ORTONNE, J. P., UNNEBRINK, K., KAUL, M., VALDES, J. M. A 52-week trial comparing briakinumab with methotrexate in patients with psoriasis. N. Engl. J. Med., 2011, 365, 17, p. 1586–1596.
26. SALIM, A., TAN, E., ILCHYSHYN, A., BERTH-JONES, J. Folic acid supplementation during treatment of psoriasis with methotrexate: a randomized, double-blind, placebo-controlled trial. Br. J. Dermatol., 2006, 154, 6, p. 1169–1174.
27. SAURAT, J. H., STINGL, G., DUBERTRET, L., PAPP, K., LANGLEY, R. G., ORTONNE, J. P., UNNEBRINK, K., KAUL, M., CAMEZ, A. CHAMPION Study Investigators. Efficacy and safety results from the randomized controlled comparative study of adalimumab vs. methotrexate vs. placebo in patients with psoriasis (CHAMPION). Br. J. Dermatol., 2008, 158, 3, p. 558–566.
28. SHEN, S., O’BRIEN, T., YAP, L. M., PRINCE, H. M., MCCORMACK, C. J. The use of methotrexate in dermatology: a review. Australas J. Dermatol., 2012, 53, 1, p. 1–18.
29. STROBER, B. E., MENON, K. Folate supplementation during methotrexate therapy for patients with psoriasis. J. Am. Acad. Dermatol., 2005, 53, 4, p. 652–659.
30. WARREN, R. B., CHALMERS, R. J., GRIFFITHS, C. E., MENTER, A. Methotrexate for psoriasis in the era of biological therapy. Clin. Exp. Dermatol., 2008, 33, 5, p. 551–554.
31. WHITTLE, S. L., HUGHES, R. A. Folate supplementation and methotrexate treatment in rheumatoid arthritis: a review. Rheumatology (Oxford), 2004, 43, 3, p. 267–271.
Štítky
Dermatológia Detská dermatológia
Článok vyšiel v časopiseČesko-slovenská dermatologie
Najčítanejšie tento týždeň
2012 Číslo 6- První zkušenosti s léčbou psoriázy bimekizumabem v české reálné praxi – kazuistika z FNUSA
- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nehoňte nemocné s mMCC od čerta k ďáblu!
- První a jediná schválená imunoterapie vzácného agresivního karcinomu kůže
-
Všetky články tohto čísla
- Retikulární exantémy – patofyziologie, etiopatogeneze, klasifikace
- Doškolování lékařů – kontrolní test
- Individualizovaná farmakoterapie ložiskové psoriázy perorálním metotrexátem: fikce nebo reálná možnost?
- Syndrom ochablého víčka vedoucí k diagnóze těžké spánkové apnoe
-
Tuberculosis verrucosa cutis –
popis případu - Klinický případ: Papulózní exantém trupu s pozitivním Darierovým příznakem
- Pigmentovaná varianta keratosis actinica a lentigo maligna – lze je dermatoskopicky rozlišit?
-
Zápis ze schůze výboru ČDS
Praha 13. září 2012 -
Zápisnica zo zasadnutia výboru SDVS
Malá zasadačka FN Nitra, Nitra 26. 5. 2012 - 6. konference akné a obličejové dermatózy
- Odborné akce 2013
- Rejstřík
- Česko-slovenská dermatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Retikulární exantémy – patofyziologie, etiopatogeneze, klasifikace
- Syndrom ochablého víčka vedoucí k diagnóze těžké spánkové apnoe
-
Tuberculosis verrucosa cutis –
popis případu - Pigmentovaná varianta keratosis actinica a lentigo maligna – lze je dermatoskopicky rozlišit?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



