-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Klinický registr TARCEVA
Autoři: J. Skřičková 1; M. Pešek 2; P. Zatloukal 3; V. Kolek 4; F. Salajka 5; L. Koubková 6; J. Krejčí 2; M. Tomíšková 1; Y. Grygárková 4; L. Havel 3; M. Hrnčiarik 5; B. Skalová 6; M. Štícha 7
Působiště autorů: Klinika nemocí plicních a tuberkulózy, LF MU a FN Brno 1; Klinika nemocí plicních a TBC, FN Plzeň 2; Klinika pneumologie a TBC, FN Bulovka, Praha 3; Klinika plicních nemocí a TBC, FN Olomouc 4; Plicní klinika, FN Hradec Králové 5; Plicní klinika FN Motol, Praha 6; Institut biostatiky a analýzy LF a PřF MU, Brno 7
Vyšlo v časopise: Klin Onkol 2010; 23(5): 361-363
Kategorie: Aktuality z registrů
Receptor epidermálního růstového faktoru (epidermal growth factor receptor – EGFR) je jednou z cílových struktur nádorové buňky nemalobuněčného karcinomu plic, neboť právě jeho nekontrolovatelná aktivace vede ke zvýšení proliferace nádorových buněk, inhibici apoptózy, zvýšení invazivity nádoru, aktivaci angiogeneze, metastazování a vzniku rezistence k chemoterapii i radioterapii [1,2].
Skupinou preparátů, které ovlivňují EGFR, jsou inhibitory tyrozinkinázové fosforylace v intracelulární části EGF receptoru.
Selektivním inhibitorem EGFR tyrozinkinázy je erlotinib (Tarceva). Jedná se o nízkomolekulární, synteticky připravený anilinochinazolinový derivát. Silně inhibuje intracelulární fosforylaci HER1/ EGFR receptoru, který je exprimován na povrchu normálních i nádorových buněk, má rovněž výrazné antiproliferační účinky, je účinný po perorálním podání a optimální dávkování u NSCLC je 150 mg denně [3].
Účinnost a bezpečnost erlotinibu u NSCLC byla potvrzena v randomizované dvojitě zaslepené placebem kontrolované klinické studii (BR.21) u 731 pacientů s lokálně pokročilým nebo metastazujícím nemalobuněčným karcinomem plic po selhání alespoň jednoho režimu chemoterapie. U většiny pacientů byl pozorován prospěšný vliv léčby erlotinibem na dobu přežití. Dalšími subanalýzami skupin nemocných s určitými charakteristikami bylo prokázáno, že z léčby erlotinibem měly prospěch všechny léčené skupiny. Nejčastěji hlášenými nežádoucími účinky u pacientů léčených erlotinibem byly vyrážka (75 %) a průjem (54 %). Stupeň závažnosti byl u většiny těchto nežádoucích účinků 1/ 2 bez nutnosti lékařské intervence. Vyrážka a průjem stupně 3/ 4 se vyskytly u 9 %, resp. 6 % pacientů léčených erlotinibem a každý z těchto nežádoucích účinků byl příčinou přerušení léčby u 1 % nemocných. Snížení dávky kvůli vyrážce a průjmu bylo třeba provést pouze u 6 %, resp. 1 % pacientů [3,4].
Erlotinib (Tarceva) je v současnosti (květen 2010) jediným inhibitorem tyrozinkinázy receptoru pro epiteliální růstový faktor (EGFR), který je v České republice registrován a kategorizován pro druhou a třetí linii léčby pokročilého NSCLC. V České republice používáme erlotinib od konce roku 2005. Vzhledem k náročnosti léčby jsou data o léčených nemocných v České republice shromažďována v registru TARCEVA. Tento registr je společným projektem České pneumologické a ftizeologické společnosti, České onkologické společnost a Institutu biostatistiky a analýz Masarykovy univerzity. Registr slouží především k monitoraci spotřeby a efektivity preparátu. Údaje o nemocných s nemalobuněčným karcinomem plic, kteří jsou léčeni Tarcevou, jsou ze 12 onkologických center České republiky, ale více než 90 % nemocných bylo a je léčeno v pneumoonkologických centrech.
Od roku 2005 do 30. 4. 2010 bylo do registru Tarceva zařazeno 1 582 nemocných. S úplným záznamem, který umožňuje hodnocení, je v registru 1 323 nemocných. Údaje o nemocných léčených erlotinibem byly zadávány na počátku retrospektivně, ale většinou jsou zadány prospektivně.
Jak se vyvíjel počet pacientů od 1. 1. 2009 do 30. 4. 2010, je patrné z obr. 1. Erlotinib byl podáván perorálně v dávce 150 mg/ den do progrese nebo nepřijatelné toxicity.
Obr. 1. Počet pacientů léčených Tarcevou – dle data zahájení léčby (rok 2009 a 2010). 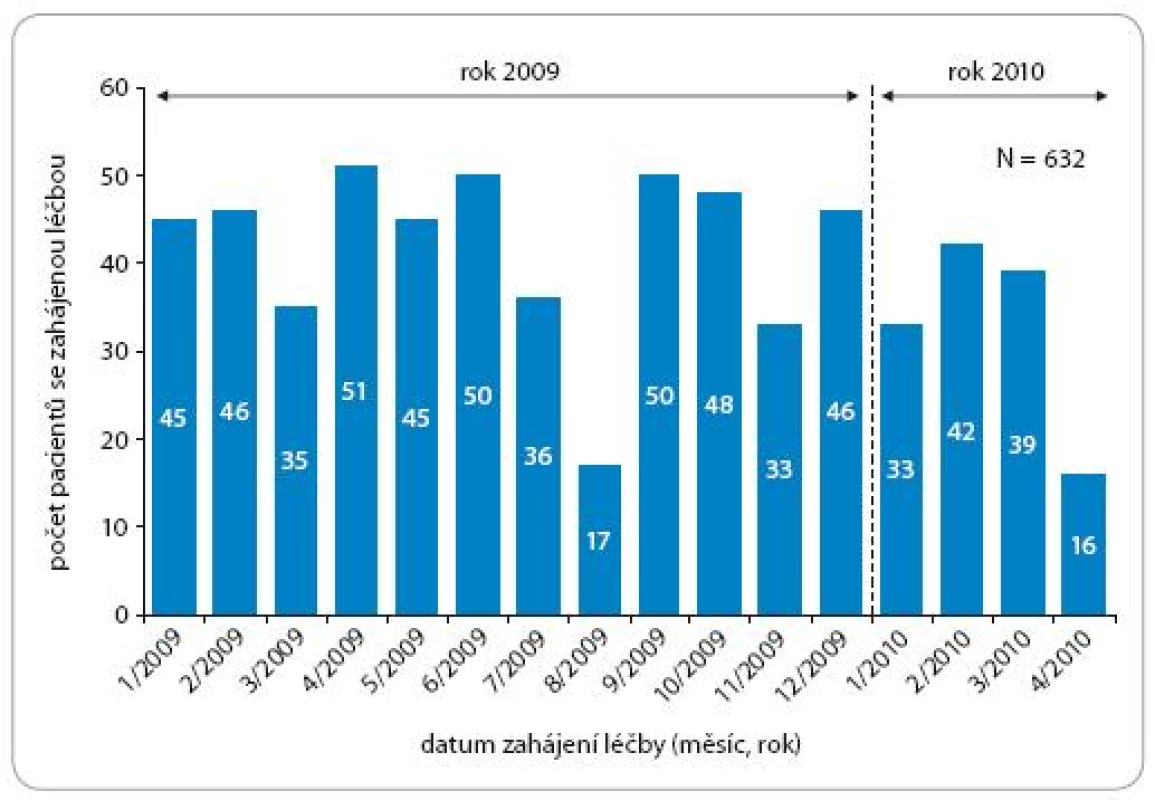
Medián věku nemocných zařazených do registru Tarceva je 64 let a zastoupení věkových kategorií je znázorněno na obr. 2, kde je i vidět srovnání s věkem nemocných dle záznamů v NOR (Národním onkologickém registru).
Obr. 2. Zastoupení věkových kategorií (vzhledem k datu zahájení léčby). 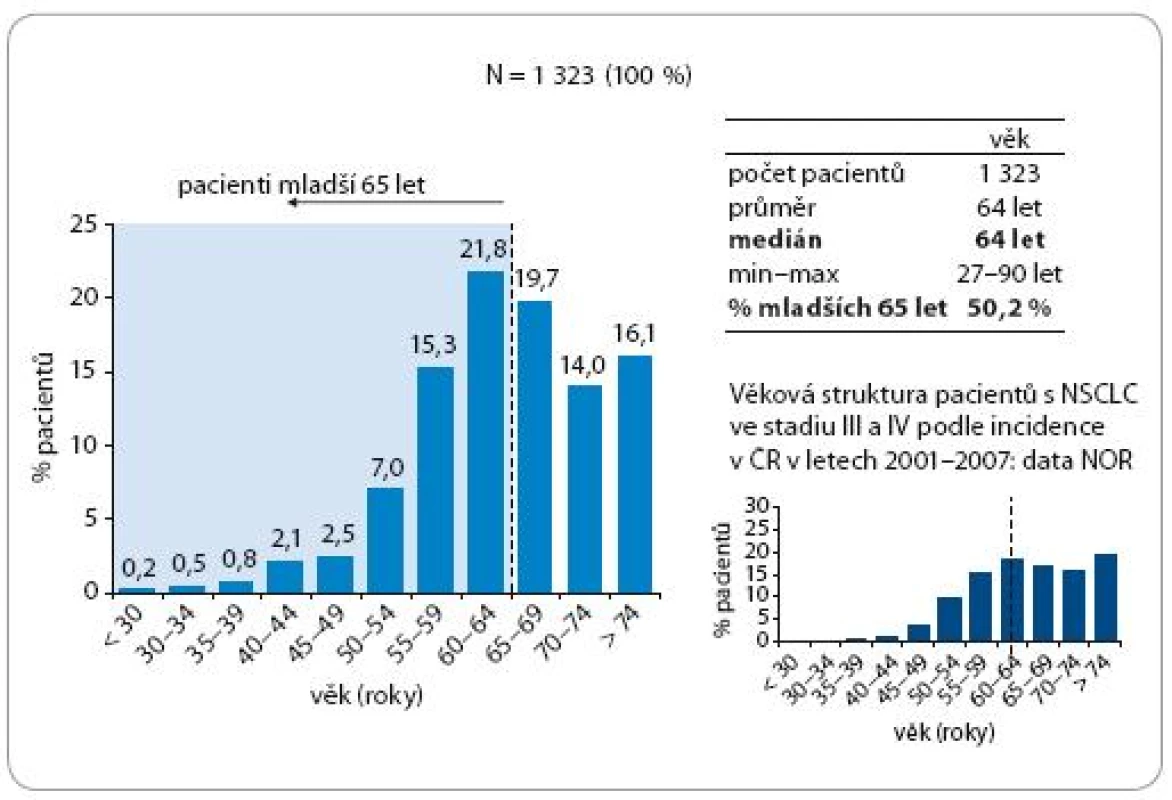
Na obr. 3 je znázorněno rozložení pohlaví. Tarcevou bylo a je léčeno 66,3 % mužů a 33,7 % žen. Na tomto obrázku je znázorněn i kuřácký status. Většina nemocných byli a jsou současní nebo bývalí kuřáci. Přesto je poměrně vysoké i procento celoživotních nekuřáků (22,2 %).
Obr. 3. Pohlaví pacientů a kouření. 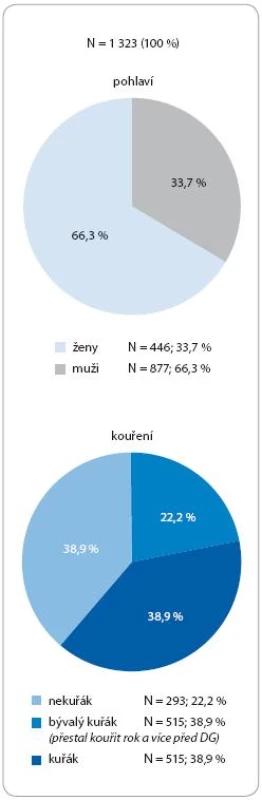
Morfologická diagnóza primárního nádoru je uvedena v obr. 4. I když v populaci České republiky převažuje epidermoidní karcinom, k léčbě Tarcevou byli v největším počtu indikováni nemocní s adenokarcinomem (45,3 %).
Obr. 4. Morfologická diagnóza primárního nádoru. 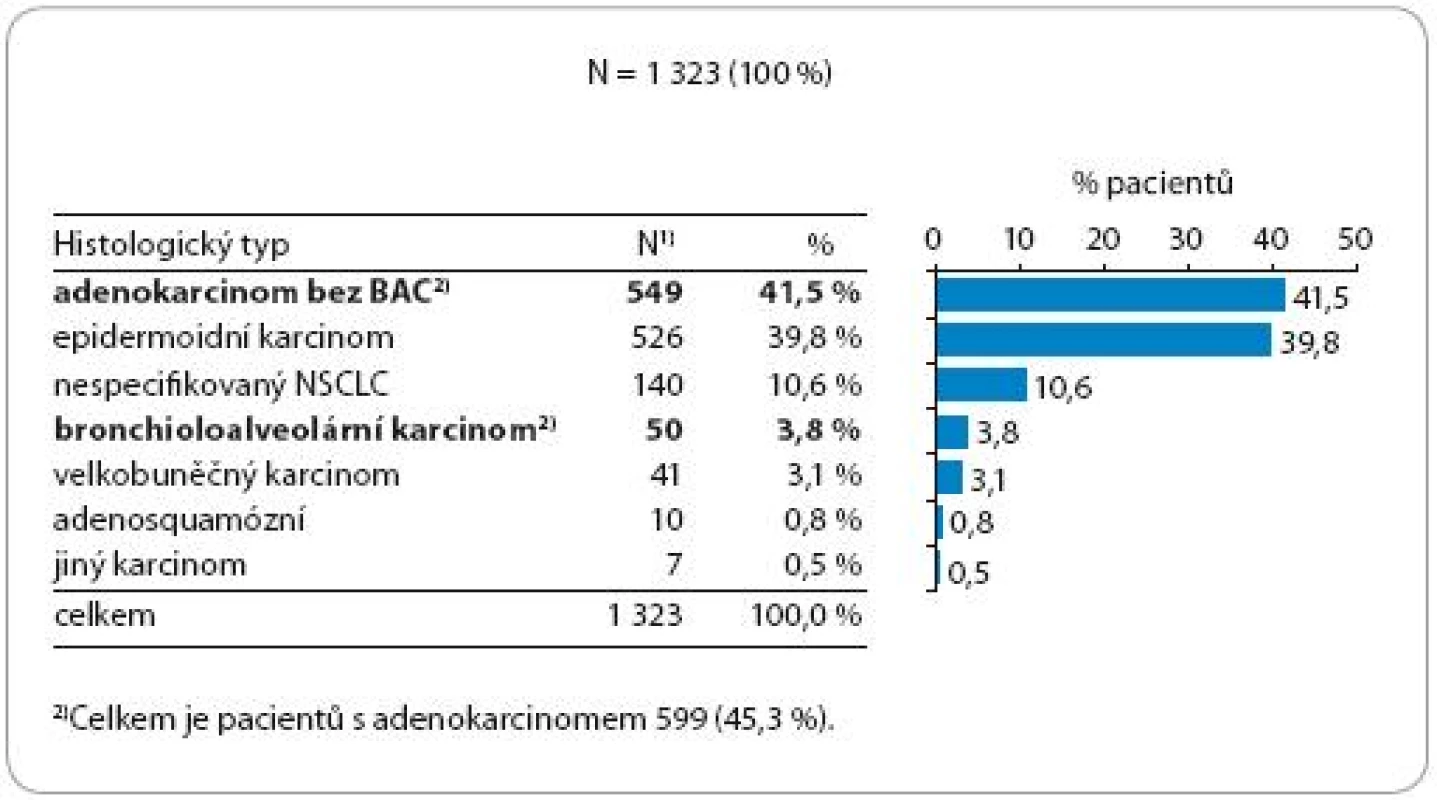
Vzhledem k tomu, že se jedná o léčbu perorální s minimem nežádoucích účinků, mohli být Tarcevou léčeni i nemocní s vyšším stavem výkonnosti (performance status – PS). Stav výkonnosti jako PS 0 byl hodnocen pouze u 7,9 % nemocných, ale jako PS 2 u 34,6 % nemocných.
Z obr. 5 je patrné, v jaké linii léčby byla Tarceva podána. Jednoznačně převažovala 2. a 3. linie léčby, ale u 14 % nemocných byla vzhledem k možné toxicitě konvenční chemoterapie a špatnému žilnímu přístupu zvolena pro první linii.
Obr. 5. Linie léčby podání Tarcevy. 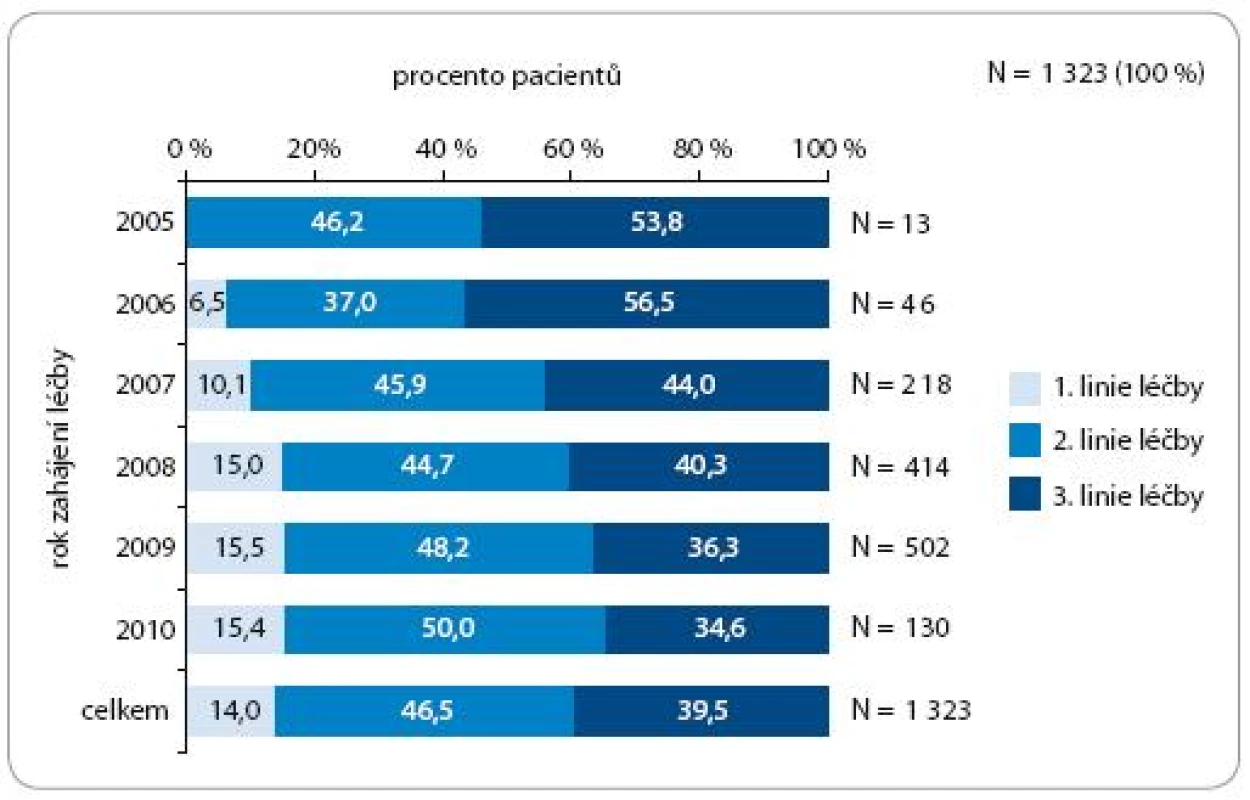
O velmi dobré toleranci léčby svědčí obr. 6. Pro nežádoucí účinky léčby bylo podávání Tarcevy ukončeno pouze u 5,5 % nemocných.
Obr. 6. Stav léčby Tarcevou a důvody jejího ukončení. 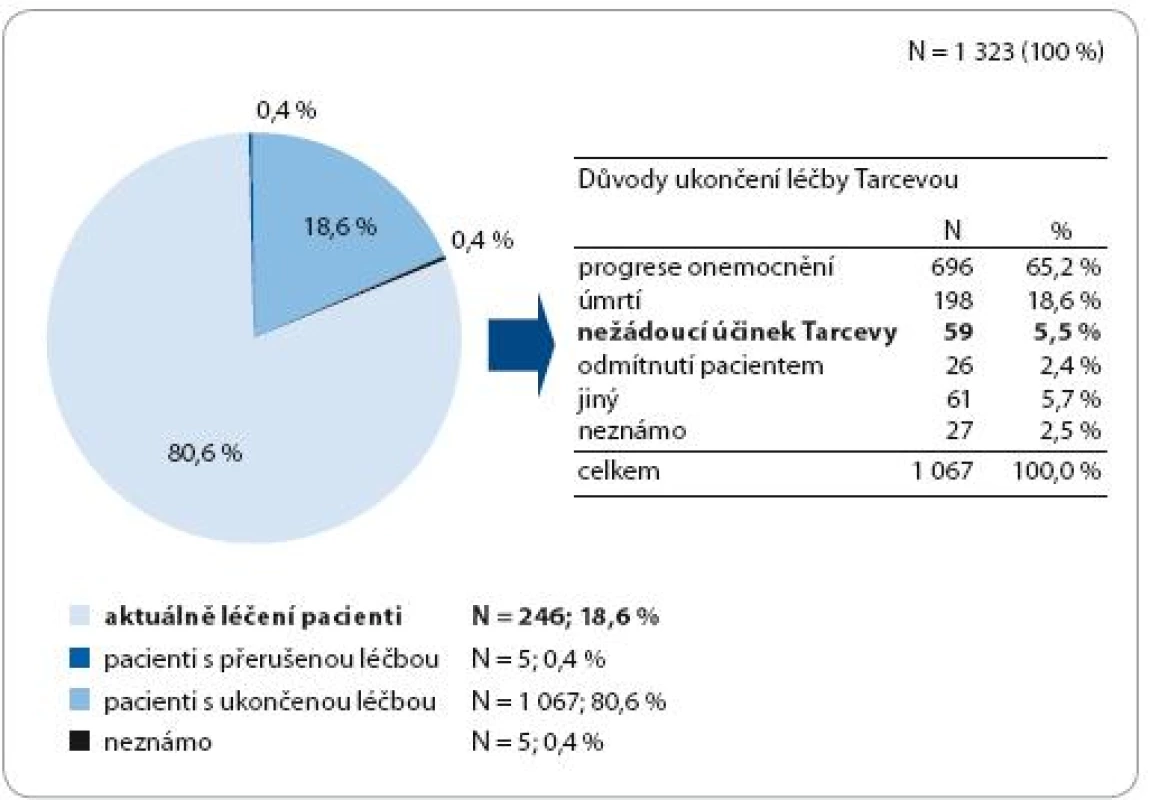
Z klinického Registru TARCEVA je možno samozřejmě zjistit další velmi cenné údaje, především o efektivitě léčby, času do progrese, celkovém přežití, ty však budou předmětem jiných zvlášť publikovaných sdělení.
Poděkování
Autoři článku děkují za přípravu podkladů pracovníkům Institutu biostatistiky a analýz MU v Brně, zejména panu Davidu Šustrovi.
prof. MUDr. Jana Skřičková, CSc.
Klinika nemocí plicních a tuberkulózy
LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: jskric@fnbrno.cz
Zdroje
1. Woodburn JR. The epidermal growth factor receptor and its inhibition in cancer therapy. Pharmacol Ther 1999; 82(2 – 3): 241 – 250.
2. Salomon DS, Brandt R, Ciardiello F et al. Epidermal growth factor‑related peptides and their receptors in human malignancies. Crit Rev Oncol Hematol 1995; 19(3): 183 – 232.
3. Souhrn údajů o přípravku Tarceva, datum revize textu 1. 7. 2010.
4. Shepherd FA, Rodrigues Pereira J, Ciuleanu T et al. Erlotinib in previously treated non‑small‑cell lung cancer. N Engl J Med 2005; 353(2): 123 – 132.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2010 Číslo 5- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Úskalí diagnostiky Kaposiho sarkomu sdruženého s HIV infekcí
- Detekcia hypermetylácie DNA ako potenciálny biomarker pre karcinóm prostaty
- Hand‑ foot syndrom po podání inhibitorů tyrozinkinázové aktivity
- Role membránových transportérů v chemorezistenci karcinomu pankreatu při terapii gemcitabinem
- Incidence a mortalita nádorových onemocnění v České republice
- 18F‑ FDG PET/ CT v diagnostice mnohočetného myelomu a monoklonální gamapatie nejistého významu: srovnání s 99mTc‑ MIBI scintigrafií
- Léčebné výsledky pacientů léčených v letech 1980– 2004 na jediném pracovišti pro nefroblastom
- České programy screeningu zhoubných nádorů v roce 2010
- Mukoepidermoidní karcinom dutiny nosní – vzácný nádor
- Kazuistika pacientky s triple negativním karcinomem prsu, která při léčbě paklitaxelem a bevacizumabem dosáhla kompletní remise plicního, uzlinového a kostního metastatického postižení
- Klinický registr TARCEVA
- Gefitinib v monoterapii u nemocných s pokročilým NSCLC nesoucím aktivující mutaci EGFR zlepšuje významně léčebné výsledky oproti standardní chemoterapii – aktualita z klinické praxe
- Profesor Koutecký osmdesátiletý
- Zápis ze schůze výboru České onkologické společnosti dne 21. 9. 2010 v Liberci
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Úskalí diagnostiky Kaposiho sarkomu sdruženého s HIV infekcí
- Hand‑ foot syndrom po podání inhibitorů tyrozinkinázové aktivity
- Mukoepidermoidní karcinom dutiny nosní – vzácný nádor
- 18F‑ FDG PET/ CT v diagnostice mnohočetného myelomu a monoklonální gamapatie nejistého významu: srovnání s 99mTc‑ MIBI scintigrafií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



