-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
RECAMO – …prostřednictvím výzkumu rakoviny k aplikované molekulární onkologii; kde, proč a jak
Autoři: B. Vojtěšek; D. Valík
Vyšlo v časopise: Klin Onkol 2012; 25(Supplementum 2): 8-10
Kategorie: Editorial
…KDE – dřívější úspěchy a současné ambice
Projekt MOÚ RECAMO byl založen Masarykovým onkologickým ústavem (MOÚ), dlouhodobým členem OECI (Organization of European Cancer Institutes). Masarykův onkologický ústav je institucí zaujímající již po pět desetiletí přední místo v komplexní léčbě rakoviny včetně jejího výzkumu. V současné době představuje největší komplexní onkologické centrum v České republice. Na základě dlouhodobé a mimořádné odbornosti získal Masarykův onkologický ústav v roce 2010 status přidruženého člena infrastruktury BBMRI (Biobanking and Biomolecular Resources Research Infrastructure), která je na seznamu ESFRI (European Strategy Forum on Research Infrastructures). Základní úlohou této infrastruktury je poskytnout vědeckým pracovníkům z oblasti biomedicíny vysoce kvalitní biologický materiál, který by mohl být použit pro základní výzkum a aplikovaný translační výzkum v oblasti nádorové biologie. V současné době se MOÚ aktivně účastní příprav konsorcia BBMRI-ERIC (European Research Infrastructure Consortium).
Projekt RECAMO si klade za cíl vytvořit multidisciplinární skupinu výzkumných pracovníků a lékařských specialistů za účelem klinicky aplikovat informace získané studiem definovaných oblastí nádorového výzkumu týkající se buněčné signalizační dráhy proteinu p53, úlohy nádorových kmenových buněk, ubikvitin-chaperonového systému a angiogeneze. Chceme využít vlastní zkušenosti v oblasti genomických a proteomických technologií pro identifikaci a evaluaci nových nádorových biomarkerů s použitím dobře charakterizovaných klinických vzorků, které máme k dispozici, a zhodnotit použitelnost nových zobrazovacích metod u onkologických pacientů. Klíčovým aspektem celkové strategie projektu je zefektivnit využití získaných znalostí v aplikovaném výzkumu zahájením spolupráce s komerční sférou. Konečným cílem projektu je pak přenést poznatky základního výzkumu do podoby klinicky použitelných markerů, které budou moci být využity ke zlepšení péče o pacienta.
Limitace a nedostatky současného výzkumu nádorů
Rozvoj metod sekvencování DNA a čipových technologií umožňuje velmi rychle stanovit genomový profil nádorů. Tyto genomické přístupy poskytují rozsáhlé informace o mutačních spektrech nádorů zahrnující změny v počtu kopií genů, bodové mutace, chromozomové translokace, epigenetické změny a úlohu regulačních nekódujících RNA. Proteomické technologie, ačkoli jsou méně vyspělé, přinášejí naopak významné informace o změnách hladin jednotlivých proteinů v nádorech. Všechny tyto poznatky nejen napomáhají porozumět vzniku rakoviny a charakterizovat její vlastnosti, ale poskytují rovněž klinicky využitelné údaje, například identifikují nové cíle protinádorové léčby. V neposlední řadě může hledání cirkulujících proteinů v krvi či jiných tělních tekutinách, jako třeba v moči, odhalit nové markery pro screening nádorů, sledování jejich progrese či odpovědi na terapii, které mohou být stanoveny neinvazivními metodami. V současnosti jsou neustále identifikovány a navrhovány nové a nové potenciální biomarkery. Největší výzvou pro vědeckou společnost je však převedení těchto nových poznatků do podoby klinicky využitelných testů, které by zlepšily péči o pacienta. Zásadní překážkou v dosažení tohoto cíle je však dostupnost vhodných vzorků od pacientů a jejich relevantní charakterizace nutná pro evaluaci nových markerů. Jinou významnou překážku pak představuje schopnost produkovat reagencie nezbytné pro vývoj a komercializaci testů použitelných v klinické praxi. Přestože se mnoho jednotlivých laboratoří pokouší o identifikaci nových nádorových biomarkerů, existuje jen velmi málo skupin schopných vyhodnotit jejich reálnou použitelnost, nebo skupin, které by měly dostatek zkušeností a byly napojeny na komerční sféru, aby mohly vyvinout testy použitelné v klinické praxi.
Jednotlivé projekty RECAMO jsou navrženy tak, aby spojily vědce zabývající se základním výzkumem nádorové biologie a lékaře se zkušenostmi z klinické praxe, a tím umožnily aplikovat nové vědecké poznatky v klinickém prostředí. Projekty jsou propojeny definovanými výzkumnými, klinickými a možnými komerčními činnostmi (obr. 1). Jádrem projektu je spolupráce mezi pracovníky základního a klinického výzkumu, kteří by shromažďovali vzorky tkání primárních nádorů, na základě současných znalostí identifikovali klíčové genetické změny v nádorech, a vytvořili tak databázi prognóz, odpovědí pacientů k aplikované léčbě a ostatních obecných výsledků. „Program nádorového výzkumu“ bude definovat: A) proteom/transkriptom//genom nádorových vzorků s cílem identifikovat jednotlivé složky (i) odpovědné za vznik metastáz a rezistenci k terapii, (ii) patřící k ubikvitin-chaperonovému systému a s cílem nalezené složky dále zhodnotit jako potenciální cíle protinádorové terapie; B) strategii pro nalezení a validaci nových biomarkerů v diagnostice včetně jejich potenciální aplikace v molekulárním zobrazování při detekci nádoru, určení stupně rychlosti růstu (tzv. grade) a predikci odpovědi na léčbu; C) použití inovativních technologií pro nalezení nových klíčových biomarkerů nádorů včetně proteinů odpovědných za maligní transformaci, metastazování a rezistenci k aplikované léčbě a proteinů, jež jsou součástí molekulárního ubikvitin-chaperonového systému s cílem obohatit „proteom“ z komplexní klinické směsi; D) strategii validace nových biomarkerů a terapeutických cílů; E) strategie vývoje imunoreagencií pro komerční využití včetně vývoje diagnostických a screeningových kitů pro testování potenciálních terapeutických látek a pro potenciální využití imunoreagencií v zobrazovacích metodách v diagnostice. Tento multidisciplinární přístup si tak klade za cíl nalézt nové proteinové biomarkery metastazování a rezistence lidských nádorů pomocí experimentálních modelů a klinického materiálu a poskytnout diagnostické markery, které by vedly ke zdokonalení zobrazovacích technik k určování stadia nemoci a odpovědi ke zvolené terapii. Nalezené proteiny budou dále hodnoceny pro budoucí vývoj nových protinádorových léčiv.
Obr. 1. Konceptuální mapa projektu RECAMO, který je strukturován do tří ramen: rameno VR specifikuje jednotlivé výzkumné cíle, rameno AMO využívá výsledky ramena VR uvnitř RECAMO či v partnerských infrastrukturách jako např. CEITEC a rameno KV, v němž dosažené výsledky přecházejí do komercializovatelných jednotek jako např. terapeutik nebo diagnostických kitů. 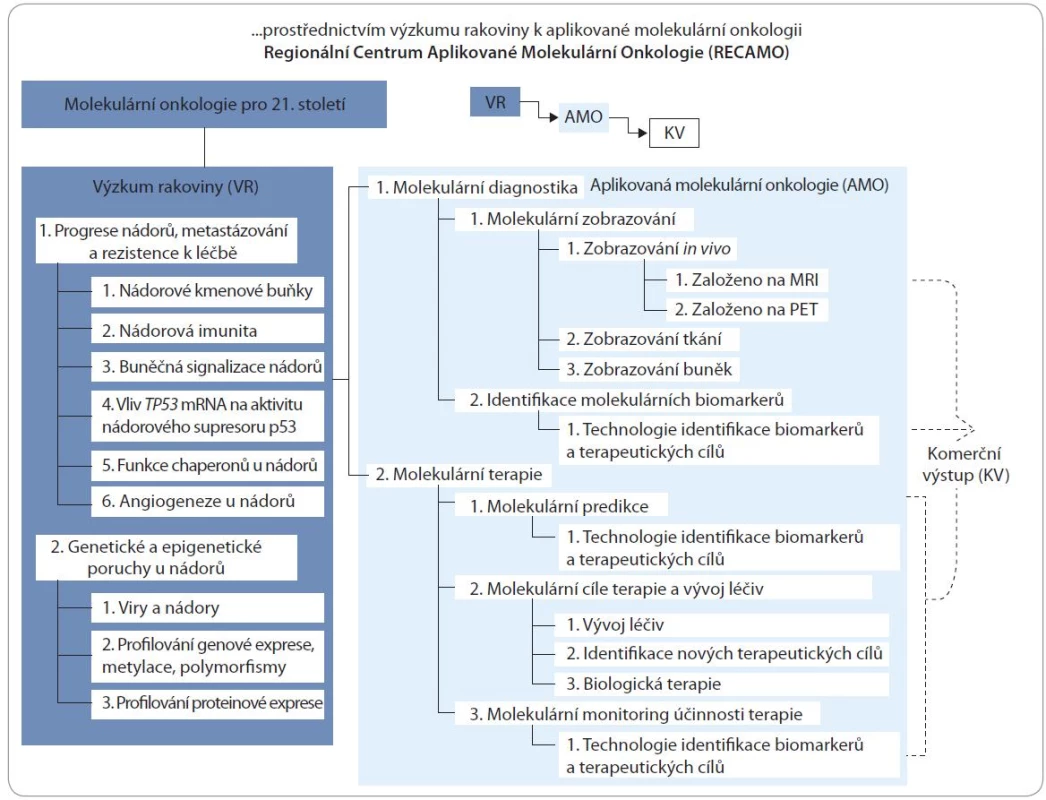
…PROČ – představy a cíle
Nové a výkonné genomické a proteomické metody biomedicínského výzkumu včetně molekulárního zobrazování ženou kupředu vývoj personalizované medicíny, v níž je léčba indikována podle fyziologických a genetických vlastností pacienta a konkrétních vlastností nádoru. Rozvoj techniky sekvencování a znalost kompletní sekvence lidského genomu zvýšily pravděpodobnost, že by znalost genomu pacienta mohla být využita k výběru vhodné a účinné terapie. Významných pokroků v terapii nádorových onemocnění bylo dosaženo zejména kombinací cytogenetických a molekulárně-biologických přístupů a využitím modelových organizmů pro stanovení funkce genů uplatňujících se při nádorové transformaci. Znalost kompletní sekvence lidského genomu taktéž umožnila rozvoj účinných a progresivních technologií, jako například DNA mikročipů. Použití mikročipů v rutinní diagnostice je však málo pravděpodobné vzhledem k náročnému zpracování vzorků a dalším technickým aspektům metody. Rakovina je heterogenní a tkáňově specifické onemocnění, jehož molekulární patologie navíc ne zcela odpovídá poznatkům získaným pomocí modelových systémů. V současné době se obecně připouští, že nádorové buněčné linie používané v základním výzkumu nemusejí plně reflektovat skutečný obraz rakoviny u člověka, a proto narůstá potřeba definovat proteom a transkriptom lidských klinických vzorků. Revoluční objevy v molekulární biologii a genomice za posledních 10 let významně posílily naděje na zdokonalení diagnostických a terapeutických postupů u mnoha typů nádorů. Objevy nových biomarkerů umožňujících přesněji diagnostikovat nádorové onemocnění či předpovědět pacientovu prognózu a odpověď na zvolenou terapii však vyžadují multidisciplinární přístup zahrnující spolupráci mezi týmy základního výzkumu nádorové biologie, onkologickými specialisty a odborným zdravotnickým personálem, výrobními technology a farmaceutickými společnostmi. Takto navržená síť skupin spolupracujících v rámci jedné instituce je nezbytná pro úspěšnou identifikaci nových biomarkerů a jejich aplikaci u specifických skupin pacientů.
...JAK – týmový přístup
K nalezení a validaci nových biomarkerů využijeme multidisciplinární přístup zahrnující buněčnou biologii, imumochemii a strukturní biologii, chemickou biologii a lékařskou chemii, peptidovou mimetiku, hmotnostní spektrometrii a proteomiku, transkriptomiku, screening nízkomolekulárních látek a klinický výzkum. Naším cílem je rozšířit znalosti týkající se proteinu p53, molekulárních chaperonů a imunitního systému, identifikovat nové diagnostické a terapeutické cíle a vyvinout cílené přístupy pro kontinuální vývoj nových protinádorových léčiv. Klíčové aspekty realizace korespondují s krátkodobými cíli projektu RECAMO: 1) prosazovat úzkou spolupráci mezi jednotlivými disciplínami pro identifikaci nových biomarkerů, 2) korelovat odpovědi pacientů k aplikované léčbě s komplexní validací biomarkerů, 3) získat přístup k důležitým biologickým vzorkům vytvořením centrálního registru a 4) vytvořit standardy klinické metodologie zaměřené na identifikaci biomarkerů. Další aspekty realizace souvisejí s dlouhodobým záměrem projektu RECAMO: 1) rozvíjet metody detekce biomarkerů souběžně s vývojem protinádorových léčiv, 2) podpořit přijetí všeobecných pravidel pro publikaci studií o biomarkerech, 3) stanovit pravidla pro validaci biomarkerů, 4) usnadnit přístup k informacím týkajícím se všech studií o biomarkerech a 5) vzdělávat zúčastněné strany ve všech aspektech výzkumu biomarkerů.
Je naprosto zřejmé, že úspěšný výzkum a nalezení nádorových biomarkerů vyžadují spojení různých vědních disciplín směřujících ke společnému cíli. Jak je nepřímo vyjádřeno v OP VaVpI, je tento přístup nezbytný zejména při výzkumu biomarkerů a vývoji protinádorových léčiv využívajících klinický materiál. Naší snahou je doplnit chybějící článek tím, že vytvoříme moderní multi disciplinární interaktivní centrum zabývající se identifikací biomarkerů, které jsou významné pro diagnostiku, léčbu rezistentních variant nádorových onemocnění a metastazování. Naším hlavním cílem je uplatnit poznatky získané ze základního výzkumu rakoviny a prostřednictvím nejnovějších technologií transkriptomiky a hmotnostní spektrometrie a s použitím velmi dobře definovaných klinických vzorků identifikovat nové biomarkery u specifických typů nádorů. Jednotlivé výzkumné aktivity v RECAMO nejenže využívají nejmodernější technologie pro dosažení požadovaných cílů, snahou také bude tyto technologie dále rozvíjet. Vzájemné spojení jednotlivých projektů (obr. 1) pak vytvoří celek, který zaručí progresivní rozvoj a úspěch v oblasti výzkumu nádorových biomarkerů.
V centru RECAMO klademe velký důraz na podporu a profesní rozvoj mladých vědeckých pracovníků. Nově vybudované výzkumné centrum významně přispěje ke zkvalitnění výuky pregraduálních a postgraduálních studentů brněnských univerzit inovací náplně stávajících kurzů a zavedením nových výukových předmětů. Prostřednictvím atraktivního výzkumného programu RECAMO usiluje o zapojení studentů magisterských a doktorských studijních programů do projektu. Úzká spolupráce se špičkovými tuzemskými a zahraničními pracovišti dále umožní pracovníkům RECAMO získat zkušenosti v renomovaných výzkumných laboratořích a na pracovištích aplikační sféry, což povede ke zlepšení profesních vyhlídek studentů v odvětvích výzkumu, zdravotnictví, v akademické sféře či farmaceutickém nebo biotechnologickém průmyslu.
RNDr. Bořivoj Vojtěšek, DrSc.
vědecký ředitel RECAMO
doc. MUDr. Dalibor Valík, Ph.D.
výkonný ředitel RECAMO
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2012 Číslo Supplementum 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejasný stín na plicích – kazuistika
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- p63 – důležitý hráč ve vývoji epidermálních struktur a nádorových onemocnění
- Detekce nádorových kmenových buněk v sarkomech
- Zvýšený počet NKT-like buněk u pacientů se solidními nádory
- Nádory jako metabolická onemocnění a diabetes jako riziko nádorů?
- Regulace syntézy p53
- Kontrola kvality proteinů a kancerogeneze
- Role molekulárních chaperonů a ko-chaperonů v biologii nádorů
- RECAMO – …prostřednictvím výzkumu rakoviny k aplikované molekulární onkologii; kde, proč a jak
- Úloha krevních destiček v rozvoji nádoru
- Cirkulující hladina faktoru aktivujícího B buňky u pediatrických onkologických pacientů s nádorovou kachexií nebo bez ní
- Kombinace přístupů imunoprecipitace a hmotnostní spektrometrie v analýze interakčních partnerů ΔNp63
- Identifikace a charakterizace prometastatických cílů, drah a molekulárních komplexů s využitím proteomických technologií
- Infrastruktura výzkumných biobank BBMRI_CZ: klíčový nástroj translačního výzkumu v onkologii
- RECAMO – …prostřednictvím výzkumu rakoviny k aplikované molekulární onkologii; kde, proč a jak
- Vývoj a využití jiných PET radiofarmak než FDG na Masarykově onkologickém ústavu
- Nové možnosti starého léku: DHFR- a non-DHFR-mediované účinky metotrexátu na nádorové buňky
- Stereotaktická radioterapie jaterních metastáz kolorektálního karcinomu; časné výsledky
- Fáze I klinických studií v onkologii – teorie a praxe
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- p63 – důležitý hráč ve vývoji epidermálních struktur a nádorových onemocnění
- Zvýšený počet NKT-like buněk u pacientů se solidními nádory
- Role molekulárních chaperonů a ko-chaperonů v biologii nádorů
- Fáze I klinických studií v onkologii – teorie a praxe
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



