-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vyšetření tenkého střeva pomocí magnetické rezonance
The examination of the small intestine by magnetic resonance imaging
Diagnostic imaging of the abdominal cavity and the gastrointestinal tract is increasingly performed by new-emerged fast MR imaging sequences and it is moving to the centers of magnetic resonance. Our work is devoted to the examination of the small intestine by magnetic resonance, so-called MR enterography. Review discusses general description - from preparation of patient to basic pathological findings, with special focus on currently most investigated small intestine disease – Crohn‘s disease.
Key words:
Crohn‘s disease – enteroclysis – MR enterography
Autoři: Jiří Vaníček 1,2; Lukáš Hruška 1; Bohuslav Kianička 3
Působiště autorů: Klinika zobrazovacích metod LF MU a FN u sv. Anny, Brno, přednosta MUDr. Jiří Vaníček, Ph. D. 1; Mezinárodní centrum klinického výzkumu – FN u sv. Anny Brno, ředitel Gorazd B. Stonkin, M. D., MSc., Ph. D. 2; Gastroenteroloígické oddělení II. interní kliniky LF MU a FN u sv. Anny Brno, přednosta prof. MUDr. Miroslav Souček, CSc. 3
Vyšlo v časopise: Vnitř Lék 2015; 61(2): 125-128
Kategorie: Přehledný referát
Souhrn
Diagnostické zobrazování břišní dutiny a gastrointestinálního traktu se díky nástupu nových tzv. rychlých zobrazovacích MR sekvencí stále více přesouvá na pracoviště magnetické rezonance. Naše práce je věnovaná vyšetření tenkého střeva magnetickou rezonancí, tzv. MR enterografií, a to jejímu obecnému popisu – od přípravy pacienta až k základním patologickým nálezům, se zvláštním zřetelem na v současné době nejčastěji vyšetřovanou chorobu tenkého střeva – Crohnovu nemoc.
Klíčová slova:
Crohnova choroba – enteroklýza – MR enterografieÚvod
Pokroky v zobrazování magnetickou rezonancí (magnetic resonance imaging – MRI), zejména pak rozvoj tzv. rychlých MR sekvencí, umožnily rozšířit pole působnosti MR vyšetření i na zobrazování gastrointestinálního traktu, včetně vyšetření tenkého střeva.
Vysoký tkáňový kontrast obrazu vyšetření magnetickou rezonancí, tzv. multiplanární zobrazování v libovolné, zejména koronální rovině, dále možnost získat i funkční informace dělají z magnetické rezonance zobrazovací metodu, která je velmi vhodná pro zobrazování onemocnění tenkého střeva. Absence ionizujícího záření, které bylo nezbytné pro vyšetření tenkého střeva v minulosti při vyšetření zvaném enteroklýza, které zatěžovalo personál i pacienta, je další výhodou a pokrokem této modality. Je třeba vnímat i fakt, že se často jedná o pacienty mladistvé a mladé dospělé, protože nejčastěji vyšetřovanou skupinou jsou nemocní se zánětlivým postižením tenkého střeva (zejména s Crohnovou nemocí). U tohoto onemocnění vzniká potřeba opakovaných kontrol v průběhu léčby, čímž by narůstala radiační zátěž organizmu, pokud by se vyšetřovalo pomocí RTG záření jako u enteroklýzy.
Velkou výhodou MRI proti konvenčním RTG technikám při vyšetření střeva je přímá vizualizace střevní stěny a jejího okolí, což radiologům umožňuje hodnotit rozsah zánětlivých a reaktivních změn. Zkušený radiolog je schopný na základě MR charakteristik i určit aktivitu onemocnění [1].
Technika vyšetření
Příprava pacienta
Plánované vyšetření tenkého střeva na našem pracovišti zahrnuje tento postup: pacient je lačný po dobu 24 hod a jeho gastrointestinální trakt je připraven k vyšetření 2 l roztoku Fortrans (nebo analogického roztoku), podanými perorálně, za účelem dokonalého vyprázdnění. Podle některých autorů postačuje 4hodinové lačnění [2], čehož na našem pracovišti využíváme zejména u akutních pacientů. V akutních případech při přípravě střeva roztokem Fortrans postupujeme individuálně dle stavu pacienta.
Perorální kontrastní látky
K validnímu hodnocení tenkého střeva v jakékoliv zobrazovací modalitě je potřeba naplnit a rozšířit jeho lumen. K tomu se u MR enterografie využívají perorální kontrastní látky. V současné době v literatuře neexistuje shoda co do množství a typu použitého kontrastního média.
Minimálním množstvím je 1 000 ml roztoku kontrastní látky, přičemž u nejčastěji používaného manitolu Ajaj et al [4] nezaznamenali signifikantní rozdíl mezi 1 000, 1 200 a 1 500 ml. Na našem pracovišti považujeme za minimum 1 000 ml 2,5% roztoku manitolu, přičemž dle tolerance pacienta podáváme množství do 1 500 ml. Rovněž není v literatuře shoda v načasování podávání kontrastní látky. Nám se osvědčilo začít podávat kontrastní látku 45 min před vyšetřením ve třech 500 ml dávkách, přičemž poslední objem pacient dopíjí při vstupu do MR vyšetřovny, což je přibližně ve shodě s prací Laghi et al [3].
Perorální kontrastní látky lze na základě signálové intenzity v jednotlivých váženích MR obrazu rozdělit na pozitivní, negativní a bifázické [4], obr. 1.
Obr. 1. Normální MR obraz tenkého střeva (MR sekvence T2 SSFSE) 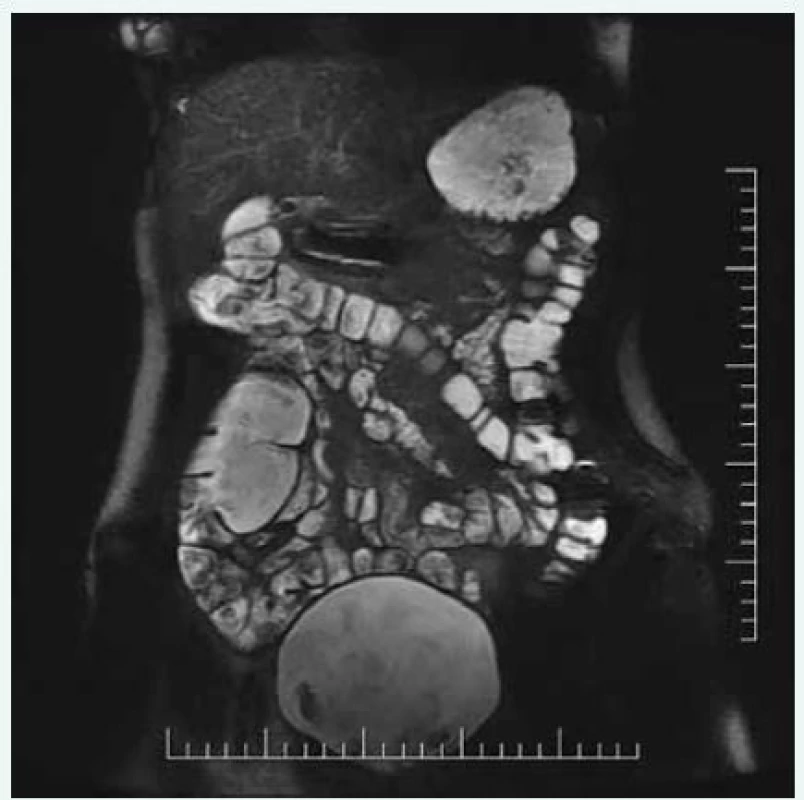
Pozitivní kontrastní látkou se rozumí paramagnetická substance, která podmiňuje zvýšení signálu v T1 vážených obrazech, přičemž se využívají koncentrace, které zkracují T1 relaxační čas a zároveň jen minimálně, nebo v lepším případě vůbec neovlivňují T2 relaxační čas. Pozitivní kontrastní látky obsahující cheláty gadolinia, ionty železa či manganu byly v začátcích MR zobrazování velmi populární, v současné době se však nepoužívají z toho důvodu, že vysoký signál intraluminálně v nativních sekvencích může maskovat postkontrastní sycení stěny, čímž dělá diagnostiku náročnější a zejména méně přesnou.
Negativní kontrastní látky jsou roztoky, které podmiňují nízký signál na T1 i T2 vážených obrazech. Tyto látky indukují lokální nehomogenity v magnetickém poli, čímž ovlivňují T1 i T2 relaxační časy. Negativní kontrastní látky (např. vysoké koncentrace síranu barnatého, oxidy železa) mají hlavní výhodu v tom, že zejména na T2 vážených obrazech podmiňují vysoký vzájemný kontrast mezi zánětlivě postiženou stěnou (typicky se zvýšeným signálem) a intraluminálním obsahem. Tento kontrast může být ještě zvýrazněn použitím sekvencí potlačujících MR signál tuku. Nicméně byl zaznamenán dramatický ústup v používání těchto kontrastních látek kvůli neprokázanému výraznějšímu přínosu proti dále uvedeným bifázickým kontrastním látkám a kvůli vyšší ceně zmíněných látek.
Bifázickou kontrastní látkou se myslí kontrastní látka, která je hypersignální na T1 vážených obrazech a zároveň hyposignální na T2 vážených obrazech, anebo opačně. První skupina (T1 hypersignální, T2 hyposignální) vykazuje stejný nedostatek jako již zmíněné pozitivní kontrastní látky, a proto se nevyužívají.
Naopak druhá skupina kontrastních látek, a sice látky hyposignální na T1 vážených obrazech a současně hypersignální na T2 vážených obrazech, patří při vyšetření tenkého střeva k celosvětově nejpoužívanějším, a to kvůli vysokému T2 signálu, který umožňuje výborně hodnotit morfologii stěny a zároveň nízký signál na T1 vážených obrazech, který v kombinaci s intravenózní aplikací MR kontrastních látek s obsahem chelátů gadolinia a s použitím tuk potlačujících MR sekvencí podmiňuje vysoký kontrast mezi intraluminálním obsahem a sytící se stěnou střevní při aktivních zánětlivých procesech.
Do této skupiny řadíme vodu a dále hyperosmolární a izoosmolární vodní roztoky. Ačkoliv je voda nejbezpečnějším a nejlevnějším agens, trpí velkým nedostatkem, a sice při pasáži gastrointestinálním traktem dochází k její absorpci, a tudíž je distenze střeva nedostatečná k validnímu hodnocení.
Z hyperosmolárních roztoků je nejrozšířenější manitol v různých koncentracích dle různých autorů. Dhafer et al [5] používá 5% roztok. Nevýhodou hyperosmolárních látek jsou jejich nežádoucí účinky, zejména průjmy, zvýšený meteorizmus a křeče. Na našem pracovišti proto používáme pouze 2,5% vodní roztok manitolu, se kterým máme v oblasti nežádoucích účinků velmi dobré zkušenosti – převážnou většinou pacientů je dobře snášen a případy, kdy bylo nutné vyšetření kvůli průjmu přerušit, jsou zcela ojedinělé.
Nejčastěji používanou izoosmolární látkou je roztok polyetylén glykolu (PEG), který je dostupný i ve formě komerčně vyráběného roztoku Volumen® (Bracco, Milano, Itálie), v naší republice však není dostupný.
Intravenózní kontrastní látky
Pro validní zhodnocení a zejména k určení aktivity onemocnění je nezbytná intravenózní aplikace Gd-kontrastní látky. Po aplikaci kontrastní látky pak vyšetřujeme dynamicky, zhotovujeme koronální scany v 15., 45. a 90. vteřině po aplikaci kontrastní látky [5].
Vzhledem k faktu, že postkontrastní T1 sekvence jsou výrazně citlivé vůči pohybovým artefaktům peristaltiky střeva, je nutná intravenózní aplikace spasmolytika. Na našem pracovišti aplikujeme butylskopolamin v dávce 20 mg intravenózně před aplikací kontrastní látky.
Zobrazovací sekvence MR vyšetření
Jak už bylo zmíněno výše, využíváme tzv. rychlé MR sekvence. Na našem pracovišti provádíme vyšetření na 3T přístroji GE Discovery 750 a standardně zhotovujeme obrazy v koronální a axiální rovině. Rovinu sagitální využíváme zřídka ve specifických případech (např. podezření na fistulace v malé pánvi). Využíváme celotělové cívky MR přístroje a velké pole zobrazení FOV (field of view), obvykle 40–44 cm, tak aby bylo zobrazené jak břicho, tak i pánev současně. Provádíme obrazy v tzv. sekvenci FIESTA s i bez potlačení signálu tuku, dále tzv. SSFSE sekvenci v T2 váženém obraze, rovněž s i bez potlačení signálu tuku v MR obraze. Postkontrastně pak provádíme dynamické LAVA sekvence v koronální rovině a FSPGR sekvenci v T1 váženém obraze s potlačením signálu tuku v axiální vyšetřovací rovině. Celé vyšetření trvá asi 20–25 min.
Nejčastější nálezy MR enterografie
Nález postižení střeva hodnotíme na T2 vážených obrazech, šíře stěny normálního tenkého střeva by při ideální distenzi neměla mít > 1–2 mm. Po aplikaci kontrastní látky provádíme T1 vážené MR sekvence gradientního echa s potlačením signálu tuku, stěna normálního střeva se přitom homogenně sytí a má při ideální distenzi již zmíněnou šíři 1–2 mm, šíře stěny nenaplněné, nedistendované střevní kličky by neměla být > 3–4 mm (obr. 2).
Obr. 2. Normální MR obraz tenkého střeva (postkontrastní tzv. LAVA MR sekvence) 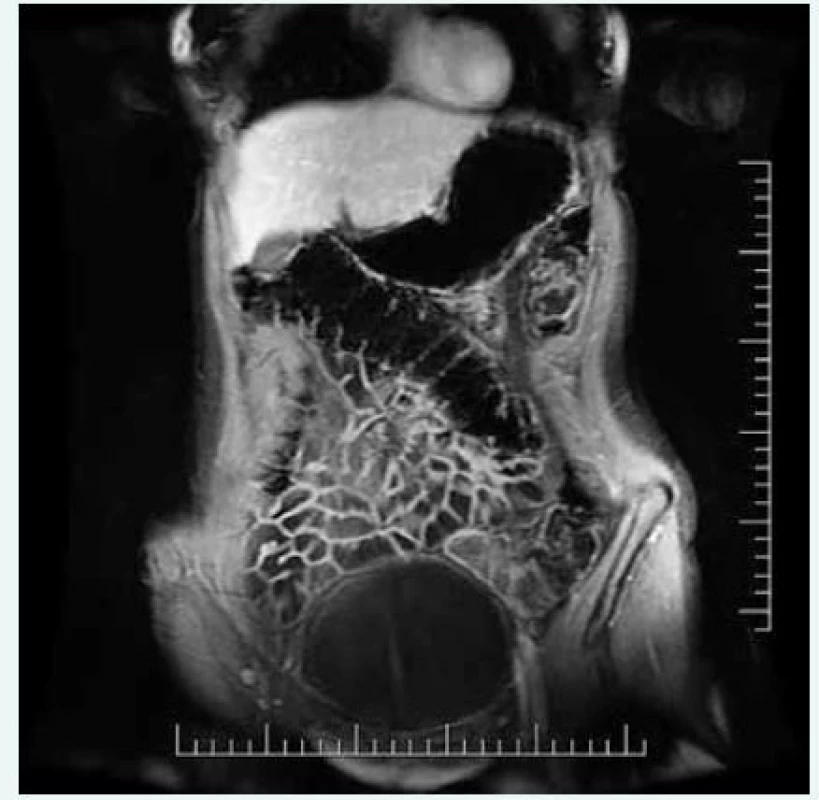
Crohnova choroba
Crohnova nemoc je nejen na našem pracovišti nejčastější indikací k provedení MR enterografie. Radiolog je na základě tohoto vyšetření schopen posoudit aktivitu onemocnění a vyjádřit se k případným komplikacím, jako jsou fistulace či mezikličkové abscesy (obr. 3).
Obr. 3. Obraz zánětlivých změn terminálního ilea (MR sekvence T2 SSFSE) 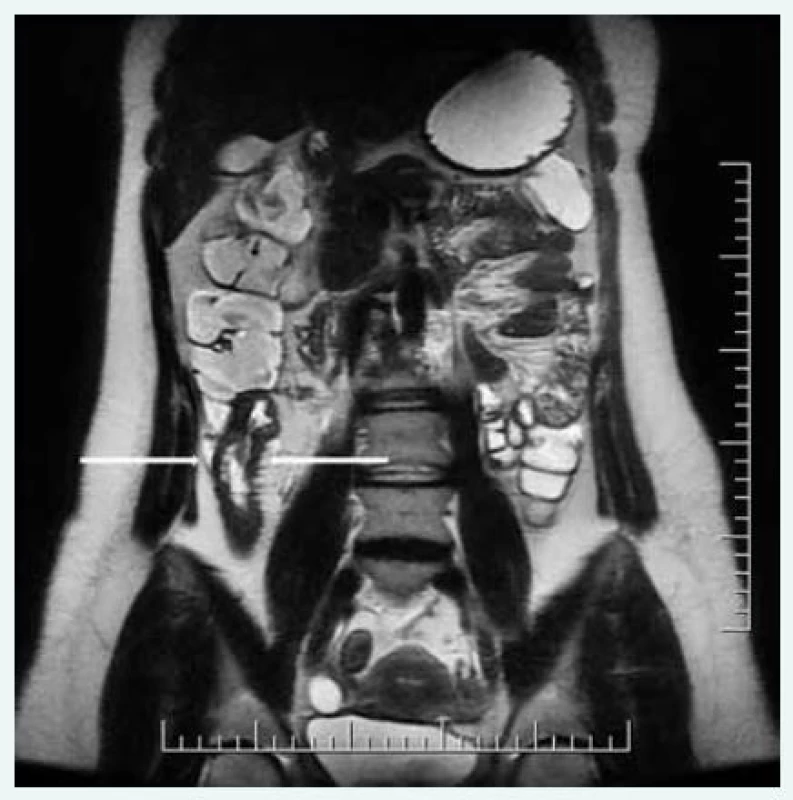
U pacientů s již diagnostikovaným onemocněním je nutno zodpovědět důležitou otázku, zda je přítomný aktivní zánět či nikoliv. Abychom se mohli vyjádřit k příčině ztluštění stěny střeva, je nutno porovnat vzhled postižených úseků na nativních T2 a postkontrastních T1 vážených MR obrazech. Aktivní zánět je charakterizován zvýšeným T2 signálem, jenž je podmíněn edémem stěny a zároveň i jejím výrazným sycením po intravenózní aplikaci kontrastní látky. Fibrostenotické postižení na podkladě dlouhodobé fibrózy bude mít na T2 vážených obrazech nízký signál a sycení stěny tak bude spíše nižší v porovnání se zdravým úsekem tenkého střeva [6]. K dalším znakům, které umožňují diferencovat mezi akutním zánětem a fibrózou, patří vzhled submukózního tuku: tento tuk by měl mít stejný signál v MR obraze jako tuk mezenteriální.
Velmi důležitou součástí vyšetření je i detekce extramurálních patologických změn. Častou komplikací Crohnovy nemoci je fistulace do okolí, do střevních kliček nebo slepě do dutiny břišní. V MR obraze má píštěl vzhled tekutinou vyplněných kanálků, které vykazují periferní postkontrastní enhacement své stěny díky jejímu reaktivně zvýšenému prokrvení. Pro gastroenterologa a zejména pro chirurga je velmi důležité případné fistulace popsat co nejpodrobněji (jejich průběh, kam ústí, co je v okolí atd).
Celiakie
Celiakie je chronický zánětlivý proces postihující gastrointestinální trakt u geneticky predisponovaných jedinců. Role MR (i jiných zobrazovacích metod) je limitovaná, vzhledem k faktu, že diagnóza je stanovená na základě jejunální biopsie. Nicméně dle literatury [7] přibližně 75 % pacientů má radiologicky detekovatelné změny, k nimž patří intestinální atonie, slizniční změny a komplikace (obr. 4).
Obr. 4. Obraz zánětlivých změn terminálního ilea (postkontrastní tzv. LAVA MR sekvence) 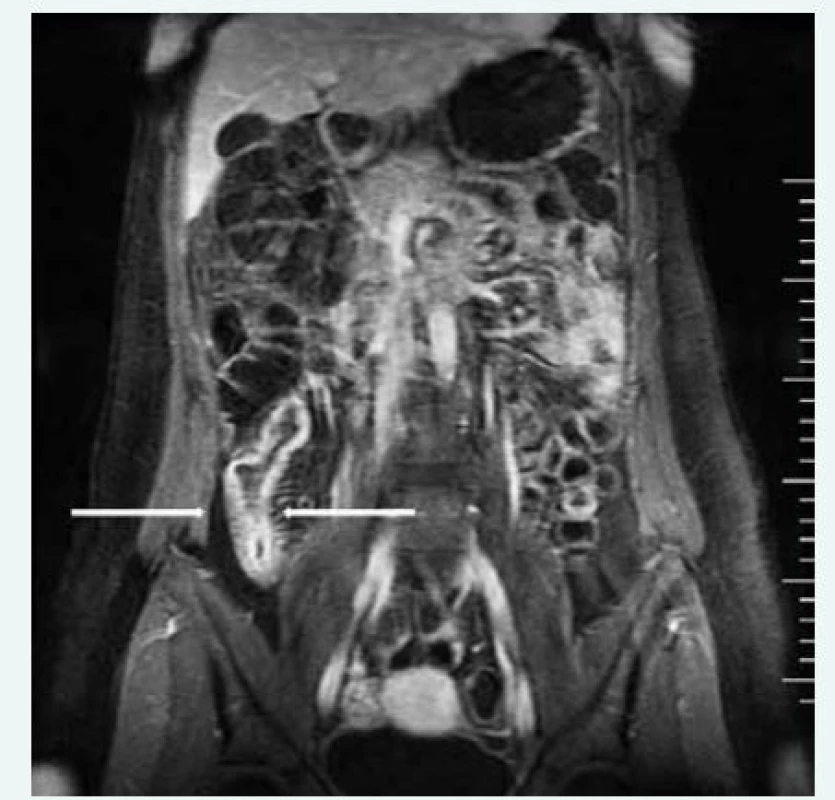
Intestinální atonie je nespecifickým znakem, projeví se jako difuzní dilatace (> 3 cm) tenkého střeva, přičemž není přítomná obstrukce. Nejvíce specifickým znakem pro celiakii jsou změny slizničního reliéfu – snížení počtu klků v jejunu a zvýšený počet klků v ileu, tzv. jejunizace ilea – tento obraz je na MRI specifický [8,9]. Tomei et al [10] dospěli na souboru 31 pacientů k závěru, že MRI má u celiakie specificitu 100 % a senzitivita se pohybovala mezi 79 % pro zvýšení počtu klků v ileu a 75 % pro snížení klků v jejunu.
K extramurálním nálezům patří hyposplenizmus a mezenteriální lymfadenopatie.
Nádory tenkého střeva
Nádory tenkého střeva jsou vzácné a jejich diagnostika je složitá, z toho důvodu chybí velké studie věnující se tématu MRI zobrazování tumorů tenkého střeva (obr. 5). Podle Fidlera et al [6] je MR přinejmenším srovnatelná s kapslovou enterografií.
Obr. 5. GIST-om tenkého střeva (postkontrastní tzv. LAVA MR sekvence) 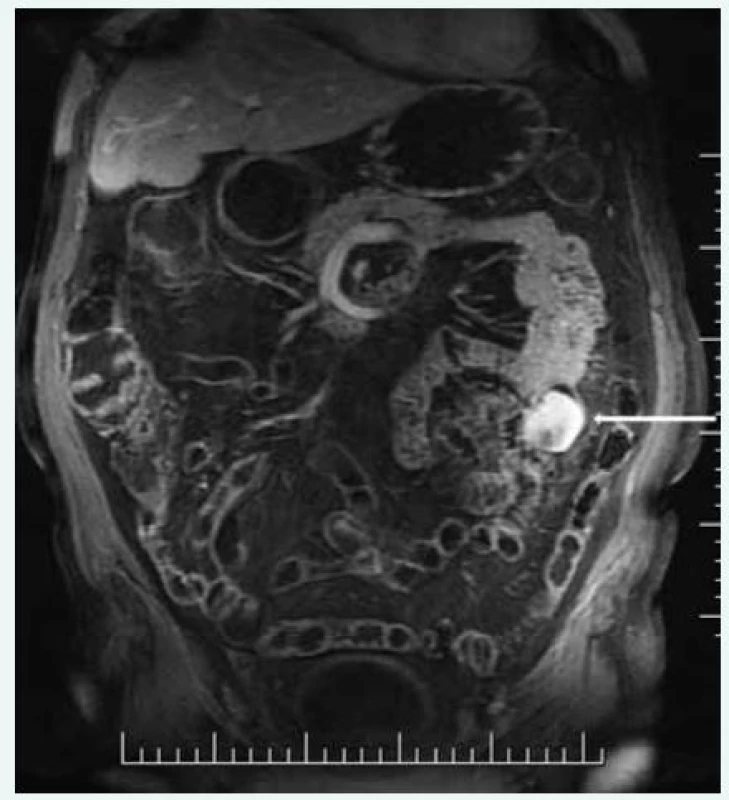
Závěr
MR enterografie těží z obecných benefitů magnetické rezonance – absence ionizujícího záření, multiplanární zobrazení, vynikající tkáňový kontrast.
Jednoduchost MR enterografie při porovnání s klasickou enteroklýzou naznačuje, že by MR měla mít přednost vždy, kdykoliv je to možné. Postupně se i u nás stává zobrazovací modalitou první volby při podezření, ale i při sledování již diagnostikovaných onemocnění tenkého střeva a má do budoucna velký potenciál v zobrazování jiných patologií, zejména v problematice onkologické. Její nejčastější využití by mělo být právě při zobrazování tenkého střeva pacientů s Crohnovou nemocí, u této diagnózy by měla mít MR vždy přednost před CT enterografií, či klasickou enteroklýzou [11]. Co se týče využití MR enterografie u celiakie, jsou výsledky zatím nejednoznačné. Sice dokáže přesně popsat změny na střevě, ale zatím v literatuře neexistuje údaj, resp. porovnání efektivity diagnostiky MR proti enterální biopsii.
Všichni zde citovaní autoři se shodují, že v současné době je MRI nejlepší zobrazovací modalitou pro vyšetřování tenkého střeva a jeho nejčastějších patologií.
Podpořeno European Regional Development Fund – Project FNUSA-ICRC (No. CZ.1.05/1.1.00/02.0123).
as. MUDr. Jiří Vaníček, Ph.D.
jiri.vanicek@fnusa.cz
Klinika zobrazovacích metod LF MU a FN u sv. Anny, Brno
www.fnusa.cz
Doručeno do redakce 10. 10. 2014
Přijato po recenzi 1. 12. 2014
Zdroje
1. Stoker J (ed). MRI of the Gastrointestinal Tract (Medical Radiology/Diagnostic Imaging). Springer-Verlag: Berlin: 2010 : 117–134. ISBN: 9783540855316.
2. Cronin CG, Lohan DG, Browne AM et al. Magnetic Resonance Enterography in the Evaluation of the Small Bowel. Semin Roentgenol 2009; 44(4): 237–243.
3. Laghi A, Paolantonio P, Hassan C. Small Bowel Imaging. Semin Roentgenol 2009; 44(2): 99–110.
4. Laghi A, Paolantonio P, Iafrate F et al. Oral contrast agent for MRI of the bowel. Top Magn Reson Imaging 2002; 13(6): 389–396.
5. Deeab DA, Dick E, Sergot AA et al. Magnetic resonance imaging of the small bowel. Radiography 2011; 17(1): 67–71.
6. Fidler JL, Guimaraes L, Einstein DM MR Imaging of the Small Bowel1. Radiographics 2009; 29(6): 1811–1825.
7. Tomei E, Semelka RC, Braga L et al. Adult celiac disease: What is the role of MRI? J Magn Reson Imaging 2006; 24(3): 625–629.
8. Laghi A, Paolantonio P, Catalano C et al. MR imaging of the small bowel using polyethylene glycol solution as an oral contrast agent in adults and children with celiac disease: Preliminary observations. AJR Am J Roentgenol 2003; 180(1): 191–194.
9. Paolantonio P, Tomei E, Rengo M et al. Adult celiac disease: MRI findings. Abdom Imaging 2007; 32(4): 433–440.
10. Ferda J, Koželuhová J, Kastner J et al: Využití MR enterografie v zobrazení Crohnovy nemoci. Čes Radiol 2006; 60(4): 203–208.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2015 Číslo 2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Zlepšil se osud gravidit žen s pregestačním diabetes mellitus za deset let?
- Význam transkutánneho monitorovania tkanivového kyslíka u pacienta s diabetes mellitus s jeho komplikáciami
- Autoimunitní pankreatitida – diagnostický konsenzus
- Intersticiální plicní procesy a granulomatózy asociované s běžným variabilním imunodeficitem
- Vyšetření tenkého střeva pomocí magnetické rezonance
- Nový lék je výrazně účinnější nežli inhibitory ACE u chronického srdečního selhání
- Spontánní bakteriální peritonitida
- Co jsou a co nám přinášejí biosimilars?
- Inzulinová analoga u pacientů s diabetem a renální dysfunkcí
- Súčasnosť a budúcnosť v manažmente vénových vaskulárnych chorôb
- Akromegalie a medikamentózní léčba
- Raritní případ mnohočetného myelomu: vícečetný solitární plazmocytom kostí bérců a předloktí
- Kalcifikující uremická arteriolopatie – léčba tiosulfátem sodným
- XXXIV. dny mladých internistů
- Empagliflozin – nový zástupce inhibitorů transportéru SGLT2 pro léčbu pacientů s diabetem 2. typu
- Václav Hána. Endokrinologie pro praxi.
- Hana Papežová a kol. Naléhavé stavy v psychiatrii.
- Peter Gavorník. Angiológia 2 pre všeobecných lekárov – Arteriológia.
- Autoimunitní pankreatitida – diagnostický konsenzus – editorial
- Akromegalie a medikamentózní léčba – editorial
- Kalcifikující uremická arteriolopatie – editorial
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Spontánní bakteriální peritonitida
- Vyšetření tenkého střeva pomocí magnetické rezonance
- Empagliflozin – nový zástupce inhibitorů transportéru SGLT2 pro léčbu pacientů s diabetem 2. typu
- Význam transkutánneho monitorovania tkanivového kyslíka u pacienta s diabetes mellitus s jeho komplikáciami
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



