-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Cyklosporín A verzus cyklofosfamid v liečbe detí s nefrotickým syndrómom
Cyclosporin A versus Cyclophosphamide in the Treatment of Nephrotic Syndrome in Children
Background.
The majority of cases of nephrotic syndrome in children is corticosensitive, however in some individuals aggressive cytotoxic therapy is necessary. Cyclosporin A and cyclophosphamide are widely used; however their relative effectiveness in maintaining remission of childhood nephrotic syndrome remains controversial.Methods and Results.
Effectiveness of long-term cytotoxic therapy (mean follow-up 7.4 years) in 63 children (mean age 6.19 ± 4.30 years) with nephrotic syndrome was retrospectively analyzed; 14 patients suffered from corticosensitive, 33 from corticodependent and 16 from corticoresistant nephrotic syndrome. Corticotherapy alone was used in 15 patients (23.8%), cyclophosphamide was added in 27 (42.9%) and cyclosporin A in 38 cases (60.3%), while 17 patients (27%) were on both immunosuppressive agents. 84% children relapsed within 24 months after cessation of cyclosporin A. In 8 corticoresistant nephrotic syndrome patients (61.5 %) from 13 children treated with cyclosporin A no remission occurred, in 5 children (38.5 %) was remission obtained within 10 weeks, however in 4 of them relapsed disease during cyclosporin A therapy. 19 (70.4%) of 27 patients on cyclophosphamide therapy were in remission, in 8 of them (42.1%) even 2 years after cyclophosphamide therapy.Conclusions.
Cyclophosphamide therapy of childhood nephrotic syndrome is more effective in maintaining long-term remission than cyclosporin A treatment.Key words:
childhood idiopathic nephrotic syndrome, corticoresistant nephrotic syndrome, cyclosporin A, cyclophosphamide.
Autoři: Ľ. Podracká 1; A. Böör 2; M. Šašinka 1
Působiště autorů: Klinika detí a dorastu LF UPJŠ, Košice, Slovenská republika 1; Ústav patologickej anatómie LF UPJŠ, Košice, Slovenská republika 2
Vyšlo v časopise: Čas. Lék. čes. 2008; 147: 38-43
Kategorie: Původní práce
Souhrn
Východisko.
Idiopatický nefrotický syndróm patrí k najčastejším chorobám glomerulov v detskom veku. Hoci sa u väčšiny detí dosiahne remisia nefrotického syndrómu podávaním kortikoidov, je u časti chorých nutná liečba cytotoxickými imunosupresívami (cyklosporínom A a cyklofosfamidom). Ktoré z imunosupresív efektívnejšie navodí dlhodobú remisiu nie je jednoznačné.Metody výsledky.
Autori retrospektívne spracovali údaje o liečbe 63 detí (x = 6,19 ± 4,3 roky) s nefrotickým syndrómom; 14 detí malo steroidosenzitívny, 33 steroidodependentný a 16 detí steroidorezistentný nefrotický syndróm, 15 detí bolo na monoterapii kortikoidmi, 27 detí užívalo prednizón a cyklofosfamid, 38 prednizón a cyklosporín A, 17 detí sa liečilo cyklosporínom A a cyklofosfamidom. Osemdesiat štyri percent detí so steroidodependentným nefrotickým syndrómom relabovalo počas 24 mesiacov po vysadení cyklosporínu A. Osem (61,5 %) z 13 detí so steroidorezistentným nefrotickým syndrómom liečených cyklosporínom A nedosiahlo remisiu, 5 pacientov dospelo do remisie v priebehu 10 týždňov, avšak u 4 z nich relaboval nefrotický syndróm počas liečby cyklosporínom A. Devätnásť (70,4 %) z 27 detí liečených cyklofosfamidom bolo v remisii, u 8 (42,1 %) trvala remisia aj po 2 rokoch od skončenia liečby.Závery.
Deti liečené cyklofosfamidom mali signifikantne dlhšie obdobie remisie nefrotického syndrómu po ukončení liečby v porovnaní so skupinou liečenou cyklosporínom A. Cyklofosfamid je efektívnejší pri navodení remisie nefrotického syndrómu ako cyklosporín A.Kľúčové slová:
deti, nefrotický syndróm, steroidorezistentný nefrotický syndróm, liečba kortikoidmi, cyklosporín A, cyklofosfamid.Idiopatický nefrotický syndróm (NS) patrí k najčastejším chorobám glomerulov v detskom veku. Pri histologickom vyšetrení sa u viac ako 90 % chorých nájdu iba malé abnormity glomerulov, ktoré majú dobrú prognózu. Základným pilierom liečby nefrotického syndrómu (NS) sú kortikosteroidy, ktoré navodia klinickú a laboratórnu remisiu u viac ako 90 % pacientov. Jedna tretina chorých má však v ďalšom priebehu časté relapsy a vyžaduje si dlhodobé a opakované podávanie kortikoidov. Podľa odpovedi na iniciálnu liečbu kortikoidmi sa nefrotický syndróm delí na steroidosenzitívny (SSNS), steroidodependentný (SDNS) a steroidorezistentný NS (SRNS).
Z klinického hľadiska predstavujú najväčšiu terapeutickú dilemu pacienti závislí na kortikoidoch a malá skupina chorých rezistentných na prednizón. Hlavné obavy sa týkajú rizika vedľajších účinkov kortikoidov na rastúci organizmus, a to osobitne ich nepriaznivého vplyvu na kostný metabolizmus a telesný rast. Liečebnú alternatívu u týchto chorých detí predstavujú imunosupresíva, z ktorých sa najviac osvedčil cyklofosfamid a cyklosporín A (1).
Cyklofosfamid (CF) je efektívny u časti pacientov, ale pre svoje potenciálne nežiadúce účinky, najmä gonádovú toxicitu, je jeho použitie u chorých v období puberty limitované (2). Nádeje a veľké očakávania sa vkladali do cyklosporínu A (CsA), ktorý sa zaviedol do terapie NS na začiatku 90. rokov minulého storočia (3). Klinické výsledky (2, 4, 5) vychádzajúce z placebom kontrolovaných štúdií (6) zistili, že pacienti so SDNS a SRNS mali priaznivú odpoveď na CsA.
Remisia však trvala len krátko a na jej prolongovanie bola nevyhnutná udržiavacia liečba. Navyše, u väčšiny pacientov sa vyvinula závislosť na cyklosporíne (7, 8), čo viedlo k opodstatneným obavám z rizika cyklosporínovej nefrotoxicity (9, 10). Preto otázka, ako dlho podávať CsA ostáva ešte dodnes nevyriešená.
Súbor pacientov a použité metódy
V retrospektívnej klinickej štúdii sme zhodnotili a porovnali úspešnosť cyklofosfamidu a cyklosporínu z pohľadu trvania remisie nefrotického syndrómu a súčasne sme vypočítali krivku prežívania našich detských pacientov.
Retrospektívne sme spracovali údaje od 63 detí s NS liečených na Klinike detí a dorastu LF UPJŠ v Košiciach a v nefrologickej ambulancii v rokoch 1987 až 2006. Do štúdie sme zaradili 63 detí od 0 do 19 rokov s klinickými a laboratórnymi známkami nefrotického syndrómu.
Sledovali sme:
- prítomnosť remisie počas liečby, resp. počet relapsov v priebehu imunosupresívnej liečby,
- dĺžku pretrvávania remisie po ukončení imunosupresie,
- zjavenie sa relapsu po prerušení liečby a
- v obidvoch skupinách sme porovnali interval do nástupu relapsu po skončení liečby.
Nefrotický syndróm sme definovali podľa kritérií International Study of Kidney Diseases in Children (ISKDC) (11) t.j. prítomnosť proteinúrie nefrotického typu, hypoalbuminémia (sérový albumín < 25g/l) a edémy. Za remisiu sme považovali pokles proteinúrie pod 100 mg/m2/deň.
Steroidodependentný nefrotický syndróm sme definovali ako relaps ochorenia pri znižovaní dávky kortikoidov. Ako steroidorezistentný nefrotický syndróm sme hodnotili stav, keď pacient nedosiahol parciálnu remisiu ani do konca 8. týždňa kortikoterapie (12).
Protokol liečby
Všetci pacienti boli v úvode liečení podľa ISKDC schémy prednizón 2 mg/kg/deň po dobu 4 týždňov s následným znížením dávky na 1 mg ob deň po dobu ďalších 4 týždňov. U chorých so SDNS alebo SRNS sme po vykonaní renálnej biopsie indikovali cyklosporín A alebo cyklofosfamid. Iniciálna dávka CsA bola 6 mg/kg/deň rozdelená do dvoch dávok denne, ktorú sme podávali spolu s kortikosteroidmi až do dosiahnutia kompletnej remisie. Dávku CsA sme upravovali tak, aby sme dosiahli terapeutické koncentrácie lieku v krvi v rozpätí 100–200 ng/ml. Cyklofosfamid sa aplikoval v dávke 2 mg/kg po dobu 8–12 týždňov spolu s kortikoidmi.
Štatistická analýza
Získané údaje sme štatisticky spracovali Mann-Whitneyho, Fisherovým exaktným a Studentovým t testom. Odhad dĺžky remisie po liečbe sme vyhodnotili Kaplan-Meierovou analýzou a štatisticky spracovali log-rank testom. Na štatistickú analýzu získaných údajov sme použili software Arcus Quickstat Biomedical. Za signifikantnú hodnotu sme považovali p < 0,05. Jednotlivé výsledky uvádzame ako aritmetický priemer ± smerodajné odchýlky.
Výsledky
Do súboru sme zaradili 63 detí s nefrotickým syndrómom, 36 chlapcov (57,1 %) a 27 dievčat (42,9 %). Priemerný vek pacientov v čase prvej manifestácie nefrotického syndrómu bol 6,19 ± 4,30 rokov. Priemerná doba sledovania bola 7,4 rokov (rozpätie od 0,5 do 16 rokov).
V tabuľke 1 uvádzame hodnoty celkového cholesterolu, sérového kreatinínu a kvantitatívnej proteinúrie pred nasadením CsA a CF.
Tab. 1. Hodnoty celkového cholesterolu, sérového kreatinínu a kvantitatívnej proteinúrie pred nasadením imunosupresív 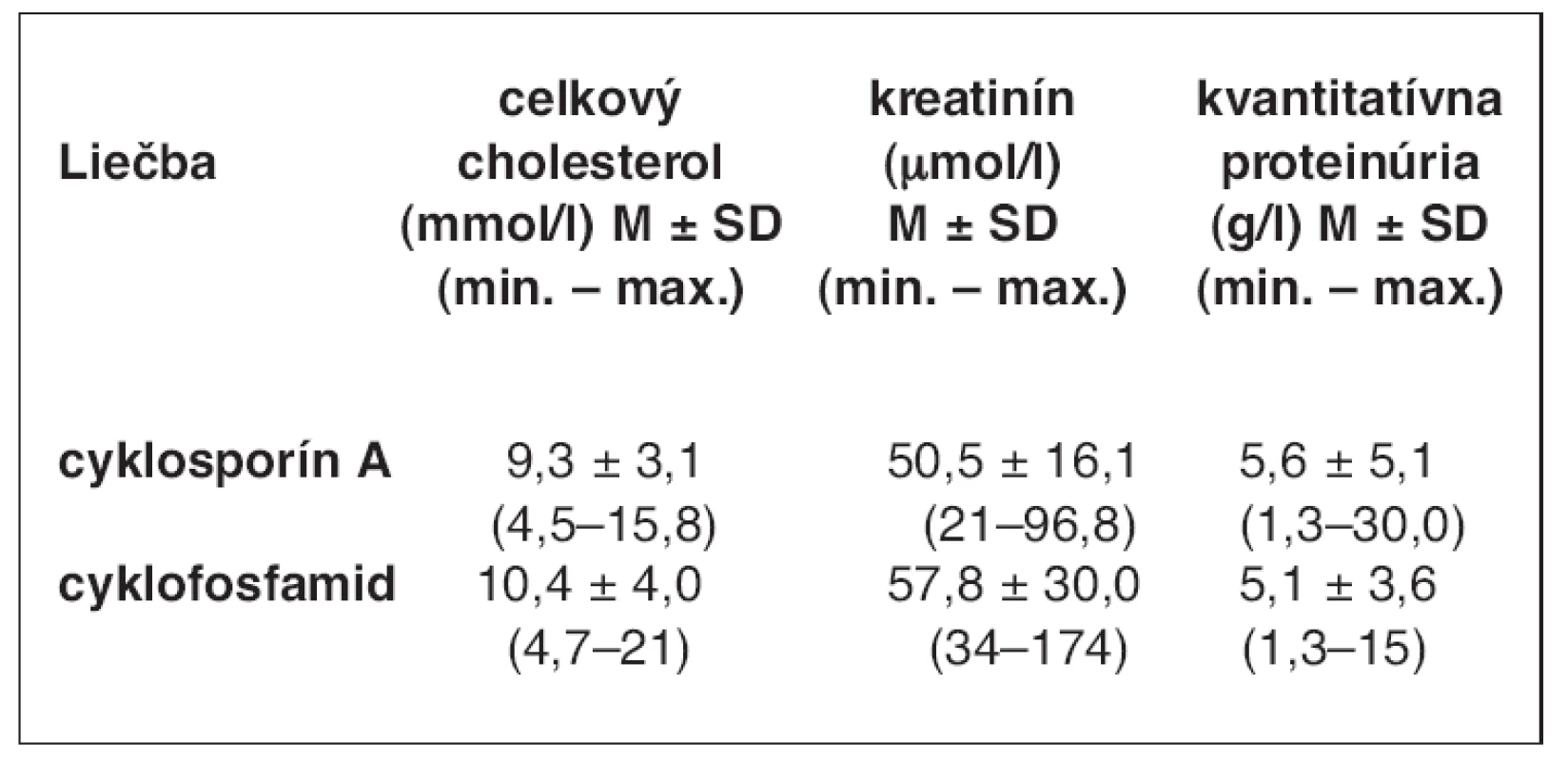
Údaje sú uvádzané vo forme priemer (M) ± SD.
Sedem detí (11,1 %) malo na začiatku ochorenia hypertenziu a 24 detí (38,1 %) hematúriu. Z celkového súboru 63 detí iba 15 chorých bolo na monoterapii kortikoidmi (23,8 %), 27 detí dostávalo kombináciu kortikoidov s cyklofosfamidom (42,9 %) a 38 chorých užívalo kortikoidy a cyklosporín A (60,3 %). U 17 detí sa v liečbe použili obidve imunosupresíva , t.j. CsA aj CF (27 %). U 10 z nich sa podával najprv CsA a potom CF, u 7 detí sa indikoval najprv CF a následne CsA.
Podľa iniciálnej odpovede na kortikoidy malo 14 pacientov steroidosenzitívny nefrotický syndróm (22,2 %), 33 steroidodependentný NS (52,4 %) a 16 detí steroidorezistentný NS (25,4 %).
U 54 detí sme vykonali obličkovú biopsiu. Najčastejší histologický obraz tvorili malé abnormity glomerulov, ktoré sa zistili u 42 detí (78 %), u 6 detí sa zistila fokálne segmentálna glomeruloskleróza (FSGS) (11 %) a u 6 fokálne zmeny (11 %). U 9 pacientov nebola vykonaná biopsia obličky (14,3 %).
Výsledky liečby cyklosporínom A
Cyklosporínom A sa liečilo 38 detí (tab. 2). Dĺžka podávania CsA bola 12 až 32 mesiacov, v priemere 20 mesiacov. CsA sme indikovali u 25 detí so SDNS a u 13 detí so SRNS.
Tab. 2. Liečba nefrotického syndrómu u detí cyklosporínom A 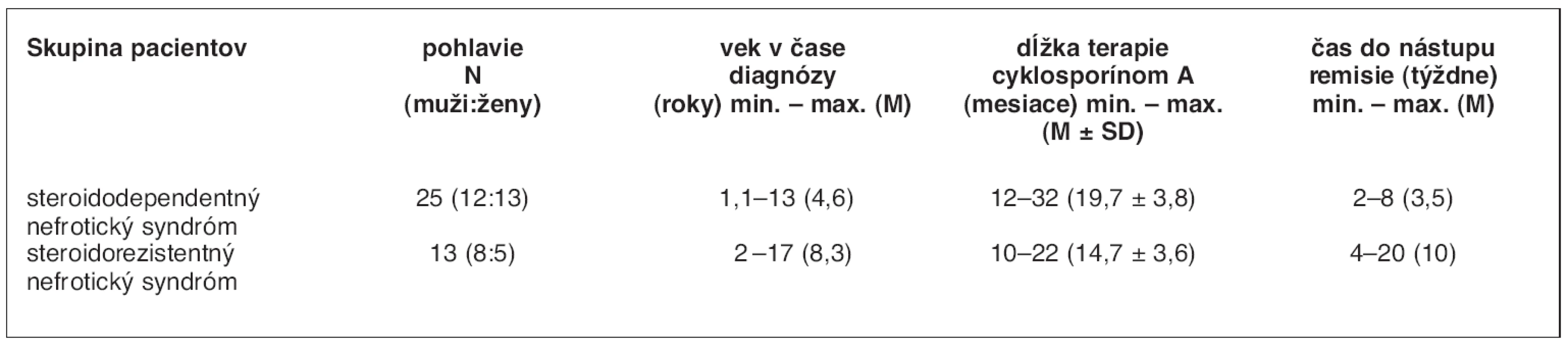
Údaje sú uvádzané vo forme priemer (M) ± SD.
V skupine detí so steroidodependentným NS nastúpila remisia priemerne medzi 3. a 4. týždňom (min. 2, max. 8 týždňov) od začiatku liečby. U 10 z 25 detí liečených CsA nastal relaps NS už počas podávania lieku (40 %). Do dvoch rokov od ukončenia terapie CsA až u 84,2 % pacientov so SDNS sa zopakoval relaps ochorenia.
Z 13 detí so steroidorezistentným NS, ktorí užívali CsA nedosiahlo remisiu počas liečby až 8 pacientov (61,5 %). U 5 detí (38,5 %) nastúpila remisia NS v priemere do 10 týždňov (min. 4, max. 20 týždňov) od začiatku liečby, ale neskôr z nich štyri choré deti zrelabovali už počas podávania CsA. Iba jedno z 5 detí so SRNS zotrvalo v remisii dva roky od vynechania CsA.
Pri sumarizovaní výsledkov všetkých 38 detí liečených CsA vyplynulo, že 8 pacientov nedosiahlo remisiu (21,1 %). U 30 detí nastala remisia počas liečby (78,9 %), avšak 14 z nich (46,7 %) zrelabovalo ešte v priebehu ďalších mesiacoch podávania lieku. Vypočítaná frekvencia relapsov počas liečby CsA bola 0,1/rok/pacient. Zo skupiny 30 pacientov ukončilo terapiu 24 detí, z nich 2 roky zotrvali v remisii 4 pacienti (16,7 %) a 20 detí zrelabovalo v priemere 3,9 mesiaca po ukončení liečby CsA (83,3 %).
Výsledky liečby cyklofosfamidom
Cyklofosfamid sme použili u 27 zo 63 detí. Pätnásť chorých malo SDNS, 11 detí sa liečilo so SRNS a jedno dieťa malo SSNS (tab. 3).
Tab. 3. Liečba nefrotického syndrómu u detí cyklofosfamidom 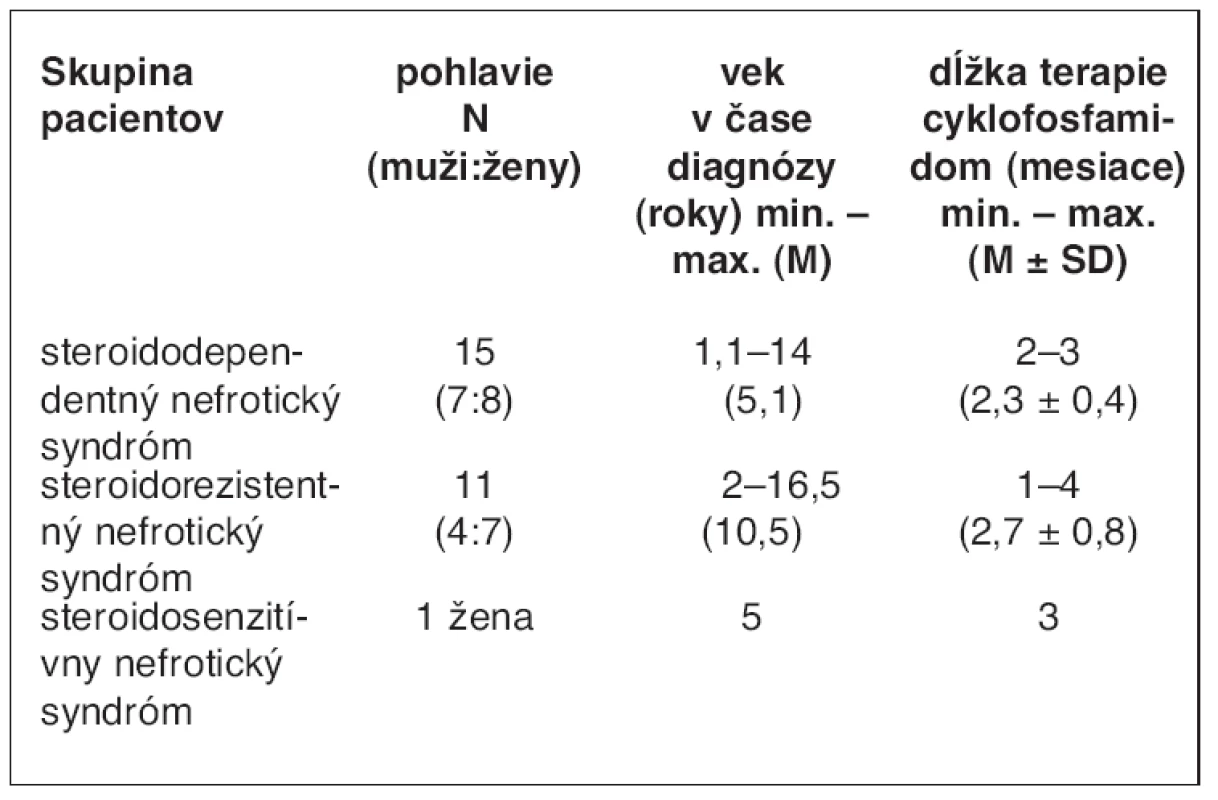
Údaje sú uvádzané vo forme priemer (M) ± SD.
Skupina SDNS. Z 15 pacientov so SDNS iba jeden pacient nedosiahol remisiu počas liečby CF (7,7 %). Priemerná dĺžka terapie bola 9 týždňov (8–12 týždňov). U štyroch zo 14 pacientov trvala remisia dva roky po skončení liečby (28,6 %), 10 chorých zrelabovalo do dvoch rokov od skončenia liečby CF (71,4 %).
Skupina SRNS. Z 11 pacientov so SRNS 7 pacientov nedosiahlo remisiu počas liečby CF (63,6 %), u 4 pacientov indukoval remisiu NS (36,4 %), ktorá trvala u troch chorých ešte dva roky po ukončení liečby CF. Jeden pacient zrelaboval o tri mesiace po vysadení CF. Pacient so SSNS mal trvalú remisiu v priebehu dvoch rokov po ukončení liečby CF.
Spolu sme liečili CF 27 pacientov s NS. Z tohto počtu ôsmi pacienti nedosiahli remisiu počas liečby (29,6 %) a 19 reagovalo na liečbu CF remisiou NS (70,4 %). Z týchto 19 pacientov ôsmi zotrvali v remisii v priebehu dvoch rokov od vynechania CF (42,1 %) a 11 pacientov dostalo relaps do dvoch rokov od skončenia liečby (57,9 %) a to v priemere o 4,9 mesiacov od vysadenia CF.
Porovnanie liečebného efektu cyklofosfamidu a cyklosporínu A
Efekt obidvoch imunosupresív sme porovnávali dva roky od ukončenia terapie pomocou Kaplan-Meierovej analýzy. Zistili sme, že cyklofosfamid indukoval štatististicky významne dlhšiu remisiu ako cyklosporín A (p = 0,023; log-rank test) (tab. 4, obr. 1).
Tab. 4. Porovnanie liečby cyklosporínom A a cyklofosfamidom 
Údaje sú uvádzané vo forme priemer (M) ± SD, Kaplan-Meierova analýza (p = 0,023; log-rank test), (p = 0,17, Fisher exact test).
Dvojročnú remisiu NS po liečbe CF dosiahlo 7 z 19 pacientov (36,8%) resp. po CsA štyria z 24 pacientov (16,7 %). Tento rozdiel však nebol na hladine štatistickej významnosti (p = 0,17, Fisher exact test).
Graf 1. Kaplan-Meierova analýza dĺžky remisie po liečbe cyklosporínom (skupina 1) a cyklofosfamidom (skupina 2) Na x-ovej osi je čas v mesiacoch (p = 0,023) 
Diskusia
Klinické pozorovania ukazujú, že odpoveď na steroidy má väčšiu prediktívnu hodnotu pre priebeh a prognózu nefrotického syndrómu ako histologický obraz. Terapeutickú dilemu predstavujú chorí s častými relapsami a dependentní na kortikoidy, keďže optimálna liečba týchto stavov nie je známa. Vo všeobecnosti sa u nich odporúča dlhodobo podávať prednizón v nízkych dávkach ob deň a pri nedostatočnej odpovedi nasadiť cyklofosfamid alebo chlorambucil. Avšak ani tieto imunosupresíva nedokážu u tretiny chorých navodiť dlhotrvajúcu remisiu a pacienti v ďalšom priebehu opätovne relabujú. Z výsledkov 38 retro/aj prospektívnych štúdií zahrňujúcich až 1573 detí vyplynulo, že rok po ukončení liečby cyklofosfamidom pretrváva remisia u 67–93 % chorých a po 5. rokoch iba u 36–66 % detí (13). Očakávalo sa, že cyklosporín A bude efektívnejšie znižovať frekvenciu relapsov ochorenia a pacienti už nebudú vystavení riziku dlhodobého vplyvu steroidov na rastúci organizmus.
S nadobúdajúcimi klinickými skúsenosťami sa v priebehu nasledujúcich rokov ukázalo, že cyklosporín indukuje remisiu až u 85 % chorých ale značné sklamanie prinieslo zistenie, že u veľkej časti pacientov ostáva problémom krátkotrvajúca remisia a opätovný relaps ochorenia po prerušení liečby (14, 15). V randomizovanej kontrolnej štúdii porovnávajúcej efekt chlorambucilu a CsA sa zistilo, že iba 20 % pacientov liečených CsA bolo v remisii 16 mesiacov po vynechaní liečby, kým v chlorambucilovom ramene malo šesť z 20 detí dlhotrvajúcu remisiu 27 až 49 mesiacov (16). Aj v našej retrospektívnej štúdií zahrňujúcej 63 detí s NS sme dosiahli signifikantne dlhšiu remisiu po CF ako po CsA (Kaplan-Meierova analýza, p = 0,023; log-rank test). Nenašli sme signifikantné rozdiely v indukcii remisie u detí liečených CsA (78,9 %) a CF (70,4 %; p = 0,38), ale dva roky po ukončení imunosupresie bolo v remisii štatisticky viac pacientov zo skupiny liečenej CF ako po CsA. Remisia po CsA nastúpila v priemere medzi 3. a 4. týždňom (min. 2, max. 8 týždňov) od začatia terapie, ale u desať z 25 detí sa zjavil nový relaps už v priebehu podávania lieku (46,7 %), čo predstavuje frekvenciu relapsov 0,1/rok/pacient. Ešte častejší výskyt relapsov 0,4/rok/pacient pozorovali japonskí autori v súbore 17 detí (7). Pri sledovaní dlhodobého efektu CsA u našich chorých sme zistili, že do dvoch rokov po vynechaní cyklosporínu sa až u 84,2 % pacientov zopakoval relaps ochorenia, čo je porovnateľné s výsledkami Satoshiho et al. (17), ktorí pozorovali relaps u 21 z 24 pacientov so SDNS (87,5 %).
Vychádzajúc z analýzy našich dlhoročných výsledkov považujeme za najdôležitejšie zistenie fakt, že relapsy sa vyskytovali signifikantne častejšie u chorých liečených CsA ako CF (84,2 % vs. 57,9 %, p < 0,05 ). S týmto pozorovaním korešpondovala aj dĺžka intervalu do vzniku prvého relapsu, ktorá bola kratšia po CsA (3,9 mesiacov) ako po CF (4,9 mesiacov). Inými slovami, remisia po cyklofosfamide pretrvávala dlhšie ako po cyklosporíne A. Naše výsledky sú v súlade so závermi početných klinických štúdií a evidence-based-medicine (EBM) odporúčaní, podľa ktorých sú liekom prvej voľby pri často relabujúcom alebo steroidodependetnom NS alkylujúce látky, lebo účinnejšie indukujú dlhotrvajúcu remisiu ochorenia ako CsA (27). CsA je druhým krokom liečby a treba ho indikovať až potom, ak nastúpi relaps po cytotoxických imunosupresívach (18, 26).
Detský nefrológ čelí ťažkému a zložitému terapeutickému rozhodnutiu pri liečbe detí so steroidorezistentným nefrotickým syndrómom. Kortikosteroidy majú závažné vedľajšie účinky a nie sú efektívne, no na druhej strane chýbajú údaje, ktoré by jasne dokazovali benefit alkylujúcich liekov (28). Parciálnu či kompletnú remisiu po CF dosiahne iba 20 % chorých, čo je takmer rovnaké percento ako efekt samotného prednizónu (19, 20). Údaje o agresívnejšej liečbe sú iba anekdotálne a vychádzajú zo skúsenosti získaných na malom počte detí (21, 25).
V našom súbore sme cyklofosfamidom liečili 5 pacientov s FSGS a 6 pacientov so SRNS. Sedem z 11 pacientov nedosiahlo remisiu počas liečby (63,6 %), 4 dospeli do remisie, z nich u 3 pretrvávala remisia aj dva roky po ukončení liečby. Podobne aj v ISKDC štúdií sa ukázalo, že CF v kombinovanej liečbe s prednizónom nepriniesol u chorých s FSGS a SRNS očakávaný efekt (11).
Najčastejšie používanú alternatívu u detí so SRNS predstavuje cyklosporín A, hoci jeho úspešnosť ostáva stále kontroverzná. Osem nekontrolovaných štúdií zahŕňajúcich 60 detí so SRNS uvádza kompletnú remisiu u 12 detí (20 %) (22). Výskyt remisií bol signifikantne vyšší, keď sa CsA kombinoval so steroidmi. Lieberman a Tejani (23) vykonali u 24 detí s FSGS dvojito-slepú, placebom kontrolovanú štúdiu, v ktorej podávali CsA. Kompletnú remisiu dosiahla tretina detí. Naše výsledky sú s týmito prácami porovnateľné, kompletnú remisiu sme pozorovali u 5 z 13 pacientov so SRNS liečených CsA (38,5 %), u 5 detí (38,5 %) nastúpila remisia NS v priemere do 10. týždňov (min. 4, max. 20 týždňov) od začiatku liečby, ale neskôr z nich 4 chorí zrelabovali už počas podávania CsA. Iba jedno z 5 detí so SRNS zotrvalo v remisii dva roky od vynechania CsA. Remisiu počas terapie nedosiahlo až 8 pacientov (61,5 %).
Z údajov porovnávacích klinických štúdií vyplynulo, že vznik chronickej renálnej insuficiencie u detí so SRNS je nižší po cyklosporíne ako po cyklofosfamide (24 % resp. 78 %). Podľa EBM sa preto u všetkých detí so steroidorezistentným NS na podklade minimálnych zmien alebo FSGS s normálnou glomerulovou filtráciou odporúča nasadiť CsA a prednizón (24). Cyklofosfamid je indikovaný v prípadoch, keď je prítomná renálna insuficiencia alebo u chorých nereagujúcich na CsA.
Záver
Na základe výsledkov našej retrospektívnej klinickej štúdie môžeme zhrnúť, že cyklofosfamid pri SDNS navodí dlhšiu remisiu ako cyklosporín A.
Efekt imunosupresív pri SRNS je značne limitovaný. Cyklofosfamid je účinný len u malej časti chorých, prechodné zlepšenie a parciálnu remisiu možno dosiahnuť cycklosporínom A. Rozhodnutie o dlhodobej liečbe detských pacientov z časti komplikuje progresívny priebeh NS s postupnou deterioráciou renálnych funkcií. Preto sa odporúča, aby tieto deti boli dispenzarizované v terciálnych nefrologických centrách, ktoré majú dostatočné klinické skúsenosti s imunosupresívnou terapiou a dlhoročným pozorovaním farmakorezistených pacientov.
Skratky
CF – cyklofosfamid
CsA – cyklosporín A
EBM – evidence – based – medicine
FSGS – fokálne segmentálna glomeruloskleróza
INS – idiopatický nefrotický syndróm
ISKDC – International Study of Kidney Diseases in Children
MCD – minimal change disease
NS – nefrotický syndróm
SDNS – steroidodependentný nefrotický syndróm
SRNS – steroidorezistentný nefrotický syndróm
SSNS – steroidosenzitívny nefrotický syndróm
Zdroje
1. Eddy, A. A., Symons, J. M: Nephrotic syndrome in childhood. Lancet, 2003, 362, s. 629–639.
2. Collaborative Study Group of Sandimmune in nephrotic syndrome: Safety and tolerability of cyclosporin A (Sandimmune) in idiopathic nephrotic syndrome. Clin. Nephrol., 1991, 35, s. 48–60.
3. Hladík, M.: Léčba nefrotického syndromu cyklosporinem A u dětí. In: Buchanec, J. et al.: Vybrané kapitoly z pediatrie V., JLF UK Martin, 1998, s. 50–52.
4. Tejani, A., Butt, K., Trachtman, H. et al.: Cyclosporin–induced remission of relapsing nephrotic syndrome in children. J. Pediatr., 1987, 111, s. 1056–1062.
5. Ponticelli, C., Edefonti, A., Rizzoni, G. et al.: Cyclosporin versus cyclophosphamide for patients with steroid–dependent and frequently relapsing idiopathic nephrotic syndrome: A multicentre randomized controlled trial. Nephrol. Dial. Transplant., 1993, 8, s. 1326–1332.
6. Tohjoh, S., Narita, M., Koyama, T.: Clinical evaluation of cyclosporin in the treatment of nephrotic syndrome: Multicenter double blind study. Jin To Tohseki, 1994, 37, s. 565–608.
7. Kitano, Y., Yoshikawa, N., Tanaka, R. et al.: Cyclosporin treatment in children with steroid-dependent nephrotic syndrome. Pediatr. Nephrol., 1990, 4, s. 474–477.
8. Meyrier, A.: Use of cyclosporin in the treatment of idiopathic nephrotic syndrome in adults. Contrib. Nephrol., 1995, 114, s. 28–48.
9. Feutren, G., Mihatsch, M.: Risk factors for cyclosporine–induced nephrotoxicity in patients with autoimmune diseases. N. Engl. J. Med., 1992, 326, s. 1654–1660.
10. Myers, B. D.: Cyclosporin nephrotoxicity. Kidney Int., 1986, 30, s. 964–974.
11. International Study of Kidney Disease in Children (ISKDC): Primary nephrotic syndrome in children: Clinical significance of histopathologic variants of minimal change and of diffuse mesangial hypercellularity. Kidney Int., 1981, 20, s. 765–771.
12. Ronald, J. H., Ronald, J. P., Dawn, M. et al.: Evaluation and Management of Proteinuria and Nephrotic Syndrome in Children: Recommendations From a Pediatric Nephrology Panel Established at the National Kidney Foundation Conference on Proteinuria, Albuminuria, Risk, Assessment, Detection, and Elimination (PARADE). Pediatrics, 2000, 105, s. 1242–1251.
13. Cameron, J. S., Chantler, C., Ogg, C. S. et al.: Long-term stability of remission in nephrotic syndrome after treatment with cyclophosphamide. Br. Med. J., 1974, 4, s. 7–11.
14. Niaudet, P., Broyer, M., Habib, R.: Treatment of idiopathic nephrotic syndrome with cyclosporin A in children. Clin. Nephrol., 1991, 35, s. 31–36.
15. Tanaka, R., Yoshikawa, N., Kitano, Y. et al.: Long-term cyclosporin treatment in children with steroid-dependent nephrotic syndrome. Pediatr. Nephrol., 1993, 7, s. 249–252.
16. Niaudet, P.: Comparison of cyclosporine and chlorambucil in the treatment of idiopathic nephrotic syndrome: A multicenter randomized controlled trial. The French Society of Pediatric Nephrology. Pediatr. Nephrol., 1992, 6, s. 1–3.
17. Satoshi, H., Tsukasa, T., Mitsuru, O. et al.: Follow-Up Study of Children With Nephrotic Syndrome Treated With a Long-Term Moderate Dose of Cyclosporine. Am. J. Kidney Dis., 1998, 31, s. 932–939.
18. Filler, G.: Treatment of nephrotic syndrome in children and controlled trials. Nephrol. Dial. Transplant., 2003, 18, 6, s. 75–78.
19. Tarshih, P., Tobin, J. N., Bernstein, J. et al.: Cyclophosphamide does not benefit patients with focal segmental glomerulosclerosis. Pediatr. Nephrol., 1996, 10, s. 590–593.
20. Geary, D. F., Farine, M., Thorner, P. et al.: Response to cyclophosphamide in steroid resistant focal segmental glomerulosclerosis. Clin. Nephrol., 1984, 22, s. 109.
21. Hladík, M.: Nefrotický syndrom u dětí. In: Buchanec, J. et al.: Vybrané kapitoly z pediatrie V., JLF UK Martin, 1999, s. 68–70.
22. Niaudet, P., Habib, R.: Cyclosporine in the treatment of idiopathic nephrosis. J. Am. Soc. Nephrol., 1994, 5, s. 1049–1056.
23. Lieberman, K. V., Tejani, A.: A randomized double–blind placebo–controlled trial of cyclosporine in steroid resistant idiopathic focal segmental glomerulosclerosis in children. J. Am. Soc. Nephrol., 1996, 7, s. 56–63.
24. Durkan, A. M., Hodson, E. M., Willis, N. S. et al.: Immunosuppressive agents in childhood nephrotic syndrome: A meta-analysis of randomized controlled trials. Kidney Int., 2001, 59, s. 1919–1927.
25. Pena, A., Bravo, J., Melgosa,M. et al.: Steroid-resistant nephrotic syndrome: long - term evolution after sequential therapy. Pediatr. Nephrol., 2007, 22, s. 1875–1880.
26. El-Husseini, A., El-Basuony, F., Mahmoud, I. et al.: Long-term effects of cyclosporine in children with idiopathic nephrotic syndrome: a single-centre experience. Nephrology Dialysis Transplantation, 2005, 20, s. 2433–2438.
27. Kyrieleis, H. A., Levtchenko, E. N., Wetzels, J. F.: Long-term outcome after cyclophosphamide treatment in children with steroid-dependent and frequently relapsing minimal change nephrotic syndrome. Am. J. Kidney Dis., 2007, 49, s. 592–597.
28. Reusz, G., Szabo, A., Telete, A.: Nephrotic syndrome in childhood. Orv Hetil, 2006, 147, s. 2251–2260.
Štítky
Adiktológia Alergológia a imunológia Angiológia Audiológia a foniatria Biochémia Dermatológia Detská gastroenterológia Detská chirurgia Detská kardiológia Detská neurológia Detská otorinolaryngológia Detská psychiatria Detská reumatológia Diabetológia Farmácia Chirurgia cievna Algeziológia Dentální hygienistka
Článok vyšiel v časopiseČasopis lékařů českých
Najčítanejšie tento týždeň
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Subkutánne vs. intravenózne imunoglobulíny u pacientov s CLL
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Facilitovaná subkutánna imunoglobulínová terapia u seniorov s imunodeficienciami v reálnej praxi
-
Všetky články tohto čísla
- Zima, T. et al.: Laboratorní diagnostika
- Esenciálna hypertenzia ako syndróm alebo kompenzačný mechanizmus?
- Krajíček, M., Peregrin, J. H., Roček, M. et al.: Chirurgická a intervenční léčba cévních onemocnění
- Zapojení mikroRNA do patogeneze nádorových onemocnění a možnosti jejich využití v diagnostické a prediktivní onkologii
- Předoperační příprava a vyšetření pacienta před plánovaným kardiochirurgickým výkonem
- Blok TXA2 v léčení svědivé dermatózy
- Neuropeptidové léčení pruritu (komentář)
- Vliv nízkokalorické diety na sérové koncentrace a expresi cytoadhezivních molekul v tukové tkáni u obézních žen
- Weiss, P. et al.: Sexuální zneužívání dětí
- Cyklosporín A verzus cyklofosfamid v liečbe detí s nefrotickým syndrómom
- Rudolf, G., Henningsen, P.: Psychotherapeutische Medizin und Psychosomatik
- Psychomotorické tempo a rychlost vyhledávání v sémantické paměti
- Fotodynamická terapie i viditelným světlem
- Migrační tendence u českých lékařů
- Politická korektnost a myšlení lékařů
- Historicko-medicínská výročí v roce 2008
- Celostátní sjezd Společnosti lékařské genetiky ČLS JEP a 40. výroční cytogenetická konference
- Obezitologie 200714. výroční kongres České obezitologické společnosti ČLS JEP
- Bohemica non legantur
- JIŽ POTŘETÍ BYLA UDĚLENA Cena časopisu lékařů českých
- K pětadevadesátinám farmakologické legendy prof. MUDr. Dr.h.c. Heleny Raškové, DrSc. (*2. ledna 1913)
- Prof. MUDr. Vladimír Bencko, DrSc. JUBILUJÍCÍ
- Výpověď biochemických markerů remodelace kosti při nádorovém postižení skeletu
- Laureáti Nobelovy ceny
- Časopis lékařů českých
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Esenciálna hypertenzia ako syndróm alebo kompenzačný mechanizmus?
- Předoperační příprava a vyšetření pacienta před plánovaným kardiochirurgickým výkonem
- Psychomotorické tempo a rychlost vyhledávání v sémantické paměti
- Zima, T. et al.: Laboratorní diagnostika
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



