-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Postavení farmakoterapie v současné péči o obézní
Status of pharmacotherapy in current care of obese
Weight loss drugs or anti-obesity drugs have a long history but are still far from being successful. Only in two last decades have the drugs been launched, which, when appropriately indicated, may be significantly beneficial to patients in need of weight loss as they are comparably effective to intensive programs to promote changes in eating habits and lifestyles. The combination naltrexone/bupropion is promising for food intake control including the reward mechanism, but the experience with its use has only been short-term. The lipase inhibitor orlistat remains the safest therapeutic option. The already restricted use of phentermine, newly classified as a controlled opiate substance, has become practically blocked. The range of weight loss drugs can be extended with some antidiabetics, particularly liraglutide and gliflozins. A number of other substances is still in the research stage.
Keywords:
obesity, overweight, pharmacotherapy, naltrexone, bupropion, reward system
Autoři: Petr Sucharda
Působiště autorů: 3. interní klinika 1. LF UK a VFN v Praze
Vyšlo v časopise: Čas. Lék. čes. 2017; 156: 319-322
Kategorie: Přehledové články
Souhrn
Léky podporující snižování nadměrné tělesné hmotnosti (antiobezitika) mají dlouhou, ale dosud málo úspěšnou historii. Až v posledních dvou desetiletích byly na trh uvedeny léčivé přípravky, které – správně indikované – mohou nemocným významně pomoci v úsilí o redukci nadměrné tělesné hmotnosti, neboť jejich účinnost je srovnatelná s intenzivními programy změn stravovacích návyků a životního stylu.
Kombinace naltrexon/bupropion slibuje komplexní ovlivnění příjmu potravy včetně reward mechanismu, zkušenosti s ním jsou však zatím krátké. Nejbezpečnějším lékem zůstává blokátor lipáz orlistat. Již tak omezené užívání fenterminu bylo převedením do „opiátového“ režimu prakticky zablokováno. Spektrum antiobezitik mohou rozšířit některá antidiabetika, zejména liraglutid a glifloziny. Řada dalších látek je dosud ve fázi výzkumu.Klíčová slova:
obezita, nadváha, farmakoterapie, naltrexon, bupropion, systém odměnÚVOD
Zmnožování zásobního tělesného tuku je důsledkem pozitivní energetické bilance. To se nemusí rovnat – a nepochybně se v mnoha případech také nerovná – nadměrnému příjmu energie (jedním z mnoha problémů etiologie obezity je ovšem neexistence nějakých norem či limitů pro energetický metabolismus). Naopak podmínkou zmenšování tukových zásob je větší spotřeba energie než její příjem.
„Antiobezitika“ – jakkoli to název naznačuje – nejsou léky, které by přímo měnily ukládání a uvolňování tělesného tuku, ale jedná se „pouze“ o látky přispívající k ovlivnění vztahu mezi příjmem a výdejem energie. Na termínu antiobezitika je navíc zavádějící skutečnost, že jejich indikace nikdy nebyly, nejsou a ani nebudou omezeny na obezitu, definovanou hodnotou BMI ≥ 30. Naopak, v souhrnech údajů o léčivých přípravcích (SPC) jsou často uváděny i nižší hodnoty BMI v případech, kdy pacient má diagnostikovánu některou z chorob provázejících nadměrné ukládání tělesného tuku. To odpovídá probíhající změně paradigmatu, přesunu důrazu od množství tělesného tuku k chorobám tímto hromaděním vyvolaným, tedy k „obezitě“ jakožto progresivnímu chorobnému procesu (1).
První pokusy léčit obezitu medikamentózně spadají do konce 19. století, kdy byly (neúspěšně) zkoušeny výtažky ze štítné žlázy (2). Hledání léčivých přípravků, které by příznivě ovlivnily nadměrnou kumulaci tělesného tuku, znovu začíná v první polovině 50. let 20. století – možná trochu překvapivě ve stejné době jako první pokusy ovlivnit obezitu chirurgicky. Amfetamin a další budivé aminy však představovaly slepou uličku, kterých bohužel na cestě k moderním antiobezitikům bylo ještě hodně.
Mazindol, jeden z prvních alespoň krátkodobě účinných léků, byl pro své nežádoucí vedlejší účinky stažený, podobně jako později dexfenfluramin, trochu nevinná oběť hromadného a mnohdy neuváženého předepisování kombinace fenfluraminu s fenterminem, což vedlo k serotoninovému syndromu a plicní hypertenzi. Samotný fentermin byl ve většině evropských států vyřazen z registrace; v Česku, kde v posledních letech představoval jediné centrálně působící antiobezitikum, byl v květnu 2017 převeden do tzv. opiátového režimu (předpis na recept s modrým pruhem), což v praxi zřejmě způsobí definitivní ukončení jeho preskripce. Z trhu byl před několika lety stažen i sibutramin, téměř 15 let považovaný za lék nejen účinný, ale i bezpečný, a tedy hojně předepisovaný. Výsledky studie SCOUT však nejen nesplnily očekávání, že bude sibutramin možno předepisovat i nejohroženějším skupinám, zvláště kardiakům, ale vedly – s jistými rozpaky – k opuštění tohoto blokátoru zpětného vychytávání dopaminu a serotoninu (3).
V současné dekádě se na trh v USA (a se zpožděním a omezením i v Evropské unii) dostává několik buď zcela nových účinných látek, nebo kombinace léčivých látek již dříve používaných, jejichž bezpečnost byla ověřena i s ohledem na zkušenosti s výše zmíněnými přípravky. Navíc je zřejmé, že pro léčbu budou postupně uvolňovány další léky původně vyvinuté pro léčbu jiných onemocnění, zejména diabetu.
Jak již bylo řečeno, nelze dosáhnout poklesu množství tukové tkáně, aniž by bylo dosaženo negativní energetické bilance. Tomu lze medikamentózně napomoci několika způsoby, jak uvádí tab. 1. Z praktického hlediska je lepší se přidržet kritéria dostupnosti.
Tab. 1. Možnosti medikamentózního dosažení negativní energetické bilance 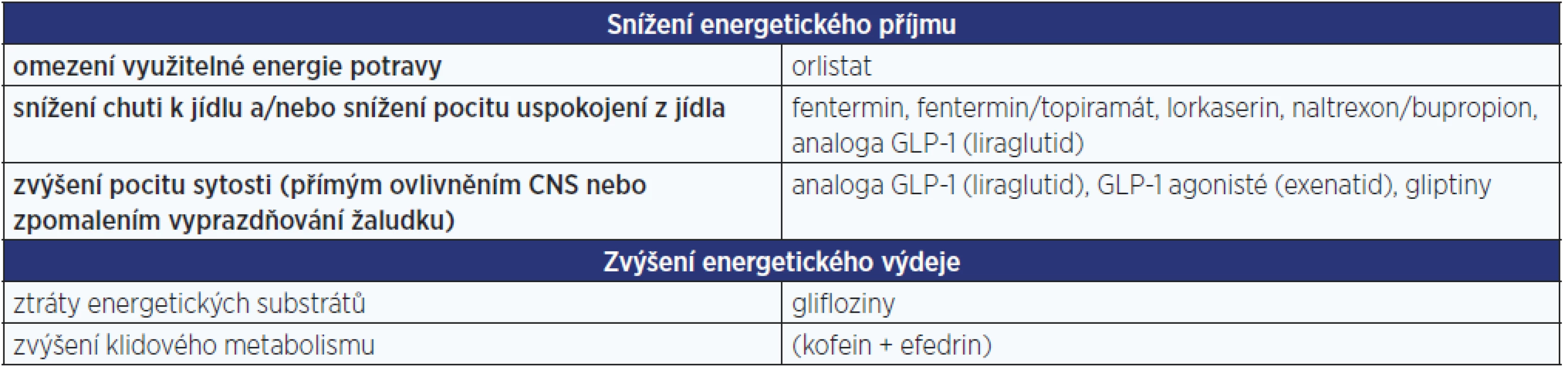
LÉČIVÉ PŘÍPRAVKY DOSTUPNÉ V ČR
Orlistat
Orlistat (Orlistat Sandoz 60/120 mg cps., Orlistat Teva 60 mg cps.; Xenical® Roche 120 mg cps., Alli® Glaxo 27/60 mg; 120mg kapsle jsou vázány na lékařský recept) je blokátor střevních lipáz, který snižuje energetický příjem omezením vstřebávání triacylglycerolů; užívá se přímo s jídlem obsahujícím (pochopitelně v omezeném množství) tuk. Zablokuje přeměnu asi 1/3 molekul triacylglycerolů v dané porci na monoacylglyceroly; při optimálním použití sníží energetický příjem asi o 500–600 kJ (4).
Vzhledem k tomu, že účinná látka se nevstřebává, se jedná o lék principiálně bezpečný a bez závažnějších vedlejších účinků (5). Častější vyprazdňování, olejovité stolice a zcela vzácně inkontinence, vyplývající z přítomnosti triacylglycerolů v tračníku, mají individuální výskyt i závažnost, závisejí na dávce (60 nebo 120 mg) a zejména na délce podávání (nejčastější jsou na začátku podávání). Omezené vstřebávání vitaminů rozpustných v tucích je spíše teoretické a lze mu zabránit doporučeným podáváním multivitaminového přípravku; kontraindikací je současné podávání s antiepileptiky (valproát, lamotrigin) a cyklosporinem (6). Z vysoce lipofilních léků bylo snížené vstřebávání prokázáno pouze u amiodaronu (7). Uváděnému možnému snížení absorpce levothyroxinu lze snadno předejít, pokud pacient užívá levothyroxin standardním způsobem, tedy samostatně a nejméně půl hodiny před jídlem. Opatrnosti je třeba při současném podávání warfarinu (kvůli omezenému vstřebávání vitaminu K) (8).
Fentermin
Fentermin (Adipex ret.® Gerot 15 mg cps., pouze na předpis s modrým pruhem) je klasické anorektikum, nepřímé sympatomimetikum v CNS, které potlačuje chuť k jídlu a zvyšuje lipolýzu. Má řadu kontraindikací (glaukom, plicní hypertenze, nekorigovaná arteriální hypertenze, adenom prostaty, anorexie, deprese aj.) a podle SPC by trvání léčby nemělo překročit 3 měsíce, s možným opakováním až po stejně dlouhé pauze. Je však sporné, zda se toto omezení opírá o vědecky získané důkazy – již v jedné z prvních studií bezpečnosti nebyly při 18týdenním podávání zjištěny ani tolerance, ani podezření na závislost (9). Účinek fenterminu je zvyšován alkoholem a kofeinem.
Naltrexon SR/bupropion SR
V létě roku 2016 bylo v Česku registrováno nové kombinované centrálně působící antiobezitikum naltrexon SR/bupropion SR (Mysimba® Orexigen, 8/90 mg tbl., na lékařský předpis). Přípravek obsahuje dvě účinné látky, obě s pomalým uvolňováním: antagonistu opioidních receptorů naltrexon a inhibitor zpětného vychytávání noradrenalinu a dopaminu bupropion. Obě tyto účinné látky se již delší dobu používají, naltrexon jako součást komplexní terapie při odvykání závislosti na opioidech a alkoholu, bupropion v terapii depresivních onemocnění a jako podpůrný lék při odvykání kouření (i když v současnosti to není mezi indikacemi ani jednoho z dostupných léčivých přípravků).
Obě složky snižují chuť k jídlu ovlivněním hypotalamické proopiomelanokortinové (POMC) anorexigenní osy. Bupropion jakožto inhibitor zpětného vychytávání dopaminu a noradrenalinu tuto osu aktivuje, naltrexon potlačuje inhibiční působení beta-endorfinu na POMC a současně ovlivňuje systém odměn (reward) v CNS a tím snižuje uspokojení z jídla. Naltrexon také působí proti návyku na chuťově atraktivní potraviny a potlačuje nezvládnutelné nutkání jíst (craving) (10).
Léčba se zahajuje podáváním 1 tablety denně, při toleranci se zvyšuje po týdnu na 2, 3 až maximálně 4 tablety denně. Podávání je indikované v kombinaci se stravou se sníženou energetickou hodnotou a zvýšenou fyzickou aktivitou (pokud lze) u pacientů starších 18 let s počátečním indexem tělesné hmotnosti (BMI) 30 kg/m2 a více (obezita) nebo mezi 27 a 30 kg/m2 (nadváha) za přítomnosti jedné nebo více přidružených chorob souvisejících s hmotností (např. diabetes 2. typu, dyslipidemie nebo kontrolovaná hypertenze). Léčba musí být přerušena po 16 týdnech, pokud pacient nesnížil svoji tělesnou hmotnost alespoň o 5 % – toto omezení vychází z dat 4 randomizovaných, placebem kontrolovaných studií (2043 pacientů, kteří dokončili 56 týdnů léčby). Úbytek hmotnosti alespoň o 5 % v 16. týdnu indikoval pokles hmotnosti po 56 týdnech o 11,7 %, udržení minimálně 5% poklesu v 56. týdnu u 85 % pacientů a správný odhad alespoň 5% poklesu v 56. týdnu u 80 % pacientů (11).
Účinnost a bezpečnost kombinace naltrexonu a bupropionu byla ověřována experimentálními, preklinickými i klinickými studiemi. Byl potvrzen výrazný aditivní účinek kombinace na elektrofyziologickou aktivitu anorexigenních POMC neuronů v oblasti nucleus arcuatus hypotalamu myší i na snížení příjmu potravy obézních myší. Aditivní efekt byl prokázán i v multicentrické randomizované dvojitě zaslepené a placebem kontrolované studii. Průměrný pokles hmotnosti v intervenované skupině byl po 56 týdnech 8,1 % vstupní hmotnosti (8,0 kg), zatímco v placebové skupině pouze 1,8 % (12). V obdobné studii zhubli diabetici 2. typu 5,9 % vstupní hmotnosti, kdežto v kontrolní skupině 2,2 % (13).
V klinické jednoroční (56 týdnů trvající) studii byly účinné látky nebo placebo podávány téměř 1500 obézních pacientů. Za 28 týdnů snížilo hmotnost o 5 a více procent 55 % intervenovaných (při placebu 17,5 %) a z těch, co studii dokončili, zhublo alespoň desetinu hmotnosti 39 % intervenovaných (8 % při placebu); téměř jedna pětina zhubla o více než 15 % hmotnosti (14).
Nejčastějšími nežádoucími účinky v této studii i dalších sledováních byly nauzea, bolest hlavy, závratě a zvracení. Nežádoucími účinky vedoucími k přerušení léčby byly nejčastěji nauzea, bolest hlavy, závratě a zvracení a velmi často úzkost, nespavost, neklid, bolest břicha, artralgie, myalgie. Studie, kterou provedli Hong et al., prokázala, že nauzea ustupovala velmi rychle, během prvních 4 týdnů, a že pokles hmotnosti byl stejný u pacientů s nauzeou i bez ní, a to jak v intervenované, tak také kontrolní skupině (15).
LÉČIVÉ PŘÍPRAVKY NEDOSTUPNÉ V ČR
Fentermin ER/topiramát ER
Předpokládaným mechanismem účinku kombinace fentermin ER/topiramát ER (QsymiaTM, 3,75/23 mg tbl.) je potlačení chuti k jídlu zvýšeným uvolňováním noradrenalinu, indukcí vyšších koncentrací leptinu (fentermin) a navozením časného pocitu sytosti (topiramát). Ve firemní studii OB-303 (n = 2487) dosáhlo za 56 týdnů 5% snížení hmotnosti 68,4 % účastníků (v placebové skupině 19,1 %) a 10% snížení hmotnosti 47,4 % (placebo 7,4 %) (16).
Liraglutid
Liraglutid (Saxenda® Novo Nordisk, 3,0 mg s. c. inj. 1× denně) určený k léčbě obezity se od antidiabetika Victoza inj. liší pouze dávkou účinné látky. Ve studii srovnávající liraglutid s placebem a orlistatem po dobu 20 týdnů dosáhl pokles hmotnosti 7,2 kg po liraglutidu v dávce 3 mg (placebo 2,8 kg, orlistat 4,1 kg) a též došlo k poklesu TK. Nejčastějším vedlejším účinkem byla přechodná nevolnost a zvracení (17).
Lorkaserin
Lorkaserin (Belviq® Arena, 10 mg tbl. 2× denně) je selektivní agonista serotoninových receptorů 5-HT2C. Zvyšuje výdej proopiomelanokortinu, mechanismem poklesu hmotnosti je snížení energetického příjmu. Na serotoninový syndrom, který stál za stažením dexfenfluraminu na konci 90. let, bylo vysloveno podezření (ale nebyl potvrzen) jen v jediném případu ze 3 tisíc. Ve studiích BLOSSOM a BLOOM-DM (n = 189 + 63) bylo dosaženo poklesu hmotnosti o 6,6 kg/24 týdnů a o 7,2 kg/52 týdnů; přitom byl prokázán větší úbytek tuku než při užití placeba (18).
PERSPEKTIVNÍ LÉKY
Rozšíření indikace z diabetu i na obezitu bez diabetu, ke které došlo u liraglutidu, lze očekávat u dalších analog GLP-1 i u exenatidu (19). Ten již byl zkoušen s částečným úspěchem u pacientů s hypotalamickou obezitou (20) a se syndromem Pradera a Williho, u kterých sice nedošlo k poklesu hmotnosti, ale bylo pozorováno snížení chuti k jídlu (21).
Za velmi perspektivní lze považovat podávání gliflozinů, inhibitorů receptorů SGLT2, které v důsledku ztrát glukózy močí zvyšují výdej energie. Glifloziny se jeví jako komplexní lék při metabolickém syndromu – snižují glykemii, hmotnost, krevní tlak a příznivě ovlivňují i krevní lipidy. Empagliflozin má navíc velmi impresivní data z hlediska snížení morbidity i mortality (22, 23). V randomizované prospektivní studii (12 týdnů) s podáváním 5 mg dapagliflozinu 1× denně (nebo sitagliptinu 50 mg) 80 diabetikům 2. typu poklesl HbA1c o 7,5 mmol/mol. Dapagliflozin (na rozdíl od sitagliptinu) významně snížil hmotnost, systolický krevní tlak, triacylglyceroly a jaterní transaminázy, došlo ke zvýšení HDL2 cholesterolu o 18 % a také apolipoproteinu A1, klesl sd-LDL cholesterol o 20 % (24).
ANTIOBEZITIKA VE VÝVOJI A VÝZKUMU
V různých fázích výzkumu je odhadem až několik desítek různých látek. Za zmínku stojí antiepileptikum zonisamid, které je testováno i v kombinaci s bupropionem, trojitý inhibitor zpětného vychytávání noradrenalinu, dopaminu a serotoninu tesofensin, antagonista neuropeptidu Y5 velneperit, tzv. twinkretiny, které souběžně aktivují receptory pro GLP-1 i GIP, dále blokátory acylace ghrelinu, analoga cholecystokininu nebo peptid uvolňující prolaktin.
Za slibný byl považován inhibitor methionin aminopeptidázy 2 (MetAP2) beloranib, syntetický analog fumagilinu, přirozeného produktu Aspergillus fumigatus. Původně byl vyvíjen jako antiangiogenní působek pro léčbu malignit. Ve studiích fáze I byl dobře tolerován a vedl k poklesu hmotnosti o 1 kg týdně, resp. o 4,3 kg/25 dnů, snížil triglyceridemii o 38 % a koncentraci LDL cholesterolu o 2 %. Ve 12týdenní dvojitě slepé randomizované studii fáze II (n = 147) došlo k průměrnému poklesu hmotnosti o 5,5, 6,9 a 10,9 kg (25). Svoji účinnost prokázal i v multicentrické studii, do které bylo zařazeno více než 100 pacientů s Praderovým-Williho syndromem (26), ale po úmrtí dvou dobrovolníků na tromboembolickou nemoc byl vývoj léku zastaven.
Pozornost je také věnována sirtuinům (SIRTs – silent information regulators), zejména resveratrolu, obsaženém v červeném vínu; významný pokles hmotnosti však dosud zaznamenán nebyl (27).
Kapsaicin z pálivého pepře, resp. nepálivá analoga kapsinoidy, mají mít termogenní a anorektický účinek.
Za pouze experimentální lze označit blokádu vagových impulzů laparoskopicky implantovaným generátorem elektrických impulzů o nízké energii a vysoké frekvenci do kmene n. vagus. Možnost ovlivnění střevní mikrobioty (inkorporací modifikovaných bakterií produkujících látky fyziologicky vznikající po příjmu potravy v tenkém střevě a snižující příjem potravy a nadměrnou tělesnou hmotnost) zatím nepřekročily testování na laboratorních zvířatech. Zcela recentně publikovaná metaanalýza 14 studií zabývajících se možným vlivem laktobacilů na snižování nadměrné hmotnosti (z celkem 1567 článků na toto téma!) ukázala, že pozorovaný pokles jednak nebyl pozorován ve všech studiích, jednak zřejmě záleží na tom, který kmen je studován a v jaké kombinaci (28). Ve střevě však žijí desítky různých bakteriálních kmenů.
ZÁVĚR
Přes nepochybně obrovský tlak na vývoj bezpečného a účinného antiobezitika a nesmírné prostředky vkládané do tohoto vývoje zůstávají léčivé přípravky pouze podpůrnou metodou v léčbě obezity a zdravotně závažné nadváhy. Je to pochopitelné vzhledem k patogenezi naprosté většiny případů obezity, kdy nepoměr mezi energií dodanou energeticky denzní stravou a energií vydanou často minimální fyzickou aktivitou nejsou naše adaptační mechanismy (navíc zřejmě minimální) schopny korigovat. Vzhledem k tomu, že důvodem pro příjem potravy už zdaleka není jen příjem potřebných živin, nelze v současnosti předpokládat vývoj léku, který by bez vedlejších účinků vedl k významnému a soustavnému poklesu nadměrné tělesné hmotnosti.
Aktuálně dostupná farmakoterapie zdaleka nedosahuje takových efektů jako bariatrická, resp. metabolická chirurgie (29) ani další metody, které využívají nefarmakologické způsoby ovlivnění hormonálního prostředí – endoskopické výkony (zvláště tzv. duodenojejunální rukáv) (30, 31) nebo tzv. bariatrická embolizace dosahující významného poklesu hmotnosti snížením produkce orexigenního hormonu ghrelinu uzavřením tepen žaludečního fundu (32, 33). Přesto mohou být antiobezitika v indikovaných případech bezpečnou oporou při dodržování komplexních změn stravovacích a pohybových návyků.
Z hlediska poměru účinnosti a nežádoucích účinků je aktuálně nejlépe hodnocena trojice naltrexon/bupropion, liraglutid a fentermin/topiramát (34); podle rozsáhlé metaanalýzy účinnosti dosáhla průměrná redukce při podávání naltrexonu/bupropionu 6,15 kg (v 67. týdnu), fenterminu s topiramátem 7,45 kg (v 59. týdnu) a liraglutidu 5,50 kg (v 65. týdnu) (35).
Adresa pro korespondenci:
MUDr. Petr Sucharda, CSc.
3. interní klinika 1. LF UK a VFN
U Nemocnice 1
128 08 Praha 2
Tel.: 224 962 920
e-mail: petr.sucharda@lf1.cuni.cz
Zdroje
1. Bray GA. Treatment of obesity with drugs in the new millennium. In: Eckel RH (ed.). Obesity. Mechanism and Clinical Management. Lippincott Williams & Wilkins, Philadelphia, 2003.
2. Bray G, Kim KK, Wilding J. Obesity: a chronic relapsing progressive disease process. A position statement of the World Obesity Federation. Obes Rev 2017; 18 : 715–723.
3. Maggioni AP, Caterson ID, Urso R et al. Relation between weight loss and causes of death in patients with cardiovascular disease: finding from the SCOUT trial. J Cardiovasc Med (Hagerstown) 2017; 18 : 144–151.
4. James WP, Avenell A, Broom J, Whitehead J. A one-year trial to assess the value of orlistat in the management of obesity. Int J Obes Relat Metab Disord 1997; 21(Suppl 3): S24–S30.
5. Acharya NV, Wilton LV, Shakir SA. Safety profile of orlistat: results of a prescription-event monitoring study. Int J Obes (Lond) 2006; 30 : 1645–1652.
6. Filippatos TD, Derdemezis CS, Gazi IF et al. Orlistat-associated adverse effects and drug interactions: a critical review. Drug Saf 2008; 31 : 53–65.
7. Zhi J, Moore R, Kanitra L, Mulligan TE. Effects of orlistat, a lipase inhibitor, on the pharmacokinetics of three highly lipophilic drugs (amiodarone, fluoxetine, and simvastatin) in healthy volunteers. J Clin Pharmacol 2003; 43 : 428–435.
8. MacWalter RS, Fraser HW, Armstrong KM. Orlistat enhances warfarin effect. Ann Pharmacother 2003; 37 : 510–512.
9. Langlois KJ, Forbes JA, Bell GW, Grant GF jr. A double-blind clinical evaluation of the safety and efficacy of phentermine hydrochloride (Fastin) in the treatment of exogenous obesity. Curr Ther Res Clin Exp 1974; 16 : 289–296.
10. Billes SK, Sinnayah P, Cowley MA. Naltrexone/bupropion for obesity: an investigational combination pharmacotherapy for weight loss. Pharmacol Res 2014; 84 : 1–11.
11. Greenway FL, Fujioka K, Plodkowski RA et al.; COR-I Study Group. Effect of naltrexone plus bupropion on weight loss in overweight and obese adults (COR-I): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2010; 376 : 595–605.
12. Apovian CM, Aronne L, Rubino D et al.; COR-II Study Group. A randomized, phase 3 trial of naltrexone SR/bupropion SR on weight and obesity-related risk factors (COR II). Obesity 2013; 21 : 935–943.
13. Hollander P, Gupta AK, Plodkowski R et al.; COR-Diabetes Study Group. Effects of naltrexone sustained-release/bupropion sustained-release combination therapy on body weight and glycemic parameters in overweight and obese patients with type 2 diabetes. Diabetes Care 2013; 36 : 4022–4029.
14. Fujioka K, Plodkowski R, O'Neil PM et al. The relationship between early weight loss and weight loss at 1 year with naltrexone ER/bupropion ER combination therapy. Int J Obes (Lond) 2016; 40 : 1369–1375.
15. Hong K, Herrmann K, Dybala C et al. Naltrexone/bupropion extended release-induced weight loss is independent of nausea in subjects without diabetes. Clin Obes 2016; 6 : 305–312.
16. Garvey WT, Ryan DH, Look M et al. Two-year sustained weight loss and metabolic benefits with controlled-release phentermine/topiramate in obese and overweight adults (SEQUEL): a randomized, placebo-controlled, phase 3 extension study. Am J Clin Nutr 2012; 95 : 297–308.
17. Astrup A, Rössner S, Van Gaal L et al.; NN8022-1807 Study Group. Effects of liraglutide in the treatment of obesity: a randomised, double-blind, placebo-controlled study. Lancet 2009; 374 : 1606–1616.
18. Apovian C, Palmer K, Fain R et al. Effects of lorcaserin on fat and lean mass loss in obese and overweight patients without and with type 2 diabetes mellitus: the BLOSSOM and BLOOM-DM studies. Diabetes Obes Metab 2016; 18 : 945–948.
19. Bhat SP, Sharma A. Current drug targets in obesity pharmacotherapy – a review. Curr Drug Targets 2017; 18 : 983–993.
20. Lomenick JP, Buchowski MS, Shoemaker AH. A 52-week pilot study of the effects of exenatide on body weight in patients with hypothalamic obesity. Obesity (Silver Spring) 2016; 24 : 1222–1225.
21. Salehi P, Hsu I, Azen CG et al. Effects of exenatide on weight and appetite in overweight adolescents and young adults with Prader-Willi syndrome. Pediatr Obes 2017; 12 : 221–228.
22. Fitchett D, Butler J, van de Borne P et al.; EMPA-REG OUTCOME® trial investigators. Effects of empagliflozin on risk for cardiovascular death and heart failure hospitalization across the spectrum of heart failure risk in the EMPA-REG OUTCOME® trial. Eur Heart J 2017, doi: 10.1093/eurheartj/ehx511.
23. Fitchett D, Zinman B, Wanner C et al.; EMPA-REG OUTCOME® trial investigators. Heart failure outcomes with empagliflozin in patients with type 2 diabetes at high cardiovascular risk: results of the EMPA-REG OUTCOME® trial. Eur Heart J 2016; 37 : 1526–1534.
24. Hayashi T, Fukui T, Nakanishi N et al. Dapagliflozin decreases small dense low-density lipoprotein-cholesterol and increases high-density lipoprotein 2-cholesterol in patients with type 2 diabetes: comparison with sitagliptin. Cardiovasc Diabetol 2017; 16 : 8.
25. Kim DD, Krishnarajah J, Lillioja S et al. Efficacy and safety of beloranib for weight loss in obese adults: a randomized controlled trial. Diabetes Obes Metab 2015; 17 : 566–572.
26. McCandless SE, Yanovski JA, Miller J et al. Effects of MetAP2 inhibition on hyperphagia and body weight in Prader-Willi syndrome: A randomized, double-blind, placebo-controlled trial. Diabetes Obes Metab 2017; 19(12): 1751–1761.
27. Timmers S, Konings E, Bilet L et al. Calorie restriction-like effects of 30 days of resveratrol supplementation on energy metabolism and metabolic profile in obese humans. Cell Metab 2011; 14 : 612–622.
28. Crovesy L, Ostrowski M, Ferreira DMTP et al. Effect of Lactobacillus on body weight and body fat in overweight subjects: a systematic review of randomized controlled clinical trials. Int J Obes (Lond) 2017; 4 : 1607–1614.
29. Heymsfield SB, Wadden TA. Mechanisms, patophysiology, and management of obesity. N Engl J Med 2017; 376 : 254–266.
30. Sullivan S, Edmundowicz SA, Thompson CC. Endoscopic bariatric and metabolic therapies: new and emerging technologies. Gastroenterology 2017; 152 : 1791–1801.
31. Forner PM, Ramacciotti T, Farey JE, Lord RV. Safety and effectiveness of an endoscopically placed duodenal-jejunal bypass device (EndoBarrier®): Outcomes in 114 Patients. Obes Surg 2017, doi: 10.1007/s11695-017-2939-4.
32. Weiss CR, Kathait AS. Bariatric embolization: a new and effective option for the obese patient? Expert Rev Gastroenterol Hepatol 2017; 11 : 293–302.
33. Bai ZB, Qin YL, Deng G et al. Bariatric embolization of the left gastric arteries for the treatment of obesity: 9-month data in 5 patients. Obes Surg 2017, doi: 10.1007/s11695-017-2979-9.
34. Khera R, Murad MH, Chandar AK et al. Association of pharmacological treatments for obesity with weight loss and adverse events: A systematic review and meta-analysis. JAMA 2016; 315 : 2424–2434.
35. Dong Z, Xu L, Liu H et al. Comparative efficacy of five long-term weight loss drugs: quantitative information for medication guidelines. Obes Rev 2017; 18 : 1377–1385.
Štítky
Adiktológia Alergológia a imunológia Angiológia Audiológia a foniatria Biochémia Dermatológia Detská gastroenterológia Detská chirurgia Detská kardiológia Detská neurológia Detská otorinolaryngológia Detská psychiatria Detská reumatológia Diabetológia Farmácia Chirurgia cievna Algeziológia Dentální hygienistka
Článek ÚvodemČlánek Kam směřuje diabetologie?
Článok vyšiel v časopiseČasopis lékařů českých
Najčítanejšie tento týždeň
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Srovnání analgetické účinnosti metamizolu s ibuprofenem po extrakci třetí stoličky
-
Všetky články tohto čísla
- Úvodem
- Kam směřuje diabetologie?
- Kam míří technologie v diabetologii?
- Hyperlipoproteinemie a (nejen) ateroskleróza: střípky z historie i současnosti
- Glykemická variabilita a mikrovaskulární komplikace diabetu
- Nové směřování chirurgické léčby obezity a některých metabolických onemocnění
- Postavení farmakoterapie v současné péči o obézní
- Incidence diabetu z pohledu dávek systému sociálního zabezpečení
- Tzv. protikuřácký zákon a poskytovatelé zdravotních služeb
- Biomarkery v onkologii: nové horizonty a výzvy v diagnostice a léčbě onkologických onemocnění ISOBM – 44. kongres Mezinárodní společnosti pro onkologii a biomarkery
- Nobelovy ceny za fyziologii a lékařství v letech 1940–1960
- Životní výročí prof. MUDr. Štěpána Svačiny, DrSc., MBA
- Doc. MUDr. Radana Neuwirtová, CSc., se dožívá 90 let
- K 85. narozeninám docenta Milana Macka sr.
- 80 let prof. MUDr. Petra Broulíka, DrSc.
- 80 let profesora Petra Goetze
- Ocenění ČLS JEP pro členy Společnosti pro epidemiologii a mikrobiologii ČLS JEP u příležitosti konání KMINE 2017
- Dvorana slávy slovenské medicíny
- PŘEDNÁŠKOVÉ VEČERY SPOLKU ČESKÝCH LÉKAŘŮ V PRAZE (LISTOPAD – PROSINEC 2017)
- Časopis lékařů českých
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Kam míří technologie v diabetologii?
- K 85. narozeninám docenta Milana Macka sr.
- Nové směřování chirurgické léčby obezity a některých metabolických onemocnění
- Glykemická variabilita a mikrovaskulární komplikace diabetu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



