-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Těhotenství u žen po transplantacích solidních orgánů
Pregnancy in women with solid-organ transplants
Objective:
Evaluation of pregnancies and deliveries in women after solid organ transplantations with respect to the maternal and fetal risks.Design:
Overview article.Setting:
Department of Obstetrics and Gynaecology, Second Faculty of Medicine, Charles University and Motol University Hospital, Prague.Methods:
Literature search using the Web of Science, Ovid, Cochrane, Google Scholar and Medline databases with keywords (transplantation, pregnancy, immunosuppression) and analysis of articles published in impact and reviewed journals from 1958 to 2017.Results:
Pregnancy in patients after solid organ transplantions is associated with the higher risk of complications, particularly preeclampsia, and high incidence of comorbidities. Women after transplantation have an increased risk of premature deliveries and low birth weight newborns. The highest risk of complications is documented after lung transplantation. For immunosuppression in pregnancy inhibitors of calcineurin, azathioprine and prednisone are used.Conclusion:
Pregnancies and deliveries in women after solid organ transplants are in a high risk. With early transplantation, adequate patient health compensation, properly planned pregnancy, adequate immunosuppressive therapy and specialized prenatal and obstetric care, women can give birth to healthy newborns after transplantation.Keywords:
pregnancy, delivery, transplantation, immunosuppression
Autoři: Marta Nováčková 1,2
; Zlatko Pastor 1
; J. Matěcha 1
; M. Čekal 1
; J. Froněk 1; Roman Chmel 1,2
Působiště autorů: Gynekologicko-porodnická klinika 2. LF UK a FN Motol, Praha, přednosta doc. MUDr. L. Rob, CSc. 1; Klinika transplantační chirurgie IKEM, Praha, přednosta doc. MUDr. J. Froněk, Ph. D., FRCS, MHA 2
Vyšlo v časopise: Ceska Gynekol 2018; 83(1): 62-68
Souhrn
Cíl studie:
Zhodnocení průběhu těhotenství a porodů žen po transplantacích solidních orgánů s ohledem na rizika pro matku a plod.Typ studie:
Přehledový článek.Název a sídlo pracoviště:
Gynekologicko-porodnická klinika 2. LF UK a FN Motol, Praha.Metodika:
Literární rešerše s využitím databází Web of Science, Ovid, Cochrane, Google Scholar a Medline podle klíčových slov (transplantation, pregnancy, immunosuppression) a analýza článků publikovaných v impaktovaných a recenzovaných časopisech v letech 1958–2017.Výsledky:
Těhotenství žen po transplantaci solidního orgánu je zatíženo vyšším rizikem komplikací, zejména preeklampsie, a vysokou incidencí komorbidit. Ženy po transplantacích mají zvýšené riziko předčasného porodu a častěji rodí novorozence s nízkou porodní hmotností. Největší riziko komplikací je dokumentováno u těhotných po transplantaci plic. Pro imunosupresi v těhotenství se používají zejména inhibitory kalcineurinu, azathioprin a prednison.Závěr:
Těhotenství a porody u žen po transplantacích solidních orgánů jsou vždy rizikové. Při včasně provedené transplantaci, adekvátní kompenzaci zdravotního stavu pacientky, optimálně naplánovaném těhotenství, odpovídající imunosupresivní terapii a specializované prenatální a porodnické péči, mohou ženy po transplantacích porodit zdravého novorozence.Klíčová slova:
těhotenství, porod, transplantace, imunosupreseÚVOD
Pokroky transplantologie a moderní adjuvantní terapie imunosupresivy zlepšily ženám po transplantacích (Tx) solidních orgánů fertilní potenciál a umožnily porody zdravých novorozenců. Ženy tvoří v transplantačních programech 38 % příjemců orgánů a 14 % představují ženy v reprodukčním věku [10].
První těhotenství a porod po alogenní transplantaci proběhl v roce 1958 v USA u 23leté ženy, která byla dva roky po transplantaci ledviny [38]. V Čechách porodila poprvé žena po renální transplantaci v roce 1975 (tab. 1) [1]. Do roku 2001 bylo celosvětově zaznamenáno více než 14 000 těhotenství u žen po transplantaci ledvin [31].
Tab. 1. Transplantace orgánů a porody u žen po transplantacích solidních orgánů v datech 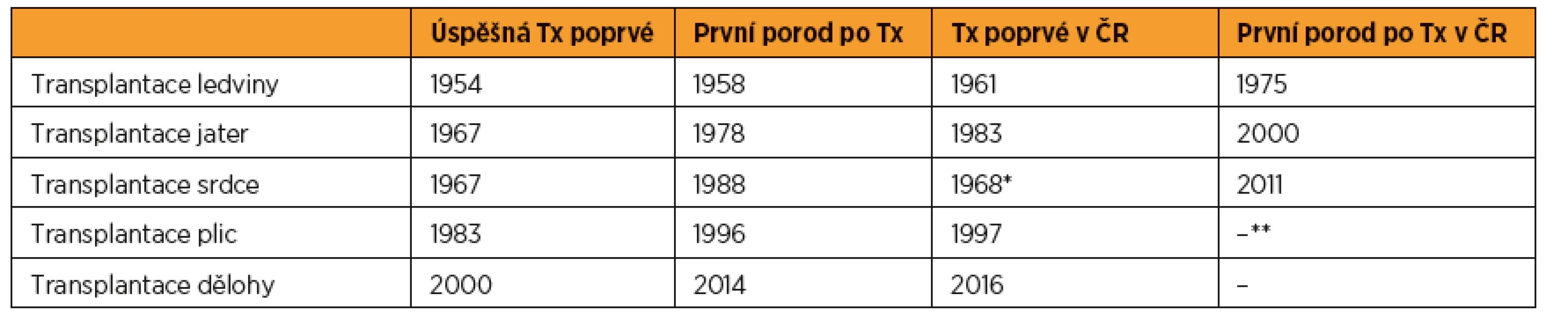
[1, 3, 6, 14, 18, 26, 27, 29, 37, 38, 42, 43, 51, 54] Tx – transplantace *První transplantace srdce v ČSSR, v Bratislavě **Autorům není známo, že by v ČR porodila žena po transplantaci plic S těhotenstvím po transplantaci mohou být spojena rizika rejekce transplantovaného orgánu, infekce, poruchy vývoje plodu, těhotenské ztráty, zhoršení celkového zdravotního stavu a úmrtí ženy v těhotenství nebo po porodu [40]. Na perinatologické výsledky (porodnické komplikace, vrozené vývojové vady) má vliv závažnost primárního onemocnění a jeho komorbidity, interval mezi transplantací orgánu a těhotenstvím, imunosuprese i věk matky [11, 12].
Cílem této publikace je podat přehled rizik hrozících v průběhu těhotenství a porodu u žen po transplantacích solidních orgánů, včetně prezentace doporučení týkajících se plánování koncepce, vlivu imunosupresivní léčby na plod a specifik průběhu gravidity a peripartálního období.
MATERIÁL A METODIKA
Přehledový článek vznikl analýzou metaanalytických a přehledových článků, které se zabývaly hodnocením výsledků, úspěšností a riziky těhotenství a porodů u žen po transplantaci solidního orgánu v letech 1958–2017. Pro vyhledání informací jsme použili databáze Web of Science, Ovid, Cochrane, Medline a Google Scholar. K identifikaci zdrojů jsme použili klíčová slova v kombinaci: transplantace, imunosuprese, těhotenství/transplantace, těhotenství/imunosuprese, porod/transplantace v českém a anglickém jazyce.
PŘEHLED TRANSPLANTOVANÝCH ORGÁNŮ
Transplantace ledvin
Nejčastěji transplantovaným orgánem je ledvina [8, 9]. V těhotenství u pacientek po transplantaci ledvin se vyskytuje hypertenze (až v 54 %), preeklampsie (24–38 %), diabetes mellitus (8 %), předčasné porody a vyšší podíl císařských řezů v porovnání s běžnou populací (tab. 2) [5, 12, 40, 48]. Častější porodnické komplikace (potrat, intrauterinní růstová restrikce, předčasný porod) byly zaznamenány u žen s hypertenzí a zvýšenou sérovou koncentrací kreatininu a proteinurií již před otěhotněním [5, 12, 49]. Těhotenství nemá negativní vliv na funkci transplantované ledviny [12, 16, 23, 25, 28, 48].
Tab. 2. Incidence komplikací v průběhu těhotenství a porodu u pacientek po transplantacích orgánů 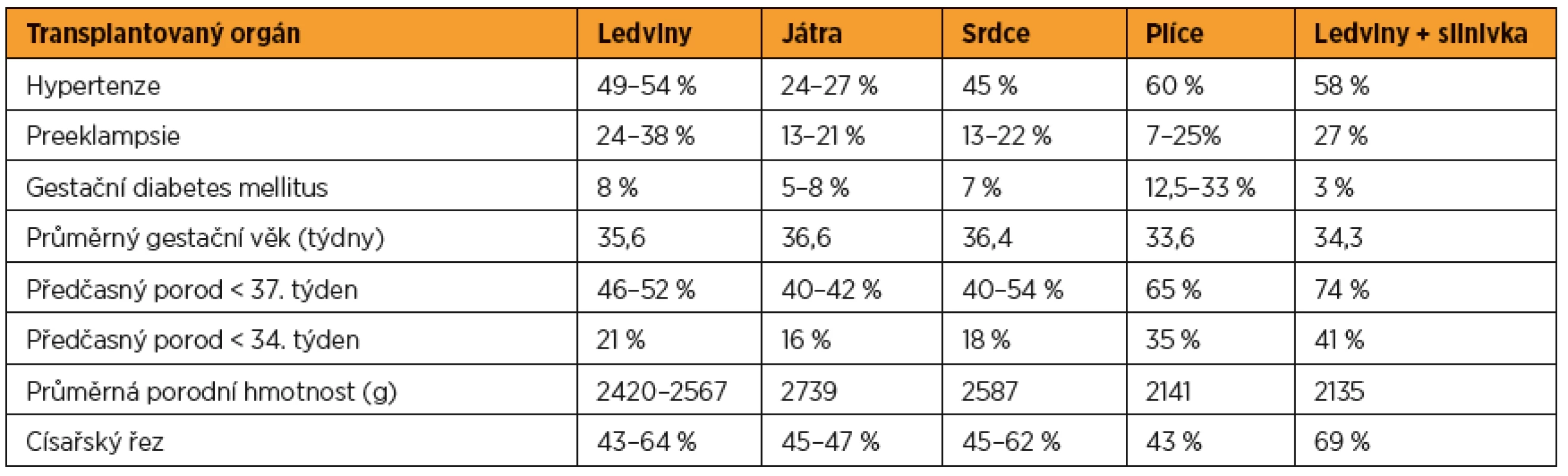
[5, 11, 12, 34, 40, 48, 52] Transplantace jater
Incidence hypertenze (27 %) a preeklapmsie (21 %) u těhotných po transplantaci jater je vyšší než v běžné populaci, avšak nižší než u žen po transplantaci ledvin. Průměrný gestační věk novorozenců a porodní hmotnost jsou vyšší než u žen, které porodily po transplantaci ledviny (tab. 2) [11, 34, 40]. U žen po transplantaci jater je šestkrát vyšší incidence cholestázy v těhotenství [36].
Transplantace srdce
Severoamerický National Transplantation Pregnancy Registry (NTPR) dokumentuje 96 porodů u žen po transplantaci srdce s průměrnou délkou gestace 36,4 týdnů. Celkem 40 % porodů proběhlo před ukončeným 37. týdnem a 18 % před 34. týdnem gravidity. U 45 % žen byla v graviditě léčena hypertenze a preeklampsie se vyskytla u 22 % těhotných. Ve 45 % byl porod veden císařským řezem. U čtyř novorozenců byly diagnostikovány vrozené vady, u dvou z nich (neplánované otěhotnění) byla zaznamenána intrauterinní expozice mykofenolát mofetilu [40].
Transplantace plic
Těhotenství u pacientek po transplantaci plic jsou velmi riziková s vysokým výskytem předčasných porodů (65 %) a novorozenců s velmi nízkou porodní hmotností, vysokým procentem mateřské morbidity a mortality [40]. Porody žen po této transplantaci nejsou časté a údaje o nich se vyskytují pouze v malých souborech nebo kazuistikách. NTPR v Severní Americe zaznamenal 23 porodů u žen po transplantaci plic, Tharkar popisuje výsledky osmi porodů ve Velké Británii [40, 52].
Transplantace ostatních orgánů
Porody zdravých dětí jsou dokumentovány i po transplantaci jiných orgánů (pankreatu, tenkého střeva, po kombinovaných transplantacích ledvin s pankreatem, jater a ledvin). NTPR eviduje 78 porodů žen po kombinované transplantaci ledvin a slinivky. Jedná se o polymorbidní pacientky, těhotenství jsou vysoce riziková i v porovnání s těhotenstvími žen po ostatních typech transplantací (58 % hypertenze, 27 % preeklampsie, 74 % předčasných porodů před dokončeným 37. týdnem gestace a 41 % před 34. týdnem, průměrná porodní hmotnost 2135 g, 69 % císařských řezů) [40]. V České republice proběhl první porod po kombinované transplantaci ledvin a pankreatu v roce 2005 [59].
Transplantace dělohy
První dítě po experimentální transplantaci dělohy (UTx) se narodilo v roce 2014 ve Švédsku [6]. UTx patří mezi kvalitu života zvyšující dočasné transplantace. V rámci studií je dnes indikována zejména u žen s agenezí dělohy (Mayerův-Rokitanskyho-Küsterův-Hauserův syndrom), ale může být provedena i u žen po hysterektomii z různých důvodů. Otěhotnění probíhá cestou asistované reprodukce a gravidita je ukončena primárně císařským řezem. Transplantovaná děloha se odstraňuje po porodu maximálně dvou dětí. Na rozdíl od jiných typů transplantací jsou mladé ženy podstupující UTx zdravé, zpravidla s normální funkcí všech ostatních orgánů. Proto je možné očekávat lepší perinatologické výsledky než po ostatních transplantacích, kdy jsou pacientky zatíženy základním onemocněním a jeho konsekvencemi. Transplantace dělohy byla v ČR poprvé provedena v roce 2016 a výzkumný projekt s tímto zaměřením dále pokračuje (tab. 2) [20, 44].
IMUNOSUPRESIVNÍ LÉČBA V GRAVIDITĚ PO TRANSPLANTACI SOLIDNÍCH ORGÁNŮ
Imunosupresivní terapie po Tx brání odhojení štěpu, a proto se musí užívat v průběhu celého těhotenství. Imunosuprese v graviditě přináší známé obecné nežádoucí účinky (zvýšená náchylnost k infekcím, poruchy krvetvorby), navíc může potenciálně ovlivnit vývoj plodu. Nejproblematičtější je možný teratogenní vliv na plod a vyšší riziko vzniku infekce u matky.
V těhotenství se používají zejména inhibitory kalcineurinu, azathioprin a nízké dávky prednisonu, které jsou považovány z hlediska plodu za bezpečné [8, 48]. Při užívání mykofenolát mofetilu byl zaznamenán zvýšený výskyt (24 %) vrozených vývojových vad (VVV). Z tohoto důvodu se jeho podávání ukončuje minimálně šest týdnů před plánovanou koncepcí a nahrazuje se vhodnějším imunosupresivem [8, 24, 40, 50]. Data o užívání sirolimu a everolimu v graviditě jsou dosud nedostatečná, a proto je k nim třeba přistupovat jako k potenciálně teratogenním a vysadit je šest týdnů před plánovanou koncepcí [48, 55, 57]. Azathioprin má u zvířat teratogenní účinky. U lidských plodů sice také přestupuje do fetálního oběhu, ale plod ještě nemá vytvořen enzym, který by jej konvertoval na účinný metabolit, a proto je z teratogenního hlediska považován za bezpečný [46].
Přehled základních imunosupresiv a jejich vliv na plod uvádí tabulka 3 (tab. 3).
Tab. 3. Přehled nejčastějších nežádoucích účinků imunosupresivní léčby v graviditě po transplantaci solidních orgánů 
PREKONCEPČNÍ OBDOBÍ
Téměř pětina žen po transplantacích solidních orgánů je ve fertilním věku [10]. Jejich plodnost je základní chorobou snížená a provedená Tx insuficientního orgánu jejich fertilitu zlepšuje. Například úspěšná transplantace jater vede až u 97 % žen k obnově menstruačního cyklu a zvyšuje u nich šanci na otěhotnění. Tím současně narůstá i riziko neplánované gravidity, která může být komplikována negativním vlivem imunosupresiv s teratogenními účinky [11]. Ovulační cyklus se může objevit již během prvního měsíce po Tx [10, 32], a proto je vhodné doporučit ženám po transplantaci vhodnou antikoncepci. Každá gravidita u žen po transplantacích solidních orgánů by měla být plánovaná. Doporučená doba k otěhotnění je u dobře kompenzované pacientky za jeden až dva roky po Tx [33]. Dřívější koncepce zvyšuje riziko rejekce štěpu, těhotenských ztrát a předčasného porodu [10]. Podle American Society of Transplantation je těhotenství možné tehdy, pokud nedošlo v průběhu posledního roku ke známkám rejekce transplantovaného orgánu, funkce štěpu je dostatečná a stabilní, není přítomna akutní infekce a pacientka užívá udržovací dávky imunosupresiv, které nemají prokazatelně teratogenní efekt [33].
NEJČASTĚJŠÍ TĚHOTENSKÉ KOMPLIKACE U ŽEN PO TRANSPLANTACI
Riziko preeklampsie (38 % po Tx ledviny, 21 % po Tx jater) je u žen po transplantaci signifikantně vyšší než udávaný 5% výskyt preeklampsie v běžné populaci [53]. Příjemkyně orgánů mají vysokou incidenci komorbidit, zejména hypertenze (ve 27 % u příjemkyň jater a 54 % u příjemkyň ledviny) [10, 11]. Hypertenze matky před graviditou je spojena s rizikem intrauterinní růstové restrikce, předčasným porodem a nízkou porodní hmotností novorozence [33]. Gestační diabetes se u žen po Tx vyskytuje častěji (8 %) než v běžné populaci (4 %) [11, 12], obdobně to platí i pro anémii [45, 55].
Riziko odhojení štěpu během dvou let po porodu se liší podle typu transplantovaného orgánu. Po transplantaci ledvin a jater dosahuje 2–4 %, nejvyšší je u žen po transplantaci plic (16 %) [34, 40]. U žen po transplantaci srdce a po těhotenství je vyšší riziko rejekce v porovnání s transplantovanými ženami, které těhotné nikdy nebyly [21]. Riziko mateřského úmrtí v letech po porodu je nejvyšší po transplantaci srdce, plic a po kombinované transplantaci ledviny se slinivkou [17, 40].
ZPŮSOB VEDENÍ PORODU
U žen po transplantaci je vyšší frekvence porodů císařským řezem než v běžné populaci. Souvisí to zejména s jejich komorbiditami, častějším výskytem preeklampsie a předčasných porodů. Transplantace solidního orgánu v anamnéze těhotné však není u fyziologicky probíhající gravidity automatickým důvodem k porodu plodu císařským řezem [48, 55]. Sectio caesarea je primárně indikován při porodu u žen po transplantaci dělohy [20].
KOJENÍ
Kojení u žen po Tx se vzhledem k užívání imunosupresivní terapie sice nedoporučuje, přesto NTPR zaznamenává v posledních 20 letech vzrůstající trend v počtu kojících žen. V roce 2015 kojilo již více než 65 % pacientek po transplantaci [40]. Při užívání standardních dávek prednisonu, cyklosporinu a takrolimu nebyly u kojících žen zjištěny žádné negativní účinky na novorozence. Při užití azathioprinu byla popsána přechodná neutropenie kojenců [7, 13, 58]. Při užívání mykofenolát mofetilu, sirolimu, everolimu a belataceptu je kojení kontraindikováno [40].
NEJČASTĚJŠÍ NEGATIVNÍ VLIVY TRANSPLANTACE NA PLOD A NOVOROZENCE
V porovnání s běžnou populací je u žen po transplantaci vyšší riziko intrauterinní růstové restrikce, předčasného porodu (12 % resp. 46 %) a nižší porodní hmotnosti novorozence (3298 g resp. 2420 g po Tx ledviny) [12, 40, 55]. Porody nezralých dětí s nízkou porodní hmotností jsou komplikovány zvýšenou morbiditou i mortalitou [32]. U novorozenců matek po Tx byl častěji než u dětí zdravých žen zaznamenán novorozenecký ikterus, hyperglykémie a hyperkalémie, zpravidla v mírné formě bez negativních klinických následků [55]. Registr NTPR nezaznamenal vyšší riziko vrozených vad u dětí, které se narodily matkám užívajícím inhibitory kalcineurinu, azathioprin a nízké dávky prednisonu v průběhu gravidity [40]. U dětí žen po transplantaci ledviny nebyl zjištěn zvýšený výskyt mentální a vývojové retardace [56].
DISKUSE
Z naší analýzy vyplývá, že přestože je těhotenství a porod žen po Tx provázeno riziky a komplikacemi pro matku i plod, je při adekvátní komplexní péči možné.
Nejčastěji se diskutuje o možných negativních vlivech imunosuprese na plod. V minulosti byly při užívání kortikosteroidů v dávkách vyšších než 20 gramů denně zaznamenány sporadické případy novorozenecké adrenální imunosuprese, hypoplazie thymu a rozštěp patra [19]. Studie posuzující vliv užívaných kortikosteroidů u 1449 těhotných v prvním trimestru riziko vzniku rozštěpu patra či VVV nepotvrdila [4]. Nebyly také potvrzeny spekulace o autoimunitních onemocněních, renálním selhání a neurokognitivních deficitech u dětí, jejichž matky užívaly v graviditě imunosupresiva [8, 11, 47].
Většina popsaných těhotenství a porodů se týká žen po transplantaci ledviny nebo jater [40]. Častější výskyt předčasných porodů a novorozenců s nižší porodní hmotností je pravděpodobně způsoben spíše primárním zdravotním stavem matky (např. vyšší riziko hypertenze a preeklampsie u těhotných žen po transplantaci ledvin) než působením imunosuprese [41]. Vyšší výskyt preeklampsie u těhotných po Tx ledviny souvisí s vysokým výskytem hypertenze (54 %) již před těhotenstvím [12, 30, 48].
U těhotných po transplantaci ledviny je obtížnější odlišit preeklampsii od hypertenze než u zdravých těhotných. K vzestupu krevního tlaku dochází u transplantovaných často již po 20. týdnu gravidity. Hyperfiltrací krve ledvinami se zhoršuje preexistující proteinurie. Hodnota kyseliny močové v krvi je při hodnocení preeklampsie méně spolehlivá při léčbě inhibitory kalcineurinu, které vyvolávají hyperurikémii [35, 48]. Akutní rejekce ledviny se projevuje náhlým zhoršením hypertenze a významným nárůstem proteinurie, což se může diferenciálně diagnosticky jevit jako preeklampsie [49].
Při správném načasování koncepce, kompenzaci onemocnění matky a včasném vysazení léků s teratogenním efektem nemá imunosupresivní léčba v graviditě negativní vliv na plod [40].
DOPORUČENÍ PRO PRAXI
Již před transplantací je vhodné doporučit vhodnou antikoncepci k zabránění neplánované graviditě minimálně po dobu jednoho roku po Tx [10].
Pro úspěšný průběh gravidity je důležitá podrobná edukace pacientek již v době jejího plánování a jejich psychologická podpora během léčby a těhotenství. Ženy by měly být informovány, že mohou otěhotnět i po Tx. Mělo by to být v optimálním období, po konzultaci s ošetřujícím týmem lékařů a po výběru adekvátního typu a dávky imunosupresivní terapie. Při plánování gravidity musí být oba rodiče poučeni, že těhotenství je vždy vysoce rizikové pro matku i plod [33].
Prekoncepční a prenatální péči by měl zajistit tým erudovaných specialistů v gynekologii a porodnictví, transplantologii a souvisejících oborech (neonatologie, interna, imunologie a psychologie) [33]. Během celého těhotenství jsou nutné pravidelné (minimálně jednou měsíčně) kontroly sérových hladin imunosupresiv [55].
LIMITY NAŠÍ PUBLIKACE
V dostupné literatuře jsou průběh a výsledky těhotenství dokumentovány pouze u části žen po transplantacích. Dostupná data jsou limitována neexistencí národních registrů. Výjimkou jsou pouze National Transplantation Pregnancy Registry v USA, registr ve Velké Británii, jehož činnost však byla přerušena, a registr v Austrálii a na Novém Zélandu [5, 34, 40]. Deshpande uvádí, že ačkoli data z těchto zdrojů jsou velmi dobře zpracovaná a vysoce přínosná, představují celkově pouze třetinu popsaných případů [12]. Ostatní výsledky jsou prezentovány formou malých souborů a kazuistik. U těhotenství po Tx ledvin a jater převažují studie jednotlivých center, v případě pacientek po transplantaci srdce a plic se jedná většinou o kazuistiky. Články používají různou metodiku a jsou většinou retrospektivní. K dispozici je omezený počet randomizovaných studií. Většina informací o bezpečnosti imunosupresiv v graviditě vychází z výsledků studií na zvířatech.
VÝHLEDY DO BUDOUCNA
Transplantací solidních orgánů stále přibývá, a protože příjemkyněmi orgánů jsou i ženy ve fertilním věku, narůstá také celkový počet porodů těchto pacientek. Na základě dostupných informací, zejména z velkých registrů, víme, že při optimální péči a adekvátní terapii je možné dosáhnout dobrých výsledků, přestože se jedná o velmi riziková těhotenství. V budoucnu očekáváme vývoj bezpečnějších imunosupresiv a léků s minimálním teratogenním efektem. Očekáváme longitudinální studie o zdravotním stavu dětí porozených ženám po Tx a vlivu této léčby na zdravotní stav jedince, případě ovlivnění genetických a jiných konsekvencí.
ZÁVĚR
Pokroky v transplantační chirurgii, která nahrazuje nefunkční orgán funkčním, zlepšují zdravotní stav pacientů z pohledu základního onemocnění, což vede ke snížení morbidity i mortality, zvýšení kvality života a pacientům v konečném důsledku dává větší šanci na naplnění reprodukčních funkcí. Těhotenství žen po transplantaci solidních orgánů jsou stále častější a přinášejí komplikace, které vyplývají z konsekvencí základního onemocnění a souvisí s chronickou medikací a jejím vlivem na plod. V případě včas provedené transplantace, při adekvátní kompenzaci zdravotního stavu pacientky, správně naplánovaném těhotenství, zvolení odpovídající imunosupresivní terapie a komplexní prenatální a porodnické péči existuje reálná naděje, že perinatologické výsledky a zdravotní stav ženy po porodu budou srovnatelné se situací v běžné populaci.
Podpořeno MZ ČR - RVO FN v Motole 00064203.
MUDr. Marta Nováčková, Ph.D.
Gynekologicko-porodnická klinika
2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: marta.novackova@fnmotol.cz
Zdroje
1. 50 let transplantací ledvin - půl století na cestě k životu. Medical tribune, 2016, 6. http://www.tribune.cz/clanek/39043-let-transplantaci-ledvin-pul-stoleti-na-ceste-k-zivotu.
2. Armenti, VT., Moritz, MJ., Cardonick, EH., Davison, JM. Immunosuppression in pregnancy: choices for infant and maternal health. Drugs, 2002, 62(16), p. 2361–2375.
3. Barnard, CN. Human heart transplantation. Can Med Assoc J, 1969, 100(3), p. 91–104.
4. Bay Bjorn, AM., Ehrenstein, V., Hundborg, HH., et al. Use of corticosteroids in early pregnancy is not associated with risk of oral clefts and other congenital malformations in offspring. Am J Ther, 2014, 21(2), p. 73–80.
5. Bramham, K., Nelson-Piercy, C., Gao, H. Pregnancy in renal transplant recipients: a UK national cohort study. Clin J Am Soc Nephrol, 2013, 8(2), p. 290–298.
6. Brännström, M., Johannesson, L., Bokström, H., et al. Livebirth after uterus transplantation. Lancet, 2015, 385(9968), p. 607–616.
7. Constantinescu, S., Pai, A., Coscia, LA., et al. Breast-feeding after transplantation. Best Pract Res Clin Obstet Gynaecol, 2014, 28(8), p. 1163.
8. Coscia, LA., Constantinescu, S., Moritz, MJ., et al. Report from the National Transplantation Pregnancy Registry (NTPR): outcomes of pregnancy after transplantation. Clin Transpl, 2010, p. 65–85.
9. Coscia, LA., Constantinescu, S., Moritz, MJ., et al. Report from the National Transplantation Pregnancy Registry (NTPR): outcomes of pregnancy after transplantation. Clin Transpl, 2009, p. 103–122.
10. Deshpande, NA., Coscia, LA., Gomez-Lobo, V., et al. Pregnancy after solid organ transplantation: a guide for obstetric management. Rev Obstet Gynecol, 2013, 6(3–4), p. 116–125.
11. Deshpande, NA., James, NT., Kucirka, LM., et al. Pregnancy outcomes of liver transplant recipients: a systematic review and meta-analysis. Liver Transpl, 2012, 18(6), p. 621–629.
12. Deshpande, NA., James, NT., Kucirka, LM., et al. Pregnancy outcomes in kidney transplant recipiens: a systematic review and meta-analysis. Am J Transplant, 2011, 11, p. 2388–2404.
13. Durst, JK., Rampersad, RM. Pregnancy in women with solid-organ transplants: a review. Obstet Gynecol Surv, 2015, 70(6), p. 408–418.
14. Fageeh, W., Raffa, H., Jabbad, H., Marzouki, A. Transplantation of the human uterus. Int J Obstet Gynecol, 2002, 76, p. 245–251.
15. Goldstein, LH., Dolinski, G., Greenberg, R., et al. Pregnancy outcome of women exposed to azathioprine during pregnancy. Birth Defects Res A Clin Mol Teratol, 2007, 79(10), p. 696–701.
16. Gorgulu, N., Yelken, B., Caliskan, Y., et al. Does pregnancy increase graft loss in female renal allograft recipiens? Clin Exp Nephrol, 2010, 14, p. 244–247.
17. Gyi, KM., Hodson, ME., Yacoub, MY. Pregnancy in cystic fibrosis lung transplant recipiens: Case series and review. J Cyst Fibros, 2006, 5(3), p. 171–175.
18. Humlová, D. Žena s transplantovaným srdcem porodila zdravou holčičku. Nemocniční listy. Fakultní nemocnice Brno. 2016, 1, s. 20.
19. Chhabria, S. Aicardi´s syndrome: are corticosteroids teratogens? Arch Neurol, 1981, 38(1), p. 70.
20. Chmel, R., Nováčková, M., Pastor, Z., et al. Možnosti transplantace dělohy v České republice – indikace, výzkum a klinické zkušenosti. Čas Lék čes, 2017, 156(1), s. 28–35.
21. Johnson, MR., Naftel, DC., Hobbs, RE., et al. The incremental risk of female sex in heart transplantation: a multiinstitutional study of peripertum cardiomyopathy and pregnancy. Cardiac Transplant Research Database Group. J Heart Lung Transplant, 1997, 16(8), p. 801–812.
22. Kanbay, M., Akcay, A., Huddam, B. Influence of cyclosporine and tacrolimus on serum uric acid levels in stable kidney transplant recipients. Transplant Proc, 2005, 37(7), p. 3119–3120.
23. Kashanizadeh, N., Nemati, E., Sharifi-Bonab, M., et al. Impact of pregnancy on the outcome of kidney transplantation. Transplant Proc, 2007, 39, p. 1136–1138.
24. Kim, M., Rostas, S., Gabardi, S. Mycophenolate fetal toxicity and risk evaluation and mitigation strategies. Am J Transplant, 2013, 13(6), p. 1383–1389.
25. Kim, HW., Seok, HJ., Kim, TH. The experience of pregnancy after renal transplantation: pregnancies even within postoperative 1 year may be tolerable. Transplantation, 2008, 85(10), p. 1412–1419.
26. Koordinační středisko transplantací. Dostupné na www.kst.cz.
27. Kořístek, V., Černý, J., Gregor, Z., et al. Naše první zkušenosti s klinickou transplantací jater. Čas Lék čes, 1984, 123, s. 93–96.
28. Levidiotis, V., Chang, S., McDonald, S., et al. Pregnancy and maternal outcomes among kidney transplant recipients. J Am Soc Nephrol, 2009, 20, p. 2433–2440.
29. Löwenstein, BR., Vain, NW., Perrone, SV., et al. Successful pregnancy and vaginal delivery after heart transplantation. Am J Obstet Gynecol, 1988, 158, p. 589–590.
30. Majak, GB., Sandven, I., Lorentzen, B. Pregnancy outcomes following maternal kidney transplantation: a national cohort study. Acta Obstet Gynecol Scand, 2016, 95(10), p. 1153–1161.
31. McKay, DB., Josephson, MA. Pregnancy after kidney transplantation. Clin J Am Soc Nephrol, 2008, 3, Suppl. 2, p. 117–125.
32. McKay, DB., Josephson, MA. Pregnancy in recipients of solid organs – effect on mother and child. N Engl Med, 2006, 354, p. 1281.
33 McKay, DB., Josephson, MA., Armenti, VT., et al. Reproduction and transplantation: report on the AST Consensus Conference on Reproductive Issues and Transplantation. Am J Transplant, 2005, 5(7), p. 1592–1599.
34. Mohamed-Ahmed, O., Nelson-Piercy, C., Bramham, K., et al. Pregnancy outcomes in liver and cardiothoracic transplant recipients: a UK national cohort study. PLoS One, 2014, 9(2), e89151.
35. Morales, JM., Hernández Poblete, G., Andrés, A., et al. Uric acid handling, pregnancy and cyclosporin in renal transplant women. Nephron, 1990, 56(1), p. 97–98.
36. Moritz, MJ., Coscia, LA., Armenti, DP., Constantinescu, S. National Transplantation Pregnancy Registry: Cholestasis of pregnancy in liver transplant recipients. Am J Transplant, 2015, 15, p. 110A.
37. Murray, JE., Reid, DE., Harrison, KH., et al. Successful pregnancies after human renal transplantation. Engl J Med, 1963, 269, p. 341–343.
38. Murray, JE., Merrill, JP., Harrison, JH. Kidney transplantation between seven pairs of identical twins. Ann Surg, 1958, 148(3), p. 343–359.
39. Natekar, A., Pupco, A., Bozzo, P., Koren, G. Safety of azathioprine use during pregnancy. Can Fam Physician, 2011, 57(12), p. 1401–1402.
40. National Transplantation Pregnancy Registry. 2015 Annual report. Zpráva je dostupná na www.ntpr.giftoflifeinstitute.org.
41. Nevers, W., Pupco, A., Koren, G., Bozzo, P. Safety of tacrolimus in pregnancy. Can Fam Physician, 2014, 60(10), p. 905–906.
42. Pafko, P., Kabát, J., Schützner, J., et al. První transplantace plic v České republice. Rozhl Chir, 1999, 78(4), s. 148–149.
43. Parry, D., Hextall, A., Robinson, VP., et al. Pregnancy following a single lung transplant. Thorax, 1996, 51, p. 1162–1164.
44. Pastor, Z., Fronek, J., Novackova, M., Chmel, R. Sexual life of women with Mayer-Rokitanski-Küster-Hauser syndrome after laparoscopic Vecchietti vaginoplasty. Sex Med, 2017, 5(2), p. 106–113.
45. Rocha, A., Cardoso, A., Malheiro, J., et al. Pregnancy after kidney transplantation: graft, mother, and newborn complications. Transplant Proc, 2013, 45(3), p. 1088–1091.
46. Saarikoski, S., Seppälä, M. Immunosuppression during pregnancy: transmission of azathioprine and its metabolites from the mother to the fetus. Am J Obstet Gynecol, 1973, 115(8), p. 1100–1106.
47. Scott, JR., Branch, DW., Holman, J. Autoimmune and pregnancy complications in the daughter of a kidney transplat patient. Transplantation, 2002, 73, p. 815–816.
48. Shah, S., Verma, P. Overview of pregnancy in renal transplant patients. Int J Nephrol, 2016;2016 : 4539342. doi: 10.1155/2016/4539342.
49. Sibanda, N., Briggs, JD., Davison, JM., et al. Pregnancy after organ transplantation: a report from the UK Transplant pregnancy registry. Transplantation, 2007, 83(10), p. 1301–1307.
50. Sifontis, NM., Coscia LA., Constantinescu, S., et al. Pregnancy outcomes in solid organ transplant recipients with exposure to mycophenolate mofetil or sirolimus. Transplantation, 2006, 82(12), p. 1698–1702.
51. Starzl, TE., Groth, CG., Brettschneider, L. Orthotopic homotransplantation of the human liver. Ann Surg, 1968, 168, p. 852–856.
52. Thakrar, MV., Morley, K., Lordan, JL. Pregnancy after lung and heart-lung transplantation. J Heart Lung Transplant, 2014, 33(6), p. 593–598.
53. Vlk, R., Matěcha, J., Drochýtek, V. Prevence preeklampsie – přehledový článek. Čes Gynek, 2015, 80(3), s. 229–235.
54. Walcott, WO., Derick, DE., Jolley, JJ., Snyder, DL. Succsessful pregnancy in a liver transplant patient. Am J Obstet Gynecol, 1978, 132, p. 340–341.
55. Wielgos, M., Pietrzak, B., Bobrowska, K., et al. Pregnancy after organ transplantation. Neuro Endocrinol Lett, 2009, 30(1), p. 6–10.
56. Willis, FR., Findlay, CA., Gorrie, MJ., et al. Children of renal transplant recipient mothers. J Paediatr Child Health, 2000, 36, p. 230–235.
57. Yamamura, M., Kojima, T., Koyama, M., et al. Everolimus in pregnancy: Case report and literature review. J Obstet Gynecol Res, 2017, 43(8), p. 1350–1352.
58. Zheng, S., Easterling, TR., Hays, K. Tacrolimus placental transfer at delivery and neonatal exposure through breast milk. Br J Clin Pharmacol, 2013, 76(6), p. 988–996.
59. Živný, J., Adamec, M., Pařízek, A., et al. Těhotenství a porod po kombinované transplantaci ledviny a pankreatu v České republice. Čes Gynek, 2005, 70(5), s. 362–366.
Štítky
Detská gynekológia Gynekológia a pôrodníctvo Reprodukčná medicína
Článok vyšiel v časopiseČeská gynekologie
Najčítanejšie tento týždeň
2018 Číslo 1- Ne každé mimoděložní těhotenství musí končit salpingektomií
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Mýty a fakta ohledně doporučení v těhotenství
- Gynekologické potíže pomáhá účinně zvládat benzydamin
-
Všetky články tohto čísla
- Využití medroxyprogesteron acetátu k blokádě LH při stimulaci dárkyní vajíček
- Vývoj prenatální diagnostiky vrozených srdečních vad, zisk z jednotlivých ultrazvukových projekcí
- Možnosti přípravy endometria ke kryoembryotransferu
- Validácia nového nástroja pre indentifikáciu bariér v prevencii rakoviny krčka maternice na Slovensku
- Malformace Galenovy žíly u plodu
- Dopad císařského řezu na soukromou zdravotní službu v Brazílii: indikace a míra morbidity a úmrtnosti novorozenců
- Subarachnoidální krvácení u matky v graviditě
- Non-Hodgkinův B-lymfom ovarií s nepříznivou prognózou – náhodný nález při císařském řezu
- Hysteroskopicky asistovaná laparoskopická salpingostomie při řešení tubární gravidity
- Intravenózní leiomyomatóza jako vzácný nádor myometria
- Metoda One-Step Nucleic Acid Amplification – jaká je budoucnost zpracování sentinelových uzlin?
- Těhotenství u žen po transplantacích solidních orgánů
- Antibiotická terapie v graviditě
- Česká gynekologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Možnosti přípravy endometria ke kryoembryotransferu
- Antibiotická terapie v graviditě
- Malformace Galenovy žíly u plodu
- Využití medroxyprogesteron acetátu k blokádě LH při stimulaci dárkyní vajíček
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



