Trombolytická terapie mozkového infarktu
Thrombolytic therapy of cerebral infarction
The purpose of thrombolytic therapy is to recanalize the cerebral vessel occluded by a thrombus or an embolus. According to applicable guidelines, the standard therapy of acute cerebral infarcti on consists in intraveno us thrombolysis within three ho urs from the occurrence of the vascular event. Current rese arch is focused on the selecti on of candidates who are still suitable for thrombolysis after the expirati on of the three - ho ur peri od, and on incre asing the percentage of recanalizati ons (enhanced thrombolysis, interventi on techniques). The a uthors present new results of the ECASS III study which justify the extensi on of the therape utic window to 4.5 ho urs from the occurrence of symptoms.
Key words:
acute cerebral infarction – systemic thrombolysis – combined thrombolysis – ECASS III
:
D. Goldemund; R. Mikulík; M. Reif
:
Kardiol Rev Int Med 2008, 10(4): 168-176
Trombolytická terapi e má za cíl dosáhno ut rekanalizace mozkové tepny uzavřené trombem nebo embolem. Standardní terapi í akutního mozkového infarktu je dle aktu álních guidelines intravenózní trombolýza do tří hodin od vzniku cévní příhody. Aktu ální výzkum se so ustřeďuje jednak na selekci kandidátů vhodných k trombolýze i po uplynutí tříhodinového časového okna, jednak na dosažení vyššího procenta rekanalizací (zesílená trombolýza, intervenční techniky). Prezentovány budo u čerstvé výsledky studi e ECASS III, které opodstatňují prodlo užení terape utického okna pro intravenózní trombolýzu na 4,5 hodiny od vzniku symptomů.
Klíčová slova:
akutní mozkový infarkt – systémová trombolýza – kombinovaná trombolýza – ECASS III (Europe an Co operative Acute Stroke Study)
Úvod
Cévní mozkové příhody (CMP) jso u celosvětově druho u nejčastější příčino u úmrtí jak v rozvojových, tak rozvinutých zemích. CMP jso u zodpovědné za více než pět mili onů úmrtí ročně a jso u nejčastější příčino u invalidity u starších nemocných. Cílem léčby CMP není tedy po uze snížení mortality, ale zejména zachování soběstačnosti paci enta. Stupeň soběstačnosti je hodnocen dle tzv. modifikované Rankinovy škály (mRS) (tab. 1). Za úspěšné vyléčení je považována hodnota ≤ 1, resp. ≤ 2 v závislosti na tíži ne urologického deficitu při vzniku CMP.
![Modifikovaná Rankinova škála (mRS) [1].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/5744eeeb18326eb0456936c1db118c05.png)
80 % všech CMP tvoří mozkové infarkty. Většina mozkových infarktů vzniká uzávěrem mozkové tepny na podkladě trombózy či embolizace s následno u hypoperfuzí mozkové tkáně. Při poklesu krevního průtoku z normálních hodnot > 50 ml/ 100 g/ min na hodnotu mezi 12 – 18 ml/ 100 g/ min vzniká reverzibilní porucha funkce (penumbra). Klesá‑li perfuze na < 10 ml/ 100 g mozkové tkáně/ min, následují ireverzibilní změny (nekróza). Ne urony penumbry zůstávají vitální minuty až hodiny po okluzi tepny a celý proces je reverzibilní při včasné reperfuzi.
Základní terapi í mozkového infarktu je dosažení časné reperfuze. Paci enti, u kterých dojde k rekanalizaci uzavřené mozkové tepny, mají po třech měsících až 13krát větší šanci, že nezůstano u invalidní [2]. Čas rekanalizace hraje kriticko u roli. Z analýzy šesti nejvýznamnějších trombolytických studi í vyplývá, že nejdůležitějším faktorem pro dobrý výsledný klinický stav je čas od rozvoje příznaků k zahájení trombolýzy. Při podání v čase 0 – 90 min je šance na vyléčení dvojnásobná oproti zahájení terapi e po 181. min (obr. 1) (proto heslo „time is brain“) [3].
![Při podání t- PA v čase 0– 90 minut je šance (Odd Rati o – OR) na dosažení dobrého výsledného stavu 2,81 (95% CI 1,75– 4,50), zatímco mezi 181.– 270. minuto u je to jen 1,40 (1,05– 1,85). OTT – Onset to Treatment Time – čas od počátku příznaků k zahájení terapie [3].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/dda82f33811160a71afedf3186209e63.jpg)
V so učasnosti je považována za standardní terapii akutního mozkového infarktu do tří hodin intravenózní trombolýza (IVT) tkáňovým aktivátorem plasminogenu (t - PA) [4].
Intravenózní trombolýza do tří hodin
Studi e NINDS (The Nati onal Institute of Ne urological Disorders and Stroke t - PA Stroke Study) s t - PA a časovým oknem 3 hod ukázala jednoznačně lepší výsledný stav paci entů léčených t - PA ve srovnání s placebem. Paci enti měli přinejmenším o 30 % větší relativní pravděpodobnost, že nebudo u mít žádný deficit nebo budo u mít jen minimální postižení (mRS ≤ 1), obr. 2 [5].
![Výsledky studie NINDS, modifikovaná Rankinova škála (mRS) po třech měsících u pacientů léčených t-PA a placebem [5].](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/bb73f402c17bf34ecaea5044dd218df7.jpg)
Symptomatická intrakrani ální krvácení (symptomatic IntraCrani al Haemorrhage – sICH) se vyskytla během prvních 36 hod u 6,4 % paci entů léčených t - PA oproti 0,6 % paci entů léčených placebem. Mortalita se po třech měsících navzdory vyšší incidenci krvácení signifikantně nelišila (17 % t - PA vs 21 % placebo).
Na našem pracovišti byl trombolytický program zahájen v roce 1999. Byl vytvořen trombolytický protokol určený pro rychlo u ori entaci lékaře aplikujícího léčbu. Obsahuje mj. seznam absolutních i relativních kontraindikací, so učástí je protokol vyšetření pomocí škály NIHSS (Nati onal Institute of He alth Stroke Scale) (tab. 2) [6], dále protokol pro střední zdravotnický personál a protokol pro management tlaku krve (TK) a eventu álních krvácivých komplikací. Všichni paci enti jso u hospitalizováni na iktové jednotce, je provedeno CT vyšetření mozku, CT angi ografi e, ultrazvukové vyšetření krčních a intrakrani álních tepen a klinické a laboratorní vyšetření. Vždy je nezbytná verifikace přesné doby vzniku cévní příhody. Při splnění indikačních kritéri í (tab. 3) podáváme rt - PA (Actilyse©) v celkové dávce 0,9 mg/ kg, 10 % aplikujeme bolusově během 1 – 2 min, zbytek injektomatem po dobu jedné hodiny. Paci enti jso u pečlivě monitorováni. Při výrazné regresi nebo normalizaci klinického nálezu je kontrolní CT mozku provedeno většino u do 2 – 3 dnů, u všech ostatních paci entů do 24 hod od trombolýzy, při zhoršení stavu ihned. Pokud paci ent užívá anti agregační terapii, léčbu nepřerušujeme, v ostatních případech nasazujeme anti agreganci a za 24 hod, jakmile kontrolní CT vylo učí hemorhagicko u komplikaci [4]. S ohledem na preskribční omezení nasazujeme nejčastěji Aggrenox (2 × 1 tbl.) nebo Anopyrin v dávce 100 – 300 mg a léčba je trvalá.


Naše so učasné výsledky jso u z hlediska účinnosti i bezpečnosti léčby srovnatelné se studi í NINDS (tab. 3). Do července 2008 jsme trombolýzu podali již 334 paci entům (u malé části z nich intraarteri álně).
![Tab. 3 Srovnání souboru pacientů z našeho pracoviště (FN USA – Fakultní nemocnice u sv. Anny) se studií NINDS (v roce 2007). ICH – intracerebrální hematom, NIHSS (National Institute of Health Stroke Scale) – škála užívaná ke klinickému hodnocení tíže neurologického deficitu [6]. OTT (Onset to Treatment Time) – čas od počátku příznaků k zahájení terapie, ATT (Arrival to Treatment Time) – čas od příjezdu pacienta k zahájení terapie.](https://pl-master.mdcdn.cz/media/image/a2042d0598fe3c3e2dc76152ad2f82a5.png?version=1537795662)
V Evropě byla trombolýza mozkového infarktu schválena pod podmínko u, že bezpečnost a účinnost t - PA bude potvrzena v běžné klinické praxi. S využitím dat mezinárodního on‑line registru trombolyzovaných paci entů (Safe Implementati on of Thrombolysis in Stroke – SITS) byla provedena monitorovací studi e SITS - MOnitoring STudy (SITS - MOST). Hodnoceno bylo 6 483 paci entů z 285 evropských klinických pracovišť. Výsledky byly srovnatelné s předchozími studi emi a potvrdily bezpečnost i účinnost rutinního podávání t - PA v běžné klinické praxi [7].
Intravenózní trombolýza je technicky jednoduchá, ale kromě relativně malé účinnosti (kompletní rekanalizace je dosaženo po uze asi u 18 % paci entů do dvo u hodin od podání, 40 % paci entů umírá nebo zůstává upo utáno na lůžko) dovoluje kvůli úzkému terape utickému oknu léčit jen omezeno u skupinu nemocných (v ČR 1 – 2 % paci entů s CMP). Aktu ální výzkum se tedy so ustředí na:
- selekci kandidátů vhodných k systémové trombolýze i po uplynutí tříhodinového časového okna,
- dosažení vyššího procenta rekanalizací (intervenční techniky, akcelerovaná trombolýza).
Intravenózní trombolýza po 3. hod
I přes původně ne utrální výsledky studi í ECASS I, II a ATLANTIS s časovým oknem 3 – 6 hod, ukazují post‑hoc analýzy možný prospěch intravenózní t - PA i v tomto časovém okně. Studi e ECASS II (Europe an - Australasi an Acute Stroke Study) neprokázala, že by t - PA podaná mezi 3. – 6. hod vedla ve srovnání s placebem ke zvýšení počtu paci entů s žádným nebo minimálním deficitem (mRS 0 – 1). Post‑hoc analýza však ukázala, že t - PA signifikantně snižuje počet paci entů invalidních (mRS > 2) [8]. Stejně tak meta‑analýza studi í ECASS, ECASS II a NINDS zahrnující dohromady 2 044 paci entů (1 034 t - PA, 1 010 placebo) ukázala statisticky signifikantní efekt t - PA na snížení počtu invalidních paci entů [9].
V září 2008 byly ve Vídni prezentovány výsledky studi e ECASS III (Europe an Co operative Acute Stroke Study), která hodnotila účinnost a bezpečnost IVT mezi 3. a 4,5. hod [10]. Do studi e bylo v řadě evropských center (včetně ČR) zařazeno 821 paci entů, kterým byla intravenózně podána buď altepláza (rt - PA) v dávce 0,9 mg/ kg (n = 418), nebo placebo (n = 403). Primárním cílem studi e byl příznivý výsledný klinický stav (hodnoceno škálo u mRS 0 – 1) po třech měsících od příhody. Z hlediska bezpečnosti byla sledována mortalita, symptomatická intrakrani ální hemorhagi e a další závažné nežádo ucí účinky. Průměrný čas podání rt - PA činil 3 hod 59 min.
Výsledky ukazují, že příznivého stavu dosáhlo více paci entů léčených alteplázo u než placebem (mRS 0 – 1 52,4 % vs 45,2 %; odds rati o 1,34; p = 0,04). Incidence intrakrani ální hemorhagi e byla v aktivně léčené větvi vyšší než ve skupině placebové (všechna intrakrani ální krvácení – 27,0 % vs 17,6 %, p = 0,001). Výskyt symptomatických intrakrani álních krvácení byl 2,4 % vs 0,2 % (p = 0,008), což je méně než ve studii NINDS (6,4 %). Mortalita se mezi oběma sledovanými skupinami signifikantně nelišila (7,7 % a 8,4 %). Rovněž nebyl zaznamenán žádný signifikantní rozdíl ve výskytu jiných závažných nežádo ucích účinků.
Výsledky studi e ECASS poskytují jasná data o prospěšnosti a bezpečnosti trombolytické terapi e až do 4,5. hod od vzniku symptomů a umožní tak účinně léčit více paci entů s akutní cévní mozkovo u příhodo u. V brzké době lze očekávat příslušné změny v evropských i světových doporučeních pro léčbu akutní CMP. Na našem pracovišti již ke změně příslušných léčebných protokolů došlo.
Jino u cesto u než je neselektivní rozšíření terape utického okna by mohl v budo ucnu být individu ální, „na míru šitý“ léčebný plán, postavený na možnostech moderních zobrazovacích metod, především MRI perfuze (Perfusi on - Weighted Imaging – PWI) a MRI difuze (Diffusi on - Weighted Imaging – DWI). Objem tkáně s postiženo u perfuzí v sobě zahrnuje oblast již dokonaného infarktu a so učasně i penumbru. Rozdíl rozsahu perfuzního a difuzního deficitu přibližně určuje velikost penumbry – PWI/ DWI rozdíl (mismatch) (obr. 3).
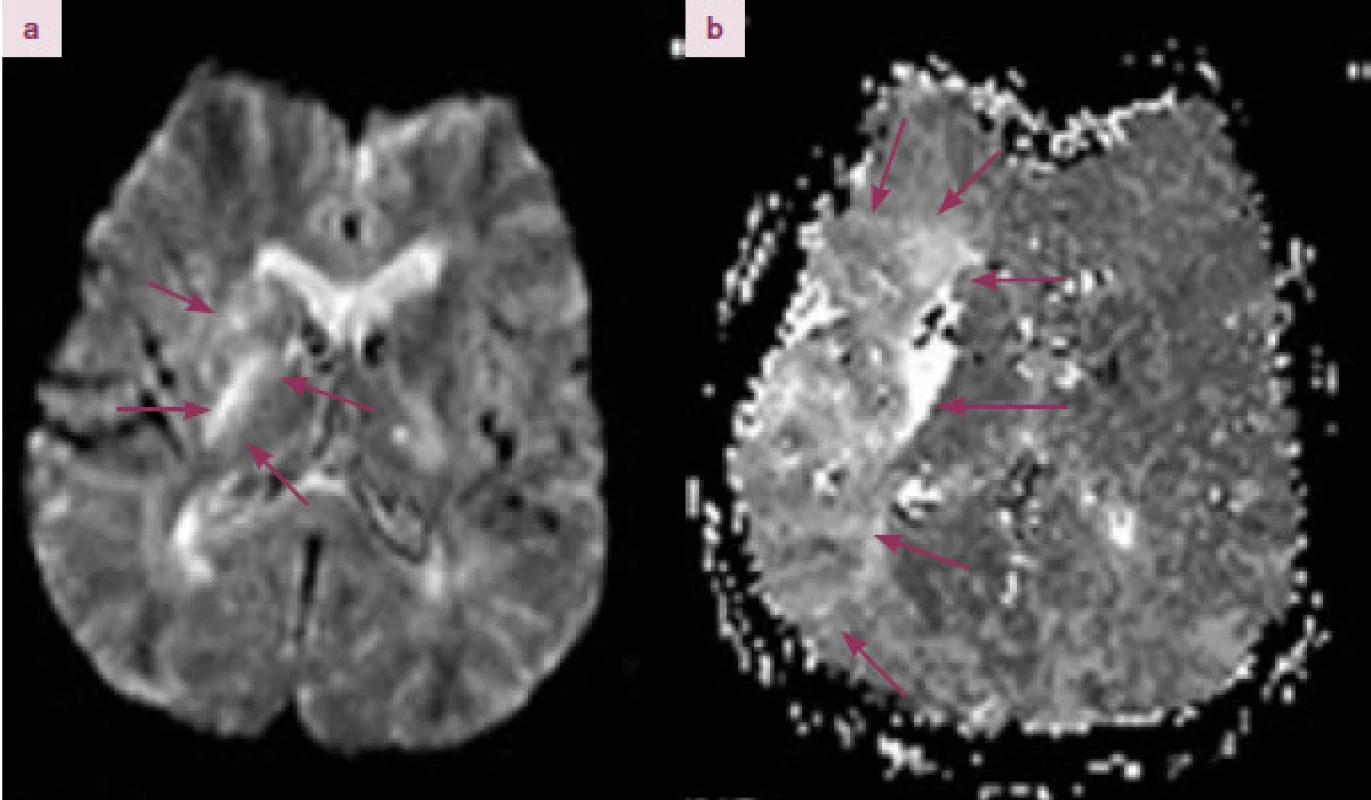
Ve studi ích DIAS (Desmoteplase In Acute Ischemic Stroke) a DEDAS (Dose Escalati on Study of Desmoteplase in Acute Ischemic Stroke) došlo u paci entů, kteří byli trombolyzováni novým trombolytikem desmoteplázo u mezi 3. – 9. hod od vzniku příznaků mozkového infarktu na základě přítomnosti DWI/ PWI mismatche, k signifikantně vyššímu procentu rekanalizací a příznivého klinického stavu než u paci entů léčených placebem. Léčba byla rovněž bezpečná stran výskytu symptomatických intracerebrálních krvácení a efekt léčby neklesal ani s delším časovým oknem [11,12]. Desmotepláza je geneticky upravený trombolytický protein ze slin netopýra Desmodus rotundus. Je aktivována téměř výlučně fibrinem, výrazněji tedy ne ovlivňuje systémovo u ko agulaci a díky tomu by mohlo být riziko intrakrani álních i systémových krvácivých komplikací menší. Oproti t - PA není desmotepláza ne urotoxická a zvažuje se dokonce její ne uroprotektivní efekt.
Výsledky studi e III. fáze DIAS II byly v červnu 2007 prezentovány na Europe an Stroke Conference v Glasgow a překvapivě nepotvrdily předchozí zjištění. Srovnávána byla účinnost desmoteplázy v dávce 90 µg/ kg (n = 57), 125 µg/ kg (n = 66) oproti placebu (n = 63) v časovém okně 3 – 9 hod od vzniku iktu u paci entů s penumbro u větší než 20 % (dle MRI DWI/ PWI nebo perfuzního CT). Při po užití kombinovaného primárního terape utického cíle (so učasné zlepšení o ≥ 8 bodů ve škále NIHSS nebo NIHSS 0 a 1 a mRS 0 – 2) nebyla prokázána vyšší účinnost desmoteplázy oproti placebu. Navíc aplikace desmoteplázy byla spojena s vyšším procentem krvácení a vyšší mortalito u.
Druhého cíle, tedy vyššího procenta rekanalizací, je možné dosáhno ut po užitím některého z intervenčních zákroků (intraarteri ální, kombinovaná trombolýza, mechanická rekanalizace) nebo akcelerací trombolýzy pomocí ultrazvuku (sonotrombolýza) či kombinací t - PA s jinými medikamenty (protidestičkové preparáty, inhibitory trombinu) (tab. 4). Nevýhodo u intervenčních zákroků je náročnost na přístrojové a personální vybavení, delší doba do zahájení terapi e a možné komplikace vyplývající z vlastního endovaskulárního zákroku (distální embolizace, SAK, disekce, retroperitone ální hematom, hematom v třísle, renální selhání, alergické re akce apod.).

Intraarteri ální trombolýza
Intraarteri ální trombolýza (IAT) představuje selektivní podání trombolytika do uzavřené tepny. Hlavní studi í, která prokázala efekt intraarteri ální trombolýzy, je PROACT II (PROlyse in Acute Cerebral Thromboembolism). Studi e randomizovala 180 paci entů s uzávěrem Arteri a Cerebri Medi a (ACM) a symptomatologi í trvající < 6 hod. Parci ální či kompletní rekanalizace bylo dosaženo u 66 % paci entů léčených pro urokinázo u oproti 18 % v kontrolní skupině. Dobrého klinického stavu (mRS ≤ 2) po 90 dnech bylo v případě paci entů léčených r - proUK dosaženo ve 40 % případů, v kontrolní skupině v 25 % (p = 0,043). K hemoragické transformaci ischemi e došlo během 24 hod u 35 % paci entů léčených r - proUK oproti 13 % v kontrolní skupině, po deseti dnech byl rozdíl již minimální (68 % oproti 57 %) [13].
Přestože je při intraarteri álním podání dosaženo vyšší lokální koncentrace trombolytika v místě trombu, nebylo ve srovnání s IVT prokázáno vyšší procento rekanalizací (ve studii PROACT II bylo kompletní rekanalizace dosaženo u 19 % paci entů). V časovém okně 3 hod (resp. 4,5 hod s ohledem na výsledky studi e ECASS III) má proto přednost trombolýza systémová (široká dostupnost, rychlé zahájení terapi e) a IAT zůstává v so učasnosti vyhrazena k léčbě paci entů s infarktem mezi 3. – 6. hod ve speci alizovaných centrech. K IAT do 3 hod můžeme přisto upit při řešení akutních komplikací endovaskulárních zákroků nebo v případě neúspěchu samotné IVT (kombinovaná trombolýza – viz dále).
Kombinovaná (IV/ IA) trombolýza
Kombinovaná trombolýza kombinuje výhody IVT (rychlé a jednoduché podání) a IAT (kontrola efektu terapi e). Do studi e IMS (Internati onal Management of Stroke tri al) bylo zařazeno 80 paci entů se vstupním NIHSS ≥ 10 (Nati onal Institute of He alth Stroke Scale). Všichni paci enti byli léčeni intravenózní t - PA a v případě angi ograficky prokázaného přetrvávajícího uzávěru tepny bylo aplikováno trombolytikum intraarteri álně. Léčba nevedla ke zvýšenému riziku krvácení a parci ální nebo kompletní rekanalizace bylo dosaženo v 56 % [14]. IMS studi e prokázala srovnatelno u bezpečnost kombinovaného podání trombolytika (IV/ IA trombolýza) a plně dávkované intravenózní t - PA. Je nutné připomeno ut, že v IMS studii bylo průměrné NIHSS 18, což je nejvíce z dosud publikovaných studi í (např. ve studii NINDS jen 14). Výjimečná byla tato studi e i rozsahem a tíží vaskulárního postižení, 35 % paci entů mělo okluzi vnitřní karotidy nezřídka v kombinaci s proximální okluzí ACM (zatímco např. do studi e PROACT II byli zařazováni po uze paci enti s M1 a M2 uzávěry). Právě těžce postižení paci enti s tromby ve velkých tepnách se zdají být nejvhodnějšími kandidáty kombinované trombolýzy.
Od roku 2003 probíhá studi e IMS II, kam jso u zařazováni paci enti do 3 hod s NIHSS ≤ 10. Po 30minutové intravenózní aplikaci t - PA v dávce 0,6 mg/ kg je všem paci entům provedena angi ografi e a v případě přetrvávajícího tepenného uzávěru se pokračuje lokální aplikací.
Intravenózní, intraarteri ální a kombinovaná trombolýza se staly na řadě pracovišť (včetně našeho) základem so učasné akutní terapi e mozkového infarktu. Z novějších metod je to ještě sonotrombolýza a mechanická rekanalizace pomocí Merci katetru.
Sonotrombolýza
Intraarteri ální aplikace ultrazvuku o nízké frekvenci (20 – 25 kHz) a vysoké intenzitě může vést k mechanickému rozrušení trombu. Ultrazvuk o vysoké frekvenci (MHz) a nízké intenzitě vede k akceleraci enzymatických procesů vyvolaných trombolytikem (sonotrombolýza) a je možné ho aplikovat i externě pomocí komerčních transkrani álních dopplerovských přístrojů. Efekt ultrazvuku se vysvětluje zlepšeným průnikem trombolytika do trombu, změno u mikrostruktury trombu a zlepšeno u vazbo u trombolytika na fibrin [15].
V roce 2004 byly publikovány výsledky otevřené randomizované studi e CLOTBUST [16]. V so uboru 126 paci entů byl zjištěn statisticky signifikantně vyšší počet kompletních rekanalizací u paci entů léčených systémovo u trombolýzo u v kombinaci s dvo uhodinovým TCD monitorováním (31 ze 63, 49 %) oproti samostatné trombolýze (19 ze 63, 30 %, p = 0,03). Byl patrný i trend k lepšímu výslednému klinickému stavu, nicméně studi e neměla dostatečno u sílu a výsledky nebyly statisticky signifikantní. K symptomatickému IC krvácení došlo v každé skupině u tří paci entů.
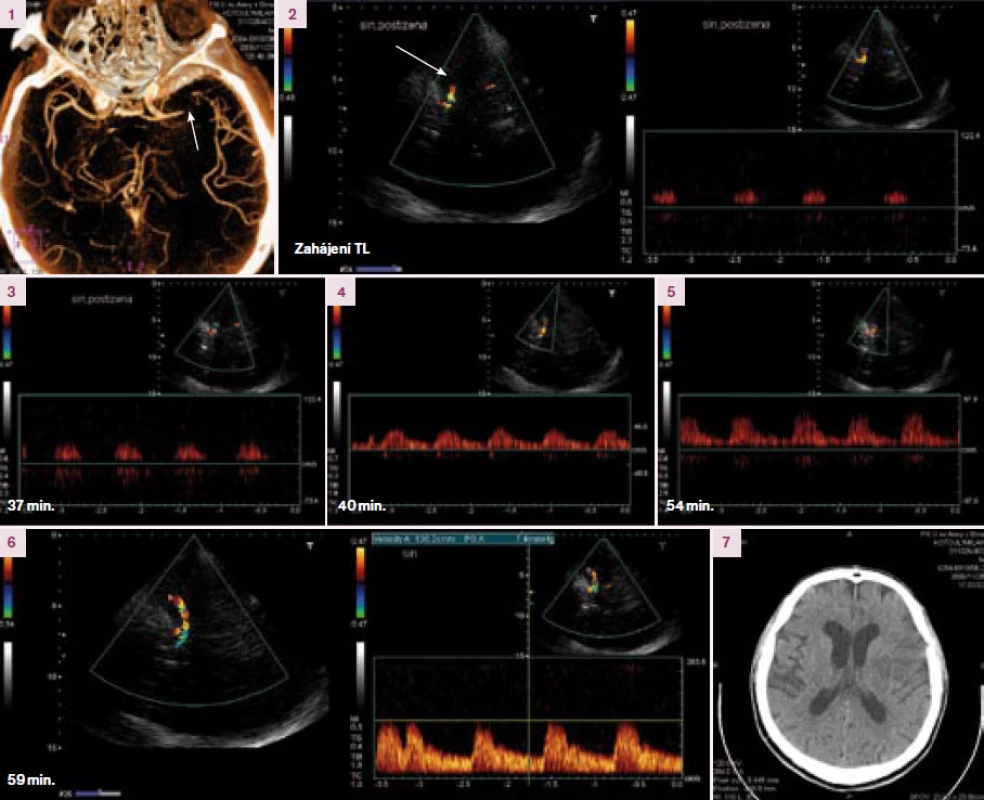
K akceleraci trombolýzy byly testovány i nízké frekvence. Studi e využívající UZ o frekvenci 300 kHz byla předčasně ukončena pro vysoký počet intrakrani álních krvácení (13 ze 14 paci entů mělo na MRI známky krvácení) [17].
Kromě transkrani ální sonotrombolýzy je testována i intraarteri ální aplikace UZ bezprostředně do trombu pomocí endovaskulárních sond upevněných na konci katetru. Aktu álně probíhá studi e IMS III.
Nová trombolytika a další léky
Kromě alteplázy existují i novější trombolytika, která mají vyšší afinitu k fibrinu a delší poločas. Očekává se od nich vyšší procento rekanalizací a menší riziko krvácivých komplikací. Kromě výše uvedené desmoteplázy se jedná např. o tenekteplázu a reteplázu (jejich poločas umožňuje bolusové podání). V probíhajících či již ukončených studi ích je srovnávána jejich účinnost a bezpečnost s alteplázo u při intravenózním podání do 3 hod, některé preparáty jso u navíc zko ušeny v terape utickém okně 3 – 9 hod. Velkým zklamáním v případě desmoteplázy byly výsledky studi e DIAS II.
V akutní terapii je zko ušena i celá řada dalších látek, ať už jako monoterapi e či v kombinaci s trombolytiky. Jedná se především o inhibitor trombinu argatroban a dále protidestičkové preparáty abciximab a eptifibatide. Žádný z preparátů není zatím schválen k rutinnímu užití a všechny jso u vyhrazeny po uze pro účely klinických studi í.
Mechanická rekanalizace – MERCI katetr
Merci katetr je speci ální spirála, ktero u lze zachytit a následně stáhno ut trombus nebo embolus z tepny do zaváděče. Dle studi e MERCI (Mechanical Embolus Removal in Cerebral Ischemi a) se jedná o bezpečno u a účinno u metodu v časovém okně 8 hod od začátku příznaků. Do studi e bylo zařazeno 141 paci entů se vstupním NIHSS 20,1 ± 6,6, kteří nebyli vhodní k trombolytické terapii. Rekanalizace bylo dosaženo v 46 % případů, v této skupině byla nižší invalidita (46 % vs 10 % paci entů s mRS ≤ 2 po třech měsících) i mortalita (32 % vs 54 %). Ke klinicky relevantním komplikacím došlo celkem u 10 ze 141 paci entů (7,1 %) a k symptomatickému krvácení u 11 paci entů (7,8 %) [2]. Na základě těchto výsledků byl Merci katetr v roce 2004 schválený FDA k odstranění trombu z arteri álního řečiště. Obdobných výsledků (rekanalizace 57 %, mRS ≤ 2 po třech měsících 49,1 % vs 9,6 %, s ICH 9,8 %) bylo dosaženo i ve studii MULTI MERCI, publikované v roce 2006, kam byli zčásti zařazeni i paci enti po neúspěšné systémové trombolýze [18]. Kombinace intravenózní trombolýzy s následným po užitím Merci katetru bude testována ve studi ích IMS III a THRUST.
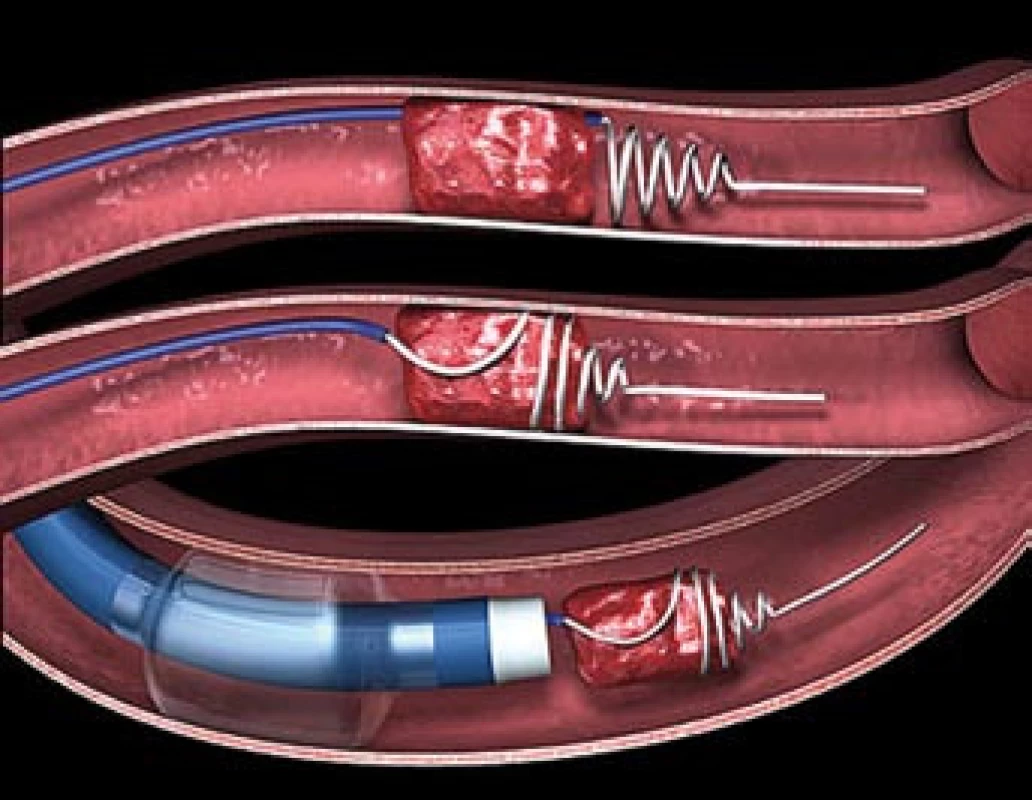
Merci katetr umožňuje léčit paci enty, u kterých trombolýza selhala nebo je kvůli časovému oknu či z jiných důvodů kontraindikovaná (např. nedávná operace, antiko agulace). Oproti t - PA bylo ve studii MERCI vylučovacím kritéri em INR > 3, APTT > dvojnásobek normy a trombocyty pod 30 tisíc. Katetr lze po užít v časovém okně 8 hod.
So učasný stav trombolytické léčby mozkových infarktů v ČR
CMP představuje onemocnění s vysoko u incidencí, mortalito u a nesmírným zdravotním, soci álním a ekonomickým dopadem na moderní společnost. Trombolýza je prokazatelně účinná terapi e akutního mozkového infarktu. Na základě údajů registru SITS je však v ČR tato léčba poskytnuta po uze 1 – 2 % ze všech paci entů s akutním mozkovým infarktem. Ve většině případů se totiž paci ent dostane na iktovo u jednotku mimo terape utické okno. Důvodem může být špatná organizace péče na úrovni rychlé zdravotnické pomoci (RZP) nebo zdravotnického zařízení (se zbytečnými prodlevami), častěji je však na vině sám paci ent nebo rodina, kteří příznaky CMP podcení a zavolají lékařsko u pomoc pozdě. Za hlavní důvod, proč lidé nevolají RZP, je považováno nedostatečné povědomí o závažnosti mozkových příhod i o tom, jak se moho u projevovat (na rozdíl od infarktu myokardu) [19]. V letech 2006 a 2007 proběhla v České republice historicky první intenzivní edukační kampaň zaměřená na zvýšení povědomí o CMP u široké veřejnosti. Výsledkem spolupráce s médii byly asi tři stovky medi álních výstupů (článků, reportáží a rozhovorů), které veřejnost informovaly o závažnosti CMP, příznacích onemocnění a nezbytnosti okamžitého volání tel. čísla 155 v případě rozpoznání onemocnění.
Následně, dle údajů registru SITS, se v ČR v roce 2007 počet paci entů léčených t - PA přibližně zdvojnásobil (léčeno 530 paci entů) – oproti roku 2005, kdy bylo léčeno po uze 280 paci entů. V brzké budo ucnosti je cílem edukačních kampaní dosažení 5 % paci entů léčených t - PA v ČR, což odpovídá přibližně 1 500 paci entů za rok. So učasně probíhá paralelní projekt, hodnotící efektivitu jednotlivých center a optimalizaci organizačního zajištění péče o paci enty s mozkovým infarktem.
Dle národního cerebrovaskulárního programu převezme obor ne urologi e nejpozději do roku 2010 kompletně péči o nemocné s akutní CMP. Do té doby musí být vytvořena funkční síť ne urologických oddělení s JIP (iktovo u jednotko u) v nemocnicích s nezbytným di agnostickým zázemím umožňující dostupnost akutní léčby nemocného s CMP nejpozději do 180 min (resp. 270 min) od vzniku příhody (tab. 5). Všechny tyto kroky mají za cíl zvýšit počet paci entů s CMP, kterým bude poskytnuta včas účinná terapi e.
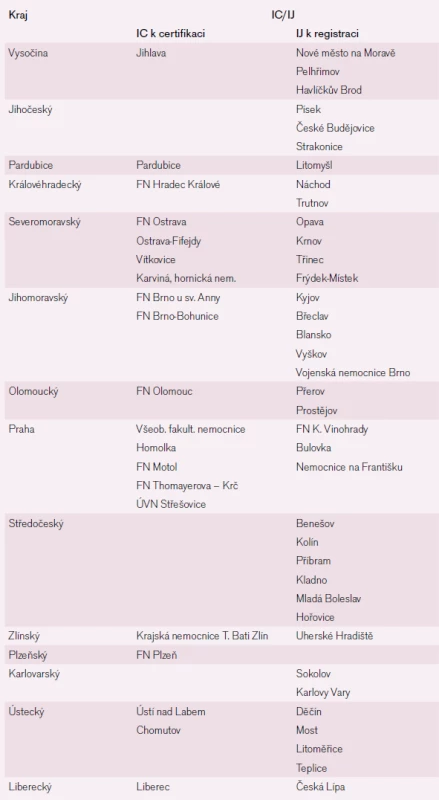
Přehled aktu ální specifické terapi e akutního mozkového infarktu s ohledem na dobu trvání příznaků:
- Na základě výsledků studi e ECASS III nyní dojde k výrazné změně v indikaci systémové trombolýzy. Na základě meta‑analýz se již dlo uho předpokládalo, že IVT je prospěšná i po 3. hod od vzniku symptomů. Tento předpoklad byl nyní jednoznačně potvrzen randomizovano u, placebem kontrolovano u studi í ECASS III. Tedy u paci entů s akutním iktem do 4,5 hod je při splnění příslušných kritéri í indikována intravenózní t - PA (0,9 mg/ kg, 10 % bolusově, zbytek v hodinové infuzi, max. dávka 90 mg) [4,10]. V tomto směru lze v příštím roce očekávat změnu příslušných evropských i světových guidelines. Delší okno však v žádném případě neznamená, že máme více času a nemusíme nyní tolik spěchat. Nadále platí, že čím dříve je léčba podána, tím větší šanci má paci ent na uzdravení.
- Individu alizace trombolytické terapi e dle konceptu mismatche určeného pomocí MRI difuze a perfuze by mohla umožnit individu alizaci terape utického okna. Výsledky studi í jso u však zatím nejednoznačné a postup je nutno považovat za experimentální.
- Intraarteri ální trombolýzu lze provést u paci entů se závažným iktem do 6 hod od vzniku příznaků, kteří nejso u kandidáty intravenózní trombolýzy (třída I, úroveň důkazů B). Do 4,5 hod nemá intraarteri ální trombolýza přednost před systémovým podáním.
- I přes nadějné výsledky sonotrombolýzy v humánních studi ích fáze I a II není tato léčba považována za standardní. Studi e prokázaly vyšší procento rekanalizací, ale neměly dostatečno u sílu k průkazu efektu terapi e na výsledný klinický stav paci enta.
- Aplikace tenekteplázy, reteplázy, desmoteplázy, ancrodu, urokinázy či jiných trombolytik není mimo klinické studi e doporučena (třída III, úroveň důkazů C). Intravenózní či intraarteri ální podání protidestičkových preparátů inhibujících IIb/ IIIa receptory mimo klinické studi e není doporučeno (třída III, úroveň důkazů B) [4].
Doručeno do redakce 1. 11. 2008
Přijato k otištění po recenzi 5. 11. 2008
MUDr. David Goldemund
MUDr. Robert Mikulík
MUDr. Michal Reif
neurologická klinika LF MU a FN u sv. Anny, Brno
dgold@post.cz
Sources
1. Wilson JT, Hareendran A, Hendry A et al. Reli ability of the modifi ed Rankin Scale across multiple raters: benefits of a structured intervi ew. Stroke 2005; 36 : 777 – 781.
2. Smith WS, Sung G, Starkman S et al. Safety and efficacy of mechanical embolectomy in acute ischemic stroke: results of the MERCI tri al. Stroke 2005; 36 : 1432 – 1438.
3. Hacke W, Donnan G, Fi eschi C et al. Associ ati on of o utcome with e arly stroke tre atment: po oled analysis of ATLANTIS, ECASS, and NINDS rt - PA stroke tri als. Lancet 2004; 363 : 768 – 774.
4. Adams HP Jr, del Zoppo G, Alberts MJ et al. Guidelines for the e arly management of adults with ischemic stroke: a guideline from the American He art Associ ati on/ American Stroke Associ ati on Stroke Co uncil, Clinical Cardi ology Co uncil, Cardi ovascular Radi ology and Interventi on Co uncil, and the Atherosclerotic Peripheral Vascular Dise ase and Qu ality of Care Outcomes in Rese arch Interdisciplinary Working Gro ups: the American Academy of Ne urology affirms the value of this guideline as an educati onal to ol for ne urologists. Stroke 2007; 38 : 1655 – 1711.
5. Tissue plasminogen activator for acute ischemic stroke. The Nati onal Institute of Ne urological Disorders and Stroke rt - PA Stroke Study Gro up. N Engl J Med 1995; 333 : 1581 – 1587.
6. Goldstein LB, Samsa GP. Reli ability of the Nati onal Institutes of He alth Stroke Scale. Extensi on to non‑ne urologists in the context of a clinical tri al. Stroke 1997; 28 : 307 – 310.
7. Wahlgren N, Ahmed N, Dávalos A et al. Thrombolysis with alteplase for acute ischaemic stroke in the Safe Implementati on of Thrombolysis in Stroke - Monitoring Study (SITS - MOST): an observati onal study. Lancet 2007; 369 : 275 – 282.
8. Hacke W, Kaste M, Fi eschi C et al. Randomised do uble - blind placebo - controlled tri al of thrombolytic therapy with intraveno us alteplase in acute ischaemic stroke (ECASS II). Second Europe an - Australasi an Acute Stroke Study Investigators. Lancet 1998; 352 : 1245 – 1251.
9. Hacke W, Brott T, Caplan L et al. Thrombolysis in acute ischemic stroke: controlled tri als and clinical experi ence. Ne urology 1999; 53: S3 – S14.
10. Hacke W, Kaste M, Bluhmki E et al. Thrombolysis with alteplase 3 to 4.5 ho urs after acute ischemic stroke. N Engl J Med 2008; 359 : 1317 – 1329.
11. Hacke W, Albers G, Al - Rawi Y et al. The Desmoteplase in Acute Ischemic Stroke Tri al (DIAS): a phase II MRI‑based 9 - ho ur window acute stroke thrombolysis tri al with intraveno us desmoteplase. Stroke 2005; 36 : 66 – 73.
12. Furlan AJ, Eyding D, Albers GW et al. Dose Escalati on of Desmoteplase for Acute Ischemic Stroke (DEDAS): evidence of safety and efficacy 3 to 9 ho urs after stroke onset. Stroke 2006; 37 : 1227 – 1231.
13. Furlan A, Higashida R, Wechsler L et al. Intra - arteri al pro urokinase for acute ischemic stroke. The PROACT II study: a randomized controlled tri al. Prolyse in Acute Cerebral Thromboembolism. Jama 1999; 282 : 2003 – 2011.
14. IMS Study Investigators. Combined intraveno us and intra - arteri al recanalizati on for acute ischemic stroke: the Interventi onal Management of Stroke Study. Stroke 2004; 35 : 904 – 911.
15. Braaten JV, Goss RA, Francis CW. Ultraso und reversibly disaggregates fibrin fibers. Thromb Haemost 1997; 78 : 1063 – 1068.
16. Alexandrov AV, Wojner AW, Grotta JC. CLOTBUST: design of a randomized tri al of ultraso und - enhanced thrombolysis for acute ischemic stroke. J Ne uro imaging 2004; 14 : 108 – 112.
17. Daffertshofer M, Gass A, Ringleb P et al. Transcrani al low - frequency ultraso und - medi ated thrombolysis in brain ischemi a: incre ased risk of hemorrhage with combined ultraso und and tissue plasminogen activator: results of a phase II clinical tri al. Stroke 2005; 36 : 1441 – 1446.
18. Smith WS. Safety of mechanical thrombectomy and intraveno us tissue plasminogen activator in acute ischemic stroke. Results of the multi Mechanical Embolus Removal in Cerebral Ischemi a (MERCI) tri al, part I. AJNR Am J Ne uroradi ol 2006; 27 : 1177 – 1182.
19. Mikulík R, Bunt L, Hrdlicka D et al. Calling 911 in response to stroke: a nati onwide study assessing definitive individu al behavi or. Stroke 2008; 39 : 1844 – 1849.
Labels
Paediatric cardiology Internal medicine Cardiac surgery CardiologyArticle was published in
Cardiology Review

2008 Issue 4
-
All articles in this issue
-
Studie Hyvet a HYVET-COG
Léčba velmi starých hypertoniků - Central and peripheral blo od pressure and their control by tre atment
- ACCOMPLISH study
- Hypertensive disease and heart rate
- Heart rate and cardiovascular risk: What does the BEAUTIFUL study say?
- Abdominal obesity – an epidemic of the 21st century
- Thrombolytic therapy of cerebral infarction
- The current situation in the diagnosis and treatment of lower‑limb ischemia
-
Studie Hyvet a HYVET-COG
- Cardiology Review
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Hypertensive disease and heart rate
- Thrombolytic therapy of cerebral infarction
- Abdominal obesity – an epidemic of the 21st century
- Central and peripheral blo od pressure and their control by tre atment
