Klinicky významné lékové interakce antiretrovirotik
Clinically significant drug interactions of antiretrovirals
Evaluating of the clinical significance of drug interactions is one of the domains of clinical pharmacist expertise. Drug interactions are discussed when two or more drugs co-administer and the effect of one of them changes. Drug interactions can be a serious cause of toxicity and side effects. They can also lead to the failure of the treatment. On the other hand, they can also play a positive role, e. g. in the treatment of people living with HIV. The combination of some antiretrovirals with boosters is based on the principle of drug interaction.
The article presents pharmacokinetic drug interactions of antiretrovirals. Their occurrence is not unique in the clinical practice. The pharmacokinetic profiles of the individual antiretrovirals, whose knowledge is essential for the correct assessment of the clinical significance of drug interactions, are reviewed.
Keywords:
clinical pharmacist – HIV – pharmacokinetics – Drug interactions – antiretrovirals
Authors:
Irena Murínová 1,2
Authors‘ workplace:
Oddělení klinické farmacie, Ústřední vojenská nemocnice – Vojenská fakultní nemocnice, Praha
1; Ústav aplikované farmacie, Farmaceutická fakulta VFU, Brno
2
Published in:
Čas. Lék. čes. 2019; 158: 289-294
Category:
Review Article
Overview
Vyhodnocování klinické významnosti lékových interakcí je jednou z domén odbornosti klinického farmaceuta. O lékových interakcích hovoříme, pokud při současném podávání dvou či více léčiv dojde ke změně účinku některého z nich. Lékové interakce mohou být závažnou příčinou toxicity a nežádoucích účinků léčiv. Mohou vést i k selhání terapie. Na druhé straně mohou hrát i pozitivní úlohu, například v léčbě lidí infikovaných HIV. Na principu lékové interakce je postavena kombinace některých antiretrovirotik s boostery.
Článek prezentuje farmakokinetické lékové interakce antiretrovirotik. Jejich výskyt není v klinické praxi ojedinělý. V textu jsou přehledně rozebrány farmakokinetické profily jednotlivých antiretrovirotik, jejichž znalost je esenciální pro správné posouzení klinické významnosti lékové interakce.
Klíčová slova:
HIV – lékové interakce – farmakokinetika – antiretrovirotika – klinický farmaceut
ÚVOD
Pokud při současném podávání dvou nebo více léčiv dojde ke změně účinku některého z nich, hovoříme o lékové interakci (LINT). Výsledkem může být účinek synergický, antagonistický nebo kvalitativně změněný (1). LINT mohou být závažnou příčinou toxicity a nežádoucích účinků léčiv. Mohou vést až k selhání léčby.
Problematika LINT antiretrovirotik (AR) je rozsáhlé a nepříliš jednoduché téma. Některé skupiny AR mají vysoký interakční potenciál. Jelikož se moderní léčba pacientů infikovaných HIV opírá o použití kombinovaných léčivých přípravků, které obsahují 2–3 účinné látky, popřípadě ještě nezbytnou pomocnou složku (booster), je vhodné na výskyt LINT pomýšlet již při vzájemném kombinování AR a při sestavování individuálního léčebného režimu. Navíc stárnutím může řadě lidí žijících s HIV (PLWH – people living with HIV) do portfolia užívaných léčiv přibývat i medikace z jiných farmakoterapeutických skupin s potenciálem pro další výskyt LINT. PLWH mohou procházet i specifickými situacemi, jež se vážou na jejich základní onemocnění. Mohou tak ke své bazální antiretrovirové medikaci užívat rovněž vysoce interakční léčiva, např. ze skupiny antituberkulotik, antimykotik, přímo působících antivirotik proti viru hepatitidy C, antiepileptik. Samostatnou problematikou je souběžné užívání návykových látek, neregistrovaných anabolických přípravků nebo různých potravních doplňků.
LINT může mít v medikaci i pozitivní úlohu. Na principu LINT je postavena kombinace některých AR s boostery (ritonaviru a kobicistatu).
Cílem článku není vytvořit dlouhý seznam všech potenciálních LINT AR, ale poukázat na základní principy, které je potřeba při vyhodnocování LINT reflektovat. Text je doplněn přehlednými tabulky s farmakokinetickými parametry AR.
TYPY LÉKOVÝCH INTERAKCÍ ANTIRETROVIROTIK
Podle mechanismu vzniku se obecně dělí LINT do tří skupin – farmaceutické (jedná se hlavně o farmaceutické nekompatibility), farmakodynamické a farmakokinetické. Farmakodynamické interakce probíhají většinou na receptorových systémech (případně v rámci signálních drah nacházejících se „za receptorem“ apod.). K farmakokinetickým interakcím může docházet na všech úrovních cest léčiva v lidském organismu (absorpci, distribuci, biotransformaci, eliminaci) (2).
FARMAKOKINETICKÉ LÉKOVÉ INTERAKCE ANTIRETROVIROTIK
Výskyt farmakokinetických LINT AR v klinické praxi není vzácný. Řada skupin AR, například nenukleosidové inhibitory reverzní transkriptázy (NNRTI) a inhibitory proteázy (PI), interaguje hojně.
Mezi hlavní mechanismy, na jejichž základě mohou AR v lidském organismu interagovat s jinými léčivy, patří absorpce z trávicího traktu a jaterní metabolismus.
Farmakokinetické interakce na úrovni absorpce z GIT zahrnují mimo jiné:
- Léčiva snižující pH GIT: Například atazanavir se nedoporučuje podávat současně s inhibitory H2 a inhibitory protonové pumpy (3).
- Léčiva a doplňky stravy obsahující polyvalentní kationty: Ty se mohou vázat na některá AR a snižovat jejich absorpci. Tento lékový problém se týká hlavně inhibitorů integrázy (INSTI). Je doporučováno užívat INSTI 2 hodiny před užitím léčiv obsahujících polyvalentní kationty nebo 6 hodin po něm. Jedná se o antacida, laxativa, Fe, Ca, Mg, Al, Zn, minerály, sukralfát, multivitaminy aj.
- Léčiva, která indukují či inhibují cytochrom P450 (CYP), konkrétně izoenzym CYP3A4, nebo transportní enzym glykoprotein P (P-gp) ve střevech.
Farmakokinetické interakce na úrovni jaterního metabolismu nastávají mimo jiné prostřednictvím:
- Enzymatického systému cytochromu 450: například NNRTI, PI.
- Enzymu uridindifosfát glukuronosyltransferázy (UGT): například INSTI.
Většina klinicky významných LINT AR je zprostředkována inhibicí či indukcí metabolismu jaterních enzymů. Inhibitory jaterních enzymů zpomalují odbourávání léčiva, a mohou tak způsobit jeho zvýšenou toxicitu. Na druhé straně urychlování metabolismu léčiva díky souběžnému podávání s induktory jaterních enzymů může vést k jeho suboptimálním hladinám v organimu a následně k zásadnímu snížení nebo až selhání očekávaného klinického efektu.
Mezi specifičtější mechanismy LINT AR patří například působení renálních transportérů.
Intracelulární koncentrace tenofoviru (TFV) v renálních tubulech může být modifikována léčivy, jež specificky inhibují transportéry MRP (multidrug resistant protein). Například NSAIDs, aciklovir či ganciklovir mohou inhibovat transportér MRP4, což může vést ke snížení clearance TFV, jeho cytoplazmatické akumulaci v epitelových tubulárních buňkách a k následnému rozvoji toxicity.
Jiný příklad se týká inhibitoru integrázy dolutegraviru (DTG) a metforminu. DTG inhibuje in vitro renální transportér organických kationtů 2 (OCT2 – organic cation transporter) a transportér vylučování léčiv a toxinů 1 (MATE1 – multidrug and toxic compound extrusion). In vivo tak může zvyšovat plazmatické koncentrace léčiv, u nichž je exkrece závislá na OCT2 či MATE1 (např. metforminu). Při současném podávání metforminu s DTG 50 mg 1× denně bylo pozorováno zvýšení AUC metforminu, které bylo vyjádřeno změnou geometrického průměru o 79 % a stejně tak navýšení Cmax, opět vyjádřené změnou geometrického průměru, o 66 %. Při současném podávání s DTG 50 mg 2× denně byl nárůst těchto farmakokinetických parametrů, při použití stejné statistické metody pro vyhodnocení, ještě vyšší – AUC metforminu o 145 %, Cmax o 111 % (4).
Při zahájení, změně dávky nebo ukončování podávání DTG spolu s metforminem je třeba zvážit úpravu dávky metforminu, aby se zachovala optimální kontrola hladin glykemie. S možností zvýšených plazmatických koncentrací metforminu souvisí i větší opatrnost při podávání DTG u pacientů se středně těžkou poruchou funkce ledvin a potenciálním rizikem rozvoje laktátové acidózy.
Výsledky studií naznačují, že v určitých klinických situacích můžeme očekávat obdobný lékový problém i při podávání nového INSTI biktegraviru s metforminem (4) (5).
Boostery
Úkolem boosterů AR přidávaných konkrétně k PI (v současných režimech k atazanaviru, darunaviru a lopinaviru) a INSTI (k elvitegraviru) je optimalizovat jejich farmakokinetické vlastnosti. Mezi boostery patří ritonavir (RTV) a kobicistat (COBI).
RTV je PI, který byl původně v plné terapeuticky účinné dávce (denní dávka činila 1200 mg per os) součástí kompletních antiretrovirových režimů. Pro řadu vedlejších nežádoucích účinků se v této indikaci a dávce již nepoužívá. Dnes se uplatňuje výhradně jako booster v malé denní dávce 200 mg, rozdělené zpravidla do 2 dávek.
COBI je k PI či INSTI přidáván v dávce 150 mg v dávkovacím intervalu 1× denně. Nevykazuje žádnou aktivitu vůči HIV.
RTV i COBI jsou silné inhibitory CYP3A. Inhibice metabolismu CYP3A zprostředkovaného RTV či COBI zvyšuje systémovou expozici substrátů CYP3A. Mezi substráty CYP3A patří právě PI a některé INSTI.
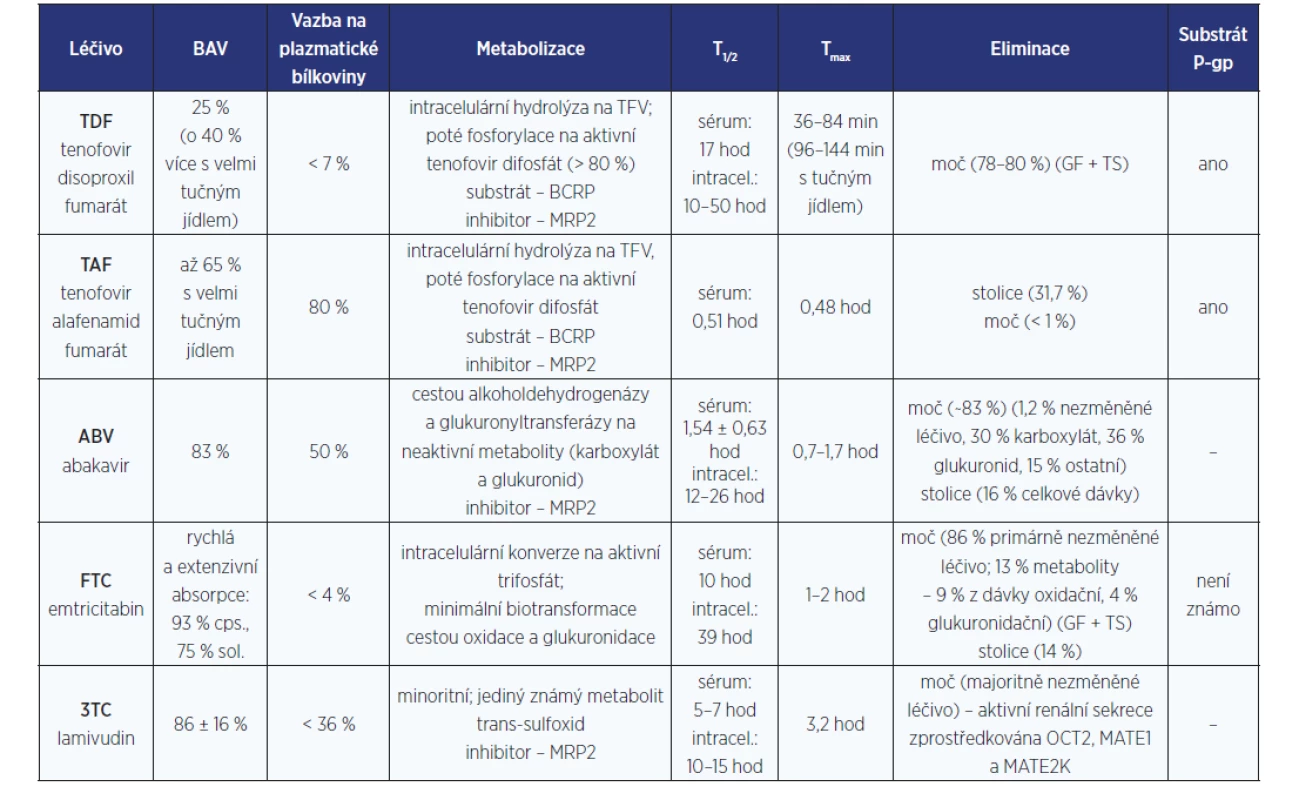
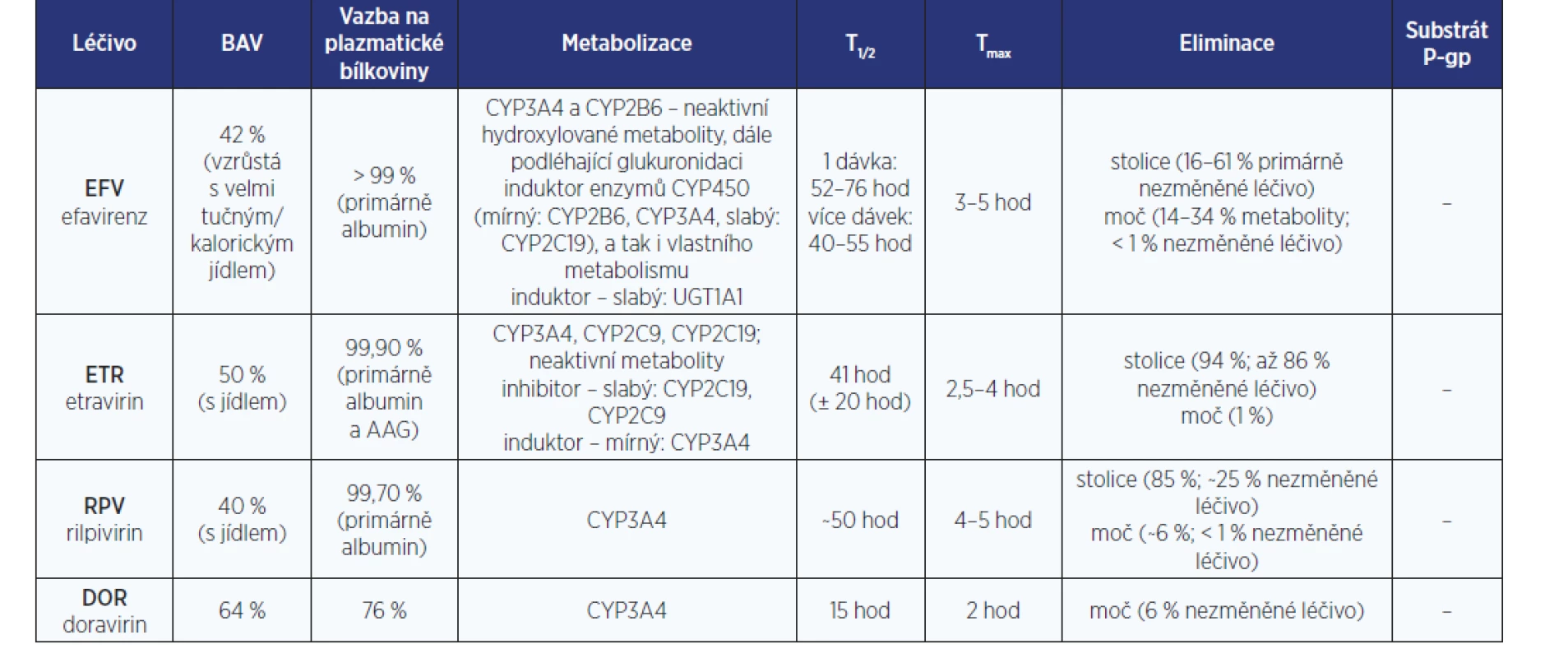
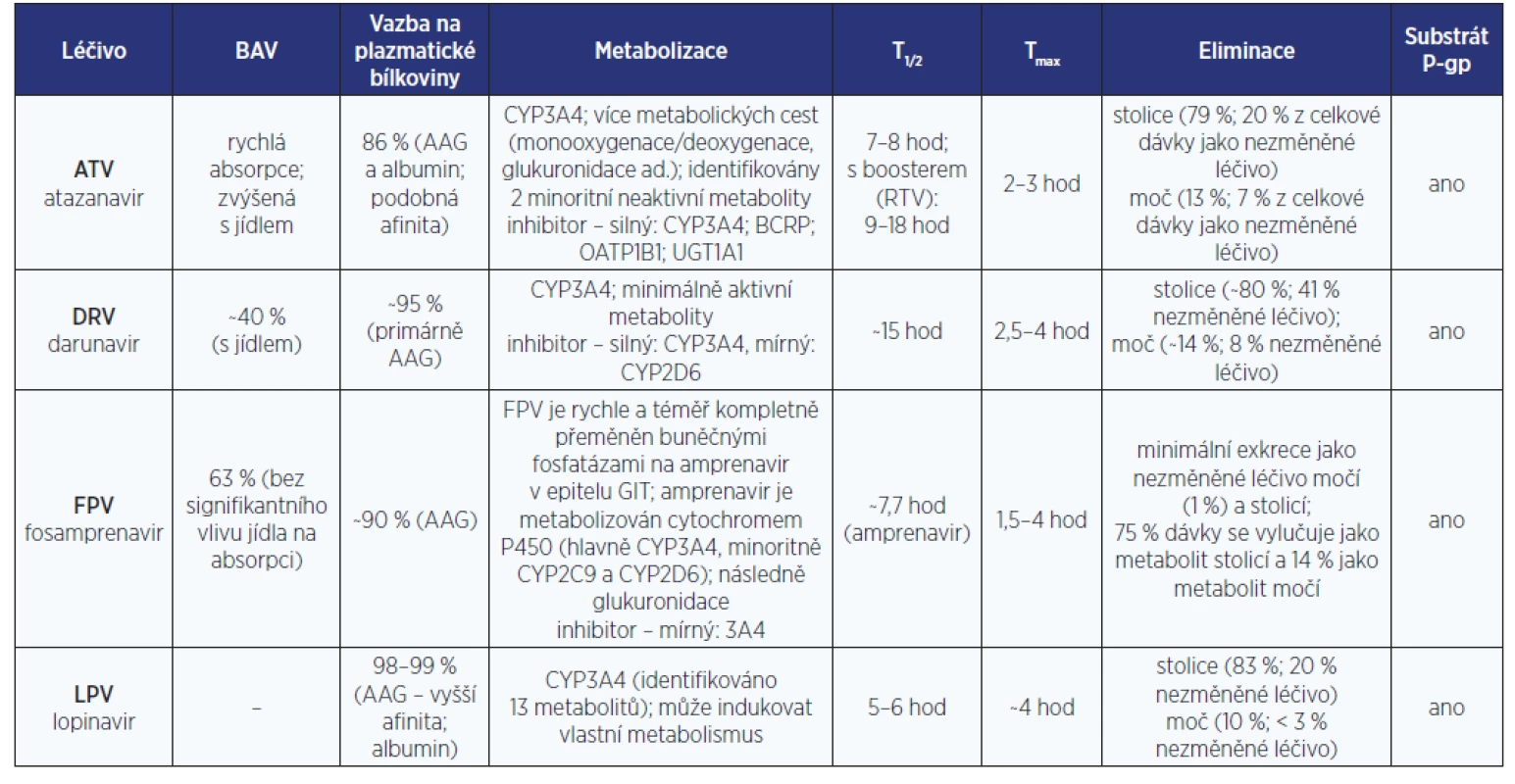
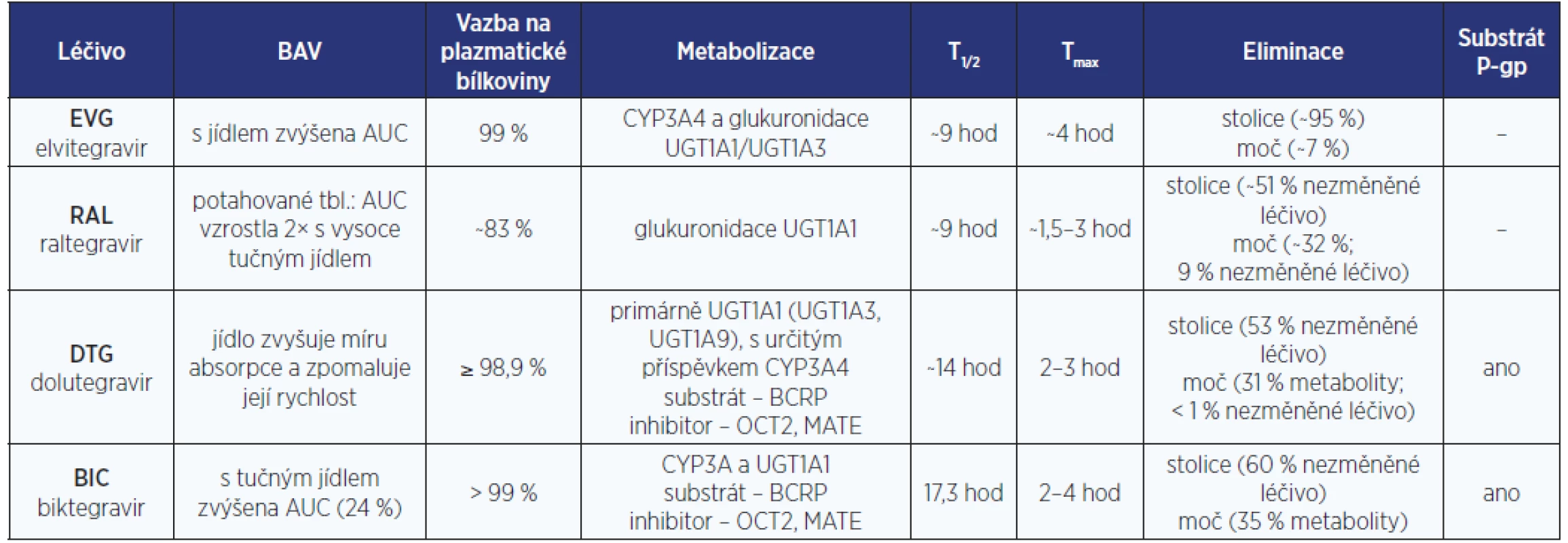
Tabulky s farmakokinetickými parametry antiretrovirotik
Pro hodnocení LINT je zásadní zorientovat se v množství farmakologických dat (nejen) o AR.
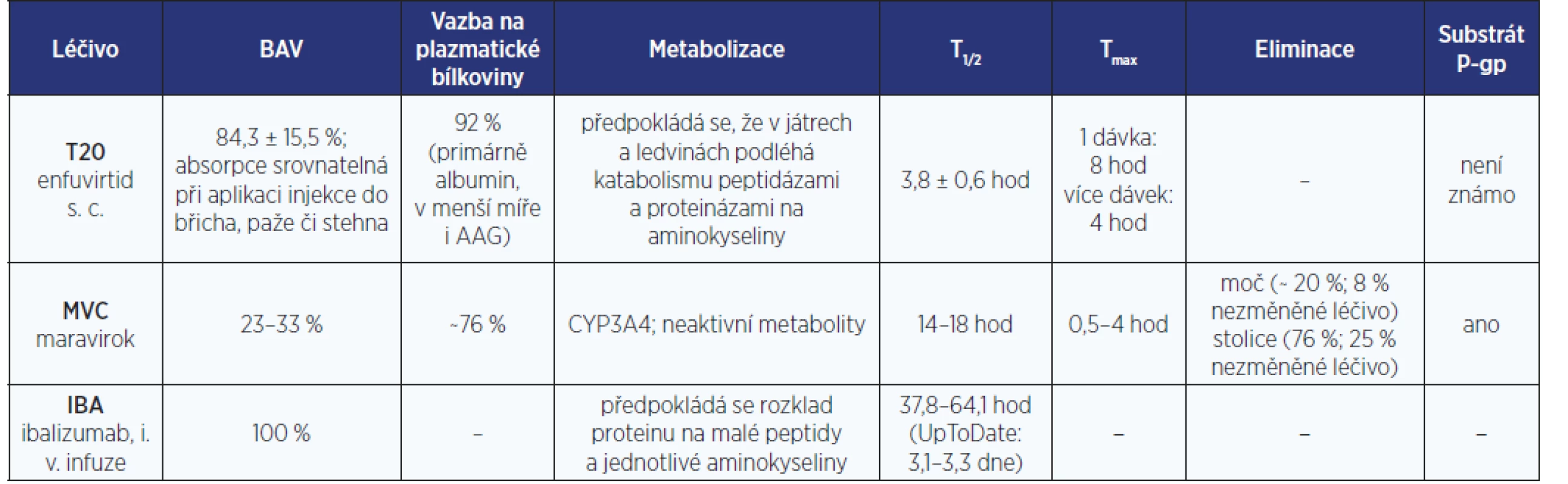
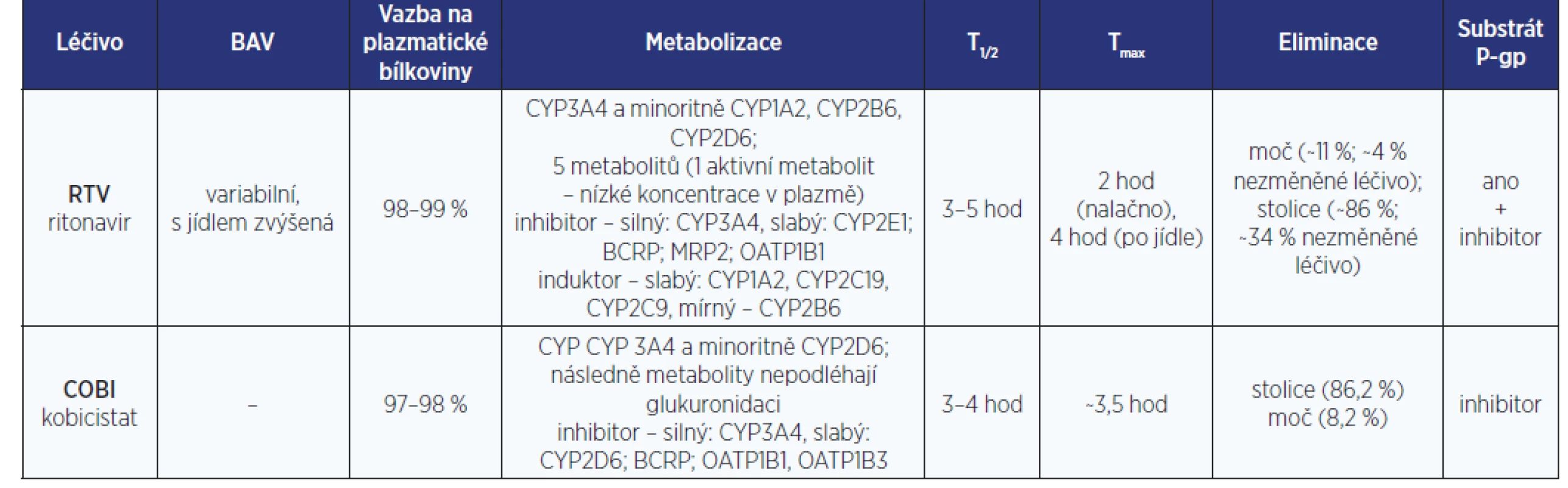
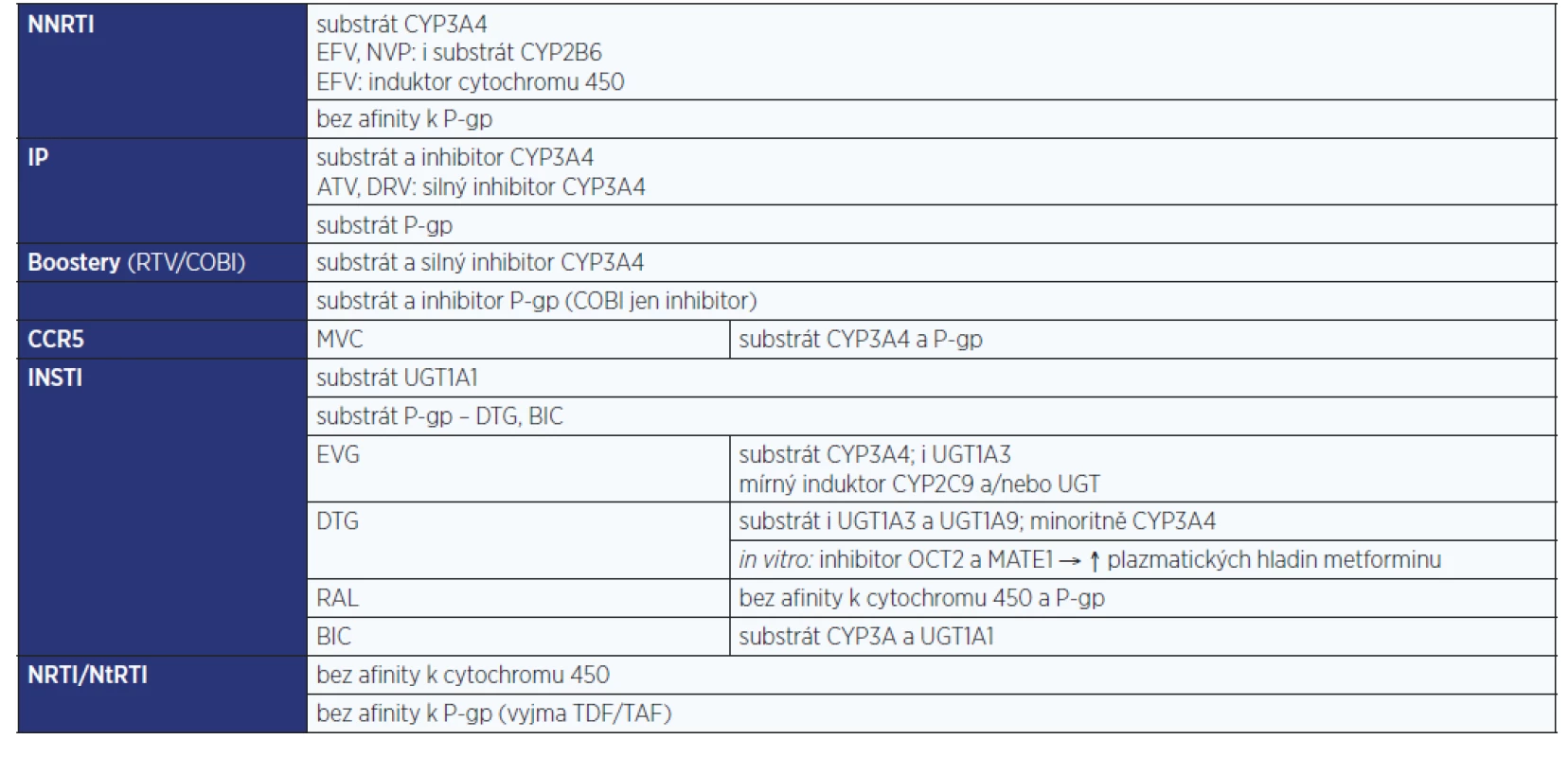
Těžištěm tohoto článku jsou tabulky s bazálními farmakokinetickými daty jednotlivých AR. (tab. 1–6). Z míst v procesu metabolizace léčiv, kde může dojít k LINT, je zpracován cytochromový systém P450 a UGT. Z transportních proteinů je podrobněji uváděna jen role efluxního transportéru P-gp. Přehledy v sobě kompletně nezahrnují specifickou problematiku některých dalších enzymových transportérů (MRP, hOAT, OCT2, MATE1, BCRP ad.). Jejich význam a klinický dopad na osud AR v lidském organismu je často zatím jen předmětem výzkumu. Tyto základní farmakokinetické profily AR jsou mj. podstatné i pro rozhodování jak řídit dávku léčiva při renálním či hepatálním selhání. Informace v tabulkách se týkají pouze dospělé populace.
Současně je publikována i jedna souhrnná tabulka (tab. 7), jejíž praktické využití spočívá například v prvním zhodnocení potenciálního lékového problému/LINT během vizity u lůžka pacienta.
DISKUSE
Terapeutickým kombinacím s potenciálním výskytem klinicky významných LINT AR je vhodné se vyhýbat a volit spíše alternativy. Pokud to není možné, mělo by být zajištěno pečlivé sledování plazmatické HIV RNA, případně úprava dávky léčiv, a pokud je zavedeno, tak i terapeutické monitorování plazmatických hladin léčiv.
Problematika LINT (nejen AR) je komplikované téma a navrhnout jednotné postupy managementu LINT není vůbec reálné. Při řešení tohoto lékového problému je na začátku vždy více proměnných. Záleží na kvalitativním a kvantitativním potenciálu daného léčiva pro vznik LINT s jinými léčivy a na celkovém počtu léčiv v lékovém režimu pacienta. Mezi faktory, jež mohou dále ovlivnit výslednou míru rizika LINT, patří velikost dávky a režim terapie s interagujícím léčivem (dle potřeby vs. pravidelně; jednorázově vs. chronicky), pořadí a časový odstup, v jakém jsou léčiva zařazována do lékového režimu, funkční stav eliminačních orgánů pacienta ad. Management i tíže LINT se tak mohou v různých klinických situacích zásadním způsobem lišit.
Znalost farmakokinetických parametrů léčiv je však základem pro následné hodnocení klinické významnosti LINT již u konkrétního pacienta. V klinické praxi je možné postupovat takto:
- V případě výskytu silných inhibitorů nebo induktorů enzymů metabolizačního procesu léčiv či transportních proteinů v pacientově medikaci, tj. v případě jasné klinické relevance LINT, provádět kvalifikovaný management LINT na základě znalosti farmakokinetických parametrů a klinické zkušenosti.
- V případě středních inhibitorů/induktorů návrhy řešení ještě konfrontovat s publikovanými daty (klinickými studiemi, kazuistikami apod.) o daném lékovém problému.
Kvalifikovaný odhad je někdy obtížné provést při současném výskytu více LINT najednou. K těmto typům lékového problému většinou žádnou literaturu najít nelze. Každý případ je specifický. Pokud je k dispozici, je zde velkým pomocníkem právě terapeutické monitorování hladin léčiv. Rozšíření palety běžně monitorovaných léčiv o AR by bylo výhodou.
Existuje velké množství nápomocných interakčních tabulek, viz též zdroj (8), a webových mechanických „kontrolorů“, např. Medscape Drug Interactions Checker (6) či HIV Drug Interactions University of Liverpool (9). Jejich nedostatkem je ovšem, že neumějí individuálně zhodnotit klinickou významnost dané LINT v kontextu celé pacientovy medikace a jeho aktuálního zdravotního stavu. Své místo mohou mít v roli primárního rychlého pomocníka, například při zjišťování interakčního potenciálu léčiva, s nímž se klinický farmaceut ve své praxi rutinně nesetkává.
Samozřejmostí poskytované klinickofarmaceutické péče je návrh monitorování potenciální/očekávané LINT a managementu případných nežádoucích událostí, jež z ní vyplývají. Návrh je součástí písemného farmakoterapeutického doporučení určeného ošetřujícímu lékaři.
ZÁVĚR
Při vyhodnocování klinicky významných lékových interakcí AR je v multidisciplinárním týmu zdravotníků pečujících o PLWH nezastupitelná role klinického farmaceuta. Jeho předností je znalost farmakodynamických a farmakokinetických parametrů léčiv a umění správného zacházení s těmito informacemi.
Čestné prohlášení
Autorka práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Seznam použitých zkratek
- AAG α1-kyselý glykoprotein
- AR antiretrovirotika
- AUC plocha pod křivkou plazmatické koncentrace léčiva
- BAV biologická dostupnost
- BCRP breast cancer resistance protein
- Cmax maximální plazmatická koncentrace léčiva
- cps. kapsle
- CYP cytochrom P450
- EI inhibitory vstupu
- GF glomerulární filtrace
- HIV virus lidského imunodeficitu
- INSTI inhibitory integrázy
- LINT lékové interakce
- MATE transportér vylučování léčiv a toxinů
- MRP multidrug resistant protein
- NNRTI nenukleosidové inhibitory reverzní transkriptázy
- NRTI/NtRTI nukleosidové/nukleotidové inhibitory reverzní transkriptázy
- OATP polypeptidy transportující organické anionty
- OCT transportér organických kationtů
- P-gp glykoprotein P
- PI inhibitory proteázy
- PLWH lidé žijící s infekcí HIV
- sol. roztok
- T1/2 biologický (eliminační) poločas
- Tmax čas dosažení maximální plazmatické koncentrace léčiva
- tbl. tableta
- TS tubulární sekrece
- UGT uridindifosfát glukuronosyltransferáza
Adresa pro korespondenci:
PharmDr. Irena Murínová
Oddělení klinické farmacie
Ústřední vojenská nemocnice – Vojenská fakultní nemocnice
U Vojenské nemocnice 1200, 169 02 Praha 6
Tel.: 737 366 568
e-mail: irena.murinova@uvn.cz
Sources
- Květina J, Grundmann M. Farmakologické interakce. Klinická farmakologie a farmacie 2003; 17 : 17–21.
- Dostálek M, Janoštíková E, Juřica J a kol. Farmakokinetika. Grada, Praha, 2006.
- Snopková S, Rozsypal H, Aster V a kol. Doporučený postup péče o dospělé infikované HIV a postexpoziční profylaxe infekce HIV. Dostupné na: www.infekce.cz/DPHIV19.htm
- Databáze léků. SÚKL. Dostupné na: www.sukl.cz/modules/medication/search.php
- UpToDate. Wolters Kluwer Health. Dostupné na: www.uptodate.com
- Qureshi S. Drug Interactions with Antiretroviral Therapy. Medscape, 2019 Apr 9. Dostupné na: https://emedicine.medscape.com/article/2039809
- Drug Interaction Checker. Medscape. Dostupné na: https://reference.medscape.com/drug-interactionchecker
- European AIDS Clinical Society. Guidelines, version 9.1. Dostupné na: www.eacsociety.org/files/2018_guidelines-9.1-english.pdf
- HIV Drug Interactions. University of Liverpool. Dostupné na: www.hiv-druginteractions.org/checker
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental HygienistArticle was published in
Journal of Czech Physicians

- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
-
All articles in this issue
- Klinická farmacie v České republice
- Vyplatí se bezpečná farmakoterapie?
- Specializační a kontinuální vzdělávání v oboru klinická farmacie
- Klinický farmaceut v pediatrii: možný přínos?
- Podání léčiv nutričními sondami: příklady, pracovní skupina
- Inhibitory protonové pumpy v praxi klinického farmaceuta
- Klinicky významné lékové interakce antiretrovirotik
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Management metabolických nežádoucích účinků everolimu u pacientů s renálním karcinomem
- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Kombinace mirtazapinu a paroxetinu: možná klinicky projevená interakce?
- Fatální Stevensův-Johnsonův syndrom: komplikace při hospitalizaci pacienta na gerontopsychiatrii a prostor pro multioborovou spolupráci
- Spánek a jeho poruchy v neurologii
- Specifika spánku u žen a jeho poruch
- Precizní psychiatrie – reálná možnost?
- Přednáškové večery spolku českých lékařů v Praze (BŘEZEN 2020)
- Význam spánkové medicíny v pediatrii
- Princip posuzování a uznávání nemocí z povolání v České republice
- Journal of Czech Physicians
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Spánek a jeho poruchy v neurologii
- Inhibitory protonové pumpy v praxi klinického farmaceuta
