Altepláza v intrapleurální terapii: Co víme a nevíme?
Intrapleural alteplase therapy: what are the knowns and unknowns?
In pneumology, enzymatic properties of plasmin are used to disrupt fibrin adhesions and septations formed during pathological conditions of the pleural cavity. In that case, fibrinolytics are administrated locally via a chest tube in the pleural cavity to evacuate pathological effusion. Although the first intrapleural administration of fibrinolytic occurred seventy years ago, there has been no consensus on dosing or a uniform procedure of their application. The aim of the article is to summarize current knowledge of alteplase usage in pneumology and discuss practical aspects of its intrapleural application regarding specific possibilities in the Czech Republic.
Keywords:
intrapleural fibrinolytics – alteplase – pleural infection – fibrinolytic therapy
Authors:
Judita Staša 1; Jana Gregorová 1,2; Norbert Pauk 3
Authors‘ workplace:
Oddělení klinické farmacie, Nemocnice Na Bulovce, Praha
1; Ústav aplikované farmacie, Farmaceutická fakulta VFU Brno
2; Klinika pneumologie 3. LF UK a Nemocnice Na Bulovce, Praha
3
Published in:
Čas. Lék. čes. 2019; 158: 295-299
Category:
Review Article
Overview
V pneumologii se využívá enzymatické schopnosti plazminu k rozrušení fibrinových adhezí a sept vzniklých při patologických stavech pleurální dutiny. V tomto případě se fibrinolytika aplikují lokálně hrudním drénem ve snaze o evakuaci patologického obsahu z pleurální dutiny. Přestože však první intrapleurální aplikace fibrinolytika proběhla před 70 lety, neexistuje konsenzus v dávkování ani jednotný postup pro aplikaci. Záměrem článku je sumarizovat dosavadní poznatky o použití alteplázy v pneumologii a diskutovat praktické aspekty její intrapleurální aplikace s přihlédnutím ke konkrétním možnostem v České republice.
Klíčová slova:
intrapleurální fibrinolytika – altepláza – pleurální infekce – fibrinolytická terapie
ÚVOD
Intrapleurální fibrinolytická terapie doplňuje spektrum současných léčebných možností pleurální infekce. Jedná se o postup schválený odbornými společnostmi v České republice (1) i v zahraničí (2,3), ale rovněž o off-label použití léčiva.
Intrapleurální fibrinolytická terapie se používá již 70 let (4), stále však existuje řada nezodpovězených otázek. Chybějí data týkající se přímého srovnání jednotlivých fibrinolytik v intrapleurální aplikaci, není definována optimální dávka fibrinolytika ani dávkovací režim či délka intrapleurální terapie. Stejně tak jsou nedostačující informace o kombinované terapii alteplázy s enzymem deoxyribonukleázou (DNáza).
Fibrinolytika konvertují plazminogen na plazmin, který štěpí fibrin a další produkty bílkovinné povahy. V pneumologii se fibrinolytika podávají pomocí hrudního drénu přímo do pleurální dutiny. Principem jejich lokálního působení je využití enzymatické schopnosti plazminu. Lokální lýza fibrinových adhezí a sept vzniklých při patologických stavech v pleurální dutině zefektivní hrudní drenáž. Výsledkem je sjednocení pleurální dutiny a kompletní evakuace patologického obsahu hrudním drénem.
Prvním fibrinolytikem použitým tímto způsobem byla streptokináza (4), která se v intrapleurální aplikaci vyžívala také v České republice. V roce 2014 ji nahradil tkáňový aktivátor plazminogenu altepláza – v současnosti jediné dostupné fibrinolytikum na českém trhu (5).
PŘÍPRAVA ALTEPLÁZY PŘED INTRAPLEURÁLNÍ APLIKACÍ
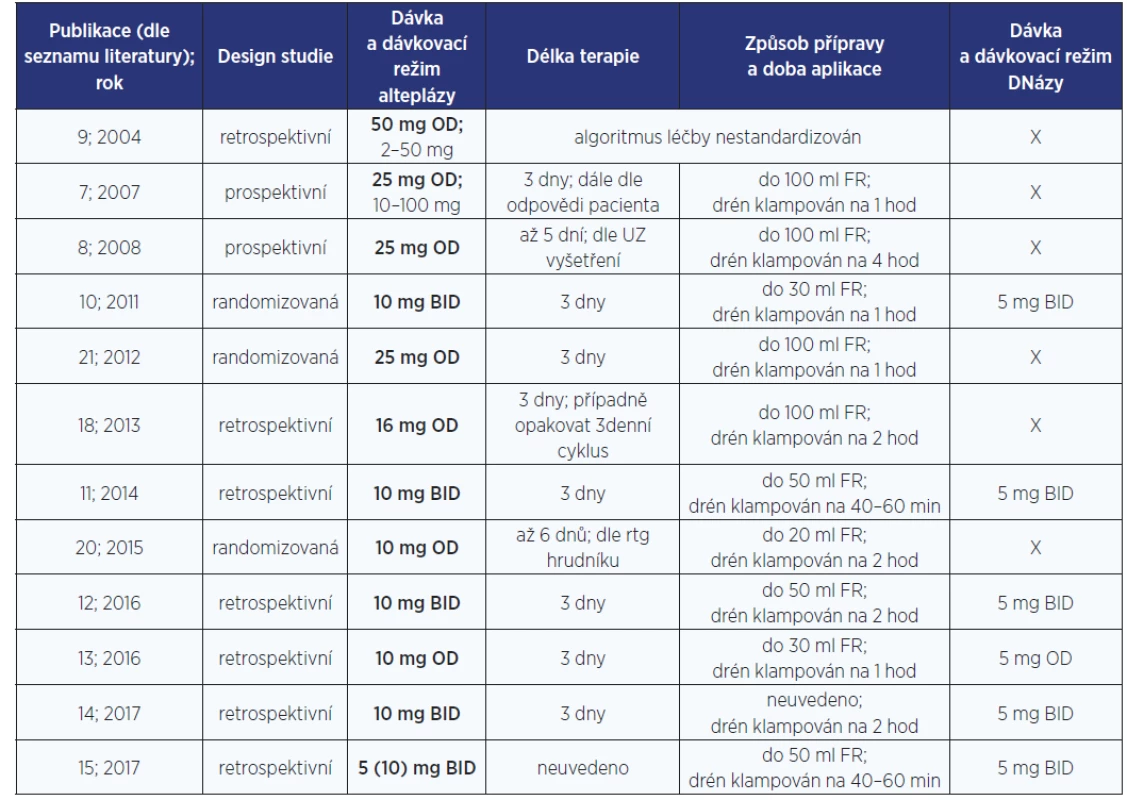
V jednotlivých studiích je altepláza aplikována v maximálním množství 100 ml fyziologického roztoku (tab. 1). Takový postup koresponduje s doporučením České pneumologické a ftizeologické společnosti ČLS JEP (ČPFS) (1) a se souhrnem údajů o přípravku (SPC) obsahujícím alteplázu (6). Dle SPC je před použitím nutné prášek rozpustit ve vodě pro injekci, která je součástí balení přípravku, a dále roztok naředit na minimální koncentraci 0,2 mg/ml. To znamená, že k 20mg ampuli alteplázy lze přidat maximálně 100 ml fyziologického roztoku. Naředěný roztok je určen k okamžitému použití. Jeho chemická a fyzikální stabilita je prokázána po dobu 24 hodin při teplotě 2–8 ºC (6). V žádné z uvedených studií není při přípravě altepláza mísena s lokálními anestetiky ani dezinfekčními roztoky. S ohledem na způsob podání, ke kterému je léčivý přípravek s obsahem alteplázy primárně určen, je logické, že SPC nic takového nedovoluje.
DÁVKA ALTEPLÁZY V INTRAPLEURÁLNÍ APLIKACI
Mezinárodní doporučení American College of Chest Physicians (ACCP) a British Thoracic Society (BTS) se k dávkování alteplázy nevyjadřují (2, 3). Ani napříč studiemi nepanuje jednoznačná shoda (tab. 1). Ve starších studiích se dávkování alteplázy pohybuje v širokém rozmezí 2–100 mg, s nejčastěji aplikovanou dávkou 25 mg (7, 8) a 50 mg (9).
Multicentrická studie MIST2, kterou v roce 2011 publikovali Rahman et al., randomizovala pacienty s pleurální infekcí do 4 skupin: placebo, altepláza, DNáza a kombinace alteplázy a DNázy. Intrapleurální terapie (altepláza 10 mg, DNáza 5 mg) se podávala 2× denně po dobu 3 dnů v celkovém počtu 6 dávek každého léčiva. Pouze kombinovaná léčba fibrinolytika s DNázou zlepšila drenáž pleurálního výpotku, snížila potřebu chirurgického zákroku a významně zkrátila délku hospitalizace v porovnávání s ostatními režimy intrapleurální léčby nebo placebem (10). Vzhledem k příznivým výsledkům studie MIST2 ostatní autoři převzali použitý dávkovací protokol nebo se jím alespoň inspirovali (11–15, 17, tab. 1), přestože dávky a dávkovací schéma studie MIST2 měly pouze empirický základ.
Některé modifikace dávky a dávkování alteplázy zohledňovaly potenciální riziko krvácení i finanční náklady spojené s intrapleurální fibrinolytickou terapií. Popowiczová et al. prokázali úspěšnou léčbu sníženou dávkou alteplázy na 5 mg podle originálního protokolu studie MIST2 (15). Pouze u 11 % pacientů bylo potřebné zvýšení dávky na 10 mg (15). Ještě nižší dávky pak byly použity u pacientů s vysokým rizikem krvácení.
Lan et al. pacientce se závažnou pancytopenií intrapleurálně aplikovali 0,5 mg alteplázy s příznivým výsledkem (16). Podobně úspěšný byl i případ použití alteplázy v dávce 1 mg společně s 5 mg DNázy pro léčbu pleurální infekce u nemocné s koagulopatií (17).
Důvodem nesouladu v dávkování alteplázy může být odlišné množství účinné látky v jednotlivých registrovaných přípravcích v zahraničí. V České republice je altepláza dostupná pouze ve dvou koncentracích: 20 mg (což odpovídá 11 600 000 IU) a 50 mg (29 000 000 IU) (6). ČPFS v doporučeném postupu „Diagnostika a léčba hrudního empyému“ uvádí dávku alteplázy 10 mg (1). Z dokumentu však není jasné, zda se jedná o maximální denní dávku.
Lékovou formou přípravku je prášek pro infuzní roztok ve formě lyofilizátu. Rozdělení přípravku o síle 20 mg na menší podíly je dle SPC možné, ale omezené dobou použitelnosti. Druhou část dávky je nutné spotřebovat do 24 hodin (6). Jiný přístup zvolili Abu-Daff et al., když rozdělili naředěnou ampuli s 50 mg alteplázy na tři 16mg podíly, které následně zmrazili (18). Pokud by však měl být takový postup zvolen, vyžadovalo by to nejprve provedení nových stabilitních testů.
DOBA PONECHÁNÍ ALTEPLÁZY V PLEURÁLNÍ DUTINĚ
Standardní doba klampování hrudního drénu po aplikaci fibrinolytika není stanovena. ČPFS doporučuje 3hodinové klampování drénu (1). Ve studiích je altepláza v pleurálním prostoru ponechána různě dlouhou dobu, od 40 minut až po 4 hodiny (tab. 1). Žádná z těchto prací však nezmiňuje důvod zvoleného postupu.
Kheir et al. se v roce 2018 zaměřili na zjednodušení dávkovacího protokolu studie MIST2 (19). Dle protokolu MIST2 se altepláza a DNáza aplikovaly postupně zvlášť. Každá jednotlivá aplikace léčiva byla oddělena klampováním drénu po dobu 1 hodiny a drenáží (10). Autoři studie porovnali sekvenční podání dle protokolu MIST2 se souběžnou aplikací alteplázy a DNázy hrudním drénem s rozdílnou dobou klampování. Nezjistili žádný významný rozdíl v účinnosti a bezpečnosti takto vedené kombinované intrapleurální terapie (19). Doba ponechání alteplázy v pleurálním prostoru zřejmě není rozhodující ani pro účinnost fibrinolytika, ani pro výskyt nežádoucích účinků.
DÁVKOVACÍ SCHÉMA INTRAPLEURÁLNÍ APLIKACE ALTEPLÁZY
Standardní dávkovací režim alteplázy ani délka intrapleurální terapie nejsou určeny. Zahraniční doporučení počet denních dávek alteplázy neuvádějí (2, 3). Český doporučený postup zmiňuje pouze jednotlivou dávku alteplázy, zároveň však neříká nic o možnosti opakované aplikace týž den (1). Stejně tak nám otázku délky intrapleurální terapie nezodpoví žádný ze současně platných doporučených postupů (1–3).
Protokol studie MIST2 stanovil dávkovací režim 2× denně (10). To však s sebou nese některé nevýhody, například náročnost pro zdravotnický personál a nutnost opakované manipulace s hrudním drénem. Aktuálním trendem je proto snaha o zjednodušení dávkovacího schématu, a to buď změnou sekvenčního na souběžné podání fibrinolytika s DNázou (12, 14), nebo přechodem na jednodenní aplikaci (13). Jednotlivé úpravy dávkovacího schématu neměly vliv na účinnost či zvýšení frekvence nežádoucích účinků kombinované léčby (12–14).
Délka terapie alteplázou se v některých studiích odvíjela od klinického stavu pacienta a perzistence pleurálního výpotku zachyceného pomocí zobrazovacích vyšetření (8, 20). Ve většině studií délka terapie nepřesáhla 3 dny a maximálně bylo aplikováno 6 dávek alteplázy (10–14, 21, tab. 1). Alemánová et al. podávali intrapleurální terapii alteplázou v 1 denní dávce 6 dní (20) a Thommi et al. u několika pacientů až 8 dní (7). Maximální počet dávek intrapleurální terapie při aplikaci 2× denně uvádějí McClune et al. (22). V této studii bylo aplikováno 16 dávek kombinované léčby alteplázy s DNázou v 8denní terapii bez zvýšení frekvence výskytu krvácivých komplikací (22).
BEZPEČNOST INTRAPLEURÁLNÍ TERAPIE ALTEPLÁZY
Všechny uvedené studie potvrzují dobrý bezpečnostní profil alteplázy (tab. 1), a to i v případě symptomatické léčby lokulárních maligních výpotků u dlouhodobé hrudní drenáže (16, 23). Froudarakis et al. popisují pouze mírné komplikace, jako je bolest během aplikace fibrinolytika a lokální krvácení, jež nebyly statisticky významné ve srovnání s placebem (8). Vznik lokálního krvácení autoři připisují enzymatickému štěpení sept nebo manipulaci s hrudním drénem (8). Další práce zmiňují také bolest na hrudi, erytém a otok v místě drénu. Ze závažnějších nežádoucích účinků je uváděno pleurální krvácení, které se však nevyskytlo u statisticky významného počtu zařazených osob (7, 11–15, 19, 21, 23). V žádné ze jmenovaných studií nedošlo po intrapleurální aplikaci alteplázy k systémovému krvácení.
Naproti tomu prospektivní studie z roku 2015 zaznamenala při podávání alteplázy v dávce 20 mg přítomnost hemoptýzy či hemothoraxu u 5 z 18 subjektů. Z tohoto důvodu byla dávka alteplázy pro další pokračování studie snížena na 10 mg (20).
Ve studii, kterou provedli Thommi et al., byli pacienti během intrapleurální léčby alteplázou zajištěni standardní antikoagulační profylaxí (enoxaparin v dávce 40 mg nebo heparin v dávce 10 000 IU), bez zvýšeného výskytu krvácení v porovnání s placebovou skupinou (21). Tuto skutečnost ostatní studie nezmiňují.
Pacienti s aktivním krvácením, těžkou nekontrolovanou hypertenzí, hemothoraxem, bronchopleurální píštělí, hypersenzitivitou na alteplázu nebo koagulačními parametry INR > 4, PTT > 50 s či trombocyty < 50 × 109/l vůbec nebyli do studií zařazováni (7, 13, 21).
S ohledem na výskyt zmíněných nežádoucích příhod ve studiích je zřejmé, že součástí správného managementu pacientů s hrudním drénem je dostatečná analgetická terapie pacienta, zejména prvních 24 hodin intrapleurální terapie (11, 13). Dále jsou nezbytné pravidelné kontroly krevního obrazu a koagulačních parametrů. U pacientů s perorální antikoagulační léčbou je nutné provést včasné převedení na nízkomolekulární heparin pro snazší úpravu dávek.
Zvýšit bezpečnost intrapleurální aplikace fibrinolytik lze dodržením kontraindikací jejich podání, jimiž jsou aktivní krvácení, poruchy koagulace, těžká nekontrolovaná hypertenze, přítomnost bronchopleurální píštěle, recentně proběhlé trauma či operační výkon (1).
S bezpečnou aplikací fibrinolytika hrudním drénem souvisí také informovaný souhlas pacienta s hrudní drenáží a zároveň souhlas s off-label použitím alteplázy.
KOMBINOVANÁ TERAPIE ALTEPLÁZOU A DNÁZOU
Cílem kombinované intrapleurální léčby je snaha o zefektivnění hrudní drenáže ovlivněním viskozity výpotku. Viskozita výpotku se během infekce zvyšuje zejména přítomností extracelulární DNA vzniklé buněčným rozpadem. Tento předpoklad byl potvrzen studií MIST2, která jako první poskytla důkazy o úspěšnosti kombinované intrapleurální terapie alteplázy a DNázy (10). Z tohoto důvodu mnohé z pozdějších studií (11–15, 19) ověřovaly účinnost a bezpečnost různých dávkovacích schémat alteplázy pouze v kombinované terapii s DNázou (tab. 1).
DNáza je v České republice dostupná v přípravku používaném pro léčbu pacientů s cystickou fibrózou. Dávkování uváděné ve studiích se pohybuje mezi 5 a 10 mg na den (tab. 1). Jedna ampule přípravku obsahuje 2,5 mg DNázy a její přibližná cena činí 500 Kč. Případné použití kombinované terapie je pak otázkou pečlivé selekce pacientů.
ZÁVĚR
Nejvhodnější protokol intrapleurální fibrinolytické léčby dosud chybí. V klinické praxi se běžně setkáváme s různorodostí dávek a dávkovacích schémat.
Nejnižší dostupná dávka alteplázy v Česku je 20 mg. Aktuální studie však naznačují, že dostatečně účinné je i nižší dávkování alteplázy. Při aplikaci vyšších dávek než 20 mg fibrinolytika se ovšem neprokázal zvýšený výskyt významných nežádoucích účinků. Otázkou tedy je, jaký ekonomický benefit rozdělení ampule alteplázy přinese.
Léková forma alteplázy je lyofilizát pro přípravu injekčního roztoku. Po rekonstituci je možné roztok rozdělit na více částí. Z pohledu fyzikální a chemické stability lze druhou část dávky fibrinolytika ještě tentýž den použít, z mikrobiologického hlediska však ne. Zajímavá je možnost zmrazení rekonstituovaných roztoků alteplázy za předpokladu existence stabilitních zkoušek.
Ve specifických případech může modifikace dávky fibrinolytika představovat bezpečnější alternativu. Například rozdělení ampule pro použití nižší dávky bude výhodné u pacientů s vysokým rizikem krvácení.
Ukazuje se, že různá dávkovací schémata mají srovnatelný bezpečnostní profil a že podání alteplázy v 1 denní dávce je dostatečně účinné a bezpečné. Proto stojí za úvahu, zda je potřebné podávat alteplázu v režimu 2× denně, i s ohledem na časovou náročnost praktické stránky aplikace.
Některé ze studií popsaly souběžnou intrapleurální aplikaci alteplázy a DNázy v rámci kombinované terapie. Vyvstává otázka, zda smísením léčiv před aplikací do hrudního drénu nebo v pleurální dutině nedojde ke ztrátě jejich terapeutické účinnosti. Tyto obavy vyvrací řada studií, jež potvrzují úspěšnost kombinované intrapleurální terapie alteplázou a DNázou.
Altepláza a lokální anestetika jsou patrně také vzájemně kompatibilní, ale z terapeutického pohledu je tato kombinace neracionální. Pacienti s hrudním drénem s intrapleurální terapií či bez ní jsou indikovaní k analgetické terapii včetně využití opioidů. Optimální dávky analgetik s dostatečně dlouhou dobou působení jsou zcela zásadní, to však lokální anestetika s krátkým analgetickým efektem nesplňují. Pokud je zvolena odpovídající analgetická terapie, je podávání lokálního anestetika do pleurálního prostoru zcela bezpředmětné.
Za zmínku stojí hypotéza, která by dávku fibrinolytik individualizovala na základě aktivity inhibitoru aktivátorů plazminogenu (PAI) stanoveného v pleurální tekutině nemocných. PAI je nadměrně exprimován v pleurálním výpotku při poranění pleury s velkou variabilitou hladin mezi nemocnými. PAI podporuje tvorbu fibrinových sept a svým inhibičním působením přispívá k selhání účinku aktivátoru tkáňového plazminogenu (24).
Studie zabývající se problematikou dávkování alteplázy, které by pomohly objasnit některé sporné otázky její intrapleurální aplikace, v České republice prozatím chybějí.
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Seznam použitých zkratek
- ACCP American College of Chest Physicians
- BID dvakrát denně
- BTS British Thoracic Society
- ČPFS Česká pneumologická a ftizeologická společnost ČLS JEP
- DNA deoxyribonukleová kyselina
- DNáza deoxyribonukleáza
- FR fyziologický roztok
- INR mezinárodní normalizovaný poměr
- IU mezinárodní jednotka
- MIST2 Multi-center Intrapleural Sepsis Trial 2
- OD jedenkrát denně
- PAI inhibitor aktivátorů plazminogenu
- PTT parciální tromboplastinový čas
- rtg rentgen
- SPC souhrn údajů o přípravku
- UZ ultrazvuk
Adresa pro korespondenci:
PharmDr. Judita Staša
Oddělení klinické farmacie
Nemocnice Na Bulovce
Budínova 67/2, 180 81 Praha 8
Tel.: 737 286 062
e-mail: judita.stasa@bulovka.cz
Sources
- Žáčková P, Vašáková M. Diagnostika a léčba hrudního empyému. Česká pneumologická a ftizeologická společnost ČLS JEP, 2016. Dostupné na: www.pneumologie.cz/guidelines
- Colice GL, Curtis A, Deslauriers J et al. Medical and surgical treatment of parapneumonic effusions: an evidence-based guideline. Chest 2000; 118 : 1158–1171.
- Davies HE, Davies RJ, Davies CW et al. Management of pleural infection in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax 2010; 65: ii41–ii53.
- Tillett W, Sherry S. The effect in patients with streptococcal fibrinolysis (streptokinase) and streptococcal desoxyribonuclease on fibrinous, purulent, and sanguinous pleural exudations. J Clin Invest 1949; 28 : 173–190.
- Státní ústav pro kontrolu léčiv. Databáze léků. Dostupné na: www.sukl.cz/modules/medication/search.php
- SPC Actilyse. Dostupné na: www.sukl.cz/modules/medication/detail.php?code=0093650&tab=texts
- Thommi G, Nair CK, Aronow WS et al. Efficacy and safety of intrapleural instillation of alteplase in the management of complicated pleural effusion or empyema. Am J Ther 2007; 14 : 341–345.
- Froudarakis ME, Kouliatsis G, Steiropoulos P et al. Recombinant tissue plasminogen activator in the treatment of pleural infections in adults. Respir Med 2008; 102 : 1694–1700.
- Skeete DA, Rutherford EJ, Schlidt SA et al. Intrapleural tissue plasminogen activator for complicated pleural effusions. J Trauma 2004; 5 : 1178–1183.
- Rahman NM, Maskell NA, West A et al. Intrapleural use of tissue plasminogen activator and DNase in pleural infection. N Engl J Med 2011; 365 : 518–526.
- Piccolo F, Pitman N, Bhatnagar R et al. Intrapleural tissue plasminogen activator and deoxyribonuclease for pleural infection. An effective and safe alternative to surgery. Ann Am Thorac Soc 2014; 11 : 1419–1425.
- Majid A, Kheir F, Folch A et al. Concurrent intrapleural instillation of tissue plasminogen activator and DNase for pleural infection. A single-center experience. Ann Am Thorac Soc 2016; 13 : 1512–1518.
- Mehta HJ, Biswas A, Penley AM et al. Management of intrapleural sepsis with once daily use of tissue plasminogen activator and deoxyribonuclease. Respiration 2016; 91 : 101–106.
- Bishwakarma R, Shah S, Frank L et al. Mixing It Up: Coadministration of tPA/DNase in complicated parapneumonic pleural effusions and empyema. J Bronchology Interv Pulmonol 2017; 24 : 40–47.
- Popowicz N, Bintcliffe O, De Fonseka D et al. Dose de-escalation of intrapleural tissue plasminogen activator therapy for pleural infection. The alteplase dose assessment for pleural infection therapy project. Ann Am Thorac Soc 2017; 14 : 929–936.
- Lan NSH, Vekaria S, Sidhu C et al. Very low-dose intrapleural tPA for indwelling pleural catheter-associated symptomatic fluid loculation. Respirol Case Rep 2019; 7(7): e00457.
- Hart JA, Badiei A, Lee YCG. Successful management of pleural infection with very low dose intrapleural tissue plasminogen activator/deoxyribonuclease regime. Respirol Case Rep 2019; 7(3): e00408.
- Abu-Daff S, Maziak DE, Alshehab D et al. Intrapleural fibrinolytic therapy (IPFT) in loculated pleural effusions-analysis of predictors for failure of therapy and bleeding: a cohort study. BMJ Open 2013; 3 : 2–7.
- Kheir F, Cheng G, Rivera E et al. Concurrent Versus Sequential Intrapleural Instillation of Tissue Plasminogen Activator and Deoxyribonuclease for Pleural Infection. J Bronchology Interv Pulmonol 2018; 25 : 125–131.
- Alemán C, Porcel JM, Alegre J et al. Intrapleural fibrinolysis with urokinase versus alteplase in complicated parapneumonic pleural effusions and empyemas: a prospective randomized study. Lung 2015; 193 : 993–1000.
- Thommi G, Shehan JC, Robison KL et al. A double blind randomized cross over trial comparing rate of decortication and efficacy of intrapleural instillation of alteplase vs placebo in patients with empyemas and complicated parapneumonic effusions. Respir Med 2012; 106 : 716–723.
- McClune JR, Wilshire CL, Gorden JA et al. Safety and efficacy of intrapleural tissue plasminogen activator and DNase during extended use in complicated pleural space infections. Can Respir J 2016; 2016 : 9796768.
- Thomas R, Piccolo F, Miller D et al. Intrapleural fibrinolysis for the treatment of indwelling pleural catheter-related symptomatic loculations: a multicenter observational study. Chest 2015; 148 : 746–751.
- Komissarov AA, Florova G, Azghani AO. Dose dependency of outcomes of intrapleural fibrinolytic therapy in new rabbit empyema models. Am J Physiol Lung Cell Mol Physiol 2016; 311: L389–L399.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental HygienistArticle was published in
Journal of Czech Physicians

- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
-
All articles in this issue
- Klinická farmacie v České republice
- Vyplatí se bezpečná farmakoterapie?
- Specializační a kontinuální vzdělávání v oboru klinická farmacie
- Klinický farmaceut v pediatrii: možný přínos?
- Podání léčiv nutričními sondami: příklady, pracovní skupina
- Inhibitory protonové pumpy v praxi klinického farmaceuta
- Klinicky významné lékové interakce antiretrovirotik
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Management metabolických nežádoucích účinků everolimu u pacientů s renálním karcinomem
- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Kombinace mirtazapinu a paroxetinu: možná klinicky projevená interakce?
- Fatální Stevensův-Johnsonův syndrom: komplikace při hospitalizaci pacienta na gerontopsychiatrii a prostor pro multioborovou spolupráci
- Spánek a jeho poruchy v neurologii
- Specifika spánku u žen a jeho poruch
- Precizní psychiatrie – reálná možnost?
- Přednáškové večery spolku českých lékařů v Praze (BŘEZEN 2020)
- Význam spánkové medicíny v pediatrii
- Princip posuzování a uznávání nemocí z povolání v České republice
- Journal of Czech Physicians
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Spánek a jeho poruchy v neurologii
- Inhibitory protonové pumpy v praxi klinického farmaceuta
