-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Současné možnosti kontinuálního neinvazivního monitorování arteriálního tlaku
Current techniques of continuous non-invasive monitoring of arterial blood pressure
Blood pressure is one of the most important parameters monitored in anaesthesia and intensive care medicine. Two possibilities of automatic blood pressure monitoring are at hand in contemporary practice: intermittent measurements obtained via an oscillometric cuff or continuous monitoring based on arterial catheterisation. In recent years novel technologies have been developed enabling continuous non-invasive monitoring of blood pressure. This review article describes the two most developed of these technologies: the volume clamp method and appalanation tonometry. Devices based on these principles might in near future help to significantly improve patients’ safety and quality of care.
Keywords:
blood pressure monitoring – non-invasive technologies – volume clamp – applanation tonometry
Autoři: Beneš Jan; Šimanová Alena; Kasal Eduard
Působiště autorů: Anesteziologicko-resuscitační klinika, Fakultní nemocnice Plzeň
Vyšlo v časopise: Anest. intenziv. Med., 25, 2014, č. 3, s. 222-230
Kategorie: Intenzivní medicína - Přehledový článek
Souhrn
Krevní tlak je jedním z nejdůležitějších vitálních parametrů sledovaných u nemocných v anesteziologii a intenzivní péči. Jeho automatické monitorování je prováděno buď intermitentně pomocí oscilometrie, nebo kontinuálně přímým měřením napojením na tepenné řečiště. Tento článek se zabývá problematikou současných možností monitorování krevního tlaku novými technologiemi, které umožňují kontinuální sledování bez nutnosti arteriální kanylace. Hlavním zaměřením jsou přístroje na principu volume clamp a aplanační tonometrie, které v současné době dosahují nejlepších výsledků v porovnání s přímým měřením. Tato nová zařízení by mohla po odstranění stávajících nedostatků významně zvýšit kvalitu péče a bezpečnost pacientů.
Klíčová slova:
krevní tlak – monitorování – neinvazivní technologie – volume clamp – aplanační tonometrieÚVOD
Sledování hodnot systémového krevního tlaku je základní součástí monitorování nemocných a generace kliniků jej používají jako základní informaci o funkci kardiovaskulárního aparátu. U anestezovaných nemocných je měření krevního tlaku minimálně v intervalu pěti minut vyžadováno doporučením Americké společnosti anesteziologie (ASA) [1], které zohledňuje i závazný postup České společnosti anesteziologie, resuscitace a intenzivní medicíny (ČSARIM) [2]. V současné době užívané techniky automatického neinvazivního měření krevního tlaku jsou až na výjimky založeny na principu oscilometrického měření s nutností naložení nafukovací manžety, nejčastěji na paži nemocného. Čas potřebný na změření tlaku, tedy nafouknutí a vyfouknutí manžety, se liší podle jednotlivých výrobců, ale v průměru se pohybuje kolem 30 sekund. V případě abnormálně vysokých nebo nízkých tlaků, či při pohybových artefaktech, dochází k automatickému zopakování měření a výsledek je tedy znám s odstupem i více než 1 minuty od vzniku klinického požadavku. Příliš časté nafukování manžety (metoda „stat“ některých výrobců, či příliš krátké zotavovací intervaly) nejsou ale bez rizika vzniku poškození kožního krytu nebo nervových poranění [3, 4]. Doporučený pětiminutový interval je tedy stanoven arbitrárně, bez podpory důkazů, jako jistý kompromis mezi technickými možnostmi monitorovacího zařízení, možností poranění nemocného a rizikem závažné fluktuace tlaku.
U nemocných, kde není frekvence intermitentního neinvazivní měření dostačující (rizikoví nemocní, předpoklad prudkých změn tlaku), bylo až do nedávné doby jedinou alternativou provedení kanylace arteriálního řečiště a přímé měření tlaku. Současná praxe kanylace a. radialis tenkými potaženými katétry je relativně bezpečným postupem užívaným u naprosté většiny rizikových anestezií [5]. Potenciál vzniku komplikací ovšem není zcela zanedbatelný [6] a indikace k provedení punkce by měla být důsledně klinicky podpořena. Přímé měření arteriálního tlaku je v podmínkách anestezie a intenzivní medicíny v současné době považováno za „zlatý standard“. Arteriální katetrizace má vedle stanovení přesnější numerické hodnoty aktuálního krevního tlaku také další výhody. Kontinuální zobrazení křivky s sebou přináší celou řadu klinicky podstatných informací [7]: charakter vzestupu a poklesu křivky, přítomnost a poloha dikrotického zářezu, respirační variabilita atd. Zhodnocení je možné i pouhým pohledem, v současné době je navíc dostupná celá řada technologií provádějících následnou analýzu tepové křivky [8].
Z hlediska klinického přístupu existuje tedy v rámci monitorování krevního tlaku poměrně zásadní mezera mezi neinvazivním postupem s nižší přesností, který poskytuje výsledky intermitentně, a kontinuálním – přesným, nicméně invazivním, postupem. Nezatěžující techniky kontinuálního měření krevního tlaku, které by si ponechaly výhody arteriální katetrizace bez nutnosti invaze, by významně umožnily vyplnit tuto „klinickou mezeru“. V nedávné době bylo uvedeno na trh několik zařízení pracujících na různých fyzikálních základech. V tomto přehledovém článku se budeme podrobně věnovat jejich charakteristikám a přínosu pro klinickou praxi.
PŘEHLED HISTORICKÉHO VÝVOJE
První pokusy o záznam pulsu a měření krevního tlaku jsou poměrně starého data. O významu pulsu byl přesvědčen již Galén. Nicméně až techniky sfygmografie vyvinuté koncem 19. století Karlem Vierordtem (1855) a následně upravené Etihenem Mareyem (1860) umožnily kontinuální záznam mechanické srdeční aktivity pomocí přenosu pulzace na grafické záznamové zařízení. Sfygmografické techniky nicméně vyžadovaly přesné uložení a okluzi radiální tepny, nebyly navíc schopné poskytnout zásadní informaci: přesnou hodnotu krevního tlaku. První sfygmomanometr založený na principu okluze tepny manžetou sestrojil v roce 1881 Karl Ritter von Bach. Jím sestrojené zařízení vyžadovalo uložení na zápěstí, komprese radiální tepny byla způsobena manžetou naplněnou vodou. Přístroj nedoznal velikého klinického rozšíření, nicméně předznamenal následné zdokonalení Scpionem Riva-Roccim, který v roce 1896 sestrojil první pažní sfygmomanometr. Pomocí okluze tepen paže manžetou naplněnou vzduchem a následným pohmatem pulsací na a. radialis bylo umožněno přesné stanovení hodnoty systolického tlaku. Za rozšíření metody vděčíme americkému neurochirurgovi Harvey Cushingovi, který v roce 1901 přístroj mírně poupravil a zavedl do klinické praxe k monitorování nemocných ve Spojených státech. Následná adaptace, provedená Nikolajem Korotkovem v roce 1905, byla založená nikoli na pohmatu pulsu, ale na poslechu charakteru proudění v tepnách těsně pod manžetou. To umožnilo vedle záznamu systolického krevního tlaku také stanovení diastoly. Tyto vynálezy okluzivní techniky měření krevního tlaku v zásadě poznamenaly vývoj a techniku měření do dnešní doby, kdy je auskultometrické hodnocení podle Korotkoffova stále považováno za zlatý standard neinvazivního měření, ke kterému se odvolávají nadnárodní standardy monitorování krevního tlaku [9, 10].
S nástupem automatických monitorů do běžné klinické praxe v 60. a 70. letech 20. století bylo učiněno několik pokusů o adaptaci Riva-Rocci--Korotkovovy techniky pomocí vložení dopplerového senzoru nebo mikrofonu. Nutné přesné uložení senzoru a extrémní citlivost k artefaktům ovšem záhy vedla k opuštění této techniky. Naprostá většina v současné době užívaných automatických manžetových tonometrů je založena na oscilometrickém postupu. Změny velikosti oscilací daných přenosem pulsací na vnější prostředí při různém transmurálním tlaku zaznamenal poprvé Ethien Marey (1876) [11]. První digitální automatický oscilometrický přístroj byl nicméně sestrojen až v 70. letech 20. století. Nevýhodou tohoto postupu je relativní nepřesnost ve stanovení systolického a diastolického tlaku. Oscilace se totiž objevují již při tlacích vyšších, než je systola a naopak úplného vymizení je dosaženo při hodnotách pod diastolickým tlakem [12]. Přesné je naopak stanovení středního arteriálního tlaku (okamžik největších oscilací). Hodnota systoly a diastoly je tedy v různých monitorech adaptována ze znalosti středního tlaku a charakteristik změny oscilací, přesné algoritmy nicméně podléhají autorským právům výrobců a nejsou v literatuře popsány. V rámci srovnání oscilometrického měření dochází většinou k podhodnocení systolických a nadhodnocení diastolických hodnot [13]. Obě techniky (oscilometrická i auskultační) využívající nafukovacích manžet jsou shodně zatíženy potenciální chybou při nesprávné volbě velikosti manžety (šířka přibližně 46 % obvodu použité končetiny) [14].
Historii přímého měření krevního tlaku je možno datovat do roku 1711, kdy reverend Stephen Hales napojil krční tepnu koně na dlouhou skleněnou trubici a přímo sledoval pulsace krve. Tato technika ovšem nebyla nikdy klinicky aplikována na člověka (kůň vždy po experimentu zhynul). První invazivní záznam tlaku tak provedl až o více než sto let později (v roce 1856) Faivre, který po provedení amputace vsunul přímo do tepny Carl Ludwigův kymograf – U trubici se záznamovým plovákem. Významný rozvoj nicméně zaznamenala tato technika až v druhé polovině 20. století díky zlepšení materiálů používaných na výrobu katétrů, zavedením automatických proplachovacích systémů a piezoelektrických krystalů pro převod tlakové vlny na elektrický signál. Pro oblast anestezie a intenzivní medicíny je invazivní měření považováno za zlatý standard, ačkoli hodnoty měřeného tlaku se mohou odlišovat v různých částech řečiště v důsledku propulzního a reflexního šíření pulzní vlny [15].
MĚŘENÍ POMOCÍ TECHNIKY VOLUME CLAMP
Měření krevního tlaku pomocí techniky volume clamp, nebo také vascular unloading, je založeno na postupu popsaném v roce 1973 českým fyziologem Janem Peňázem [15] – obrázek 1. Na rozdíl od okluzivních technik, při nichž jsou sledovány změny v pulzacích, toku či oscilacích vyvolané plným uzavřením arterie, je technika založena na částečném stištění – semiokluzi. Pomocí foto-pletyzmografické absorpce světla je stanovena velikost krevního kompartmentu a jeho pulzatilita. Nafukovací manžetou je pak na příslušnou část vyvíjen takový proměnlivý tlak, aby byla velikost krevního kompartmentu setrvale stejná (volume clamp). Tlak měřený v manžetě odpovídá intramurálnímu arteriálnímu tlaku, což umožňuje rekonstrukci arteriální tlakové křivky. K získání optimální přesnosti měření je nutné, aby nedocházelo ke ztrátám tlaku v důsledku poddajnosti vaskulární stěny a okolních tkání. Vstupně je tedy nutné najít optimální zevní tlak, při kterém dojde k vyrovnání transmurálních tlaků (vascular unloading). Toho je dosaženo v okamžiku maximálního přenosu oscilací foto-pletyzmografického signálu (klinicky odpovídá hodnotě středního arteriálního tlaku) [11]. Peňázem popsaná technologie byla následně převedena do životaschopné praxe Wesselingem [17] a integrovaná do zařízení Finapres (FINger Arterial PRESsure, Ohmeda, Englewood, CO – USA).
Obr. 1. Profesor Peňáz s prototypem přístroje (fotografie zapůjčena se souhlasem prof. MUDr. Nataši Honzíkové, CSc.) 
Výše popsaný postup s sebou přináší několik základních problémů. Za prvé, použitá část těla musí být dostatečně malá, aby umožnila prosvícení světelným signálem v kvalitě umožňující foto-pletyzmografické zhodnocení. A za druhé, musí umožnit naložení zevní manžety. Optimálním místem jsou tedy články prstů horních končetin. Získaná křivka i hodnoty arteriálního tlaku pak odpovídají prstovým arteriím. V průběhu let byla vytvořena různá konstrukční řešení, která vedou k aproximaci hodnot na tlaky brachiální či radiál-ní. Dalším problémem je vliv jiných faktorů na velikost krevního a nekrevního kompartmentu. Vzhledem k tomu, že v průběhu měření nedochází jen ke změnám objemu daných srdečním cyklem, ale také ke změnám tonu arterie, došlo by časem při užívání pouze volume clamp módu k závažné chybě měření. Jednotlivé výrobky se odlišují právě na základě řešení těchto problémů, čímž je dána i jejich poněkud odlišná přesnost a spolehlivost.
Vzhledem k tomu, že tlak v manžetě přesahuje žilní tlak, dochází při užití přístroje k venostáze periferní části prstu tzv. blue finger. Podle stávajících studií ani delší (řádově hodinové) užívání nevedlo ke známkám poruchy kyslíkového metabolismu v příslušném prstu [18]. Přesto je nutno zvážit naložení u nemocných s poruchami prokrvení periferie (Raynaudův syndrom apod.) či periferními otoky. Porucha periferního prokrvení u nemocných s těžkou oběhovou alterací v důsledku extrémní vazokonstrikce, při užití vysokých dávek vazopressorů nebo podchlazených nemocných s centralizací oběhu je dalším relativně málo prozkoumaným omezením metody. V současné době jsou komerčně dostupné dvě technologie/zařízení založené na Peňázově principu, v našich podmínkách se bohužel jedná zatím pouze o technologii CNAP®, eventuálně její integraci do jiných monitorovacích systémů firem Draeger a LiDCO.
Zařízení Nexfin
Zařízení Nexfin (pro ČR v budoucnu dostupné jako modul ClearSight pro platformu EV 1000 – Edwards Lifesciences Inc., Irvine, California, USA – obrázek 2) je přímým pokračovatelem původního, dnes již nevyráběného, patentového přístroje Finapress vyvinutého Wesselingem et al. [17] v osmdesátých letech 20. století. Přístroj pracuje s manžetou naloženou na střední článek druhého až čtvrtého prstu. V manžetě jsou uloženy foto-pletyzmografické elementy a její objem je adaptovatelný rychle pracujícím kompresorem umístěným na zápěstí. Velikost objemu a tlaku v manžetě je monitorována a adaptována s frekvencí 100 Hz. V intervalech daných kvalitou signálu (po 5–70 pulsech) je prováděna autokalibrace metodou Physiocal™. Tlak v manžetě je na přechodnou dobu mírně navýšen/snížen a je sledován vliv změny na kvalitu signálu [19]. Tím je udržována stěna tepny pod optimálním transmurálním tlakem. Tlaková křivka získaná z prstových arterií je následně pomocí matematického modelu převedena na křivku brachiálního tlaku [20]. Obdobně jako při přímém měření je nutno přístroji nastavit nulovou hladinu tlaku uložením sondy „heart reference“ do správné výšky. Spolehlivost zařízení Nexfin byla sledována v několika experimentálních pracích, jejichž výsledky jsou shrnuty v tabulce 1.
Obr. 2. Přístroj ccNexfin (vyobrazení poskytnuto výrobcem) 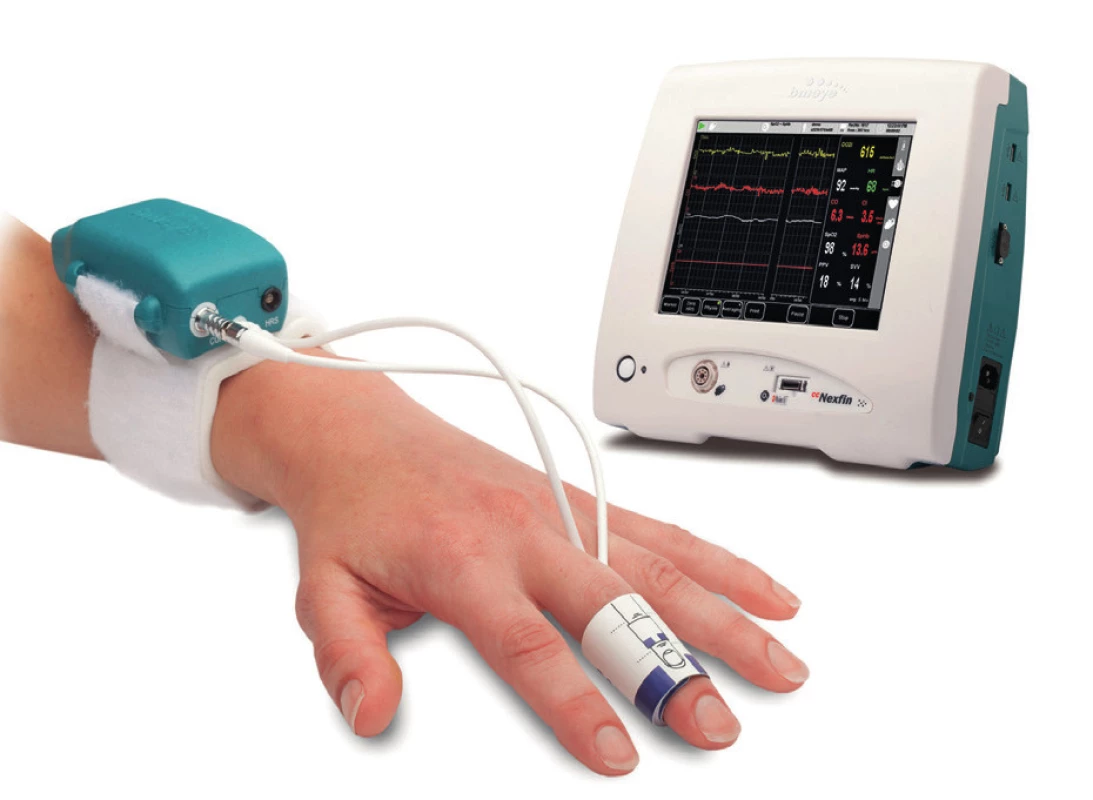
Tab. 1. Přehled studií zabývajících se validací přístroje Nexfin (porovnání s invazivním i neinvazivním standardem) 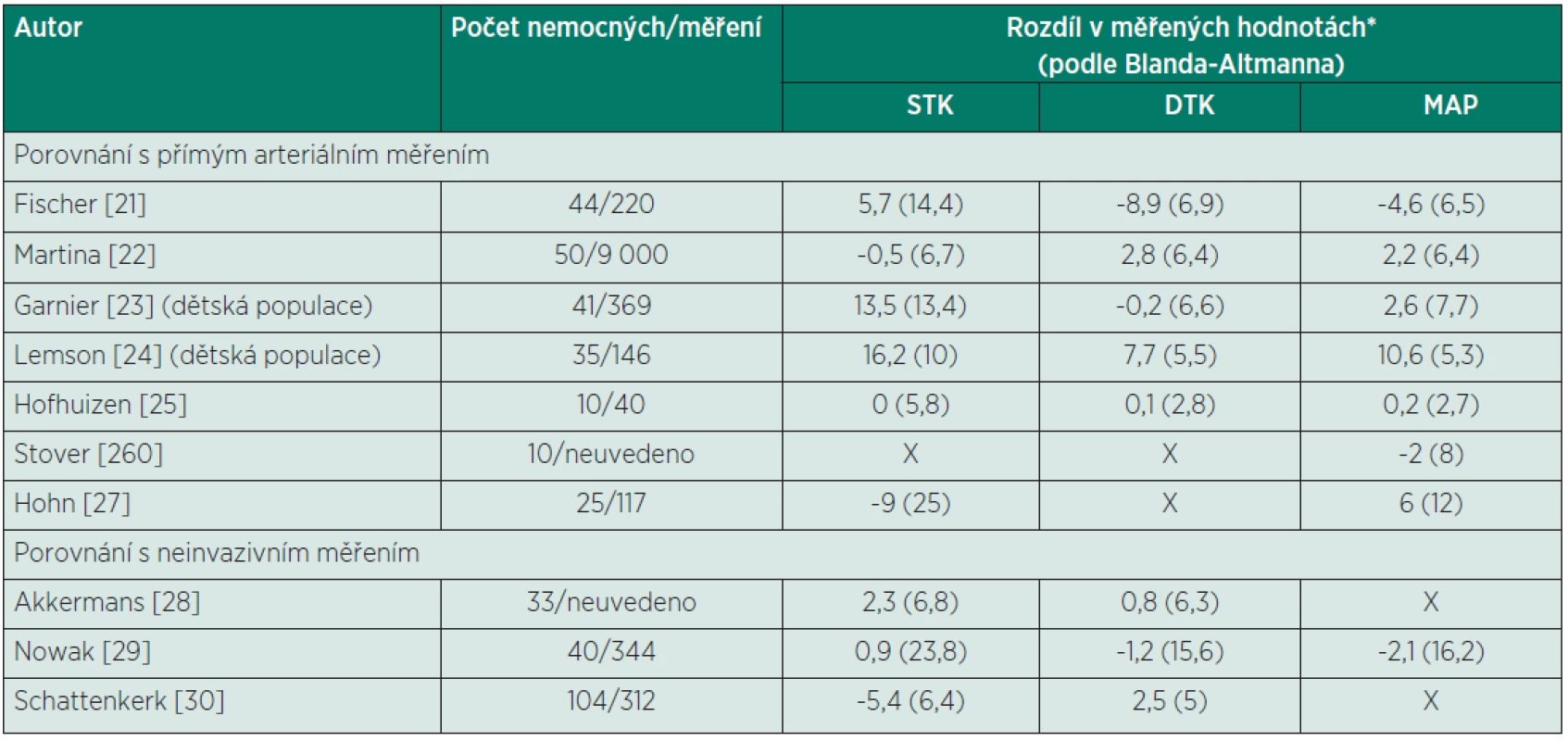
STK – systolický krevní tlak, DTK – diastolický krevní tlak, MAP – střední arteriální tlak Výsledné hodnoty ve většině případů částečně splnily požadavek kladený na zařízení měřící krevní tlak podle Association for the Advancement of Medical Instrumentation (AAMI/ANSI) [31]. Tento standard vyžaduje, aby průměrný rozdíl mezi párovým měřením podle Blanda-Altmanna byl menší než 5 mm Hg a směrodatná odchylka maximálně ± 8 mm Hg. Směrodatné odchylky v rozdílu párových měření, které blíže určují preciznost, ovšem vykazují vysokou variabilitu (viz tab. 1). Z tohoto pohledu zařízení nedosahuje dostatečné přesnosti. Dále byly pozorovány výraznější odchylky v dětské populaci, kde může sehrát významnou roli větší poddajnost periferního cévního systému a výsledná nepřesnost v matematickém modelu kalibrujícím prstový tlak na hodnoty v brachiální tepně [23, 25]. Rozdíly pozorované proti neinvazivnímu oscilometrickému měření dosahovaly větších hodnot [28–30], zde je nicméně nutno vzít v úvahu i významnou chybovost referenční neinvazivní metody [32].
Vedle kontinuálního monitorování krevního tlaku je monitor vybaven analýzou tepové křivky umožňující kalkulaci srdečního výdeje a odvozených parametrů. Princip měření je založen na dvouelementovém Windkessel modelu Oto Franka upraveném Wesselingem jako tzv. Modelflow metoda [33]. Ta vedle celkové poddajnosti (kompliance) velkých cév (Cw) a periferní rezistencí (Rp) počítá i s charakteristickou impedancí proximální aorty (Zc). Současný model zařízení ccNexfin je vybaven algoritmem Nexfin CO-Trek, který integruje zmíněné modely. Využívá analýzu plochy pod systolickou částí křivky a demografické charakteristiky ke stanovení celkové poddajnosti a impedance aorty. Vedle toho setrvale adaptuje hodnoty předpokládané periferní rezistence s využitím charakteristik poklesu tlaku v diastole. Podrobné vysvětlení algoritmu Nexfin Co--Trek je dostupné v přehledovém článku Trujenaet al. [34]. Validace algoritmu proti robustním měřením transpulmonální termodilucí nebo jícnovým dopplerem jsou zatím velmi limitovaná a rozporuplná [21, 26, 35–41]. Procentuální chyba měření srdečního výdeje metodou podle Critchleye [42] se pohybuje v rozmezí 25–50 %, což přesahuje požadovaných 30 %. Vedle klasických hemodynamických dat přístroj provádí kalkulaci dynamických parametrů preloadu (např. variace pulsního tlaku – PPV), které jsou podle dostupných údajů srovnatelné s intraarteriálním měřením [43].
CNAP
Druhým zařízením pracujícím na metodě volume clamp/vascular unloading je zařízení CNAP (CNSystems, Graz, Rakousko – obrázek 3). I v tomto případě je analyzován průtok prstovými arteriemi. Na rozdíl od zařízení Nexfin jsou manžety monitoru CNAP fixně nastavené pro naložení na dva sousedící proximální články druhého až čtvrtého prstu. Měření jsou prováděna vždy jednou z manžet, v nastavitelném intervalu potom dochází k rekalibraci a výměně, čímž odpadá spíše vizuálně nepříjemné zfialovění prstu. Auto-kalibrace vascular unloading techniky je u CNAP řešena pomocí Verifi algoritmu – systému několika uzavřených zpětných vazeb s různou časovou konstantou sledujících rychlé i pomalé změny vaskulárního tonu [44]. Převod na tlak v úrovni brachiální tepny z hodnot měřených na prstových arteriích je proveden intermitentní kalibrací vůči oscilometrické manžetě naložené na paži nemocného. K dosažení dostatečné spolehlivosti u nemocných bez významné fluktuace tlaku či změn polohy je výrobcem doporučen interval kalibrace à 30 minut a výměna prstů à 15 minut. Několik autorů se v poslední době věnovalo stanovení přesnosti zařízení v různých klinických scénářích (tab. 2). Ti porovnávali hodnoty získané invazivním měřením tlaku v průběhu celkové anestezie [44, 45] s hodnotami získanými zařízením CNAP. Podle těchto výsledků zařízení mírně podhodnocuje hodnoty systolického a nadhodnocuje hodnoty diastolického tlaku, u středního arteriálního tlaku je shoda většinou v rámci tolerance, ale s velikou směrodatnou odchylkou. Odchylka v měření systolického a diastolického tlaku může být částečně ovlivněna kalibrací na různé úrovně arteriálního řečiště (brachiální vs. radiální tepna). V celkovém pohledu tak monitor CNAP hraničně naplňuje požadavek AAMI/ANSI [31] na přesnost monitorování krevního tlaku, nelze ale uvažovat o plném nahrazení intraarteriálního měření. Přesnost přístroje navíc pravděpodobně významně klesá při prudké změně tlaku nebo výrazné hypotenzi [18, 47]. Patrné je zlepšení výsledků s inovací verze Verify algoritmu [48]. Ani to ovšem dostatečně nenaplňuje zmíněné požadavky AAMI/ANSI. Na druhou stranu (jak výstižně uvádí v diskusi Hahn) [48]: „Technologie nemá za cíl nahradit přímé měření tlaku, ale spíše umožnit kontinuální sledování nemocných, kteří jsou ve stávající situaci nedostatečně monitorování intermitentní oscilometrickou metodou, jejíž přesnost je taktéž sporná [32], a která je použita jako referenční metoda pro kalibraci“. Pro klinickou použitelnost zařízení CNAP svědčí práce, které dokladují schopnost predikovat odpověď na tekutinu [49, 50], nebo včas odhalit pokles krevního tlaku [51].
Obr. 3. Přístroj CNAP™ (vyobrazení poskytnuto výrobcem) 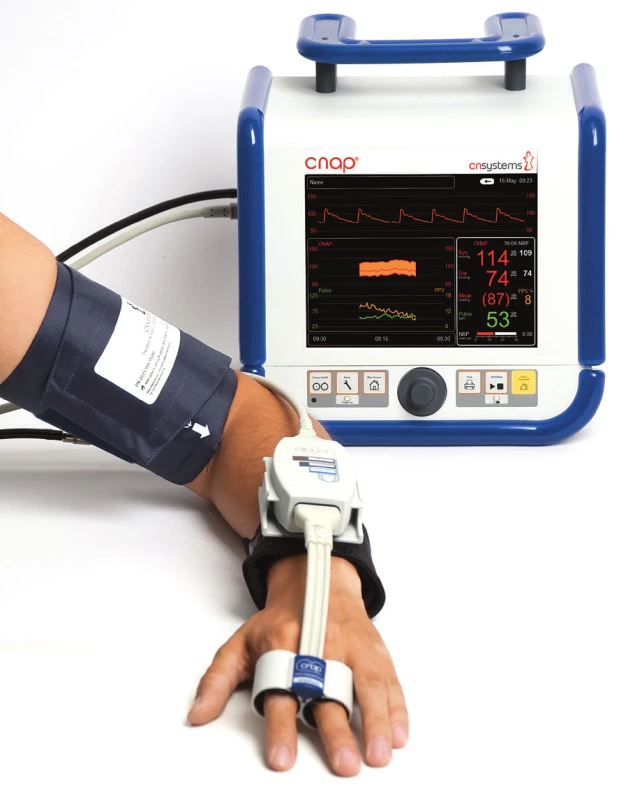
Tab. 2. Přehled studií zabývajících se přesností zařízení CNAP® (porovnání s invazivním měřením) 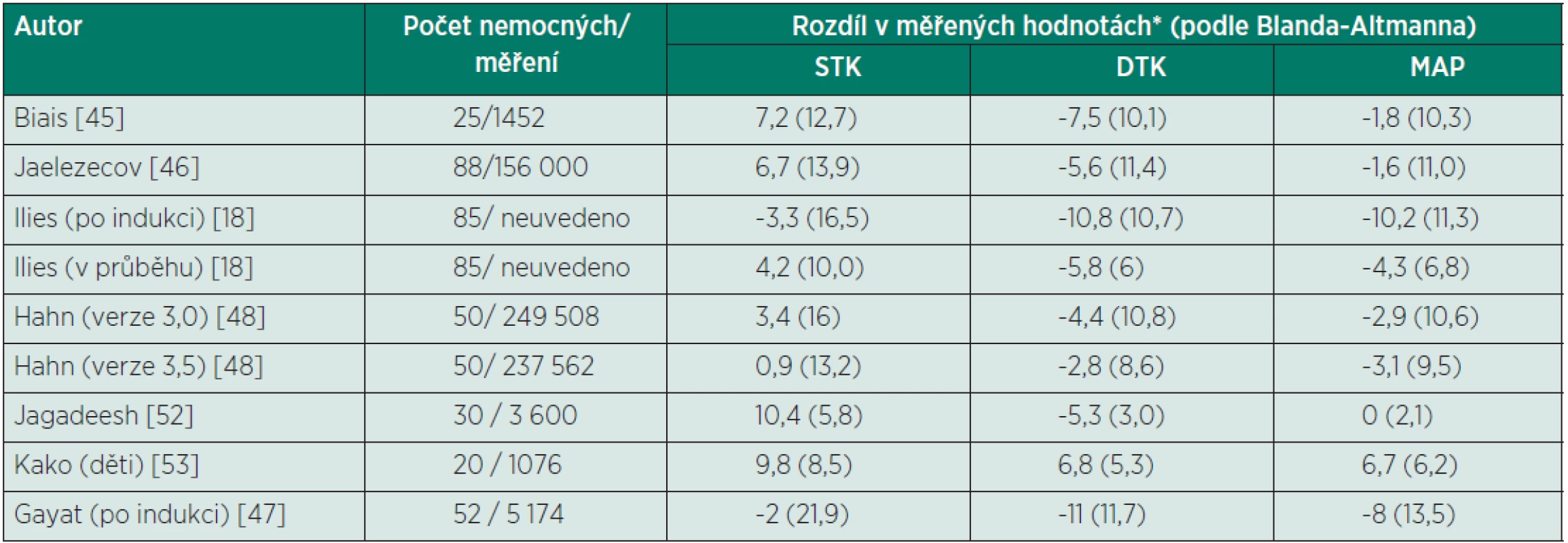
*Rozdíl mezi měřeními je definován jako referenční – neinvazivní technologie. Data jsou uváděna jako průměrný rozdíl (směrodatná odchylka). STK – systolický krevní tlak, DTK – diastolický krevní tlak, MAP – střední arteriální tlak Na rozdíl od zařízení Nexfin stávající verze CNAP prozatím nedisponuje algoritmem pro analýzu tepové křivky a stanovení srdečního výdeje. Nutné adaptace již byly výrobcem provedeny a novější verze přístroje budou obsahovat i tuto modalitu, její verifikace v klinickém užití není zatím dostupná. Už v současné verzi přístroje je prováděna kalkulace variace pulzního tlaku. Hodnota PPV získaná pomocí přístroje CNAP byla shodná s parametry získanými pomocí referenčních metod jak u nemocných v celkové anestezii [49], tak na jednotce intenzivní péče [50]. Vedle toho je již v současné době dostupná kombinace technologie CNAP s PulsePower analýzou – LiDCO Unity. Vzhledem k nedávnému uvedení tohoto monitoru na trh dosud nejsou dostupná validační data.
Aplanační tonometrie
Další možností kontinuálního neinvazivního monitorování arteriálního tlaku je aplanační tonometrie. Metoda je historicky užívaná k měření tlaku v tělesech (např. k monitorování nitroočního tlaku). Princip je založen na aplikaci Imbert-Fickova zákona: tlak potřebný k oploštění komprimovatelného povrchu koule je přímo úměrný nutné síle a nepřímo ploše, na kterou je síla rozložena. První aplanační tonometr pro měření krevního tlaku byl vytvořen G. L. Pressmanem a P. M. Newgardem v roce 1963. Pro kontinuální měření byla tato technologie použita až nedávno. Aby bylo možné provést měření aplanační tonometrií na cévním řečišti, je nutné vzít v úvahu celou řadu dalších faktorů – sílu a elastické vlastnosti stěny tepny, charakter a tloušťku kůže a podkoží. Přesnost měření je významně ovlivněna přesnou pozicí senzoru nad tepnou v místě komprimovatelném proti kosti. V současné době je dostupná řada zařízení umožňujících aplanometrické měření tlaku jednorázově, pro kontinuální užití je dostupný pouze přístroj T-line (TL verze 200-400, Tensys Medical Inc. San Diego, CA, USA – obrázek 4). Zařízení sestává z náramku naložitelného na předloktí nemocného a speciálního senzoru, který je nutné umístit s maximální přesností nad místo palpovatelné arteria radialis. Přístroj následně pomocí síly pulzací nalezne optimální polohu proti stěně tepny tak, aby byl senzor umístěn kolmo nad tepnou. Po nalezení optimální polohy je na tepnu vyvinut tlak nutný k parciálnímu oploštění (cílem je dosažení maximálního přenosu oscilací tlaku), tím se získá přesná hodnota středního arteriálního tlaku [12]. Následné změny tlaku v tepně jsou přenášeny na piezoelektrický krystal senzoru a přímo převáděny na digitalizovatelný signál. Získaná křivka a hodnoty tlaku musí být následně matematicky modelovány na základě demografických údajů nemocného a vnitřního adaptačního systému k odstranění vlivu tloušťky podkoží atp. [54]. Jednou z hlavních nevýhod metody je extrémní citlivost na správné uložení senzoru proti tepně, posunutí řádově o jeden milimetr (při pohybu nemocného atp.) má za následek nepřesnost měřených hodnot, nebo dokonce nutnost přesazení celého systému. Počet prací sledujících přesnost aplanometrického měření je podstatně menší než u metod založených na volume-clamp (tab. 3). Shoda s přímým měřením je podstatně lepší, a to jak pro starší zařízení TL 100, tak pro novější TL200. Vyšší přesnost může být dána mj. shodou lokalizace měření – a. radialis na distálním předloktí. Naopak extrémní citlivost k pohybům výrazně limituje užití u nesedovaných nemocných – ve studii Saugela et al. [55] bylo nutno vyřadit 6 ze 41 nemocných (15 %) buď pro technické problémy [5], nebo pro pohyby rušící monitorování (1 nemocný). Nejnovější generace přístroje(TL 300 a TL 400) již obsahují algoritmus umožňující výpočet srdečního výdeje a dalších hemodynamických parametrů. Validace těchto verzí (tlakového i hemodynamického algoritmu) nejsou v současné době dostupné.
Obr. 4. Přístroj TL400 (vyobrazení poskytnuto výrobcem) 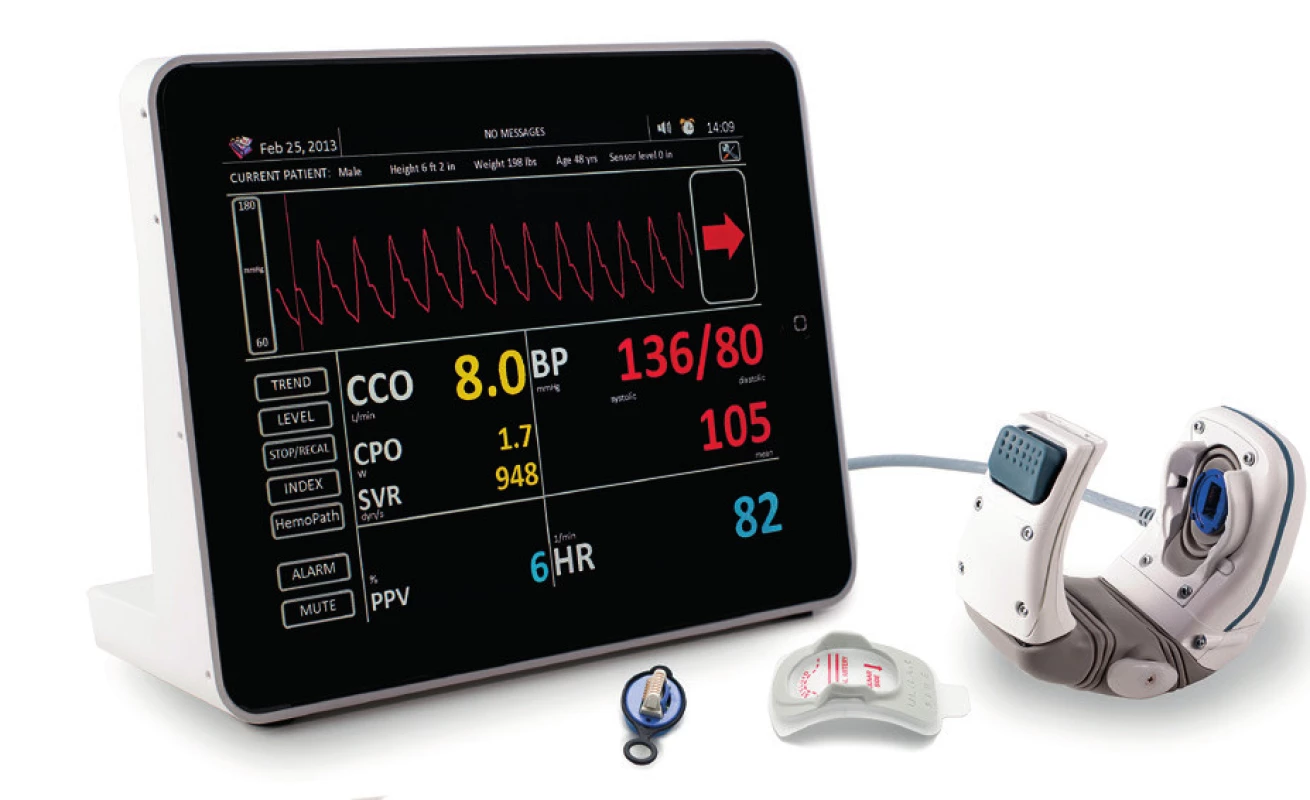
Tab. 3. Přehled prací zabývajících se přesností přístrojů řady T-line (porovnání s invazivním měřením) 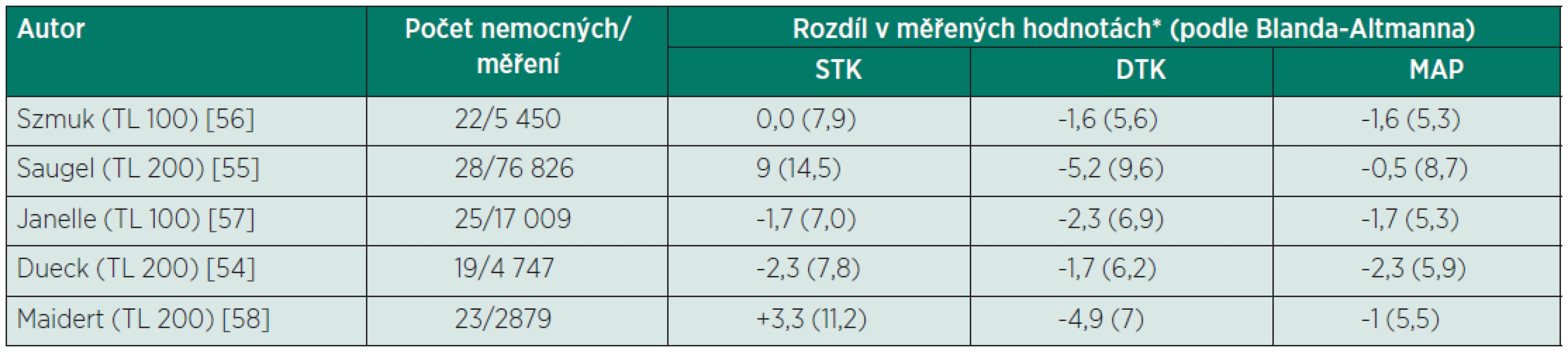
*Rozdíl mezi měřeními je definován jako referenční – neinvazivní technologie. Data jsou uváděna jako průměrný rozdíl (směrodatná odchylka). STK – systolický krevní tlak, DTK – diastolický krevní tlak, MAP – střední arteriální tlak Další možné techniky
Vedle popsaných technologií existuje ještě několik dalších principů, které mohou potenciálně umožnit zcela neinvazivní cestou analýzu hemodynamických parametrů. Jednou z metod je sledování rychlosti propagace pulzní vlny (pulse wave velocity, pulse transit time – PTT). Rychlost šíření pulzní vlny je podle Moen-Kortwegovy rovnice závislá na elasticitě tepny, která roste exponenciálně se systolickým tlakem [59]. Vzhledem k tomu, že stanovení PPT je možné pomocí stávajícího monitorování, křivky EKG (vlna R) a pulzní oxymetrie (počátek mechanického pulsu v periferii), jedná se o metodu zcela nezatěžující. Experimentální práce zaměřené na tuto problematiku poukazují na celou řadu nevyjasněných faktorů [59, 60]. Pre-ejekční perioda, tzn. čas mezi vlnou R a otevřením aortální chlopně, je většinou ve výpočtech opomíjena. Rychlost šíření (PTT) je mimo systolického tlaku závislá na mnoha jiných faktorech s velikou interindividuální variabilitou. Stanovení diastolického a středního tlaku není pomocí PTT možné bez užití dalších adaptací. V současné době není k dispozici zařízení, které by umožnilo měření pomocí PTT mimo experiment. Jediný monitor využívající stanovení PTT pro monitorování hemodynamiky je esCCO (Nihon Kohden, Japonsko). Toto zařízení využívá korelace PTT a tepového objemu k trendovému stanovení srdečního výdeje. Validace přístroje byla zatím provedena jen v jedné publikované práci provedené firemním výzkumným týmem [61]. Obdobně techniky založené na bioimpedanci či bioreaktanci umožňují sledovat pulzatilní změny krevního kompartmenu a z toho odvodit hodnotu srdečního výdeje. Pro analýzu tlaku v současném stavu vhodné nejsou.
ZÁVĚR
Arteriální tlak je jedním z nejdůležitějších parametrů hemodynamiky monitorování u nemocných v anestezii. Stávající metody monitorování jsou významně zatíženy buď nízkou přesností a nutností intermitentního měření, nebo invazivitou. Rozvoj současných možností neinvazivního sledování arteriálního tlaku kontinuálně buď pomocí volume clamp metody, nebo aplanační tonometrií s sebou může přinést významné zkvalitnění anesteziologické péče a bezpečí pro nemocného. Dosavadní validace všech zmíněných přístrojů se zatím jeví jen jako hraničně postačující pro klinické užití u běžné anesteziologické populace. Lze předpokládat, že další adaptace popsaných postupů povedou ke zpřesnění monitorovaných hodnot. Ve spojení s analýzou tepové křivky, kontinuálním stanovením srdečního výdeje a odvozených parametrů mají popsané technologie v budoucnu veliký potenciál k ovlivnění naší každodenní péče. Před případným běžným užitím těchto monitorovacích metod je ovšem nutná jejich širší klinická validace.
Poděkování: Podpořeno rozvojovým projektem P36 „PRVOUK“.
Poděkování paní prof. MUDr. Honzíkové, CSc. z Fyziologického ústavu Masarykovy univerzity v Brně a všem výrobcům za poskytnutí fotografických podkladů.
Konflikt zájmů: JB je členem Advisory board fy Edwards Lifesciences Inc., ostatní autoři nemají v současné době ani v minulosti finanční ani jinou vazbu na jakýkoli subjekt, který by mohl mít z publikace textu finanční či jiný prospěch.
Do redakce došlo dne 16. 9. 2013.
Do tisku přijato dne 1. 12. 2013.
Adresa pro korespondenci:
As. MUDr. Jan Beneš, Ph.D.
Anesteziologicko-resuscitační klinika
Fakultní nemocnice Plzeň
Alej Svobody 80
304 60 Plzeň
e-mail: benesj@fnplzen.cz
Zdroje
1. ASA House of Delegates STANDARDS FOR BASIC ANESTHETIC MONITORING. [online] 2011 [cit.2013-07-12]. Dostupný na www: http://www.asahq.org/For-Members/~/media/For%20Members/documents/Standards%20Guidelines%20Stmts/Basic%20Anesthetic%20Monitoring%202011.ashx.
2. Cvachovec, K., Černý, V., Herold, I., Kozlík, P., Šturma, J. Zásady bezpečné anesteziologické péče. [online] 2012 [cit.2013-07-12]. Dostupný na www: http://www.csarim.cz/Public/csim/22%20%20DP_safety_anesth_CSARIM_final_approval_140212.pdf.
3. Sy, W. P. Ulnar nerve palsy possibly related to use of automatically cycled blood pressure cuff. Anesth. Analg., 1981, 60, p. 687–688.
4. Bause, G. S., Weintraub, A. C., Tanner, G. E. Skin avulsion during oscillometry. J. Clin. Monit., 1986, 2, p. 262–263.
5. Cannesson, M., Pestel, G., Ricks, C., Hoeft, A., Perel, A. Hemodynamic monitoring and management in patients undergoing high risk surgery: a survey among North American and European anesthesiologists. Crit. Care, 2011, 15, R197.
6. Scheer, B., Perel, A., Pfeiffer, U. J. Clinical review: complica-tions and risk factors of peripheral arterial catheters used for haemodynamic monitoring in anaesthesia and intensive care medicine. Crit. Care, 2002, 6, p. 199–204.
7. Lamia, B., Chemla, D., Richard, C., Teboul, J. L. Clinical review: interpretation of arterial pressure wave in shock states. Crit. Care, 2005, 9, p. 601–606.
8. Montenij, L. J., de Waal, E. E. C., Buhre, W. F. Arterial waveform analysis in anesthesia and critical care. Curr. Opin. Anaesthesiol., 2011, 24, p. 551–556.
9. O‘Brien, E. et al. Working Group on Blood Pressure Monitoring of the European Society of Hypertension International Protocol for validation of blood pressure measuring devices in adults. Blood Press Monit, 2002, 7, p. 3–17.
10. Pickering, T. G. et al. Recommendations for blood pressure measurement in humans and experimental animals: Part 1: blood pressure measurement in humans: a statement for professionals from the Subcommittee of Professional and Public Education of the American Heart Association Council on High Blood Pressure Research. Hypertension, 2005, 45, p. 142–161.
11. Marey, E. Pression et vitesse du sang. Physiologie Expe-rimentale, 1876.
12. Drzewiecki, G., Hood, R., Apple, H. Theory of the oscillometric maximum and the systolic and diastolic detection ratios. Ann. Biomed. Eng., 1994, 22, p. 88–96.
13. Smulyan, H., Safar, M. E. Blood pressure measurement: retrospective and prospective views. American Journal of Hypertension, 2011, 24, p. 628–634.
14. Marks, L. A., Groch, A. Optimizing cuff width for noninvasive measurement of blood pressure. Blood Press Monit., 2000, 5, p. 153–158.
15. Avolio, A. P., Butlin, M., Walsh, A. Arterial blood pressure measurement and pulse wave analysis-their role in enhancing cardiovascular assessment. Physiol. Meas., 2010, 31, R1-47.
16. Penaz, J. Photoelectric measurement of blood pressure, volume and flow in the finger. In Digest of the 10th International Conference on Medical and Biological Engineering , Dresden
17. Wesseling, K. A century of noninvasive arterial pressure measurement: from Marey to Penaz and Finapres. Homeostasis., 1995, p. 2–3.
18. Ilies, C. et al. Investigation of the agreement of a continuous non-invasive arterial pressure device in comparison with invasive radial artery measurement. Br. J. Anaesth., 2012, 108, p. 202–210.
19. Wesseling, K. H., de Wit, B., van der Hoeven, G. M. A., van Goudoever, J., Settels, J. Physiocal, calibrating finger vascular physiology for Finapres. Homeostasis, 1995, 36, p. 67–82.
20. Gizdulich, P., Prentza, A., Wesseling, K. H. Models of brachial to finger pulse wave distortion and pressure decrement. Cardiovasc. Res., 1997, 33, p. 698–705.
21. Fischer, M. O. et al. Non-invasive continuous arterial pressure and cardiac index monitoring with Nexfin after cardiac surgery. Br. J. Anaesth., 2012, 109, p. 514–521.
22. Martina, J. R. et al. Noninvasive continuous arterial bloodpressure monitoring with Nexfin®. Anesthesiology, 2012, 116, p. 1092–1103.
23. Garnier, R. P., van der Spoel, A. G. E., Sibarani-Ponsen, R., Markhorst, D. G., Boer, C. Level of agreement between Nexfin non-invasive arterial pressure with invasive arterial pressure measurements in children. Br. J. Anaesth., 2012, 109, p. 609–615.
24. Lemson, J. et al. The reliability of continuous noninvasive finger blood pressure measurement in critically ill children. Anesth. Analg., 2009, 108, p. 814–821.
25. Hofhuizen, C. M. et al. Continuous non-invasive finger arterial pressure monitoring reflects intra-arterial pressure changes in children undergoing cardiac surgery. Br. J. Anaesth., 2012, 105, p. 493–500.
26. Stover, J. F. et al. Noninvasive cardiac output and bloodpressure monitoring cannot replace an invasive monitoring system in critically ill patients. BMC Anesthesiology, 2009, 9, 6.
27. Hohn, A. et al. Non-invasive continuous arterial pressure monitoring with Nexfin(R) does not sufficiently replace invasive measurements in critically ill patients. Br. J. Anaesth., 2013, 111, p. 178–184.
28. Akkermans, J. et al. Continuous Non-Invasive Blood Pressure Monitoring, a Validation Study of Nexfin in a Pregnant Population. Hypertension in Pregnancy, 2009, 28, p. 230–242.
29. Nowak, R. M. et al. Noninvasive continuous or intermittent blood pressure and heart rate patient monitoring in the ED. Am. J. Emerg. Med., 2011, 29, p. 782–789.
30. Eeftinck Schattenkerk, D. W. et al. Nexfin noninvasive continuous blood pressure validated against Riva-Rocci/Korotkoff. American journal of hypertension, 2009, 22, p. 378–383.
31. ANSI/AAMI American National Standard for Manual, Electronic, or Automated Sphygmomanometers. In, Arlington, VA.
32. Bur, A. et al. Accuracy of oscillometric blood pressure measurement according to the relation between cuff size and upper-arm circumference in critically ill patients. Crit. Care Med., 2000, 28, p. 371–376.
33. Wesseling, K. H., Jansen, J. R., Settels, J. J., Schreuder, J. J.Computation of aortic flow from pressure in humans using a nonlinear, three-element model. J. Appl. Physiol., 1993, 74, p. 2566–2573.
34. Truijen, J., van Lieshout, J. J., Wesselink, W. A., Wester-hof, B. E. Noninvasive continuous hemodynamic monitoring.J. Clin. Monit. Comput., 2012, 26, p. 267–278.
35. Fischer, M. O. et al. Assessment of changes in cardiac index and fluid responsiveness: a comparison of Nexfin and transpulmonary thermodilution. Acta Anaesthesiol. Scand., 2013, 57, p. 704–712.
36. Monnet, X. et al. The estimation of cardiac output by the Nexfin device is of poor reliability for tracking the effects of a fluid challenge. Crit. Care, 2012, 16, R212.
37. Broch, O. et al. A comparison of the Nexfin® and transcardiopulmonary thermodilution to estimate cardiac output during coronary artery surgery. Anaesthesia, 2012, 67, p. 377–383.
38. Trinkmann, F. et al. Is arterial pulse contour analysis using Nexfin a new option in the noninvasive measurement of cardiac output? A pilot study. J. Cardiothorac. Vasc. Anesth., 2013, 27, p. 283–287.
39. van der Spoel, A. G. E., Voogel, A. J., Folkers, A., Boer, C., Bouwman, R. A. Comparison of noninvasive continuous arterial waveform analysis (Nexfin) with transthoracic Doppler echocardiography for monitoring of cardiac output. J. Clin. Anesth., 2012, 24, p. 304–309.
40. Chen, G. et al. Comparison of noninvasive cardiac output measurements using the Nexfin monitoring device and the esophageal Doppler. J. Clin. Anesth., 2012, 24, p. 275–283.
41. Bogert, L. W. J. et al. Pulse contour cardiac output derived from non-invasive arterial pressure in cardiovascular disease. Anaesthesia, 2010, 65, p. 1119–1125.
42. Critchley, L. A., Critchley, J. A. A meta-analysis of studies using bias and precision statistics to compare cardiac output measurement techniques. J. Clin. Monit. Comput., 1999, 15, p. 85–91.
43. Lansdorp, B. et al. Non-invasive measurement of pulsepressure variation and systolic pressure variation using a finger cuff corresponds with intra-arterial measurement. Br. J. Anaesth., 2011, 107, p. 540–545.
44. Fortin, J. et al. Continuous non-invasive blood pressure monitoring using concentrically interlocking control loops. Comput. Biol. Med., 2006, 36, p. 941–957.
45. Biais, M. et al. Continuous non-invasive arterial pressure measurement: evaluation of CNAP device during vascular surgery. Ann. Fr. Anesth. Reanim., 2010, 29, p. 530–535.
46. Jeleazcov, C. et al. Precision and accuracy of a new device (CNAPTM) for continuous non-invasive arterial pressure monitoring: assessment during general anaesthesia. Br. J. Anaesth., 2010, 105, p. 264–272.
47. Gayat, E. et al. CNAP(®) does not reliably detect minimal or maximal arterial blood pressures during induction of anaesthesia and tracheal intubation. Acta Anaesthesiol. Scand., 2013, 57, p. 468–473.
48. Hahn, R., Rinösl, H., Neuner, M., Kettner, S. C. Clinical validation of a continuous non-invasive haemodynamic monitor (CNAP 500) during general anaesthesia. Br. J. Anaesth., 2012, 108, p. 581–585.
49. Biais, M. et al. The ability of pulse pressure variations obtained with CNAP™ device to predict fluid responsiveness in the operating room. Anesth. Analg., 2011, 113, p. 523–528.
50. Monnet, X. et al. Prediction of fluid responsiveness by a continuous non-invasive assessment of arterial pressure in critically ill patients: comparison with four other dynamic indices. Br. J. Anaesth., 2012, 109, p. 330–338.
51. Ilies, C. et al. Detection of hypotension during Caesarean section with continuous non-invasive arterial pressure device or intermittent oscillometric arterial pressure measurement. Br. J. Anaesth., 2012, 109, p. 413–419.
52. Jagadeesh, A. M., Singh, N. G., Mahankali, S. A comparison of a continuous noninvasive arterial pressure (CNAP™) monitor with an invasive arterial blood pressure monitor in the cardiac surgical ICU. Ann. Card. Anaesth., 2012, 15, p. 180–184.
53. Kako, H., Corridore, M., Rice, J., Tobias, J. D. Accuracy of the CNAP™ monitor, a noninvasive continuous blood pressure device, in providing beat-to-beat blood pressure readings in pediatric patients weighing 20–40 kilograms. Paediatr. Anaesth., 2013.
54. Dueck, R., Goedje, O., Clopton, P. Noninvasive continuous beat-to-beat radial artery pressure via TL-200 applanation tonometry. J. Clin. Monit. Comput., 2012, 26, p. 75–83.
55. Saugel, B. et al. The T-Line TL-200 system for continuous non-invasive blood pressure measurement in medical intensive care unit patients. Intensive Care Med., 2012, 38, p. 1471–1477.
56. Szmuk, P., Pivalizza, E., Warters, R. D., Ezri, T., Gebhard, R. An evaluation of the T-Line Tensymeter continuous noninvasive blood pressure device during induced hypotension. Anaesthesia, 2008, 63, p. 307–312.
57. Janelle, G. M., Gravenstein, N. An accuracy evaluation of the T-Line Tensymeter (continuous noninvasive blood pressure mana-gement device) versus conventional invasive radial artery monitoring in surgical patients. Anesth. Analg., 2006, 102, p. 484–490.
58. Meidert, A. S. et al. Evaluation of the radial artery applanation tonometry technology for continuous noninvasive blood pressure monitoring compared with central aortic blood pressure measurements in patients with multiple organ dysfunction syndrome.J. Crit. Care, 2013.
59. Chen, W., Kobayashi, T., Ichikawa, S., Takeuchi, Y., Toga-wa, T. Continuous estimation of systolic blood pressure using the pulse arrival time and intermittent calibration. Med. Biol. Eng. Comput., 2000, 38, p. 569–574.
60. Ahlstrom, C., Johansson, A., Uhlin, F., Länne, T., Ask, P. Noninvasive investigation of blood pressure changes using the pulse wave transit time: a novel approach in the monitoring of hemodialysis patients. J. Artif. Organs., 2005, 8, p. 192–197.
61. Ishihara, H. et al. The ability of a new continuous cardiac output monitor to measure trends in cardiac output following implementation of a patient information calibration and an automated exclusion algorithm. J. Clin. Monit. Comput., 2012, 26, p. 465–471.
Štítky
Anestéziológia a resuscitácia Intenzívna medicína
Článok vyšiel v časopiseAnesteziologie a intenzivní medicína
Najčítanejšie tento týždeň
2014 Číslo 3- DESATORO PRE PRAX: Aktuálne odporúčanie ESPEN pre nutričný manažment u pacientov s COVID-19
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Metamizol v liečbe pooperačnej bolesti u opioid-tolerantnej pacientky – kazuistika
- e-Konzilium.cz — Masivní plicní embolie při tromboembolické nemoci
-
Všetky články tohto čísla
- Terapeutická hypotermie po zástavě oběhu - máme přestat? Ani náhodou!
- Bužií asistovaná koniotomie (BACT) na prasečím modelu – pilotní studie
- Kontinuální kaudální epidurální analgezie extrémně nedonošeného dítěte – kazuistika
- Postpunkční cefalea v porodnictví
- Úloha krátkodobých betablokátorů v anestezii a intenzivní péči
- Kandidová sepse jako komplikace u pacienta s polytraumatem
- Význam tromboelastografie (TEG) a tromboelastometrie (ROTEM) na jednotke intenzívnej starostlivosti
- Současné možnosti kontinuálního neinvazivního monitorování arteriálního tlaku
- Možnosti využití ultrazvuku u neuroaxiálních blokád
- Centrální žilní porty a jejich využití k zajištění dlouhodobého cévního přístupu
- Premedikace a lačnění
- Valsalvův manévr
- Consensus guidelines for the management of postoperative nausea and vomiting
- Mezioborové stanovisko k používání terapeutické hypotermie u pacientů po zástavě oběhu
- Použití vysokofrekvenční ventilace/oscilace u pacientů s ARDS: jen jako rescue postup!
- Souhlas k pitvě – právní a etický problém?
- Vladimír Lemon a hudba v korespondenci z let 2009–2010
- Anesteziologie a intenzivní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Postpunkční cefalea v porodnictví
- Valsalvův manévr
- Centrální žilní porty a jejich využití k zajištění dlouhodobého cévního přístupu
- Význam tromboelastografie (TEG) a tromboelastometrie (ROTEM) na jednotke intenzívnej starostlivosti
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



